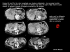
Plaie des voies biliaires - Chirurgie
Transcription
Plaie des voies biliaires - Chirurgie
SOMMAIRE Organisateur : J. GUGENHEIM (Nice) Modérateurs : J. GUGENHEIM (Nice) A. HAMY (Angers) 1. Classification des plaies chirurgicales iatrogènes des voies biliaires extrahépatiques. A. HAMY (Angers) 2. Plaie des voies biliaires reconnue en peropératoire : les 8 erreurs à ne pas commettre. G. MANTION (Besançon) 3. Prise en charge des plaies des voies biliaires après cholécystectomie. Place de la radiologie interventionnelle P. CHEVALIER (Nice) 4. Plaies des voies biliaires au cours d’une cholécystectomie : prise en charge à la phase retardée. J. GUGENHEIM (Nice) 5. Les formes complexes O. FARGES (Paris) FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie CLASSIFICATIONS DES PLAIES CHIRUGICALES IATROGENES DES VOIES BILIAIRES EXTRA-HEPATIQUES A. Hamy, S. Mucci, J. Gugenheim, J. Paineau La plaie chirurgicale iatrogène de la voie biliaire extrahépatique, principalement durant la réalisation d'une cholécystectomie, est un accident chirurgical associé à une élévation significative de la morbidité et de la mortalité. Cette plaie iatrogène, qui peut survenir aussi au décours d'autres procédures chirurgicales que la cholécystectomie, modifie la qualité de vie des patients et est souvent responsable de difficultés chirurgicales réparatrices [sources de complications ultérieures propres] et éventuellement de procédures de recours judiciaires et d'indemnisation. Les possibilités de prise en charge de ces plaies reposent sur plusieurs facteurs comme le moment (peropératoire, post-opératoire précoce ou tardif) où est reconnue la plaie, l'extension de celle-ci, son type anatomique ou l'état général péri-opératoire du patient. Le but de la réparation chirurgicale est la restauration de la perméabilité biliaire, la prévention à court ou moyen terme d'une fuite biliaire, la diminution du risque d'abcès intraabdominal aggravant les risques de sténose à long terme et la prévention d'une sténose biliaire définitive avec le risque de cholangite sclérosante secondaire. Un des facteurs déterminant la prise en charge (appréciation du risque et de la difficulté opératoires, appréciation de la qualité de la réparation, risques de complications et de séquelles) est le type anatomique et la localisation de la plaie biliaire. Ce facteur primordial nécessite donc une tentative de classification. Il est généralement considéré qu'une plaie de la voie biliaire principale ou du canal hépatique distal était d'une prise en charge et d'une réparation relativement plus aisée que la localisation proximale sur le canal hépatique vers la convergence ou de la convergence ellemême. Schématiquement, plus la localisation traumatique biliaire est haut située, se rapprochant de la convergence biliaire, plus les difficultés de réparation sont importantes et moins le résultat à long terme est potentiellement satisfaisant. Une des premières, et, principales classifications des plaies des voies biliaires, est celle proposée par Bismuth (1) basée sur l'expérience des plaies des voies biliaires faites en chirurgie par laparotomie. Cette classification est considérée avoir une bonne corrélation avec le résultat final attendu de la réparation chirurgicale (2). Cette classification [tableau 1] décrit un type I correspondant à une sténose de la voie bilaire pédiculaire à distance de la FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie convergence qui peut être réparée sans dissection hilaire, sans ouverture du canal hépatique gauche et sans abaissement de la plaque hilaire. Le type II est défini par une sténose soushilaire (VBP résiduelle < à 2 cm) nécessitant l'ouverture du canal hépatique gauche de façon à élargir la surface anastomotique. Dans ce type II, l'abaissement de la plaque hilaire n'est pas nécessaire ni réalisée de façon systématique. Dans le type III seul le toit de la convergence biliaire est intact. Un abaissement de la plaque hilaire et une ouverture du canal hépatique gauche seront nécessaires lors de la réparation chirurgicale. Il n'y a pas, dans ce cas, de nécessité d'ouverture du canal hépatique droit. Avec le type IV, l'atteinte de la convergence est bilatérale et celle-ci est interrompue : les canaux droit et gauche sont séparés. Ceci justifiera une reconstruction indépendante avec deux (ou plus) anastomoses bilio-digestives. Enfin, Bismuth décrit un type V où la sténose siège sur le canal hépatique droit associée à un abouchement anormal de ce canal hépatique droit sectoriel sur la voie biliaire principale extrahépatique. Dans ce cas, il faut associer à la réparation de la voie biliaire hépatique principale une réparation de ce canal sectoriel droit qui présente cette variation anatomique très classique d'implantation. Notons que Bismuth réalise ainsi une classification des sténoses biliaires posttraumatiques de la voie biliaire, et non réellement, une classification des plaies notamment récentes (diagnostic précoce). Dans la pratique, cette classification est cependant souvent utilisée pour classer des plaies vues plus précocement avant le stade cicatriciel de sténose. Type Description 1 sténose distale de la VBP avec un canal hépatique sain > à 2 cm / à la convergence 2 sténose proximale de la VBP avec un canal hépatique sain < à 2 cm / à la convergence 3 sténose hilaire sans canal hépatique résiduel sain mais avec toit de la convergence respectée 4 atteinte de la convergence avec perte de la communication entre les canaux biliaires droit et gauche 5 atteinte d'un canal hépatique sectoriel droit indépendant avec ou sans atteinte de la VBP Tableau 1. Classification de Bismuth (1) FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie En 1995, Mac Mahon et al. (3) [tableau 2] proposent une classification simplifiant la notion topographique mais insistant sur la gravité du type lésionnel en introduisant la notion de lacération, de trans-section, de résection et de sténose caractérisant la localisation traumatique biliaire. Cette classification de Mac Mahon permet, en théorie, et, selon les auteurs, en tenant compte du type de traumatisme et de sa localisation, d'envisager une simple suture, une suture sur un drain biliaire en T ou, en cas de plaie majeure, d'envisager immédiatement une dérivation bilio-digestive. Type de plaie Description Plaie majeure (au moins 1 critère) > à 25% du diamètre de la VBP section du cholédoque ou du CH commun distal sténose post-opératoire de la VBP Plaie mineure < à 25% du diamètre de la VBP Plaie de la convergence canal cystique/VBP Tableau 2. Classification de Mc Mahon et al. (3) Cependant, la classification de Bismuth même, en tenant compte des sous-groupes introduits par Mac Mahon et al., ne tient pas compte de l'ensemble du spectre des plaies des voies biliaires apparues et décrites depuis l'avènement de la laparoscopie. En effet, il y a une incontestable modification du type lésionnel par rapport aux plaies réalisées lors des cholécystectomies par laparotomie et du contexte de leur survenue (4-6): - perte du contrôle visuel par hémorragie de la région pédiculaire, - tentative "aveugle" de contrôle d'une hémorragie, - non reconnaissance des la VBP ou confusion de celle-ci avec le canal cystique, - résection d'une partie de la VBP, - lésion artérielle hépatique droite, - électrocoagulation directe ou par diffusion de la VBP, - perte de contact lors de la dissection du triangle de Calot avec plaie, section ou mise de clips sur un canal sectoriel droit s'abouchant directement sur la VBP, - les lésions de lacérations plus ou moins circonférentielles des canaux biliaires principaux ou accessoires - …/… FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie Globalement, l'élément central pathologique responsable des plaies réalisée sous laparoscopie est représentée par la mauvaise identification de la voie biliaire principale ce qui peut aboutir au maximum, à une résection de toute ou partie de celle-ci éventuellement associée un traumatisme de l'artère hépatique droite: c'est cette absence d'identification correcte qui aboutit, avec des atteintes diverses de degrés de sévérité, à la genèse des complications chirurgicales. En 1995, Strasberg et al. (7) ont tenté d'adapter la classification de Bismuth en y introduisant les nouvelles données physiopathologiques propres à la chirurgie par laparoscopie. Cette classification permet de décrire 5 types lésionnels de A à E, le type E réintroduisant spécifiquement les éléments de la classification de Bismuth et permet la description de 5 sousgroupes de E1 à E5 [tableau 3]. Notons que le type A (fuite biliaire du canal cystique ou de canaux accessoires du lit vésiculaire) élargit la notion de plaie iatrogène de la voie biliaire aux atteintes de la voie biliaire accessoire ou du lit vésiculaire qui ne sont pas pris en compte dans la classification de Bismuth. Type Description A Fuite biliaire du canal cystique ou de canaux accessoires du lit vésiculaire B Obstruction partielle de l'arbre biliaire incluant un canal sectoriel droit aberrant C Section sans ligature d'un canal sectoriel droit aberrant D Plaies latérales de la VBP E (de 1 à 5) reprenant la classification de Bismuth Tableau 3. Classification de Strasberg et al. (7) FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie Figure 1 : Classification de Strasberg (trait plein) reprenant au stade de sténose la classification de Bismuth (B1 à B5, pointillés) FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie Dans le même souci d'introduire et de tenir compte des nouveaux mécanismes lésionnels propres à la coelioscopie, de nombreux auteurs (8-15) ont eux aussi proposé de nouvelles classifications. L'ensemble de ces classifications tentent d'associer, à des degrés divers, le niveau anatomique lésionnel et/ou les lésions vasculaires associées [tableau 4]. Parmi ces classifications, celle que Lau et Lai (12) ont proposé en 2007 essayait de faire la synthèse des différents types et de mécanismes de plaie biliaire ainsi que de leurs localisations [tableau 4]. Selon ces auteurs, cette classification aurait l'avantage de tenir compte d'une sévérité croissante de la plaie biliaire (type de 1 à 5), du mécanisme de la plaie qui peut être différent à chaque type, de proposer les mesures préventives propres à chaque type et d'offrir la possibilité d'une concordance thérapeutique en fonction du type et de l'anatomie en fonction d'un diagnostic précoce ou tardif de l'accident chirurgical. FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie Tableau 4 : diverses classifications des plaies des voies biliaires Publiée en 2007 par Bektas et al. (16) la classification dite « de Hanovre » semble globalement la plus complète au regard de la nouvelle complexité des plaies iatrogènes des voies biliaires [tableau 5]. Cette classification présente par rapport aux autres classifications la meilleure corrélation entre la distinction du type lésionnel et le pourcentage de nécessité de recours à une hépatectomie ou une dérivation hépatico-jejunale dans le traitement de la plaie biliaire. Malgré son [apparente] complexité, peut-être devrait-elle être adoptée pour homogénéiser les descriptions lésionnelles, adapter le geste de réparation biliaire et comparer les résultats. Mais elle ne peut être appliquée que si le chirurgien décrit très précisément les lésions, ce qui ne peut être que prospectif et réalisé que le diagnostic est immédiat ou précoce. FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie Nous verrons que le recueil rétrospectif des observations dans le cadre de cette enquête de l'AFC ne peut utiliser correctement cette classification. Tableau 5. Classification « de Hanovre » (16) FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie L'évolution et le pronostic fonctionnel des patients ayant eu une plaie de la voie biliaire sont moins bons si elle est combinée à une plaie artérielle que chez les patients ayant un système vasculaire pédiculaire intact. Les répercussions de l'ischémie biliaire sont importantes à prendre en compte. L'artère hépatique droite croise la voie biliaire principale au niveau d'une zone anatomique volontiers en cause lors des plaies et traumatismes de la voie biliaire ce qui explique les associations traumatiques biliaires et vasculaires. Les classifications proposées par Stewart-Way, Lau-Lei, Siewert et celle dite « de Hanovre » tiennent compte, en pratique, de ces associations lésionnelles artérielles (11-12, 15-16). Stewart et al. ont aussi montré que le traumatisme associé de l'artère hépatique droite augmente la morbidité et est significativement associé à des lésions biliaires plus graves (de type III et IV) (11). Par contre, dans le travail de Stewart et al., le traumatisme de l'artère hépatique droite n'augmente pas forcement la mortalité péri-opératoire et peut ne pas altérer le résultat final de la réparation biliaire (11). En effet, pour eux tout dépend des conditions de ré-intervention face à cette double plaie biliaire et vasculaire : si la réparation biliaire est réalisée par le chirurgien initial, la chirurgie de réparation est associée à une élévation de la morbidité périopératoire à type d'abcès ou de fistule biliaires conduisant à une proportion plus élevée d'hépatectomie de nécessité; à l'opposé, si le patient est transféré dans une équipe de chirurgie hépato-biliaire pour envisager la réparation, cette élévation de morbidité n'est pas retrouvée. Conclusion Dans le but de définir les types de plaies des voies biliaires, plusieurs classifications lésionnelles ont été proposées mais aucune d'entre elles n'est réellement acceptée ou utilisée de façon universelle et univoque. Elles présentent chacune leurs propres limites. L'état général du patient, les conditions péri-opératoires, le moment où la plaie est reconnue et la présence ou non d'un sepsis intra-abdominal ne sont pas pris en compte dans ces différentes classifications. Néanmoins, les classifications de Bismuth et Strasberg semblent les deux classifications les plus communément, en pratique, utilisées par les chirurgiens pour caractériser les plais biliaires faites en laparotomie et maintenant plus généralement en laparoscopie du fait de leur simplicité. Plus complexe la classification dite de "Hanovre" prend en compte à la fois l'atteinte vasculaire et le type lésionnel biliaire par rapport à la convergence biliaire. Les classifications les plus récentes (Lau-Lai et de Hanovre) offrent la possibilité d'une concordance entre le type lésionnel et la stratégie thérapeutique. FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie Bibliographie. 1- Bismuth H. Postoperative strictures of the bile ducts. In Blumgart LH (ed.) The biliary tract V. New York, NY: Churchill-Linvingstone; 1982: 209-218. 2- Bismuth H, Majno PE. Biliary strictures: classification based on the principles of surgical treatment. World J Surg 2001; 25: 1241-1244. 3- McMahon AJ, Fullarton G, Baxter JN, O'Dwyer PJ. Bile duct injury and bile leakage in laparoscopic cholecystectomy. Br J Surg 1995; 82: 307-313. 4- Davidoff AM, Pappas TN, Murray EA, Hilleren DJ, Johnson RD, Baker ME et al. Ims of major biliary injury during laparascopic cholecystectomy. Ann Surg 1992; 215: 196-202. 5- Branum G, Schmitt C, Baillie J, Suhocki P, Baker M, Davidoff A et al. Management of major biliary complications after laparoscopic cholecystectomy. Ann Surg 1993; 217: 532541. 6- McFadyen BV, Vecchio R, Ricardo AE, Mathis CR. Bile duct injury after laparoscopic cholecystectomy. The US experience. Surg Endosc 1998; 12: 315-321. 7- Strasberg SM, Hertl M, Soper NJ. An analysis of the problem of biliary injury during laparoscopic cholecystectomy. J Am Coll Surg 1995; 180: 101-125. 8- Bergman JJ, Van den Brink GR, Rauws EA, de Witt L, Obertop H, Huibregtse K et al. treatment of bile duct lesions after laparoscopic cholecystectomy. Gut 1996; 38: 141-147. 9- Neuhaus P, Schmidt SC, Hintze RE, Adler A, Veltzke W, Raakow R et al. Classification and treatment of bile duct injuries during laparoscopic cholecystectomy. Chirurg 2000; 2000: 71: 166-173. 10- Csendes A, Navarrete C, Burdiles P, Yarmuch J. Treatment of common bile duct injuries during laparoscopic cholecystectomy. Endoscopic and surgical management. World J Surg 2001; 25: 1346-1351. 11- Stewart L, Robinson TN, Lee M, Liu K, Whang K, Way LW. Right hepatic artery injury associated with laparoscopic bile duct injury: incidence, mechanism, and consequences. J Gastrointest Surg 2004; 8: 523-531. 12- Lau WY, Lai E. Classification of iatrogenic bile duct injury. Hepatobiliary Pancreat Dis Int 2007; 6: 459-463. 13- Olsen D. Bile duct injuries during laparoscopic cholecystectomy. Surg Endosc 1997; 11: 133-138. 14- Schol FP, Go PM, Gouma DJ. Risk factors for bile duct injury in laparoscopic cholecystectomy: analysis of 49 cases. Br J Surg 1994; 82: 565-566. 15- Siewert JR, Ungeheuer A, Feussner H. Bile duct lesions in laparoscopic cholecystectomy. Chirurg 1996; 67: 467. 16- Bektas H, Schrem H, Winny M, Klempnauer J. Surgical treatment and outcome of iatrogenic duct lesions after cholecystectomy and the impact of different clinical classification systems. Br J Surg 2007; 64: 1119-1127. FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie PLAIE DES VOIES BILIAIRES RECONNUE EN PER-OPERATOIRE: LES 8 ERREURS A NE PAS COMMETTRE. J. Lubrano, G. Mantion (CHU Besançon) La plaie des voies biliaires complique 0,1% des cholécystectomies par laparotomie et 0,5% des cholécystectomies par coelioscopie avec un risque de plaie sévère multiplié par 4 en coelioscopie. Elles représentent un problème majeur de santé publique avec des conséquences pour le patient, la société et le chirurgien. Si les « règles d’or » de la cholécystectomie et les facteurs de risques de plaie sont bien connus, la conduite à tenir en per-opératoire en cas de plaie des voies biliaires, en dehors des modalités des réparations, est moins codifiée. Ainsi, une fois la plaie faite, il existe à notre sens, 8 erreurs à ne pas commettre. 1. Méconnaître la plaie 2. Ne pas convertir / Ne pas appeler / Ne pas prévenir le malade et/ou sa famille 3. Surestimer ses capacités 4. Ne pas prendre en compte les conditions locales 5. S’acharner à vouloir réparer 6. Croire ce que l’on voit et pense 7. Ne pas prendre en compte les facteurs environnementaux 8. Oublier les règles d’or des réparations 1. Méconnaître la plaie Y penser n’est pas assez. Comme cela a été montré dans la littérature, le taux de détection d’une plaie des voies biliaires en per-opératoire reste faible, variant de 47 à 80% [1]. L’intérêt de la cholangiographie de routine reste discuté tant sur le taux de détection que pour le diagnostic de la gravité des plaies [2, 3]. En Italie et en Grande Bretagne, le taux de plaie des voies biliaires est équivalent au taux français malgré un taux de cholangiographie de routine de seulement 10 et 24% respectivement. Néanmoins, ce taux faible de diagnostic per-opératoire résulte sans doute d’une insuffisance de qualité de lecture des cholangiogrammes. Pour preuve, le taux de reconnaissance est directement corrélé à l’expérience du praticien en chirurgie hépato-biliaire et non à son âge ou à sa durée d’exercice [4, 5]. FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie 2. Ne pas convertir / Ne pas appeler / Ne pas prévenir le malade et/ou sa famille Des cas de réparation en coelioscopie sont rapportés dans la littérature. Néanmoins, devant une plaie sévère, la conversion doit rester la règle. De là même façon, le recours à tiers, non impliqué émotionnellement est d’une aide majeure. En chirurgie, comme dans les jeux télévisés, le « coup de fil à un ami » est nécessaire. Pour cette raison, en Angleterre, il existe la possibilité de recourir à des spécialistes en chirurgie hépato-biliaire se déplaçant sur site, pour la prise en charge dans le même temps opératoire d’une plaie des voies biliaires reconnue [6]. Il est essentiel d’informer le patient à son réveil de cette complication dont les circonstances doivent figurer dans le compte rendu opératoire : le patient a d’ailleurs déjà été prévenu de ce risque certes faible lors de la consultation initiale. Dans tous les cas ne pas informer le patient au moment de la complication va aboutir à une rupture de confiance qui va perturber la prise en charge et ouvrir la porte à des poursuites médicolégales 3. Surestimer ses capacités. Dans la prise en charge d’une plaie des voies biliaires, l’influence du type de chirurgien, spécialiste ou non en chirurgie hépato-biliaire, est un facteur pronostic majeur. Cette influence est vraie tant sur le taux de réussite des réparations, passant de 17 à 95% lorsqu’elle est effectuée par un spécialiste, que sur la diminution du taux de décès des patients, passant alors de 11 à 1,7% [4, 7-9]. 4. Ne pas prendre en compte les conditions locales La prise en charge d’une plaie des voies biliaires doit intégrer les autres données peropératoires. Ainsi, les réparations en milieu septique ont un taux d’échec supérieur [10]. Elles doivent faire renoncer à une réparation idéale et discuter le recours à un drainage biliaire externe. De la même façon, la réparation d’une plaie des voies biliaires survenant dans le cadre d’une pathologie lithiasique de la voie biliaire principale ne se conçoit qu’après s’être assuré de la vacuité de celle-ci. Enfin la réflexion doit intégrer la reconnaissance d’une plaie artérielle associée pouvant conduire à un échec de réparation immédiate ou à distance par phénomène ischémique. La fréquence de ces plaies est estimée dans la littérature à 20% et impliquent majoritairement la branche droite de l’artère hépatique [11, 12]. 5. S’acharner à vouloir réparer Il faut toujours garder à l’esprit que chaque tentative infructueuse de réparation entraîne une perte de substance de la voie biliaire compliquant toute réintervention [13]. Le délai de la réparation restant un facteur pronostic discuté [9, 12], alors que l’expertise du chirurgien non [4, 7, 8], il convient de s’avoir référer le patient plutôt que de s’acharner. FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie En outre, comme cela a clairement été montré, la prise en charge par le même chirurgien non spécialiste est un facteur d’augmentation du taux de procès et du montant des compensations financières allouées au plaignant [14, 15]. 6. Croire ce que l’on voit et pense Au-delà des erreurs techniques et du non respect des bonnes pratiques de la cholécystectomie, la plaie des voies biliaires pourrait s’expliquer par une perception erronée de l’anatomie alors même qu’elle est considérée comme réelle par le chirurgien. Les sciences cognitives nous éclairent sur ce qui détermine une action consciente. La conjonction de stimuli et de la mémoire à long terme dans le subconscient va provoquer la genèse de l’action. En coelioscopie, seuls demeurent les stimuli visuels sans l’apport de la 3ème dimension, ce qui accentue le risque d’erreur d’interprétation. En outre, lorsqu’une situation anatomique est supposée, même si celle-ci est fausse, les mécanismes de rétrocontrôle ne permettent pas toujours une analyse corrigée de la situation. En effet, l’esprit, pour éviter le statu quo et conduire l’action à son terme, maximise les éléments confortant l’interprétation et minimise les informations allant à l’encontre de l’anatomie supposée. Enfin, même informé, l’esprit ne parvient pas toujours à s’affranchir d’une perception erronée. L’exemple du triangle de Kanisza illustre cela (Figure 1). L’œil y perçoit un triangle blanc qui n’est qu’une pure construction cérébrale du fait des formes géométriques noires adjacentes. Néanmoins, même informé de l’erreur, il est difficile de ne pas continuer à voir et croire à l’existence de ce triangle blanc. Ainsi, la tendance sera de toujours vouloir coller à l’anatomie modale, d’une vésicule à droite de la voie biliaire principale raccordée par le canal cystique à angle droit. Toute situation modifiant la perception (modification anatomique ou superposition des éléments) peut conduire à une plaie des voies biliaires sans diagnostic per-opératoire. Ceci a été clairement montré par Hunter et al. [16 ] dans une étude de 252 cas de plaie des voies biliaires, publiée dans Annals of Surgery et ayant donné lieu à de nombreuses controverses [17, 18]. Pour les auteurs, ces mécanismes pourraient expliquer un taux incompressible de plaie et un diagnostic per-opératoire faible. Ainsi, à chaque étape, une check list mental doit faire remettre en cause la véracité des informations visuelles et de l’action qui en découle pouvant permettre d’éviter une plaie des voies biliaires tout comme d’augmenter leur taux de détection une fois celle-ci faite. FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie Figure 1 : Motif de Gaëtano Kanisza Rivista di Psicologia 1955 7. Ne pas prendre ne compte les facteurs environnementaux La chirurgie a bénéficié de l’étude des causes d’accidents appliquée aux domaines à haute technicité telle que l’aviation ou le nucléaire. Ainsi, la notion de « near misses » anglosaxonne ou « incidents évités de justesse » en Français doivent alerter le chirurgien et lui faire remettre en cause la véracité de son action [19]. En outre, la multiplicité de facteurs environnementaux défaillants (nuisances sonores dans la salle d’opération, rotations d’équipes infirmières, matériel défaillant, relation conflictuelle au sein du « couple » anesthésiste-chirurgien) doit alerter le chirurgien sur un sur-risque de plaie des voies biliaires [19]. Ces facteurs aggravants doivent être pris en compte dans l’évaluation final de l’intervention et conduire à rechercher une plaie pouvant être passée inaperçue. 8. Oublier les règles d’or des réparations Quelques règles simples sont à respecter pour toute réparation en cas de plaie des voies biliaires. Toute réparation doit se faire sans tension sur une muqueuse biliaire saine. En cas de recours à une anastomose hépatico-jéjunale, la reconstruction doit se faire sur FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie une anse biliaire de 70cm, passée en transmésocolique à droite de la colica media et comportant un refend sur la voie biliaire gauche, selon la technique de Hepp-Couinaud, pour diminuer le risque de sténose anastomotique. Enfin, toute reconstruction biliaire nécessite un suivi prolongé car ne s’évalue qu’à 10 ans. Références 1. Ludwig K, Bernhardt J, Steffen H, Lorenz D. Contribution of intraoperative cholangiography to incidence and outcome of common bile duct injuries during laparoscopic cholecystectomy. Surg Endosc. 2002 ;16 :1098-104. 2. Flum DR, Koepsell T, Heagerty P, Sinanan M, Dellinger EP. Common bile duct injury during laparoscopic cholecystectomy and the use of intraoperative cholangiography: adverse outcome or preventable error? Arch Surg. 2001 ;136 :1287-92. 3. Fletcher DR, Hobbs MS, Tan P, Valinsky LJ, Hockey RL, Pikora TJ, Knuiman MW, Sheiner HJ, Edis A. Complications of cholecystectomy: risks of the laparoscopic approach and protective effects of operative cholangiography: a population-based study. Ann Surg. 1999 ; 229 : 449-57. 4. Sicklick JK, Camp MS, Lillemoe KD, Melton GB, Yeo CJ, Campbell KA, Talamini MA, Pitt HA, Coleman J, Sauter PA, Cameron JL. Surgical management of bile duct injuries sustained during laparoscopic cholecystectomy: perioperative results in 200 patients. Ann Surg. 2005 ; 241 : 786-92. 5. Massarweh NN, Devlin A, Symons RG, Broeckel Elrod JA, Flum DR. Risk tolerance and bile duct injury: surgeon characteristics, risk-taking preference, and common bile duct injuries. J Am Coll Surg. 2009 ; 209 : 17-24. 6. Silva MA, Coldham C, Mayer AD, Bramhall SR, Buckels JA, Mirza DF. Specialist outreach service for on-table repair of iatrogenic bile duct injuries--a new kind of 'travelling surgeon'. Ann R Coll Surg Engl. 2008 ; 90 : 243-6. 7. Carroll BJ, Birth M, Phillips EH. Common bile duct injuries during laparoscopic cholecystectomy that result inlitigation. Surg Endosc. 1998 ; 12 : 310-3. 8. Flum DR, Cheadle A, Prela C, Dellinger EP, Chan L. Bile duct injury during cholecystectomy and survival in medicare beneficiaries. JAMA. 2003 ; 290 : 2168-73. 9. Stewart L, Way LW. Laparoscopic bile duct injuries: timing of surgical repair does not influence success rate. A multivariate analysis of factors influencing surgical outcomes. HPB (Oxford). 2009 ; 11 : 516-22. 10. Schmidt SC, Langrehr JM, Hintze RE, Neuhaus P. Long-term results and risk factors influencing outcome of major bile duct injuries following cholecystectomy. Br J Surg. 2005 ; 92 : 76-82. 11. Alves A, Farges O, Nicolet J, Watrin T, Sauvanet A, Belghiti J. Incidence and FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie consequence of an hepatic artery injury in patients with postcholecystectomy bile duct strictures. Ann Surg. 2003 ; 238 : 93-6. 12. Bachellier P, Nakano H, Weber JC, Lemarque P, Oussoultzoglou E, Candau C, Wolf P, Jaeck D. Surgical repair after bile duct and vascular injuries during laparoscopic cholecystectomy: when and how? World J Surg. 2001 ; 25 : 1335-45. 13. Tocchi A, Costa G, Lepre L, Liotta G, Mazzoni G, Sita A. The long-term outcome of hepaticojejunostomy in the treatment of benign bile duct strictures. Ann Surg. 1996 ; 224 : 162-7. 14. Perera MT, Silva MA, Shah AJ, Hardstaff R, Bramhall SR, Issac J, Buckels JA, Mirza DF. Risk factors for litigation following major transectional bile duct injury sustained at laparoscopic cholecystectomy. World J Surg. 2010 ;34 : 2635-41. 15. de Reuver PR, Wind J, Cremers JE, Busch OR, van Gulik TM, Gouma DJ. Litigation after laparoscopic cholecystectomy: an evaluation of the Dutch arbitration system for medical malpractice. J Am Coll Surg. 2008 ; 206 : 328-34. 16. Way LW, Stewart L, Gantert W, Liu K, Lee CM, Whang K, Hunter JG. Causes and prevention of laparoscopic bile duct injuries: analysis of 252 cases from a human factors and cognitive psychology perspective. Ann Surg. 2003 ; 237 : 460-9. 17. Lillemoe KD. To err is human, but should we expect more from a surgeon? Ann Surg. 2003 ; 237 : 470-1. 18. Cook RI. Seeing is believing. Ann Surg. 2003 ; 237 : 472-3. 19. Carthey J, de Leval MR, Reason JT. The human factor in cardiac surgery: errors and near misses in a high technology medical domain. Ann Thorac Surg. 2001 ; 72 : 300-5. FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie Prise en charge des plaies des voies biliaires après cholécystectomie. Place de la radiologie interventionnelle P. Chevallier (Nice) Service d’Imagerie Diagnostique et Interventionnelle. Hôpital Archet, Nice Les plaies iatrogènes des voies biliaires interviennent le plus souvent lors des cholécystectomies. Après cholécystectomie laparoscopique, l’incidence de ces complications varie de 0.2% à 0.9% et serait plus élevée qu’en cas de voie d’abord par laparotomie. La mauvaise analyse des éléments anatomiques situés dans le triangle de Calot en raison de phénomènes inflammatoires ou de variantes anatomiques est le plus fréquemment en cause. Les anomalies canalaires ainsi crées correspondent à des solutions de continuité avec fuite de bile et/ou des sténoses, avec des degrés de complexité très différents suivant les cas ; elles peuvent de plus être associées dans près de 40% des cas à des lésions artérielles synchrones et plus tardivement à des calculs. La complexité et le site anatomique de ces plaies biliaires iatrogènes peuvent être définis en utilisant la classification de Strasberg (1) ou celle de Bismuth. La classification de Strasberg comprend cinq stades notés de A à E. Le stade A correspond à une fuite de bile par le moignon du canal cystique, les stades B et C correspondent à la section d’un canal segmentaire ou sectoriel droit sans (stade B) ou avec fuite de bile (stade C). Le stade D correspond à une plaie latérale sur la voie biliaire principale (VBP) et le stade E est divisé en 5 sous-groupes en fonction de la complexité de l’atteinte canalaire suivant sa position par rapport à la convergence biliaire primaire et le nombre d’atteintes. La prise en charge de ces complications en imagerie interventionnelle consiste en la réalisation de drainages biliaires ou de collections de bile, voire beaucoup plus exceptionnellement à l’exclusion de faux anévrysmes artériels hépatiques par voie endo artérielle. Nous ne traiterons pas ici le traitement de ces faux anévrysmes. Indications du traitement percutané mené sous contrôle de l’imagerie Le traitement par radiologie interventionnelle d’une sténose biliaire bénigne a été rapporté pour la première fois en 1974. Depuis cette date beaucoup de données concernant ce type de traitement ont été publiées et ont permis de dégager des indications de drainage FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie radiologique en complément ou substitution des drainages endoscopique ou des réparations chirurgicales. Une lésion simple, unique et sur la voie biliaire principale est traitée en première intention par voie endoscopique. Ce type d’indication représentait près de 75% des sténoses biliaires bénignes traitées dans une étude multicentrique Française rétrospective endoscopique publiée récemment (2). Dans cette étude et tous stades confondus, on notait 66.7% de succès primaire à 19.7±36.6 mois et 82.3% de succès secondaire à 6.4±3.8 ans au moyen de plusieurs prothèses en plastique changées tous les 3 mois pendant 1 an. Des complications étaient observées pour 21.9% des patients et correspondaient en règle à des pancréatites ou angiocholites. En termes de succès clinique, ces chiffres sont peu différents de ceux observés pour des séries radiologiques utilisant des calibrages au long terme ; ceci n’est pas surprenant , un calibrage techniquement identique produisant des résultats identiques. En termes de sécurité, les pourcentages de complication sont aussi voisins de ceux observés pour la voie radiologique ; à ce sujet un guide international des bonnes pratiques défini des pourcentages de complication acceptables pour le drainage biliaire radiologique, avec moins de 5% pour chacune des complications hémorragiques ou infectieuse et moins de 2% de complications pleurales. En dépit de ces données, la voie endoscopique s’est imposée au fil des années sur la voie radiologique en particulier du fait de son apparente plus grande facilité de mise en œuvre ; néanmoins, dans l’étude citée précédemment (2), 22.5% des sténoses ne pouvaient être franchies et dans une autre publiée en 2001 (3) on notait 20% de traitements non réalisés, ce qui parait élevé comparativement à la majorité des séries radiologiques. Au final, la voie endoscopique s’est imposée sur la voie radiologique sans essai randomisé et sans démontrer depuis une supériorité indéniable, en dehors de la non nécessité de laisser une voie d’abord permanente par drain biliaire interne-externe comme c’est le cas avec la voie trans hépatique. Tout ceci doit conduire au moins à proposer un abord trans hépatique pour les patients ayant une lésion simple et sélectionnés pour un traitement endoscopique ayant échoué. Les atteintes complexes sont plutôt traitées par voie chirurgicale, en confectionnant le plus souvent une anastomose bilio digestive. Une étude rétrospective incluant 292 patients ayant eu une anastomose bilio digestive après une plaie biliaire post cholécystectomie montrait 33.3% de morbidité, 1.3% de mortalité et 90% de succès clinique à 9.5 ans (4). Un drainage radiologique peut s’envisager en préparation d’une réparation chirurgicale complexe, chez un patient fragile ou en post opératoire en cas de fistule ou sténose anastomotique. FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie Parmi les atteintes complexes, le traitement d’une plaie d’un canal sectoriel ou segmentaire droits peut être différencié. Ce type de complication correspond aux stades B et C de la classification de Strasberg (1) et représente de 6 à 9% des complications biliaires après laparoscopie. Ces plaies sont liées à l’absence de reconnaissance per opératoire d’une variante d’implantation de ce type de canaux sur le canal cystique ou à proximité de ce dernier sur la VBP. Ces variantes anatomiques sont vues dans 4.8% à 8.4% des cholangiographies per opératoires. Si le canal biliaire incriminé est exclu de la VBP, avec ou sans fistule intra péritonéale, l’opacification biliaire rétrograde endoscopique ne le met pas en évidence et une cartographie biliaire par IRM est particulièrement indiquée. En l’absence de fistule, cette complication est souvent asymptomatique et peut dans ces cas ne pas être traitée. En cas de sténose symptomatique les reconstructions chirurgicales en monothérapie sont associées à des pourcentages élevés de récidives compris entre 33% et 37%. En cas de fistule intarissable, la suture chirurgicale n’est pas recommandée en étant associée à des pourcentages élevés de cholangite et d’abcès. Ainsi pour les patients symptomatiques, une approche multidisciplinaire est nécessaire, la radiologie interventionnelle ayant une place centrale pour le drainage de bilomes, le drainage biliaire en monothérapie ou en préparation d’une intervention chirurgicale réservée aux patients complexes et/ou avec des plaies vasculaires associées. Mise en œuvre du traitement percutané mené sous contrôle de l’imagerie Une cartographie biliaire précise non invasive peut être obtenue par IRM et est très utile pour établir un plan de traitement. Les drainages biliaires sont réalisés en règle sous anesthésie générale et avec une antibioprophylaxie dans une salle de radiologie interventionnelle devant fonctionner comme un bloc opératoire et disposant de multiples techniques d’imagerie. L’abord trans hépatique est sécurisé par l’usage d’un double guidage fluoroscopique et échographique. Pour certaines anastomoses bilio digestives, avec anse fixée en position antérieure, une voie d’abord transcutanée via l’anse grêle montée est possible bien que techniquement plus difficile. Sténose Le meilleur traitement, utilisé également par voie endoscopique, consiste en une dilatation première de la sténose suivi de la mise en place d’un drain interne-externe dont on augmente le calibre en quelques semaines jusqu’à 14 à 16 French. Ce drain est changé tous les mois et est laissé en place au moins 1 an (5). Les plasties seules de la sténose, FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie proposées dans les années 80-90 sont associées à des pourcentages de récidives plus élevés. La mise en place de prothèses métalliques non extractibles n’est pas non plus conseillé avec des pourcentages de perméabilité primaire, très faibles, variant de 25 à 46% à 3 ans et de 0 à 25% à 5 ans. Leur désobstruction devient problématique avec le temps avec un risque de décès par sepsis et leur extraction secondaire est très difficile au prix d’hépatectomies morbides ou impossibles. Des prothèses métalliques couvertes extractibles, en les laissant en place jusqu’à 12 à 15 semaines, pourraient représenter une alternative intéressante bien que devant encore être mieux validées en termes de récidives à long terme et de complications (occlusion de canaux non concernés par la plaie à traiter). La décision d’ôter le drain est établie sur l’absence de signes cliniques, la normalisation ou quasi normalisation biologique et la normalité de la cholangiographie dans la zone traitée. La régression complète de la sténose sur la cholangiographie parait être un facteur prédictif de succès majeur, démontré dés 1985 par les radiologues, puis retrouvé très récemment dans une série endoscopique (2). Fistule Il faut faire un drainage biliaire externe pour quelques semaines et drainer aussi un éventuel bilome associé, sous contrôle échographique ou scannographique. L’injection de produits sclérosants par le drain dans les voies biliaires peut se discuter en cas de secteur exclu avec fistule ne se tarissant pas. Lorsque la fistule est tarie, il se développe le plus souvent une sténose cicatricielle et le drain biliaire est alors laissé en place comme pour le traitement d’une sténose sans fistule. Atteinte hilaire complexe, stades E3 à E5 de la classification de Strasberg On peut drainer plusieurs secteurs exclus les uns des autres avec plusieurs drains en cas de plaies complexes de la convergence biliaire. Néanmoins, pour des raisons de tolérance, on ne met pas plus de deux drains lorsque l’on envisage un calibrage au long cours. Enfin il n’est pas toujours nécessaire d’aborder tous les secteurs exclus, un secteur exclu peu volumineux pouvant rester asymptomatique et s’atrophier dans le temps du fait de la cirrhose biliaire secondaire. Le contrôle de l’opacification par un produit de contraste iodé des différents territoires est important, un secteur opacifié devant être en règle drainé, l’opacification pouvant être septique. Pour ces atteintes complexes, la cartographie biliaire pré thérapeutique par IRM est particulièrement utile et la voie trans hépatique permet un meilleur contrôle de l’opacification des différents secteurs biliaires que ne le permet la voie endoscopique. FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie Calculs biliaires Leur traitement peut être réalisé par voie radiologique antégrade en utilisant les mêmes outils que ceux utilisés par voie rétrograde endoscopique. Résultats du drainage biliaire mené sous contrôle de l’imagerie Anastomoses bilio-digestives Le calibrage à long terme donne des pourcentages de succès primaire compris entre 94% à 97.5% à 1 an, 83% et 93.8% à 2 ans et 70.6% et 77% à 3 ans (5). Une étude récente ayant inclus 39 patients (6) fait état de 61.4% de succès primaire avec retrait du drain à 19±16.1 mois et suivi évolutif de 53.7±28.4 mois. Les complications ne sont pas toujours évaluées de manière identique suivant en particulier les définitions données par la Société Nord Américaine de radiologie interventionnelle. Leur analyse est aussi rendue délicate du fait du caractère rétrospectif de la plupart des études disponibles. A ces limites près, les complications infectieuses ou hémorragiques sont décrites dans 8 à 11.4% des cas (5). Les complications mineures, rencontrées pour au moins la moitié des patients, correspondent essentiellement à l’occlusion du drain, son déplacement ou à une fuite de bile en périphérie de ce dernier ; un changement mensuel du drain et son nursing par du personnel paramédical entraîné réduit de manière considérable ces complications mineures. Plaie d’un canal segmentaire ou sectoriel droit Très peu de données sont disponibles dans la littérature. En cas de fistule, le drainage radiologique du bilome à duré pour une courte série de patients 56 jours en moyenne (7). Pour le traitement de sténoses la prise en charge est en règle multidisciplinaire. Conclusion Avec la chirurgie et l’endoscopie, l’imagerie interventionnelle complète le tryptique d’une prise en charge très spécialisée des plaies iatrogènes des voies biliaires, devant être réservée à des centres de référence pour les cas complexes, et devant être la résultante d’une discussion pluridisciplinaire. FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie Références 1. Strasberg SM, Hertl M, Soper NJ. An analysis of the problem of biliary injury during laparoscopic cholecystectomy. J Am Coll Surg 1995;180:101-25 2. Tuvignon N, Liguory C, Ponchon T, Meduri B, Fritsch J, Sahel J, et al. Long-term follow-up after biliary stent placement for postcholecystectomy bile duct strictures: a multicenter study. Endoscopy 2011;43:208-16 3. Bergman JJ, Burgemeister L, Bruno MJ, Rauws EA, Gouma DJ, Tytgat GN, Huibregtse K. Long-term follow-up after biliary stent placement for post operative bile duct stenosis. Gastrointest Endosc 2001;54:154-61 4. Sikora SS, Pottakkat B, Srikanth G, Kumar A, Saxena R, Kapoor VK. Postcholecystectomy benign biliary strictures – long-term results. Dig Surg 2006;23:304-12 5. Köcher M, Cerná M, Havlik R, Král V, Gryga A, Duda M. Percutaneous treatment of benign bile duct strictures. Eur J Radiol 2007;62:170-4 6. Glas L, Courbière M, Ficarelli S, Milot L, Mennesson N, Pilleul F. long-term outcome of percutaneous transhepatic therapy for benign bilioenteric anastomotic strictures. J Vasc Interv Radiol 2008;19:1336-43 7. Perera MTPR, Monaco A, Silva MA, Bramhall SR, Mayer AD, Buckels JAC, Mirza DF. Laparoscopic posterior sectorial bile duct injury: the emerging role of nonoperative management with improved long-term results after delayed diagnosis. Surg Endosc 2011 (published online):1630-4 FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie PLAIES DES VOIES BILIAIRES AU COURS CHOLECYSTECTOMIE : PRISE EN CHARGE A LA RETARDEE D’UNE PHASE C. Schaaf, J. Gugenheim (Nice) Service de Chirurgie Digestive Centre de Transplantation Hépatique Hôpital de l’Archet 2 BP 3079 06202 Nice email : [email protected] En 1882, Carl Labgenbuch réalise la première cholécystectomie par laparotomie. Un premier cas de plaie de la voie biliaire principale au cours de cette intervention est rapporté en 1888 par Von Riedel. La première réparation immédiate est décrite par Kehr en 1899. La première anastomose bilio-digestive après décollement de la plaque hilaire et utilisation de la branche gauche est réalisée en 1956 par Hepp et Couinaud. Depuis 1987, où Mouret pratique pour la première fois une cholécystectomie sous contrôle coelioscopique, cette voie d’abord est de plus en plus utilisée, jusqu’à devenir l’intervention de référence (1). Le taux de plaies des voies biliaires (PVB) au cours d’une cholécystectomie coelioscopique varie de 0.3% à 0.86% (2-6). La plupart des PVB (70 à 90%) ne sont pas reconnues en per opératoire ; le diagnostic est établi généralement dans les 2 semaines qui suivent l’intervention (en moyenne 10 jours). (4) Diagnostic En post opératoire, le diagnostic de PVB peut être posé grâce à la présence de signes cliniques évocateurs. Ceux-ci sont dus soit à l’écoulement de la bile dans la cavité péritonéale soit à un obstacle sur la voie biliaire principale. La PVB peut être découverte rapidement après l’intervention, ce qui est généralement le cas, ou de manière beaucoup plus tardive (plusieurs mois voire années après la cholécystectomie). FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie Tableaux cliniques précoces - péritonite biliaire : le drainage est le seul geste à réaliser en urgence. Il peut être radiologique si la fuite se manifeste par un biliome. Sinon, une intervention chirurgicale en urgence s’impose pour réaliser une toilette péritonéale et mettre en place un drain sous hépatique. - fistule biliaire externe : écoulement de bile par un drain ou un orifice de trocart. - ictère cholestatique Tableaux cliniques tardifs: - cirrhose biliaire secondaire - tableaux septiques : abcès hépatique, angiocholite. Prise en charge Diagnostic lesionnel La réussite de la réparation biliaire nécessite une compréhension de l’ensemble des lésions, qu’elles soient biliaires ou vasculaires. L’échographie et le scanner permettent le diagnostic d’une fuite biliaire. Une cholangiographie per cutanée ou une cholangioIRM permettent de faire un bilan des lésions biliaires : type, niveau, étendue, et de définir précisément l’anatomie de l’arbre biliaire. (7) La présence d’une plaie vasculaire associée augmente la morbi-mortalité des plaies biliaires (8) et doit donc systématiquement être recherchée. Elle existe dans 7 à 47% des plaies biliaires après cholécystectomie laparoscopique (9, 10) En effet, l’anatomie de la plaque hilaire peut être modifiée par une atrophie d’une partie du foie et une hypertrophie de l’autre partie et la stratégie chirurgicale peut s’en trouver changée. Préparation du patient La préparation du patient est une composante essentielle de la prise en charge. Une fistule biliaire externe pouvant être à l’origine de troubles hydro-électrolytiques, une correction de ces troubles doit être réalisée. De même, la cholestase peut être responsable d’une carence en vitamine K qui doit être corrigée. Le sepsis doit impérativement être contrôlé en pré opératoire par l’instauration d’une antibiothérapie ciblant les germes d’origine biliaire. (11) FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie La dénutrition, l’hypoalbuminémie sont fréquentes et nécessitent un suivi nutritionnel rapproché la survenue de complications post opératoires étant favorisée par ces conditions. (12) Place du traitement endosopique ou radiologique interventionnel Si ces méthodes constituent de bons outils diagnostiques et thérapeutiques de première intention, ils n’ont qu’une place limitée dans la prise en charge définitive des PVB. La cholangiographie et le drainage biliaire percutanés sont deux éléments essentiels de la prise en charge initiale avant la réparation définitive. Les sténoses biliaires et les contre-indications à la chirurgie sont les principales indications de ces méthodes non chirurgicales utilisées seules. Leur taux de morbidité est estimé à 20%. Elles bénéficient d’un taux de réussite à court terme de 92%, taux retrouvé dans une étude rétrospective (13) Cependant elles n’ont pas été évaluées à long terme. La dilatation par voie transpariéto-hépatique ou rétrograde des sténoses et le drainage biliaire au travers de la sténose pendant plusieurs mois donnent également de bons résultats. (14) Place du traitement chirurgical Le but de la prise en charge initiale d’une PVB est d’obtenir une dilatation des voies biliaires afin de pouvoir, dans un second temps, réaliser une anastomose bilio-digestive. Dans certains cas, une résection hépatique voire une transplantation peuvent être nécessaires. 1) Dérivations bilio-digestives : Principes généraux : (15 – 18) - préparation d’un ou plusieurs segments de voie biliaire bien vascularisés en amont de la lésion pour assurer le drainage de la totalité du parenchyme hépatique. - création d’une anse en Y de 70 cm de long (afin d’éviter les reflux biliaires). - réalisation d’une anastomose bilio-digestive de grand calibre sur des tissus de bonne qualité. Elle doit être réalisée sans tension, à points séparés de monofilament résorbable (6/0). Les points sont noués en dehors. Un bon affrontement muco-muqueux doit être recherché. La technique d’Hepp et Couinaud (15) permet de réaliser une anastomose de calibre satisfaisant sur le canal hépatique gauche et est recommandée dans les réparations des PVB. Une anastomose plus basse expose au risque de sténose secondaire à d’éventuelles lésions ischémiques d’électrocoagulation de la voie biliaire principale. La dissection de la voie biliaire doit donc commencer par l’exposition du canal hépatique gauche. La capsule de FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie Glisson est incisée au niveau du bord inférieur du segment IV et la plaque hilaire est progressivement abaissée. Cela constitue la manœuvre principale d’exposition du canal hépatique gauche. La dissection doit cependant rester prudente, notamment dans un tissu cicatriciel et fibreux, en raison de possibles adhérences entre la face postérieure de la voie biliaire principale et de la veine porte. - drainage trans anastomotique : celui-ci n’est pas obligatoire. Sa mise en place doit être décidée au cas par cas en fonction de plusieurs paramètres ; il n’est pas nécessaire si l’anastomose est large (>5mm de diamètre), sur une muqueuse biliaire bien vascularisée, non inflammatoire, non cicatricielle et sans tension (19). Prise en charge des plaies de la voie biliaire en fonction de la classification de Strasberg • En cas de plaie « mineure » (type A de la classification de Strasberg : fuite biliaire à partir du canal cystique ou du lit vésiculaire), un simple drainage sous-hépatique suffit. • En cas de plaie latérale de la voie biliaire principale (type D de la classification de Strasberg), une réparation par suture directe est possible. Elle doit être réalisée au moyen d’un fil monobrin à résorption lente de petit calibre (5/0 ou 6/0). Une suture verticale peut être réalisée en cas de plaie verticale sur une voie biliaire principale (VBP) large. En revanche, une suture transversale est préconisée en cas de VBP fine. Cependant, les mauvais résultats observés de ce type de réparation doivent inciter à la prudence et font conseiller soit une anastomose bilio-digestive, soit un drainage de la région sous-hépatique. • En cas de plaie « majeure », section complète de la voie biliaire principale sans interruption de la convergence et sans lésion vasculaire associée (type E1, 2 et 3 de la classification de Strasberg), une réparation immédiate peut être envisagée. Une anastomose au niveau de la convergence et du canal hépatique gauche (technique de Hepp et Couinaud) réalisée par un chirurgien spécialisé donne de bons résultats (20,21). • En cas de plaie complexe avec interruption de la convergence ou en cas de brûlure ne permettant pas une identification précise du niveau de la lésion, il semble plus prudent de réaliser un simple drainage de la région hépatique et de transférer le patient vers un centre spécialisé. • En cas de plaie vasculaire associée, la même attitude s’impose en l’absence d’un chirurgien rompu aux techniques de réparation vasculaire. Les lésions artérielles (le plus souvent interruption de la branche droite de l’artère hépatique) sont fréquentes après une cholécystectomie. Elles n’entraînent en général aucune conséquence importante et passent le plus souvent inaperçues. Leur incidence après cholécystectomie par voie ouverte a été estimée à 7% (donnée autopsique) (22). FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie 2) Hépatectomies : Elles constituent le plus souvent un geste de deuxième intention après échec de la réparation biliaire. Sa principale indication est l’existence d’une plaie vasculaire associée (8, 24-27). Même si une plaie de l’artère hépatique droite est généralement tolérée (revascularisation par le plexus hilaire, les collatérales diaphragmatiques et rétropéritonéales), elle peut être responsable à distance d’abcès hépatiques, de nécrose ischémique d’une hémi-foie, d’atrophie du foie droit ou d’épisodes d’angiocholite itératifs pouvant conduire à une cirrhose biliaire. (28, 29) 3) Transplantation hépatique : Elle est le seul traitement possible en cas de cirrhose biliaire secondaire évoluée (avec insuffisance hépatique sévère). (30) CONCLUSION : Les PVB secondaires à une cholécystectomie laparoscopique sont des complications relativement rares mais peuvent être graves et menacer le pronostic vital du patient. Fréquemment diagnostiquées en post opératoire, elles nécessitent une prise en charge pluridisciplinaire où la chirurgie tient une place importante. La réussite d’une réparation nécessite une préparation afin d’optimiser les conditions locales et générales et de choisir la meilleure technique. La réparation d’une plaie biliaire doit être réalisée par un chirurgien hépato-biliaire ; la technique de référence est l’anastomose bilio-digestive. Les stratégies telles que la résection hépatique ou la transplantation sont d’indication plus rare mais peuvent s’avérer nécessaires en cas d’évolution défavorable. FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie REFERENCES : (1) Haute Autorité de Santé. Recommandations de pratique clinique : prise en charge de la lithiase biliaire. 2010 (2) Schlumpf R, Klotz HP, Wehrli H et al. A nation’s experience in laparoscopic cholecystectomy. Prospective multicenter analysis of 3722 cases. Surg Endosc 1994;8:35-41 (3) Diamantis T, Tsigris C, Kiriakopoulos A et al. Bile duct injuries associated with laparoscopic and open cholecystectomy : an 11-year experience in one institute. Surg today 2005;35:841-845 (4) Karvonen J, Gullichsen R, Laine S et al. bile duct injuries during laparoscopic cholecystectomy ; primary and long-term results from a single institution. Surg Endosc 2007;21:1069-1073 (5) Cuschieri A, dubois F, Mouiel J. et al. The European experience with laparoscopic cholecystectomy. Am J Surg 1991;161:385-387 (6) Collet D, Edye M, Périssat J. conversions and complications of laparoscopic cholecystectomy. Results of a survey conducted by French Society of Endoscopic Surgery and International Radiology. Surg Endosc 1993;7:334-338 (7) Blumgart L. Surgery of the liver, biliary tract and pancreas. Philadelphie : Sauders, 2007. (8) Robertson AJ, Rela M, Karani J et al. Laparoscopic cholecystectomy injury : an unsual indication for liver transplantation. Transpl Int 1998;11:449-451 (9) Wu YV, Linehan DC. Bile duct injuries in the era of laparoscopic cholecystectomies. Surg Clin north Am 2010;90:787-802 (10) Alves A, Farges O, Nicolet J et al. Incidence and consequence of an hepatic artery injury in patients with postcholecystectomy bile duct stricture. Ann surg 2003;238:93-96 (11) Hochwald SN, Aubry MC, Houle R et al. Association of preoperative biliary stenting with increased postoperative infectious complications in proximal cholangiocarcinome. Arch Surg 1999;134:261-266. (12) Blumgart LH, Kelley Cj, Benjamin IS. Benign bile duct stricture following cholecystectomy : critical factors in management. Br J Surg 1984;71:836-843. (13) Lillemoe KD, Martin SA, Cameron JL et al. Major bile duct injuries during laparoscopic cholecystectomy. Follow-up after combined surgical and radiological management. Ann Surg 1997;225:459-468. (14) Nuzzo G, Giulante F, Giovannini et al. Advantages of multidisciplinary management of bile duct injuries occurring during cholecystectomy. Am J Surg 2008;195:763-769 (15) Hepp J. l’abord et l’utilisation du canal hépatique gauche dans les réparations de la voie biliaire principale. Presse Méd 1956 ;64 :1648-1653 FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie (16) Matthews JB, Blumgart LH. Benign biliary strictures. In : Zinner MJ, Schwartz SI, Ellis H. Maingot’s abdominal operations. Stamford: Appleton & Lange 1997:1803-1834 (17) Sutherland F, Launois B, Stanescu M et al. A refined approach to the repair of postcholecystectomy bile duct strictures. Arch Surg 1999;134:299-302 (18) Launois B, Catheline JM, Maddern GJ. Intrahepatic anastomosoes for malignant and benign biliary obstruction. Arch Surg 1995;130:137-142 (19) Bachellier P, Nakano H, weber JC et al. Surgical repair after bile duct and vascular injuries during laparoscopic cholecystectomy: when and how ? World J Surg 2001;25:13351345 (20) Thomson BN, Parks RW, Madhavan KK, Wigmore SJ, Garden OJ : Early specialist repair of biliary injury. Br J Surg 2006;93:216-20. (21) Perera MTPR, Silva MA, Hegab et al : Specialist early and immediate repair of post- laparoscopic cholecystectomy bile duct injuries is associated with an improved long-term outcome. Ann Surg 2011;253:553-60. (22) Halasz NA : Cholecystectomy and hepatic artery injury Arch Surg 1991;126:137-8. (23) Strasberg SM, Hertl M, Soper NJ. An analysis of the problem of biliary injury during laparoscopic cholecystectomy. J Am Coll Surg 1995;180:101. (24) Madariaga JR, Dodson SF, Selby R et al. Corrective treatment and anatomic considerations for laparoscopic cholecystectomy injuries. J Am Coll Surg 1994;179:321-325 (25) Frilling A, Li J, Weber F et al. Major bile duct injuries after laparoscopic cholecystectomy : a tertiary center experience. J Gastrointest Surg 2004;8:679-685 (26) Davidoff AM, Pappas TN, Murray EA et al. Mechanisms of major bile duct injury during laparoscopic cholecystectomy. Ann Surg 1992;215:196-202 (27) Scott-Conner CE, Hall TJ. Variant arterial anatomy in laparoscopic cholecystectomy. Am J Surg 1992;163:590-592 (28) Mays ET, Wheeler CS. Demonstration of collateral arterial flow after interruption of hepatic arteries in man. N Engl J Med 1974;290:993-996 (29) Schmidt SC, Langrehr JM, Raakow R et al. Right hepatic lobectomy for recurrent cholangitis after combined bile duct and right hepatic artery injury during laparoscopic cholecystectomy : a report of two cases. Langenbecks Arch Surg 2002;387:183-187 (30) Nordin A, Halme L, Makisato H et al. Management and outcome of major bile duct injuries after laparoscopic choelcystectomy : from therapeutic endoscopic to liver transplantation. Liver Transpl 2002;8:1036-1043. FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie NOTES FCC 5 – Prise en charge des plaies des voies biliaires après cholécystectomie