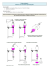COMMENT EXTRAIRE L`HUILE ESSENTIELLE DE L`ECORCE D
Transcription
COMMENT EXTRAIRE L`HUILE ESSENTIELLE DE L`ECORCE D
Spécialité TS
Nom : …………………………… Coéquipier : …………………………….
COMMENT EXTRAIRE L’HUILE ESSENTIELLE DE L’ECORCE D’ORANGE ?
BUT
On se propose
- d'effectuer un entraînement à la vapeur - ou hydrodistillation - de l'huile essentielle d'écorce d'orange constituée
principalement de limonène
Lors du chauffage d'un système non miscible (ici eau - molécules organiques), l'ébullition intervient à une température
inférieure aux températures d'ébullition des corps purs du système. Après condensation du système, on obtient deux
phases.
- de séparer les phases organique et aqueuse dans une ampoule à décanter
Remarque : On cherchera à identifier le ou les produits obtenus par chromatographie sur couche mince (c.c.m.).
Données sur les substances utilisées :
CH3
Limonène :
Masse molaire : 136 g.mol-1
Densité : 0,86
Tébullition : 176°C
Insoluble dans l’eau
Soluble dans le dichlorométhane
CH3
CH2
limonène
Dichorométhane :
Masse molaire : 85 g.mol-1
Densité : 1,326
Tébullition : 40°C
Insoluble dans l’eau
1- Hydrodistillation
Laver les fruits (oranges ou citrons) afin d'éliminer les produits de conservation.
Prélever le zeste d'une orange avec le moins de peau blanche possible.
Couper le zeste en petits morceaux et les placer dans le
ballon.
Ajouter 100 mL d'eau et quelques grains de pierre
ponce.
Effectuer l'hydrodistillation pendant 1 heure environ
Noter la température atteinte lors de la distillation.
Recueillir dans l’erlenmeyer environ 60 mL de distillat
qui contient de l'eau sur laquelle surnagent quelques
gouttes d'huile essentielle.
Noter son odeur.
1) Sur le schéma indiquer la légende de la verrerie et du
matériel utilisé : ballon, chauffe-ballon, support élévateur
("boy"), thermomètre, réfrigérant, erlenmeyer, allonge,
entrée de l'eau de réfrigération, sortie de l'eau de
réfrigération.
2) Justifier le terme d'hydrodistillation. Quelle est la
différence avec une distillation classique ?
-1TS Spécialité Chimie TP2 - Michel LAGOUGE
3) Donner la température atteinte lors de la distillation et justifier.
4) Quelle est la substance qui surnage dans les deux phases récupérées ? (justifier la réponse).
2- Extraction de l'huile essentielle
Introduire le distillat dans l'ampoule à décanter.
Rincer l'éprouvette graduée avec un peu d'eau que l'on versera dans l'ampoule à décanter.
À l'aide d’une petite éprouvette, ajouter 5 mL de dichlorométhane.
le dichlorométhane est un solvant chloré nocif par inhalation ou absorption cutanée. Jeter les déchets dans un flacon
approprié et pas dans l'évier.
L'extraction se fait à l'aide d'une ampoule à décanter.
Agiter (en dégazant plusieurs fois).
Ajouter 3 g de chlorure de sodium solide.
Agiter (en dégazant régulièrement).
Laisser décanter quelques minutes.
Extraire la phase inférieure et la recueillir
dans un petit erlenmeyer bouché de 50 mL
Ajouter à nouveau 5 mL de dichlorométhane
dans l'ampoule à décanter et recommencer les
opérations.
Rassembler les deux phases organiques dans
l’erlenmeyer.
5) Qu'observe-t-on lorsqu'on rajoute 3 g de NaCl
dans l'ampoule à décanter ? Quel est l’intérêt de
cet ajoût ?
L'ampoule ne doit jamais être remplie au-delà des deux tiers de son
volume afin de pouvoir assurer une bonne agitation et éviter les
surpressions trop importantes.
6) Sur le schéma de l'ampoule à décanter placer et nommer les constituants principaux de chaque phase. Justifier le fait que
la phase inférieure soit la phase organique.
-2TS Spécialité Chimie TP2 - Michel LAGOUGE
3- Chromatographie sur couche mince
Dans la cuve à chromatographie, placer un peu d’éluant (toluène-acétate d’éthyle proportion 90/10 en volume) sur un
hauteur d’environ 1/2 cm. Refermer la cuve.
Dans 5 mL de dichlorométhane, mettre 3 gouttes de limonène pur du laboratoire.
Préparer la plaque de chromatographie (ligne de départ,
emplacement des taches).
Sur la plaque de chromatographie, en utilisant une
micropipette différente à chaque prélèvement, faire deux
tâches respectivement avec la solution de limonène extrait et
limonène du laboratoire
Placer 1a plaque dans la cuve à chromatographie contenant
l’éluant et laisser l’élution se produire pendant une dizaine de
minutes, le front de l’éluant doit monter à environ 1 cm du
haut de la plaque.
Une fois l’élution terminée, noter le niveau atteint par le solvant.
Révéler avec une solution de permanganate ou dans des vapeurs de diiode ou observer le tâches avec la lampe UV.
Repérer les tâches obtenues et mesurer les Rf
Définition du R
plaque
d'origine
f
plaque
rélévée
front du
solvant
dsolv
tache après
migration
dsubst
tache initiale
On repère le milieu de la tâche
Le Rf "Retarding Factor" ou "rapport frontal" - est défini par le rapport suivant :
dsubst
R =d
f
solv
Pour un système chromatoplaque-éluant donné, le Rf ne dépend que de la nature
de la substance. Cette grandeur peut donc servir pour identifier une substance
inconnue ou analyser un mélange de substances inconnues.
7) Reproduire soigneusement le chromatogramme sur la figure ci-dessus.
8) Que peut-on déduire de l’examen du chromatogramme ?
-3TS Spécialité Chimie TP2 - Michel LAGOUGE