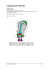III. Influence du pH de la solution - Hal
Transcription
III. Influence du pH de la solution - Hal
Propriétés électrochimiques de la nicotinamide et de ses dérivés en solution aqueuse : III. Influence du pH de la solution et de la concentration de nicotinamide sur la réduction polarographique de ce composé Daniel Thévenot, R. Buvet To cite this version: Daniel Thévenot, R. Buvet. Propriétés électrochimiques de la nicotinamide et de ses dérivés en solution aqueuse : III. Influence du pH de la solution et de la concentration de nicotinamide sur la réduction polarographique de ce composé. Journal of electroanalytical chemistry and interfacial electrochemistry, Elsevier, 1972, 40, pp.197-207. <10.1016/S0022-0728(72)801396>. <hal-01179296> HAL Id: hal-01179296 https://hal.archives-ouvertes.fr/hal-01179296 Submitted on 23 Jul 2015 HAL is a multi-disciplinary open access archive for the deposit and dissemination of scientific research documents, whether they are published or not. The documents may come from teaching and research institutions in France or abroad, or from public or private research centers. L’archive ouverte pluridisciplinaire HAL, est destinée au dépôt et à la diffusion de documents scientifiques de niveau recherche, publiés ou non, émanant des établissements d’enseignement et de recherche français ou étrangers, des laboratoires publics ou privés. Laus n e DE DE SE CONCENTRATION DE CE Avenu Marne, de Universtd Paris-Val 1972) dans m6 e au de r6f enc de concentration de 0-10 augmente. par suive r6duction de lorsque les une des en (vague le pH aqgmente. variations des de nicotinamide potentiels d'Eta Physiques 10- DILU~ES M 10 tous con- solution tr6s dilu6e I) qui cel -ci se d6place vers acide, de pH inf6rieur vague (vague I) asez se d6place aus i vers M. de Ces mileu deuxi6me prot ns -4 demi-vague variations de sont ces les ~t 4, mal les deux lin6aires : solutions la nicotinamide une vague En qui compar bles lorsque cet du pH de la solution sur la posices solutions tr6s dilu6es, nous concentration de r6actif, par sur les r6percus ions que poursur les conclusions quanti- : de pH le pH En COM ANDI~E ~t environ l'influence ensuite pr6sent r. polarographique ap ar itre lorsque STIL ATION inf6rieure une TRES x est AQUEUSES 2 27 de nicotinamide restent quanti ativement en 6videnc polarographiques obtenus pour mur de l'azote pyridnique nous avons entrepris en solution aque se. forment un ensemble en aucun cas d'en d~ uire 1 SOLUTIONS EN MERCURE reviendrons No. 40 DE DE metre vagues de th~se RI~DUCTION GOUT E 1 Chem., ~ * Electroan. Paris. LA de la quaternisation des pyridnes substiu6es, de la nicotinamide publi6es sur ce r6actif -7 et ne permet ent 6tendu LA 10 10 x 2 < (c J. 197 l'importance avril 4 SUR le 2 pH les ph6nom6nes observ6s centration varie. Pour tion et la hauteur des compare ons les r6sultas ex mple -4 M. Nous raient avoir un changement taives que nous alons La r6duction -4 M) fait potentiels plus n6gatifs cet vague est g6n ralement d6fine car proche du potentiels plus n6gatifs La Fig. pr6sent vagues avec le pH des et ont pour expres ion Octobre Multidscpnare, Centr forme Si la concentration la RI~DUCTION revis6 en SUR de ET DE POLAROGRAPHIQUE § DU Partie ET (France) ; 197 INFLUENCE NICOTINAMIDE NICOTINAMIDE SOLUTION LA Dans le but d'ilustrer sur les propri6t s d'oxydo-r6duction l'6tude de la r6duction 61ectrochimque ef t les don 6es 61ectrochimques n'est ni tr~s coh6rent, ni tr6s un comportement g6nral. 1. DE LA Biochmque, 94-Cr~teil Gaule, de G~n&al le d6cembr LA BUVET d'[~nergtiqu 14 pH SUR doctorat CNRS: (1972) A.O 6s-Scien DI~RV]S D. du Labortie et R. Netherlands AQUEUSE DU THI~VENOT in The DE INFLUENCE NICOTINAMIDE (ReCu Electrohmisy ]~LECTROCHIMIQUES SOLUTION EN I. DE COMPOSI~* Printed 614. PROPRIETIES - S_A., Interacil and Chemistry Electroanyi Elsevir Sequoia 197 soutenu par Daniel Th6venot le 14 R. BUVET . THt~VENOT, N 198 D. ~J -0.8 \NH2 10 -4 M -0.6 uel -1.0 • vague --..~ I -1.2. de pH : mV/ENH 10 mV/ENH de vagues haute rs et compositon sur les de capilare potentiels mercue no. 10, demi-vague. de relv6s dans montre 35.0 des solutions le pH ne que stilation g goute cm comde mercue, 10 .4 pr6sent pas CAPIL AIRES POUR LA POLAROGRAPHIE A DES Chem., b 2.16 s-1 0.65 2.54 3.04 3.61 0.63 0.92 8.5-10 6.-74 5.4-60 1.8 1.45 mercue ont 6t de mesur6 en cir uit ouvert, capilre. du inf6reu de l'extr6mi 4.6 4.8-9 1.72 1.92 au-desu corig6es, (1972) 4.07 2.40 2.10 45 libre permut6. l'eau no et d6bits 40 J. Electroan l. de goute mercure 1.83-90 3.50 12.0-8 73 25 20 dans de mercu , de 1.7 4. - 48 5 65 72.5 de D~bit /mg 3.92-45 35 35 Haute rs Temps ° 4.15-3 35 35 35 goute Cb/s 8.6-90 12.5 13.0- 2.1-7 ~ 30 35 6.5 5 65 10 de tl 25 5 45 8 10 Temps libre 2.80 30 10 de 70 30 4 5 30 1 Hauteur mercure /cm 7 3 Longueur /cm 20 COM ANDI~E No. " pH UTILS~ CARCTI~RSTIQUES STIL ATION b sur 1 TABLEAU pH)_+20 pH)_+ des nicotinamide M 8 compar ison Influenc 0.2°C (-690-75 (-970-30 25.0 s, Conditons + I. de nicotinamide polarographiques du M I 10 .4 dif6rents, vague La en E~ E~ I vague vague 0.5 impos6 10 aques = vague I, (O) goute solutions (0) pH = de de 6 4 1. R6duction : Fig. mand6e temps 2 0 -1.4- le capil re 6tan plong6 0.4 ~ + - : - phosphate) nous qui 6gal/t pr6sente et/l 306 SA SUR plus Ib sont de hauteur Ib est g6n raleLa a valeur si le 10. mM lieu co de solutions le courant nicotinamide. inf6rieure ~t 2-5). Pour de nico- ~ 40 (1972) 8) 5 c c ~ M 15 I I 15~o ef t 0.5 _ 7 1 (§1), + 4 4 2 : ?t la concentration A limte en inf~rieure tr6s la concentration de nicotinamide varie tout en restant inf6rieure ~t la °, la vague garde des car ct6ristiques semblables cel s que nous en solution tr~s dilu6e. E½ de la vague varie de moins de mV lorsque dans la m~ e la concentration de nicotinamide pas e de 10-5 la valeur °. est g6n6ralement proportion el ~t la concentration de r6actif. On que log (- Ilim)/A log c= 1.0_+.04 (Fig. 4) et que la hauteur varie au plus de _+ avec (Figs. et dans tout le domaine de c Lorsque pr6c dente de pr6senter Le potentiel tampon nicotinamide un de proces us I Ia Ia 8- joue co 3 de 16 REDUCTION NICOTAMDE SUR COMANDI~E STILAON EN MERCU DE 4.7 autres 1480 (tampon 10 mV/ENH Ip/c est 6.4 des et CONETRAI DE l'6chel pH IV ~t vagues 6. 12, la concentration la pyrimidne de nicotinamide lorsqu'ele d6pas e un certain seuil, sur la nature des observ6s. En ef t, lorsque les solutions de nicotinamide ne vague Iest d6 oubl6e en deux vagues bien distinctes et - Ilim/C La som e des hauteurs relatives. des vagues et hauteur relative de la vague dans la m~ e solution tampon. de nicotinamide au des us de laquele ce remplacement pH. Ele est de 2_ 0.5 mM si le pHest inf6rieur ~t 2, 0.25 entre et 7, mM si le pHest compris entre et vague I dont nous avons signal6 l'existence lors de la r6duction de pH inf6rieur/t n'a pu &re trac6e qu'en soustrayant la solution tampon seul du courant obtenu en pr6sence de en g6n ral observable que si la concentration de ce r6actif est Met ne peut ~tre d6fine que d'une faqon tr6s impr6cise (Figs. raisons nous ne pr6senterons ic que l'efet de la concentration sur la vague I. Chem., Electroan. solution Le courant consta e relative pH 6tudi6. et pH not6 pour Concentration borne venons J. que -Ilim/C 2.1 r61e d6terminant r6duction dilu6es, la dif6rente. ment 6gale de la concentration d6pend du pHest compris La tr6s dilu6es obtenu dans Ele n'est environ 10ces deux tinamide m~ e ac6tae) h De (tampon mM-1 mM- 1 + 3.6 = 3.0 +__ 0.5 pA p.A 0.8 = I 1 INFLUEC GOUTE DE 19 1). s) a 2÷ + de Cd s, T1 impos6 6tait -- LA AQUES des courants limtes mais que d'une solution pr6sentent des 6carts importants (_ 25~). Les darts les m~ es conditons de temperature (25.0_ (0.5 et ont 6t cor ig6s de l'influence du d6bit dif6rent de la valeur rel v6e avec le capilaire no. 10 mercure (Tableau Une 6tude pr6al ble men6e sur la en ef t montr6 que, si le temps de gout e impos6 est proportion el au d6bit la puis ance 0.86_ -- 2. SOLUTIN la valeur obtenues ~t d'influence sy t6matique sur tampon ~t l'autre les valeurs courants limtes ont rel v~s 0.2°C) et de temps de gout e de mercure lorsque ce dernier pour une hauteur de 35.0 cm r6duction des cations et est 6gal/t 0.5 le courant limte En r6sum6 pour: la vague -Ilim/C la vague I -Ilim/C D'autre part,/t pH 4.8 avons observ6 un pic polarographique une hauteur consid6rable/t pA mMrespectivement/ EN NICOTAMDE LA DE I~LECTROHIME BUVET R. THI~VENO, P D. 20 -0,9 >.10 Z 10 I 1° .... -1.2 10 -2 derni~res temps sa nicotamde. de nicotamde. de con, la nicotamde. goute vague sur (pH vague hospate ercu,m I conh, la montre - la concentration vague en portant de pente I de logarithme conh, le la et logarithme le et vague vagu¢ de hauters nieotamd. con, 8, capilre le logarithme le et ¢t min I, vague dans solutin comand6e: mV demi-vagu 250 relativs de la solution log 1/(50_+ as ez dilu6e tend vers que cel -ci [/ (Ilim-I)1 5) mV- la 1. - les h~/uteurs constate en ~ la vague la concentration est de J. Electroanl. On Chem., (1972) que sont suf isamment proportion el es pour les s6par6es, condit ons exp6rimentales el s pr6sentent la concentration comme de cit6es nicoau §1 : des Ia et g6n6ralement en ef t h la vague tinamide. vagues 40 Lorsque ]b 10). de de (0) de Ib (env, sur lorsque de cet e obtenus une droite de Ib, Ia lorsque I g6n6ralement que celui 2,6 et de a, (A) de 1.96) nicoti~amide est comprise entre la valeur 10M, la vagt~e Iest remplac6e par deux vagues notbes sont d'autant mieux s6par6es que la concentration est plus la concentration augmente, le potentiel de la vague augmente 60 mV par d6cade de concentration) puis devient constant tandis diminue (- 30 60 mV par d6cade de concentration) (Figs. + Ia 61ev. b. Ces En ef t (A) 35 cm 1/(E~-E~), par mVforme points sup~rieur 2 d6fine I pr6c6demment no. -1. de tampon co la vague nicotinamide concentration et un co de (O) de I, rep6r e 1/(37_+ 10) et tend vers 1/(5 _+ 5) °. L'analyse logarithmique de la en solution tr~s dilu6e: les du potentiel sont en ef t align6s Lorsque et des cet e Concentraion 2. en des aguesv ed en de de 10 -2 /M polarghiques: stilaon nicotamde Condits ercum la onc, 0.5 pente 10 -3 2 c ~ 6gale valeur est clas ique en fonction les × La 0.2°C, le esl esl hauters logarithme pents potenils 5. s, 25.0_+ de impos6 aguev outeg entr entr entr entr 3. I. Relations Relations Relations elationsR s te 2. de sur Influec 2-5. 4. I, (E) 10 de nieotinamide 4. Fig. Fig. Fig. Fig. libre aguev 6ductionr Figs. concentraion 10 -5 logarithme 10 -3 1 10 "4 10 .2 ~ 10 -5 -3 10 .13 10 -4 .4 10.5 -0.9 201 O I ~C"NH2 _1. > vw= i _1.0 pH _1.2 4.8 "7 ii "-i . . . f-i :~ "°~'%L I i 8'i _IA IV 10 -z -3 10 -s 10 10 "2 1 -'l 10 10 -s 10 -s 10 \ eli _1.6 -4 _1.5 10~ ~ 40 so ! ~ -.L2o 0 10 -2 7. 8. 9. com and6e no. : les les 250 potentiels mV pentes les hauteurs hauteur des dans 4, 35.0 et de vagues relatives relative solution (©) cm un tampon I, (A) vague de mercure, demi-pic ac6tae vague (pH temps de et le logarithme (A) vague gout e de sur libre la conch, sa (0) set Ib, en 8.6 nicotinamide stilation capilaire min-1. de demi-vague en ---~ de nico- et le logarithme de la conch, de nicotinamide. de vague et le logarithme de la conch, de nicotinamide. pic IV et le logarithme de la conch, de nicotinamide. du \~ l _0.9 O!(HCl) _0.7 pH pH ZO (phosphate) de 4.7) la conc , mer ure 6. Figs. 6-9. Influence de r6duction sur goute de pic IV. Conditons polarographiques impos6 0.5 s, 25.0+0.2°C, Fig. Relations entre tinamide. Fig. Relations entre Fig. Relations entre Fig. Relative entre la nicotamide Ia, de : cone traion M 10 -3 / 10 -4 ~ 10 -s -r ° i,., Lira 3k~(formiet ) -. i ./ Z LI . ~_1.1 PH e) ~ 3H 4,8 (acet pH 6. tphosphate) pH 7.2 (imda pH 9.6 (borate) _1.3 zole "'-. L ., ' I .. 40 (1972) (9.57) et borate sa r6duction et le logarithme formiate sur gout e de la cohen, ac6tae de mercure de nicotinamide stilation comdans phosphate (6.4), de demi-vague phosphate sur h nicotinamide (4.7), de -2 (3.61), la conc , les potentiels (pH 10 3 if 0.58), de entre (7.20) : 10. Influence relations chlorhydrique Chem., J. Electroan. Fig. mand6e tampons imidazole 10' / 10 -4 cN~mtraion 'I~-5 " _1.5 (1.96), I,l les 1 1 BUVET 0.9, en et 0.95 pA mM-1 obtenues montrent pr6c dent s neutre ou 16g¢remnt acide 1/(E~- E_~), de la concentration que les vagues soient plus faible ___ mVa) que de la forme des vagues solution concentr6e: les points potentiel sont en ef t, avec une de pente respectivement -1/68 pH dans une solution logarithmique en du fonction des droites I~ et Ib relv6es 1.96), on soustrait la courbe de tampon seul de cel obtenue en pr6senc non d6 oubl6e et la vague I d6j/l d6crite, tr6s n6gatifs (mV/ENH) (Fig. com e le car6 de la concenest inf6rieure environ 10puis vers 10 -2 la concentration tend (Fig. la concentration est inf6rieure ~t 10par d6cade de concentration) pour les con- 2). M 3 4). M 3 x 2 M × 2 it 1230 I (pH 3.6 (1/5 beaucoup 5) d6pend pour 2). M 130 Electroan. a x 2 CONCENTRATION DE NICOTINAMIDE ET DU 40 compris pH darts laquel sont de de pH que de Les lb. I 1): la r6sum6e trois en soit pr6c dents. ou non conti f- I ex mple (Fig. de le pH : 2. et 20 + 75 par Fig. pH finalement fonction de la concentration les trois domaines valeur de la concentration deux vagues Ia et E~-pH de la nicotinamide de ces concentrations, sorte que la vague domaines de pH 1), la vague existe relv6e entre E~ et M 10 concentr6e, entre pH) La 6t 10 a ce compos6 et du mV/ENH 10-3 le diagram e M, la vague potentiel-pH I moyen ement si le pHest (- 690- 7 solution que E~ nicotinamide et dans le Tableau de demi-vague en relv6s dans et 7-10, suivant la remplac6e par les du diagram e Les valeurs num6riques sont choise de tel dans chacun des trois ex mple -4 (Fig. la relation lin6aire 2 ~< pH de de = 0 3 12 1, 1 et montrent de la concentration 10- 4, 10par les vagues En solution tr6s de pH 0-10 ainsi -2 : 12 10, d61imts laquel la concentration polarographique 1 et les potentiels les comportements soit 0-2, 2-7 la vague Iest l'6volution de r6actif. et M, Ia et Ib dilu6e, par que l'indique 1, pH, pour de 10 it avons En J. la r6duction Figs. ilustre vague d6 oubl6e sur quatre dif6rents I ment les conjug 6e Chem., c'est-/~dir remplac6e la vague par R. SOLUTION L'influence solution darts port6s, nicotinamide, nous r6actif Figures fonction LA 10 LA DE ~ DE CONJUGUE (1972) 3. INFLUENCE est 5) 1 - ~ valeurs + la hauteur relative de la vague trois fois plus grande que cel de La pente des vagues I, et lb, rep6 e de nicotinamide. Lorsque cel -ci est sufisam ent bien s6pares, la pente de la vague Ia est cel de la vague (1/30 mVa). L'analyse I, et Ib montrent que cel s-ci sont clas iques obtenus en portant log [/ (Ilim" I)] en asez bon e ap roximation, align6s sur mVet 1/40 mVpour les vagues 10 -2 M. Lorsque, dans le tampon orthophosphate intensit6-potenfiel obtenue en pr6senc de nicotinamide, il ap ar R, outre la vague une trois~me vague not6e I ~t des potentiels Cel -ci aune hauteur qui varie ap roximativement tration de nicotinamide si la concentration tend vers une valeur limte de 370 pA si Son potentiel reste/t peu pr6s constant si puis diminue tr6s rapidement (mV centrations sup6rieures/l 10(Fig. Ib que 0.8 num6riques mileu it et mMmM- THI~VENOT, Ia. 8.2 valeurs Les gA pA 61ev 1.9, des 0.2 0.4 Ib pH = derni¢re + aux cet I!,n/C 3.0 Iur,/C = 1.2-4 9.6 respectivement donc environ - h l'exception Ia la vague la vague pour I~ pour pour - 20 D. n'est I~LECTROCHIME DE NICOTINAMIDE EN CONCENTRATION POTENTIELS DE D-E DEMI-VAGUE -I~4- 7 3.2 : I: pH)+4 I: Ib: Vague (-800-63pH)+20 Vague Ia: (-862-47pH)-1-15 Vague (-660-87pH)+25 mV/ENH varient lin6aremnt _ = 840) vague dans le tampon chlorhydrique 61ev, 15 entre et ~t pH potentiels I1 faut des d'autre 2 [~J~H les 7. 4 _ _+ 20 "~t0 -0,S. mV/ENH mV/ENH i! -2 B -0,7-. mV/ENH _ 63 de disconti ut6 des vagues potentiels 2 les pH) pH) Ib l'absence (- 80 (- 80 - pH) EI/zV(NH) de remarquer et entre 64 I E~ E~ = 2~<pH~<7 7~<pH~<10 (- mV/ENH 63 E~ ___ 10 (-840) = ~< = pH b: Ib demi-vague cet le -3 a ~l de - plus [~ ~DNH NH "Eil/ v )o[ (E (- pour 2~<pH~<3.2 important pH potentiels 635 mV 2 vagues vagueI vagueI: ~ I1 est Iet Ia: = vagueI 10 ~o -1,3- . de 7<pH< Vague (-690-75pH)_ 20 Vague Ia: (-635 -64 Vague (-800-63pH)+15 Vague Ia: (-668-54pH)_10 Vague (-860-56pH)_20 E~ est Ia -- STIL ATION 10 Ia: E~ 2 ~< obtenue la valeur a: 0.6) ~< pH 3.2~< -- SOLUTION selon: 0 1,excption de -- pH)+ Les la solution vague qui LA Ib: Ib: de -- DE Ib: 10 compl+tem nt le pH pH I: 10 t: Vague (-690-75pH)_ 20 10 pH)+10 I: I dif6rent. alors DU POLAROGRAPHIE 3.2<pH< Ib: I I: est avec PAR Ib: 20 Vague (-860-56pH)+20 -o,s -1#i Vague (-690-75pH)_+20 Vague (-970-30 Vague (-840)+ Vague (-800-63pH)+15 Vague (-6 8-54pH)-I-10 Vague (-860-56pH)+20 : M I: 75 10 -z 2<pH< Vague (-690-75pH) Vague (-970-30 Vague (-840)+ M 10 -a ET RELVI~S M 10 -4 NICOTINAMIDE (mV/ENH). E LES LA 0<pH<2 (pH 203 AQUEUSE A DE 7 INFLUENCE SUR COM ANDE, -1,5"- les les (1972) poteniels poteniels de demi-vague de demi-vague vague I, (A) vague et le pH de solutions et le pH de solutions (&) vague 1010- Ib, (O) Ia, com and6c 10-2 2 a 10-3et ~ InfluencedupHsurlar6ductiondesolutionsaqueuses stila on entr entr 40 J. Electroan. goute Fig. Fig. p# Chem., Figs. I1 ct 12. de mcrue 1. Relations 12. Relations p# : ~t SOLUTION 2 TABLEAU LA Men Men Men icotinamidesur (0) vague nicotnamide. nicotnamide. I. 3.2) pH En concentr6e, de la cas ure de la nicotinamide par par du diagram e en ex mple les 10 -2 deux avec lin6airement E½-PH solution le pH M, BUVET la vague qui aqueuse la vague et Ib (Fig. de la solution, vagues de Iest Les vaut dans potentiels une discontinuit6 cete vague tout le de se ~ Electroanl. des positon, en r6actif en termes il serait en Chem., 2.4) + 15 _ pos 6dons Ia obserconpH 7.0 DE varie POLARGHIQUE de la vague dans les solutions de la vague vague de r6duction il ~ nous Ia = _ = - ; chlorhydrique que r6sultas hauteur et de pH de m6canismes fait n6ces aire r6sum6s de cel s mercure les 10-3 3 parfois Tableaux 2, dans la don 6es de M x 4, 5, don 6es ces quelques de mercure stilation (6carts inf6rieurs de pH pr6c6dem ent de la concentration d'6tapes de r6duction une valeur critque qui des 10-4 gout e de 1-3 de que nous avons obtecom and6e de solutions 10M, 50 mV). Ce travail blargit donc con6tudi6. I1 fait 6galement res orti de r6actif sur son mode de r6duction est fix6 par la.valeur de cete cond6pend du pH de la solution. 4 indiqu6e les sur de concentration la r~duction quelques A les la r6duction sur M en 2 aque se non ?t la nicotinamide r6unies pr6cisant avons 7 solutions nous confirment concernent Cel s-ci 40 (1972) 0.6) 20 AQUES aqueuse des 87 (pH mV/ENH mV/ENH __+ 25 mV/ENH pH) pH) rdsultas obtenus est d'une et forme des vagues dif6rents, ne permet de r~actions. de d6terminer tele complexit6 que rel v6e A paraison centration d6fintive nismes solution le nombre -47 relatives que d'interp~taion L'ensemble ant~rieu s 61ectrochimques rap rochons sur gout e bon ac ord domaine pH) (pH ~ 15). r6f. Es ais dondes (1, don 6es nicotinamide en ant6rieures disponibles. stilation libre de et souvent de concentration la Si nous nues par r6duction nous observons un sid6rablement le l'importance fondamentale polarographique: centration par rap ort 4.2 les ~ Les 56 le tampon avec les valeurs des potentiels existe 6galement des potentiels cete premi6re un potentiel si la discontinuit6 nicotinamide La discontinuit6 potentiel de le pH. RELATIFS avec ~ 4.1 Compar ison EN mV/ENH dans LA a NICOTAMDE DISCUON RI~SUI~TA S (- 860(- 862 (- 660- d6form6e 10 pour RI~DUCTON est pH) glycine A telement de lui at ribuer pos ible de savoir du pK de la par ex mple. puisque le de 150 mV avec DES 7 1.9 b: E½ E~ E~ SOLUTIN qu'il est dif cile n'est donc pas v6e au voisnage centr6es, 10est tr6s importante brusquement a: <~ 54 le tampon = vague dans <~ pH 7~<pH~<10 7~<pH~<10 (- 68 = La 0.6 : vague vagueI vagueI Ia - Ib de 50 mV E½ obtenue M est la valeur plus faible, ~< 7 de 2 qui ~< pH : Ia vague l'exception J. pH pKa Ia as ez de pH 6tudi6 remplac6e varient encore pH 7: - LA du du solution domaine demi-vague maintenant 4. la valeur de cel R. 12). rap rocher THI~VENO, Ia part (environ . D. 3.51 204 Pour avec nos yeux d6finr compl6tement des aucune avec la simple com- solutions de con- interpr6tation sfiret6 l'influence ces m6casur les de des la sur faciltan Nous mercue, de technique goute de disque-an eau des cep ndant 205 exp6rimentaux la nature mercue ou/t ausi ap orteait l'61abortin pouvons parm6tres la temp6rature, esayr, hypoth&es partant en interp6taives. r6sultas des disque de car- certainem nt pr6cdents de prola nous transfert ou prop ser finalem nt moins entre La pH voisn de Chem., les (63 mV) E~/ApH A r6duite), 7 de solutions de limtaion la concentration ~ ~ la fois d'un tel de r6actif doit de la hauteur nicotinamide de la cart6is- r6actif. d6pend t L'ap ariton d'adsorption hypoth6se Cet de Les Ib la solution. de r6actions de &re ic de l'intervention ~ observ6 ~ pH et Ia d6oubl6es la concentraion sup l6mentaire ce difcult6 I co 61etrochimqu de vagues la surface nous n'avons lorsque de la m~e l'iodure de h donkes relativs r6actif. prop rtion el Men une des diagr m es E~-pH 10 -4 M, en iodure de Nl-m6thyl quel s observations int6resantes. la r6duction de l'iodure de de la nicotinamide. Cet augment consid6rablem nt 40 (1972) dans 2 ~ ajoute eft, mV), que facile E~ J. Electroan l. d'abord, 70 cel Tout la valeur simultan6e Nl-m~thyl relatifs/L nicotamide des concentraions identi- nicotinamide Nl-m6thyl faible et en nicotinamide nicotinamide en si est mileu pH acide est sup6rieu toujours (augmentaion it ~ conduit quasi que le exmpl 13) (Fig. compar ison et 10, la vague et du reli6 avec Comparisn ques, par des nicotinamide cas rest 10-: solutions La la valeur r6duction sur auc n cel-i des 4.3 dans entre et forme) r6action la fixation Not ns de de les de que improba le. d6 oublem nt fr6quem ent : rejt6 Ia Le de est RH + Ia et lb. est sup6rieu du mode hauteur car vague dans H +2 nicotinamide compr6hensio tiques (posit n, de la concentraion ph6nom6ne ou de produit parise compris ~t pH R+2eVagues bien l'61ectrod. nicotinamide, plut6t/ : -o Men no ce tel RH~ ~ nombre la nicotinamide de particules rep6snte R d'un 10-3 conduirat R+2e-+3H + I: relv6s pouvons la pent de la rapide d'un lent de deux com e interet 10 pour la 0 ~ un plus La un simple. sur transfert L'an - 6gal/~ clasique relativem nt est signfcative pas la vague conduit/ I. mV, 6changs cel-i est r6action le de per- 75 soit non pH polarographiques relv6s les du cor espondant/l mV) 61ectron 61ectrons (si pr6taion vague l'infuenc d'61ectrons le lyse raisonablem nt concentraion vague plus de sur tr6s solution met valeur rap ort concerna t 3/2. interp6taions plausible. Vague I. La juxtapositon des r6sultas et de la concentraion de nicotinamide d'av ncer certaines hypoth&es pour le procesu num6rique de AE~/A pH en solution du nombre de prot ns sur nombre logarithmique de sa forme ay nt montr6 que suposer que m6canisme de de nicotinamide ay nt une influenc I, il est proba le que nous ayions af ire ( E~-E~)= 56 mais plut6t/ un (28 ~< (E~-E,)~< 56 mV). On pourait plausible/t l'ensmble des observations et la quel s dilu6e, poser de 61ectrod/~ cylique informations AQUE SE de des goutes L'utilsation sur tampons. voltam6trie SOLUTION polarographiques chute la voltam6trie ou vagues 61ectrod/l la toues EN les de fr6quenc car t6risques com e concentraion com e bone des LA NICOTINAMIDE dif6rent DE 61ectrohimqu I~LECTROCHIME environ 3. t .... 1~0-4m R. BUVET 1 -4 il i 3 Z -t .o- U,J ;_0,5 \NH2 THI~VENOT, c~O ,I- I ILN 2 CH C ~0 "NH ~ D. ~ 206 _1,0 • 12 Ii I 6 4 2 0 " _1,5 p/ de potentiel de demi-vague- pH nicotinamide (C)-C) et en nicotinamide ~Q- ~) de solutions de mercue goute premi res 6tapes de r6duction ains de 380 mV ~t pH et de lieu, aux situ6e hun deux sup6rieus potentiel Nl-m6thyl6. r6actifs dbriv6 de ces con lusion, pH En situ6e sont la premi6re outre, de r6duction de la tr6s voisn de celui la deuxi6me &ape de en mileu acide les secondes 6tapes de exactem nt au mSe poteniel. de razote h6t rocy lique de la nicotinamide premier puisque cet premi6re simultan~e de prot n. Cet quaternisade la deuxi6me 6tape de r6duction en la charge positve port6e par l'azote h6trodes 61ectrons: une fois cet charge en r6duction de fa~on tr6s sembla e ~t la quaternisation doric beaucoup la fixaton d'un ne n~cesit alors pas de fixaton est par contre san eft sur le potentiel acide. I1 semble donc que ce soit qui favorise beaucoup l'ap roche le radical libre form6 se comporte nicotinamide no r6duite. Rap elons enfi qu'il exist entre ces est relative ~t l'ef t de leur concentration vagues polarographiques de r6duction. nicotinamide entraine des d6placem nts que raugmentaion de la concentraion de la premi6re vague de r6duction. 6tape de 61ectron second du PARTIE est 10. est En des 3 ~ nicotinamide r6duction r6duction E~ pH En deux r6actifs sur une dif6renc importane. le potentiel L'augmentaion et m~e la concentraion de des de poteniels le nombre de de nicotinamide demi-vague, entraine en plus un EXPERIMENTALE de polarographique 40 tampons provena ce n'a d6j~t 6t solutions utils6e, des (1972) Son Chem., J. Electroan. tique. d'impuret6 compositon nicotinamide comportement 61ectroaiv. La La a ROactifs 5.1 5. r6duction sur 7 des mV Cel -ci des Na-m6thyl alors d6 oublement par com and6e. difernce favorise r6duction tion mileu cy lique neutralis6e, la obtenus h La 60 iodure diagram es 1-m6thyl 10-4 Men en stilation des N Compar ison 13. Fig. Fluka indqu6 d6crite et Merk, la pr6senc 1. est de puret6 d'auc ne an lytrace 14. Tableau l'ens mble SOLUTION exp6rimental don e 207 AQUEUSE (ap areils des car ct6ristques et celu ) capiU res utils6 6t de Le indcatrie. 61ectrod d6crite compositon EN les La NICOTINAMIDE 1 Ap areiUage 5.2 LA d6j/L DE a ELECTROCHIMIE com e RgSUMg 6tudi com and6e. observ6e En entre d'une anormalement pH unit6. Aux pH 61ev. sur son vagues mode de hauteur el-m~ e en solutions que la quaternisation d'un premier 61ectronations aque se solution qui et de tr6s son poten- inf6rieurs/t cet La concentraion de r6duction ~lectrodif6rent d6s que la d6pend du pH de la tr6s dilu6es de N1de l'azote pyrisur l'h&6rocy le 4 est tr~s : solutions : stilation (I) nicotinamide utilsant dilu6e en nicotnamide, tiel dimnue de 75 mV vague Iest suive par de nicotinamide aune chimque la vague concentraion est sup~rieure/l solution. La compar ison m6thyl nicotinamide dinque facilte consid6rablem nt mais ne modife que de 10 la r6duction 61ectrohimque la polarographie/~ une m~e vague lorsque le pH augment une vague I de hauteur importance fondamentale Iest de oubl6e en deux une valeur critque des r6sultas obtenus et de nicotinamide montre la fixaton peu l'6nerg6tique des 0 avons en 61ectron Nous ult6rieu s. SUM ARY dilute nisation on the studie wave pH by has In the range hig limtng curent. mode of reduction when this concentration the el ctrochemical nicotinamide are promotes the fixation change the el ctron a drop-time be n conobserv d. 0-4 this wave Concentration of nicotnamide. is higer reduction compared. of first (I) be n unit. lev. a given has consi tent (I) of nicotinamide Over the pH range 0-1 , potential shift -75 mV per pH by second wave (I) of abnormaly fundamental factor in the control of the split into two waves of difernt height pH-dep ndent Dat obtained in solutions of Nl-methylnicotinamide and of the pyridne nitrogen considerably het rocy le ring but does not further a of reduction I Wave mode a a is troled Its half-wave is fol wed The polarography. than of very Quaterel ctron enrgetics. Electroan. 80 Fol. Chim. Chemistry, Hetrocyli in Methods Physical (Ed.) Gaz. 604. Ital., (1950) 132. (196) 31 1459. (1960) Zashi, Kagku Nipon I, Academic Pres, I, Academic Pres, 34. (194) 1 128. (1968) 47. (1972) 429. (1972) 317. 1970, p. Vol. in 39 39 Chemistry, Hetrocyli 647. 196. Mas., Methods Chem., Chem., 1903. (196} (196). Phys., 6 18 ostn,B 197)( Thias, Chim. 268 Paris, (196) 148. Polargphie, de r#.,O , s e r g n o C upl.,S Physical Electroan. Electroan. J. Anal., Jap. 17 Zentralb., Mas on, (Ed.), Exper. Biophysc Electrohim. Inter. Third Journkes Elemnts Chem. KopeckS, 40 J. (1972) J. et G. Ham ouya, in A. R. Katrizky I963, p. 1-08. et R. Buret, et R. Buvet, Chem., 4 6 5 9 8 7 10 15 14 13 12 1 J. Volke London, K. Wenig Y. Okaz ki, R. Pointeau D. Th6venot, D. Th6venot, D. Th6venot, D. Th~venot, D. Th6venot A. Albert London, D. Th6venot D. Th6venot et L. I. Denisovitch, M. Stroc hi et G. Adamo, in A. R. Katrizky p. 296- 7. et M. J. Otsuki, K. Miyas ka et J. Nabikawa, et J. Bonastre, G. Ham ouya et R. Buret, C.R, G. Ham ouya et R. Buvet, J. P. Ciusa, Skulachev 1963, P. V. W. 3 2 1 J. Nak ya, Biokhmya, 81 BI LIOGRAPHIE