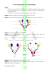Téléchargez
Transcription
Téléchargez
Contrôle du système endocrinien Le système endocrinien est constitué d’un ensemble de glandes situées dans des différentes parties du corps. Elles synthétisent et sécrètent des messages chimiques appelés hormones qui circulent dans tout le corps. Les hormones sont des composés de nature chimique variable : protéines, acides aminés, lipides ou dérivés de stérols qui sont actifs à concentration plasmatique très faible sur des récepteurs tissulaires spécifiques. Les hormones stimulent des glandes ou tissus cibles influençant leurs activités cellulaires, métaboliques et autres et contrôlant la croissance ainsi que la maturation corporelle. Le système endocrinien comprend l’hypothalamus, la thyroïde, les parathyroïdes, le thymus, le pancréas, les glandes surrénales et les gonades. La pathologie endocrinienne consiste en syndrome d’hypo ou d’hyperfonctionnement des différentes glandes endocrines, suivant que leur sécrétion hormonale est augmentée ou diminuée. Toutefois une diminution quantitative ou qualitative des récepteurs sera à l’origine d’un syndrome d’insuffisance malgré des taux hormonaux élevés. Il est nécessaire de connaître les caractéristiques de sécrétion, de transport et d’élimination des hormones. Il faut aussi, bien connaître les mécanismes de contrôle ainsi que les facteurs externes qui peuvent modifier la réponse périphérique. Feed-back L’hypophyse est la glande endocrine la plus importante, elle sert d’amplificateur à l’hypothalamus qui sécrète des substances polypeptidiques stimulatrices ou inhibitrices en quantité très faible dans la circulation. Les hormones hypophysaires sont actuellement dosables dans le sang périphérique. La plupart de ces hormones déclenchent au niveau des glandes cibles la libération d’hormones en concentration plus élevée. Il y’a un effet en cascade dont le point final est l’action métabolique périphérique . . 1 Antéhypophyse Posthypophyse Détermina tion Ac. Am. Pds Mol. TRH Alph a 89 Bêta 112 29 00 0 FSH Alph a 89 Bêta 115 29 000 LH Alph a 89 Bêta 115 29 000 STH 191 21 80 0 PRL 198 22 500 ACTH 39 4500 ADH Ocytocine 9 9 Type Lieu d’action Contrôle hypothalamiq ue. Thyroïde TRH Testicules Ovaires LHRH Métabolisme Foie GRF Ovaires Seins PIF Surrénales CRF Glycoprotéi ne Polypeptide Polypeptide Rein Seins Utérus Principales sécrétions hypophysaires Sécrétion hypothal. Il existe entre les glandes cibles, l’hypophyse antérieure et l’hypothalamus un système de feed-back qualifié de long, court ou ultra court suivant les interrelations. 2 SNC Ultra court Stimuli Hypothalamus RF ou IF Court Hypophyse Stimuline Long Glande périphérique Hormone Il est dit négatif lorsqu’une augmentation de sécrétion par une glande freine la libération hormonale de l’autre glande et inversement, il est positif lorsque les glandes fonctionnent dans la même direction. Par exemple il existe un feed-back long négatif entre cortisol d’une part et CRF, ACTH d’autre part. Feed-back court : des feed-back ultra courts ont été décrits pour la LHRH et la somatostatine. Le Feed-back testicule hypophyse utilise deux médiateurs différents : la testostérone pour la LH et l’inhibine pour la FSH. L’œstradiol exerce un Feed-back positif (milieu du cycle) ou négatif (ménopause) sur la sécrétion de LH suivant les concentrations et le rapport œstradiol/hormones hypophysaires. 3 Le Feed-back peut exister entre une hormone et le produit de son effet périphérique. Par exemple la STH qui ne stimule pas de glande est régulée par la glycémie et la somatomédine. Il en est de même pour des hormones non hypophysaires : insulineglucose, parathormone-calcium. Souvent dans ces cas le système de régulation devient complexe avec intrication de différentes hormones. La glycémie est sous contrôle de nombreux facteurs hyperglycémiants : catécholamines, glucagon, STH… Les amines biogènes: le système adrénergique ou cholinergique et probablement les prostaglandines aussi sont des modulateurs qui interviennent de façon centrale ou périphérique. Les neuropeptides : les endorphines et les enképhalines sont des peptides produits à la fois au niveau du cerveau et de l’hypophyse. En plus de leur rôle de médiateur dans la douleur, les endorphines interviennent indirectement dans la régulation hypophysaire : elles sont stimulatrices pour la GH et la prolactine et inhibitrices pour la TSH, la FSH, la LH, et l’ACTH. Les conséquences pratiques de ces mécanismes physiologiques sont, qu’on peut distinguer en pathologie, des formes primaires, secondaires et tertiaires des atteintes endocriniennes. Par exemple l’hypothyroïdie primaire par lésion de la thyroïde, secondaire par lésion de l’hypophyse et tertiaire par lésion de l’hypothalamus. Dans le syndrome de Cushing, l’hyperfonctionnement peut être dû à une tumeur surrénalienne, à une tumeur hypophysaire ou à une dysfonction hypothalamique. La sécrétion hormonale se fait de façon continue ou pulsatile. Dans certains cas, il existe des cycles réguliers (journaliers ou menstruels) ou bien il y’a réponse à la demande. Le rythme circadien a été bien étudié pour l’ACTH et le cortisol avec un taux élevé le matin et bas l’après midi. Ce genre de rythme peut être constaté pour d’autre hormones telles que la STH, la TSH, la prolactine… le cycle le plus long est le cycle menstruel avec des variations de sécrétions qui se produisent au niveau de l’hypophyse et de l’ovaire. Les variations suivant les demandes métaboliques ou les stimuli nerveux sont particulièrement caractéristiques de l’insuline, de l’adrénaline, de la PTH et de l’AVP. En pratique, le taux hormonal circulant doit être interprété en fonction du moment et des conditions de la prise de sang : à jeun, matin, ou après midi, état de repos ou d’exercice… Les hormones sont sécrétées soit directement sous leur forme active soit sous une forme inactive donnant ensuite l’hormone active. Ce dernier type a été mis en évidence pour l’insuline dont le précurseur est la pro insuline qui pour s’activer perd le peptide C. de même la dihydrotestostérone est le produit actif de la testostérone. La thyroxine est convertie en majeure partie en triodo-thyroxine pour exercer son effet cellulaire. D’autres hormones exercent leur effet par le biais de la somatomédine. 4 Au cours de la synthèse hormonale des blocages métaboliques peuvent entraîner un défaut de formation d’hormone. Ces troubles ont été particulièrement bien étudiés en ce qui concerne la corticosurrénale et la thyroïde. Beaucoup d’hormones particulièrement celles de faible poids moléculaire nécessitent des protéines de transport qui leur sont spécifiques, exemple la transcortine pour les stéroïdes surrénaliens. Il est important de savoir que seule l’hormone libre dans le sang est disponible pour une liaison tissulaire et une activité périphérique. La thyroxine libre, ne représente que 0,04% de la thyroxine totale. Le métabolisme hormonal se fait essentiellement par le foie et le rein. Les hormones sont souvent glyco ou sulfo conjuguées avant d’être éliminées par urines. Toute atteinte hépatique ou rénale peut modifier l’excrétion urinaire hormonale. De plus des lésions de ces organes peuvent modifier les protéines transporteuses et il faut en tenir compte dans l’interprétation des dosages hormonaux. De nombreux médicaments d’origine hormonale ou non peuvent interférer avec la fonction endocrinienne ou les explorations hormonales. Ils peuvent agir de façon centrale (ex. les neuroleptiques) ou en périphérie (ex. les barbituriques qui stimulent la dégradation des stéroïdes au niveau des microsomes intra hépatocytaires). La diphenylhydantoïnes agit à des niveaux multiples : foie, protéine de transport d’où la nécessité de retrouver dans l’anamnèse toutes les prises médicamenteuses qui ont précédé une exploration. Mode d’action des hormones : 1- Au niveau cellulaire, les hormones se fixent sur des sites récepteurs qui leur sont spécifiques et leur activité sera en rapport avec l’affinité de liaison et le nombre de sites récepteurs. Il s’agit en général de polypeptides qui peuvent participer au transport de l’hormone vers le noyau. 2- Les hormones polypeptidiques agissent sur un récepteur membranaire qui déclenche un second messager : AMPc, Ca++ intra cellulaire ou phospholipides. Les actions de ces seconds messagers sont intriqués entre elles particulièrement en ce qui concerne le Ca++ et les phospholipides. Elles subissent des effets inhibiteurs ou stimulateurs d’autres protéines. 3- Il est démontré que le nombre de récepteurs peut être régulé par le taux d’hormone circulante exemple l’insuline pour les récepteurs périphériques insuliniques ou les hormones thyroïdiennes et les glucocorticoïdes pour les récepteurs de TRH. 4- L’implication pratique de ces récepteurs est qu’en pathologie on a décrit des situations où ils pouvaient être absents : dans le testicule féminisant la 5 testostérone normalement sécrétée est activée n’agit pas sur les tissus périphériques. Dosage hormonal : 1- Dosages biologiques : exemple : le taux de gonadotrophines urinaires est mesuré en fonction de l’augmentation de poids de l’ovaire de souris ou de rates impubères après injection des extraits d’urine à tester. 2- Dosages chimiques : ils reposent sur la mesure de la coloration ou de la fluorescence des hormones après transformation chimique : mesure calorimétrique des chromogènes pour les 17 hydroxycorticoïdes et fluorescence de lutines pour la mesure des catécholamines. 3- Dosages radio immunologiques ou radio immuno métriques : il sont très utilisés à cause de leur sensibilité et de leur précision. Ils utilisent la propriété de liaison spécifique d’une hormone avec sa protéine de transport, son récepteur tissulaire ou un anti corps. La mesure se fait sur des variations de radioactivité. 4- Dosages immuno enzymatiques : aussi sensibles et précis que les précédents, auxquels ils peuvent être combinés, ils évitent l’utilisation des produits radio actifs. Ils sont toutefois moins spécifiques. 5- Chromatographie liquide à haute pression et la résonnance magnétique nucléaire sont grâce aux équipements de plus en plus performants, utilisés en hormonologie. 6- Lorsque des mesures directes d’hormones hypophysaires ne sont pas possibles ou trop peu sensibles on peut utiliser des méthodes dynamiques. Dans ce cas les mesures d’hormones circulantes se font avant et après administration d’hormones exogènes. Lorsqu’on a affaire à une insuffisance on utilise des stimulations, exemple : en cas d’insuffisance thyroïdienne on peut stimuler l’hypophyse par la TTH ou la thyroïde par la TSH. En cas d’hyperfonction on peut utiliser des épreuves de freinage : la dexaméthasone dans le diagnostic de l’hypercorticisme permet de différencier la pathologie surrénalienne primaire de la pathologie d’origine haute. 7- Méthodes immunologiques : pour arriver à un diagnostic étiologique on peut mesurer les anticorps spécifiques d’une glande car certains troubles endocriniens sont d’origine immunitaire. Ceci est particulièrement vrai pour la pathologie thyroïdienne. Référence : Ross et Wilson. Anatomie et physiologie normales et pathologiques Bakiri et Benmiloud. Maladies des glandes endocrines Morgan Le Gal. Comprendre la situation clinique par l’anatomie physiologie 6