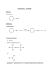2,5-Dimethoxy-4-iodamphetamin (DOI): eine neue
Transcription
2,5-Dimethoxy-4-iodamphetamin (DOI): eine neue
T + K (2006) 73 (2): 57 2,5-Dimethoxy-4-iodamphetamin (DOI): eine neue synthetische Droge des illegalen Marktes G. Fritschi1, P. Rösner2 1 Kriminalwissenschaftliches und – technisches Institut des Hessischen Landeskriminalamtes Hölderlinstr. 5, 65187 Wiesbaden 2 Posenerstr. 18, 24161 Altenholz/Stift Zusammenfassung In einer Abfalllösung, die bei einer Wohnungsdurchsuchung sichergestellt wurde, konnte in einer geschätzten Menge von ca. 2-3 g 2,5-Dimethoxy-4-iod-amphetamin (DOI) bestimmt werden. DOI ist eine nach dem bisherigen Kenntnisstand auf dem illegalen Markt bislang nicht aufgetretene Designerdroge. Bei DOI handelt es sich entsprechend den Ausführungen im PIHKAL [1] um ein potentes Halluzinogen mit einer Dosierung von wenigen Milligramm. Geht man entsprechend der Auffindesituation davon aus, dass es bei den vorgefundenen Mengen um Abfallmengen handelt, sind die eigentlichen Produktausbeuten im 10-20g Bereich anzusetzen entsprechend etlichen tausend Einzeldosen. Das Reinprodukt, Edukte oder Synthesevorschriften konnten jedoch nicht aufgefunden werden. Einleitung Im Zusammenhang mit Ermittlungen wegen des Verdachts des Verstoßes gegen das Chemikaliengesetz, Betäubungsmittelgesetz, Waffengesetz und Sprengstoffgesetz wurden eine Wohnung und dazugehörige Kellerräume eines Chemikalien-Shop-Betreibers durchsucht. Hierbei wurde u. a. eine Vielzahl von brand- und explosionsgefährlichen Chemikalien aufgefunden. Es ist nur schwer vorstellbar, dass diese in einem normalen Wohnhaus noch dazu in dem vorgefundenen Umfang gelagert werden durften. Der Betreiber dieses Shops hatte überdies die Wohnung einem Dritten überlassen, der in Thüringen einschlägig wegen Vergehen gegen das Betäubungsmittelgesetz sowie das Sprengstoffgesetz bekannt ist. In den durchsuchten Räumen wurden überwiegend solche Chemikalien aufgefunden, die sich in das deklarierte Spektrum des Chemikalien-Shops einpassen ließen. Darüber hinaus konnten jedoch auch Vorstufen zur Herstellung von Betäubungsmittel sichergestellt und Anhaftungen von Verbindungen bestimmt werden, die eindeutig Verstöße gegen das Betäubungsmittelgesetz sowie das Sprengstoffgesetz belegen. Sichergestellte Glasgeräte mit typischen Anhaftungen lassen ebenfalls den Schluss zu, dass Betäubungsmittel auch in der Wohnung hergestellt wurden. Material u. Methoden In einer vollständig gefüllten 2,5 l Glasflasche befand sich ein „typischer“ weitgehend aus diversen Lösungsmitteln bestehender Syntheseabfall. Material im Sinne des Untersuchungsauftrags war nur in geringen Mengen enthalten; Nebenprodukte der Amphetaminsynthese sowie Spuren von Amphetamin waren vorherrschend. Der nach extremer Anreicherung der komplex zusammengesetzten Lösung eher zufällige Nachweis von 2,5-Dimethoxyamphetamin (2,5-DMA) wurde zuerst mit der Synthese von 4Brom-2,5-dimethoxy-N-methyl-amphetamin (DOB), das in der Wohnung in kleinen Mengen sichergestellt worden war, in Zusammenhang gebracht. DOB kann über 2,5-DMA durch Bromierung der 4-Position hergestellt werden [2]. T + K (2006) 73 (2): 58 Die detaillierte massenspektroskopische Analyse und das Säure-/Baseverhalten der in der konzentrierten Lösung erkennbaren Komponenten ließ ferner vermuten, dass neben Amphetamin und dem 2,5-Dimethoxyamphetamin möglicherweise eine weiteres Amphetaminderivat enthalten war. Die Ergebnisse der Derivatisierung mit MSTFA, Essigsäureanhydrid, Trifluoressigsäureanhydrid erhärteten den Verdacht, dass es sich bei der unbekannten Verbindung um ein weiteres Dimethoxyamphetaminderivat handeln könne. Aufgrund der massenspektroskopischen Hinweise wurde zwar 2,5-Dimethoxy-4-iod-amphetamin diskutiert, eine eindeutige Identifikation war jedoch mit den im HLKA vorhandenen analytischen Mitteln nicht möglich. Eine NMR-spektroskopische Messung, mit deren Hilfe die Frage beantwortet werden kann, scheiterte primär daran, dass das DOI trotz aller präparativer Anstrengungen nicht in genügender Reinheit aus dem Rückstand isoliert werden konnte. Als Ausweg bot sich die Anwendung einer unabhängigen Synthese [3] an, bei der 2,5-methoxysubstituierte Aromaten bevorzugt in 4-Stellung (untergeordnet in 2-Stellung) iodiert werden. Bei Umsetzung von 2,5-Dimethoxyamphetamin sollte demnach bevorzugt 2,5Dimethoxy-4-iod-amphetamin entstehen. Die 3- bzw. 6-Stellung ist aus energetischen bzw. sterischen Gründen weniger günstig. Die chromatographischen und massenspektroskopischen Daten des in einer unabhängigen Synthese hergestellten DOI und seiner Derivatisierungsprodukte entsprachen in vollem Umfang den entsprechenden Daten der unbekannten Verbindungen, so dass die Annahme einer Substitution des Aromaten in 4-Stellung weitgehend gesichert war. Das synthetisierte DOI stand ferner in ausreichender Menge und Reinheit für eine NMRMessung zur Verfügung und belegte eindeutig die Struktur des 2,5-Dimethoxy-4iodamphetamin. MS-Daten des 2,5-Dimethoxy-4-iodamphetamins und seiner Derivate Das Massenspektrum des 2,5-Dimethoxy-4-iod-amphetamins (Abb. 1) zeigt erwartungsgemäß ein durch α-Spaltung entstandenes Immoniumion als Basispeak bei dem m/z-Wert 44. Bei dem m/z-Wert 278 findet man das durch Umlagerung eines Alkylamino-H-Atoms in die ortho-Position des Aromaten mit nachfolgender α-Spaltung entstandene Radikalkation. 2,5-Dimethoxy-4-iodo-amphetamine 1-(4-Iodo-2,5-dimethoxy-phenyl)propan-2-amine DOI 44 CH 3 . + O + NH2 MW:321.15805 MM:321.02258 C11H16 INO2 H H3C I 77 91 105 GC/MS EI 70 eV TSQ 70 QI:997 H O 53 63 CAS:82830-44-2 RI: 1885 (SE-30) 247 CH3 278 263 Abb. 1. Massenspektrum von 2,5-Dimethoxy-4-iod-amphetamin 321 T + K (2006) 73 (2): 59 Das Massenpektrum des acetylierten 2,5-Dimethoxy-4-iod-amphetamins (Abb. 2) zeigt ein durch Methylabspaltung aus dem Mc Lafferty-Produkt entstandenes Fragment bei dem m/zWert 44. Bei dem m/z-Wert 304 findet man das durch Mc Lafferty-Reaktion (induktiver Zweig) entstandene Radikalkation als Basispeak. Die einfache Benzylspaltung liefert das Fragment bei dem m/z-Wert 277. . 2,5-Dimethoxy-4-iodo-amphetamine AC 304 H 44 MW:363.19533 MM:363.03314 C13 H18 INO3 + + O RI: 2229 (SE-30) O C O N GC/MS EI 70 eV CH3 TSQ 70 QI:996 H3 C + H3 C H O CH3 O I I 363 86 162 105 63 247 277 232 Abb. 2. Massenspektrum von N-Acetyl-2,5-dimethoxy-4-iod-amphetamin Das Massenspektrum des silylierten 2,5-Dimethoxy-4-iod-amphetamins (Abb.3) zeigt das Trimethylsilylkation erwartungsgemäß bei m/z 73 und das durch α-Spaltung entstandenes Immoniumion als Basispeak bei dem m/z-Wert 116. Induktive Abspaltung der ionisierten Silylgruppe liefert das Fragment bei m/z 320; das Fragment der bei Silylderivaten typischen Methylabspaltung ist bei dem m/z-Wert 378 zu finden. 2,5-Dimethoxy-4-iodo-amphetamine TMS 116 CH3 + Si CH3 CH3 CH3 Si N + 73 CH3 CH3 MW:393.34007 MM:393.06210 C14H24INO2 Si + N CH3 O CH3 RI: 2024 (SE-54) H H3C H O CH3 GC/MS EI 70 eV GCQ QI:936 I 45 251 91 150 236 320 278 305 M-15 378 Abb. 3. Massenspektrum von N-Trimethylsilyl-2,5-dimethoxy-4-iod-amphetamin Das Massenpektrum des trifluoracetylierten 2,5-Dimethoxy-4-iod-amphetamins (Abb. 4) zeigt das durch Mc Lafferty-Reaktion (induktiver Zweig) entstandene Radikalkation als Basispeak bei dem m/z-Wert 304. Einfache Benzylspaltung liefert das Fragment bei dem m/z-Wert 277. T + K (2006) 73 (2): 60 . + 2,5-Dimethoxy-4-iodo-amphetamine TFA MW:417.16672 MM:417.00488 C13H15F3INO3 304 O RI: 2023 (SE-54) H3C O + H3 C O O 277 CH3 GC/MS EI 70 eV GCQ QI:965 CH3 I 417 I 150 247 91 105 122 77 232 Abb. 4. Massenspektrum von N-Trifluoroacety-2,5-dimethoxy-4-iod-amphetamin 1H-NMR-Daten Das 300 MHz 1H-NMR-Spektrum der synthetisierten Verbindung zeigt im Bereich der aromatischen Protonen zwei Singuletts bei 6,66 und 7,28 ppm. Auch bei starker Spreizung des Spektrums ist keine Kopplung der aromatischen Protonen sichtbar. Dies belegt die para-Ständigkeit der aromatischen Protonen, da bei einer ortho- oder meta- Ständigkeit eine sichtbare Kopplung der aromatische Protonen eintritt. Aus geometrischen Gründen existiert beim 2,5Dimethoxyamphetamin nur die 4-Positon, deren Substitution para-ständige aromatische Protonen generiert. Alle 1H-NMR-Signallagen sind in guter Übereinstimmung mit den Vorhersagen der NMRDatenbank NMRShiftDB [4]. CH3 1,10 (d) 3,20 (m) 2,60 (d) NH2 O 3,75 (s) 6,66 (s) H3 C 7,218 (2) O CH3 3,81 (s) I Abb. 5. NMR-Daten von 2,5-dimethoxy-4-iod-amphetamin Literatur [1] A. Shulgin, A.Shulgin. PIHKAL-A Chemical Love Story, Synthese #67 [2] A. Shulgin, A.Shulgin. PIHKAL-A Chemical Love Story, Synthese #62 [3] Literaturzitat kann bei den Verfassern abgerufen werden [4] www.nmrshiftdb.org