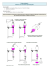2nde Cours Chapitre 2 : Les techniques d`extraction 1.
Transcription
2nde Cours Chapitre 2 : Les techniques d`extraction 1.
Chimie : 2nde Cours Chapitre 2 : Les techniques d’extraction 1. Les techniques d’extraction ancestrales : L’enfleurage : C’est une technique qui permet d’extraire les parfums des fleurs par dissolution dans des graisses. La macération : C’est une technique au cours de laquelle on immerge longuement des matières végétales ou animales dans un liquide froid afin d’en extraire les espèces chimiques solubles dans ce liquide. La décoction : C’est une technique au cours de laquelle on immerge les plantes dans de l’eau froide, puis on porte l’ensemble à ébullition. L’infusion : C’est une technique au cours de laquelle on verse de l’eau bouillante sur des feuilles ou des fleurs pour libérer leurs arômes. Voir exercice d’application n°1 2. Les techniques d’extraction actuelles : 2.1 : L’extraction par solvant : Voir TP2 L’extraction par solvant permet d’extraire une espèce chimique d’un milieu solide ou liquide par solubilisation dans un solvant. Le solvant d’extraction doit satisfaire plusieurs critères : L’espèce chimique à extraire doit être le plus soluble possible dans le solvant d’extraction. Le solvant d’extraction doit être non miscible avec le liquide contenant l’espèce chimique à extraire. Pour effectuer une extraction par solvant on utilise une ampoule à décanter représentée ci-contre : Les différentes étapes d’une extraction par solvant sont les suivantes : Schéma ci-dessous Introduction dans l’ampoule à décanter de l’espèce chimique à extraire et du solvant d’extraction (Robinet de l’ampoule fermé). Agitation du mélange (Bouchon maintenu avec la paume de la main). Dégazage (Bouchon toujours maintenu avec la paume de la main et ouverture du robinet, l’ampoule à décanter étant retournée). Décantation (Bouchon ôté). La densité des espèces chimiques permet de déterminer la phase supérieure et la phase inférieure dans l’ampoule après décantation : L’espèce chimique qui possède la densité la plus faible constitue la phase supérieure. Remarque : la densité notée d est une grandeur sans unité. Voir exercice d’application n°2 Chimie : 2nde 1/4 2.2 : Entraînement à la vapeur ou hydrodistillation : Voir TP3 Une hydrodistillation est la distillation d’un mélange d’eau et d’une espèce chimique à extraire. On porte le mélange à ébullition, la vapeur d’eau qui s’échappe du ballon se charge en huile essentielle. Au contact du réfrigérant à eau, le mélange eau-huile essentielle se condense, et on récupère le distillat. Le distillat possède deux phases superposées, une phase aqueuse et une phase organique qui contient l’huile essentielle. Schéma du montage de l’hydrodistillation Voir exrcice d’application n°3 Chimie : 2nde 2/4 Exercices d’application : Les techniques d’extraction Exercice 1 : Associer à chaque préparation, la technique d’extraction mise en œuvre : enfleurage, décoction, macération, infusion. 1. Préparation d’un vinaigre aromatisé. 2. Préparation d’une tisane. 3. Préparation d’une essence parfumée à l’aide de pétales de fleurs. 4. Préparation d’un fond de veau. 5. Préparation de fruits dans l’alcool. Exercice 2 : Le sucre vanillé est composé essentiellement de vanilline, d’acide vanillique et d’acide hydroxybenzoïque. On cherche à extraire la vanilline du sucre vanillé à l’aide d’un solvant approprié. On dissout le contenu du sachet de sucre vanillé dans 100,0 mL d’eau distillée. On homogénéise le mélange. On introduit le mélange dans une ampoule à décanter puis on ajoute 20,0 mL du solvant choisi. Données : Densité Solubilité de la vanilline dans le solvant Miscibilité avec l’eau Dichlorométhane 1,33 Très bonne Eau 1,00 Très faible Ethanol 0,80 Très faible Nulle Très bonne Dichlorométhane Xn Ethanol F 1. A l’aide du tableau des données, indiquer le solvant le plus approprié pour effectuer l’extraction de la vanilline. Justifier. 2. Quelles sont les consignes de sécurités à respecter pour manipuler le solvant choisi ? Justifier. 3. Quelles sont les différentes étapes d’une extraction par solvant ? 4. Représenter l’ampoule à décanter après l’étape de décantation, légender en justifiant. Exercice 3 : L’extraction de l’huile essentielle de lavande s’effectue à l’aide d’un montage à l’entraînement à la vapeur (ou hydrodistillation) représenté ci-dessous. Chimie : 2nde 3/4 1. Compléter ce schéma en utilisant les termes suivants : Chauffe-ballon/Ballon à fond rond/Support/Distillat/Réfrigérant à eau/Arrivée d’eau froide/Sortie d’eau tiède Support élévateur/Erlenmeyer/Phase supérieure/Phase inférieure. 2. Quel est le rôle de la vapeur d’eau ? Celui du réfrigérant à eau ? 3. Représenter le contenu de l’erlenmeyer après l’hydrodistillation. Justifier. 4. Afin de récupérer l’huile essentielle du distillat, on effectue une extraction par solvant. On introduit dans une ampoule à décanter le distillat, 10,0 mL d’eau salée et 10,0 mL du solvant extracteur. On bouche, on agite, on dégaze et on laisse décanter. Quel est l’intérêt d’ajouter de l’eau salée ? 5. A l’aide des données du tableau ci-dessous, quel solvant extracteur peut-on choisir ? Justifier. 6. Représenter l’ampoule à décanter après décantation. Légender en justifiant. Données : Densité Solubilité dans l’eau Solubilité dans l’eau salée Solubilité dans l’éther éthylique Solubilité dans le cyclohexane Chimie : 2nde Eau 1,00 Eau salée 1,13 Cyclohexane 0,78 Nulle Essence de lavande 0,89 Faible x x x x Nulle Très faible Nulle Nulle Nulle x Elevée x Nulle Nulle x Très élevée Ether éthylique 0,71 Nulle x 4/4