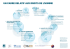le tissu adipeux
Transcription
le tissu adipeux
UNIVERSITE TOULOUSE III – PAUL SABATIER U.F.R sciences de la vie et de la terre THESE Pour obtenir le grade de DOCTEUR DE L’UNIVERSITE TOULOUSE III Discipline : Innovation pharmacologique Présentée et soutenue par Sandra DE BARROS Le 29 octobre 2007 Les métalloprotéases matricielles 2 et 9 et la différenciation des cellules progénitrices du tissu adipeux humain JURY Professeur Marie-Christine RIO Rapporteur Docteur Jean-Philippe BASTARD Rapporteur Docteur Annie QUIGNARD-BOULANGE Examinateur Professeur Philippe VALET Président Docteur Jean GALITZKY Directeur de thèse 1 A mes parents A Christophe, Carole et Adrien, A Laurent. 2 Remerciements En préambule à ce travail, je tiens à exprimer toute ma reconnaissance et mes sincères remerciements à tous ceux qui ont participé de près ou de loin à ce travail. Je tiens à remercier le Professeur Marie-Christine RIO et le Docteur Jean-Philippe BASTARD d’avoir spontanément accepté d’évaluer ce travail en tant que rapporteur. J’exprime également ma gratitude au Professeur Philippe VALET et au Docteur Annie QUIGNARD-BOULANGE pour avoir si gentiment acceptés de participer à ce jury de thèse. Les recherches qui ont fait l’objet de cette thèse ont été effectuées dans l’unité INSERM U858 équipe 1, encadrées par les Docteurs Jean GALITZKY, Virginie BOURLIER, Coralie SENGENES et Anne BOULOUMIE. Je leur suis très profondément reconnaissante de m’avoir apporté leur soutien, leur confiance et leur disponibilité au cours de ces trois années de thèse. Je tiens tout particulièrement à remercier Max LAFONTAN pour ses précieux conseils. Je dis un grand merci à tous les membres (ou ex-membres) de l’équipe des allées et particulièrement à Karine, Alec et Marie-Adeline pour toute l’aide qu’elles ont pu m’apporter. J’adresse mes remerciements à l’ensemble du personnel de l’unité INSERM U858 et plus particulièrement à l’ex-unité INSERM U586 dirigé par le professeur Dominique LANGIN, pour les nombreux services rendus. Une petite attention particulière pour Danièle, Carine et Corinne régulièrement « nounous » des plaques taqman, ainsi que Pascale et Lydia pour toutes les questions administratives que j’ai pu rencontrer… Je tiens également à remercier les personnes du Laboratoire de Pharmacologie Médicale et Clinique, ainsi que celle du Centre de Pharmacovigilance, deux services dirigés par le Professeur Jean-Louis MONTASTRUC que je remercie. Enfin, je ne saurai clore cette partie sans adresser mes sincères remerciements à ma famille. J’adresse un grand merci à mes parents, à mon frère, à Carole et à Adrien. Je remercie également Laurent pour sa présence, sa patience et son soutien quotidien. 3 Table des matières Table des matières 4 Liste des figures 7 Liste des tableaux 9 Principales abréviations utilisées 10 Avant propos 12 Introduction 14 I- Le tissu adipeux 14 A) Les fonctions du tissu adipeux 14 A.1) Les fonctions métaboliques du tissu adipeux 15 A.1.1) Le stockage des lipides : la lipogenèse et la synthèse des triglycérides 15 A.1.2) La mobilisation des lipides : la lipolyse 16 A.2) Les fonctions sécrétoires du tissu adipeux B) Le développement normal du tissu adipeux 17 18 B.1) Le processus de détermination adipocytaire 19 B.2) Le processus de différenciation adipocytaire 22 B.2.1) Les étapes du processus de différenciation adipocytaire 22 B.2.2) Contrôle transcriptionnel de la différenciation adipocytaire 23 B.2.2.1) Les PPARs 23 B.2.2.2) Les C/EBPs 24 B.2.2.3) Le facteur SREBP-1 24 B.2.2.4) Les autres facteurs de transcription 25 B.2.3) Régulation hormonale et intracellulaire de la différenciation adipocytaire 25 B.3) La vascularisation du tissu adipeux 26 C) Le développement excessif du tissu adipeux : l’obésité C.1) Les modifications cellulaires du tissu adipeux 28 29 C.1.1) Les adipocytes et les cellules progénitrices/souches 29 C.1.2) Les cellules endothéliales 29 C.1.3) Les macrophages 30 4 C.2) Les modifications des fonctions métaboliques du tissu adipeux 31 C.3) Les modifications des fonctions sécrétoires du tissu adipeux 32 D) La régression du tissu adipeux : la lipoatrophie D.1) Les modifications cellulaires du tissu adipeux 34 35 D.1.1) Les adipocytes 35 D.1.2) Les cellules progénitrices/souches 37 D.1.3) Les cellules endothéliales 39 D.1.4) Les macrophages 40 D.2) Les modifications des fonctions métaboliques du tissu adipeux 40 D.3) Les modifications des fonctions sécrétoires du tissu adipeux 41 II- Les métalloprotéases matricielles 43 A) Classification et structure 43 B) Les régulations des MMPs 45 B.1) Les Régulations transcriptionnelles et post-transcriptionnelles 45 B.2) Les régulations de la sécrétion 46 B.3) Les processus de maturation des MMPs 46 B.4) Les processus d’inhibition des MMPs 48 C) Mode d’action des MMPs 49 D) Les fonctions biologiques et pathologiques des MMPs 50 III- Les métalloprotéases matricielles dans le tissu adipeux 54 A) La régulation de l’adipogenèse 54 B) La régulation de l’angiogenèse 55 C) La régulation de l’infiltration macrophagique 55 D) Les régulateurs des MMPs dans le tissu adipeux 56 Objectifs 58 Résultats 59 I- Implication des MMPs dans la différenciation adipocytaire des cellules de la fraction stroma-vasculaire du tissu adipeux humain 59 A) Influence d’un inhibiteur des MMPs et des inhibiteurs de la protéase du VIH sur 5 la différenciation adipocytaire 59 B) Influence d’un anticorps neutralisant dirigé contre MMP-9 sur la différenciation adipocytaire 61 C) Détermination des mécanismes impliqués dans la chute de l’expression de MMP-9 par les inhibiteurs de la protéase du VIH 62 D) Études préliminaires et perspectives sur l’étude des cibles moléculaires de MMP- 9 65 II- Implication des MMPs dans la différenciation des cellules CD34+/CD31isolées de la fraction stroma-vasculaire du tissu adipeux humain 68 A) Influence d’un inhibiteur des MMPs sur la différenciation adipocytaire des cellules CD34+/CD31- 69 B) Mise au point d’une condition de culture permettant simultanément les capacités adipogéniques et angiogéniques des cellules CD34+/CD31- 70 B.1) Etude de l’accumulation intracellulaire des triglycérides et de la formation d’un réseau cellulaire positif pour le CD31 par les cellules CD34+/CD31- cultivées dans un milieu mixte 70 B.2) Etude de l’expression en ARNm des marqueurs adipocytaires et endothéliaux par les cellules CD34+/CD31- cultivées dans un milieu mixte 72 B.3) Etude cinétique sur l’évolution des cellules CD34+/CD31- au cours de la culture en milieu mixte. 73 C) Implication des contacts cellule-cellule dans les capacités adipogéniques et angiogéniques des cellules CD34+/CD31- 76 C.1) Influence de la densité cellulaire sur les cellules CD34+/CD31- cultivées en milieu mixte 76 C.2) Influence de la communication cellulaire via les jonctions gaps sur les cellules CD34+/CD31- cultivées en milieu mixte 77 Conclusions et perspectives 80 Références bibliographiques 83 Annexes 103 6 Liste des figures Figure 1 : Le tissu adipeux Figure 2 : Lipogenèse et synthèse des triglycérides dans l’adipocyte Figure 3 : Contrôle de la lipolyse dans l’adipocyte humain Figure 4 : Les sécrétions du tissu adipeux Figure 5 : Détermination et différenciation adipocytaires Figure 6: Evolution de la matrice extracellulaire et de la forme cellulaire au cours de la différenciation adipocytaire Figure 7 : Progression des facteurs de transcription au cours de l’adipogènese dans les préadipocytes de la lignée 3T3-L1 Figure 8 : Balance entre les facteurs de transcription pro- et anti-adipogéniques Figure 9 : Comparaison entre les modifications du tissu adipeux lors d’une obésité ou d’une lipoatrophie Figure 10 : Les métalloprotéases matricielles Figure 11 : Régulation de l’activité des métalloprotéases matricielles Figure 12 : Eléments de liaison aux facteurs de transcription sur les promoteurs des métalloprotéases matricielles Figure 13 : Mode d’action des métalloprotéases matricielles Figure 14 : Effet d’un anticorps neutralisant pour la MMP-9 sur la différenciation adipocytaire des cellules de la FSV du tissu adipeux humain Figure 15 : Hypothèse du mode d’action des IPs-VIH sur l’expression génique de MMP-9 Figure 16 : Influence d’un substrat matriciel sur la différenciation adipocytaire des cellules de la FSV du TA humain Figure 17 : Technique d’isolement des différentes populations de la FSV du tissu adipeux humain Figure 18 : Sécrétion des MMP-2 et -9 au cours de la différenciation adipocytaire des cellules progénitrices CD34+/CD31- isolées Figure 19 : Influence du batimastat sur la différenciation adipocytaire des cellules progénitrices CD34+/CD31Figure 20 : Détermination de l’accumulation des TGs et de la formation d’un réseau cellulaire positif pour le CD31 des cellules CD34+/CD31- cultivées en milieu adipogénique, endothélial ou mixte 7 Figure 21 : Détermination de l’expression en ARNm des marqueurs adipocytaires et endothéliaux des cellules CD34+/CD31- cultivées en milieu adipogénique, endothélial ou mixte Figure 22 : Evolution du contenu en ADN, TGs et du réseau cellulaire positif pour le CD31 des cellules CD34+/CD31- cultivées en milieu mixte Figure 23 : Evolution de l’expression en ARNm des marqueurs adipocytaires et endothéliaux des cellules CD34+/CD31- cultivées en milieu mixte Figure 24 : Influence de la présence de cellules endothéliales matures sur la formation du réseau cellulaire positif pour le CD31 des cellules CD34+/CD31- cultivées en milieu mixte Figure 25 : Influence de la densité cellulaire sur les capacités adipogéniques et angiogéniques des cellules CD34+/CD31- cultivées en milieu mixte Figure 26 : Evolution de l’expression en ARNm des connexines 43 et 45 des cellules CD34+/CD31- cultivées en milieu mixte Figure 27 : Effet d’un inhibiteur des jonctions gaps sur les capacités adipogéniques et angiogéniques des cellules CD34+/CD31- cultivées en milieu mixte 8 Liste des tableaux Tableau 1: Les différents modèles de culture cellulaire utilisés pour l’étude de l’adipogenèse Tableau 2: Facteurs extracellulaires et molécules de signalisation régulant l’adipogenèse Tableau 3 : Classification des adultes maigres, normaux, en surpoids et obèses selon l’IMC Tableau 4: Sécrétions du tissu adipeux modulées ou non au cours de l’obésité Tableau 5: Classification des différentes lipoatrophies humaines Tableau 6: Impact des IPs-VIH et des INRTs sur les sécrétions adipocytaires in vitro et in vivo Tableau 7: Classification des métalloprotéases matricielles Tableau 8 : Les activateurs des MMPs Tableau 9: Phénotypes des souris déficientes pour les MMPs Tableau 10: Les inhibiteurs des MMPs dans le cancer Tableau 11: Composition des milieux adipogénique, endothélial et mixte utilisés Tableau 12: Détermination de l’expression en ARNm des marqueurs adipocytaires et endothéliaux par des adipocytes matures, des cellules progénitrices CD34+/CD31- et des cellules endothéliales capillaires CD34+/CD31+ Tableau 13: Expression en ARNm des connexines 43, 45, 40 et 37 dans des adipocytes matures, des cellules progénitrices CD34+/CD31- et des cellules endothéliales capillaires CD34+/CD31+ 9 Principales abréviations utilisées ACC : Acetyl Co-A carboxylase ADAM: A Disintegrine And Metalloprotease domain AGA: 18α-glycyrrhetinic acid AGNE: acide gras non estérifié AP-1: Activator protein-1 aP2 : fatty acid binding protein ATGL : adipocyte triacylglycerol lipase bFGF : basic fibroblast growth factor bHLH : basic helix-loop helix BMP : Bone morphogenetic protein CD : Cluster de différenciation C/EBP : CCAAT/enhancer binding protein CHOP-10 : C/EBP homologous protein 10 CRABP-1 : Cytoplasmic retinoic acid binding protein-1 ECBM : Endothelial cell basal medium ECGM : Endothelial cell growth medium FAS : Fatty acid synthase FSV: Fraction stroma-vasculaire GLUT : Glucose transporteur GZA : glycyrrhizic acid IDV : Indinavir IGF : Insulin growth factor IκB: Inhibitor NF-κB IL : Interleukine IMC : Indice de masse corporelle INRT : Inhibiteur nucléosidique de la réverse transcriptase INNRT: Inhibiteur non nucléosidique de la réverse transcriptase IPs-VIH : Inhibiteur de la protéase du VIH LHS : Lipase hormono-sensible LPL : Lipoprotéine lipase MCP-1 : Monocyte chemoattractant proteine 1 10 MEC : Matrice extracellulaire MMP : Métalloprotéase matricielle MT-MMP : Métalloprotéase matricielle de type membranaire NF-κB : Nuclear factor kappa B NFV : Nelfinavir PAI-1 : Plasminogen activator inhibitor 1 PDGF : Platelet-derived growth factor PKA : Protein kinase A RT-PCR :Real-time polymerase chain reaction RTV : Ritonavir RXR : Récepteur de l’acide 9-cis-rétinoique SDF-1 : Stromal cell-derived factor-1 SQV : Saquinavir SREBP: Sterol regulatory element binding protein TA : Tissu Adipeux TCF/LEF : T-cell factor/lymphoid enhancer factor TIMP : Tissue inhibitor of matrix metalloproteinases TGs : Triglycérides TNF-α : Tumor necrosis factor α VEGF : Vascular endothelial growth factor VIH : Virus de l’immunodéficience humaine VLDL : Very low density lipoprotein vWF : von Willebrand Factor 11 Avant-propos Le tissu adipeux (TA) adulte peut subir des processus de développement excessif (surpoids, obésité) mais aussi des processus de régression (lipoatrophie). Ces deux phénomènes entraînent des altérations de la composition cellulaire et des fonctions du TA. Il est désormais reconnu qu’un excès ou une perte de masse grasse constitue un facteur aggravant de nombreuses pathologies telles que le diabète de type 2 et les désordres cardiovasculaires. Le surpoids touche, aujourd’hui, près d’un milliard de personnes à l’échelle de la planète, soit un sixième de la population mondiale. Parmi elles, 300 millions sont obèses et l’obésité infantile est en plein essor. Les causes de l’obésité sont multiples et dépendent aussi bien de facteurs génétiques qu’environnementaux. A l’heure actuelle, quelques médicaments avec une indication pour l’obésité (orlistat, sibutramine) ont été développés mais leur efficacité reste insuffisante. Les syndromes de lipodystrophies étaient des événements rares (moins de 1 cas sur 100000) et de causes principalement génétiques. Ces dix dernières années sont apparues des formes de lipodystrophies liées aux traitements antirétroviraux de l’infection par le virus de l’immunodéficience humaine (VIH). En effet, si l’utilisation des inhibiteurs de la protéase du VIH (IPs-VIH) et des inhibiteurs nucléosidiques de la reverse transcriptase (INRTs) ont permis de diminuer significativement la morbidité et la mortalité des patients infectés par le VIH, plus de 50% des patients traités ont développé un syndrome lipodystrophique se caractérisant par une redistribution des dépôts adipeux et des complications métaboliques. Le signe clinique majeur du syndrome lipodystrophique est une lipoatrophie au niveau de la face et des membres associée ou non à une accumulation du TA au niveau des régions dorsocervicales et abdominales. Quelques approches thérapeutiques pour le traitement des lipoatrophies ont été développées (thiazolidinedione, metformine) mais elles agissent plus sur les complications métaboliques associées que sur l’altération du TA elle-même. Ainsi, une meilleure connaissance des mécanismes impliqués dans l’extension et la régression de la masse grasse est maintenant nécessaire afin d’identifier de nouvelles cibles thérapeutiques. Dans ce chapitre d’introduction, nous allons dans une première partie nous intéresser au TA, à ses fonctions et à son développement normal. Nous aborderons aussi les modifications tant cellulaires que fonctionnelles que le TA subit lors d’une obésité ou d’une lipoatrophie. Puis dans une deuxième partie, nous nous intéresserons aux principaux acteurs 12 impliqués dans la régulation des phénomènes de remodelage tissulaire, les métalloprotéases matricielles ou MMPs. Leur classification, leur structure ainsi que la régulation de leur activité seront présentées. Enfin, leur mode d’action et les fonctions biologiques auxquelles ces protéases sont associées seront décrits. Enfin nous aborderons le rôle potentiel de ces enzymes dans la plasticité du TA. Nos travaux de recherche portant sur la caractérisation (i) du rôle de la MMP-9 dans les processus de différenciation adipocytaire et (ii) des interactions entre les inhibiteurs de protéases utilisées lors de la thérapie du VIH avec les voies dépendantes de MMP-9, seront ensuite exposés. Enfin, une dernière partie de notre travail portant sur la caractérisation des cellules progénitrices du TA humain en condition de culture permettant d’exprimer leurs capacités angiogéniques et adipogéniques sera décrite. 13 Introduction I. Le tissu adipeux Le tissu adipeux (TA) est doué d’une importante plasticité. Il est en effet capable de croître ou d’involuer de manière spectaculaire. Avant de nous intéresser au développement excessif du TA ainsi qu’à sa capacité de régression, un aperçu de la fonction propre du TA nous semble nécessaire. A) Les fonctions du tissu adipeux Deux grands types de TA sont présents chez les mammifères : le TA blanc et le TA brun. Ces deux tissus ont des propriétés biochimiques et fonctionnelles distinctes. Le TA brun se retrouve surtout chez les rongeurs et, chez l’homme, il est initialement présent chez le nouveau-né et joue un rôle clé dans la gestion de la thermogenèse (libération d’énergie sous forme de chaleur). Le TA blanc, dont nous parlerons exclusivement dans la suite de ce travail, constitue la principale réserve d’énergie de l’organisme. Il comprend différents dépôts anatomiques localisés dans les territoires sous-cutanés et viscéraux. Cette notion de localisation du TA est essentielle puisque selon que le TA soit sous-cutané ou viscéral, son organisation cellulaire va varier ainsi que son activité métabolique et sécrétoire (81, 136, 270). Au cours de ces dernières années, les recherches sur le TA ont permis de faire émerger les concepts et rôles clés du TA dans le contrôle des flux métaboliques ainsi que la notion de TA endocrine. Ainsi, le TA n’est plus décrit comme un simple tissu de soutien et de protection. Les adipocytes sont le type cellulaire majeur du TA. Ils assurent la fonction métabolique du tissu (stockage et dégradation des triglycérides (TGs)) mais sont également considérés comme une source cellulaire des sécrétions du TA. L’adipocyte est caractérisé par une morphologie polygonale et une grande taille avec un diamètre moyen de 70µm chez le sujet normo-pondéré. La quasi-totalité de la cellule est occupée par une unique vacuole lipidique et le cytoplasme et les organites constituent un fin liseré périphérique (figure 1A). Ces caractéristiques ainsi que sa flottaison in vitro permettent de le distinguer et de l’isoler facilement de la fraction non adipocytaire du TA, la fraction stroma-vasculaire (FSV), 14 A Noyau de l’adipocyte Membrane cytoplasmique de l’adipocyte Vacuole lipidique B Adipocyte Macrophage Préadipocyte Cellule souche/ progénitrice Figure 1 : Le tissu adipeux (A) Morphologie des adipocytes (B) Composition cellulaire Microcirculation contenant principalement des cellules progénitrices/souches, des cellules vasculaires et des cellules immuno-inflammatoires (figure 1B). A.1) Les fonctions métaboliques du tissu adipeux Brièvement, nous aborderons dans les paragraphes suivants les mécanismes et les voies de régulation des principales fonctions métaboliques adipocytaires : le stockage des lipides (lipogenèse et synthèse de TGs) et leur dégradation (la lipolyse). A.1.1) Le stockage des lipides : la lipogenèse et la synthèse des triglycérides Le stockage des lipides dans l’adipocyte se fait par 2 voies (figure 2). La première voie correspond à la capture directe des TGs associés aux chylomicrons et aux lipoprotéines de très faible densité (ou VLDL pour « very low density lipoprotein ») circulants, provenant de l’alimentation ou de la lipogenèse hépatique. La LPL (lipoprotéine lipase), produite et sécrétée par les adipocytes, est ancrée par des protéoglycanes à héparane sulfate à la surface endothéliale (87). En coopération avec GPIHBP1 (glycosylphosphatidylinositol-anchored high density lipoprotein-binding protein 1) récemment décrite comme étant exprimée à la surface endothéliale et comme jouant le rôle de récepteur potentiel aux chylomicrons et VLDL, la LPL hydrolyse les lipoprotéines (11, 297). Les acides gras non estérifiés issus de ce clivage sont ensuite recaptés par l’adipocyte, qui les transforme alors en acyl-Co enzyme A (Acyl-CoA). Ils seront ré-estérifiés en TGs en présence de glycérol. La deuxième voie correspond à la lipogenèse de novo. Le terme de lipogenèse proprement dit désigne la néosynthèse d’acides gras à partir du glucose. Après l’entrée du glucose dans l’adipocyte, grâce à des transporteurs spécifiques (GLUT-1 et 4), le glucose est dégradé en pyruvate par le processus de la glycolyse. A partir du pyruvate, l’acétyl-CoA carboxylase (ACC) et la synthase des acides gras (FAS, « fatty acid synthase ») interviennent de façon successive pour catalyser la formation des acides gras à longue chaîne saturée. L’action des différentes désaturases permet de synthétiser des acides gras plus ou moins saturés. Comme précédemment, ces acides gras sont ensuite ré-estérifiés pour donner les TGs. Il est nécessaire de préciser que chez les rongeurs, la lipogenèse est réalisée dans le foie et le TA. Par contre, chez l’homme, la lipogenèse est majoritairement hépatique et elle n’est qu’accessoire dans le TA (145), excepté suite à un régime alimentaire riche en glucides (105). De nombreux facteurs endocrines et paracrines tels que les catécholamines, l’hormone de croissance et la 15 Glycéro l-3-P DHAP Glucose-6-P Pyruvate Acétyl-CoA Estérification ACC Malonyl-CoA TG Glucose GLUT FAS Palmitate Acyl-CoA Glucose AGNE LPL Transporteur TG: Chylomicrons VLDL AGNE LPL Glycolyse Lipogenèse de novo Origine alimentaire des acides gras Vaisseau capillaire Figure 2 : Lipogenèse et synthèse des triglycérides dans l’adipocyte GLUT: glucose transporter; DHAP: dihydroxyacétone phosphate; TG: triglycérides; ACC: acétyl Coenzyme A (CoA) carboxylase; FAS: fatty acid synthase; AGNE: acide gras non estérifié; LPL: lipoprotéine lipase; VLDL: very low density lipoprotein D’après Fève B., Médecine clinique, 2003 leptine sont capables de contrôler le stockage des TGs mais le facteur majeur est l’insuline qui stimule cette voie en augmentant le captage du glucose via le recrutement du transporteur GLUT-4 à la membrane, et en activant les enzymes glycolytiques et lipogéniques (120). De façon intéressante, les effets inhibiteurs de la leptine et de l’hormone de croissance sur le stockage des TGs passent par l’inhibition des effets stimulateurs de l’insuline. A.1.2) La mobilisation des lipides : la lipolyse La lipolyse assure la dégradation des TGs contenus dans les vacuoles lipidiques de l’adipocyte, en glycérol et acides gras non estérifiés. Plusieurs lipases interviennent de façon séquentielle dans cette hydrolyse des réserves lipidiques (figure 3). La lipase hormonosensible (LHS) clive les TGs en diglycérides puis les diglycérides en monoglycérides, et constitue l’enzyme limitante du processus lipolytique. La lipase des monoglycérides (LMG) dégrade ensuite les monoglycérides en glycérol et acides gras non estérifiés. Cependant, la mise en évidence d’une activité lipolytique diminuée mais toujours présente chez des souris invalidées pour le gène de la LHS a laissé supposer l’existence d’au moins une autre lipase capable d’hydrolyser les TGs dans les adipocytes (196). Trois laboratoires différents ont identifié une nouvelle lipase dénommée « adipocyte triacyglycerol lipase » (ATGL), isoforme ζ d’une phospholipase indépendante du calcium (iPLA 2 ζ) ou desnutrine (113, 277, 303). L’ATGL jouerait un rôle clé dans la lipolyse basale, mais l’hydrolyse des TGs et des diglycérides par la LHS demeurerait l’étape limitante dans la lipolyse stimulée par les principaux agents lipolytiques chez l’homme, les catécholamines et le peptide atrial natriuretique (142). Les mécanismes susceptibles de réguler l’activité de la LHS sont bien connus et sont présentés dans la figure 3 (135). L’activité de cette lipase dépend spécifiquement de sa phosphorylation réversible par une kinase dépendante de l’AMPc (PKA) (100) ou du GMPc (PKG) (240). La phosphorylation de la LHS active l’enzyme, en démasquant le site catalytique. Par ailleurs, cette phosphorylation permet une redistribution de la lipase du cytoplasme vers la vacuole lipidique. Les périlipines, protéines abondamment exprimées à la surface des gouttelettes lipidiques, interviennent dans la localisation et la stabilisation de la LHS à la surface des vacuoles. La phosphorylation des périlipines par la PKA et la PKG réduit leur ancrage à la gouttelette lipidique et favorise ainsi l’accès de la LHS à ses substrats lipidiques. 16 Activation Noradrénaline Adrénaline (β1- β2-AR) Parathormone (PTH-R) Gs Membrane Plasmique KHD αs GC GTP GMPc γ β + R C R C PKG PKA γ α β i PI3K PKB Akt P-Tyr-P + + - 5’-AMP R C R C Gi ATP AMPc + Inhibition Inhibition Adrénaline (α2A-AR) Insuline (I-R) Adénosine (A1-R) Prostaglandines (EP3-R) Neuropeptide Y/peptide YY (NPY1-R) Acide nicotinique (HM74A) Adenylyl cyclase Activation Atrial Natriuretic Peptide Brain Natriuretic Peptide (NPR-A) PDE-3B PDE-3B Ser-P TG ATGL AGNE Diacylglycérol Ser-P + LHS AGNE Monoglycéride LMG AGNE Glycérol Figure 3 : Contrôle de la lipolyse dans l’adipocyte humain Les catécholamines activent les récepteurs α2-adrénergiques (α2–AR) et β1/2/3-adrénergiques (β1/2/3– AR) modulant négativement et positivement l’activité de l’adénylyl-cyclase (AC) respectivement. Outre le récepteur α2–AR, de nombreux autres récepteurs sont couplés négativement à l’AC. C’est notamment le cas des récepteurs à l’adénosine (A1-R), aux prostaglandines (EP3-R), au neuropeptide Y (NPY-Y1-R) et à l’acide nicotinique (HM74A). L’AC produit de l’AMPc qui va activer une protéine kinase dépendante de l’AMPc (PKA). L’insuline possède une action antilipolytique. Son mécanisme d’action implique la phosphatidyl-inositol 3 kinase (PI3-K), la protéine kinase B (PKB/Akt) et la phosphodiestérase-3B (PDE-3B) qui diminue les taux intracellulaires d’AMPc transformé en 5’-AMP. L’ANP et le BNP stimulent le NPR-A dont l’activité guanylyl-cyclase (GC) génère du GMPc. Le GMPc stimule une protéine kinase dépendante du GMPc (PKG ou cGK-I). La PKA et la PKG activent par phosphorylation les périlipines et la lipase hormono-sensible (LHS) qui va transloquer à la vacuole lipidique et participer, avec l’adipocyte triacylglycérol lipase (ATGL) et la monoglycéride lipase (LMG), à l’hydrolyse des triglycérides (TGs) en glycérol et acides gras non estérifiés (AGNE). A.2) Les fonctions sécrétoires du tissu adipeux D’un point de vue quantitatif, les acides gras libres, issus de la lipolyse et libérés dans la circulation sanguine, représentent le principal produit de sécrétion du TA (265). Cependant le TA est également capable de synthétiser et de sécréter une multitude de facteurs qui agissent soit localement de façon autocrine et/ou paracrine, soit parfois de façon endocrine. On désigne sous le terme « adipokines », l’ensemble des facteurs bioactifs produits et sécrétés par le TA. Historiquement, la LPL est la première adipokine découverte (49). Toutefois, c’est la découverte de la leptine, hormone synthétisée par le TA et intervenant dans le contrôle de la prise alimentaire, qui a permis au TA d’acquérir le statut d’organe endocrine (302). Suite à cette découverte, d’autres facteurs produits et sécrétés par le TA ont été décrits, on en compte actuellement plus d’une cinquantaine qui diffèrent tant au niveau de leur structure que de leur fonction : des hormones (stéroïdes et glucocorticoïdes), des cytokines (TNFα, IL-6, IL-8), des facteurs de croissance (TGF-β), des protéases (MMP-2 et 9) et des anti-protéases (TIMP, PAI-1) (81). Plusieurs fonctions physiologiques leur sont associées, du contrôle du métabolisme lipidique, à l’angiogenèse et l’inflammation (figure 4). Excepté la leptine et l’adiponectine considérées comme spécifiques des adipocytes, les adipokines apparaissent comme étant également exprimées et produites par les cellules de la fraction non adipocytaire du TA, i.e la FSV (72). Des différences dans l’activité de sécrétion mais également dans le type d’adipokines ont été décrites dans les TA humains sous-cutanés et viscéraux (72, 136). En résumé, l’adipocyte présente deux fonctions principales, le stockage des lipides selon le processus de lipogenèse ainsi que celui de la synthèse des TGs, et la mobilisation des lipides via le processus de lipolyse. Ces activités métaboliques sont étroitement régulées par des signaux neuro-humoraux. De plus, grâce à une capacité sécrétoire aussi multiple que variée, le TA joue un rôle endocrine permettant d’assurer une communication avec de nombreux organes et tissus mais aussi un rôle paracrine et autocrine permettant une communication locale entre les différents types cellulaires qui le composent. Voyons à présent les mécanismes impliqués dans le développement normal de la masse grasse. Nous nous intéresserons ensuite aux modifications cellulaires du TA et de ses principales fonctions au cours d’un développement excessif ou d’une régression. 17 Métabolisme lipidique et des lipoprotéines Tonus vasculaire et angiogenèse Lipoprotéine lipase Acylation stimulating protein (ASP) Prostaglandines Acide lysophosphatidique (LPA) Retinol binding protein (RBP) Cholesteryl ester transferase protein (CETP) Autotaxine (phospholipase D) Vascular endothelial growth factor (VEGF) Monobutyrine Leptine FIAF (PGAR ou angiopoietin like 4) Angiopoietin 2 Angiotensinogène et Angiotensine II Metalloprotéases de type 2 et 9 (MMP-2 et -9) Apeline Adipocytes Réponse immunitaire et inflammatoire Tumor necrosis factor α (TNF-α) Interleukines 6 et 8 (IL-6 et IL-8) Plasminogen activator inhibitor-1 (PAI-1) Haptoglobine Serum amyloïd A (SAA) Monocyte chemoattractant protein (MCP-1) Métallothionéïne Métabolisme et homéostasie énergétique Leptine Adiponectine Résistine Interleukine 6 (IL-6) Apeline Figure 4 : Les sécrétions du tissu adipeux B) Le développement normal du tissu adipeux Le développement de lignées cellulaires fibroblastiques pluripotentes ou unipotentes a largement contribué à l’identification et à la compréhension des événements cellulaires et moléculaires impliqués dans la formation des adipocytes, i.e. la différenciation adipocytaire ou adipogenèse. Le tableau 1 présente les principaux modèles de préadipocytes utilisés in vitro pour l’analyse de l’adipogenèse ainsi que leur origine tissulaire (d’après (91)). Notons que la majorité de ces modèles cellulaires sont d’origine embryonnaire et murine. Tableau 1: Les différents modèles de culture cellulaire utilisés pour l’étude de l’adipogenèse Nature de la culture Phénotype pluripotentes Lignées unipotentes Origine tissulaire Cellules ES Blastocystes murins Muscle, 10T1/2 Embryons de souris C3H adipocyte blanc hMADS TA humain Lignées totipotentes Lignées Nom Adipocyte blanc 3T3-L1, Embryon de souris Swiss 3T3-F442A Ob17 TA épididymaire de souris ob/ob adulte Clone TA1 Clone dérivé des 10T1/2 traités par 5azacytidine Adipocyte brun Cultures Primaires Adipocytes Clone A31T Lignée murine Balb/c3T3 Clone 1246 Carcinome embryonnaire de souris C3H PAZ6 Fœtus humain HIB 1B TA brun de souris FSV du TA TA blanc ou brun (rongeurs, lapins, blanc ou bruns porcs, hommes…) Voyons à présent les voies de régulation des processus de détermination et de différenciation adipocytaires. 18 B.1) Le processus de détermination adipocytaire Comme l’indique la figure 5, la détermination adipocytaire correspond à l’orientation d’une cellule précurseur, supposée d’origine mésenchymateuse, vers la lignée adipocytaire. Bien que les mécanismes impliqués dans ce processus soient encore peu connus, certains facteurs susceptibles d’orienter le précurseur mésenchymateux vers le lignage adipeux ont été identifiés (pour revue (79, 226)). C’est notamment le cas des voies de signalisation de delta fos B et de l’acide rétinoïque mais aussi de Wnt, une glycoprotéine sécrétée impliquée dans la croissance et le devenir cellulaire et des BMPs (bone morphogenic protein) appartenant à la superfamille du TGF-β et impliqués dans le devenir des cellules mésenchymateuses. Le facteur delta fos B inhibe l’adipogenèse en favorisant la différenciation ostéogénique (234). L’activation de la voie Wnt inhibe également la différenciation adipocytaire en favorisant l’orientation myogénique (230). Enfin, une exposition des cellules mésenchymateuses multipotentes CH310T1/2 à du BMP-4 engage les cellules vers un lignage adipogénique (261). L’influence du BMP-2 sur ces cellules CH310T1/2 semble en revanche plus complexe puisqu’à faibles concentrations il stimule l’engagement vers le lignage adipogénique alors qu’à de fortes concentrations il stimule l’engagement vers le lignage ostéogénique (283). Il est à noter que l’origine des précurseurs des adipocytes n’est pas claire. Chez l’embryon, l’apparition d’adipocytes est concomitante à l’apparition du système vasculaire (52) et la culture de cellules souches embryonnaires murines en présence d’acide rétinoïque promeut la différenciation adipocytaire (58, 207). Chez l’adulte, des cellules mésenchymateuses de la moelle osseuse caractérisées par leur capacité d’adhésion sur plastique, leur capacité de prolifération et leur expression de différents marqueurs de surface tels que le CD105 et l’absence du marqueur des cellules souches hématopoïétiques CD34, sont capables in vitro de s’orienter vers des voies adipogéniques, chondrogéniques et ostéogéniques (210). De plus, des analyses clonales ont permis de montrer qu’une même cellule conservait ces capacités multiples de détermination (210). Récemment, une étude réalisée chez des souris soumises à un régime gras a permis de montrer par l’utilisation d’approches de repopulation des cellules de la moelle osseuse par des cellules souches qui expriment une protéine fluorescente verte (GFP) que certains adipocytes des dépôts profonds pourraient être originaires de cellules de la moelle osseuse (54). De plus, des cellules sanguines circulantes ont été montrées comme pouvant exprimer une capacité de différenciation adipocytaire, suggérant que des cellules de la moelle osseuse peuvent, sous des stimuli à préciser, être mobilisées dans la circulation sanguine et être recrutées dans les 19 Type cellulaire Précurseur multipotent Chondrobastes Ostéoblastes Myoblastes Evènements moléculaires •Voie Wnt •Delta Fos B •Acide rétinoïque Etapes Détermination Adipoblaste Phase exponentielle de croissance Pref 1 Arrêt de croissance (confluence) Préadipocyte C/EBP β et δ PPAR γ Expansion clonale (mitoses post-confluence) C/EBP α Engagement (commitment) Différenciation Remodelage de la MEC et du •Gènes adipocytaires cytosquelette •Enzymes lipogéniques et synthèse de TG Maturation terminale •Lipolyse •Activités sécrétoires Adipocyte mature Figure 5 : Détermination et différenciation adipocytaires D’après Gregoire F. M., Physiol. Rev., 1998. dépôts adipeux (101). Le TA adulte contient également au sein de la FSV des cellules résidentes capables d’exprimer des capacités multiples de différenciation (304). De plus, diverses approches in vivo ont montré la capacité réparatrice de ces cellules dans des modèles animaux d’ischémie vasculaire et cardiaque ou de dommages osseux et musculaires. La revue qui suit : « le TA un donneur de cellules souches » présente ces données. 20 biologie générale biologie générale LE TISSU ADIPEUX : UN DONNEUR DE CELLULES SOUCHES ?* Anne BOULOUMIÉ, Sandra DE BARROS, Marie MAUMUS, Jean GALITZKY, Coralie SENGENES Les cellules souches sont caractérisées par leur capacité d’autorenouvellement et leur capacité à produire des cellules différenciées fonctionnelles. Différents types de cellules souches sont définis en fonction de leur origine et de leur devenir : (1) les cellules souches embryonnaires totipotentes capables de former toutes les couches embryonnaires ainsi que les annexes extra-embryonnaires qui supportent la croissance de l’embryon, (2) les cellules souches embryonnaires pluripotentes qui donnent naissance au mésoderme, endoderme et ectoderme, (3) les cellules souches multipotentes, capables de générer plusieurs types cellulaires, (4) les cellules progénitrices ou précurseurs qui présentent une capacité limitée d’autorenouvellement et qui se différencient en un type cellulaire défini [1]. Des progrès récents dans l’isolement et la caractérisation des cellules souches/progénitrices ont conduit à la mise en évidence de cellules présentant certaines propriétés de cellules souches/progénitrices dans divers tissus adultes, tels que le cœur, le rein, le cerveau, le muscle et également le tissu adipeux. Ces cellules constitueraient un réservoir de cellules réparatrices prêtes à être mobilisées et à se différencier en réponse à une ischémie et/ou à un dommage. Ces cellules présentent un intérêt croissant en médecine réparative et régénérative avec un rôle thérapeutique potentiel dans une grande variété d’applications cliniques. Cependant, la présence de cellules souches/progénitrices dans les tissus adultes a conduit à de nombreuses questions et controverses quant à leurs identités et potentialités réelles de différenciation [2]. Inserm, Équipe Avenir, INSERM U858, Institut de médecine moléculaire de Rangueil, Toulouse ; Université Paul Sabatier, Institut Louis Bugnard IFR31, Toulouse. Correspondance : Anne Bouloumié, INSERM équipe AVENIR, Faculté de médecine, 37, allées Jules Guesde, 31000 Toulouse. Email : [email protected] * Conférence donnée dans le cadre de la 47e Journée Annuelle de Nutrition et de Diététique, le vendredi 26 janvier 2007. Cah. Nutr. Diét., 42, 2, 2007 Chez l’adulte, la moelle osseuse est considérée comme le tissu réservoir de cellules souches [3]. Deux familles au moins de cellules souches/progénitrices qui représentent une fraction mineure de la population totale de la moelle (0,001 à 0,01 % des cellules nuclées), ont été identifiées : les cellules souches hématopoiétiques qui comprennent des cellules multipotentes capables de reconstituer l’ensemble des lignées hématopoiétiques, des cellules progénitrices monopotentes donnant naissance à un lignage, et les cellules souches mésenchymateuses qui présentent la capacité de se différencier en cellules des tissus connectifs, dont les os, le tissu adipeux et le cartilage. Une population de cellules immatures capables de prolifération sans sénescence et capables de s’orienter vers des lignages distincts, i.e. endothélial, endodermal et neural in vitro et in vivo, a été également décrite dans la moelle adulte et définie comme « cellules souches adultes multipotentes » [4]. Cependant, leur existence est soumise à de fortes controverses. Finalement, des cellules endothéliales progénitrices sont également présentes dans la moelle osseuse. Ces cellules contribueraient à la néovascularisation de tissus ischémiques après leur mobilisation et leur recrutement vers les sites ischémiques [5]. En plus de la moelle osseuse, d’autres sources de cellules souches/progénitrices ont été décrites chez l’adulte, tels que la peau [6], le muscle [7], le cerveau [8] et le tissu adipeux humain [9]. 73 biologie générale Caractéristiques in vitro des cellules souches/progénitrices du tissu adipeux humain La présence de cellules progénitrices dans le tissu adipeux humain est reconnue depuis les travaux de Bjorntorp sur l’évolution de la cellularité de la masse adipeuse avec le développement de l’obésité. Les préadipocytes En effet, ses travaux ont montré clairement que l’obésité chez l’homme se caractérise par une phase d’hypertrophie adipocytaire suivie d’une phase d’hyperplasie adipocytaire [10, 11]. Les adipocytes étant des cellules matures différenciées, incapables de proliférer. L’augmentation du nombre d’adipocytes dans le tissu adipeux (TA) de patients obèses est expliquée par la différenciation de cellules progénitrices présentes dans la fraction stroma-vasculaire (FSV), i.e. la fraction non-adipocytaire, du TA [12]. En effet, l’isolement de la FSV de TA humain et sa mise en culture in vitro en condition adipogénique [13, 14], i.e. en présence de facteurs favorisant la différenciation adipocytaire tels que l’insuline, la triodothryronine et le cortisol, conduit à la formation de cellules in vitro qui expriment des transcripts spécifiques des adipocytes. De plus, ces cellules différenciées présentent des activités fonctionnelles métaboliques, i.e. lipolyse et lipogénèse, et sécrétoires (production de leptine) des adipocytes matures. Des expériences chez les rongeurs ont permis de plus de montrer que ces cellules forment in vitro des adipocytes matures fonctionnels au site de leur injection [15, 16]. Ces résultats démontrent la présence, au sein du TA, de cellules immatures capables de se différencier in vitro et in vivo en adipocytes fonctionnels. Différenciation in vitro des cellules de la FSV du TA humain Outre leur capacité de différenciation en adipocyte in vitro, de nombreux laboratoires ont, par la suite, montré que les cellules de la FSV humaine pouvaient acquérir selon les conditions de culture in vitro des marqueurs biochimiques caractéristiques de lignages cellulaires variés [17] : lignage ostéogénique [18], chondrogénique [19, 20] et myogénique [21, 22] mais également l’expression de marqueurs du lignage neuronal [21, 23], endothélial [24-26], épithélial [27-29] et même cardiaque [30]. De plus, des approches « clonales », c’est-à-dire d’analyse des capacités de différenciation des cellules dérivant d’une cellule unique après multiples passages, ont montré que plusieurs clones cellulaires pouvaient se différencier en plusieurs lignages [22, 23], suggérant la présence de cellules de type « cellules souches adultes multipotentes » et non pas seulement un mélange de population de cellules progénitrices unipotentes. Ces résultats sont en accord avec les résultats obtenus par le groupe de Christian Dani [31] montrant dans la FSV isolée à partir de TA de jeunes donneurs, la présence de cellules plus immatures et multipotentes (hMADS ou Human Multipotent Adipose Derived Stem Cell). Des expériences parallèles chez les rongeurs mettaient également en évidence une plasticité importante des cellules de la FSV des TAs murins [32-34]. 74 Limites des approches in vitro sur les cellules de la FSV du TA humain La majorité des approches réalisées in vitro utilisent des phases d’expansion cellulaire en présence de fortes concentrations de sérum, conditions associées à des altérations phénotypiques des cellules [35]. En effet, alors que les cellules natives, i.e. directement isolées, de la FSV humaine expriment des marqueurs membranaires de type CD34, marqueur des cellules souches hématopoiétiques, et sont dépourvues des marqueurs des cellules souches mésenchymateuses Stro-1 et CD105, les cellules placées en culture expriment un profil inverse, i.e. perte du CD34 et gain de CD105 et Stro-1 [25, 36-38]. De plus, peu ou pas d’analyses fonctionnelles ont été associées aux études relatives aux potentialités de différenciation des cellules. Ces analyses sont cependant nécessaires pour statuer clairement quant à la capacité réelle de différenciation en cellules fonctionnelles. De plus, certains résultats obtenus chez les rongeurs n’ont pas été confirmés chez l’homme suggérant que les capacités de différenciation des cellules de la FSV humaine sont plus restreintes que chez le rongeur. Enfin, la FSV du TA n’est pas constituée d’une population de cellules homogènes mais contient, comme son nom l’indique, des populations cellulaires de la composante vasculaire [25] et de la composante stromale, i.e. macrophages et lymphocytes infiltrés [39]. Isolement des cellules progénitrices/souches natives de la FSV du TA humain Afin d’isoler et de caractériser la population de cellules progénitrices présentes dans la FSV du TA humain, notre groupe a développé une approche d’immunosélection/ déplétion permettant d’isoler les différentes populations cellulaires. Nous avons ainsi démontré que les cellules « natives » positives pour le CD34 et négatives pour le marqueur endothélial CD31 sont la seule population cellulaire parmi les cellules endothéliales capillaires (CD34+/ CD31+), les macrophages (CD34–/CD14+) et les cellules CD34–/CD31–/CD14–, à présenter la capacité de se différencier en adipocytes in vitro [38]. De plus, une partie de cette même population cellulaire possède, en milieu de culture endothélial, la capacité d’exprimer des marqueurs endothéliaux et de s’organiser en structures semblables à des capillaires [25]. Ces résultats montrent que la fraction cellulaire CD34+/CD31– native, i.e. n’ayant subi aucune étape d’expansion in vitro, de la FSV du TA humain présente des propriétés de cellules progénitrices capables de donner naissance à des cellules qui expriment des marqueurs phénotypiques des adipocytes et des cellules endothéliales. Il reste à déterminer si cette population cellulaire native est constituée d’un mélange de cellules progénitrices unipotentes ou de cellules souches multipotentes. Caractéristiques in vivo des cellules souches/progénitrices du TA humain Les approches in vitro ont donc apporté des observations intéressantes sur la plasticité potentielle des cellules dérivées de la FSV du TA humain, justifiant la mise en place d’approches in vivo d’injection de cellules humaines dans des modèles animaux présentant des ischémies/dommages Cah. Nutr. Diét., 42, 2, 2007 biologie générale tissulaires afin de suivre la potentialité réparatrice de ces cellules. Les mécanismes responsables des interactions entre cellules implantées et cellules hôtes restent à être caractérisés. Cependant, des travaux récents apportent des données intéressantes concernant la réponse de l’hôte ainsi que le comportement des cellules injectées en fonction des environnements locaux distincts. Réponse immune de l’hôte Les cellules dérivées de la FSV des TAs humains semblent présenter une nature non-immunogénique [40]. En effet, in vitro les cellules ne provoquent pas d’alloréactivité de lymphocytes incompatibles mais apparaissent de plus exercer des propriétés immunosuppréssives [40, 41]. De plus, in vivo, l’implantation des cellules humaines chez des souris immunocompétentes n’induit pas d’accumulation de lymphocytes au site d’implantation [31]. Les processus exacts impliqués nécessitent une caractérisation plus approfondie. Cependant, ces observations pourraient avoir un impact important en termes de thérapie allogénique ou pour le transfert de cellules dans un organisme hôte dérivées d’un autre donneur [42]. Mécanismes d’adressage des cellules Plusieurs types de modes d’administration des cellules ont été utilisés de l’injection intraveineuse à l’application directe au site endommagé. Quand les cellules sont injectées par voie systémique chez la souris, les cellules s’infiltrent en conditions basales dans différents tissus [43] dont les poumons, le foie, le cœur, le thymus et le cerveau [44]. Toutefois, en présence de dommages tissulaires, une infiltration plus élevée est observée au niveau du site endommagé. Par exemple, une hépatectomie partielle chez la souris conduit à l’augmentation de l’infiltration des cellules dérivées de la FSV dans le foie [44]. Les mécanismes qui guident les cellules aux sites endommagés ne sont pas connus. Nous avons initié des expériences sur la capacité de migration des cellules CD34+/CD31–. Nos résultats montrent que les cellules migrent fortement en réponse à un gradient de facteurs produits par les cellules endothéliales. Des recherches complémentaires sont nécessaires pour déterminer quels facteurs, tels que des chimiokines ou des signaux relatifs à l’état hypoxique, sont responsables de l’attraction des cellules souches/progénitrices de la FSV des TAs humains. Devenir in vivo Le principe de la thérapie cellulaire est que les cellules souches/progénitrices vont au niveau du site endommagé se différencier sous l’influence de facteurs locaux en cellules d’un phénotype approprié. Cependant la différenciation « réelle » des cellules souches/progénitrices in vivo est soumise à controverse et plusieurs processus alternes ont été suggérés comme participant aux activités réparatrices des cellules telles que la fusion cellulaire aboutissant à la reprogrammation nucléaire et la production par les cellules souches/progénitrices de facteurs trophiques et « réparateurs » agissant de manière paracrine sur les cellules hôtes. La capacité réparatrice des cellules souches/progénitrices de la FSV du TA humain a été clairement mise en évidence dans différents modèles chez la souris. Dans un modèle de souris immunotolérante avec une ischémie de la patte arrière provoquée par ligature de l’artère fémorale, l’injection de cellules de la FSV brute [24, 45, 46] ou des cellules Cah. Nutr. Diét., 42, 2, 2007 CD34+/CD31– [25] conduit à une amélioration de la néovasularisation du membre ischémique. Toutefois, il reste à déterminer si cette néovascularisation est due à une incorportion des cellules injectées dans la vasculature de la souris et à leur différenciation en cellules endothéliales ou à la production locale par les cellules injectées de facteurs proangiogéniques [46, 47]. Des activités réparatrices de dommages osseux ont été également rapportées dans différents modèles murins [48, 49]. Enfin, l’injection des cellules souches multipotentes chez des souris « mdx », modèle de myopathie de Duchenne, est associée à une expression importante et prolongée de la dystrophine humaine, protéine nécessaire à l’intégrité de la fibre musculaire [31]. Des expériences en parallèle sur les cellules de la FSV murine montrent également des capacités réparatrices multiples [50-52]. Limites et questions Un nombre important d’observations suggère que le processus néoplastique impliquerait des cellules souches [53]. Une étude récente montre le risque de transformation des cellules de la FSV. En effet, la culture à long terme des cellules de la FSV du TA humain adulte a été associée à l’immortalisation et la transformation spontanée des cellules, conduisant in vivo à la formation de tumeur après injection des cellules chez la souris athymique [54]. Des études complètes sont donc nécessaires pour établir clairement le risque associé à l’expansion in vitro des cellules de la FSV humaine. Le déclin du potentiel régénératif est une signature du vieillissement et pourrait être dû à des changements relatifs à l’âge des cellules souches spécifiques des tissus. Des études récentes chez la souris montrent que le déclin de l’activité des cellules progénitrices lié au vieillissement peut être réversible suite à une exposition à un environnement « jeune » alors qu’à l’inverse l’environnement d’un animal âgé empêche la régénération tissulaire stimulée par des cellules progénitrices issues d’animaux « jeunes » [55]. Les études de l’équipe de C. Dani montrant la présence de cellules souches multipotentes dans la FSV ont été réalisées chez des patients jeunes [31]. Il serait maintenant intéressant de déterminer l’impact de l’âge sur les cellules souches/progénitrices du tissu adipeux tant au niveau de leur potentialité intrinsèque que sur leur interaction avec l’environnement. Finalement, la présence de ces cellules dans la FSV pose la question de leur origine et de leur spécificité. Récemment, Hong et al. [56] a décrit que les fibrocytes circulant CD45+ étaient capables en culture d’accumuler des triglycérides. Les études de Crossno et al. [57] réalisées chez la souris en transplantant des cellules de la moelle osseuse de souris transgéniques qui expriment la protéine fluorescente verte (GFP) à des souris sauvages soumises à un régime riche en graisse, montrent l’apparition d’adipocytes GFP positifs dans les tissus adipeux. Ces deux études suggèrent que certaines cellules progénitrices du tissu adipeux pourraient avoir une origine sanguine/moelle osseuse. Nos expériences montrent que les cellules CD34+/CD31– circulantes sanguines ne présentent cependant pas les mêmes potentialités que les cellules CD34+/CD31– du tissu adipeux humain, i.e. production de colonies de cellules sanguines mais absence de différenciation adipocytaire [38], ce qui suggère que si ces cellules ont la même ori75 biologie générale gine, le micro-environnement dans lequel elles résident définit leur potentialité et leur spécificité. Des études complémentaires sont donc nécessaires pour mieux définir l’influence du micro-environnement sur la potentialité des cellules souches/progénitrices. Conclusion De nombreuses données obtenues in vitro et in vivo montrent la présence au sein des TAs humains de populations cellulaires présentant des capacités similaires aux cellules progénitrices/souches. La capacité multiple de différenciation reste soumise à controverse et nécessite des recherches supplémentaires pour statuer clairement. Entre autres, des méthodes standardisées et validées d’isolement, de caractérisation, de sélection, de purification, de culture, de stockage et d’injection des cellules à partir du TA humain doivent être développées. Les cellules souches/progénitrices du TA humain pourraient, de part leur accessibilité et leur nombre au sein de la FSV, devenir un modèle cellulaire intéressant pour des approches de thérapie cellulaire pour la régénération et la réparation tissulaire [58, 59]. Toutefois, de nombreux challenges scientifiques restent encore à être réalisés avant d’envisager de telles approches. Les mécanismes d’infiltration et d’adressage des cellules doivent être mieux caractérisés ainsi que le rôle relatif de la différenciation, fusion et production de facteurs paracrines dans les effets réparateurs de ces cellules. Résumé De nombreux laboratoires ont montré que les cellules issues de la fraction stroma-vasculaire des tissus adipeux humains pouvaient exprimer in vitro selon les conditions de culture des marqueurs biochimiques de lignages cellulaires variés : adipogénique, ostéogénique, chondrogénique, myogénique, endothélial, neuronal et épithélial. De plus, diverses approches in vivo ont montré la capacité réparatrice des cellules de la fraction stroma-vasculaire du tissu adipeux humain dans des modèles animaux d’ischémie vasculaire et cardiaque ou de dommages osseux et musculaires. Ces résultats suggèrent fortement que le tissu adipeux humain contient des cellules qui présentent des propriétés similaires à celles des cellules souches ou progénitrices. Toutefois, la nature exacte de ces cellules, leur potentialité réelle de différenciation in vivo ainsi que les mécanismes impliqués dans leur capacité de réparation et de régénération restent à être caractérisés pour envisager leur utilisation dans des approches de régénération et réparation tissulaire. Mots-clés : Cellule progénitrice – Préadipocyte – Cellules endothéliales – Réparation – Régénération. Abstract Several laboratories have shown that the cells from the stroma-vascular fraction of the human adipose tissue express, depending on cell culture conditions, biochemical markers of multiple cell lineages including adipogenic, osteogenic, chondrogenic, myogenic, endothelial, neuronal and epithelial cell lineage. Furthermore, various 76 in vivo approaches revealed the ability of the cells derived from the stroma-vacsular fraction of adipose tissue to repair ischemic or damaged tissues. Altogether these data strongly suggest that the stroma-vascular fraction of the human adipose tissue contains cells that exhibit properties like stem/progenitor cells. However, the exact nature of the cells, their potentiality to lead to differentiated cells in vivo as well as the mechanisms involved in their repair capability remain to be characterized to consider their use in regenerative and reparative medicine. Key-words: Progenitor – Preadipocyte – Endothelial cell – Repair – Regeneration. Bibliographie [1] Lakshmipathy U., Verfaillie C. – Stem cell plasticity. Blood Rev., 2005, 19, 29-38. [2] Pessina A., Gribaldo L. – The key role of adult stem cells: therapeutic perspectives. Curr. Med. Res. Opin., 2006, 22, 2287-2300. [3] Pittenger M.F., Mackay A.M., Beck S.C. et al. – Multilineage potential of adult human mesenchymal stem cells. Science, 1999, 284, 143-147. [4] Jiang Y., Jahagirdar B.N., Reinhardt R.L. et al. – Pluripotency of mesenchymal stem cells derived from adult marrow. Nature, 2002, 418, 41-49. [5] Asahara T., Murohara T., Sullivan A. et al. – Isolation of putative progenitor endothelial cells for angiogenesis. Science, 1997, 275, 964-967. [6] Toma J.G., Akhavan M., Fernandes K.J. et al. – Isolation of multipotent adult stem cells from the dermis of mammalian skin. Nat. Cell. Biol., 2001, 3, 778-784. [7] Jackson K.A., Mi T., Goodell M.A. – Hematopoietic potential of stem cells isolated from murine skeletal muscle. Proc. Natl. Acad. Sci. USA, 1999, 96, 14482-14486. [8] Bjornson C.R., Rietze R.L., Reynolds B.A., Magli M.C., Vescovi A.L. – Turning brain into blood: a hematopoietic fate adopted by adult neural stem cells in vivo. Science, 1999, 283, 534-537. [9] Zuk P.A., Zhu M., Mizuno H. et al. – Multilineage cells from human adipose tissue: implications for cell-based therapies. Tissue Eng., 2001, 7, 211-228. [10] Bjorntorp P., Gustafson A., Persson B. – Adipose tissue fat cell size and number in relation to metabolism in endogenous hypertriglyceridemia. Acta Med. Scand., 1971, 190, 363-367. [11] Sjostrom L., Smith U., Krotkiewski M., Bjorntorp P. – Cellularity in different regions of adipose tissue in young men and women. Metabolism, 1972, 21, 1143-1153. [12] Bjorntorp P., Karlsson M., Pertoft H., Pettersson P., Sjostrom L., Smith U. – Isolation and characterization of cells from rat adipose tissue developing into adipocytes. J. Lipid Res., 1978, 19, 316-324. [13] Deslex S., Negrel R., Vannier C., Étienne J., Ailhaud G. – Differentiation of human adipocyte precursors in a chemically defined serum-free medium. Int. J. Obes., 1987, 11, 19-27. [14] Hauner H., Entenmann G., Wabitsch M. et al. – Promoting effect of glucocorticoids on the differentiation of human adipocyte precursor cells cultured in a chemically defined medium. J. Clin. Invest., 1989, 84, 1663-1670. [15] Vannier C., Gaillard D., Grimaldi P. et al. – Adipose conversion of ob17 cells and hormone-related events. Int. J. Obes., 1985, 9 (Suppl. 1), 41-53. [16] Choi Y.S., Cha S.M., Lee Y.Y., Kwon S.W., Park C.J., Kim M. – Adipogenic differentiation of adipose tissue Cah. Nutr. Diét., 42, 2, 2007 biologie générale [17] [18] [19] [20] [21] [22] [23] [24] [25] [26] [27] [28] [29] [30] [31] [32] [33] derived adult stem cells in nude mouse. Biochem. Biophys. Res. Commun., 2006, 345, 631-637. Gimble J., Guilak F. – Adipose-derived adult stem cells: isolation, characterization, and differentiation potential. Cytotherapy, 2003, 5, 362-369. Halvorsen Y.D., Franklin D., Bond A.L. et al. – Extracellular matrix mineralization and osteoblast gene expression by human adipose tissue-derived stromal cells. Tissue Eng., 2001, 7, 729-741. Erickson G.R., Gimble J.M., Franklin D.M., Rice H.E., Awad H., Guilak F. – Chondrogenic potential of adipose tissue-derived stromal cells in vitro and in vivo. Biochem. Biophys. Res. Commun., 2002, 290, 763-769. Estes B.T., Wu A.W., Guilak F. – Potent induction of chondrocytic differentiation of human adipose-derived adult stem cells by bone morphogenetic protein 6. Arthritis Rheum., 2006, 54, 1222-1232. Zuk P.A., Zhu M., Ashjian P. et al. – Human adipose tissue is a source of multipotent stem cells. Mol. Biol. Cell., 2002, 13, 4279-4295. Rodriguez L.V., Alfonso Z., Zhang R., Leung J., Wu B., Ignarro L.J. – Clonogenic multipotent stem cells in human adipose tissue differentiate into functional smooth muscle cells. Proc. Natl. Acad. Sci. USA, 2006, 103, 12167-12172. Guilak F., Lott K.E., Awad H.A. et al. – Clonal analysis of the differentiation potential of human adipose-derived adult stem cells. J. Cell. Physiol., 2006, 206, 229-237. Planat-Benard V., Silvestre J.S., Cousin B. et al. – Plasticity of human adipose lineage cells toward endothelial cells: physiological and therapeutic perspectives. Circulation, 2004, 109, 656-663. Miranville A., Heeschen C., Sengenes C., Curat C.A., Busse R., Bouloumie A. – Improvement of postnatal neovascularization by human adipose tissue-derived stem cells. Circulation, 2004, 110, 349-355. Martinez-Estrada O.M., Munoz-Santos Y., Julve J., Reina M., Vilaro S. – Human adipose tissue as a source of Flk-1+ cells: new method of differentiation and expansion. Cardiovasc. Res., 2005, 65, 328-333. Brzoska M., Geiger H., Gauer S., Baer P. – Epithelial differentiation of human adipose tissue-derived adult stem cells. Biochem. Biophys. Res. Commun., 2005, 330, 142150. Talens-Visconti R., Bonora A., Jover R. et al. – Hepatogenic differentiation of human mesenchymal stem cells from adipose tissue in comparison with bone marrow mesenchymal stem cells. World J. Gastroenterol., 2006, 12, 5834-5845. Timper K., Seboek D., Eberhardt M. et al. – Human adipose tissue-derived mesenchymal stem cells differentiate into insulin, somatostatin, and glucagon expressing cells. Biochem. Biophys. Res. Commun., 2006, 341, 11351140. Gaustad K.G., Boquest A.C., Anderson B.E., Gerdes A.M., Collas P. – Differentiation of human adipose tissue stem cells using extracts of rat cardiomyocytes. Biochem. Biophys. Res. Commun., 2004, 314, 420-427. Rodriguez A.M., Pisani D., Dechesne C.A. et al. – Transplantation of a multipotent cell population from human adipose tissue induces dystrophin expression in the immunocompetent mdx mouse. J. Exp. Med., 2005, 201, 1397-1405. Planat-Benard V., Menard C., Andre M. et al. – Spontaneous cardiomyocyte differentiation from adipose tissue stroma cells. Circ. Res., 2004, 94, 223-229. Cousin B., Andre M., Arnaud E., Penicaud L., Casteilla L. – Reconstitution of lethally irradiated mice by cells isolated from adipose tissue. Biochem. Biophys. Res. Commun., 2003, 301, 1016-1022. Cah. Nutr. Diét., 42, 2, 2007 [34] Charriere G., Cousin B., Arnaud E. et al. – Preadipocyte conversion to macrophage. Evidence of plasticity. J. Biol. Chem., 2003, 278, 9850-9855. [35] Javazon E.H., Beggs K.J., Flake A.W. – Mesenchymal stem cells: paradoxes of passaging. Exp. Hematol., 2004, 32, 414-425. [36] McIntosh K., Zvonic S., Garrett S. et al. – The immunogenicity of human adipose-derived cells: temporal changes in vitro. Stem Cells, 2006, 24, 1246-1253. [37] Mitchell J.B., McIntosh K., Zvonic S. et al. – Immunophenotype of human adipose-derived cells: temporal changes in stromal-associated and stem cell-associated markers. Stem Cells, 2006, 24, 376-385. [38] Sengenes C., Lolmede K., Zakaroff-Girard A., Busse R., Bouloumie A. – Preadipocytes in the human subcutaneous adipose tissue display distinct features from the adult mesenchymal and hematopoietic stem cells. J. Cell. Physiol., 2005, 205, 114-122. [39] Bouloumie A., Curat C.A., Sengenes C., Lolmede K., Miranville A., Busse R. – Role of macrophage tissue infiltration in metabolic diseases. Curr. Opin. Clin. Nutr. Metab. Care, 2005, 8, 347-354. [40] Yanez R., Lamana M.L., Garcia-Castro J., Colmenero I., Ramirez M., Bueren J.A. – Adipose tissue-derived mesenchymal stem cells have in vivo immunosuppressive properties applicable for the control of the graft-versus-host disease. Stem Cells, 2006, 24, 2582-2591. [41] Puissant B., Barreau C., Bourin P. et al. – Immunomodulatory effect of human adipose tissue-derived adult stem cells: comparison with bone marrow mesenchymal stem cells. Br. J. Haematol., 2005, 129, 118-129. [42] Niemeyer P., Kornacker M., Mehlhorn A. et al. – Comparison of Immunological Properties of Bone Marrow Stromal Cells and Adipose Tissue-Derived Stem Cells Before and After Osteogenic Differentiation in Vitro. Tissue Eng., 2007, 13, 111-121. [43] Meyerrose T.E., De Ugarte D.A., Hofling A.A. et al. – In vivo Distribution of Human Adipose-Derived MSC. Stem Cells, 2007, 25, 220-227. [44] Kim D.H., Je C.M., Sin J.Y., Jung J.S. – Effect of partial hepatectomy on in vivo engraftment after intravenous administration of human adipose tissue stromal cells in mouse. Microsurgery, 2003, 23, 424-431. [45] Moon M.H., Kim S.Y., Kim Y.J. et al. – Human adipose tissue-derived mesenchymal stem cells improve postnatal neovascularization in a mouse model of hindlimb ischemia. Cell. Physiol. Biochem., 2006, 17, 279-290. [46] Rehman J., Traktuev D., Li J. et al. – Secretion of angiogenic and antiapoptotic factors by human adipose stromal cells. Circulation, 2004, 109, 1292-1298. [47] Sumi M., Sata M., Toya N., Yanaga K., Ohki T., Nagai R. – Transplantation of adipose stromal cells, but not mature adipocytes, augments ischemia-induced angiogenesis. Life Sci., 2007, 80, 559-565. [48] Hattori H., Masuoka K., Sato M. et al. – Bone formation using human adipose tissue-derived stromal cells and a biodegradable scaffold. J. Biomed. Mater. Res. B. Appl. Biomater., 2006, 76, 230-239. [49] Peterson B., Zhang J., Iglesias R. et al. – Healing of critically sized femoral defects, using genetically modified mesenchymal stem cells from human adipose tissue. Tissue Eng., 2005, 11, 120-129. [50] Miyahara Y., Nagaya N., Kataoka M. et al. – Monolayered mesenchymal stem cells repair scarred myocardium after myocardial infarction. Nat. Med., 2006, 12, 459-465. [51] Bacou F., el Andalousi R.B., Daussin P.A. et al. – Transplantation of adipose tissue-derived stromal cells increases mass and functional capacity of damaged skeletal muscle. Cell Transplant., 2004, 13, 103-111. [52] Conejero J.A., Lee J.A., Parrett B.M. et al. – Repair of palatal bone defects using osteogenically differentiated fat77 biologie générale [53] [54] [55] [56] 78 derived stem cells. Plast. Reconstr. Surg., 2006, 117, 857-863. Marx J. – Cancer research. Mutant stem cells may seed cancer. Science, 2003, 301, 1308-1310. Rubio D., Garcia-Castro J., Martin M.C. et al. – Spontaneous human adult stem cell transformation. Cancer Res., 2005, 65, 3035-3039. Conboy I.M., Conboy M.J., Wagers A.J., Girma E.R, Weissman I.L., Rando TA. – Rejuvenation of aged progenitor cells by exposure to a young systemic environment. Nature, 2005, 433, 760-764. Hong K.M., Burdick M.D., Phillips R.J., Heber D., Strieter R.M. – Characterization of human fibrocytes as circu- lating adipocyte progenitors and the formation of human adipose tissue in SCID mice. Faseb, 2005, 19, 2029-2031. [57] Crossno J.T., Majka S.M., Grazia T., Gill R.G., Klemm D.J. – Rosiglitazone promotes development of a novel adipocyte population from bone marrow-derived circulating progenitor cells. J. Clin. Invest., 2006, 116, 3220-3228. [58] Rodriguez A.M., Elabd C., Amri E.Z., Ailhaud., Dani C. – The human adipose tissue is a source of multipotent stem cells. Biochimie, 2005, 87, 125-128. [59] Casteilla L., Planat-Benard V., Cousin B. et al. – Plasticity of adipose tissue: a promising therapeutic avenue in the treatment of cardiovascular and blood diseases? Arch. Mal. Cœur Vaiss., 2005, 98, 922-926. Cah. Nutr. Diét., 42, 2, 2007 Afin d’isoler et de caractériser la population de cellules progénitrices présentes dans la FSV, notre groupe a développé une technique d’isolement des différentes populations cellulaires de la FSV qui se fonde sur l’utilisation de nanoparticules magnétiques couplées à des anticorps dirigés spécifiquement contre les marqueurs de surface CD34 (marqueur des cellules souches hématopoïétiques et des cellules endothéliales capillaires), CD31 (marqueur des cellules endothéliales et de la lignée hématopoïétique) et CD14 (marqueur des monocytes/macrophages). Nous avons ainsi démontré que les cellules positives pour le CD34 et négatives pour le CD31 (CD34+/CD31-) sont la seule population cellulaire présente dans la FSV capable de présenter la capacité de différenciation adipocytaire en condition adipogénique (241). De plus, notre groupe a récemment mis en évidence que cette population cellulaire CD34+/CD31- possède, en milieu endothélial, la capacité d’exprimer des marqueurs endothéliaux et de s’organiser en structures semblables à des capillaires (173). Ces résultats indiquent que la fraction cellulaire CD34+/CD31- de la FSV du TA humain, n’ayant subi aucune étape d’extension in vitro, présente des propriétés de cellules progénitrices capables de donner naissance à des cellules qui expriment des marqueurs phénotypiques des adipocytes et des cellules endothéliales. Il reste cependant à déterminer si cette population cellulaire est constituée d’un mélange de cellules progénitrices unipotentes ou de cellules souches multipotentes. D’autre part et de façon inattendue, les cellules CD34+/CD31présentent des caractéristiques différentes des cellules souches mésenchymateuses et hématopoïétiques puisqu’elles ne sont capables ni d’exprimer le marqueur CD105, propre aux cellules souches mésenchymateuses, ni douées d’activité hématopoïétique, en conditions de culture adaptées (241). Ainsi, l’origine mésenchymateuse des précurseurs adipocytaires communément admise jusqu’ici est remise en question. Toutefois, il est important de noter que la quantité de cellules souches mésenchymateuses dans la moelle osseuse est très faible et que leur isolement requiert des phases d’expansion in vitro (210). Ainsi, aucune étude n’a pu pour l’instant être réalisée sur des cellules souches mésenchymateuses fraîchement isolées. L’expression de nombreux marqueurs de surface est modulée par la culture et l’état de prolifération des cellules (112). Ainsi, l’expression du marqueur CD34 est connue pour être diminuée alors que celle de CD105 est augmentée par l’état de prolifération cellulaire (170, 173, 174, 241). On peut donc penser que l’expression du CD34 des cellules progénitrices CD34+/CD31- du TA et l’absence du marqueur CD105 est relative au fait que ces cellules n’ont pas subi de phases d’expansion. Il est à noter que certaines équipes suggèrent que les précurseurs adipocytaires pourraient être originaires d’une dédifférenciation des adipocytes matures (5, 186, 211). Cependant, peu de données sont en 21 accord avec cette hypothèse et l’on peut supposer que cette dédifférenciation apparente des adipocytes pourrait être due à une contamination des adipocytes matures par des cellules progénitrices. En effet, les études de Miyazaki et al. montrent qu’en condition de culture flottantes (c’est-à-dire quand la surface cellulaire adhérente se trouve au-dessus des cellules), des progéniteurs adipocytaires, fixés sur les adipocytes, sont capables de migrer sur la surface de culture et de se différencier en adipocytes (175). B.2) Le processus de différentiation adipocytaire B.2.1) Les étapes du processus de différenciation adipocytaire La différenciation adipocytaire proprement dite ou adipogenèse représente le passage du préadipocyte à l’adipocyte mature. Après une phase de croissance exponentielle, le précurseur déterminé vers la lignée adipocytaire ou adipoblaste marque un arrêt de croissance à confluence (figure 5). Ces cellules deviennent alors des préadipocytes et s’engagent dans l’adipogenèse proprement dite. Tout au long du processus d’adipogenèse vont se succéder différents événements morphologiques, biochimiques et moléculaires, que l’on regroupe en deux catégories, les événements précoces et tardifs. Les événements précoces concernent en particulier le remodelage de la matrice extracellulaire (MEC) et du cytosquelette (figure 6). Au cours de la différenciation adipocytaire, la composition de la MEC est fortement modifiée. D’une structure riche en fibronectine, sa composition va évoluer vers une structure de type lame basale, composée essentiellement de laminine, collagène IV et d’entactine (151). En effet, une diminution de la production du collagène fibrillaire de type I et III et de la fibronectine et une augmentation de la production de la laminine, des protéoglycans, de l’entactine et du collagène de type IV ont été observés au cours de la différenciation des préadipocytes d’origine murine et bovine (132, 133, 184). Des cultures de préadipocytes murins, porcins et humains réalisées sur différents supports matriciels ont souligné la variation d’adipogenèse selon le type de matrice utilisé suggérant le rôle essentiel de la composition et de l’organisation de la MEC dans la différenciation adipocytaire (95, 98, 133). Ainsi, l’ensemble de ces données suggère l’importance du remodelage de la MEC durant le processus adipogénique. Grâce à un remodelage matriciel, les tensions avec le cytosquelette sont modifiées. Des changements dans la forme de la cellule sont possibles par une réorganisation du réseau intracellulaire d’actine (252). L’ensemble de ces remodelages matriciels, du cytosquelette et de la forme de 22 Collagène I, III Fibronectine Structure fibroblastique des préadipocytes Confluence et engagement des préadipocytes C/EBP PPARγ Remodelage du cytosquelette et transcription de gènes adipogéniques (C/EBP et PPARγ) Remodelage matriciel via des protéases Synthèse d’aP2, LPL, FAS … Synthèse de la MEC par les préadipocytes au cours de la différenciation Collagène IV et Entactine Adipocytes matures Figure 6 : Evolution de la matrice extracellulaire et de la forme cellulaire au cours de la différenciation adipocytaire D’après Lilla J, Am J Path, 2002 la cellule permet alors aux préadipocytes de subir une étape d’expansion clonale liée à une série de réplications de l’ADN ou mitoses dites post-confluentes. A la suite de ces événements précoces, les préadipocytes sont dits « engagés dans la différenciation adipocytaire ». En anglais, on parle encore de « commitment » des préadipocytes. Enfin, une étape de maturation terminale permet d’obtenir les adipocytes matures. Cette maturation terminale est marquée par l’acquisition des propriétés métaboliques et sécrétoires des adipocytes matures (91). B.2.2) Contrôle transcriptionnel de la différenciation adipocytaire Les changements morphologiques majeurs qui accompagnent la différenciation adipocytaire, tels que l’arrondissement des cellules et l’accumulation progressive de vacuoles lipidiques dans le cytoplasme, sont la conséquence de variation d’expression d’un très grand nombre de gènes. Cette reprogrammation génétique profonde est sous le contrôle de facteurs de transcription pro- ou anti-adipogéniques dont les principaux sont les facteurs PPARs (Peroxisome proliferator-activated receptors), les C/EBPs (CCAAT/enhancer binding proteins) et le facteur ADD1/SREBP-1c (Adipocyte determination and differentiation factor 1/sterol regulatory element binding protein-1c) (pour revue (74, 226). B.2.2.1) Les PPARs Les facteurs de transcription PPARs appartiennent à la superfamille des récepteurs nucléaires. Une fois activés par la liaison à leur ligand, ils forment des hétérodimères avec les récepteurs de l’acide 9-cis-rétinoïque (RXR) qui reconnaissent spécifiquement des éléments de réponse PPRE (« PPAR Responsive Element ») situés dans les régions promotrices de gènes cibles. Chez les mammifères, trois isoformes de PPARs α, β (ou δ ou NUC-1 (nuclease abnormal-1)), et γ ont été décrites, chacun codé par un gène différent et caractérisés par une distribution tissulaire, des ligands, des co-facteurs et des fonctions qui leur sont propres. De multiples études démontrent que PPARγ, et plus particulièrement PPARγ2, est préférentiellement exprimée dans les adipocytes et joue un rôle majeur dans le contrôle transcriptionnel de la maturation terminale de l’adipocyte. En effet, il transactive de nombreux gènes marqueurs de la différenciation adipocytaire, tels que celui de la LPL ou celui codant pour la protéine de transport aux acides gras (aP2) (228). Plusieurs ligands capables d’activer le PPARγ majorent le taux de conversion adipocytaire et l’amplitude de la 23 différenciation. C’est notamment le cas des thiazolidinediones qui sont utilisées dans le traitement du diabète et de l’insulino-résistance. De plus, la 15-déoxy-δ prostanglandine et l’acide lysophosphatidique (LPA) sont décrits comme des activateurs du facteur de transcription (23, 171). Toutefois leur affinité pour le PPARγ est beaucoup plus faible que celle habituellement décrite pour les récepteurs nucléaires avec leurs ligands physiologiques. B.2.2.2) Les C/EBPs Les facteurs C/EBPs appartiennent à la famille des facteurs de transcription à motifs basiques et glissières de leucines (bHLH, « basic Helix Loop Helix »). Le domaine basique permet à ces facteurs de se lier à l’ADN alors que le motif en glissières de leucines leur permet de s’homo- ou de s’hétéro-dimériser. Trois isoformes de C/EBPs, α, β et γ, possèdent un rôle inducteur dans l’adipogenèse (227, 228). Les C/EBPs β et γ sont induits de façon très précoce et transitoire au cours de l’adipogenèse, et jouent un rôle clé dans l’enclenchement de la maturation terminale. L’induction de C/EBPα se fait plus tardivement et permet de transactiver différents gènes marqueurs de la différenciation adipocytaire tels qu’aP2, PPARγ et la leptine mais également d’induire sa propre expression (227, 228). Récemment, des travaux ont montré que des souris déficientes pour CHOP-10 (CCAAT/enhancer binding protein (C/EBP) homologous protein), un facteur de transcription anti-adipogénique appartenant à la famille des C/EBPs présentent une adiposité importante mais aucun désordre métabolique associé (6). Cet effet semble impliquer les facteurs C/EBPs. Les nombreuses données expérimentales obtenues depuis ces dernières années et sur les lignées murines principalement, ont permis de proposer un modèle de progression des ces facteurs de transcription au cours de l’adipogenèse (figure 7) (7). B.2.2.3) Le facteur SREBP-1 Le facteur ADD1/SREBP-1 fait partie de la famille des facteurs à motifs héliceboucle-hélice (bHLH-LZ pour basic helix-loop-helix-leucine zipper). Le domaine HLH permet à ces facteurs de former des homo- ou hétero-dimères avec des protéines de la même famille. Après dimérisation, le complexe se lie par le domaine basique à des séquences spécifiques dites E-box, situées au niveau des promoteurs de gènes cibles. De nombreuses études ont montré l’implication de SREBP-1 au niveau hépatique et adipocytaire dans la 24 Figure 7 : Progression des facteurs de transcription au cours de l’adipogènese dans les préadipocytes de la lignée 3T3-L1 D’après Avram MM., J. Am. Acad. Dermatol., 2007 régulation de nombreux gènes impliqués dans le métabolisme du cholestérol, des TG et des acides gras (65, 103). Au niveau du TA, il favorise l’adipogenèse en induisant l’expression de PPARγ (73, 122). B.2.2.4) Les autres facteurs de transcription En dehors de ces intervenants essentiels dans l’adipogenèse, d’autres facteurs transcriptionnels aux fonctions pro- ou anti-adipogéniques constituent potentiellement des régulateurs importants de la différenciation adipocytaire. Ces différents facteurs sont identifiés et présentés dans la figure 8 (d’après revue (78)). Notons que les facteurs de transcription Kruppel-like factor 15 et 5 (KLF15 et 5), appartenant à la famille des facteurs à doigts de zinc, sont décrits comme étant pro-adipogéniques alors que KLF2 est antiadipogénique (177, 194, 292). Le facteur Krox 20 apparaît comme le facteur le plus précoce induit directement par les signaux hormonaux (39). De manière intéressante, le facteur de transcription CREB (cAMP-response-element binding protein) a été impliqué dans l’accumulation des TGs dans des préadipocytes murins soumis à une dysfonction mitochondriale par un traitement avec l’antimycin A (272). B.2.3) Régulation hormonale et intracellulaire de la différenciation adipocytaire Le processus d’adipogenèse que nous venons d’aborder est hautement contrôlé par de nombreux facteurs de nature très variée: hormones, cytokines, nutriments et molécules de signalisation cellulaire. Les principaux facteurs connus sont présentés dans le tableau 2 et classés selon leur effet pro- ou anti-adipogénique. 25 CHOP CUP Ids δ-IP δ-FosB GATA-2 et -3 RARα SMADs TCF/LEF KLF2 PPARγ et δ C/EBP α, β et γ SREBP-1 CREBs STATs NFATs FOXC2 Foxa-2 HMGs LXR KLF5 et 15 Krox20 Rev-erb- α Notch Facteurs de transcription anti-adipogéniques Facteurs de transcription pro-adipogéniques Figure 8 : Balance entre les facteurs de transcription pro- et anti-adipogéniques (CHOP: C/EBP homologous protein; CUP: C/EBP unidentified protein; Ids: inhibitor of DNA binding; RARα: retinoic acid receptor α;TCF/LEF: T-cell factor/Lymphoid enhancer factor; KLF: Kruppel like factor; CREBs: cAMP responsive element binding protein; STATs: signal transducers and activators of transcription; NFATs: nuclera factor of activated T cells; FOXC2: Forkhead box C2; HMGs: high mobility group proteins; LXR: liver X receptor) D’après Fève B. , Best. Pract. Res. Clin. Endocrinol. Metab., 2005 Tableau 2: Facteurs extracellulaires et molécules de signalisation régulant la différenciation adipocytaire Facteurs pro-adipogénique Hormone Facteurs anti-adipogéniques Hormone de croissance, Prolactine Déhydroépiandrostérone Insuline, T3 Vitamine D (selon les modèles) Glucocorticoïdes Endothéline Vitamine D (selon les modèles) Résistine Prostaglandines I 2 et J 2 Prostaglandines F 2α Angiotensinogène (via la synthèse de prostaglandines) IGF1 (insulin-like growth factor 1) EGF (epidermal growth factor) facteurs de LIF (leukaemia inhibitory factor) PDGF (plateled-derived growth factor) croissance FGF10 (fibroblast growth factor 10) TGF-α et β (transforming growth factor) BMPs (Bone morphogenetic proteins) bFGF (basic fibroblast growth factor) MCSF (macrophage colony stimulating TNF-α (tumor necrosis factor α) factor) Interleukine 1, 6 et 8, Interféron γ Cytokines et Adiponectine Nutriments Acides gras, glucose, acides aminés Molécules de AMPc, H 2 0 2 (à faibles doses) Protéine kinase C signalisation Ras et Erk1 et 2 (à un stade précoce et MAP kinase Erk1 et 2 (à un stade tardif) transitoire) Kinase AMP-dépendante (AMPK) MAP Kinase p38 c-Jun amino-terminal kinases (JNK) Phosphatidy-inositol 3-kinase Protéine kinase B Autres Voie NF-κB Pref 1, Wnt10b, B.3) La vascularisation du tissu adipeux Au cours du développement embryonnaire du TA, l’angiogenèse est étroitement liée à l’adipogenèse (52, 285). Des études d’implantation sous-cutanée de préadipocytes de la lignée 3T3F442A chez des souris athymiques, ont clairement associé l’apparition de marqueurs adipocytaires aux marqueurs endothéliaux au site d’injection (90, 185). Ces résultats sont confirmés par les travaux de Fukumura et al. montrant que des préadipocytes 26 transfectés par un dominant négatif de PPARγ empêchant l’adipogenèse, inhibe l’angiogenèse au site d’implantation. En parallèle, l’inhibition de l’angiogenèse par un traitement avec un anticorps neutralisant anti-VEGF-R2, inhibe l’adipogenèse (83). Ainsi, adipogenèse et angiogenèse sont donc deux phénomènes étroitement liés. Le rôle de l’endothélium dans le développement du TA est reconnu depuis longtemps (285). Cependant, il a été négligé par le fait que le TA était généralement considéré comme peu vascularisé. Cette observation est essentiellement liée à la difficulté d’accès aux capillaires du TA, du fait de la grande taille des adipocytes matures et de leur organisation en couches multiples. En effet, l’analyse du TA après une période de jeûne chez l’animal qui s’accompagne d’une diminution du diamètre des adipocytes a permis de mettre en évidence l’ensemble du réseau vasculaire de ce tissu (225). Ainsi, en évaluant la densité capillaire du TA ou en marquant les érythrocytes au chrome 51, des études ont montré que le réseau vasculaire du TA est aussi important que celui du muscle squelettique et que chaque adipocyte présente des contacts étroits avec au moins un capillaire sanguin (94, 107). L’importance de l’endothélium pourrait en partie s’expliquer par le rôle clé de la surface endothéliale dans le contrôle de la lipogenèse adipocytaire via la LPL, enzyme sécrétée par les adipocytes et active à la surface des cellules endothéliales. En effet, les cellules endothéliales semblent jouer un rôle direct dans les phénomènes de trafic intercellulaire de la LPL par la sécrétion d’un facteur qui, sous stimulation de l’insuline, libèrerait la LPL des protéoglycans à héparane sulfate adipocytaires (126). En résumé, les lignées cellulaires murines ont permis une étude approfondie des processus de détermination et de différenciation adipocytaires. Le processus de détermination adipocytaire est cependant peu connu contrairement à la différenciation adipocytaire qui a suscité de nombreuses études. Par ailleurs, la mise en évidence récente de cellules souches multipotentes au sein de la FSV permet au TA d’acquérir un nouveau statut de « source d’approvisionnement de cellules souches/progénitrices » pour d’éventuelles thérapies cellulaires. Cependant, de nombreux points restent encore à élucider, notamment déterminer si la FSV du TA renferme un pool de cellules souches aux potentialités variées ou bien une seule et unique cellule multipotente. De même, malgré des similitudes, il est nécessaire de déterminer si les cellules souches/progénitrices issues du TA adulte sont identiques aux préadipocytes d’origine embryonnaire et si des différences inter-espèces sont observées (hommes vs rongeurs). 27 C) Le développement excessif du tissu adipeux : l’obésité L’indice de masse corporelle (IMC), rapport du poids sur la taille au carré, permet d’évaluer la corpulence d’un individu adulte. Le tableau 3 présente la classification des adultes de poids normal, en surpoids, obèse ou maigre (sous-poids). Tableau 3: Classification des adultes maigres, normaux, en surpoids et obèses selon l’IMC IMC (kg/m2) Classification Sous-poids < 18,50 Maigreur sévère < 16,00 Maigreur modérée 16,00 - 16,99 Maigreur légère 17,00 - 18,49 Poids normal 18,50 - 24,99 Surpoids ≥ 25,00 Pré-obèse 25,00 - 29,99 Obésité ≥ 30,00 Obésité de classe I 30,00 - 34,99 Obésité de classe II 35,00 - 39,99 Obésité de classe III ≥ 40,00 Classification définie par l’organisation mondiale de la Santé D’après WHO expert consultation, The Lancet, 2004,.(48) L’obésité correspond à une surcharge pondérale résultant d’un développement excessif du TA. Les potentialités d’extension du TA sont uniques. En effet, la masse grasse peut-être multipliée par quatre chez un individu obèse et peut représenter jusqu'à 60 à 70% de sa masse corporelle. De nombreux événements cellulaires et biochimiques sont responsables de la croissance excessive du TA adulte. Dans les paragraphes suivants, nous allons voir les modifications du TA lors de l’obésité, aussi bien dans sa composition cellulaire que dans ses fonctions métaboliques et sécrétoires. 28 C.1) Les modifications cellulaires du tissu adipeux C.1.1) Les adipocytes et les cellules souches/progénitrices Les changements dans la masse du TA sont associés à des modifications de la taille et du nombre des adipocytes (214). L’augmentation du volume des adipocytes correspond à une hypertrophie adipocytaire. Le diamètre moyen d’un adipocyte peut aller jusqu’à 120µm chez le sujet obèse. Selon l’hypothèse dite de la « taille critique », la cellule adipeuse se chargerait en TGs jusqu'à atteindre une taille critique au-delà de laquelle une phase d’hyperplasie apparente apparaîtrait au sein du tissu. Ces nouveaux adipocytes proviendraient de la prolifération et/ou du recrutement de cellules progénitrices associés à leur différenciation. Les études de Crossno et al montrent que des souris soumises à un régime gras sont capables de recruter des cellules souches de la moelle osseuse dans le TA afin de former de nouveaux adipocytes (54), cependant les mécanismes impliqués ne sont pas caractérisés. Ainsi deux phases adipocytaires auraient lieu dans le TA une phase d’hypertrophie cellulaire suivie dans les cas d’obésité sévère d’une hyperplasie adipocytaire (15, 249). Les mécanismes responsables de l’hypertrophie adipocytaire s’expliquent par des altérations des activités métaboliques (lipogenèse et lipolyse) des adipocytes. Nous le verrons dans le chapitre suivant. L’augmentation du nombre d’adipocytes est moins bien définie. Récemment, les travaux de Tchoukalova et al. indiquent que la proportion des préadipocytes de la FSV, positifs pour le marqueur aP2 et négatifs pour le CD68 (un marqueur des macrophages), est diminuée avec l’obésité (262). Ces travaux peuvent être associés à ceux de van Harmelen indiquant que la capacité de différenciation adipocytaire des cellules de la FSV est négativement corrélée avec l’IMC (271). C.1.2) Les cellules endothéliales Des travaux de notre groupe indiquent que l’évolution du réseau vasculaire est parallèle à celui de la masse adipeuse suggérant que le développement du TA est associé à une néovascularisation. En effet, le pourcentage de cellules endothéliales des capillaires sanguins, caractérisées par la double expression CD34 et CD31, au sein de la FSV, reste constant avec l’augmentation de l’IMC (173). La dépendance du TA vis-à-vis de son réseau vasculaire au cours de l’obésité a été mise en évidence grâce à de récents travaux montrant que des facteurs anti-angiogéniques limitent le développement de la masse grasse dans 29 différents modèles de souris obèses (19, 233). De plus, l’apoptose sélective des cellules endothéliales, in vivo par l’utilisation d’un phage contenant un peptide pro-apoptotique associé à la prohibitine, une protéine membranaire de surface, entraîne une réversion de l’obésité chez la souris (129). Ainsi, le réseau vasculaire joue un rôle déterminant dans la croissance mais également dans le maintien de la masse grasse. Les mécanismes impliqués dans l’extension du réseau vasculaire lors du développement du TA ne sont pas connus. Cependant, de nombreuses évidences montrent que les adipocytes sécrètent de nombreux facteurs angiogéniques (16, 17, 154, 301) et que cette production est augmentée avec l’état d’obésité (247). De plus, on peut supposer que les cellules CD34+/CD31- pourraient également via des processus de vasculogenèse, i.e. différenciation en cellules endothéliales, participer à l’augmentation du résseau vasculaire du TA. Récemment, une étude réalisée sur un modèle de souris obèse db/db a évalué simultanément l’angiogenèse et l’adipogenèse et a montré une étroite relation spatiale et temporelle entre la formation de nouveaux vaisseaux sanguins à partir de vaisseaux préexistants et le processus de différenciation adipocytaire (189). C.1.3) Les macrophages La présence de macrophages au sein du tissu adipeux a été mise en évidence depuis longtemps par les histologistes (263) mais n’a suscité que très peu d’intérêt jusqu'à ces dernières années. Des observations récentes suggèrent l’implication de cette population cellulaire dans l’installation d’un état pro-inflammatoire, au sein du TA, lors de son développement excessif. En effet dans différents modèles animaux d’obésités, une accumulation de macrophages a été observée lors du développement de la masse grasse (286, 293). De plus, notre groupe a montré que le pourcentage de macrophages au sein de la SVF est corrélé de façon positive avec l’IMC dans les tissus adipeux sous-cutanés (55) et viscéraux (56) humains. Inversement, l’équipe de K. Clément a montré que la quantité de macrophages infiltrés dans le TA est diminuée après une perte de poids chez des sujets obèses (24, 46). L’origine de cette augmentation de la population macrophagique au sein du TA des sujets obèses n’est pas bien comprise. De par les similitudes d’expression génique entre adipocytes et macrophages et l’observation des capacités de phagocytose décrites dans le préadipocyte humain, il a été suggéré que les macrophages puissent provenir de la différenciation des préadipocytes (235). Cependant notre équipe n’a pu mettre en évidence 30 d’activité hématopoïétique à partir de précurseurs adipocytaires humains (241). Des expériences de transplantation de moelle osseuse chez la souris démontrent que 80% des macrophages du TA sont d’origine médullaire, suggérant ainsi que les macrophages du TA sont issus de l’infiltration de monocytes sanguins circulants (286). De plus, notre groupe a montré que les sécrétions adipocytaires stimulent l’activation endothéliale conduisant à une augmentation de l’adhérence et de la transmigration des monocytes sanguins à travers l’endothélium du TA humain (55). En conditions normales, la fonction majeure des macrophages résidents au sein d’un tissu est d’éliminer le matériel étranger et les cellules apoptotiques, processus essentiel dans le maintien de l’homéostasie tissulaire. Le rôle des macrophages au niveau du TA lui-même reste à être clairement défini. Toutefois, des travaux récents chez la souris indiquent que l’infiltration des macrophages due à une obésité induite par un régime hypercalorique semble être plus liée à l’insulino-résistance associée à l’obésité qu’à l’augmentation de la masse grasse (155, 192, 286). C.2) Les modifications des fonctions métaboliques du tissu adipeux Au cours de l’obésité, une augmentation de la lipogenèse semble évidente. Quelques études ont rapporté que l’activité de la LPL était associée à la taille des adipocytes (66, 75). Un excès de masse grasse s’accompagne également d’une altération de la fonction lipolytique du TA au repos et au cours de l’exercice physique (102). Plusieurs travaux in vitro menés au laboratoire ont évalué l’effet de l’obésité et du surpoids sur la régulation adrénergique de la lipolyse. Le nombre de récepteurs α2A -adrénergiques des adipocytes. Ainsi, les récepteurs a été corrélé positivement avec la taille α2A -adrénergiques sont fortement exprimés dans le TA sous-cutané où les adipocytes sont hypertrophiés, et bien plus dans le tissu fémoral qu’abdominal suggérant une faible activité lipolytique de l’adrénaline dans le TA abdominal voire antilipolytique dans le TA fémoral chez la femme (13, 166). Chez le sujet obèse, les réponses lipolytiques mesurées in situ dans le TA sous-cutané, sont très diminuées par rapport à des sujets de poids normal au cours d’un exercice physique. Ceci s’explique par une activation soutenue des récepteurs α2A -adrénergiques, surnuméraires dans les adipocytes hypertrophiés de l’obèse (255). Par ailleurs, de nombreux travaux mentionnent une perte de sensibilité du TA sous-cutané aux catécholamines au repos, ce qui entraîne une diminution des réponses β -adrénergiques. Cette résistance aux catécholamines dans l’adipocyte d’obèse pourrait provenir d’une diminution de la fonction β2 -adrénergique (70), d’une diminution de l’activité et de l’expression de la LHS (143), ou encore de l’expression majoritaire d’une 31 isoforme catalytiquement inactive (219). Notons que des différences dans la lipolyse et la lipogenèse ont été décrites dans les TA humains sous-cutanés et viscéraux de patients obèses (72, 136). C.3) Les modifications des fonctions sécrétoires du tissu adipeux Comme nous l’avons précédemment évoqué, le TA se comporte comme un organe endocrine. Ainsi, de nombreuses études se sont focalisées sur les modifications des sécrétions de ce tissu au cours de l’obésité (72). Dans le tableau 4 sont présentés les principaux facteurs connus pour être modulés lors du développement excessif de la masse grasse. Tableau 4: Sécrétions du tissu adipeux modulées au cours de l’obésité Augmentation Hormone Leptine Facteurs de croissance TNF-α et cytokines IL-1, 6, 8 et 10 Diminution Adiponectine Résistine Apeline iNOS TGF-β MCP-1 HGF Protéases et inhibiteurs PAI-1 de protéases Cathepsine K et S MMP-9 Autres Angiotensine Tissue factor Facteur VII C-reactive protein (TNF-α: tumor necrosis factor- α, IL: interleukine, iNOS: inducible nitric oxide synthase, TGF-β: transforming growth factor-β, MCP-1: monocyte chemoattractant protein-1, HGF: hepatocyte growth factor, PAI1:plasminogen activator inhibitor 1, MMP-9 : matrix metalloprotease 9) 32 En résume, l’obésité chez l’homme s’accompagne d’un remodelage important de la masse grasse associé à des modulations des fonctions métaboliques et sécrétoires du TA. Les mécanismes responsables de ces changements ne sont pas totalement définis mais ces altérations semblent être impliquées directement dans la genèse des pathologies associées à l’obèsité. Ainsi l’augmentation de la population macrophagique inflammatoire et les changements dans la production d’adipokines dont principalement la leptine et l’adiponectine sont deux éléments clés dans le développement de l’insulinorésistance et de la dysfonction endothéliale, évènements précoces impliqués dans le diabète de type II et les pathologies cardiovasculaires. 33 D) La régression du tissu adipeux : la lipoatrophie En plus de ces capacités de croissance, le TA est également capable de régression. On parle de lipoatrophie ou lipodystrophie. La classification des syndromes de lipoatrophies est indiquée dans le tableau ci-dessous. Tableau 5: Classification des différentes lipoatrophies humaines Classification des lipoatrophies humaines 1) Génétiques - Lipodystrophie congénitale généralisée (Syndrome de Berardinelli-Seip) Type 1 : mutations d’une acyltransférase codée par AGPAT2 Type 2 : mutations de la séipine - Lipodystrophie familiale partielle Type Dunnigan : mutations de la lamine A/C Associée à PPARγ : mutations de PPARγ Associée à Akt2/PKB : mutations de Akt/PKB - Dysplasie mandibuloacrale Type A, partielle, mutations de la lamine A/C Type B, généralisée, mutations de ZMPSTE24 (une métalloprotéase à zinc) - Syndromes progéroïdes (Syndrome de Werner, syndrome Cockayne) - Syndrome de déficience en carbohydrate glycoprotéine - Syndrome SHORT (Short stature, Hyperextensibility, Hernia, Ocular depression, Rieger anormaly and Teething delay) 2) Présumées inflammatoires ou autoimmunes - Lipoatrophie acquise généralisée (Syndrome de Lawrence) - Lipoatrophie acquise partielle (Syndrome de Barraquer-Simons) - Lipoatrophie acquise associée à des dermatomyosites - Lipodystrophie associée à une hypocomplémentémie 3) Acquises, de causes inconnues - Lipodystrophie associée aux traitements anti-VIH D’après Reitman et al, TEM, 2000 et Garg et al, Clinical Cornestone, 2006 34 Dans certains syndromes de lipoatrophie, l’absence localisée au niveau de la face et des membres ou généralisée de TA est associée à une accumulation du TA au niveau des régions abdominales, dorso-cervicales et mammaires. On parle dans ce cas de lipodystrophies. Ces syndromes peuvent avoir des causes génétiques, immunes ou associées aux traitements thérapeutiques lors d’infection en particulier pour le VIH (pour revue (25, 222). Paradoxalement elles sont, comme l’obésité, associées à des complications métaboliques telles que l’hypertriglycéridémie, l’insulino-résistance, la stéatose hépatique et les pathologies cardio-vasculaires. Les syndromes lipoatrophiques étaient très rares (moins de 1 cas pour 100 000) jusqu’à ces dix dernières années où sont apparues les formes liées aux traitements antirétroviraux de l’infection par le VIH. Ce sont les inhibiteurs de la protéase du VIH (IPsVIH) qui ont été initalement associés à l’émergence de ce syndrome (31, 33, 34). Cependant, des travaux démontrent que des patients séropositifs recevant des inhibiteurs nucléosidiques de la reverse transcriptase du VIH en particulier la stavudine et la zidovudine (INRTs) et naïfs pour les IPs-VIH développent également une lipoatrophie périphérique (20, 32, 157). Par ailleurs, il a été rapporté que ces traitements pourraient agir en synergie entraînant une atrophie profonde du TA (158, 269). Au cours de ce paragraphe, nous allons faire le point sur les modifications cellulaires, métaboliques et sécrétoires du TA lors d’une régression importante. Nous nous appuierons essentiellement sur les données des lipoatrophies associées aux traitements anti-VIH qui sont actuellement les lipoatrophies les plus fréquentes et les plus étudiées (276). D.1) Les modifications cellulaires du tissu adipeux Les études réalisées sur le TA sous-cutané des patients traités par les IPs-VIH et les INRTs montrent une atteinte profonde de la morphologie du TA (62, 110, 152). Les effets décrits des IP-VIH et des INRTs sur les différents types cellulaires qui composent le TA vont être abordé dans les paragraphes suivants. D.1.1) Les adipocytes Une perte de poids est forcément associée à une diminution de la taille et/ou du nombre des adipocytes. Si l’existence d’une différenciation adipocytaire après les phases de développement normal est maintenant connue, la possibilité d’une perte des adipocytes est 35 moins bien documentée. Les études sur l’apoptose dans le TA sont peu abondantes (250). Cependant, il est admis que l’apoptose peut se produire dans le TA et notamment dans les adipocytes matures. Un certain nombre de facteurs ont été rapportés pour entraîner l’apoptose des adipocytes in vitro, notamment des cytokines inflammatoires telles que le TNFα (213), des flavonoïdes et des acides gras polyinsaturés (121, 188). Une augmentation de l’apoptose des adipocytes a été décrite chez des patients infectés par le VIH et ayant développé une lipoatrophie du TA suite aux traitements antirétroviraux (62, 63, 110). Il est admis que les traitements antirétroviraux influent sur ce processus apoptotique. En effet, il a été rapporté que le nelfinavir (NFV), un IP-VIH, favorise l’apoptose des préadipocytes différenciés murins des lignées 3T3-L1 et 3T3F442A (12, 64). Notons que les mécanismes directement mis en jeu ne sont pas encore définis. Par ailleurs, ces effets apoptotiques ne sont pas retrouvés dans les préadipocytes murins non différenciés (64). Le NFV a également été rapporté pour induire la nécrose des préadipocytes différenciés de la lignée 3T3F442A via une augmentation des espèces réactives de l’oxygène (278) associée à un stress du réticulum endoplasmique (264). Concernant les INRTs, une étude indique que la stavudine (un INRT) entraîne une apoptose des préadipocytes différenciés murins de la lignée 3T3F442A (28). De plus, des patients traités avec la stavudine ont une augmentation de l’apoptose dans le TA mise en évidence par la technique TUNEL (terminal deoxynucleotidyl transferase dUTP digoxigenin nick-end labeling) (168). Il semblerait que l’apoptose adipocytaire induite par les INRTs soit due à la genèse d’une toxicité mitochondriale. En effet, le TA des patients infectés par le VIH et traités avec les INRTs, dont principalement la stavudine, présente des dysfonctionnements mitochondriaux tels qu’une baisse des taux d’ADN mitochondrial (ADNmt) et des anomalies de structure des mitochondries (169, 281). De plus, le remplacement de la stavudine par d’autres INRTs tels que l’abacavir ou la zidovudine améliore les taux d’ADNmt et prévient l’apoptose (168). Ces phénomènes peuvent s’expliquer par le fait que les INRTs pourraient inhiber, outre la réverse transcriptase du VIH, d’autres ADN polymérases et notamment, l’ADN polymérase mitochondriale γ. Cette polymérase est impliquée dans la réplication de l’ADNmt et son inhibition conduit à une déplétion des taux d’ADNmt et/ou à des altérations de la structure génomique de l’ADNmt (245) provoquant ainsi une augmentation des espéces réactives de l’oxygène et l’apoptose cellulaire. L’apoptose des adipocytes joue donc un rôle important dans l’apparition du syndrome de lipoatrophie associée aux traitements antirétroviraux. Les travaux de Pajvani et al. ont permis de montrer par l’utilisation de souris transgéniques surexprimant de manière conditionnelle la caspase 8, une enzyme pro36 apoptotique, spécifiquement dans les adipocytes, l’expression du transgène étant sous le contrôle du promoteur d’aP2, que le déclenchement de l’apotose adipocytaire par activation de la caspase 8 s’accompagnait d’un phénotype lipoatrophique. Ces travaux démontrent ainsi que l’induction et le maintien d’une apoptose adipocytaire pourraient contribuer à la genèse des lipoatrophies (201, 266) D.1.2) Les cellules progénitrices/ souches Outre les effets des composés antirétroviraux sur l’apoptose adipocytaire, de nombreux travaux montrent que ces composés altèrent également le processus de différenciation adipocytaire. De nombreuses études ont évalué l’effet des IPs-VIH tels que le saquinavir (SQV), le nelfinavir (NFV) et l’indinavir (IDV) sur la différenciation des préadipocytes murins des lignées 3T3-L1 et 3T3F442A et ont montré que ces inhibiteurs de protéases limitent leur différenciation adipocytaire (64, 144, 176, 300). Chez l’homme, il existe peu de données concernant les effets des IPs-VIH sur la différenciation adipocytaire. Deux études réalisées sur des cellules de la FSV du TA humain d’origine mammaire et des cellules souches mésenchymateuses humaines confirment les effets anti-adipogéniques de l’IDV et du SQV (109, 288). A l’inverse, les effets des INRTs sur la différenciation des préadipocytes murins ne sont pas clairs. Certaines études rapportent que ces inhibiteurs entraînent une diminution de l’adipogenèse (224) et d’autres n’observent aucun effet (28, 198). Récemment un inhibiteur non nucléosidique de la reverse transcriptase du VIH (INNRT), l’efavirenz, a également fait l’objet d’une étude in vitro. Il a été observé que cet INNRT inhibe la différenciation des préadipocytes murins de la lignée 3T3-L1 et humains (68) suggérant que la troisième classe de médicaments utilisée pour le traitement du VIH contribue à l’altération de la masse grasse. In vivo, sur des biopsies de TA sous-cutané provenant de patients infectés par le VIH et ayant développé une atrophie adipocytaire, suite au traitement antirétroviral, des altérations des taux de CEBP/α, de PPARγ et de SREBP-1 ont également été décrites (10). Ces résultats suggèrent que les IPs-VIH altèrent les processus de différenciation adipocytaire dans les étapes précoces. Cependant, les cibles exactes de ces composés ne sont pas encore totalement définies. L’effet anti-adipogénique des IPs-VIH pourrait tout d’abord s’expliquer par des interactions avec la voie de signalisation de l’acide rétinoïque. En effet, la région catalytique de la protéase du VIH qui lie les IPs-VIH a environ 60% d’homologie avec CRABP-1 (cytoplasmic retinoic acid binding protein-1), un régulateur intracellulaire des taux d’acide 37 rétinoïque. Ainsi, les IPs-VIH peuvent inhiber la fonction de CRABP-1 et limiter le processus d’adipogenèse qui nécessite l’expression des gènes dépendants de l’acide rétinoïque (34). De plus, les IPs-VIH ont été également décrits pour être des inhibiteurs du cytochrome P450 3A, l’unique enzyme connue pour convertir l’acide rétinoïque en acide cis-9-rétinoïque, le ligand du RXR (Retinoïd X Receptor) qui par la suite s’hétérodimérise avec PPARγ (34). Cependant, il faut rester prudent quant à ces données puisque des études ont rapporté que des altérations du facteur de transcription PPARγ n’expliquent pas la diminution, induite par les IPs-VIH, de la différenciation des préadipocytes murins et humains (144, 288, 300). Des interactions entre SREBP-1 et les IPs-VIH ont également été décrites. Ainsi, le traitement des préadipocytes de la lignée 3T3F442A par l’IDV et le NFV s’accompagne d’une séquestration du facteur de transcription SREBP-1 au niveau de l’enveloppe nucléaire des préadipocytes contrairement aux préadipocytes contrôles qui accumulent SREBP-1 au niveau nucléaire (30). Le mécanisme responsable de cette séquestration de SREBP-1 consécutive à un traitement par les IPs-VIH n’est pas totalement élucidé. Cependant, certains travaux suggèrent un rôle clé de la lamine A, protéine majeure de l’enveloppe nucléaire. Le facteur SREBP-1 est synthétisé sous forme d’un précurseur inactif ancré au niveau du réticulum endoplasmique ou de l’enveloppe nucléaire puis maturé par clivage protéolytique. La forme mature active de SREBP-1 peut ensuite être transférée dans le noyau et activer directement la transcription génique (21, 22, 284). Une interaction entre SREBP-1 et la lamine A/C a déjà été décrite (153). La lamine A est synthétisée sous forme de prélamine A et sa maturation est assurée par clivage à l’aide d’une métalloprotéinase, FACE chez l’homme et Zmpste24 chez la souris. Les souris déficientes pour Zmpste24 présentent une lipoatrophie associée à une accumulation de prélamine A au niveau de l’enveloppe nucléaire (206). Le rôle clé de la lamine A et de la régulation de l’interaction lamineA/SREBP-1 dans le contrôle de la différenciation adipocytaire est de plus souligné par les syndromes majeurs de lipoatrophies génétiques qui sont dus à des mutations de la lamine A. Enfin, récemment il a été montré que les IPs-VIH provoquaient une accumulation de prélamine A dans des fibroblastes humains, suggérant que les IPs-VIH pourraient interagir avec FACE pour inhiber la maturation de la lamine et empêcher l’accès du noyau au facteur adipogénique SREBP-1 (27, 47). Enfin, une interaction des IPs-VIH avec le protéasome qui constitue la principale machinerie de dégradation protéique chez les eucaryotes (51) a été envisagée. Des études ont rapporté que les IPs-VIH sont des inhibiteurs de l’activité protéasomique de certaines cellules cancéreuses (239) mais aussi de préadipocytes murins de la lignée 3T3-L1 (202). Or, les 38 inhibiteurs spécifiques du protéasome tels que la lactacystine inhibent la différenciation des myoblastes (124), des ostéoclastes (299) mais aussi la différenciation des préadipocytes de la lignée 3T3-L1 (212). Nous verrons dans le chapitre Résultats les données que nous avons obtenues sur les interactions entre les IPs-VIH et le protéasome dans les préadipocytes humains. A ce jour, les mécanismes moléculaires des INRTs responsables de la baisse de l’adipogenèse observée dans les travaux de Roche et al. sont inconnus. Etant donné l’action des INRTs sur la fonction mitochondriale, il est tentant de spéculer que les INRTs peuvent diminuer l’adipogenèse via une augmentation des espèces réactives de l’oxygène. En effet, les espèces réactives de l’oxygène diminuent la prolifération et la différenciation adipocytaire des lignées murines (35, 36). Ainsi, l’ensemble de ces données suggère que la lipoatrophie associée au traitement antirétroviral semble également être due à un défaut du processus de différenciation adipocytaire. D’ailleurs, une étude récente implique majoritairement une altération de l’adipogenèse plutôt qu’une induction de l’apoptose des adipocytes dans la lipoatrophie de patients infectés par le VIH et sous tri-thérapie (181). D.1.3) Les cellules endothéliales Chez les patients infectés par le VIH et sous traitement antirétroviral, peu de données concernent les cellules endothéliales. On peut noter que l’infection au VIH est associée à l’activation de cellules endothéliales, observée par une augmentation plasmatique des marqueurs cellulaires de surface tels que VCAM (Vascular Cell Adhesion Molecule), Eselectin et ICAM1 (Intercellular Adhesion Molecule) chez des patients séropositifs (40). Par ailleurs, les traitements antirétroviraux entraînent des altérations de la fonction endothéliale chez des patients sains (244) et des dommages de l’ADNmt dans les cellules endothéliales humaines (114). Enfin, il a été observé, comme pour les adipocytes, une apoptose des cellules endothéliales chez des patients infectés par le VIH et sous traitement antirétroviral (62). Cependant, une augmentation de la densité des vaisseaux du TA atrophié de patients infectés par le VIH et traités a également été observée (110) et on peut se demander si cette augmentation apparente n’est pas relative en fait à la diminution du nombre et du volume adipocytaire. Toutefois, il récemment a été observé que les INRTs favorisent l’angiogenèse des cellules endothéliales humaines in vitro (61). A ce jour, il est difficile de conclure sur 39 l’effet de la régression du TA au niveau des cellules endothéliales. D’autres investigations sont nécessaires. D.1.4) Les macrophages Dans le TA sous-cutané de patients infectés par le VIH et sous tri-thérapie est observée une infiltration macrophagique (10, 62, 110, 190) similaire à celle observée dans le TA de patients obèses (24, 286). Cette accumulation de macrophages pourrait être due à l’apoptose des adipocytes. En effet, les travaux de Cinti et al. indiquent la présence de macrophages dans les TA de souris et d’humains obèses au niveau des adipocytes nécrosés (45). De manière identique, dans le modèle de souris lipoatrophiques surexprimant la caspase 8 dans le TA, il a été rapporté une augmentation du nombre de macrophages à proximité des adipocytes en cours d’apoptose (201). D.2) Les modifications des fonctions métaboliques du tissu adipeux Les traitements antirétroviraux affectent également les deux grandes fonctions métaboliques du TA. Ainsi, des études ont mis en évidence que les IPs-VIH diminuent la lipogenèse des préadipocytes murins différenciés (64, 137, 144). Ces effets semblent être dus à une diminution de l’activité de la LPL et de la synthèse de novo de lipides (218). Etant donné que les IPs-VIH ont la capacité d’interagir avec le transporteur du glucose GLUT-4, il a été suggéré que les effets des IPs-VIH sur la synthèse de novo de lipides passe par une inhibition de l’activité de GLUT-4 et du captage du glucose (99, 179, 180). Récemment, une inhibition de la lipogenèse a également été observée sur des préadipocytes murins différenciés et traités avec des INRTs mais aussi avec l’efavirenz, un INNRT (68, 137). La lipolyse est également touchée par les traitements antirétroviraux puisqu’ils sont associés à une augmentation des taux circulants d’AGNE (93). L’activation de la lipolyse semble être due à une combinaison complexe entre l’infection au VIH et les traitements associés. En effet, une augmentation de la lipolyse a été rapportée chez des patients infectés par le VIH et ce indépendamment du type de thérapie (268). In vitro, de nombreuses études ont mis en évidence que les IPs-VIH stimulent la lipolyse des préadipocytes différenciés murins (111, 144, 218, 231). De plus, une interruption de la prise de ces inhibiteurs diminue l’activation de la lipolyse et les taux d’AGNE chez les patients (268). Récemment, une étude 40 indique que l’effet stimulateur des IPs-VIH sur la lipolyse semble être du à une baisse des taux de périlipine par une augmentation de leur protéolyse lysosomale (130). L’ensemble de ces phénomènes pourraient donc expliquer la diminution de la taille des adipocytes chez des patients infectés par le VIH sous traitement antirétroviral (10, 152). D.3) Les modifications des fonctions sécrétoires du tissu adipeux Comme nous l’avons vu précédemment, le profil sécrétoire du TA varie au cours de l’obésité. Aussi, il n’est pas surprenant que lors d’une perte importante de TA, ce profil soit également modifié. Quelques études se sont intéressées aux modifications des sécrétions adipocytaires dues aux IPs-HIV et aux INRTs in vitro sur des préadipocytes différenciés murins et humains (118, 137, 139, 274) et in vivo dans le plasma et le TA de patients séropositifs sous traitement antirétroviral (43, 110, 115, 182, 259, 275). Les principaux facteurs connus pour être modulés par les traitements antirétroviraux in vitro et in vivo sont présentés dans le tableau 6. Notons que l’effet des traitements antirétroviraux sur la leptine n’est pas clair puisque deux études réalisées sur des préadipocytes différenciés humains diffèrent (138, 274). Par ailleurs, la diminution de la sécrétion de leptine observée in vivo est directement corrélée à la diminution de la quantité de TA des patients (275). Tableau 6: Impact des IPs-VIH et des INRTs sur les sécrétions adipocytaires in vitro et in vivo Augmentation Diminution Pas de modification IL-6 (137, 138, 274) TNF-α (137, 138, 274) Adiponectine IL-1β (137, 138) (137, 138, 274) Leptine (274) Leptine (138) IL-6 (137, 138) Adiponectine TNF-α (137, 138) (137, 138) IL-1β (137, 138) Leptine (138) Patients sous IL-6 (43, 115) Adiponectine (259) IPs-VIH et INRTs TNF-α (43, 115) Leptine (115) IPs-VIH INRTs 41 IL-1β (43) Les modifications importantes des sécrétions adipocytaires dues aux traitements antirétroviraux in vitro et in vivo pourraient contribuer à l’atrophie du TA et aux complications métaboliques qui lui sont associées. En effet, ces sécrétions peuvent altérer les principales fonctions métaboliques des adipocytes ainsi que leur survie cellulaire. De plus, certaines d’entre elles peuvent également moduler l’adipogenèse telles que le TNF-α et l’IL-6 (pour revue (89)). Pour conclure, les lipoatrophies résultent donc d’une profonde altération de la composition cellulaire et des grandes fonctions métaboliques et sécrétoires du TA. Suite à un défaut du maintien de l’homéostasie énergétique lors d’une perte de TA, ces phénomènes sont associés à des complications métaboliques similaires à celles rapportées lors d’un excès de TA. A l’heure actuelle, quelques approches thérapeutiques pour le traitement des lipoatrophies ont été développées (thiazolidinedione, metformine) mais elles agissent plus sur les complications métaboliques associées que sur l’altération du TA elle-même. Ainsi, une meilleure connaissance des mécanismes impliqués dans la régression de la masse grasse est nécessaire afin d’identifier de nouvelles cibles thérapeutiques. En conclusion de cette première partie, le TA subit donc un remodelage important lors d’un développement excessif (obésité) ou d’une régression (lipoatrophie) (pour illustration figure 9). Ainsi, la modification de la composition cellulaire du TA et les altérations des fonctions métaboliques et sécrétoires de ce tissu pourraient jouer un rôle clé dans les pathologies associées à l’obésité et aux lipoatrophies telles que le diabète de type II et les pathologies cardiovasculaires. Une meilleure compréhension des mécanismes impliqués dans la perte et le gain de poids ainsi que la découverte de nouvelles cibles thérapeutiques sont donc nécessaires. Il est évident que la plasticité du TA est possible grâce à fort remodelage tissulaire, au niveau cellulaire mais aussi au niveau matriciel. De nombreuses protéases ont été décrites pour être impliquées dans la régulation du remodelage tissulaire. Toutefois, les MMPs sont les acteurs majeurs du remodelage matriciel. Dans le chapitre suivant, nous aborderons la classification, la structure ainsi que la régulation de l’activité des MMPs. Puis, les modes d’action et les fonctions biologiques auxquels les MMPs sont associées seront présentés. Enfin nous aborderons le rôle potentiel de ces enzymes dans la plasticité du TA. 42 OBESITE LIPOATROPHIE Monocyte/ macrophage Monocyte/ macrophage Cellules endothéliales Cellules endothéliales Cytokines pro-inflammatoires Adipocyte nécrosé Acides gras libres Adipocyte nécrosé Adiponectine Insulino-résistance Macrophage Adipocyte Adipocyte Macrophage Dyslipidémie Syndrome métabolique Figure 9 : Comparaison entre les modifications du tissu adipeux lors d’une obésité ou d’une lipoatrophie D’après Villaroya F., Int J Obes (Lond), 2007 II. Les métalloprotéases matricielles Les MMPs font partie de la grande famille des metzincines. Elles sont impliquées dans tous les processus nécessaires au développement et jouent un rôle majeur dans le remodelage tissulaire via la dégradation de la MEC. Ainsi, elles sont associées à différentes pathologies telles que l’arthrite rhumatoïde, les maladies cardiovasculaires et le développement tumoral. Au cours de ce chapitre, nous allons nous intéresser aux MMPs en général, à leur régulation, leur mode d’action et aux principales fonctions biologiques qui leurs sont associées. Enfin, nous aborderons leur rôle dans le TA. A) Classification et structure Les MMPs constituent une famille d’endopeptidases à doigt de zinc comprenant, à ce jour, au moins 24 membres dénommés soit par un nom descriptif, soit par un numéro. En accord avec la spécificité de leur substrat et de leur structure, les membres de la famille des MMPs ont été classés en au moins 5 familles distinctes: les collagénases, les gélatinases, les stromélysines, les matrilysines et les MMPs de type membranaires (MT-MMPs) (Tableau 7). Malgré une certaine spécificité de substrats, les spectres protéolytiques des différentes MMPs sont assez larges et se recouvrent permettant ainsi la dégradation de l’ensemble des composants de la MEC. Dans le tableau 7 se trouvent les différents substrats matriciels des MMPs répertoriés grâce à des études in vitro (37, 254). Il est important de préciser qu’à ce jour, tous les substrats des différentes MMPs ne sont pas encore connus et restent à être déterminés. C’est notamment le cas des MMP-11 et -18. La structure primaire des MMPs contient au minimum trois domaines: un prédomaine, un pro-domaine et un domaine catalytique proprement dit. Le pré-domaine, au niveau N-terminal, correspond à un peptide signal. Il est nécessaire à la sécrétion des MMPs puis est rapidement dégradé. Le pro-domaine maintient l’activité enzymatique sous forme latente et est classiquement constitué d’une séquence peptidique comprenant un résidu cystéine qui interagit avec l’atome de zinc au niveau du domaine catalytique (figure 10). Les MMPs sont donc sécrétées sous forme latente ou zymogène. Pour être actives, le prodomaine doit être éliminé ou modifié par clivage protéolytique, libérant ainsi l’atome de zinc du résidu cystéine et entraînant l’activation du domaine catalytique qui peut alors se lier à son substrat. La plupart des MMPs possèdent en plus un domaine charnière riche en proline et un domaine C-terminal contenant une séquence homologue à de l’hemopexine ou de la 43 vitronectine. Ce dernier domaine intervient dans la reconnaissance du substrat des MMPs. Des particularités de structure sont observées pour certaines MMPs. Les MMP-2 et -9 possèdent, à l’intérieur de leur domaine catalytique, un domaine homologue à la fibronectine qui est responsable de la forte affinité de ces enzymes pour la gélatine et le collagène. Les MT-MMPs possèdent un domaine additionnel qui leur permet l’ancrage à la membrane plasmique (254). Tableau 7: Classification des métalloprotéases matricielles Collagénases Nom MMPs 1 1 2 8 3 13 4 A 18 2 B 9 1 3 2 10 Matrilysines 3 1 11 7 MT-MMPs 2 1 26 14 2 3 4 5 6 15 16 17 24 25 12 Gélatinases Stromélysines Autres 19 20 21 22 23 28 Substrats matriciels Collagènes (I, II, III, VII, VIII et X), gélatine, PG Collagènes (I, II, III, V, VII, VIII et X), gélatine et PG Collagènes (I, II, III, IV, IX, X et XIV), gélatine, PG, FN, laminine, tenascine, ostéonectine, fibrilline ? Gélatine, collagènes (I, IV, V, VII, X, XI, et XIV), élastine, tenascine, fibrilline, laminine, FN, ostéonectine et PG Gélatine, collagènes (IV, V, VII, X, XI et XIV), élastine, fibrilline, FN, laminine, entactine, ostéonectine et PG Collagènes (II, III, IV, V, IX et X), FN, élastine, gélatine, laminine, fibrilline, FN, tenacsine, entactine, ostéonectine et PG Collagènes (II, III, IV, V, IX et X), FN, élastine, gélatine, laminine, caséine et PG ? Collagènes (IV et X), élastine, FN, laminine, tenascine, entactine, ostéonectine, gélatine, caséine et PG Collagène IV, gélatine et FN Collagènes (I, II, III et IV), gélatine, élastine, FN, laminine, vitronectine, perlecan, fibrilline, tenascine, entactine et PG FN, laminine, tenascine, perlecan, entactine et PG Collagène III, FN, gélatine, PG, laminine, caséine Fibrine, fibrinogène PG Collagène IV, FN, fibrine, gélatine Collagène IV, gélatine, FN, laminine, vitronectine, élastine, fibrilline, caséine et PG Gélatine ? ? ? ? ?? (FN: fibronectine ; PG: protéoglycanes) 44 A Structure de base des MMPs MMP-1 MMP-3 MMP-8 MMP-10 MMP-11 MMP-12 MMP-13 MMP-19 MMP-20 MMP-21 MMP-27 MMP-28 MMPs avec un domaine fibronectine MMP-2 MMP-9 MMP liées à la membrane Transmembranaire: MMP-14 MMP-15 MMP-16 MMP-24 Domaine minimum des MMPs MMP-7 MMP-26 Pro-domaine Protéase Ancré au GPI MMP-17 MMP-25 MMP-13 Domaine fibronectine de type II Domaine catalytique Domaine charnière Domaine hémopoxine B Domaine membranaire Figure 10 : Les métalloprotéases matricielles (A) Structure (B) Activation par clivage du pro-domaine D’après Page-McCaw A., Nat Rev Mol Cell Biol, 2007 B) Les régulations des MMPs Pour éviter une protéolyse excessive et des dommages tissulaires, l’activité des MMPs est régulée par de multiples contrôles aussi bien au niveau de leur transcription, traduction et sécrétion que de leur localisation, activation et inhibition (figure 11 et pour revue (254)). Nous aborderons dans ce paragraphe les principales régulations des MMPs. B.1) Les régulations transcriptionnelles et post-transcriptionnelles L’expression des MMPs est normalement faible dans les tissus et est induite lorsqu’un remodelage tissulaire est requis. Une large variété de facteurs solubles incluant des facteurs de croissance et des cytokines tels que les interleukines 1α et β, les interférons α, β, et γ, l’EGF, le FGF, le PDGF, le TGF-β et le TNF-α influent sur l’expression des MMPs. Il en est de même pour les protéines de la MEC notamment les collagènes (290). De plus, des facteurs non solubles tels que les contacts cellule-cellule et cellule-MEC ainsi que la forme de la cellule modulent l’expression des MMPs (183, 254, 290). En effet, il a été observé que des altérations morphologiques de divers types cellulaires entraînent une augmentation de l’expression des collagénases (2) ainsi que l’activation de certaines intégrines (106). L’étude des promoteurs des différentes MMPs a mis en évidence la présence de plusieurs éléments de liaison pour divers facteurs de transcription tels qu’AP1 (activator protein-1), PEA3 (polyoma enhancer A binding protein-3), NF-κB (nuclear factor-κB) et la β-catenin (figure 12) (289, 295). Il est connu qu’AP1 lie les facteurs de transcription c-fos et c-jun et que les sites PEA3 lient ceux de la famille ETS (E26 transformation specific). Le facteur de transcription NF-κB est connu pour être impliqué dans les processus d’inflammation et la β-caténine répond à la voie de signalisation de Wnt (187, 294). Comme on peut l’observer dans la figure 12, plusieurs promoteurs des MMPs sont similaires en terme de composition en éléments de liaison aux facteurs de transcription suggérant que plusieurs MMPs sont co-régulées dans leur expression. Cependant et de manière surprenante, les promoteurs des MMPs appartenant à la même famille telles que les MMP-2/MMP-9 (gélatinases) et les MMP-1/MMP-8 (collagénases) n’ont aucune similitude. Des groupes de promoteurs de MMPs ont pu ainsi être formés en fonction de leur composition en élément de liaison (figure 12 et pour revue (37). Il a ainsi été observé que l’expression des MMP-2, 14 et 28 est majoritairement « constitutive » avec tout de même une induction possible par certains facteurs de croissance ou cytokines (37). 45 2) Traduction 1) mRNA transcription 3) Sécrétion Sécrétion régulée Noyau Sécrétion constitutive Domaine catalytique Prodomaine 4) Localisation Transmembranaire ou GPI liée Associée à la membrane Liaison à la MEC Protéase 5) Activation 7) Dégradation 6) Inhibition α2-macroglobuline TIMP Figure 11 : Régulation de l’activité des métalloprotéases matricielles D’après Page-McCaw A., Nat Rev Mol Cell Biol, 2007 Groupe 1 Groupe 2 MMP-1 MMP-8 MMP-3 MMP-11 MMP-7 MMP-21 MMP-9 Groupe 3 MMP-10 MMP-2 MMP-12 MMP-14 MMP-13 MMP-28 MMP-19 MMP-26 Figure 12 : Eléments de liaison aux facteurs de transcription sur les promoteurs des métalloprotéases matricielles (AP-1: activator protein-1; AP-2 : activator protein-2; C/EBP-β : CCAAT/enhancer binding protein-β ; GC : Sp-1 binding site ; HBS : HIF-binding site ; KRE-M9 : keratinocyte differentiation factor1responsive element-4 ; LBP-1 : leader-binding protein ; NF-1 : nuclear factor-1 ; NF-κB : nuclear factorκB ; OSE-2 : osteoblast-specific element-2 ; p53/AP-2 : p53/AP-2 composite binding site ; PA : polyadenylation signal ; PEA3 : polyoma enhancer A binding protein-3 ; RARE : retinoic acid responsive element ; SBE : STAT-binding element ; Si : silencer sequence ; SPRE : stromelysin-1 PDGF-responsive element ; TATA : TATA box ; Tcf-4 : T-cell factor-4/β-catenin-binding site ; TIE : TGF-β inhibitory element ; TRF : octamer binding protein ; SAF-1 : serum amyloid A activating factor-1. D’après Yan C., J. Cell. Physiol., 2007 Il est important de signaler que la régulation transcriptionnelle des MMPs ne dépend pas uniquement de la présence de site de liaison au niveau de leur promoteur. En effet, des polymorphismes du promoteur et des régulations épigénétiques (i.e, la méthylation de l’ADN ou des altérations de la structure de la chromatine) jouent également un rôle dans l’expression des MMPs. Enfin des régulations post-transcriptionnelles des MMPs sont possibles et correspondent le plus souvent à des processus de stabilisation ou de dégradation des transcrits (pour revue (295)). B.2) Les régulations de la sécrétion Les MMPs sont sécrétées par de nombreux types cellulaires notamment les fibroblastes, neutrophiles, macrophages, cellules épithéliales et endothéliales (290). Certains types cellulaires tels que les macrophages et les neutrophiles, qui ont la capacité de stocker les MMPs dans des granules intracytoplasmiques, régulent la sécrétion des MMPs par les actions de la plasmine ou de la thrombine sur le processus de libération des granules (220). B.3) Les processus de maturation des MMPs Comme il a été précisé un peu plus tôt, l’activation des MMPs dépend de l’élimination ou de la modification de leur pro-domaine par clivage protéolytique. Différents types d’activation des MMPs ont été décrits. En général, l’activation des MMPs se produit à l’extérieur de la cellule. Le tableau 8 présente les principaux activateurs des MMPs (pour revue (37)). La plasmine issue de la dégradation du plasminogène est l’un des activateurs physiologiques majeur des MMPs et de ce fait les activateurs de sa production tels que les activateurs du plasminogène de type urokinase (uPA) ou de type tissulaire (tPA) le sont également (26). Les MMPs elles-mêmes sont capables d’activer d’autres MMPs. De plus, il a été rapporté que d’autres protéases telles que les kallikréines, les cathepsines et les chymases permettaient la maturation des MMPs (67). Les espèces réactives de l’oxygène ont aussi été impliquées dans l’activation des MMPs (217, 287). Les travaux de Pei et Weiss ont démontré pour la première fois que la pro-MMP11 (ou pro-stromélysine 3) était activée à l’intérieur de la cellule avant sa sécrétion. Cette activation se fait par les furines, une famille de sérine protéases (204). Plus tard, il a été montré que cette activation par les furines concerne les MMPs contenant une séquence 46 spécifique (RRKR) dans leur pro-domaine. C’est également le cas pour la MMP-14 (ou MT1-MMP) (37). Tableau 8 : Les activateurs des MMPs Collagénases Gélatinases Stromélysines Matrilysines MT- MMPs Autres MMP Activée par Activateur de 1 MMP-3 et 10, plasmine, kallikréine et chymase MMP-3 et 10 et plasmine MMP-2, 3, 10, 14 et 15 et plasmine ? MMP-1, 7, 13, 14, 15, 16, 17 24 et 25 MMP-2, 3 et 13 et plasmine Plasmine, kallikréine, chymase et tryptase Elastase et cathepsine G Furine MMP-3 et 10 et plasmine ? Plasmine et furine ? ? ? ? ? ? Trypsine ? ? ? ? ? MMP-2 8 13 18 2 9 3 10 11 7 26 14 15 16 17 24 25 12 19 20 21 22 23 28 ? MMP-2 et 9 ? MMP-9 et 13 ? MMP-1, 7, 8, 9 et 13 MMP-1, 7, 8, 9 et 13 ? MMP-2 ? MMP-2 et 13 MMP-2 et 13 MMP-2 MMP-2 MMP-2 MMP-2 ? ? ? ? ? ? ? Un troisième mécanisme d’activation a été décrit au niveau de la surface de la cellule. Il s’agit d’un mécanisme unique de régulation de la gélatinase-A (MMP-2). La forme inactive de cette MMP peut se lier à une MMP transmembranaire, la MT1-MMP, ainsi qu’à une protéine nommée TIMP-2 (tissue inhibitor of matrix metalloproteinases 2) qui agit ici comme une molécule adaptatrice (nous aborderons les TIMPs dans le paragraphe suivant). La formation de ce complexe à trois partenaires au niveau de la surface cellulaire permet à une seconde molécule de MT1-MMP de couper le peptide N-terminal de la pro-MMP-2 et d’activer ainsi la protéase (258). Ici, MT1-MMP joue un double rôle de molécule réceptrice et activatrice. Il faut préciser que les autres MT-MMPs sont également capables d’activer 47 MMP-2 même si la protéolyse par la MT1-MMP reste prédominante (37). En revanche, les activateurs physiologiques de nombreuses MMPs sont encore inconnus (tableau 8). Une fois leur pro-domaine clivé, les MMPs sont protéolytiquement actives mais très rapidement elles peuvent être inactivées par liaison à des protéines inhibitrices. Ces protéines vont se fixer directement au niveau du domaine catalytique empêchant l’accès au substrat. Dans le paragraphe qui suit nous nous intéresserons aux différents inhibiteurs endogènes des MMPs. B.4) Les processus d’inhibition des MMPs In vivo, l’activité des MMPs est contrôlée par les TIMPs (tissue inhibitors of matrix metalloproteinases). A ce jour, quatre TIMPs différents ont été identifiés (TIMP-1 à -4). Ce sont des protéines de petites tailles (20 à 29 kDa), sécrétées mais qui peuvent être retrouvées à la surface cellulaire associées à des protéines liées à la membrane plasmique ou séquestrées au niveau de la MEC. C’est le cas de TIMP-3 qui peut interagir avec des protéoglycanes (298). Les TIMPs sont exprimés par de nombreux types cellulaires incluant les fibroblastes, les cellules épithéliales et endothéliales, les ostéoblastes, les chondroblastes, les cellules du muscle squelettiques ainsi que des cellules cancéreuses. Tandis que l’expression de TIMP-2 est constitutive, celle des TIMP-1, 3 et 4 est inductible. Avec un certain degré de spécificité, les TIMPs sont capables d’inhiber l’activité des MMPs. Ils forment un complexe équimoléculaire avec les formes actives des MMPs où le domaine amino-terminal des TIMPs se lie au domaine catalytique des MMPs et, de ce fait, bloque l’accès à la poche contenant l’atome de zinc. Cette inhibition est réversible. Les TIMPs ont aussi la capacité d’inhiber d’autres protéases telles que les ADAMs (A Disintegrine And Metalloprotease domain) (141). La régulation des MMPs par les TIMPs est un facteur majeur dans le contrôle de la dégradation de la MEC. Elles jouent également un rôle dans le contrôle de nombreux processus cellulaires tels que la prolifération mais aussi l’apoptose et des événements physiologiques tels que l’angiogenèse et pathophysiologiques tels que le développement tumoral (41). Toutefois, de plus en plus d’évidences indiquent que certaines de ces fonctions semblent être complètement indépendantes des MMPs. Par exemple, récemment, il a été rapporté que TIMP-2 et 3 pouvaient lier l’intégrine α3 β1 et entraîner une cascade de signalisation négative conduisant à un arrêt du cycle cellulaire des cellules endothéliales (243). De la même manière, TIMP-3 est capable d’interagir avec le récepteur 2 du VEGF empêchant ainsi l’accès à son substrat et entraînant une inhibition de l’angiogenèse (216). 48 Ces effets étant retrouvés quand les TIMPs sont mutés au niveau de leur domaine nécessaire pour l’inhibition des MMPs, il est donc fortement suggéré que les TIMPs pourraient exercer des fonctions indépendamment de leurs effets sur les MMPs. L’α2-macroglobuline, une protéine de 722 KDa, peut également inhiber l’activité des MMPs (251). Trouvée en abondance dans le plasma, elle serait, de ce fait, l’inhibiteur endogène majeur des MMPs dans les liquides physiologiques alors que les TIMPs agiraient plus localement dans l’espace extra- et péri-cellulaire. D’autres protéines ont été rapportées pour inhiber certaines MMPs. C’est le cas de la protéine RECK (Reversion-inducing cysteine-rich protein with kazal motifs), une glycoprotéine GPI-ancrée qui inhibe les MMP-2, -9 et -14, et bloque l’angiogenèse (193). Une déficience de cette protéine chez des souris est létale suggérant des fonctions importantes de RECK dans le développement. Enfin, un certain nombre de protéines contenant des séquences similaires au TIMPs peuvent inhiber les MMPs. Ce sont les « TIMPlike molecules » qui incluent notamment les neltrines, les protéines frizzled, la PCPE (type 1 collagen C-proteinase enhancer protein) et le TFPI-2 (tissue factor pathway inhibitor 2) (pour revue (8)). Ainsi, l’activité des MMPs dans l’espace extracellulaire dépend de l’équilibre entre leur inhibition et leur activation. C’est cet équilibre qui régule le renouvellement de la MEC et le remodelage tissulaire durant les processus de développement normal ou pathologique. Voyons à présent les différents modes d’action des MMPs. C) Mode d’action des MMPs La MEC est un réseau dynamique de protéines incluant du collagène, de la fibronectine, de la laminine et des protéoglycanes qui forme une barrière structurale. La dégradation de la MEC a été longtemps considérée comme un simple remodelage de cette barrière structurale. Depuis, des études ont montré que la MEC n’était pas juste une structure passive. Elle peut influencer le comportement des cellules et notamment leur détermination et leur différenciation (257). Jusqu'à récemment, on pensait que les MMPs participaient à ces processus via leurs effets sur la MEC mais il est maintenant clair que les MMPs ont d’autres mécanismes d’action (figure 13 et pour revue (178)). Il a ainsi été rapporté que la dégradation des composants de la MEC par les MMPs peut générer des fragments matriciels 49 Interactions cellule-cellule Interactions cellule-matrice Récepteurs et autres protéines de surface Facteurs de croissance, facteurs angiogéniques, chémoattractants et inhibiteurs Fragments matriciels actifs Protéines de liaison et autres protéines solubles Figure 13 : Mode d’action des métalloprotéases matricielles D’après Sternlicht and Werb, Annu Rev Cell Dev Bio, 2001 biologiquement actifs tels que l’endostatine (fragment du collagène XVIII) (77), l’angiostatine (fragment du plasminogène) (195), des fragments de laminine et certains peptides dérivés de la fibronectine (178). La MEC est également un réservoir de facteurs de croissance et de cytokines qui sont libérés lors de la dégradation matricielle. C’est notamment le cas du TGF-β lors de la dégradation de la décorine par les MMP-2, -3 ou -7 (108). En plus de leur capacité à dégrader l’ensemble des composants de la MEC, les MMPs peuvent également cliver de nombreuses protéines cellulaires de surface, péri-cellulaires ou circulantes. Ainsi, les MMPs peuvent activer la forme pro-TGF-β et pro-TNF-α ou cliver les IGFBPs (insulin-like growth factor binding protein) et par conséquent augmenter la biodisponibilité de l’IGF (80). De plus, le changement de l’environnement cellulaire peut indirectement moduler des voies dépendantes des protéines d’ancrages telles que celles des intégrines. Enfin des études récentes suggèrent que certaines MMPs (MMP-2, -3, -11 et -14) pourraient avoir également des cibles intracellulaires telles que PARP (poly ADP-ribose polymérase, une enzyme de réparation à l’ADN (88, 134, 156, 248). Ces nouvelles données rendent le champ d’action des MMPs encore plus large qu’il ne l’était. D) Les fonctions biologiques et pathologiques des MMPs Comme nous l’avons déjà évoqué, la MEC joue un rôle prépondérant dans le comportement cellulaire (257). Il n’est donc pas surprenant que les principaux acteurs de son remodelage aient un rôle tout aussi important. Au niveau cellulaire, ces enzymes jouent un rôle majeur dans la migration cellulaire, la prolifération, l’apoptose et la différenciation de nombreux types cellulaires notamment les neurones, les chondrocytes, les ostéoblastes et les adipocytes (dont nous parlerons un peu plus tard) (pour revue (162)). Récemment, des études ont également suggéré un rôle des MMPs dans le devenir des cellules souches mésenchymateuses (159). En effet des travaux indiquent que la composition et la rigidité de la MEC modulent l’orientation des cellules souches mésenchymateuses vers différents lignages (69) par des modifications des adhésions focales. De par leurs fonctions au niveau cellulaire, les MMPs régulent plusieurs processus du développement incluant la morphogenèse, l’angiogenèse, la cicatrisation, la menstruation et le développement mammaire et osseux (pour revue (280). Des approches de transgenèse ont permis d’étudier les fonctions biologiques des MMPs dans le développement. A ce jour, 16 modèles de souris déficientes pour les MMPs ont été développés. Toutes les souris déficientes pour les MMPs sont viables avec cependant des différences notoires sur les 50 phénotypes des animaux qui sont présentés dans le tableau 9 (199). Le fait que ces souris soient viables, malgré l’importance des MMPs dans le développement, suggère de forts mécanismes de compensation vis-à-vis d’autres MMPs. Tableau 9: Phénotypes des souris déficientes pour les MMPs Géne invalidé MMP-2 MMP-3 MMP-7 MMP-8 MMP-9 MMP-10 MMP-11 MMP-12 MMP-13 MMP-14 MMP-19 MMP-20 MMP-23 MMP-24 MMP-28 Phénotype des animaux Diminution de la taille corporelle, réduction de la néovascularisation, diminution de l’invasion primaire du conduit de la glande mammaire ; réduction du développement pulmonaire Altération de la structure des jonctions neuromusculaires, altération de la morphogenèse de la glande mammaire Défaut de l’immunité innée, diminution de la re-épithélialisation après une blessure du poumon Augmentation des tumeurs de la peau, résistance aux hépatites létales induites par le TNFα Défauts du développement osseux, défaut de la re-myélinisation neuronale après une blessure nerveuse, retard de la cicatrisation des fractures osseuses, altération du remodelage vasculaire, altération de l’angiogenèse Augmentation de l’inflammation et de la mortalité en réponse à une infection ou une blessure Retard de la tumorigenèse mammaire Diminution de la récupération d’une compression de la moelle épinière, augmentation de l’angiogenèse due à une diminution de l’angiostatine Défaut du remodelage osseux, réduction des fibroses hépatiques, augmentation de l’accumulation du collagène dans les plaques d’athérosclérose Défaut du remodelage squelettique, défaut de l’angiogenèse, inhibition de l’éruption dentaire et de l’élongation des racines, défauts au niveau des poumons et des glandes submandibullaires Obésité Défaut de l’émail dentaire Pas de phénotype rapporté Réponse anormale à une blessure du nerf sciatique Augmentation de la réponse inflammatoire D’après Page-McCaw A., Nat Rev Mol Cell Biol, 2007 En plus de ces données sur les principales fonctions des MMPs, il est important de préciser la complexité des MMPs, en terme d’activité biologique. En effet, certaines d’entre elles sont paradoxales, puisqu’une MMP peut avoir des effets diamétralement opposés. Par exemple, il est connu que les MMP-2 et -9 favorisent l’angiogenèse mais des effets antiangiogéniques leurs sont également attribués (pour revue (232)). Il en est de même pour les 51 processus apoptotiques puisque les MMP-2, -3, -7 et -9 peuvent être pro- et anti-apoptotiques (pour revue (160)). Du fait de leurs fonctions biologiques, les MMPs ont été associées à diverses pathologies. Ce sont des modulateurs importants de l’inflammation (pour revue (203)) et elles sont fortement augmentées dans toutes les pathologies associées à une inflammation notamment l’arthrite rhumatoïde. A ce jour, un inhibiteur des MMPs, le périostat, est utilisé pour le traitement de la parodontite, une inflammation des tissus de soutien qui relient la dent au maxillaire. Des dérégulations des MMPs ont également été impliquées dans diverses pathologies cardiovasculaires telles que l’athérosclérose et l’infarctus du myocarde (85, 253). Enfin, l’importance des MMPs dans la progression du cancer n’est plus à démontrer (60). Leur expression est fortement augmentée dans de nombreux cancers. Elles interviennent dans toutes les phases du cancer c’est-à-dire de la croissance tumorale, l’invasion, l’extravasation dans des sites plus éloignés ainsi que dans l’effet angiogénique requis pour nourrir la formation de la nouvelle tumeur. Ainsi, les MMPs sont devenues la première cible pour les programmes de découverte de nouveaux médicaments à but anti-cancéreux. De nombreux inhibiteurs des MMPs ont été développés (tableau 10). Malgré un début très prometteur, la survenue d’effets indésirables au cours des phases de développement clinique et le peu de bénéfice par rapport aux effets indésirables a conduit à l’arrêt de nombreux d’entre eux. A l’heure actuelle, d’autres inhibiteurs plus spécifiques sont en cours de développement (pour revue (161). 52 Tableau 10: Les inhibiteurs des MMPs dans le cancer Inhibiteurs Spécificité MMPs Collagènes synthétiques peptidomimétiques Batimastat Large spectre des (BB-94) MMPs et ADAM-17 Solimastat Large spectre (BB-3643) Marimastat MMP-1, -2, -3, -7, -9 (BB-2516) et -12 Collagènes synthétiques non peptidiques Prinomastat (AG3340) MMP-1, -2, -3, -7, -9 et -14 Tanomastat (BAY 12-9566) MMP-2, -3, -9 et -13 D2163 MMP-1, -2 et -9 Effets indésirables Péritonite Courbatures musculosquelettiques Douleur musculaire et articulaire (Légère à sévère) Arthralgie et affection associée aux articulations Légère douleur articulaire, élévation des enzymes hépatiques, nausée et thrombocytopénie ? Phase clinique Arrêt en phase II Arrêt en phase II Arrêt en phase III Arrêt en phase II Arrêt en phase III En phase II et III Tétracycline modifiée Métastat (Col-3) MMP-1, -2, -8, -9 et -13 Toxicité systémique limitée, légère Utilisé dans phototoxicité, anémie le sarcome sidéroblastique réversible de Kaposi Biphosphonate synthétique Alendronate MMP-2 ? En Phase I Néovastat (AE-941) MMP-2, -9, -12 et -13 En Phase III Catéchines MMP-2 et -9 Douleur musculosquelettiques et raideur articulaire Toxicité légère à modérée, effets neurologiques et gastrointestinaux Acide acétylsalicylique MMP-2 Composés naturels ? D’après Mannello F., Curr. Cancer Drug Targets, 2005 53 En Phase I En cours d’étude III. Les métalloporotéases matricielles dans le tissu adipeux L’intérêt des MMPs dans le remodelage du TA est très récent et la majorité des études ont été effectuées chez le rongeur. In vivo, dans des modèles de souris génétiquement obèses (ob/ob et db/db) ou rendues obèses à l’aide d’un régime hyperlipidique, des variations d’expression de différentes MMPs dans le TA ont été observées. On peut noter une augmentation des MMP-2, -3, -11, -12, -13, -14, -19 et une diminution des MMP-7, -9, -16 et -24 (38, 149, 164). De plus, un traitement au galardin, un inhibiteur des MMPs à large spectre, limite le développement du TA de ces animaux (148). Ces premières données suggèrent un rôle primordial du remodelage matriciel dans le développement de la masse grasse. A) La régulation de l’adipogenèse In vitro, des travaux menés par notre équipe et celle de Croissandeau, indiquent que des préadipocytes murins des lignées 3T3F442A (17) et 3T3L1 (53) produisent au cours de leur différenciation adipocytaire deux MMPs appartenant à la famille des gélatinases : MMP2 et -9. Par ailleurs, l’inhibition de la différenciation adipocytaire est également observée dans ces préadipocytes murins traités par des inhibiteurs des MMPs à large spectre (batimastat et illomastat) ou des anticorps neutralisants dirigés contre les MMP-2 ou -9 suggérant un rôle majeur de ces deux MMPs dans l’adipogenèse chez les rongeurs (17, 53). Récemment, la MT1-MMP a été identifiée comme importante dans le développement de la masse grasse. En effet, les travaux de Chun et al. montrent que des souris déficientes pour la MT1-MMP présentent un phénotype lipodystrophique (44). In vitro et de manière surprenante, les préadipocytes issus de ces souris sont doués d’une adipogenèse normale dans un modèle de culture classique en 2 dimensions. Cependant, lorsque ces préadipocytes sont cultivés sur un support en 3 dimensions, leur adipogenèse est inhibée. Les auteurs démontrent qu’in vivo les précurseurs adipocytaires sont entourés d’un riche réseau de fibres de collagène de type 1. Ce réseau est profondément modifié notamment par la MT1-MMP en début de différenciation. Ce remodelage modifie les contraintes physiques que fait subir la matrice de collagène au cytosquelette des préadipocytes et induit des cascades de signalisation pour la poursuite de la différenciation adipocytaire. En l’absence de MT1-MMP, le réseau de collagène reste très dense, les contraintes du cytosquelette ne sont pas modifiées et le 54 programme de différenciation ne peut pas continuer. La MT1-MMP serait un facteur adipogénique qui permet la croissance de l’organe adipeux en 3 dimensions. De façon intéressante, trois autres MMPs, MMP-3 et -11 appartenant à la famille des stromélysines (Stro1 et Stro-3 respectivement) et MMP-19, ont été décrites comme ayant des effets inhibiteurs sur le développement du TA et sur l’adipogenèse. In vivo, des souris transgéniques mutées pour la MMP-3 ont une adipogenèse au niveau de la glande mammaire accélérée et une hypertrophie adipocytaire (3) et des souris déficientes pour les MMP-3, -11 et -19 soumises à un régime gras développent plus de TA que des souris contrôles (150, 163, 205). In vitro, Alexander et al. rapportent que la MMP-3 augmente au cours de la différenciation des préadipocytes murins de la lignée 3T3 L1 et qu’un traitement avec des inhibiteurs des MMPs (GM6001 et TIMP-1) accélère l’accumulation des lipides (3). Ces données sont à l’opposé de celles obtenues par l’équipe de Croissandeau sur le même type cellulaire. La spécificité et la sélectivité des inhibiteurs des MMPs utilisés pourraient expliquer ces différences. Enfin, en plus de leur rôle majeur dans la différenciation adipocytaire, il a récemment été suggéré une implication des MMPs dans la détermination des cellules précurseurs vers le lignage adipocytaire. En effet, les travaux d’Otto et al, indiquent qu’un traitement au BMP-4 entraîne une diminution des MMP-3 et -13 associée à l’engagement des cellules C3H10T1/2 vers le lignage adipogénique (197). B) La régulation de l’angiogenèse A ce jour, il existe peu de données concernant les MMPs et la régulation de l’angiogenèse dans le TA. Toutefois, il a récemment été rapporté in vivo chez des rongeurs que des macrophages positifs pour LYVE-1 (lymphatic vessel endothelial hyaluronan receptor 1) et originaire de la moelle osseuse, induisent une angiogenèse notamment à travers la sécrétion des MMP-9, -12 et -7 (42). C) La régulation de l’infiltration macrophagique La MMP-12 est requise pour la dégradation de la MEC par les macrophages et l’invasion tissulaire (246). De plus, cette MMP est fortement augmentée chez des souris obèses (38, 164). Les travaux de Huber et al. montrent que la MMP-12 est exprimée et produite par les macrophages et les adipocytes matures suggérant que ces deux types 55 cellulaires contribuent à la production de MMP-12 dans le TA de sujets obèses. Ainsi, les auteurs suggèrent que la production de MMP-12 pourrait favoriser l’infiltration macrophagique mais aussi faciliter la croissance des adipocytes durant le développement de la masse grasse (104). Toutefois cette hypothèse reste encore à démontrer. Récemment, les travaux de Cho et al. montrent qu’un traitement avec un inhibiteur de l’activité des MMPs, l’acide zoledronique, diminue le recrutement et l’infiltration des macrophages positifs pour LYVE-1. Ces macrophages exprimant principalement les MMP-7, -9 et -12, l’implication de l’activité de ces MMPs dans l’infiltration macrophagique est suggérée (42). Chez l’homme, les études concernant les MMPs dans le TA sont peu nombreuses. Notre équipe a rapporté que des préadipocytes humains en culture primaire produisent et sécrètent les MMP-2 et -9 au cours de leur différenciation. Sachant qu’il existe de grandes différences entre les modèles humains et murins, la confirmation de l’implication des MMPs dans l’adipogenèse chez l’homme est nécessaire et a fait l’objet d’une partie de notre étude. De plus, de manière intéressante, une augmentation de la MMP-9 plasmatique a été associée à l’obésité (86) et sa diminution à une perte de poids (140) suggérant un rôle clé de cette protéase dans le remodelage du TA humain. D) Les régulateurs des MMPs dans le tissu adipeux Des travaux ont impliqués TIMP-1 et -3 dans le développement de la masse grasse chez la souris. Les travaux de Fata et al. sur l’involution de la glande mammaire dans des souris déficientes pour TIMP-3 montrent une reconstitution adipocytaire accélérée durant le remplacement des cellules épithéliales de la glande mammaire par la formation du TA (76). Toutefois, un effet de TIMP-3 sur les autres dépôts de TA de ces souris n’est pas décrit. Les travaux de Lijnen et al. indiquent que des souris déficientes pour TIMP-1 sont protégées d’une obésité induite par un régime gras (147). De plus, une augmentation de l’adipogenèse du TA mammaire est observée in vivo chez des souris surexprimant TIMP-1 et l’addition d’une protéine recombinante TIMP-1 accélère la différenciation des préadipocytes de la lignée 3T3L1 in vitro (3). Toutefois, les travaux de Demeulemeester et al. ne sont pas en accord avec ces résultats et indiquent qu’une surexpression de TIMP-1 par un adénovirus n’affecte pas le développement du TA des souris, in vivo et in vitro, et n’affecte pas l’adipogenèse des préadipocytes de la lignée 3T3F442A (59). Concernant l’expression et la sécrétion de TIMP-1, une augmentation de l’expression de TIMP-1 chez des souris 56 génétiquement obèses ou soumises à un régime gras a été décrite (38, 164) et au cours de l’adipogenèse in vitro les résultats ne sont pas très clairs puisque des études indiquent qu’au cours de la différenciation des préadipocytes de la lignée 3T3F442A, l’expression de TIMP-1 augmente (164), et d’autres, notamment notre groupe, que son expression et sa sécrétion diminuent (17, 116). Chez l’homme, les taux plasmatiques de TIMP-1 sont corrélés avec le pourcentage de la masse grasse mais pas à l’IMC ni au tour de taille (131). Des travaux complémentaires seraient nécessaires pour mieux comprendre le rôle précis des TIMPs dans le TA, notamment chez l’homme, et si leurs effets sont directement liés aux MMPs ou indépendants. En plus des TIMPs, d’autres régulateurs des MMPs tels que le système plasminogène/plasmine jouent un rôle majeur dans le remodelage du TA. Toutefois, ce dernier a déjà fait l’objet de nombreuses études et ne sera pas abordé ici. Pour conclure, les MMPs sont nécessaires à tous les processus du développement de l’organisme. Elles constituent une grande famille de protéases dont l’activité est régulée à de multiples niveaux. Il est clairement admis que les substrats des MMPs peuvent être des composants matriciels ou des facteurs solubles cellulaires rendant ainsi le champ d’action des MMPs très vaste. Elles sont considérées comme des protéases majeures dans le remodelage tissulaire. Cependant, quelques études seulement se sont intéressées à l’implication des MMPs dans le remodelage du TA et aucune étude n’a encore démontré un rôle de ces protéases dans le TA humain. 57 Objectifs Comme nous l’avons déjà évoqué, le TA est soumis à des processus de développement excessif (obésité) mais aussi de régression (lipoatrophie). Il est admis que cette plasticité du TA n’est possible que grâce à un remodelage cellulaire et matriciel. Les MMPs, comme nous venons de le voir, sont des acteurs majeurs du remodelage tissulaire. Quelques études ont montré l’importance des MMPs dans la différenciation adipocytaire des préadipocytes de lignées murines. De plus, les inhibiteurs de la protéase du VIH, décrits comme associés à l’émergence du syndrome de lipodystrophie, sont également associés à une inhibition de l’adipogenèse chez les rongeurs. Les effets anti-adipogéniques observés avec les inhibiteurs de protéases matricielles et de protéases du VIH nous ont conduit à émettre l’hypothèse d’un lien entre les IPs-VIH et les MMPs. L’influence de ces protéases dans l’adipogenèse chez l’homme reste cependant à être déterminée. Dans la première partie de ce travail de thèse, nous nous sommes intéressés à l’implication des MMPs dans la différenciation des cellules issues de la fraction stromavasculaire (FSV) du TA humain en culture primaire. L’effet des IPs-VIH sur la différenciation de ces cellules en culture primaire a également été étudié ainsi qu’un lien potentiel entre les IPs-VIH et les MMPs. Nous avons ainsi observé que les IPs-VIH affectent l’expression génique de la MMP-9. Peu de données étant connues quant à la régulation génique de la MMP-9 et aux cibles potentielles des IPs-VIH, les mécanismes moléculaires responsables de la diminution de l’expression de MMP-9 par les IPs-VIH ont été déterminés. Dans une deuxième partie de ce travail, sachant que la FSV est formée de plusieurs populations cellulaires telles que les cellules progénitrices aux capacités adipogéniques et angiogéniques (241), les cellules endothéliales capillaires et les cellules immunoinflammatoires, nous avons voulu confirmer l’influence de MMP-9 sur l’adipogénèse des cellules progénitrices isolées. Puis, afin de déterminer les mécanismes qui contrôlent le devenir des cellules progénitrices, une condition de culture permettant l’étude simultanée de leurs capacités adipogéniques et angiogéniques a été mise au point. 58 Résultats I) Implication des MMPs dans la différentiation adipocytaire des cellules de la fraction stroma-vasculaire du tissu adipeux humain Un rôle primordial des MMPs et du remodelage matriciel dans le développement du TA est maintenant suggéré (38, 148, 149, 164). En effet, des travaux menés par notre équipe et celle de Croissandeau, indiquent que des préadipocytes murins produisent les MMP-2 et -9 (17, 53). De plus, un traitement par des inhibiteurs des MMPs à large spectre (batimastat et illomastat) ou des anticorps neutralisants dirigés contre les MMP-2 ou -9 limitent l’adipogenèse suggérant un rôle majeur de ces 2 MMPs dans l’adipogenèse des préadipocytes murins (17, 53). Toutefois, chez l’humain, les données concernant les MMPs dans le TA sont peu nombreuses. Des travaux menés par notre équipe ont mis en évidence que des cellules issues de la FSV du TA humain en culture primaire sécrètent les MMP-2 et -9 au cours de leur différenciation adipocytaire. Dans la publication 1, nous avons donc cherché à déterminer l’implication de ces MMPs dans l’adipogenèse chez l’homme. En parallèle, nous avons également voulu confirmer l’effet anti-adipogénique des IPs-VIH chez l’homme. En effet, si de nombreuses études ont mis en évidence un effet inhibiteur des IP-VIHs sur la différenciation de préadipocytes murins (64, 144, 176, 300), deux études seulement ont été réalisées sur des cellules souches mésenchymateuses humaines et sur des préadipocytes humains d’origine mammaire (109, 288). Enfin, un lien potentiel entre les MMPs et les IPs-VIH a été recherché. A) Influence d’un inhibiteur des MMPs et des inhibiteurs de la protéase du VIH sur la différenciation adipocytaire Publication 1 : Protease inhibitor treatments reveal specific involvement of matrix metalloproteinase-9 in human preadipocyte differentiation. V. Bourlier, A. Zakaroff-Girard, S. De Barros, C. Pizzacalla, V. Durand de Saint Front, M. Lafontan, A. Bouloumié and J. Galitzky. J Pharmacol Exp Ther, 312:1272-1279, 2005 59 0022-3565/05/3123-1272–1279$20.00 THE JOURNAL OF PHARMACOLOGY AND EXPERIMENTAL THERAPEUTICS Copyright © 2005 by The American Society for Pharmacology and Experimental Therapeutics JPET 312:1272–1279, 2005 Vol. 312, No. 3 77263/1194036 Printed in U.S.A. Protease Inhibitor Treatments Reveal Specific Involvement of Matrix Metalloproteinase-9 in Human Adipocyte Differentiation Virginie Bourlier, Alexia Zakaroff-Girard, Sandra De Barros, Christophe Pizzacalla, Véronique Durand de Saint Front, Max Lafontan, Anne Bouloumié, and Jean Galitzky Unité de Recherche sur les Obésités, Institut National de la Santé et de la Recherche Médicale, Institut Louis Bugnard, Hôpital Rangueil, Université Paul Sabatier, Toulouse, France (V.B., A.Z.-G., S.D.B., C.P., V.D.d.S.F., M.L., J.G.); and Institut für Kardiovaskuläre Physiologie, Frankfurt/Main, Germany (A.B.) Received September 6, 2004; accepted November 9, 2004 ABSTRACT We previously showed that human and murine 3T3-F442A preadipocytes produced and released matrix metalloproteinases (MMPs) 2 and 9 and that a treatment by MMP inhibitors resulted in the blockade of murine fat cell adipose conversion. In parallel, investigators reported that other protease inhibitors, the human immunodeficiency virus (HIV) protease inhibitors (PIs) involved in lipodystrophy in humans, also reduced the adipocyte differentiation process of several murine cell lines. The present work was performed to define the effects of MMP inhibitors and HIV-PIs on the human adipocyte differentiation process, to clarify the involvement of MMPs in the control of human adipogenesis, and to determine whether HIV-PIs interact with MMPs in the control of this process. The effect of two MMP inhibitor and four HIV-PI treatments on the differentiation The mechanisms responsible for the growth of adipose tissue (AT) are still not well defined. Adipocyte hypertrophy and hyperplasia, due to the recruitment and differentiation of adipocyte precursor cells, or preadipocytes, into adipocytes are major cellular events in the development of the fat mass. Together with the hypertrophy and the hyperplasia events, recent investigations have clearly demonstrated that angiogenesis and extracellular matrix (ECM) remodeling are required for coordinated growth of the fat depot (Lijnen et al., 2002; Rupnick et al., 2002). Among the enzymes involved in the degradation of the ECM components, the matrix metalloproteinase (MMP) family is considered to play a major role (Sternlicht and Werb, 2001). In a previous report, we demonstrated that mature human adipocytes and preadipocytes This work was supported by Grants 01 128 and 02 197 from the Agence Nationale de Recherche sur le SIDA. Article, publication date, and citation information can be found at http://jpet.aspetjournals.org. doi:10.1124/jpet.104.077263. of primary culture human preadipocytes, as well as the putative relationships between HIV-PIs and MMP-2 and -9 expression, release, or activity were investigated. We showed that MMP inhibitors and HIV-PIs reduced the human adipocyte differentiation process as assessed by the decrease of cell protein and/or triglyceride contents and expression of fatty acid binding protein and hormone-sensitive lipase, two adipocyte markers. Unlike MMP inhibitors, HIV-PIs were devoid of any effect per se on recombinant MMP-2 and 9 activities but reduced the expression and release of MMP-9 by human preadipocytes. Thus, the present study indicates that the modulation of the extracellular matrix components through the production and/or activity of MMPs, and, more precisely, MMP-9 might be a key factor in the regulation of human adipose tissue development. produce and release two members of the MMP family, MMP-2 and -9, the expression and activity of which were shown to be dependent on the adipocyte differentiation process (Bouloumié et al., 2001). Interestingly, we also reported that treatment of the murine 3T3-F442A preadipocytes, which also produced MMP-2 and -9 during adipose conversion, with MMP inhibitors decreased the rate of adipocyte differentiation, suggesting that MMP activities are required for adipogenesis in rodents. However, no data are available concerning the potential role of MMPs in the regulation of AT development in humans. A lipodystrophy syndrome, characterized by body fat redistribution, hyperlipidemia, and insulin resistance, has been associated with the recent use of protease inhibitors (PIs) in the therapy of AIDS as consequence of human immunodeficiency virus (HIV) infection (Carr et al., 1998). The most prominent clinical sign of HIV-PI-associated lipodystrophy is a loss of subcutaneous fat (lipoatrophy) in the face and the extremities that can be accompanied, in some cases, by fat ABBREVIATIONS: AT, adipose tissue; ECM, extracellular matrix; MMP, matrix metalloproteinase; PI, protease inhibitor; HIV, human immunodeficiency virus; IDV, indinavir; RTV, ritonavir; SQV, saquinavir; NFV, nelfinavir; RT-PCR, reverse transcriptase-polymerase chain reaction; HSL, hormone-sensitive lipase; aP2, fatty acid binding protein; NF-B, nuclear factor-B; IL, interleukin. 1272 MMP-9 Involvement in Human Adipocyte Differentiation accumulation in the neck, back, and visceral depots, suggesting that it most likely involves HIV-PI-mediated dysregulation of the balance between the development and the regression of the AT depending on the anatomical location of the fat deposits. Numerous studies have examined the effect of HIVPIs on adipocyte differentiation of murine cell lines and evidenced that they are potent inhibitors of adipogenesis in vitro (Zhang et al., 1999; Vernochet et al., 2003). Further analysis of the putative targets of HIV-PIs has focused on the transcription factors that regulate the expression of adipocytespecific markers (Dowell et al., 2000; Caron et al., 2001). The present work was performed to define the effects of MMP inhibitors and HIV-PIs on the differentiation of preadipocytes isolated from the stroma vascular fraction of human AT. It was also expected to clarify the involvement of MMPs in the control of the adipocyte differentiation process in human AT and to determine whether HIV-PIs interact with MMPs in the control of this process. We evidenced that the broad-spectrum MMP inhibitor batimastat strongly inhibited human adipocyte differentiation. Moreover, HIV-PIs such as indinavir (IDV), ritonavir (RTV), saquinavir (SQV), and nelfinavir (NFV) also lead to a strong reduction of the human adipocyte differentiation process by a mechanism that may involve their inhibitory effect on MMP-9 expression and release by treated preadipocytes. Finally, we showed that MMP-9 inhibitor also reduced the differentiation of human preadipocytes, suggesting that MMP-9 is specifically involved in the batimastat-mediated inhibition of human adipogenesis. These data suggest that the modulation of the ECM components through the production and/or activity of MMPs and, more precisely, MMP-9 might be a key regulator of human AT development. Materials and Methods Cell Culture and Treatment. Chemicals were from Sigma-Aldrich (Saint-Quentin Fallavier, France), and cell culture reagents were from Invitrogen (Cergy Pontoise, France), Roche Diagnostics (Meylan, France), or Cambrex Bio Science (Verviers, Belgium). Human subcutaneous abdominal white AT was obtained from moderately overweight women undergoing plastic surgery (mean age 39 ⫾ 2 years, mean body mass index 26.5 ⫾ 0.8 kg/m2). The isolation of human AT-derived stromal cells and the culture of stromal preadipocytes (i.e., fat cell precursors) differentiated into adipocytes were performed as previously described (10). Briefly, sterile AT was cut into small pieces and digested under agitation with collagenase (300 U/ml) for 1 h 30 min at 37°C. After centrifugation, washing, and filtration steps, the stromal cells were suspended in Dulbecco’s Modified Eagle’s medium F-12 supplemented with 10% fetal calf serum and plated at 60,000 cells/cm2. After 24 h, the medium was changed for medium consisting of Dulbecco’s Modified Eagle’s medium F-12 supplemented with 33 M biotin, 17 M pantothenate, and 50 g/ml gentamycin (basal medium) in the presence of 66 nM insulin, 1 nM triiodothyronine, 100 nM cortisol, 10 g/ml human transferrin (adipogenic medium), and, for the first 3 days, 1 g/ml ciglitazone. After the 3-day priming period, the cells were cultured in the adipogenic medium supplemented with 1) the MMP inhibitor batimastat [BB94 or [4-(N-hydroxyamino)-2R-isobutyl-3S-(thienylthiomethyl)-succinyl]-L-phenylalanine-N-methylamide, kindly provided by British Biotech, Oxford, UK] or MMP-9 inhibitor [MMP-9/MMP-13 inhibitor II or N-hydroxy-1-(4-methoxyphenyl)sulfonyl-4-benzyloxycarbonylpiperazine-2-carboxamide from Calbiochem, VWR International, Strasbourg, France]; or 2) HIV-PIs IDV (kindly provided by Merck, Whitehouse Station, NJ), SQV (kindly provided by Roche, Welwyn Garden City, UK), RTV (kindly provided by Abbott Diagnostics, 1273 Abbott Park, IL), or NFV (kindly provided by Roche Diagnostics) for 10 days. Batimastat was dissolved in ethanol, whereas HIV-PIs and MMP-9 inhibitor were dissolved in pure dimethylsulfoxide. Control cells were treated using an appropriate concentration of each vehicle. Medium was replaced every 2 days. Before the experiments, the cells were placed in basal medium with or without 0.1% bovine serum albumin (MMP inhibitors versus HIV-PIs, respectively) overnight, supplemented with the various treatments. The medium was then collected and used in zymography analysis. Cell triglyceride and total protein contents were determined using kits from Sigma-Aldrich and Bio-Rad S.A (Marnes-la-Coquette, France), respectively. Gelatin Zymography. Proteins with gelatinolytic activity were identified by electrophoresis in the presence of SDS in 8% polyacrylamide gels containing 1 mg/ml gelatin. Briefly, culture medium batches (20 l) were directly loaded onto gels; after electrophoresis, proteins were renatured by exchanging SDS with 2.5% Triton X-100 (20-min incubation repeated twice). The gels were then incubated for 16 h at 37°C in 50 mM Tris-HCl, pH 8.8, 5 mM CaCl2, and 0.02% NaN3 and stained with Coomassie Blue. The presence of gelatinolytic activity in the culture medium batches was visualized as uncolored areas on an otherwise blue gel. Migration of proteins was compared with that of prestained molecular weight markers. The gels were scanned by an imaging densitometer and quantified using the NIH image program (developed at the U.S. National Institutes of Health). Fluorometric Activity Assay on Recombinant MMP-2 and -9. In vitro assays were performed on 96-well plates. Human recombinant activated MMP-2 (2 nM) or MMP-9 (4 nM) (Calbiochem) were preincubated in the presence or absence of increasing concentrations of batimastat (from 0.01 nM to 0.01 M) or HIV-PIs (from 1 nM to 100 M) for 30 min at 37°C. Twenty micromolar of the fluorogenic substrate Mca-Pro-Leu-Gly-Leu-Dnp-Ala-Arg (Bachem, Bubendorf, Switzerland) were then added to each well, and fluorescence (excitation, 325 nm; emission, 390 nm) was recorded every 2 min for 60 min. MMP activity was evaluated by the maximum rate per minute on five separate measurements in each well. Real-Time Reverse Transcriptase-Polymerase Chain Reaction (RT-PCR). Changes in mRNA levels from specific genes were quantified by real-time RT-PCR. Total RNAs were extracted using Qiagen Rneasy Mini Kit according to the manufacturer’s instructions, and RNA concentrations were determined using a fluorometric assay (Ribogreen; Molecular Probes, Eugene, OR). RNA (0.5 g) was reverse-transcribed using the ThermoScript RT system (Invitrogen) according to the manufacturer’s instructions. Reverse transcription was also performed without Thermoscript enzyme on RNA samples to check for any genomic DNA contamination. PCR primers were designed using Primer Express software according to the recommendations of Applied Biosystems (Foster City, CA). The forward and reverse primer sequences for fatty acid binding protein (aP2), hormone-sensitive lipase (HSL), and MMP-9, respectively, were as follows: aP2, GCATGGCCAAACCTAACATGA (forward) and CCTGGCCCAGTATGAAGGAAA (reverse); HSL, GTGCAAAGACGGAGGACCACTCCA (forward) and GACGTCTGGAGTTTCCCCTCAG (reverse); and MMP-9, CCCTGGAGACCTGAGAACCA (forward) and CCACCCGAGTGTAACCATAGC (reverse). Each amplification reaction was performed with 15 ng of cDNA sample in duplicate in 96-well optical reaction plates with a GeneAmp 5700 sequence detection system. The PCR mixture contained forward and reverse primer mix (final concentration, 900 nM for HSL or MMP-9 and 300 nM for aP2) and SYBR Green PCR Master Mix. For ribosomal RNA control (18S rRNA), a mixture containing primers and fluorogenic probe mix, TaqMan Universal PCR Master Mix (Applied Biosystems) was used. All reactions were performed under the same conditions: 50°C for 2 min and 95°C for 10 min, followed by 40 cycles of 95°C for 15 s and 60°C for 1 min. Results were analyzed with the GeneAmp 5700 software, and all values were normalized to the levels of 18S rRNA. 1274 Bourlier et al. Statistical Analysis. Values are expressed as means ⫾ S.E.M. Data were analyzed with one-way analysis of variance coupled with post hoc Dunnett’s multiple comparison test. Statistical significance was set at p ⬍ 0.05. Results MMP Inhibitor Batimastat Treatment Decreases the Differentiation of Human Preadipocytes. To determine whether the broad spectrum MMP inhibitor batimastat could affect the human adipocyte differentiation process, primary cultures of human preadipocytes were treated with 1 or 5 M batimastat for 10 days. Total protein and cell triglyceride contents were quantified, and the expression of two adipocyte differentiation markers, aP2 and HSL, was analyzed by realtime RT-PCR. As is clearly shown in Fig. 1A, 5 M batimastat led to a strong inhibition of the adipocyte differentiation process since treated cells exhibited no changes in shape and less cytoplasmic accumulation of lipid droplets. Quantification of total protein and triglyceride contents, used as lipogenic indices, demonstrated that batimastat treatment statistically decreased adipogenesis (23 and 44% decrease in protein and triglyceride concentrations, respectively) (Fig. 1B). Moreover, the analysis of aP2 and HSL mRNA levels showed that batimastat led to a reduction of the expression of both adipocyte differentiation markers (29 and 33% decrease in aP2 and HSL mRNA expression, respectively) (Fig. 1B). Batimastat at 1 M had no effect on the differentiation process (data not shown). HIV-PI Treatments Decrease the Differentiation of Human Preadipocytes. We then investigated the effect of four HIV-PIs on the human adipocyte differentiation process. Thus, primary cultures of human preadipocytes were treated for 10 days with increasing concentrations of HIV-PIs: 5, 10, 25, or 50 M for SQV and IDV; 1, 5, and 10 M for NFV; and 5, 10, and 25 M for RTV. These concentrations were chosen according to those usually found in the plasma of treated patients and proved to be effective on murine adipocyte differentiation (Lenhard et al., 2000; Roche et al., 2002). Total protein and cell triglyceride contents were quantified, and the expression of aP2 and HSL was analyzed by real-time RT-PCR. Only the concentrations for which a maximal effect on the differentiation process was observed, without detected toxicity (measured by the Toxilight kit, Cambrex Bio Sciences; data not shown), are presented. As shown in Fig. 2, A and B, the protein and/or triglyceride contents of the cells were decreased under HIV-PIs: 25% decrease in triglyceride concentration for IDV (50 M), 28% decrease in triglyceride concentration for RTV (10 M), and 27 and 46% decrease in protein and triglyceride concentrations, respectively, with SQV (10 M); and 34 and 56% decrease in protein and triglyceride concentrations, respectively, with NFV (5 M). The expressions of aP2 and HSL mRNAs were also decreased, respectively, by: 28 and 42% with IDV (50 M), 38 and 47% with RTV (10 M), 72 and 82% with SQV (10 M), and 76 and 87% with NFV (5 M) (Fig. 2, C and D). These results indicate an alteration of the differentiation process with the four HIV-PIs used. However, it is noticeable, as shown for the protein and triglyceride contents, that SQV and NFV exhibited stronger effects on aP2 and HSL expression than IDV or RTV. It should be noted that higher concentrations of SQV (25 and 50 M), RTV (25 M), and NFV (10 M) lead to cell death within a few days in our model. HIV-PIs Do Not Modify the Activity of Human Recombinant MMP-9 or MMP-2. To establish whether HIVPIs could affect the human adipocyte differentiation process by interacting with the MMP-dependent pathways, we first analyzed the capacity of HIV-PIs to inhibit MMP activities. The MMP inhibitor batimastat was used as control. MMP-2 and -9 activities were determined by in vitro fluorescence assays using human recombinant activated MMP-2 and -9 Fig. 1. Effect of the MMP inhibitor batimastat on the differentiation of human preadipocytes. Stromal preadipocytes from human subcutaneous AT were cultured in an adipogenic medium in the presence of 5 M batimastat or its vehicle (control). A, light microscopy analysis performed after 10 days of treatment. Photomicrographs (⫻100) are representative of eight independent experiments. B, total protein and cell triglyceride contents, as well as aP2 and HSL mRNA expression, determined in cells maintained overnight in basal medium with treatments. For aP2 and HSL expression, total RNAs were extracted from cells, and real-time RT-PCR analysis was performed using specific cDNA primers. The results obtained were normalized to the levels of 18S rRNA. Data are means ⫾ S.E.M. expressed as a percentage of the control for eight independent experiments. ⴱ, p ⬍ 0.05 versus control; ⴱⴱ, p ⬍ 0.01 versus control. MMP-9 Involvement in Human Adipocyte Differentiation 1275 Fig. 2. Effect of HIV-PIs on the differentiation of human preadipocytes. Stromal preadipocytes from human subcutaneous AT were cultured for 10 days in an adipogenic medium with vehicle (control) or in the presence of HIV-PIs IDV, RTV, SQV, or NFV at various concentrations. The cells were maintained overnight in basal medium with treatments before use. Total protein and cell triglyceride contents were then determined (A and B). For aP2 and HSL mRNA expression, total RNAs were extracted from cells, and real-time RT-PCR analysis was performed using specific cDNA primers. The results obtained were normalized to the levels of 18S rRNA (C and D). Only the concentrations for which a maximal effect on the differentiation process was observed, without detected toxicity, are presented. Data are means ⫾ S.E.M. expressed as a percentage of the control for four to seven independent experiments. ⴱ, p ⬍ 0.05 versus control; ⴱⴱ, p ⬍ 0.01 versus control. together with a fluorogenic MMP substrate, in the presence of increasing concentrations of HIV-PIs (from 1 nM to 100 M) or batimastat (from 0.01 nM to 0.01 M). As expected, batimastat reduced, in a concentration-dependent manner, the fluorescence emission induced by the cleavage of the MMP substrate. However, none of the four HIV-PIs tested had an effect per se on the basal fluorescence detected in the MMP-9 or -2 activity assays (Fig. 3). HIV-PI Treatments Reduce MMP-9 Gelatinase Activity Released by Human Preadipocytes. To determine whether HIV-PIs could affect the gelatinase activities released by 10-day-differentiated human preadipocytes, medium conditioned overnight by preadipocytes treated with IDV (50 M), RTV (5 M), SQV (10 M), or NFV (5 M) was collected and analyzed by gelatin zymography. As observed in Fig. 4, MMP-9 (92 kDa) and MMP-2 (72 kDa) proforms (artificially activated by the gelatin zymography technique) were the major forms detectable in preadipocyte-conditioned media. An active form was visible for MMP-2 (62 kDa) but not for MMP-9 (82 kDa). Densitometric analysis of the lytic areas showed that HIV-PI treatments reduced the MMP-9 gelatinase activity (proform) released by treated preadipocytes (53, 40, 74, and 91% decrease with IDV, RTV, SQV, and NFV, respectively). Interestingly, this decrease of MMP-9 gelatinase activity in the medium, corresponding to the proform, was not accompanied by an increase of the active MMP-9 form (still not detectable), suggesting that this reduction was due to a decrease in the secretion of the enzyme rather than to an increase in the maturation. Unlike for MMP-9, the MMP-2 gelatinase activity (pro ⫹ active forms) released into the medium by treated preadipocytes did not present a common pattern for the four HIV-PIs used. Indeed, IDV treatment enhanced the MMP-2 activity released into the medium (27% increase), RTV and SQV were devoid of effect, and NFV reduced it (20% decrease) (Fig. 4). HIV-PI Treatments Reduce MMP-9 Expression by Human Preadipocytes. Considering the results obtained with the gelatin zymography technique, real-time RT-PCR analysis was performed on mRNAs extracted from the same 10-day-treated preadipocytes to investigate any effect of HIV-PIs on MMP-9 expression. As depicted in Fig. 5, all HIV-PI treatments led to a sta- 1276 Bourlier et al. Total protein and cell triglyceride contents were assayed, and the expression of aP2 and HSL was analyzed by real-time RT-PCR. As observed in Table 1, protein and triglyceride contents were significantly decreased (44 and 52% decrease in protein and triglyceride concentrations, respectively) as well as mRNA expression of aP2 and HSL (67 and 73% decrease in aP2 and HSL, respectively) in cultures receiving 5 M MMP-9 inhibitor, indicating an alteration of the differentiation process of treated preadipocytes. As for batimastat, MMP-9 inhibitor at 1 M had no effect on human adipocyte differentiation (data not shown). MMP-9 Inhibitor Treatment but Not Batimastat Treatment Decreases MMP-9 Gelatinase Activity Released by Human Preadipocytes. To determine whether the two MMP inhibitors could modify the release of the native preadipocyte-derived MMP-9 and -2, we performed gelatin zymography on medium conditioned overnight by preadipocytes treated for 10 days with 5 M batimastat or MMP-9 inhibitor. As previously reported (Fig. 4), MMP-9 (92 kDa) and MMP-2 (72 kDa) proforms (artificially activated by the gelatin zymography technique) were the major forms detectable in preadipocyte-conditioned media. Surprisingly, densitometric analysis of the lytic areas showed that a 10-day treatment with MMP-9 inhibitor reduced MMP-9 gelatinase activity released into the medium by preadipocytes (84% decrease), without affecting that of MMP-2 (pro ⫹ active forms) (Fig. 6). This decrease of MMP-9 gelatinase activity in the medium, corresponding to the proform, was not accompanied by an increase of the active-MMP-9 form (still not detectable), suggesting that this reduction was due to a decrease in the secretion of the enzyme rather than an increase in the maturation. Real-time RT-PCR analysis performed on mRNAs extracted from the same 10-day-treated preadipocytes revealed a decrease of MMP-9 expression (data not shown), confirming the results obtained with gelatin zymography. Batimastat treatment had no effect on MMP-9 or MMP-2 gelatinase activities released into the medium by treated human preadipocytes (Fig. 6). Fig. 3. Effect of the MMP inhibitor batimastat or HIV-PIs on the activity of human recombinant activated MMP-2 and -9. Human recombinant activated MMP-2 (2 nM) or MMP-9 (4 nM) was preincubated with or without increasing concentrations of batimastat (from 0.01 nM to 0.01 M) or HIV-PIs (from 1 nM to 100 M). The MMP fluorogenic substrate Mca-Pro-Leu-Gly-Leu-Dnp-Ala-Arg was then added, and fluorescence (excitation, 325 nm; emission, 390 nm) was recorded. Data are means ⫾ S.E.M. of maximum rate/minute for five separate measurements, expressed as a percentage of the control for three independent experiments. tistically significant reduction of MMP-9 expression: 64% decrease with IDV (50 M), 75% decrease with RTV (10 M), 82% decrease with SQV (10 M), and 96% decrease with NFV (5 M). These data are in accordance with those obtained by gelatin zymography, suggesting that the observed decrease of MMP-9 gelatinase activity released into the medium under HIV-PI treatments is probably due to a reduction of MMP-9 expression. MMP-9 Inhibitor Treatment Decreases the Differentiation of Human Preadipocytes. Following the previous results with batimastat and HIV-PI treatments, suggesting a particular involvement of MMP-9 subtype in human adipogenesis, primary cultures of human preadipocytes were treated or not with 1 or 5 M MMP-9 inhibitor for 10 days. Discussion We previously reported that human mature adipocytes and preadipocytes as well as murine preadipocytes produced and released two key enzymes of ECM remodeling, the matrix metalloproteinases MMP-2 and -9 (Bouloumié et al., 2001). Moreover, we showed that treatment of murine 3T3-F442A preadipocytes with MMP inhibitors decreased the rate of adipocyte differentiation. These data were recently confirmed by others, suggesting that MMP activities were required for adipogenesis in rodents (Croissandeau et al., 2002; Chavey et al., 2003). In the present work, we found that batimastat, a broad-spectrum MMP inhibitor, also reduced the differentiation of human preadipocytes in primary cultures, demonstrating for the first time that MMP activities are required for adipogenesis in humans too. This effect was strictly mediated by its action per se on MMP activities since batimastat strongly inhibited the activity of human recombinant MMP-2 and -9 without affecting their secretion by treated preadipocytes. Other protease inhibitors, i.e., HIV-PIs, involved in lipo- MMP-9 Involvement in Human Adipocyte Differentiation 1277 Fig. 4. Effect of HIV-PIs on MMP-2 or MMP-9 gelatinase activities released into culture medium by human preadipocytes. Stromal preadipocytes from human subcutaneous AT were cultured in an adipogenic medium with vehicle (control) or in the presence of 50 M IDV, 10 M RTV, 10 M SQV, or 5 M NFV. After 10 days of culture, the cells were washed and maintained overnight in basal medium with treatments. Media were then collected and analyzed by gelatin zymography. Densitometric analysis of the lytic areas was performed, and results are expressed as a percentage of the control. Data are means ⫾ S.E.M. for four to seven independent experiments. ⴱ, p ⬍ 0.05 versus control; ⴱⴱ, p ⬍ 0.01 versus control. dystrophy seen in HIV-patients receiving PI therapy (Carr et al., 1998), have been recently linked to alterations of adipocyte differentiation in murine cell lines in vitro (Zhang et al., 1999; Lenhard et al., 2000; Mondal et al., 2001). We reported here that treatments with HIV-PIs IDV, RTV, SQV, and NFV reduced the differentiation of human preadipocytes in primary cultures. The effectiveness of these products on the TABLE 1 Effect of MMP-9 inhibitor on the differentiation of human preadipocytes Stromal preadipocytes from human subcutaneous AT were cultured for 10 days in an adipogenic medium in the presence of 5 M MMP-9 inhibitor or its vehicle (control). Total protein and cell triglyceride contents, as well as aP2 and HSL mRNA expression, were determined in cells maintained overnight in basal medium with treatments. For aP2 and HSL expression, total RNAs were extracted from cells, and real-time RT-PCR analysis was performed using specific cDNA primers. The results obtained were normalized to the levels of 18S rRNA. Data are means ⫾ S.E.M. expressed as a percentage of the control for five independent experiments. MMP-9 Inhibitor (5 M) % of Control Proteins Triglycerides normalized with proteins aP2 mRNA expression HSL mRNA expression 56.24 ⫾ 8.47** 48.25 ⫾ 13.89** 32.77 ⫾ 2.71** 26.64 ⫾ 6.35** ** p ⬍ 0.01 vs. control. Fig. 5. Effect of HIV-PIs on MMP-9 expression by human preadipocytes. Stromal preadipocytes from human subcutaneous AT were cultured in an adipogenic medium with vehicle (control) or in the presence of 50 M IDV, 10 M RTV, 10 M SQV, or 5 M NFV. After 10 days of culture, the cells were washed and maintained overnight in basal medium with treatments. Total RNAs were extracted from cells, and real-time RT-PCR analysis was performed using specific primers for MMP-9 cDNAs. The results were normalized to the levels of 18S rRNA and expressed as a percentage of the control. Data are means ⫾ S.E.M. for four to six independent experiments. ⴱⴱ, p ⬍ 0.01 versus control. human differentiation process, NFV, SQV⬎RTV, and IDV, was comparable with that described in other in vitro studies (Lenhard et al., 2000; Jain and Lenhard, 2002). According to the inhibitory action of both batimastat and HIV-PIs on the human differentiation process, we then investigated the potential relationships between MMPs and, more particularly, MMP-2 and -9 and HIV-PIs. We did not find any direct effect of HIV-PIs on human recombinant MMP-2 and -9 activities. However, we found that all HIV-PI treatments reduced the release of MMP-9 by treated preadipocytes. This effect was specific to the MMP-9 gelatinase subtype since MMP-2 release did not present the same profile of changes as MMP-9 but depended on which HIV-PI was used as treatment. The decrease of MMP-9 secretion might be due to the reduction of MMP-9 mRNA expression observed with preadipocytes under HIV-PI treatments. Interestingly, the effectiveness of HIV-PIs (NFV and SQV versus RTV and 1278 Bourlier et al. Fig. 6. Effect of batimastat and MMP-9 inhibitor on MMP-2 or MMP-9 gelatinase activities released into culture medium by human preadipocytes. Stromal preadipocytes from human subcutaneous AT were cultured in an adipogenic medium in the presence of 5 M batimastat, 5 M MMP-9 inhibitor (MMP-9 Inh), or its vehicle (control). After 10 days of culture, the cells were washed and maintained overnight in basal medium with treatments. Media were then collected and analyzed by gelatin zymography. Densitometric analysis of the lytic area was performed, and results are expressed as a percentage of the control. Data are means ⫾ S.E.M. for five to seven independent experiments. ⴱⴱ, p ⬍ 0.01 versus control. IDV) on MMP-9 secretion and/or expression was similar to that observed on the differentiation process. Although few data are available in the literature concerning the potential relationships between MMPs and HIV-PIs, Mondal et al. (2001) have recently reported a strong increase in the release of active MMP-2 and a slight increase in the release of pro and active MMP-9 by differentiating 3T3-L1 cells under IDV and RTV treatment. Paradoxically, the same authors described inhibition of 3T3-L1 adipocyte differentiation with both HIV-PIs. These results are unexpected since other studies have reported an increase of secreted MMP-2 and/or -9 in murine preadipocyte models in vitro, including the 3T3-L1 cell type, during adipose conversion (Bouloumié et al., 2001; Croissandeau et al., 2002; Chavey et al., 2003). Furthermore, the use of MMP inhibitors in this model had led to a decrease of the differentiation process (Croissandeau et al., 2002). Culture conditions and experimental protocols may explain these discrepancies. Regarding our results, the differences may also be explained by the in vitro model used, i.e., murine preadipocytes versus human preadipocytes. According to the effect of HIV-PIs on the release and expression of MMP-9, an involvement of this MMP subtype in the batimastat-mediated effect was suspected. Thus, we in- vestigated the effect of MMP-9 inhibitor treatment on human preadipocytes and observed a decrease in the differentiation process. However, unlike batimastat, MMP-9 inhibitor not only decreased the activity of human recombinant MMP-9 (data not shown) but also strongly reduced MMP-9 release by treated preadipocytes. These results associated with those obtained with HIV-PI treatments strongly suggest a particular role of MMP-9 subtype in human adipogenesis. The way in which HIV-PIs affect MMP-9 expression in human preadipocytes may reside in a specificity of the MMP-9 gene, i.e., the presence of a nuclear factor-B (NF-B) binding site in its promoter region. Indeed, recent publications have reported an inhibition of the 20S and/or 26S proteasome in various cellular types using HIV-PIs (Gaedicke et al., 2002; Pajonk et al., 2002; Piccinini et al., 2002). These proteasomes are involved in the degradation of the IB family inhibitory molecules that sequester NF-B transcription factors in the cytosol in resting conditions, masking their nuclear location necessary for gene transcription (Palombella et al., 1994). It can be speculated, according to some recent works (Gaedicke et al., 2002; Pati et al., 2002), that HIV-PIs reduced proteasome activities in our model, decreasing NF-B translocation and MMP-9 gene transcription. This hypothesis is currently being investigated by our group. Thus, by reducing MMP-9 secretion, HIV-PIs may alter not only its direct influence on the degradation of structural matrix molecules but also the cleavage of several circulating, cell surface, and pericellular proteins which regulate cell behavior in numerous ways (Sternlicht and Werb, 2001). Adipocytokines (IL-8, IL-1, IL-6, or tumor necrosis factor-␣) and transforming growth factor-, whose extracellular level and/or activity can be regulated by MMPs, may be involved in the MMP-9-dependent pathway leading to inhibition of human adipocyte differentiation. In conclusion, our data reveal the specificity of impact of MMP inhibitors and HIV-PIs on the human fat cell precursors, the preadipocytes. They show that the modulation of the extracellular matrix components through the production of MMPs and, more precisely, MMP-9 might be a key factor in the regulation of human adipose tissue development. They also suggest that, by affecting the production of MMP-9, HIV-PIs promote human adipose tissue atrophy by preventing replacement of lost adipocytes. Acknowledgments We thank Marie-Thérèse Canal for technical assistance. References Bouloumié A, Sengenès C, Portolan G, Galitzky J, and Lafontan M (2001) Adipocyte produces matrix metalloproteinases 2 and 9: involvement in adipose differentiation. Diabetes 50:2080 –2086. Caron M, Auclair M, Vigouroux C, Glorian M, Forest C, and Capeau J (2001) The HIV protease inhibitor indinavir impairs sterol regulatory element-binding protein-1 intranuclear localization, inhibits preadipocyte differentiation and induces insulin resistance. Diabetes 50:1378 –1388. Carr A, Samaras K, Chisholm DJ, and Cooper DA (1998) Pathogenesis of HIV-1protease inhibitor-associated peripheral lipodystrophy, hyperlipidaemia and insulin resistance. Lancet 351:1881–1883. Chavey C, Mari B, Monthouel MN, Bonnafous S, Anglard P, Van Obberghen E, and Tartare-Deckert S (2003) Matrix metalloproteinases are differentially expressed in adipose tissue during obesity and modulate adipocyte differentiation. J Biol Chem 278:11888 –11896. Croissandeau G, Chretien M, and Mbikay M (2002) Involvement of matrix metalloproteinases in the adipose conversion of 3T3–L1 preadipocytes. Biochem J 364: 739 –746. Dowell P, Flexner C, Kwiterovich PO, and Lane MD (2000) Suppression of preadipocyte differentiation and promotion of adipocyte death by HIV protease inhibitors. J Biol Chem 275:41325– 41332. MMP-9 Involvement in Human Adipocyte Differentiation Gaedicke S, Firat-Geier E, Constantiniu O, Lucchiari-Hartz M, Freudenberg M, Galanos C, and Niedermann G (2002) Antitumor effect of the human immunodeficiency virus protease inhibitor ritonavir: induction of tumor-cell apoptosis associated with perturbation of proteasomal proteolysis. Cancer Res 62:6901– 6908. Jain RG and Lenhard JM (2002) Select HIV protease inhibitors alter bone and fat metabolism ex vivo. J Biol Chem 277:19247–19250. Lenhard JM, Furfine ES, Jain RG, Ittoop O, Orband-Miller LA, Blanchard SG, Paulik MA, and Weiel JE (2000) HIV protease inhibitors block adipogenesis and increase lipolysis in vitro. Antiviral Res 47:121–129. Lijnen HR, Maquoi E, Hansen LB, Van Hoef B, Frederix L, and Collen D (2002) Matrix metalloproteinase inhibition impairs adipose tissue development in mice. Arterioscler Thromb Vasc Biol 22:374 –379. Mondal D, Larussa VF, and Agrawal KC (2001) Synergistic antiadipogenic effects of HIV type 1 protease inhibitors with tumor necrosis factor alpha: suppression of extracellular insulin action mediated by extracellular matrix-degrading proteases AIDS Res Hum Retroviruses 17:1569 –1584. Pajonk F, Himmelsbach J, Riess K, Sommer A, and McBride WH (2002) The human immunodeficiency virus (HIV)-1 protease inhibitor saquinavir inhibits proteasome function and causes apoptosis and radiosensitization in non-HIV-associated human cancer cells. Cancer Res 62:5230 –5235. Palombella VJ, Rando OJ, Goldberg AL, and Maniatis T (1994) The ubiquitinproteasome pathway is required for processing the NF-kappa B1 precursor protein and the activation of NF-kappa B. Cell 78:773–785. Pati S, Pelser CB, Dufraine J, Bryant JL, Reitz MS Jr, and Weichold FF (2002) 1279 Antitumorigenic effects of HIV protease inhibitor ritonavir: inhibition of Kaposi sarcoma. Blood 99:3771–3779. Piccinini M, Rinaudo MT, Chiapello N, Ricotti E, Baldovino S, Mostert M, and Tovo PA (2002) The human 26S proteasome is a target of antiretroviral agents. AIDS 16:693–700. Roche R, Poizont-Martin I, Martin-El Yazidi C, Compe E, Gastaut JA, Torresani J, and Planells R (2002) Effects of antiretroviral drug combinations on the differentiation of adipocytes. AIDS 16:13–20. Rupnick MA, Panigrahy D, Zhang CY, Dallabrida SM, Lowell BB, Langer R, and Folkman MJ (2002) Adipose tissue mass can be regulated through the vasculature. Proc Natl Acad Sci USA 99:10730 –10735. Sternlicht MD and Werb Z (2001) How matrix metalloproteinases regulate cell behavior. Annu Rev Cell Dev Biol 17:463–516. Vernochet C, Azoulay S, Duval D, Guedj R, Ailhaud G, and Dani C (2003) Differential effect of HIV protease inhibitors on adipogenesis: intracellular ritonavir is not sufficient to inhibit differentiation. AIDS 17:2177–2180. Zhang B, MacNaul K, Szalkowski D, Li Z, Berger J, and Moller DE (1999) Inhibition of adipocyte differentiation by HIV protease inhibitors. J Clin Endocrinol Metab 84:4274 – 4277. Address correspondence to: Dr. Virginie Bourlier, Institut National de la Santé et de la Recherche Médicale U586, 37 Allées Jules Guesde, 31073 Toulouse, France. E-mail: [email protected] Discussion de la publication 1 Nous avons travaillé sur des cultures primaires de cellules de la FSV du TA humain, issues de dermolipectomies abdominales. Nos résultats montrent que les cellules de la FSV cultivées dans un milieu adipogénique et traitées pendant 10 jours avec un inhibiteur des MMPs à large spectre, le batimastat, ont une adipogenèse altérée. En effet, il a été constaté que les cellules traitées ont un contenu intracellulaire en TGs diminué par rapport aux cellules contrôles. Il en est de même pour l’expression en ARNm de deux marqueurs adipocytaires, aP2 et la LHS. Ces données indiquent que le batimastat limite la différenciation adipocytaire des cellules de la FSV du TA humain suggérant un rôle majeur des MMPs dans l’adipogenèse chez l’homme. En parallèle, nous avons déterminé l’effet de quatre inhibiteurs de la protéase du VIH: l’indinavir (IDV), le ritonavir (RTV), le saquinavir (SQV) et le nelfinavir (NFV) sur la différenciation des cellules de la FSV du TA humain. Nous avons observé que les quatre IPsVIH utilisés limitent la différenciation adipocytaire des cellules de la FSV en culture primaire. En accord avec nos résultats, une étude récente indiquent que le RTV bloque l’adipogenèse des préadipocytes humains de type SGBS (Syndrome de Simpson-GolabiBehmel) (92, 123). Il faut préciser que dans notre étude en accord avec des résultats décrits dans d’autres études in vitro sur des préadipocytes murins que le SQV et le NFV montrent des effets plus marqués sur la différenciation adipocytaire que l’IDV et le RTV (109, 144). Ainsi, le syndrome de lipoatrophie associé aux IPs-VIH pourrait donc être relatif aux effets apoptotiques observés sur les adipocytes matures (12, 64) mais également aux effets négatifs sur l’adipogenèse. Les effets anti-différenciant obtenus avec les inhibiteurs de protéases matricielles tels que le batimastat et les inhibiteurs de la protéase du VIH, nous ont conduit à émettre l’hypothèse d’un lien entre les MMPs et les IPs-VIH. Afin de déterminer si les IPs-VIH affectent la différenciation adipocytaire via une voie dépendante des MMPs, nous avons étudié leur capacité à inhiber directement l’activité des MMP-2 et -9 par une approche in vitro en utilisant un substrat synthétique des MMPs qui libère un peptide fluorescent après l’action des MMP-2 et -9 recombinantes en présence des IPs-VIH ou d’inhibiteurs des MMPs. Aucun effet direct des IPs-VIH sur l’activité des protéines humaines recombinantes MMP-2 et -9 n’a été observé contrairement au batimastat. Cependant et de manière surprenante, nous avons observé que les quatre IPs-VIH diminuent spécifiquement l’activité gélatinase de MMP-9 relarguée dans le milieu de culture alors que l’activité de MMP-2 reste 60 maintenue. Cette diminution de la sécrétion de MMP-9 par les IPs-VIH est associée à une diminution des taux de transcrits pour MMP-9 suggérant que l’effet anti-adipogénique des IPs-VIH est associé à l’inhibition spécifique de MMP-9 via un effet transcriptionnel sur son expression. Le rôle spécifique de MMP-9 dans l’adipogenèse a été confirmé par un inhibiteur dirigé contre MMP-9 (MMP-9/MMP-13 inhibitor II). Cet inhibiteur diminue la différenciation des cellules de la FSV du TA humain et réduit l’activité mais également l’expression de MMP-9. De plus, l’effet d’un anticorps neutralisant dirigé contre la MMP-9 dans la différenciation adipocytaire des cellules de la FSV du TA humain a fait l’objet d’une étude complémentaire. B) Influence d’un anticorps neutralisant dirigé contre la MMP-9 sur la différenciation adipocytaire Comme pour les précédents traitements décrits dans la publication 1, les cellules de la FSV ont été cultivées en milieu adipogénique et traitées avec un anticorps neutralisant dirigé spécifiquement contre la MMP-9 (Chemicon). Comme le montre la figure 14, après 10 jours de traitement, le contenu intracellulaire en TGs est fortement diminué ainsi que l’expression en ARNm des marqueurs adipocytaire aP2 et LHS. Ces résultats indiquent donc que l’activité de MMP-9 est spécifiquement requise pour le bon déroulement de la différenciation adipocytaire chez l’homme et suggèrent que les effets anti-adipogéniques des IPs-VIH pourraient être médiés par la chute de l’expression de MMP-9. Comme nous l’avons évoqué dans le chapitre d’introduction, les mécanismes d’actions des IPs-VIH sur l’adipogenèse sont encore peu connus. Des travaux ont rapporté que les IPs-VIH peuvent altérer la maturation et la stabilité de la lamine A/C, perturbant ainsi la localisation cellulaire de SREBP-1 et l’adipogenèse de préadipocytes murins (29). Il a également été décrit que les IPs-VIH pouvaient inhiber l’activité du protéasome de certaines cellules cancéreuses (4, 239) et plus récemment celle des préadipocytes murins de la lignée 3T3-L1 (202). En revanche, l’effet des IPs-VIH sur l’activité du protéasome des préadipocytes humains reste à déterminer et a fait l’objet de la suite de ce travail. L’activité du protéasome a de plus été associée à de nombreuses fonctions cellulaires telles que la progression dans le cycle cellulaire, l’apoptose et la régulation de l’expression de nombreux gènes notamment en modulant l’activité du facteur de transcription NF-κB (1, 125). Quelques données parcellaires montrent que l’expression génique de MMP-9, contrairement à celle de 61 B Contrôle Ac neutralisant MMP-9 (0.5 µg/ml) Marqueurs de la différenciation adipocytaire (en % du contrôle) A 100 75 50 * ** 25 0 ** TGs aP2 LHS ARNm Figure 14 : Effet d’un anticorps neutralisant pour la MMP-9 sur la différenciation adipocytaire des cellules de la FSV du tissu adipeux humain Les cellules de la FSV sont cultivées en conditions adipogéniques et traitées avec un anticorps neutralisant MMP-9 ou un IgG contrôle pendant 10 jours. (A) Une photographie représentative de 3 expériences indépendantes est présentée. (B) Le contenu intracellulaire en TGs normalisé à la quantité d’ADN ainsi l’expression en ARNm d’aP2 et de la LHS ont été évalués. Les résultats sont exprimés en % du contrôle. * P<0.01, **P< 0.001 vs contrôle MMP-2, peut-être régulée par NF-κB. En effet, au niveau du promoteur de MMP-9, un site de liaison pour ce facteur de transcription a été décrit (236, 256). Ainsi, en regroupant l’ensemble de ces données, nous avons émis l’hypothèse que les IPs-VIH diminuent l’activité protéasomique des préadipocytes humains empêchant ainsi la dégradation d’IκB, l’inhibiteur de NF-κB, qui interagit avec NF-κB et le séquestre dans le cytoplasme. Par conséquent, NFκB ne peut pas être transféré dans le noyau et entraîner la transcription de gènes notamment celui de MMP-9. Pour plus de clarté, cette hypothèse est schématisée dans la figure 15. C) Détermination des mécanismes impliqués dans la chute de l’expression de MMP-9 par les inhibiteurs de la protéase du VIH Publication 2 : Inhibition of human preadipocyte proteosomal activity, by HIV protease inhibitor or specific inhibitor lacatacystin, leads to a defect in adipogenesis which involves matrix metalloproteinase-9. S. De Barros, A. Zakaroff-Girard, M. Lafontan, J. Galitzky and V. Bourlier J Pharmacol Exp Ther, 320:291-299, 2007 62 IPs-VIH NF-κB IκB PROTEASOME Cytoplasme NF-κB MMP-9 Noyau Figure 15 : Hypothèse du mode d’action des IPs-VIH sur l’expression génique de MMP-9 A l’étal basal, NF-κB est séquestré dans le cytoplasme par son inhibiteur IκB. La translocation nucléaire de Nf-kB permettant l’activation des gènes cibles de ce facteur, dépend de la dégradation de son inhibiteur IκB par le protéasome. Les IPs-VIH ont été décrits comme des inhibiteurs de l’activité du protéasome de certaines cellules cancéreuses et préadipocytes murins. Ainsi, une inhibition de l’activité du protéasome par les IPs-VIH pourrait empêcher la dégradation d’IκB et la translocation nucléaire de NF-κB diminuant ainsi la transcription de ces gènes cibles et notamment MMP-9. 0022-3565/07/3201-291–299$20.00 THE JOURNAL OF PHARMACOLOGY AND EXPERIMENTAL THERAPEUTICS Copyright © 2007 by The American Society for Pharmacology and Experimental Therapeutics JPET 320:291–299, 2007 Vol. 320, No. 1 111849/3162833 Printed in U.S.A. Inhibition of Human Preadipocyte Proteasomal Activity by HIV Protease Inhibitors or Specific Inhibitor Lactacystin Leads to a Defect in Adipogenesis, Which Involves Matrix Metalloproteinase-9 Sandra De Barros, Alexia Zakaroff-Girard, Max Lafontan, Jean Galitzky, and Virginie Bourlier Unité de Recherche sur les Obésites, Institut National de la Santé et de la Recherche Médical Unité 586, Institut Louis Bugnard, Hopital Rangueil, Université Paul Sabatier, Toulouse, France Received August 2, 2006; accepted October 10, 2006 ABSTRACT In a previous publication, we reported that human immunodeficiency virus (HIV) protease inhibitors (PIs) inhibited the differentiation of human preadipocytes in primary culture, reducing the expression and secretion of matrix metalloproteinase 9 (MMP-9). The present work was performed to clarify this mechanism. Interestingly, HIV-PIs have been reported to be inhibitors of the proteasome complex, which is known to regulate nuclear factor (NF)-B activation and transcription of its target genes, among them MMP-9. We thus investigated the potential involvement of the proteasome in the antiadipogenic effects of HIV-PIs. The effect of four HIV-PIs was tested on preadipocyte proteasomal activity, and chronic treatment with the specific proteasome inhibitor lactacystin was performed to evaluate alterations of adipogenesis and MMP-9 expression/secretion. Finally, modifications of the NF-B pathway induced by either HIV-PIs or lactacystin were studied. We demonstrated that Proteasomes are highly conserved multimeric peptidases present in all eukaryotic cells. Whereas various forms of proteasomes exist, the 20S proteasome (multicatalytic core of all proteasomes) and the 26S proteasome (20S core capped with two 19S regulatory units) are major proteasomes. Proteasomes were initially thought to be just recyclers of damaged or misfolded proteins, but over the last decade the activity of this enzymatic complex has been found to be of This work was supported by Grants 01 128 and 02 197 from the Agence Nationale de Recherche sur le SIDA et les hépatites virales. Article, publication date, and citation information can be found at http://jpet.aspetjournals.org. doi:10.1124/jpet.106.111849. preadipocyte proteasomal activity was decreased by several HIV-PIs and that chronic treatment with lactacystin mimicked the effects of HIV-PIs by reducing adipogenesis and MMP-9 expression/secretion. Furthermore, we observed an intracellular accumulation of the NF-B inhibitor, IB, with chronic treatment with HIV-PIs or lactacystin as well as a decrease in MMP-9 expression induced by acute tumor necrosis factor-␣ stimulation. These results indicate that inhibition of the proteasome by specific (lactacystin) or nonspecific (HIV-PIs) inhibitors leads to a reduction of human adipogenesis, and they therefore implicate deregulation of the NF-B pathway and the related decrease of the key adipogenic factor, MMP-9. This study adds significantly to recent reports that have linked HIV-PI-related lipodystrophic syndrome with altered proteasome function, endoplasmic reticulum stress, and metabolic disorders. critical importance for many cellular functions. Cell-cycle progression, oncogenesis, apoptosis, regulation of gene expression, and inflammation or immune surveillance are all physiological functions regulated by the proteasome pathway (Kisselev and Goldberg, 2001). Among the substrates of the proteasome, cyclins (e.g., cyclin B1), cyclin-dependent kinase inhibitors (e.g., p21 and p27), tumor suppressors (e.g., p53), and inhibitors (IB) or precursors (e.g., p105) of the transcription factor NF-B are well established (Kisselev and Goldberg, 2001; Adams, 2004). Accordingly, the proteasome complex has emerged as an attractive target for cancer therapy, and numerous proteasome inhibitors have been developed (Adams, 2004; Voorhees and Orlowski, 2006). ABBREVIATIONS: IB, inhibitor of nuclear factor-B; NF-B, nuclear factor-B; HIV, human immunodeficiency virus; PI, protease inhibitor; AT, adipose tissue; MMP, matrix metalloproteinase; SQV, saquinavir; NFV, nelfinavir; TNF, tumor necrosis factor; Bay 11-7802, (E)-3-[(4-methylphenyl)-sulfonyl]-2-propenenitrile; IDV, indinavir; RTV, ritonavir; RFU, relative fluorescence units; TBST, Tris-buffered saline/Tween 20; RT, reverse transcriptase; PCR, polymerase chain reaction; aP2, fatty acid binding protein; HSL, hormone-sensitive lipase; ANOVA, analysis of variance. MG-132, carbobenzoxy-L-leucyl-L-leucyl-L-leucinal; TG, triglyceride. 291 292 De Barros et al. Recently, human immunodeficiency virus (HIV) protease inhibitors (PIs), central components of highly active antiretroviral therapy, have been reported by some authors to directly inhibit the activities of murine and human 20S and/or 26S proteasomes in purified fractions or cellular extracts (André et al., 1998; Gaedicke et al., 2002; Pajonk et al., 2002; Piccinini et al., 2002). Indeed, several cleavage sites used by the HIV protease, which were once thought to be unique and distinct from those of mammalian proteases (predicting inhibitor selectivity), were found to be similar to those recognized by the 20S proteasome (Schmidtke et al., 1999). Although HIV-PIs have been successfully used in clinical therapy of HIV infection, they were also rapidly associated with the emergence of a lipodystrophic syndrome observed in patients treated with highly active antiretroviral therapy, which includes dyslipidemia, insulin resistance, central adiposity, and peripheral lipoatrophy. It is now clear that the mechanism associated with PI-induced metabolic abnormalities is multifactorial (for reviews, see Hui, 2003; Rudich et al., 2005) but whether the action of HIV-PIs on proteasomal activity is related to their side effects has been poorly investigated to date. We previously reported, in accordance with in vivo studies performed on adipose tissue biopsies from HIV-infected lipodystrophic patients (Bastard et al., 2002; Lloreta et al., 2002), that PIs reduced the differentiation of human preadipocytes (i.e., adipocyte precursors) in primary culture isolated from subcutaneous abdominal adipose tissue (AT) (Bourlier et al., 2005). This effect was attributed to an indirect action of HIV-PIs on the expression and secretion of the matrix metalloproteinase-9 (MMP-9), an enzyme implicated in extracellular matrix remodeling and significantly involved in the human adipogenic process in vitro (Bourlier et al., 2005). Because the MMP-9 promoter contains an NF-B site (Sato and Seiki, 1993; St-Pierre et al., 2004) and because proteasomal activity is involved in the activation of NF-B pathway, we investigated the potential role of the proteasome in the antiadipogenic effect of HIV-PIs. We demonstrate here that HIV-PIs, particularly saquinavir (SQV) and nelfinavir (NFV), were direct inhibitors of the human preadipocyte 20S and 26S proteasomes. We found that chronic lactacystin (a specific proteasome inhibitor) treatment mimicked the effects of HIV-PIs by decreasing the differentiation process and the expression and secretion of MMP-9. Chronic treatment with either HIV-PIs (SQV or NFV) or lactacystin led to the accumulation of the IB protein, the inhibitor of the transcription factor NF-B and a substrate of the proteasome. Finally, acute treatment with TNF-␣ (activator of NF-B) induced a potent increase in MMP-9 expression, which was significantly reduced by SQV, lactacystin, or (E)-3-[(4-methylphenyl)-sulfonyl]-2-propenenitrile (Bay 11-7082) (inhibitor of NF-B activation) cotreatments. Overall, our data indicate that HIV-PIs, by affecting proteasomal activity, alter the NF-B pathway and implicate the reduction of MMP-9 activity in their antiadipogenic effect. Materials and Methods Cell Culture and Treatment. Chemicals were from SigmaAldrich (Saint-Quentin Fallavier, France). Cell culture reagents were either from Life Technologies (Cergy Pontoise, France), Roche Diagnostics (Meylan, France), or Cambrex Biosciences (Verviers, Belgium). Human subcutaneous abdominal white AT was obtained from moderately overweight women undergoing plastic surgery (mean age 46 ⫾ 2 years and mean body mass index 27.5 ⫾ 0.7 kg/m2). The isolation of human AT-derived stromal cells and the culture of stromal preadipocytes differentiated into adipocytes were performed as described previously (Bouloumié et al., 2001). In brief, sterile AT was cut into small pieces and digested under agitation with collagenase (2 mg/ml) (Serva; Coger, Paris, France) for ⬃1 h at 37°C. After centrifugation, washing, and filtration steps, the stromal cells were suspended in Dulbecco’s modified Eagle’s medium F-12 supplemented with 10% fetal bovine serum and plated at 60,000 cells/cm2. After 24 h, the medium was replaced by a medium consisting of Dulbecco’s modified Eagle’s medium F-12 supplemented with 33 M biotin, 17 M pantothenate, and 50 g/ml gentamicin (basal medium) in the presence of 66 nM insulin, 1 nM triiodothyronine, 100 nM cortisol, and 10 g/ml human transferrin (adipogenic medium) and 1 g/ml ciglitazone for the first 3 days. After the 3-day priming period, the cells were used for experiments or cultured in the adipogenic medium supplemented with 1) the proteasome inhibitor lactacystin or 2) HIV-PIs IDV (kindly provided by Merck Laboratories, Rahway, NJ) or SQV (kindly provided by Roche, Welwyn Garden City, UK), RTV (kindly provided by Abbott Laboratories, Chicago, IL), or NFV (kindly provided by Roche Diagnostics, Mannheim, France) for 10 days. Lactacystin and HIV-PIs were dissolved in pure dimethyl sulfoxide. Control cells were treated using an appropriate concentration of vehicle (⬍0.25%) after verification that dimethyl sulfoxide was without effect on the various parameters analyzed (i.e., lipogenic index, adipogenic gene, or MMP secretion). Medium was replaced every 2 days. Before some experiments, cells were placed overnight in basal medium supplemented with the various treatments. The medium was then collected and used in zymography analysis. Cellular triglyceride and DNA contents were determined using kits from Sigma-Aldrich and Molecular Probes (PicoGreen; Interchim, Montluçon, France), respectively, according to the manufacturer’s instructions. DNA content was used to normalize data (triglyceride content and MMP secretion) and to evaluate any cytotoxic effect of treatments. Gelatin Zymography. Proteins with gelatinolytic activity (including the gelatinase A “MMP-2” and the gelatinase B “MMP-9”) were identified by electrophoresis in the presence of SDS in 8% polyacrylamide gels containing 1 mg/ml gelatin. In brief, culture medium aliquots (20 l) were directly loaded onto gels, and, after electrophoresis, proteins were renatured by exchanging SDS with 2.5% Triton X-100 (20-min incubation repeated twice). The gels were then incubated for 16 h at 37°C in 50 mM Tris-HCl (pH 8.8), 5 mM CaCl2, and 0.02% NaN3 and stained with Coomassie Blue. The presence of gelatinolytic activity in the culture medium aliquots was visualized as clear areas on an otherwise blue gel. Migration of proteins was compared with that of prestained molecular weight markers. The gels were scanned by an imaging densitometer and quantified using the NIH Image program (developed at the National Institutes of Health, Bethesda, MD). Fluorimetric Proteasome Activity Assay. Chymotrypsin-like proteasome activity was performed on 96-well plates using the specific fluorogenic substrate N-succinyl-Leu-Leu-Val-Tyr7-amido-4methylcoumarin (Sigma). In brief, cells contained in one well were scraped in 35 l of lysis buffer containing 25 mM Tris-HCl (pH 7.5), 0.1% Nonidet P-40, 10% glycerol, 5 mM MgCl2, 1 mM ATP, and 10 mM KCl. Protein concentration was determined using a Bio-Rad kit (Bio-Rad, Marnes-la Coquette, France), and 10 g were incubated alone or with increasing concentrations of lactacystin (0.01–10 M) or HIV-PIs (1, 10, and 50 M) for 30 min at 37°C in 20 mM Tris-HCl (pH 8), 0.5 mM EDTA, and 0.035% SDS to assess 20S proteasome activity or in 20 mM Tris-HCl (pH 8), 1 mM ATP, and 2 mM MgCl2 to assess 26S proteasome activity, according to the method of Rock et al. (1994). Then, fluorogenic substrate was added to a final concentration of 50 M, and fluorescence was monitored at excitation 360 Proteasome Inhibition Reduces Human Adipogenesis nm/emission 460 nm every 5 min over a 2-h period using a Fluoroscan Ascent FL (Labsystems, Cergy Pontoise, France). Chymotrypsin-like proteasome activities of 20S and 26S were evaluated by the maximal rate (relative fluorescence units per minute) on seven separate measurements in each well. Western Blot. For Western blot analysis of IB␣ and IB, cells contained in two wells were scraped in 70 l of lysis buffer containing 20 mM Tris-HCl (pH 7.5), 150 mM NaCl, 1 mM CaCl2, 1 mM MgCl2, 1 mM Na3VO4, 1% Nonidet P-40, 10% glycerol, and a mix of protease inhibitors (Complete; Roche Diagnostics). The protein concentration was determined, and 35 to 50 g of protein were loaded and separated by electrophoresis on a 12% SDS-polyacrylamide gel under denaturing conditions. After transfer to polyvinylidene difluoride membranes (Immobilon; Millipore, Bedford, MA) and Ponceau staining to verify equal loading of the lanes, membranes were blocked for 1 h with TBST [50 mM Tris-HCl (pH 7.5), 150 mM NaCl, 0.1% Tween 20] containing 5% nonfat milk, following by incubation overnight at 4°C with primary antibody against IB␣ (ab7545) or IB (ab7547) (Abcam, Cambridge, UK) at a dilution of 1:1000 in TBST containing 1% nonfat milk. Then, membranes were washed with TBST and incubated for 1 h with a peroxidase-conjugated secondary antibody (Pierce Chemical, Brebières, France) at a dilution of 1:50,000 in TBST containing 1% nonfat milk and washed again. The immunocomplexes were detected using a chemiluminescence reagent kit (SuperSignal West Dura Extended Duration Substrate; Pierce Chemical, Rockford, IL). Human Daudi cell lysate (Imgenex, San Diego, CA) was used as positive control. For Western blot analysis of NF-B p65, cells contained in 12 wells were washed twice with cold phosphate-buffered saline and prepared using NE-PER Nuclear and Cytoplasmic Extraction Reagents kit (Pierce) according to the manufacturer’s instructions. Protein concentrations in nuclear and cytoplasmic extracts were determined as described above: 20 to 45 g of proteins were loaded and separated by electrophoresis on a 12% SDS-polyacrylamide gel electrophoresis under denaturing conditions. After transfer to polyvinylidene difluoride membranes and Ponceau staining to verify equal loading of the lanes, a WesternBreeze Chemiluminescent Western Blot Immunodetection Kit (Invitrogen, Cergy Pontoise, France) was used for signal detection. Briefly and according to the manufacturer’s instructions, membranes were blocked, washed, and then incubated with a primary antibody against NF-B p65 N-terminal (Santa Cruz Biotechnology, Le Perray-en-Yvelines, France) at a dilution of 1:1000. After washing, membranes were incubated with an alkaline phosphatase-conjugated secondary antibody provided with the kit, and immunocomplexes were detected after the addition of chemiluminescent substrate. Human nuclear extract from A-431 cells (Santa Cruz Biotechnology) was used as positive control. The autoradiographs were scanned by an imaging densitometer and quantified using the NIH Image program. To normalize results, the densitometric value of each band of interest (i.e., IB␣, IB, and NF-B p65) was reported to the densitometric value of total loaded proteins in the corresponding lane, obtained after scanning and quantification of the Ponceau staining (NIH Image program). Real-Time RT-PCR. Changes in mRNA levels from specific genes were quantified by real-time RT-PCR. Total RNAs were extracted using a QIAGEN RNeasy Mini Kit according to the manufacturer’s instructions, and RNA concentrations were determined using a Molecular Probes fluorimetric assay (RiboGreen; Interchim). RNA (0.5 g) was reverse-transcribed using the Superscript II system (Invitrogen) according to the manufacturer’s instructions. Reverse transcription was also performed without Thermoscript enzyme on RNA samples to check for any genomic DNA contamination. PCR primers were designed using Primer Express software according to the recommendations of Applied Biosystems (Courtaboeuf, France). The forward and reverse primer sequences for fatty acid binding protein (aP2), hormone-sensitive lipase (HSL), MMP-9, MMP-2, and IB were as follows (5⬘–3⬘): aP2, GCATGGCCAAACCTAACATGA (forward) and CCTGGCCCAGTATGAAGGAAA (re- 293 verse); HSL, GTGCAAAGACGGAGGACCACTCCA (forward) and GACGTCTCGGAGTTTCCCCTCAG; MMP-9, CCCTGGAGACCTGAGAACCA (forward) and CCACCCGAGTGTAACCATAGC (reverse); MMP-2 CACCCATTTACACCTACACCAAGA (forward) and AGAGCTCCTGAATGCCCTTGA (reverse), and IB TACGACGACATTGTGGTTCACA (forward) and GGGTCGTCAGGAAGAGGTTTT (reverse). Each amplification reaction was performed with 15 ng of cDNA sample in duplicate in 96-well optical reaction plates with a GeneAmp 7500 sequence detection system. The PCR mixture contained forward and reverse primer mix (final concentration: 900 nM for HSL, MMP-9, or MMP-2 and 300 nM for aP2 or IB) and SYBR Green PCR Master Mix. For ribosomal RNA control (18S rRNA), a mixture containing primers and fluorogenic probe mix, TaqMan Universal PCR Master Mix (Applied Biosystems) was used. All reactions were performed under the same conditions: 50°C for 2 min and 95°C for 10 min, followed by 40 cycles of 95°C for 15 s and 60°C for 1 min. Results were analyzed with the GeneAmp 7500 software, and all values were normalized to the levels of 18S rRNA. An interindividual variability of 10.46% within the control values was observed for all PCR data (aP2, HSL, MMP-2, MMP-9, and IB). Statistical Analysis. Values are expressed as means ⫾ S.E.M. from n independent experiments. Statistical analysis was performed using Student’s t test for paired data or one-way analysis of variance (ANOVA) coupled with post hoc Dunnett’s multiple-comparison test (GraphPad Prism 4; GraphPad Software Inc., San Diego, CA). Values of p ⬍ 0.05 were considered statistically significant. Results HIV-PIs or Lactacystin Reduced Proteasome Activity from Human Preadipocyte Homogenates. To validate our hypothesis, we first investigated the effect of HIVPIs on proteasome activity of human preadipocytes. After the 3-day priming period, undifferentiated preadipocytes were scraped into specific lysis buffer, and cellular homogenates were obtained. Then, homogenates were pretreated (30 min, 37°C) with increasing concentrations of the proteasome inhibitor lactacystin (from 0.01 to 10 M) or HIV-PIs (1, 10, and 50 M), and 20S and 26S chymotrypsin-like proteasome activities from these lysates were determined by in vitro fluorescence assays with the specific fluorogenic substrate N-succinyl-Leu-Leu-Val-Tyr7-amido-4-methylcoumarin. As expected, lactacystin reduced, in a concentration-dependent manner, the fluorescence emission induced by the cleavage of the substrate by the 20S and 26S proteasome (control maximal rate: 1.62 ⫾ 0.84 and 1.13 ⫾ 0.21 RFU/min, respectively) (Fig. 1, top and bottom). Similar results were obtained with another known proteasome inhibitor, carbobenzoxy-Lleucyl-L-leucyl-L-leucinal (MG-132) (data not shown). As shown on the top of Fig. 1, HIV-PIs, except IDV, decreased chymotrypsin-like activity of the 20S proteasome in a concentration-dependent manner with the following rank of efficiency: SQV ⱖ NFV ⬎ RTV. Higher concentrations of HIVPIs were necessary to reduce the 26S chymotrypsin-like proteasome activity in the cellular extracts (Fig. 1, bottom). Chronic Lactacystin Treatment Decreased the Differentiation of Human Preadipocytes. To determine whether the inhibition of the proteasome per se could affect the human adipocyte differentiation process, primary cultures of human preadipocytes were placed in an adipogenic medium in the presence of 0.1 or 0.5 M lactacystin for 10 days. Cellular triglyceride was quantified, and the expression of two adipocyte differentiation markers, aP2 and HSL, was analyzed by real-time RT-PCR. 294 De Barros et al. Fig. 1. Effect of HIV-PIs on chymotrypsin-like proteasome activity in human preadipocyte homogenates. Stromal preadipocytes were isolated from human subcutaneous AT. After the 3-day priming period, cells were washed and maintained overnight in basal medium before being scrapped in specific lysis buffer. Ten micrograms of protein obtained from cellular homogenates were then preincubated (30 min, 37°C) with or without increasing concentrations of lactacystin (0.01 and 10 M) or HIV-PIs (1, 10, and 50 M). The proteasome fluorogenic substrate N-succinyl-LeuLeu-Val-Tyr7-amido-4-methylcoumarin was added and fluorescence (excitation 360 nm/emission 460 nm) was recorded every 5 min over a 2-h period. Data are means ⫾ S.E.M. of maximal rate (relative fluorescence units per minute) for seven separate measurements, expressed as a percentage of the control for four to five independent experiments. ⴱ, p ⬍ 0.05 versus control; ⴱⴱ, p ⬍ 0.01 versus control. As clearly shown in Fig. 2A, 0.5 M lactacystin led to a strong inhibition of the adipocyte differentiation process because treated cells exhibited less cytoplasmic accumulation of lipid droplets. Quantification of cellular triglyceride (TG) content, used as a lipogenic index, demonstrated that lactacystin treatment significantly decreased adipogenesis (36% decrease in triglyceride concentration, i.e., 26.58 ⫾ 8.28 mg of TGs/mg of DNA for controls to 13.68 ⫾ 3.12 mg of TGs/mg of DNA for lactacystin) (Fig. 2B). Moreover, the analysis of aP2 and HSL mRNA levels showed that lactacystin led to a reduction of the expression of both adipocyte differentiation markers (41 and 60% decreases in aP2 and HSL mRNA expression, respectively) (Fig. 2B). It has to be noticed that lactacystin at 0.1 M had no effect on the differentiation process and that both 0.1 and 0.5 M lactacystin were free of any cytotoxic effects (data not shown). However, the use of concentrations higher than 1 M was associated with cell death within several days (data not shown). Chronic Lactacystin Treatment of Human Preadipocytes Reduced MMP-9 Expression and MMP-9 Gelatinase Activity Released into the Medium. MMP-9 activity has been shown 1) to be involved in the human adipocyte differentiation process (Bouloumié et al., 2001; Bourlier et al., 2005) and 2) to be reduced in human preadipocytes treated by HIV-PIs (Bourlier et al., 2005). To evaluate whether the inhibition of the proteasome per se could affect MMP-9 secretion and expression, overnight-conditioned medium from preadipocytes treated with 0.5 M lactacystin for 10 days was collected to be analyzed by gelatin zymography, and real-time RT-PCR analysis was performed on mRNAs. As observed in Fig. 3A, MMP-9 (92 kDa) and MMP-2 (72 kDa) proforms (artificially activated by the gelatin zymography technique) were the major forms detectable in preadipocyte-conditioned media. The active form was visible for MMP-2 (62 kDa) but not for MMP-9 (82 kDa). Densitometric analysis of the lytic areas showed that lactacystin treatment reduced the MMP-9 gelatinase activity (proform) released by treated preadipocytes (53.2 ⫾ 2.7% of the control value, n ⫽ 4, p ⬍ 0.001). Interestingly, this decrease of MMP-9 gelatinase activity in the medium, corresponding to the proform, was not accompanied by an increase of the active-MMP-9 form (still not detectable), suggesting that this reduction was due to a decrease in the secretion of the enzyme rather than to an increase in the maturation. In contrast to MMP-9, the MMP-2 gelatinase activity (proform ⫹ active forms) was not affected by lactacystin treatment (112.2 ⫾ 11.8% of the control value, n ⫽ 4). The analysis of MMP mRNA expression (Fig. 3B) was consistent with the data obtained by gelatin zymography because lactacystin treatment led to a statistically significant reduction of MMP-9 expression (45% decrease), whereas no change was observed for MMP-2 expression. Thus, the observed decrease of MMP-9 gelatinase activity released into the medium under lactacystin treatment was probably due to a reduction of MMP-9 expression. Chronic Treatment with HIV-PIs or Lactacystin Had No Effect on IB␣ but Increased IB Protein Level in Human Preadipocytes. To identify the link between the inhibition of the proteasome activity and the decrease in MMP-9 expression, we studied the effect of chronic lactacystin or HIV-PI treatment on IB␣ and IB proteins, known substrates of the proteasome. The degradation of these two well-known IB family members leads to NF-B translocation to the nucleus (Whiteside and Israël, 1997) and transcription of NF-B target genes, among them MMP-9 (StPierre et al., 2004). Human preadipocytes were placed in an adipogenic medium and treated for 10 days with lactacystin or various HIV-PIs at concentrations for which no cytotoxic effect was detected and the inhibition of the differentiation was maximal according to our previous publication (Bourlier et al., 2005). Cellular extracts were obtained and analyzed by the Western blot technique. As shown in Fig. 4A, none of the treatments led to the accumulation of IB␣ in human preadipocytes. In contrast, the quantification of the IB band clearly indicated that SQV, NFV, and lactacystin treatment increased the total cellular level of IB protein (83, 36, and 75% increases, respectively) in human preadipocytes (Fig. 4B). This effect was not observed with the two other HIV-PIs, IDV and RTV. Proteasome Inhibition Reduces Human Adipogenesis 295 Fig. 2. Effect of chronic lactacystin treatment on the differentiation of human preadipocytes. Stromal preadipocytes from human subcutaneous AT were cultured in an adipogenic medium in the presence of 0.5 M lactacystin or its vehicle (control). A, light microscopy analysis was performed after 10 days of treatment. Photomicrographs (100⫻) are representative of five independent experiments. B, cellular TGs, as well as aP2 and HSL mRNA expression, were determined in cells maintained overnight in basal medium with treatment. Cellular triglycerides were normalized to DNA content. For aP2 and HSL expression, total RNAs were extracted from cells and reverse-transcribed, and realtime RT-PCR analysis was performed using specific cDNA primers. The results obtained were normalized to the levels of 18S rRNA. The presented data are means ⫾ S.E.M. expressed as a percentage of the control for five independent experiments. ⴱ, p ⬍ 0.05 versus control; §, p ⬍ 0.001 versus control. Fig. 3. Effect of chronic lactacystin treatment on MMP-9 and -2 gelatinase activities released into the medium and on their expression by human preadipocytes. Stromal preadipocytes from human subcutaneous AT were cultured in an adipogenic medium with 0.5 M lactacystin or its vehicle (control). After 10 days of culture, the cells were washed and maintained overnight in basal medium with or without treatment. A, culture media were then collected and analyzed by gelatin zymography. The presented gel is representative of four independent experiments. Quantification of the lytic areas was performed with the NIH Image program. B, total RNAs were extracted from cells and real-time RT-PCR analysis was performed using specific primers for MMP-9 and MMP-2 cDNAs. The results were normalized to the levels of 18S rRNA. The presented data are means ⫾ S.E.M. expressed as a percentage of the control for five independent experiments. ⴱⴱ, p ⬍ 0.01 versus control. It has to be noticed that homogeneity of the controls (i.e., IDV, RTV, NFV, SQV, and lactacystin controls) was checked using one-way ANOVA (not significant, p ⫽ 0.83). The control raw value obtained for the densitometric analysis of IB band normalized to total loaded proteins per lane was 0.095 ⫾ 0.019 (arbitrary units). To verify that the increase in IB protein level was not due to an effect of treatments on IB expression, RT-PCR analysis was performed on mRNAs of preadipocytes treated for 10 days with NFV (5 M), SQV (10 M), or lactacystin (0.5 M), when accumulation of the protein was observed. As shown in Fig. 4C, none of the treatments significantly affected IB expression, suggesting that the accumulation of the protein in the cytosol was due mainly to a decrease of its degradation, i.e., a decrease in proteasomal activity. However, a contribution of IB mRNA expression with NFV can not be excluded, whereas no statistical significance was found compared with control values (p ⫽ 0.07, n ⫽ 6), according to the particular variability of the data in this condition. As for the Western blot experiment, homogeneity of the controls (i.e., NFV, SQV, and lactacystin controls) was checked using one-way ANOVA (not significant, p ⫽ 0.90). The control raw value obtained for the relative amount of IB mRNA normalized to 18S rRNA (i.e., 2⌬Ct ⫻ 104) was 1.42 ⫾ 0.25 (arbitrary units). Chronic Treatment with SQV or Lactacystin Did Not Lead to NF-B p65 Accumulation in the Cytoplasm of Human Preadipocytes. According to the very similar profile in IB protein increase between SQV and lactacystin chronic treatment, we measured the NF-B p65 activity in 10-day-treated preadipocytes because this subunit contains the transactivation domain necessary for gene transcription (Hayden and Ghosh, 2004) and has been recently implicated 296 De Barros et al. Fig. 4. Effect of chronic HIV-PIs or lactacystin treatment on IB␣ and IB protein level in human preadipocytes. Stromal preadipocytes from human subcutaneous AT were cultured in an adipogenic medium with vehicle (control) or in the presence of lactacystin (Lacta.; 0.5 M) or HIV-PIs: IDV (50 M), RTV (10 M), SQV (10 M), or NFV (5 M). After 10 days of culture, the cells were washed and maintained overnight in basal medium with treatment before being scrapped in a specific lysis buffer. Thirty-five to 50 g of total proteins obtained after lysis were then analyzed by Western blot using a specific antibody. A, representative autoradiographs of the IB␣ and the IB blots from four to seven independent experiments are shown. Statistically significant results are expressed as ratio of the control values. NS, nonsignificant. ⴱ, p ⬍ 0.05 versus control. B, quantification of the corresponding bands was performed with the NIH Image program and normalized to the density of the total loaded proteins per lane, obtained from the analysis of the Ponceau staining. The control value of the densitometric ratio was 0.095 ⫾ 0.019. The presented data are means ⫾ S.E.M. expressed as a percentage of the control. ⴱ, p ⬍ 0.05 versus control. C, total RNAs were extracted from cells and reverse-transcribed, and real-time RT-PCR analysis was performed using specific primers for IB cDNAs. The results were normalized to the levels of 18S rRNA. Control value of the 2⌬Ct ⫻ 104 was 1.42 ⫾ 0.25. The presented data are means ⫾ S.E.M. expressed as a percentage of the control for five to six independent experiments. in adipocyte differentiation of the 3T3-L1 cell line (Berg et al., 2004). Unfortunately, we were unable to detect NF-B p65 activity in any of our conditions (control or treated preadipocytes) using the TransAM NF-B chemiluminescent transcription factor assay kit (Active Motif Europe, Rixensart, Belgium), following the manufacturer’s instructions. Assays were performed with either cellular or nuclear preadipocyte extracts, but signal corresponding to free active NF-B p65 was always at the blank level (even with the highest protein concentration required), whereas signal from the positive control (Jurkat nuclear extract) of the kit was detected. One possible explanation was a very low presence of active NF-B p65 under basal conditions. We decided to also perform NF-B p65 Western blot analysis of cytoplasmic and nuclear extracts from 10-day-treated preadipocytes to investigate whether NF-B p65 translocation was affected by IB protein accumulation induced by SQV or lactacystin. As observed in Fig. 5A (left panel), NF-B p65 subunit was undetectable (n ⫽ 3) or not analyzable (n ⫽ 2) in nuclear extracts from control or treated human preadipocytes. This observation was in agreement with the negative results obtained with the TransAM assay kit. However, NF-B p65 was clearly present in the cytoplasmic extracts, but quantification of the corresponding bands did not reveal any significant difference in protein level between control versus treated preadipocytes (Fig. 5B). To validate the cytoplasmic to nuclear translocation of the NF-B p65 assay, control experiments were performed using human preadipocytes stimulated with TNF-␣ (25 ng/ml) for 1 h. Indeed, TNF-␣ is a standard activator of the NF-B pathway in a variety of cells (Viatour et al., 2005). As observed in Fig. 5A (right panel), cytoplasmic NF-B p65 was decreased with TNF-␣ compared with controls (55% decrease, n ⫽ 3, p ⬍ 0.05). Furthermore and although no NF-B p65 was detectable in the nucleus, a new band of ⬃35 kDa was clearly visible under TNF-␣ stimulation. This band has already been identified as a product of nuclear proteolysis of NF-B p65 (N-terminal fragment), termed NF-B p35, and observed in the physiological turnover of the transcription factor (Cressman and Taub, 1994). This result indicates that NF-B p65 has been translocated to the nucleus, validating our technique. Acute Treatment with SQV, Lactacystin, or BAY 117082 Reduced TNF-␣-Induced MMP-9 Expression in Human Preadipocytes. Because one of the possible limitations of our experiments to clearly identify NF-B was that cells were under basal conditions, we decided to investigate the acute effect of SQV and lactacystin on MMP-9 expression induced by TNF-␣. After the 3-day priming period, human preadipocytes were placed in an adipogenic medium and Proteasome Inhibition Reduces Human Adipogenesis Fig. 5. Effect of chronic SQV or lactacystin (Lacta.) treatment on cytoplasmic and nuclear NF-B p65 protein level in human preadipocytes. Stromal preadipocytes from human subcutaneous AT were cultured in an adipogenic medium with vehicle (control) or in the presence of lactacystin (0.5 M) or SQV (10 M). After 10 days of culture, the cells were washed and maintained overnight in basal medium with treatment before being scrapped and prepared using NE-PER nuclear and cytoplasmic extraction reagents kit. Twenty to 45 g of proteins from cytoplasmic (Cyto.) or nuclear (Nucl.) extracts were then analyzed by Western blot using a specific anti-NF-B p65 subunit antibody. A representative autoradiograph of five independent experiments is shown (A, left panel). Quantification of the corresponding bands in the cytoplasmic extracts was performed with the NIH Image program and normalized to the density of the total loaded proteins per lane, obtained from analysis of Ponceau staining (B).The data presented are means ⫾ S.E.M. expressed as a percentage of the control. N/A, not analyzable. To validate the technique, human preadipocytes were acutely stimulated with TNF-␣ (25 ng/ml, 1 h), and Western blot analysis was performed. A representative autoradiograph of 3 independent experiments is shown (A, right). treated for 24 h with TNF-␣ (25 ng/ml) alone or in cotreatment with SQV (10 M), lactacystin (0.5 M), or BAY 117082 (1 M), an inhibitor of IB phosphorylation, which is involved in the NF-B activation (Pierce et al., 1997). MMP-9 expression was analyzed by real-time RT-PCR. As shown in Fig. 6, TNF-␣ treatment strongly enhanced MMP-9 expression (10 times) in human preadipocytes. As expected, cotreatment with BAY 11-7082, the inhibitor of the NF-B pathway, reduced the MMP-9 expression induced by TNF-␣ (27% decrease). Similar results were obtained with SQV or lactacystin cotreatment, because MMP-9 expression was decreased by 48 and 22%, respectively, implicating NF-B as the link between proteasome activity and MMP-9 expression in our experiments. It should be noted that similar data were obtained when SQV was replaced by NFV (5 M) or when stimulation was performed with interleukin-1 (20 ng/ml) in place of TNF-␣ (data not shown). Compared with TNF-␣, which has been shown to involve preferentially IB␣, interleukin-1 is known to induce both IB␣ and IB degradation when activating the NF-B pathway (Thompson et al., 1995). 297 Fig. 6. Effect of acute SQV or lactacystin treatment on TNF-␣-induced MMP-9 expression in human preadipocytes. Stromal preadipocytes were isolated from human subcutaneous AT. After the 3-day priming period, cells were placed in an adipogenic medium for 24 h, with or without TNF-␣ (25 ng/ml) alone or in cotreatment with lactacystin (0.5 M), SQV (10 M), or BAY 11-7082 (1 M), an inhibitor of NF-B activation. Total RNAs were then extracted from cells and reverse-transcribed, and realtime RT-PCR analysis was performed using specific primers for MMP-9 cDNAs. The results were normalized to the levels of 18S rRNA. The presented data are means ⫾ S.E.M. expressed as a percentage of the TNF-␣ effect alone for three to four independent experiments. ⴱ, p ⬍ 0.05 versus TNF-␣ alone; ⴱⴱ, p ⬍ 0.01 versus TNF-␣ alone. Discussion We previously reported that HIV-PIs reduced the differentiation of human preadipocytes in primary culture. This effect was attributed to the HIV-PI-induced decrease of MMP-9 expression and secretion since we showed that blocking of MMP-9 activity by pharmacological agents led to the inhibition of human adipogenesis (Bourlier et al., 2005). In the present work, we report that HIV-PIs decreased the activity of the two major proteasome complexes, the 20S and the 26S proteasomes, in human preadipocytes. Interestingly, we showed that lactacystin, a proteasome inhibitor, mimicked the effects of HIV-PIs in reducing both human adipogenesis and MMP-9 expression and secretion. Finally, some of our results suggested that perturbations of the NF-B pathway are the link between the inhibition of proteasomal activity and the decrease in MMP-9 expression. Indeed, even if we were unable to detect NF-B p65 signal changes under basal conditions, we did observe that chronic treatments (10 days) with HIV-PIs (SQV and NFV) or lactacystin induced cellular IB accumulation. Furthermore, SQV or lactacystin reduced the expression of MMP-9 induced by acute treatment (24 h) with TNF-␣, a classic activator of NF-B. The inhibition of proteasomal activity and, more precisely, proteasome chymotrypsin-like activity by HIV-PIs was initially reported few years ago by André et al., (1998) and linked to a decrease of antigen presentation and T-cell response in infected mice. Here we show, for the first time, that proteasomes from human adipocyte precursors, which are major cell targets of HIV-PIs involved in the lipodystrophic syndrome, are also directly inhibited by several HIV-PIs at therapeutic concentrations. These data agree with recent observations made with the murine the 3T3-L1 cell line model of preadipocytes (Parker et al., 2005). As have other investigators, we found that the 20S proteasome was more 298 De Barros et al. sensitive to HIV-PIs than the 26S proteasome (Gaedicke et al., 2002; Pajonk et al., 2002). One reason may be the different tertiary structure between the 20S and 26S proteasomes, leading to better accessibility of the inhibitors to the proteolytic sites of the 20S proteasome (Piccinini et al., 2005, Voorhees and Orlowski, 2006). We found that all HIV-PIs did not have the same potency in inhibiting the chymotrypsinlike proteasome activity in our model. Indeed SQV and NFV were the most effective, followed by RTV, whereas IDV was without effect. Similar observations were made in the rare publications comparing the effect of HIV-PIs on human proteasomal activity measured on purified proteasome from erythrocytes (Piccinini et al., 2002, 2005; Parker et al., 2005). It has to be noted that even if all HIV-PIs were weaker inhibitors of proteasomal activity than the specific lactacystin inhibitors in our in vitro assay, SQV and NFV (not RTV nor IDV), can accumulate greatly into cells (20 to ⬎80 times) (Jones et al., 2001; Janneh et al., 2003). Thus, it can be expected that intracellular concentrations of these HIV-PIs are much higher that the ones tested here. Interestingly, SQV and NFV were the HIV-PIs with the major effect on the differentiation of human preadipocytes in our previous work (Bourlier et al., 2005). We thus investigated whether a blockade of proteasomal activity can affect human adipogenesis. We showed that chronic lactacystin treatment of preadipocytes in an adipogenic medium led to a decrease of the various differentiation markers studied (triglyceride content and aP2 and HSL expression). Although some authors have already implicated the proteasome in adipogenesis, their observations were on a different model, the murine 3T3-L1 cell line, using more or less specific proteasome inhibitors (calpain/proteasome), and contradictory results were obtained (Patel and Lane, 1999; Nguyen et al., 2000; Prince et al., 2002). As expected and in association with the reduction of adipogenesis, we found that lactacystin treatment, as that with HIV-PIs, selectively decreased MMP-9 expression and activity released into the culture medium by preadipocytes. The reduction of MMP-9 activity per se may be responsible for the antiadipogenic effect of lactacystin since we have previously demonstrated that treatment of human preadipocytes with pharmacological inhibitors of MMP-9 activity decreased their differentiation (Bourlier et al., 2005). However we cannot exclude any other additional phenomenon implicated in adipogenesis that might be disturbed by proteasome inhibitor treatment. Reduction of MMP-9 secretion with proteasome inhibitors has previously been reported for distinct cellular types in vitro involving NF-B pathway perturbations (Ikebe et al., 1998; Kolev et al., 2003; Lu and Wahl, 2005). We were not able to find any modification in the activity and repartition of NF-B p65 within the cytosol and the nucleus in association with chronic SQV or lactacystin treatment in our model, using two different techniques (enzyme-linked immunosorbent assay-based TransAM NF-B assay kit and Western blot). This may be partly explained by the fact that in the resting conditions that we studied, the part of active NF-B p65 was too weak to be detected. This hypothesis is in agreement with one of the rare published reports on the subject showing that NF-B p65 is mostly cytosolic in unstimulated human preadipocytes (Chung et al., 2005). Nevertheless, we showed that the same chronic treatment with NFV, SQV, or lactacystin (but not with IDV nor RTV) led to intracellular accumulation of IB protein. In contrast, none of the HIVPIs or lactacystin was effective in modifying the IB␣ protein level. These results agree with the presumed roles of these two members of the same family because 1) IB␣ has been correlated to transient activation of NF-B and IB to persistent activation that yields a more permanent change (Thompson et al., 1995) and 2) IB, but not IB␣, has been shown to function as a classic cytoplasmic inhibitor of NF-B dimers in resting cells (Malek et al., 2001). Because both NF-B inhibitors have been shown to be substrates of the proteasome (Weil et al., 1997) and because no parallel increase in IB mRNA expression was observed under our conditions, the increase in IB protein most probably reflects the reduction of its degradation resulting from proteasomal activity inhibition induced by the treatments. Furthermore, a different set of experiments conducted with the classic NF-B pathway activator TNF-␣ (Viatour et al., 2005) showed that MMP-9 expression was up-regulated within 24 h of treatment in our model, but also that this up-regulation could be reduced either by SQV, lactacystin, or the NF-B inhibitor, Bay 11-7082. Overall, according to these data on resting and TNF-␣-stimulated human preadipocytes, we can easily imagine that the decrease in MMP-9 expression observed with lactacystin and some HIV-PIs (SQV and NFV) arose in part from perturbations in the NF-B pathway. To our knowledge, this is the first investigation showing that HIV-PIs are potent inhibitors of human preadipocyte proteasomal activity and that chronic low-level proteasome inhibition reduces human adipogenesis. Disorders of the NF-B pathway, resulting from proteasome inhibition may partly explain the decrease in MMP-9 expression and secretion potentially responsible for adipogenesis reduction (Bourlier et al., 2005) and observed with both lactacystin and HIV-PI treatment. Our in vitro results suggest that HIV-PIinduced perturbation of preadipocyte to adipocyte balance noted in clinical studies (Bastard et al., 2002; Lloreta et al., 2002) may also target preadipocyte proteasome function. Interestingly, a role for the proteasome in more metabolic aspects of the HIV-related lipodystrophic syndrome has previously been reported. Indeed, apolipoprotein B and sterol regulatory element binding protein degradation have been shown to be altered by HIV-PI-related proteasome inhibition and involved in lipid metabolism disorders (Liang et al., 2001; Hui, 2003). More recently, Parker et al. (2005) has linked the reduction of proteasomal activity induced by HIVPIs and the dyslipidemia to endoplasmic reticulum stress. Finally, attention is now being focused on HIV-PI-induced proteasomal alterations and disturbances of glucose metabolism because proteasome dysfunction and/or endoplasmic reticulum stress has been closely related to insulin resistance (Ozcan et al., 2004; Rome et al., 2004). All of this information will help to better understand the etiology of the lipodystrophic syndrome but may also be of great interest for the recent clinical use of proteasome inhibitors in cancer therapy (i.e., bortezomib treatment for multiple myeloma) and possible effects on adipose tissue development. Acknowledgments We thank Drs. Bénarous, Belhaouri, and Jougla for help in obtaining the adipose tissue samples. We also thank Dr. Sorisky for critical review of this article. Proteasome Inhibition Reduces Human Adipogenesis References Adams J (2004) The development of proteasome inhibitors as cancer drugs. Cancer Cell 5:417– 421. André P, Groettrup M, Klenerman P, Giuli R, Booth BL Jr, Cerundolo V, Bonneville M, Jotereau F, Zinkernagel RM, and Lotteau V (1998) An inhibitor of HIV-1 protease modulates proteasome activity, antigen presentation, and T cell responses. Proc Natl Acad Sci USA 95:13120 –13124. Bastard JP, Caron M, Vidal H, Jan V, Auclair M, Vigouroux C, Luboinski J, Laville M, Maachi M, Girard PM, et al. (2002) Association between altered expression of adipogenic factor SREBP1 in lipoatrophic adipose tissue from HIV-1-infected patients and abnormal adipocyte differentiation and insulin resistance. Lancet 359:1026 –1031. Berg AH, Lin Y, Lisanti MP, and Scherer PE (2004) Adipocyte differentiation induces dynamic changes in NF-B expression and activity. Am J Physiol 287: E1178 –E1188. Bouloumié A, Sengenes C, Portolan G, Galitzky J, and Lafontan M (2001) Adipocyte produces matrix metalloproteinases 2 and 9: involvement in adipose differentiation. Diabetes 50:2080 –2086. Bourlier V, Zakaroff-Girard A, De Barros S, Pizzacalla C, Durand de Saint Front V, Lafontan M, Bouloumie A, and Galitzky J (2005) Protease inhibitor treatments reveal specific involvement of matrix metalloproteinase-9 in human adipocyte differentiation. J Pharmacol Exp Ther 312:1272–1279. Chung S, Brown JM, Provo JN, Hopkins R, and McIntosh MK (2005) Conjugated linoleic acid promotes human adipocyte insulin resistance through NFBdependent cytokine production. J Biol Chem 280:38445–38456. Cressman DE and Taub R (1994) Physiologic turnover of nuclear factor B by nuclear proteolysis. J Biol Chem 269:26594 –26597. Gaedicke S, Firat-Geier E, Constantiniu O, Lucchiari-Hartz M, Freudenberg M, Galanos C, and Niedermann G (2002) Antitumor effect of the human immunodeficiency virus protease inhibitor ritonavir: induction of tumor-cell apoptosis associated with perturbation of proteasomal proteolysis. Cancer Res 62:6901– 6908. Hayden MS and Ghosh S (2004) Signaling to NF-B. Genes Dev 18:2195–2224. Hui DY (2003) Effects of HIV protease inhibitor therapy on lipid metabolism. Prog Lipid Res 42:81–92. Ikebe T, Takeuchi H, Jimi E, Beppu M, Shinohara M, and Shirasuna K (1998) Involvement of proteasomes in migration and matrix metalloproteinase-9 production of oral squamous cell carcinoma. Int J Cancer 77:578 –585. Janneh O, Hoggard PG, Tjia JF, Jones SP, Khoo SH, Maher B, Back DJ, and Pirmohamed M (2003) Intracellular disposition and metabolic effects of zidovudine, stavudine and four protease inhibitors in cultured adipocytes. Antiviral Ther 8:417– 426. Jones K, Hoggard PG, Sales SD, Khoo S, Davey R, and Back DJ (2001) Differences in the intracellular accumulation of HIV protease inhibitors in vitro and the effect of active transport. AIDS 15:675– 681. Kisselev AF and Goldberg AL (2001) Proteasome inhibitors: from research tools to drug candidates. Chem Biol 8:739 –758. Kolev K, Skopal J, Simon L, Csonka E, Machovich R, and Nagy Z (2003) Matrix metalloproteinase-9 expression in post-hypoxic human brain capillary endothelial cells: H2O2 as a trigger and NF-B as a signal transducer. Thromb Haemost 90:528 –537. Liang JS, Distler O, Cooper DA, Jamil H, Deckelbaum RJ, Ginsberg HN, and Sturley SL (2001) HIV protease inhibitors protect apolipoprotein B from degradation by the proteasome: a potential mechanism for protease inhibitor-induced hyperlipidemia. Nat Med 7:1327–1331. Lloreta J, Domingo P, Pujol RM, Arroyo JA, Baixeras N, Matias-Guiu X, Gilaberte M, Sambeat MA, and Serrano S (2002) Ultrastructural features of highly active antiretroviral therapy-associated partial lipodystrophy. Virchows Arch Medicine 441:599 – 604. Lu Y and Wahl LM (2005) Production of matrix metalloproteinase-9 by activated human monocytes involves a phosphatidylinositol-3 kinase/Akt/IKK␣/NF-B pathway. J Leukoc Biol 78:259 –265. Malek S, Chen Y, Huxford T, and Ghosh G (2001) IB, but not IB␣, functions as a classical cytoplasmic inhibitor of NF-B dimers by masking both NF-B nuclear localization sequences in resting cells. J Biol Chem 276:45225– 45235. 299 Nguyen AT, Gagnon A, Angel JB, and Sorisky A (2000) Ritonavir increases the level of active ADD-1/SREBP-1 protein during adipogenesis. AIDS 14:2467–2473. Ozcan U, Cao Q, Yilmaz E, Lee AH, Iwakoshi NN, Ozdelen E, Tuncman G, Gorgun C, Glimcher LH, and Hotamisligil GS (2004) Endoplasmic reticulum stress links obesity, insulin action, and type 2 diabetes. Science (Wash DC) 306:457– 461. Pajonk F, Himmelsbach J, Riess K, Sommer A, and McBride WH (2002) The human immunodeficiency virus (HIV)-1 protease inhibitor saquinavir inhibits proteasome function and causes apoptosis and radiosensitization in non-HIV-associated human cancer cells. Cancer Res 62:5230 –5235. Parker RA, Flint OP, Mulvey R, Elosua C, Wang F, Fenderson W, Wang S, Yang WP, and Noor MA (2005) Endoplasmic reticulum stress links dyslipidemia to inhibition of proteasome activity and glucose transport by HIV protease inhibitors. Mol Pharmacol 67:1909 –1919. Patel YM and Lane MD (1999) Role of calpain in adipocyte differentiation. Proc Natl Acad Sci USA 96:1279 –1284. Piccinini M, Rinaudo MT, Anselmino A, Buccinna B, Ramondetti C, Dematteis A, Ricotti E, Palmisano L, Mostert M, and Tovo PA (2005) The HIV protease inhibitors nelfinavir and saquinavir, but not a variety of HIV reverse transcriptase inhibitors, adversely affect human proteasome function. Antivir Ther 10:215–223. Piccinini M, Rinaudo MT, Chiapello N, Ricotti E, Baldovino S, Mostert M, and Tovo PA (2002) The human 26S proteasome is a target of antiretroviral agents. AIDS 16:693–700. Pierce JW, Schoenleber R, Jesmok G, Best J, Moore SA, Collins T, and Gerritsen ME (1997) Novel inhibitors of cytokine-induced IB␣ phosphorylation and endothelial cell adhesion molecule expression show anti-inflammatory effects in vivo. J Biol Chem 272:21096 –21103. Prince AM, May JS, Burton GR, Lyle RE, and McGehee RE Jr (2002) Proteasomal degradation of retinoblastoma-related p130 during adipocyte differentiation. Biochem Biophys Res Commun 290:1066 –1071. Rock KL, Gramm C, Rothstein L, Clark K, Stein R, Dick L, Hwang D, and Goldberg AL (1994) Inhibitors of the proteasome block the degradation of most cell proteins and the generation of peptides presented on MHC class I molecules. Cell 78:761– 771. Rome S, Meugnier E, and Vidal H (2004) The ubiquitin-proteasome pathway is a new partner for the control of insulin signaling. Curr Opin Clin Nutr Metab Care 7:249 –254. Rudich A, Ben-Romano R, Etzion S, and Bashan N (2005) Cellular mechanisms of insulin resistance, lipodystrophy and atherosclerosis induced by HIV protease inhibitors. Acta Physiol Scand 183:75– 88. St-Pierre Y, Couillard J, and Van Themsche C (2004) Regulation of MMP-9 gene expression for the development of novel molecular targets against cancer and inflammatory diseases. Expert Opin Ther Targets 8:473– 489. Sato H and Seiki M (1993) Regulatory mechanism of 92 kDa type IV collagenase gene expression which is associated with invasiveness of tumor cells. Oncogene 8:395– 405. Schmidtke G, Holzhütter HG, Bogyo M, Kairies N, Groll M, de Giuli R, Emch S, and Groettrup M (1999) How an inhibitor of the HIV-I protease modulates proteasome activity. J Biol Chem 274:35734 –35740. Thompson JE, Phillips RJ, Erdjument-Bromage H, Tempst P, and Ghosh S (1995) IB- regulates the persistent response in a biphasic activation of NF-B. Cell 80:573–582. Viatour P, Merville MP, Bours V, and Chariot A (2005) Phosphorylation of NF-B and IB proteins: implications in cancer and inflammation. Trends Biochem Sci 30:43–52. Voorhees PM and Orlowski RZ (2006) The proteasome and proteasome inhibitors in cancer therapy. Annu Rev Pharmacol Toxicol 46:189 –213. Weil R, Laurent-Winter C, and Israel A (1997) Regulation of IB degradation: similarities to and differences from IB␣. J Biol Chem 272:9942–9949. Whiteside ST and Israël A (1997) IB proteins: structure, function and regulation. Semin Cancer Biol 8:75– 82. Address correspondence to: Dr. Virginie Bourlier, INSERM U586, 37 Allées Jules Guesde, 31000 Toulouse, France. E-mail: [email protected] Discussion de la publication 2 Dans cette étude, nous avons voulu déterminer les mécanismes impliqués dans la diminution de l’expression de MMP-9 par les IPs-VIH. Nous avons tout d’abord évalué l’effet des IPs-VIH sur l’activité du protéasome des cellules de la FSV du TA humain. L’activité chymotrypsine des deux formes majeures du protéasome, le protéasome 20S qui constitue la partie multicatalytique de tous les protéasomes et le protéasome 26S constitué du protéasome 20S coiffé par deux sous-unités régulatrices 19S a été déterminée sur des extraits protéiques de cellules de la FSV non différenciées. Nous avons observé que le SQV, le NFV et le RTV diminuent l’activité du protéasome 20S et dans une moindre mesure celle du protéasome 26S. Cette différence de sensibilité entre les activités des protéasomes 20S et le 26S a déjà été rapportée (84, 200) et pourrait s’expliquer par un problème d’accessibilité des IPs-VIH aux sites catalytiques situés sur le protéasome 20S quand celui-ci est coiffé par les sous-unités 19S c’est-à-dire sous une forme 26S (208, 279). Il est important de préciser que l’inhibition de l’activité protéasomique observée par les IPs-VIH est très inférieure à celle observée avec un inhibiteur spécifique du protéasome, la lactacystine. De plus, les concentrations des IPs-VIH effectives sur l’inhibition du protéasome d’extraits protéiques des cellules de la FSV sont plus élevées que celles requises pour l’inhibition de la différenciation adipocytaire in vitro. Toutefois, les IPs-VIH tels que le SQV et le NFV ont été décrits comme s’accumulant dans le cytoplasme cellulaire conduisant à une augmentation de la concentration intracellulaire de 20 à 80 fois (111, 117, 273, 274). Afin de déterminer si l’inhibition du protéasome affecte le processus de différenciation adipocytaire, les cellules de la FSV du TA humain ont été traitées avec la lactacystine. Après 10 jours de traitement, nous avons observé une diminution de l’adipogenèse associée à une baisse de la sécrétion et de l’expression de MMP-9, sans atteinte de MMP-2. Récemment, en accord avec nos résultats, les travaux de Li et al. ont montré que la lactacystine inhibe également la différenciation des préadipocytes murins de la lignée 3T3L1 (146). L’ensemble de ces données suggère que le protéasome joue un rôle majeur dans l’adipogenèse des cellules de la FSV ainsi que dans le contrôle de l’expression génique de MMP-9. Il est tentant de spéculer que l’un des mécanismes impliqués dans l’effet antiadipogénique de la lactacystine est lié à une inhibition de l’activité de MMP-9. Toutefois, d’autres voies peuvent être impliquées. Ainsi, il a été décrit que l’inhibition du protéasome des préadipocytes murins entraîne une augmentation de CHOP-10, un facteur de transcription anti-adipogénique (146). Les mécanismes impliqués dans cet effet sont encore inconnus. 63 Nous avons ensuite recherché des éventuelles perturbations de la voie NF-κB. Dans un premier temps, nous nous sommes intéressés à IκB et avons observé, par des analyses de western blot, une augmentation de la protéine IκBβ dans les préadipocytes humains traités avec le SQV et le NFV pendant 10 jours suggérant une diminution de sa dégradation via le protéasome. Dans un second temps, nous avons souhaité mettre en évidence un effet direct des IPs-VIH sur le facteur de transcription NF-κB. Cependant, malgré plusieurs tentatives, aucun effet direct des IPs-VIH et de la lactacystine sur l’activité et la localisation cellulaire (cytoplasmique ou nucléaire) de NF-κB n’a pu être mis en évidence. Ces résultats pourraient s’expliquer par le fait que nous avons travaillé dans des conditions basales c’est-à-dire non stimulées. Nous avons donc stimulé les cellules de la FSV avec un activateur connu de la voie NF-κB, le TNF-α. Comme attendu, suite à un traitement aigu avec le TNF- α, l’expression de MMP-9 est fortement augmentée et lors d’un co-traitement avec la lactacystine et les IPs-VIH tels que le SQV et le NFV, cette réponse est diminuée. Si l’on considère ces différents résultats sur les préadipocytes humains en conditions basales et stimulées, on peut penser que la chute de l’expression de MMP-9 induite par les IPs-VIH et la lactacystine est en partie due à des perturbations de la voie NF-κB. Nos résultats obtenus in vitro suggèrent donc que les IPs-VIH participent à l’atrophie du TA en inhibant l’activité du protéasome des cellules de la FSV du TA humain. De manière intéressante, l’inhibition du protéasome par les IPs-VIH a également été associée aux complications métaboliques décrites dans les lipoatrophies induites par les IPs-VIH telles que l’insulino-résistance et les désordres dans le métabolisme lipidique. Ainsi, compte tenu de l’ensemble de ces données, il est nécessaire de rester vigilant quant aux effets indésirables potentiels des inhibiteurs du protéasome dont l’un d’entre eux, le bortezomib est à ce jour utilisé pour le traitement du cancer. En résumé de cette première partie, nos résultats montrent que les MMPs et particulièrement la MMP-9 est un acteur majeur dans la différenciation adipocytaire des cellules de la FSV du TA humain. De plus, MMP-9 semble être une cible potentielle des IPsVIH. En effet, l’expression génique et la sécrétion de cette MMP est diminuée par les IPsVIH. Les mécanismes impliqués dans cet effet ont été déterminés et passent en partie par une inhibition de l’activité protéasomique des cellules de la FSV par les IPs-VIH, entraînant des perturbations de la voie NF-κB, facteur de transcription impliqué dans l’expression génique de MMP-9. La MMP-9 joue donc un rôle majeur dans le processus de différenciation adipocytaire chez l’homme. 64 En perspective à ce travail, les cibles moléculaires de MMP-9 responsables de l’effet modulateur de la différenciation adipocytaire restent à définir. Nos études préliminaires ainsi que les perspectives envisagées dans cet axe vont être brièvement présentées dans le paragraphe qui suit. D) Etudes préliminaires et perspectives sur l’étude des cibles moléculaires de MMP-9 Comme nous l’avons évoqué l’effet des MMPs s’exerce via leurs actions sur les composants de la MEC mais aussi via leurs actions sur des facteurs solubles activables par ces MMPs et/ou des facteurs piégés dans la MEC. Afin de déterminer si l’action de MMP-9 passe par la dégradation des composants matriciels, nous avons d’abord évalué l’influence de différents supports matriciels tels que des supports de collagène, fibronectine et gélatine, connus pour être des substrats de la MMP9 (57, 254), sur l’adipogenèse des cellules de la FSV du TA humain. Pour cela, des cellules de la FSV du TA ont été ensemencées (60 000 cellules/cm2) sur ces différents supports et mises en conditions adipogéniques. Après 10 jours de culture, le contenu intracellulaire en TGs a été quantifié. Comme on peut l’observer dans la figure 16, aucun des supports matriciels testés n’affecte l’accumulation lipidique des préadipocytes humains, un résultat ne suggérant aucune altération de leur adipogenèse. Ces données sont en accord avec d’autres travaux soulignant l’absence d’effet d’un support de collagène (191) et de fibronectine (95) sur l’adipogenèse des cellules de la FSV de TA humains et porcins, respectivement. A l’inverse, d’autres travaux ont rapporté un effet anti-différenciant d’un support de fibronectine sur des préadipocytes d’origine murine et humaine (98, 191, 260). Les différences observées dans ces études sont surprenantes et pourraient s’expliquer par le modèle cellulaire et/ou les conditions de culture utilisées. On note qu’un support de laminine décrit pour activer l’adipogenèse des préadipocytes porcins (95) a également été testé mais ce support n’a pas permis l’adhérence des cellules de la FSV du TA humain. Ainsi, ces résultats ne révélant aucun effet du support matriciel sur l’adipogenèse, il est tentant de suggérer que l’activité de MMP-9 n’est pas due à la dégradation de la MEC. Il faut cependant rester prudent car il est fort possible que l’action de MMP-9 passe par la dégradation d’une MEC sécrétée par la cellule, elle-même, et non pas par celle déposée au préalable sur un support. De plus, il est possible que le modèle de culture en 2 dimensions utilisé pour nos cellules ne permette pas d’observer un effet du support 65 Contenu en triglycéride (mg/mg d'ADN) 125 100 75 50 25 G él at in e tin e on ec Fi br gè ne lla Co Pl as tiq ue 0 Figure 16 : Influence d’un substrat matriciel sur la différenciation adipocytaire des cellules de la FSV du tissu adipeux humain Les cellules de la FSV sont cultivées sur un support plastique ou coaté avec du collagène de type IV, de la fibronectine, ou de la gélatine en conditions adipogéniques. A 10 jours de différenciation, le contenu intracellulaire en TGs normalisé à la quantité d’ADN a été évalué pour 4 expériences indépendantes. Les résultats sont exprimés en % du contrôle sur support plastique. matriciel. L’influence de différents supports matriciels dans un modèle de culture en 3 dimensions est à envisager. En effet, une étude récente montre que des effets de la MT1MMP ne sont révélés que sur un modèle de culture en 3 dimensions (44). En parallèle, il serait très intéressant de caractériser les principaux composants matriciels sécrétés par les cellules de la FSV du TA humain en cours de différenciation traitées ou non avec un inhibiteur de MMP-9. Une telle étude permettrait non seulement de déterminer l’évolution de la MEC au cours de l’adipogenèse chez l’homme mais aussi de définir les effets de cette métalloprotéase sur les composants matriciels. De plus, MMP-9 étant connu pour générer des fragments matriciels biologiquement actifs tels que l’endostatine (77) et certains peptides dérivés de la fibronectine (82), un traitement des cellules de la FSV du TA humain par des fragments matriciels pourraient être envisagé. En effet, les travaux de Kamiya et al. montrent qu’un fragment issu de la dégradation de la fibronectine stimule la différenciation des préadipocytes de la lignée ST-13 (119). Enfin, la recherche des cibles non matricielles susceptibles de moduler et réguler le comportement cellulaire pourrait également être envisagée. De nombreuses protéines cellulaires de surface, péri-cellulaires ou circulantes peuvent être clivées par les MMPs régulant ainsi leur biodisponibilité. Cependant, peu de données existent chez l’homme. Il nous semblerait donc intéressant de caractériser notamment la production des facteurs de croissance et/ou cytokines par les cellules de la FSV du TA humain au cours de la différenciation. Cette approche pourrait être réalisée grâce à l'utilisation de la technique des immunoarrays dédiés aux « cytokines » qui permet d’identifier et de quantifier, dans un milieu de culture ou dans un lysat cellulaire, des protéines différentes décrites comme étant des cibles de MMP-9 dans d’autres modèles cellulaires et dont les effets sur la différenciation cellulaire ont été également mis en évidence telles que les TGFs, TNFs, ILs, IGF-I, IGFBPs. En parallèle, l’influence d’un traitement avec un inhibiteur de MMP-9 pourra être évaluée et ce, afin de mettre en évidence les facteurs de croissance et/ou cytokines dont le taux extracellulaire est modifié par la présence de MMP-9 soit par leur clivage direct soit par leur libération de la MEC. Pour conclure, l’étude des cibles moléculaires de MMP-9 constitue donc un axe de recherche dont le développement pourrait permettre de mieux comprendre les effets de la MMP-9. Cependant, les cellules de la FSV étant une population cellulaire hétérogène, on peut se demander quels types cellulaires sont les cibles de MMP-9. Récemment, des travaux de notre groupe ont permis d’isoler et de caractériser la population cellulaire contenant les 66 précurseurs adipocytaires (241). Dans la suite de ce travail, nous avons déterminé si l’effet de la MMP-9 est retrouvé dans ces précurseurs adipocytaires spécifiquement isolés. 67 II- Implication des MMPs dans la différenciation des cellules progénitrices CD34+/CD31- isolées de la fraction stroma-vasculaire du tissu adipeux humain La caractérisation et l’isolement de la population cellulaire contenant les précurseurs adipocytaires a été possible grâce au développement d’une technique d’isolement des différentes populations cellulaires de la FSV qui se fonde sur l’utilisation de nanoparticules magnétiques couplées à des anticorps dirigés spécifiquement contre les marqueurs de surface CD34 (marqueur des cellules souches hématopoïétiques et des cellules endothéliales capillaires), CD31 (marqueur des cellules endothéliales et de la lignée hématopoïétique) et CD14 (marqueur des monocytes/macrophages) (figure 17). La fraction cellulaire CD34+/CD31- est la seule à exprimer les marqueurs de différenciation spécifiques des adipocytes et à acquérir les activités métaboliques adipocytaires, en réponse aux conditions adipogéniques (241). Notre groupe a également mis en évidence que ces cellules CD34+/CD31-, cultivées en condition de culture endothéliales, changent de morphologie et d’organisation et expriment des marqueurs spécifiques des cellules endothéliales tels que le CD31 et le facteur de Von Willebrand (vWF). De plus, leur injection dans la patte ischémiée d’une souris athymique entraîne une augmentation du flux sanguin et de la densité capillaire au niveau du membre ischémié (173). D’autres laboratoires ont rapporté des capacités pro-angiogéniques similaires des cellules issues de la FSV du TA (211, 221, 291). Par conséquent, la fraction cellulaire CD34+/CD31- pourrait constituer un pool local de cellules progénitrices/souches qui serait impliqué dans la formation non seulement des nouveaux adipocytes mais aussi des capillaires accompagnant le développement de la masse grasse. Les mécanismes impliqués dans le contrôle du devenir des cellules progénitrices CD34+/CD31- restent à déterminer. Il a été rapporté que le microenvironnement pouvait réguler le devenir des cellules souches hématopoïétiques et mésenchymateuses (127, 229). En effet, de nombreux facteurs solubles (cytokines et facteurs de croissance) ainsi que la composition et l’élasticité de la MEC contrôlent le devenir des cellules souches (14, 69, 71, 172). De plus, une récente publication indique que l’engagement des cellules souches mésenchymateuses vers le lignage adipogénique et ostéogénique est régulé par la densité cellulaire d’ensemencement qui altère la forme de la cellule et module les interactions cellulaires (167). Dans la deuxième partie de ce travail de thèse, nous avons d’abord vérifié et confirmé l’implication des MMPs dans la différenciation adipocytaire des cellules CD34+/CD3168 Tissu adipeux humain Digestion à la collagénase Adipocytes matures Fraction stroma-vasculaire (FSV) Billes anti-CD34 CD34+ CD34Billes anti-CD14 Billes anti-CD31 Cellules endothéliales Cellules progénitices CD34+/CD31+ CD34+/CD31- Macrophages CD34-/CD14+ CD34-/CD14- Figure 17 : Technique d’isolement des différentes populations de la FSV du tissu adipeux humain spécifiquement isolées. Suite à cet ensemble de résultats sur les cellules CD34+/CD31-, nous nous sommes ensuite demandés si l’effet anti-adipogénique observé avec des inhibiteurs de l’activité et/ou de l’expression des MMPs, particulièrement MMP-9, modulait également les autres capacités de ces cellules dont la capacité angiogénique. Ainsi, afin d’étudier les mécanismes qui contrôlent le devenir des cellules CD34+/CD31- nous avons mis au point une condition de culture permettant l’étude simultanée de l’adipogenèse et de l’angiogenèse. A) Influence d’un inhibiteur des MMPs sur la différenciation adipocytaire des cellules CD34+/CD31Nous avons isolé puis cultivé les cellules CD34+/CD31- dans des conditions adipogéniques similaires à celles décrites dans la première partie de ce travail. L’activité gélatinase des MMP-2 et -9 relarguée dans le milieu de culture au cours de la différenciation a tout d’abord été évaluée par la technique de zymographie à la gélatine comme décrite dans les précédentes publications. Comme le montre la figure 18, la sécrétion des MMP-2 et -9 par les cellules CD34+/CD31- augmente au cours de la différenciation adipocytaire des cellules CD34+/CD31- isolées. Ces données indiquent que la production de MMP-2 et -9 est strictement modulée par la différenciation adipocytaire et ne peut être attribuée à la modulation de la présence ou de l’état d’activation des autres types cellulaires (macrophages, cellules endothéliales) de la FSV. L’implication des MMPs dans la différenciation adipocytaire des cellules CD34+/CD31- a ensuite été déterminée. Pour cela et de manière similaire à la FSV, les cellules CD34+/CD31- ont été traitées avec un inhibiteur des MMPs à large spectre, le batimastat. Après 10 jours de traitement, une diminution de l’accumulation des gouttelettes lipidiques a été observée et confirmée par le dosage du contenu intracellulaire en TGs (figure 19). Ces données sont en accord avec celles obtenues sur les cellules de la FSV. Elles suggèrent un rôle majeur des MMPs dans le processus de différenciation adipocytaire des cellules progénitrices CD34+/CD31- isolées. Cependant, une étude complète serait nécessaire afin de préciser les effets du batimastat sur l’expression de gènes marqueurs de la différenciation adipocytaire (gènes précoces tels qu’aP2 et PPARγ et gènes tardifs tels que la LHS et FAS). 69 J0 J10 Standard MMP-9 MMP-2 Figure 18 : Sécrétion des MMP-2 et -9 au cours de la différenciation adipocytaire des cellules progénitrices CD34+/CD31- isolées Après avoir été isolées de la FSV, les cellules CD34+/CD31- sont cultivées en conditions adipogéniques. L’activité gélatinase des MMP-2 et -9 relarguée dans le milieu de culture à 0 (J0) et 10 (J10) jours de différenciation est évaluée par zymographie à la gélatine. L’utilisation d’un standard MMPs nous a permis de détecter les bandes spécifiques de MMP-2 et -9 actives. Le gel présenté est représentatif de 2 expériences indépendantes. B A Contrôle Contenu en triglycéride (en % du controle) 100 75 * 50 25 0 Contrôle Batimastat (5 µM) Batimastat (5 µM) Figure 19 : Influence du batimastat sur la différenciation adipocytaire des cellules progénitrices CD34+/CD31Après avoir été isolées de la FSV, les cellules CD34+/CD31- sont cultivées en conditions adipogéniques traitées ou non avec le batimastat pendant 10 jours. Une photographie représentative de 4 expériences indépendantes est présentée ainsi que la quantification du contenu intracellulaire en TGs normalisé à la quantité d’ADN. Les résultats sont exprimés en % du contrôle. * P<0.05 vs contrôle Des travaux de notre groupe ayant démontré que les cellules progénitrices CD34+/CD31- sont également capables d’angiogenèse dans des conditions de culture endothéliales (173), il nous a semblé intéressant de déterminer si l’effet anti-adipogénique observé avec le batimastat pouvait correspondre à une réorientation des cellules CD34+/CD31- vers le lignage endothélial et/ou à une simple inhibition de la différenciation adipocytaire. Ainsi, afin de déterminer les mécanismes impliqués dans le devenir des cellules progénitrices CD34+/CD31-, nous avons mis au point une condition de culture permettant l’étude simultanée des capacités adipogéniques et angiogéniques. B) Mise au point d’une condition de culture permettant simultanément les capacités adipogéniques et angiogéniques des cellules CD34+/CD31- B.1) Etude de l’accumulation intracellulaire des triglycérides et de la formation d’un réseau cellulaire positif pour le CD31 par les cellules CD34+/CD31- cultivées dans un milieu mixte Des cellules progénitrices CD34+/CD31- ont été ensemencées (120 000 cellules/cm2) dans un milieu de type ECBM (endothelial cell basal medium) supplémenté avec 10% de sérum de veau foetal et dans des puits coatés avec de la fibronectine (5 µg/cm2) afin de favoriser l’angiogenèse. Après 24 heures, les cellules ont été mises en présence d’un milieu adipogénique, endothélial ou d’un milieu mixte correspondant à une combinaison des milieux adipogéniques et endothéliaux. La composition de ces trois milieux est présentée dans le tableau 11. Notons que dans cette étude, étant donné les effets apoptotiques de la ciglitazone sur les cellules endothéliales (165), cet agoniste PPARγ a été remplacé par la rosiglitazone décrite à l’inverse comme pro-angiogénique (209, 282). Après 10 jours de culture, les cellules CD34+/CD31- cultivées en milieu adipogénique et mixte montrent un phénotype adipocytaire caractérisé par l’accumulation de gouttelettes lipidiques (figure 20A). Comme on peut le voir sur la figure 20B, une forte augmentation du contenu intracellulaire en TG est observée au cours de la différenciation des cellules CD34+/CD31- cultivées en milieu adipogénique et mixte. Cependant, aucune différence dans le contenu intracellulaire en TG n’est observée si l’on compare le milieu adipogénique versus le milieu mixte. En effet, le pourcentage de cellules différenciées en adipocytes est similaire dans les milieux adipogénique et mixte (66.4 ± 4.4 % et 70.1 ± 1.5 %, respectivement). En revanche, après 10 jours de culture en milieu endothélial, les cellules CD34+/CD31- ne stockent pas de lipides. 70 A J0 C 50 ** 40 30 * 20 10 0 Endothéliale J0 Adipo Endo J10 Mixte Longueur du réseau positif pour le CD31 (U.A.) Contenu en triglycérides (mg/mg d'ADN) B Adipogénique Mixte 150 ** 125 100 £ ** 75 50 25 0 J0 Adipo Endo Mixte J10 Figure 20 : Détermination de l’accumulation des TGs et de la formation d’un réseau cellulaire positif pour le CD31 des cellules CD34+/CD31- cultivées en milieu adipogénique, endothélial ou mixte Les cellules CD34+/CD31- sont ensemencées à 120 000 cellules/cm2 et cultivées en milieu adipogénique (Adipo), endothélial (Endo) ou mixte. Après 10 jours, les cellules sont fixées et marquées au Red Oil, au Hoechst (un colorant nucléaire) et avec un anticorps dirigé contre le CD31. Des photographies représentatives de 4 à 11 expériences indépendantes sont présentées. (A). Le contenu intracellulaire en TGs (B) ainsi que la longueur du réseau cellulaire pour le CD31 (C) ont été évalués. Les valeurs sont exprimées en mg/mg d’ADN pour le contenu en TGs et la longueur du réseau cellulaire pour le CD31 en unité arbitraires normalisées à la quantité d’ADN. ** P<0.001 et * P<0.01 vs J0 et £ P<0.001 vs Endo Tableau 11: Composition des milieux adipogénique, endothélial et mixte utilisés Milieu adipogénique Milieu endothélial Milieu mixte ECBM ECGM ECGM Insuline (66 nmol/L) VEGF (0.5 ng/mL) Insuline (66 nmol/L) T3 (1 nmol/L) IGF-1 (20 ng/mL) T3 (1 nmol/L) Cortisol (100 nmol/L) Transferrine (10 µg/mL) Transferrine (10 µg/mL) Rosiglitazone (3 µmol/L) Rosiglitazone (3 µmol/L) VEGF (0.5 ng/mL) IGF-1 (20 ng/mL) (ECBM: endothelial cell basal medium, ECGM: endothelial cell growth medium constitué d’un milieu de type ECBM supplémenté avec des facteurs de croissance tels que l’EGF (0.1 ng/ml), le bFGF (1 ng/ml) et l’hydrocortisone (1 µg/ml)) et 2 % de sérum de veau foetal) En parallèle, des analyses d’immnunohistochimie ont permis d’évaluer l’apparition d’un marquage spécifique pour le CD31, un marqueur des cellules endothéliales (pour les méthodes voir (173)). Comme on peut l’observer dans les figures 20A et C, la culture des cellules CD34+/CD31- en milieu endothélial et mixte entraîne la formation d’un réseau cellulaire positif pour le CD31. Cependant, en milieu mixte, la longueur du réseau cellulaire positif pour le CD31 est plus faible qu’en milieu endothélial suggérant une perte du potentiel angiogénique en milieu mixte. En effet, le pourcentage de cellules positives pour le CD31 est plus faible en milieu mixte comparé au milieu endothélial (14.4 ± 1.1 % et 19.1 ± 2.4 % en milieu mixte et endothélial, respectivement, P<0.05, milieu endothélial vs mixte). En revanche, la culture des cellules CD34+/CD31- en milieu adipogénique n’entraîne pas la formation d’un réseau positif pour le CD31. Il est important de préciser que le milieu mixte comme le milieu endothélial est constitué d’un milieu de base de type ECGM qui contient des facteurs de croissance et 2% de sérum de veau foetal. Ainsi, les cellules CD34+/CD31montrent une prolifération en milieu mixte et endothélial mais pas en milieu adipogénique. Cette donnée est mise en évidence dans les photographies présentées dans la figure 20A grâce au marquage des noyaux par le Hoechst, un colorant nucléaire, et confirmée par la quantification du contenu cellulaire en ADN. En effet, au cours de la culture, une forte augmentation (3,5 fois) du contenu en ADN dans les milieux endothélial (données personnelles) et mixte (figure 22A) est observée. Toutefois, notons qu’aucune différence dans le contenu en TGs, lorsqu’il est normalisé à la quantité d’ADN, n’a été observé lors de la culture des cellules CD34+/CD31- dans un milieu adipogénique constitué d’une base ECBM 71 ou d’une base ECGM, suggérant que la prolifération de ces cellules dans le milieu ECGM ne modifie pas le niveau de différenciation adipocytaire. L’ensemble de ces résultats montre que les cellules CD34+/CD31- cultivées en milieu mixte peuvent à la fois accumuler des lipides et former un réseau cellulaire positif pour le CD31. B.2) Etude de l’expression en ARNm des marqueurs adipocytaires et endothéliaux par les cellules CD34+/CD31- cultivées dans un milieu mixte Afin de confirmer les capacités adipogéniques et angiogéniques des cellules CD34+/CD31- en milieu mixte, nous avons voulu évaluer l’expression en ARNm des marqueurs adipocytaires et endothéliaux par des analyses de RT-PCR. L’expression de ces marqueurs a été tout d’abord déterminée dans des cellules CD34+/CD31-, des adipocytes matures et des cellules endothéliales capillaires CD34+/CD31+ fraîchement isolées. Les résultats présentés dans le tableau 12, montrent comme attendu que les transcrits pour les marqueurs adipocytaires sont détectés majoritairement dans les adipocytes matures et les transcrits pour les marqueurs endothéliaux sont détectés majoritairement dans les cellules endothéliales CD34+/CD31+. On peut cependant noter l’expression non négligeable d’aP2 et de PPARγ dans les cellules endothéliales capillaires CD34+/CD31+. Concernant PPARγ, ces résultats sont en accord avec d’autres observations (18). En revanche, aucune autre étude ne s’est intéressée à l’expression d’aP2 dans les cellules endothéliales. L’ensemble de ces résultats suggèrent donc que les cellules CD34+/CD31- fraîchement isolées expriment peu les marqueurs adipocytaires et endothéliaux comparés aux adipocytes matures et aux cellules endothéliales CD34+/CD31+, respectivement. L’expression de ces différents marqueurs adipocytaires et endothéliaux dans les cellules CD34+/CD31- cultivées en milieu adipogénique, endothélial et mixte pendant 10 jours a ensuite été déterminée. Comme le montre la figure 21A, en milieu mixte, une augmentation significative des taux de transcrits codant pour les marqueurs adipocytaires, excepté PPARγ, est observée par rapport au milieu endothélial. De plus, une augmentation en ARNm de tous les marqueurs endothéliaux est observée dans les cellules CD34+/CD31- en milieu mixte par rapport au milieu adipogénique (figure 21B). L’ensemble de ces résultats montre que la culture des cellules CD34+/CD31- en milieu mixte pendant 10 jours induit l’expression des ARNm codants pour des marqueurs adipocytaires d’une part et des marqueurs endothéliaux d’autre part. 72 A B 300 Adipo Mixte *** 200 *** * 100 0 aP2 PPARγ LHS FAS Marqueurs endothéliaux (en % du milieu endothélial) Marqueurs adipocytaires (en % du milieu adipogénique) Endo Mixte 100 *** 75 50 * *** * 25 0 CD31 vWF VE-cadherin VEGF-R1 Figure 21 : Détermination de l’expression en ARNm des marqueurs adipocytaires et endothéliaux des cellules CD34+/CD31- cultivées en milieu adipogénique, endothélial ou mixte Les cellules CD34+/CD31- sont ensemencées à 120 000 cellules/cm2 et cultivées en milieu adipogénique (Adipo), endothélial (Endo) ou mixte (mixte). Après 10 jours, l’expression en ARNm des marqueurs adipocytaires (aP2, PPARγ, LHS et FAS) (A) et des marqueurs endothéliaux (CD31, vWF, VE-cadherin et VEGF-R1) (B) a été déterminée par des analyses de RT-PCR. Les résultats sont exprimés en pourcentage du milieu adipogénique et endothélial pour les marqueurs adipocytaires et endothéliaux respectivement pour 3 à 6 expériences indépendantes. *** P<0.001, ** P<0.01 et P<0,05 vs milieu adipogénique ou endothélial Tableau 12: Détermination de l’expression en ARNm des marqueurs adipocytaires et endothéliaux par des adipocytes matures, des cellules progénitrices CD34+/CD31- et des cellules endothéliales capillaires CD34+/CD31+ Adipocytes matures Cellules progénitrices Cellules endothéliales CD34+/CD31CD34+/CD31+ Marqueurs adipocytaires aP2 PPARγ LHS FAS 42.67 ± 3.98 5.34 ± 0.77 21.89 ± 1.85 2.23 ± 0.55 5.67 ± 1.47 *** 1.22 ± 0.17 *** 0.14 ± 0.04 *** <0.02 *** 12.19 ± 3.43 *** 2.84 ± 0.62 * 0.55 ± 0.14 *** <0.02 *** 0.23 ± 0.03 * 0.52 ± 0.08 * 0.41 ± 0.05 * 0.07 ± 0.01 * 0.17 ± 0.04 ** 0.36 ± 0.06 ** 0.22 ± 0.05 * 0.03 ± 0.01** 0.40 ± 0.05 1.00 ± 0.17 1.21 ± 0.32 0.17 ± 0.04 Marqueurs endothéliaux CD31 vWF VE-cadherin VEGF-R1 L’expression en ARNm des marqueurs adipocytaires (aP2, PPARγ, LHS et FAS) et des marqueurs endothéliaux (CD31, vWF, VE-cadherin et VEGF-R1) a été déterminée par des analyses de RT-PCR dans des adipocytes matures, des cellules CD34+/CD31- et des cellules endothéliales capillaires CD34+/CD31+ fraîchement isolées. Les résultats sont exprimés en unités arbitraires pour 3 à 4 expériences indépendantes. *** P<0.001, ** P<0.01,* P<0.05 vs les adipocytes matures pour les marqueurs adipogéniques et vs les cellules endothéliales CD34+/CD31+ pour les marqueurs endothéliaux B.3) Etude cinétique sur l’évolution des cellules CD34+/CD31- au cours de la culture en milieu mixte Dans le développement du TA, angiogenèse et adipogenèse sont étroitement liées. Toutefois, il est décrit que l’angiogenèse précède l’adipogenèse (52). Afin de déterminer si un tel effet est observé dans nos conditions de culture. Nous avons réalisé une étude cinétique sur l’évolution des cellules CD34+/CD31- à différents jours de culture (2, 4, 6, 8 et 10) en milieu mixte. Dans un premier temps, la quantification intracellulaire en TGs ainsi que la formation du réseau cellulaire positif pour le CD31 ont été réalisées. Dans un second temps, nous avons quantifié l’expression en ARNm des marqueurs adipocytaires et endothéliaux des cellules CD34+/CD31-. Comme on peut l’observer dans la figure 22, l’augmentation du contenu en ADN devient significative à partir du 6ème jour de culture. De manière intéressante, la longueur du réseau cellulaire positif pour le CD31 apparaît et atteint son niveau maximal au 6ème jour de culture tandis que le contenu intracellulaire en TGs n’augmente significativement qu’à partir du 8ème jour de culture. Ces résultats laissent penser que la formation du réseau cellulaire 73 A Contenu en ADN (mg/ml) 0.05 *** *** 0.04 0.03 ** 0.02 0.01 0.00 0 2 4 6 8 10 Jours de différenciation B Contenu en triglycérides (mg/mg d'ADN) 40 Longueur du réseau positif pour le CD31 (U.A.) ** 20 10 0 C *** 30 0 2 4 6 8 10 Jours de différenciation 100 75 50 ** *** * 25 0 0 2 4 6 8 10 Jours de différenciation Figure 22 : Evolution du contenu en ADN, TGs et du réseau cellulaire positif pour le CD31 des cellules CD34+/CD31- cultivées en milieu mixte Les cellules CD34+/CD31- sont ensemencées à 120 000 cellules/cm2 et cultivées en milieu mixte. Après 10 jours, le contenu intracellulaire en ADN (A) et TGs (B) ainsi que la longueur du réseau cellulaire positif pour le CD31 (C) ont été évalués. Les valeurs sont exprimées en mg/mg d’ADN pour le contenu en TGs et la longueur du réseau cellulaire pour le CD31 en unité arbitraires normalisées à la quantité d’ADN pour 5 à 6 expériences indépendantes. *** P<0.001, ** P<0.01, *P<0,05 vs J0 positif pour le CD31 précède l’accumulation des TGs. Cependant, il est difficile de comparer l’apparition d’un marqueur avec la mise en place d’une activité métabolique. L’étude de l’expression en ARNm des marqueurs adipocytaires et endothéliaux, au cours de la culture des cellules CD34+/CD31- en milieu mixte nous a permis de compléter ces résultats. En effet, on note que l’expression d’aP2 et PPARγ, des marqueurs précoces du processus adipogénique, apparaît et atteint son maximum dès le 4ème jour tandis que l’expression de FAS, connu pour être un marqueur de l’activité métabolique, apparaît dès le 4ème jour mais atteint son maximum au 8ème jour de culture (figure 23). Concernant les marqueurs endothéliaux, nous avons constaté que l’expression du CD31 augmente significativement dès le 4ème jour de culture et une tendance similaire pour le facteur vWF semble être observée même si aucune différence significative n’a pu être mise en évidence du fait d’une forte variabilité interindividuelle. Ces résultats semblent indiquer qu’au cours de la culture l’expression des marqueurs endothéliaux étudiés atteint un niveau maximal plus rapidement que l’expression de FAS suggérant que les capacités angiogéniques apparaissent plus précocement que les capacités adipogéniques. Toutefois, il n’est pas exclu que l’accumulation des TGs nécessite plus de temps que l’organisation d’un réseau cellulaire positif pour le CD31. Il est important de préciser que les marqueurs endothéliaux utilisés pour ce travail sont décrits dans la littérature comme des marqueurs détectés spécifiquement dans les cellules endothéliales matures (223). Leur expression en fonction de la différenciation endothéliale n’est pas connue et à ce jour il n’est pas décrit de marqueurs géniques spécifiques de la différenciation des cellules endothéliales. Par ailleurs, il faut également rester prudent quant à la spécificité des marqueurs de la différenciation adipocytaire. En effet, certains sont également détectés dans les cellules endothéliales matures notamment PPARγ et aP2. Pour conclure, l’ensemble de ces résultats indique que les cellules CD34+/CD31cultivées en milieu mixte pendant 10 jours expriment à la fois des marqueurs adipocytaires et endothéliaux. Cette condition de culture constitue donc un nouvel outil pour l’étude des mécanismes contrôlant le devenir des cellules progénitrices CD34+/CD31-. 74 B 70 ** 60 50 40 30 * 20 10 0 2 4 6 8 10 Jours de différenciation 2.0 * 1.5 * 1.0 0.5 0.0 2 4 6 8 10 Jours de différenciation D Expression en ARNm du CD31 (U.A.) Expression en ARNm de FAS (U.A.) ** C 3 ** * 2 1 0 2 4 6 8 10 Jours de différenciation E 0.4 0.3 * 0.2 0.1 0.0 2 4 6 8 10 Jours de différenciation Expresion en ARNm du vWF (U.A.) 80 Expression en ARNm de PPARγ (U.A.) Expression en ARNm d'aP2 (U.A.) A 0.3 0.2 0.1 0.0 2 4 6 8 10 Jours de différenciation Figure 23 : Evolution de l’expression en ARNm des marqueurs adipocytaires et endothéliaux des cellules CD34+/CD31- cultivées en milieu mixte Les cellules CD34+/CD31- sont ensemencées à 120 000 cellules/cm2 et cultivées en milieu mixte. Après 10 jours, l’expression en ARNm des marqueurs adipocytaires aP2 (A), PPARγ (B) et FAS (C) et des marqueurs endothéliaux CD31 (D) et vWF (E) a été déterminée par des analyses de RT-PCR. Les résultats sont exprimés en unités arbitraires pour 4 expériences indépendantes. ** P<0.01 et P<0,05 vs J2 Toutefois, nous nous sommes demandés si l’effet angiogénique observé par les cellules CD34+/CD31- n’est pas du à une contamination par des cellules endothéliales matures CD34+/CD31+. Des analyses de cytométrie de flux ont été effectuées pour déterminer la pureté de la fraction CD34+/CD31-. Il a été observé que 92.9 ± 0.8 % des cellules retrouvées dans cette fraction sont CD34+/CD31- (données personnelles). Ainsi, la possibilité d’une contamination par des cellules endothéliales est faible. Cependant, afin de déterminer l’influence de la présence des cellules endothéliales capillaires matures sur les cellules CD34+/CD31- en milieu mixte, des expériences de coculture (CD34+/CD31- et CD34+/CD31+) ont été réalisées. Les cellules CD34+/CD31- ont été ensemencées dans un milieu ECBM/10% sérum de veau fœtal à 120000 cellules/puits en présence ou non de cellules endothéliales capillaires CD34+/CD31+ (5000 cellules/puits). Après 24 heures (J0) et 10 jours de culture en milieu mixte (J10), le marquage positif pour le CD31 a été quantifié. Les résultats présentés à la figure 24, montrent qu’après 24 heures, le nombre de cellules positives pour le CD31 lors de la coculture est augmenté (P<0,05 contrôle vs coculture) du à la présence de cellules endothéliales capillaires matures CD34+/CD31+. Cependant, après 10 jours de culture, aucune différence dans la longueur du réseau cellulaire pour le CD31 n’est observée entre les cellules CD34+/CD31- seules ou en coculture. Ce résultat indiquent que les cellules endothéliales matures quiescentes CD34+/CD31+ cultivées en milieu mixte ne s’organisent pas en réseau à la différence des cellules CD34+/CD31-. L’ensemble de ces données suggère donc que l’effet angiogénique observé est du à un potentiel angiogénique des cellules CD34+/CD31- plutôt qu’à une contamination par des cellules endothéliales CD34+/CD31+. La mise au point de cette condition de culture permettant de révéler simultanément les capacités adipogéniques et angiogéniques des cellules CD34+/CD31- nous a permis d’initier des études sur les mécanismes potentiels impliqués dans la régulation de l’expression de cette double fonctionnalité des cellules CD34+/CD31-. Trois axes ont été envisagés : l’influence des contacts cellule-cellule, l’influence de la MEC et de son remodelage notamment via les MMPs et l’influence des facteurs paracrines. Les résultats préliminaires que nous avons obtenus sont présentés dans le paragraphe suivant. 75 Marquage positif pour le CD31 (en % CD34+/CD31- seules) J0 Cellules CD34+/CD31- Cellules CD34+/CD31+ CECs B Cellules CD34+/CD31- Cellules CD34+/CD31+ CECs * 600 400 200 0 CD34+/31- + CECs J0 J10 Longueur du réseau positif pour le CD31 (en % CD34+31- seules) A 120 100 80 60 40 20 0 CD34+/31- + CECs J10 Figure 24 : Influence de la présence de cellules endothéliales matures sur la formation du réseau cellulaire positif pour le CD31 des cellules CD34+/CD31- cultivées en milieu mixte Les cellules CD34+/CD31- sont ensemencées à 120 000 cellules/cm2 seules ou en présence de cellules endothéliales matures CD34+/CD31+ (CECs) (5 000 cellules/cm2) puis cultivées en milieu mixte. Après 0 (A) et 10 (C) jours, les cellules sont fixées et marquées au Red Oil, au Hoechst (un colorant nucléaire) et avec un anticorps dirigé contre le CD31. Des photographies représentatives de 4 expériences indépendantes sont présentées. Le marquage positif pour le CD31 a ensuite été évalué. Les valeurs sont exprimées en unité arbitraires normalisées à la quantité d’ADN.*P<0,05 vs CD34+/CD31- seules. C) Implication des contacts cellule-cellule dans les capacités adipogéniques et angiogéniques des cellules CD34+/CD31- C.1) Influence de la densité cellulaire sur les cellules CD34+/CD31- cultivées en milieu mixte Etant donné que les cellules CD34+/CD31- ont une capacité de prolifération importante en milieu mixte, la densité cellulaire augmente avec le temps. L’influence des contacts cellule-cellule sur le devenir des cellules progénitrices CD34+/CD31- a donc été déterminée en modulant la densité cellulaire d’ensemencement. Pour cela, les cellules ont été ensemencées à trois densités différentes (2 000, 20 000 ou 120 000 cellules/cm2) et cultivées pendant 10 jours en milieu mixte. Comme on peut le voir dans la figure 25A, quelle que soit la densité cellulaire d’ensemencement, la quantité cellulaire d’ADN augmente au cours de la culture et à 10 jours de culture cette quantité d’ADN est identique pour les trois densités. Une augmentation du contenu intracellulaire en TGs est également observée quelque soit la densité cellulaire (figure 25B). Cependant, le contenu intracellulaire en TGs est plus faible si l’on compare la densité d’ensemencement la plus basse (2000 cellules/cm2) et la plus élevée (120000 cellules/cm2) suggérant un retard de l’adipogenèse lorsque les cellules sont ensemencées à faible densité. Concernant, la formation du réseau cellulaire positif pour le CD31, il n’est observé qu’à la plus forte densité (figure 25C) suggérant que les contacts cellule-cellule initiaux sont nécessaires à l’expression des capacités angiogéniques des cellules CD34+/CD31-. L’ensemble de ces données suggère donc que la densité cellulaire d’ensemencement peut moduler le devenir des cellules CD34+/CD31-. L’influence de la densité cellulaire sur le devenir cellulaire est connue puisque des travaux ont déjà suggéré que la densité cellulaire influence la différenciation des cellules souches mésenchymateuses (210). Cependant, ce sont les travaux de Mc Beath et al. qui ont clairement montré que la densité cellulaire d’ensemencement module l’engagement des cellules souches mésenchymateuses vers le lignage adipogénique et ostéogénique (167). Ces effets relatifs à la densité cellulaire peuvent être dus à des modulations de la forme de la cellule et des tensions du cytosquelette comme il a déjà été suggéré (167) mais également à la modulation des contacts et des communications entre les cellules. De nombreuses études ont montré l’importance des jonctions gaps dans le contrôle des processus de myogenèse (9, 215), d’ostéogenèse (237) mais aussi d’adipogenèse (238). Récemment, une étude indique que la communication par les jonctions gaps est nécessaire à l’expansion clonale durant la différenciation des préadipocytes de la lignée 3T3-L1 (296). 76 Contenu en ADN (mg/ml) A 0.05 *** 0.04 *** *** 0.03 0.02 0.01 0.00 0 10 0 2 000 Contenu en triglycérides (mg/mg d'ADN) B 10 20 000 0 10 120 000 jours cellules/cm2 * 30 *** ** 20 ** 10 0 0 10 0 2 000 10 20 000 0 10 120 000 jours cellules/cm2 C Longueur du réseau positif pour le CD31 (U.A.) 80 *** 60 40 20 0 0 10 2 000 0 10 20 000 0 10 120 000 jours cellules/cm2 Figure 25 : Influence de la densité cellulaire sur les capacités adipogéniques et angiogéniques des cellules CD34+/CD31- cultivées en milieu mixte Les cellules CD34+/CD31- sont ensemencées à 120 000, 20 000 ou 2 000 cellules/cm2 et cultivées en milieu mixte. Après 10 jours, le contenu intracellulaire en ADN (A) et TGs (B) ainsi que la longueur du réseau cellulaire pour le CD31 (C) ont été évalués. Les valeurs sont exprimées en mg/mg d’ADN pour le contenu en TGs et la longueur du réseau cellulaire pour le CD31 en unité arbitraires normalisées à la quantité d’ADN pour 4 à 10 expériences indépendantes. *** P<0.001, ** P<0.01, *P<0,05 vs J0 Dans la suite de ce travail, l’implication de la communication par les jonctions gaps dans les capacités angiogéniques et adipogéniques des cellules CD34+/CD31- a été évaluée. C.2) Influence de la communication cellulaire via les jonctions gaps sur les cellules CD34+/CD31- cultivées en milieu mixte Les jonctions gaps forment un canal intercellulaire essentiellement constitué d’un assemblage de connexines. Nous avons tout d’abord évalué l’expression en ARNm des connexines 43, 45, 40 et 37 dans des adipocytes matures, des cellules progénitrices CD34+/CD31- et des cellules endothéliales capillaires CD34+/CD31+ fraîchement isolées. Comme on peut le voir dans le tableau 13, toutes les connexines, excepté la connexine 37, sont détectées dans les trois types cellulaires testés. Le niveau d’ARNm de la connexin 40 est cependant très faible et on note que les cellules endothéliales capillaires expriment des niveaux plus élevés de connexine 43 que les adipocytes matures. L’expression en ARNm des connexines 43 et 45 a ensuite été évaluée au cours de la culture des cellules progénitrices CD34+/CD31- en milieu mixte. Les résultats sont présentés dans la figure 26 et indiquent clairement que l’expression en ARNm de ces connexines diminue au cours de la culture. Ces résultats sont en accord avec les travaux d’Umezawa et al. montrant que l’expression de la connexine 43 est diminué au cours de la différenciation adipocytaire des cellules stromales de la moelle osseuse H-1/A d’origine murine (267). Tableau 13: Expression en ARNm des connexines 43, 45, 40 et 37 dans des adipocytes matures, des cellules progénitrices CD34+/CD31- et des cellules endothéliales capillaires CD34+/CD31+ Types de connexines Connexine 43 Adipocytes matures 0.20 ± 0.06 Cellules progénitrices CD34+/CD310.51 ± 0.06 Cellules endothéliales CD34+/CD31+ 0.85 ± 0.21 * Connexine 45 0.05 ± 0.01 0.14 ± 0.06 0.18 ± 0.08 Connexine 40 <0.02 <0.02 0.04 ± 0.01 Connexine 37 Non détectable Non détectable Non détectable L’expression en ARNm des connexines 43, 45, 40 et 37 a été déterminée par des analyses de RT-PCR dans des adipocytes matures, des cellules CD34+/CD31- et des cellules endothéliales CD34+/CD31+ fraîchement isolées. Les résultats sont exprimés en unités arbitraires pour 3 expériences indépendantes. * P<0.05 vs les adipocytes matures 77 A B Expression en ARNm de la connexin 43 (U.A.) 1.0 0.8 0.6 0.4 ** *** 0.2 0.0 2 4 6 8 10 Jours de différenciation Expression en ARNm de la connexin 45 (U.A.) 0.12 1.2 0.10 0.08 0.06 0.04 *** *** 0.02 0.00 2 4 6 8 10 Jours de différenciation Figure 26 : Evolution de l’expression en ARNm des connexines 43 et 45 des cellules CD34+/CD31- cultivées en milieu mixte Les cellules CD34+/CD31- sont ensemencées à 120 000 cellules/cm2 et cultivées en milieu mixte. Après 10 jours, l’expression en ARNm des connexines 43 (A) et 45 (B) a été déterminée par des analyses de RT-PCR. Les résultats sont exprimés en unités arbitraires pour 4 expériences indépendantes. ** P<0.01 et ***P<0,001 vs J2 Le rôle direct de la communication par les jonctions gaps sur les capacités adipogéniques et angiogéniques des cellules CD34+/CD31- a été déterminé grâce à l’utilisation d’un inhibiteur des jonctions gaps, le 18α-glycyrrhetinic acide (AGA). Les cellules ont été traitées pendant 10 jours avec 5 et 10 µM d’AGA ou de GZA (glycyrrhizic acide) un analogue peptidique de l’AGA sans effet sur les jonctions gaps. Comme on peut le voir dans la figure 27, le GZA n’a aucun effet significatif ni sur le contenu intracellulaire en TGs ni sur l’apparition du réseau cellulaire positif pour le CD31. En revanche, l’AGA à 10 µM diminue de façon significative le contenu intracellulaire en TGs mais n’affecte pas significativement le réseau CD31 même si une tendance à l’augmentation du réseau est observée. Il est important de noter qu’à une concentration de 10 µM, l’AGA n’a pas effet sur le contenu cellulaire en ADN (données personnelles). Cependant, l’utilisation de cet inhibiteur à des concentrations supérieures à 30 µM est associée à une mort cellulaire au bout de quelques jours de culture. Ces résultats indiquent que la communication cellulaire via les jonctions gaps est requise pour l’adipogenèse des cellules CD34+/CD31- en accord avec les travaux de Yanagiya et al. sur les préadipocytes murins (296). Toutefois, l’effet observé sur les cellules CD34+/CD31- ne semble pas être du à une altération de l’expansion clonale comme c’est le cas pour les préadipocytes murins décrit par les résultats de Yanigaya et al. car aucune différence du contenu cellulaire en ADN dans les cellules contrôles et traitées n’a été observée (données personnelles). Une étude plus complète est toutefois nécessaire afin de préciser les effets d’un inhibiteur des jonctions gaps sur l’expression en ARNm des marqueurs de la différenciation adipocytaire et de déterminer à quel stade de l’adipogenèse les jonctions gaps sont requises. En résumé de cette deuxième partie, nous avons mis au point une condition de culture permettant simultanément l’étude des capacités angiogéniques et adipogéniques des cellules CD34+/CD31-. Ce nouvel outil va permettre l’étude des mécanismes qui contrôlent le devenir des cellules CD34+/CD31- et notamment l’influence du microenvironnement. Des premiers résultats indiquent que les contacts cellule-cellule ainsi que la communication via les jonctions gaps peuvent moduler le devenir des cellules CD34+/CD31-. 78 B Contenu en triglycérides (en % contrôle) 150 100 * 50 0 5 10 GZA 5 10 AGA µM Longueur du réseau positif pour le CD31 (en % du contrôle) A 300 200 100 0 5 10 GZA 5 10 µM AGA Figure 27 : Effet d’un inhibiteur des jonctions gaps sur les capacités adipogéniques et angiogéniques des cellules CD34+/CD31- cultivées en milieu mixte Les cellules CD34+/CD31- sont ensemencées à 120 000 cellules/cm2, cultivées en milieu mixte et traitées avec un inhibiteur des jonctions gaps, l’AGA, ou son analogue peptidique GZA. Après 10 jours, le contenu intracellulaire en TGs (A) ainsi que la longueur du réseau cellulaire positif pour le CD31 (B) ont été évalués. Les valeurs sont exprimées en pourcentage du contrôle après avoir été normalisées à la quantité d’ADN pour 3 à 4 expériences indépendantes. *P<0,05 vs GZA 10 µM En perspective à ce travail, l’influence des MMPs sur le devenir des cellules CD34+/CD31- cultivées en milieu mixte est envisagé. En effet, nos résultats indiquent que les cellules CD34+/CD31- isolées et cultivées en milieu adipogénique sécrètent les MMP-2 et -9 et une inhibition de leur activité par le batimastat limite l’adipogenèse de ces cellules. Il serait maintenant indispensable d’étudier les effets d’une inhibition des MMPs sur les capacités adipogéniques et angiogéniques des cellules CD34+/CD31-. L’influence directe de la MEC et notamment de ses composants matriciels tels que la fibronectine, le collagène, la gélatine sur les capacités adipogéniques et angiogéniques des cellules CD34+/CD31cultivées en milieu mixte pourrait ensuite être déterminée. Ces études permettraient de définir le rôle de la matrice et de sa dégradation dans le devenir des cellules progénitrices du TA humain. Enfin, un troisième axe serait également intéressant et concerne l’influence de facteurs paracrines sur le devenir de ces cellules. En effet, ces cellules contribuent certainement à la croissance du TA en fournissant adipocytes et cellules endothéliales nécessaires à son développement. Comme nous l’avons décrit dans l’introduction, le TA est une source de nombreux facteurs ou adipokines, elles-mêmes originaires des différentes populations cellulaires qui composent le TA. Ces sécrétions sont modulées au cours des phases de croissance des dépôts adipeux. On peut donc se demander si ces adipokines exercent un rôle dans le contrôle de la différenciation des cellules progénitrices. Ainsi, l’influence des sécrétions par les autres types cellulaires du TA environnant les cellules CD34+/CD31- tels que les macrophages, les cellules endothéliales, et les adipocytes matures doit être envisagée par l’utilisation de milieu conditionnés en base ECBM (condition de culture que nous avons vérifié comme étant favorable à la survie des cellules endothéliales, macrophages et adipocytes matures isolés du TA humain) sur les cellules CD34+/CD31- en milieu mixte. 79 Conclusions et perspectives Ce travail de thèse a eu pour objectif de déterminer l’implication des MMPs dans la différenciation des précurseurs adipocytaires humains. Nous avons démontré un rôle majeur de l’activité des MMPs et plus particulièrement MMP-9 dans la différenciation adipocytaire des cellules de la FSV du TA humain. De plus, MMP-9 pourrait être une cible de l’effet inhibiteur des IPs-VIH sur la différenciation adipocytaire des cellules de la FSV du TA humain. En effet, nous avons mis en évidence que les IPs-VIH diminuent l’expression et la sécrétion de MMP-9. Les mécanismes impliqués dans cet effet passent en partie par une inhibition de l’activité protéasomique des cellules de la FSV par les IPs-VIH, entraînant des perturbations de la voie NF-κB, facteur de transcription impliqué dans l’expression génique de MMP-9. L’étude des cibles moléculaires de MMP-9 impliquées dans les effets de cette protéase sur la différenciation adipocytaire, telles que la dégradation des composants de la MEC puisque celle-ci évolue au cours de la différenciation adipocytaire et/ou la biodisponibilité de facteurs solubles qui modulent l’adipogenèse doit maintenant être envisagé. De même les cibles cellulaires de MMP-9 au sein du TA doivent être mieux définies. L’ensemble de nos travaux a montré que la fraction cellulaire CD34+/CD31- contient un pool de cellules progénitrices présentant une potentialité adipocytaire et endothéliale. A présent, une nouvelle condition de culture permet simultanément l’étude des capacités adipogéniques et angiogéniques de ces cellules. Cependant, il reste à déterminer si cette population cellulaire CD34+/CD31- est constituée d’un mélange de cellules progénitrices unipotentes ou de cellules bi ou multipotentes. Notons que, la différenciation in vitro en adipocyte n’atteint jamais le pourcentage total de cellules, même si elle est nettement supérieure aux cellules exprimant des marqueurs endothéliaux tels que le CD31. Cette observation semble suggérer que les cellules CD34+/CD31- constituent une population cellulaire hétérogène. Une expérience d’analyse clonale pourrait permettre de déterminer l’homogénéité ou l’hétérogénéité de cette fraction cellulaire. Cependant ce type d’analyse est basé sur l’évaluation des capacités angiogéniques et adipogéniques de cellules dérivées après prolifération d’une cellule initiale. Or, l’effet de la prolifération sur le devenir cellulaire est à définir étant donné que jusqu'à présent nos études ont été réalisées sur des cellules en culture primaire non passagées. Nos résultats préliminaires sur les cellules CD34+/CD31- passagées 80 montrent une diminution des capacités angiogéniques alors que leur capacité adipogénique est maintenue (données personnelles). La présence de cette population cellulaire CD34+/CD31- au sein du TA humain pose la question de leur provenance et de leur mobilisation potentielle. En effet, ces cellules peuvent être résidentes et capable d’autorenouvellement, et/ou elles peuvent être recrutées à partir des cellules progénitrices circulantes issues de la moelle osseuse comme l’ont suggéré les travaux de Hong et al. (101). Différents types de signaux tels que le SDF-1 (stromal derived factor-1) mais également MMP-9 ont été montrés comme participant au recrutement des progéniteurs CD34+ avec un potentiel hématopoïétique et/ou hépatique dans le foie des souris NOD/SCID après un dommage hépatique (128). On peut donc poser l’hypothèse d’un rôle potentiel de MMP-9 sur le recrutement de cellules progénitrices circulantes au sein du TA. Une mobilisation potentielle des cellules CD34+/CD31- du TA est-elle possible ? Ces cellules sont-elles capables de migrer et de quitter le TA ? Le phénomène de mobilisation a été très étudié pour les cellules souches hématopoïétiques et consiste en leur libération depuis la moelle osseuse jusqu'à la circulation sanguine. Cette mobilisation est stimulée par de nombreux facteurs tels que le SDF-1 et le G-CSF (granulocyte colony-stimulating factor). De manière intéressante, ces facteurs entraînent la production de MMPs et notamment MMP-9 dans les cellules hématopoïétiques (50, 128). De plus, l’administration de ces composés à des souris déficientes pour MMP-9 ne permet pas la mobilisation cellulaire (96). Les mécanismes impliqués dans la migration des cellules souches vers la circulation sanguine passe par l’augmentation des quantités solubles de kit ligand, une glycoprotéine transmembranaire, induite par MMP-9 (96) qui permet non seulement la mobilisation des cellules progénitrices dans la circulation mais aussi la prolifération et la migration des mastocytes dans le tissu (97). Récemment notre groupe a montré que les cellules CD34+/CD31- migrent en réponse à des milieux conditionnés par des cellules endothéliales capillaires CD34+/CD31+ du TA humain. Cet effet est inhibé par la toxine pertussique (un inhibiteur de la protéine Gi) et par un anticorps dirigé contre le CXCR4, le récepteur du SDF-1. De plus, nous avons mis en évidence que les cellules endothéliales CD34+/CD31+ produisent et sécrètent du SDF-1 et que les sécrétions des cellules endothéliales CD34+/CD31+ permettent l’expression des capacités angiogéniques des cellules CD34+/CD31- (242). L’ensemble de ces résultats est présenté en annexe dans la publication 3. Le rôle de MMP-9 dans la migration des cellules CD34+/CD31- est à envisager d’autant plus que les expériences de migration des cellules 81 CD34+/CD31- présentés dans ce travail ont été réalisés sur un support de gélatine (données personnelles). Enfin, l’implication de MMP-9 in vivo reste à être définie. Afin de déterminer si les effets de MMP-9 observés in vitro ont une signification physiologique ou physiopathologique lors d’un développement ou d’une régression de TA, la caractérisation du TA et de ses capacités d’extension dans un modèle original de souris invalidées pour le gène de MMP-9 (souris KO MMP-9) sont à envisager. Nos premiers résultats, obtenus sur les souris KO MMP-9, sous tendent l’implication de cette métalloprotéase dans le développement du TA. En effet, en conditions nutritionnelles standard, l’absence de MMP-9 est associée à une diminution de 37% du TA sous cutané et de 27% du TA intra-abdominal (n=6), sans variation de la masse corporelle totale par rapport aux souris contrôles. De plus, la quantité de triglycérides stockés dans ces tissus est deux fois plus faible chez les souris KO MMP-9. Suite à ces résultats, il nous apparaît nécessaire de mieux caractériser ce modèle. Pour cela, dans un premier temps nous envisageons l’analyse du TA des souris KO MMP-9 aussi bien dans sa structure que dans sa composition cellulaire et matricielle. En effet, il est important de définir si la différence de masse adipeuse entre les souris KO MMP-9 et les souris contrôles est due à une diminution du nombre et/ou de la taille des adipocytes matures. Des éventuelles modifications de la vasculature, de la présence de macrophages et de la MEC dans les TA des souris KO MMP-9 et contrôles seront recherchées. De la même manière, il serait intéressant de définir la composition cellulaire de la FSV isolée des souris KO MMP-9 et contrôles. Enfin, l’isolement des différentes populations cellulaires de la FSV issues des souris KO MMP-9 et contrôles, par l’utilisation de nanoparticules magnétiques couplées à des anticorps d’intérêt ainsi que l’évaluation des capacités adipogéniques et angiogéniques in vitro sur les cellules progénitrices ainsi obtenues pourraient être envisagé. Dans un second temps, une cinétique de développement et/ou de régression du TA des souris KO MMP-9 pourrait être envisagée. L’étude des différents types cellulaires des TA et des composants matriciels de ces souris devenues obèses ou maigres pourra être réalisée, comme précédemment décrit . Pour conclure, ce travail démontre l’importance des MMPs dans le processus de différenciation adipocytaire des cellules progénitrices du TA humain. Les MMPs pourraient ainsi contribuer au développement de la masse grasse. Bien que leur rôle exact reste à déterminer les MMPs pourraient devenir de nouvelles cibles d’intérêt dans le développement de traitements efficaces pour l’obésité et la lipoatrophie. 82 Références bibliographiques 1. 2. 3. 4. 5. 6. 7. 8. 9. 10. 11. 12. 13. 14. 15. Adams, J. 2004. The development of proteasome inhibitors as anticancer drugs. Cancer Cell 5:417-21. Aggeler, J., S. M. Frisch, and Z. Werb. 1984. Changes in cell shape correlate with collagenase gene expression in rabbit synovial fibroblasts. J Cell Biol 98:1662-71. Alexander, C. M., S. Selvarajan, J. Mudgett, and Z. Werb. 2001. Stromelysin-1 regulates adipogenesis during mammary gland involution. J Cell Biol 152:693-703. Andre, P., M. Groettrup, P. Klenerman, R. de Giuli, B. L. Booth, Jr., V. Cerundolo, M. Bonneville, F. Jotereau, R. M. Zinkernagel, and V. Lotteau. 1998. An inhibitor of HIV-1 protease modulates proteasome activity, antigen presentation, and T cell responses. Proc Natl Acad Sci U S A 95:13120-4. Aoki, S., S. Toda, T. Sakemi, and H. Sugihara. 2003. Coculture of endothelial cells and mature adipocytes actively promotes immature preadipocyte development in vitro. Cell Struct Funct 28:55-60. Ariyama, Y., H. Shimizu, T. Satoh, T. Tsuchiya, S. Okada, S. Oyadomari, and M. Mori. 2007. Chop-deficient mice showed increased adiposity but no glucose intolerance. Obesity (Silver Spring) 15:1647-56. Avram, M. M., A. S. Avram, and W. D. James. 2007. Subcutaneous fat in normal and diseased states 3. Adipogenesis: from stem cell to fat cell. J Am Acad Dermatol 56:472-92. Baker, A. H., D. R. Edwards, and G. Murphy. 2002. Metalloproteinase inhibitors: biological actions and therapeutic opportunities. J Cell Sci 115:3719-27. Balogh, S., C. C. Naus, and P. A. Merrifield. 1993. Expression of gap junctions in cultured rat L6 cells during myogenesis. Dev Biol 155:351-60. Bastard, J. P., M. Caron, H. Vidal, V. Jan, M. Auclair, C. Vigouroux, J. Luboinski, M. Laville, M. Maachi, P. M. Girard, W. Rozenbaum, P. Levan, and J. Capeau. 2002. Association between altered expression of adipogenic factor SREBP1 in lipoatrophic adipose tissue from HIV-1-infected patients and abnormal adipocyte differentiation and insulin resistance. Lancet 359:1026-31. Beigneux, A. P., B. S. Davies, P. Gin, M. M. Weinstein, E. Farber, X. Qiao, F. Peale, S. Bunting, R. L. Walzem, J. S. Wong, W. S. Blaner, Z. M. Ding, K. Melford, N. Wongsiriroj, X. Shu, F. de Sauvage, R. O. Ryan, L. G. Fong, A. Bensadoun, and S. G. Young. 2007. Glycosylphosphatidylinositol-anchored highdensity lipoprotein-binding protein 1 plays a critical role in the lipolytic processing of chylomicrons. Cell Metab 5:279-91. Ben-Romano, R., A. Rudich, S. Etzion, R. Potashnik, E. Kagan, U. Greenbaum, and N. Bashan. 2006. Nelfinavir induces adipocyte insulin resistance through the induction of oxidative stress: differential protective effect of antioxidant agents. Antivir Ther 11:1051-60. Berlan, M., and M. Lafontan. 1985. Evidence that epinephrine acts preferentially as an antilipolytic agent in abdominal human subcutaneous fat cells: assessment by analysis of beta and alpha 2 adrenoceptor properties. Eur J Clin Invest 15:341-8. Bi, Y., C. H. Stuelten, T. Kilts, S. Wadhwa, R. V. Iozzo, P. G. Robey, X. D. Chen, and M. F. Young. 2005. Extracellular matrix proteoglycans control the fate of bone marrow stromal cells. J Biol Chem 280:30481-9. Bjorntorp, P., A. Gustafson, and B. Persson. 1971. Adipose tissue fat cell size and number in relation to metabolism in endogenous hypertriglyceridemia. Acta Med Scand 190:363-7. 83 16. 17. 18. 19. 20. 21. 22. 23. 24. 25. 26. 27. 28. 29. 30. Bouloumie, A., H. C. Drexler, M. Lafontan, and R. Busse. 1998. Leptin, the product of Ob gene, promotes angiogenesis. Circ Res 83:1059-66. Bouloumie, A., C. Sengenes, G. Portolan, J. Galitzky, and M. Lafontan. 2001. Adipocyte produces matrix metalloproteinases 2 and 9: involvement in adipose differentiation. Diabetes 50:2080-6. Braissant, O., F. Foufelle, C. Scotto, M. Dauca, and W. Wahli. 1996. Differential expression of peroxisome proliferator-activated receptors (PPARs): tissue distribution of PPAR-alpha, -beta, and -gamma in the adult rat. Endocrinology 137:354-66. Brakenhielm, E., R. Cao, B. Gao, B. Angelin, B. Cannon, P. Parini, and Y. Cao. 2004. Angiogenesis inhibitor, TNP-470, prevents diet-induced and genetic obesity in mice. Circ Res 94:1579-88. Brinkman, K., J. A. Smeitink, J. A. Romijn, and P. Reiss. 1999. Mitochondrial toxicity induced by nucleoside-analogue reverse-transcriptase inhibitors is a key factor in the pathogenesis of antiretroviral-therapy-related lipodystrophy. Lancet 354:1112-5. Brown, M. S., and J. L. Goldstein. 1999. A proteolytic pathway that controls the cholesterol content of membranes, cells, and blood. Proc Natl Acad Sci U S A 96:11041-8. Brown, M. S., and J. L. Goldstein. 1997. The SREBP pathway: regulation of cholesterol metabolism by proteolysis of a membrane-bound transcription factor. Cell 89:331-40. Brun, R. P., P. Tontonoz, B. M. Forman, R. Ellis, J. Chen, R. M. Evans, and B. M. Spiegelman. 1996. Differential activation of adipogenesis by multiple PPAR isoforms. Genes Dev 10:974-84. Cancello, R., C. Henegar, N. Viguerie, S. Taleb, C. Poitou, C. Rouault, M. Coupaye, V. Pelloux, D. Hugol, J. L. Bouillot, A. Bouloumie, G. Barbatelli, S. Cinti, P. A. Svensson, G. S. Barsh, J. D. Zucker, A. Basdevant, D. Langin, and K. Clement. 2005. Reduction of macrophage infiltration and chemoattractant gene expression changes in white adipose tissue of morbidly obese subjects after surgeryinduced weight loss. Diabetes 54:2277-86. Capeau, J., J. Magre, O. Lascols, M. Caron, V. Bereziat, C. Vigouroux, and J. P. Bastard. 2005. Diseases of adipose tissue: genetic and acquired lipodystrophies. Biochem Soc Trans 33:1073-7. Carmeliet, P., L. Moons, R. Lijnen, M. Baes, V. Lemaitre, P. Tipping, A. Drew, Y. Eeckhout, S. Shapiro, F. Lupu, and D. Collen. 1997. Urokinase-generated plasmin activates matrix metalloproteinases during aneurysm formation. Nat Genet 17:439-44. Caron, M., M. Auclair, B. Donadille, V. Bereziat, B. Guerci, M. Laville, H. Narbonne, C. Bodemer, O. Lascols, J. Capeau, and C. Vigouroux. 2007. Human lipodystrophies linked to mutations in A-type lamins and to HIV protease inhibitor therapy are both associated with prelamin A accumulation, oxidative stress and premature cellular senescence. Cell Death Differ. Caron, M., M. Auclair, C. Lagathu, A. Lombes, U. A. Walker, M. Kornprobst, and J. Capeau. 2004. The HIV-1 nucleoside reverse transcriptase inhibitors stavudine and zidovudine alter adipocyte functions in vitro. Aids 18:2127-36. Caron, M., M. Auclair, H. Sterlingot, M. Kornprobst, and J. Capeau. 2003. Some HIV protease inhibitors alter lamin A/C maturation and stability, SREBP-1 nuclear localization and adipocyte differentiation. Aids 17:2437-44. Caron, M., M. Auclair, C. Vigouroux, M. Glorian, C. Forest, and J. Capeau. 2001. The HIV protease inhibitor indinavir impairs sterol regulatory element-binding 84 31. 32. 33. 34. 35. 36. 37. 38. 39. 40. 41. 42. 43. 44. 45. protein-1 intranuclear localization, inhibits preadipocyte differentiation, and induces insulin resistance. Diabetes 50:1378-88. Carr, A. 2000. HIV protease inhibitor-related lipodystrophy syndrome. Clin Infect Dis 30 Suppl 2:S135-42. Carr, A., J. Miller, M. Law, and D. A. Cooper. 2000. A syndrome of lipoatrophy, lactic acidaemia and liver dysfunction associated with HIV nucleoside analogue therapy: contribution to protease inhibitor-related lipodystrophy syndrome. Aids 14:F25-32. Carr, A., K. Samaras, S. Burton, M. Law, J. Freund, D. J. Chisholm, and D. A. Cooper. 1998. A syndrome of peripheral lipodystrophy, hyperlipidaemia and insulin resistance in patients receiving HIV protease inhibitors. Aids 12:F51-8. Carr, A., K. Samaras, D. J. Chisholm, and D. A. Cooper. 1998. Pathogenesis of HIV-1-protease inhibitor-associated peripheral lipodystrophy, hyperlipidaemia, and insulin resistance. Lancet 351:1881-3. Carriere, A., M. C. Carmona, Y. Fernandez, M. Rigoulet, R. H. Wenger, L. Penicaud, and L. Casteilla. 2004. Mitochondrial reactive oxygen species control the transcription factor CHOP-10/GADD153 and adipocyte differentiation: a mechanism for hypoxia-dependent effect. J Biol Chem 279:40462-9. Carriere, A., Y. Fernandez, M. Rigoulet, L. Penicaud, and L. Casteilla. 2003. Inhibition of preadipocyte proliferation by mitochondrial reactive oxygen species. FEBS Lett 550:163-7. Chakraborti, S., M. Mandal, S. Das, A. Mandal, and T. Chakraborti. 2003. Regulation of matrix metalloproteinases: an overview. Mol Cell Biochem 253:26985. Chavey, C., B. Mari, M. N. Monthouel, S. Bonnafous, P. Anglard, E. Van Obberghen, and S. Tartare-Deckert. 2003. Matrix metalloproteinases are differentially expressed in adipose tissue during obesity and modulate adipocyte differentiation. J Biol Chem 278:11888-96. Chen, Z., J. I. Torrens, A. Anand, B. M. Spiegelman, and J. M. Friedman. 2005. Krox20 stimulates adipogenesis via C/EBPbeta-dependent and -independent mechanisms. Cell Metab 1:93-106. Chi, D., J. Henry, J. Kelley, R. Thorpe, J. K. Smith, and G. Krishnaswamy. 2000. The effects of HIV infection on endothelial function. Endothelium 7:223-42. Chirco, R., X. W. Liu, K. K. Jung, and H. R. Kim. 2006. Novel functions of TIMPs in cell signaling. Cancer Metastasis Rev 25:99-113. Cho, C. H., Y. J. Koh, J. Han, H. K. Sung, H. Jong Lee, T. Morisada, R. A. Schwendener, R. A. Brekken, G. Kang, Y. Oike, T. S. Choi, T. Suda, O. J. Yoo, and G. Y. Koh. 2007. Angiogenic role of LYVE-1-positive macrophages in adipose tissue. Circ Res 100:e47-57. Christeff, N., J. C. Melchior, P. de Truchis, C. Perronne, and M. L. Gougeon. 2002. Increased serum interferon alpha in HIV-1 associated lipodystrophy syndrome. Eur J Clin Invest 32:43-50. Chun, T. H., K. B. Hotary, F. Sabeh, A. R. Saltiel, E. D. Allen, and S. J. Weiss. 2006. A pericellular collagenase directs the 3-dimensional development of white adipose tissue. Cell 125:577-91. Cinti, S., G. Mitchell, G. Barbatelli, I. Murano, E. Ceresi, E. Faloia, S. Wang, M. Fortier, A. S. Greenberg, and M. S. Obin. 2005. Adipocyte death defines macrophage localization and function in adipose tissue of obese mice and humans. J Lipid Res 46:2347-55. 85 46. 47. 48. 49. 50. 51. 52. 53. 54. 55. 56. 57. 58. 59. 60. 61. Clement, K., N. Viguerie, C. Poitou, C. Carette, V. Pelloux, C. A. Curat, A. Sicard, S. Rome, A. Benis, J. D. Zucker, H. Vidal, M. Laville, G. S. Barsh, A. Basdevant, V. Stich, R. Cancello, and D. Langin. 2004. Weight loss regulates inflammation-related genes in white adipose tissue of obese subjects. Faseb J 18:1657-69. Coffinier, C., S. E. Hudon, E. A. Farber, S. Y. Chang, C. A. Hrycyna, S. G. Young, and L. G. Fong. 2007. From the Cover: HIV protease inhibitors block the zinc metalloproteinase ZMPSTE24 and lead to an accumulation of prelamin A in cells. Proc Natl Acad Sci U S A 104:13432-7. consultation, W. e. 2004. Appropriate body-mass index for Asian populations and its implications for policy and intervention strategies. The Lancet:157-163. Cook, K. S., D. L. Groves, H. Y. Min, and B. M. Spiegelman. 1985. A developmentally regulated mRNA from 3T3 adipocytes encodes a novel serine protease homologue. Proc Natl Acad Sci U S A 82:6480-4. Cottler-Fox, M. H., T. Lapidot, I. Petit, O. Kollet, J. F. DiPersio, D. Link, and S. Devine. 2003. Stem cell mobilization. Hematology Am Soc Hematol Educ Program:419-37. Coux, O., K. Tanaka, and A. L. Goldberg. 1996. Structure and functions of the 20S and 26S proteasomes. Annu Rev Biochem 65:801-47. Crandall, D. L., G. J. Hausman, and J. G. Kral. 1997. A review of the microcirculation of adipose tissue: anatomic, metabolic, and angiogenic perspectives. Microcirculation 4:211-32. Croissandeau, G., M. Chretien, and M. Mbikay. 2002. Involvement of matrix metalloproteinases in the adipose conversion of 3T3-L1 preadipocytes. Biochem J 364:739-46. Crossno, J. T., Jr., S. M. Majka, T. Grazia, R. G. Gill, and D. J. Klemm. 2006. Rosiglitazone promotes development of a novel adipocyte population from bone marrow-derived circulating progenitor cells. J Clin Invest 116:3220-8. Curat, C. A., A. Miranville, C. Sengenes, M. Diehl, C. Tonus, R. Busse, and A. Bouloumie. 2004. From blood monocytes to adipose tissue-resident macrophages: induction of diapedesis by human mature adipocytes. Diabetes 53:1285-92. Curat, C. A., V. Wegner, C. Sengenes, A. Miranville, C. Tonus, R. Busse, and A. Bouloumie. 2006. Macrophages in human visceral adipose tissue: increased accumulation in obesity and a source of resistin and visfatin. Diabetologia 49:744-7. Dang, D., Y. Yang, X. Li, A. Atakilit, J. Regezi, D. Eisele, D. Ellis, and D. M. Ramos. 2004. Matrix metalloproteinases and TGFbeta1 modulate oral tumor cell matrix. Biochem Biophys Res Commun 316:937-42. Dani, C., A. G. Smith, S. Dessolin, P. Leroy, L. Staccini, P. Villageois, C. Darimont, and G. Ailhaud. 1997. Differentiation of embryonic stem cells into adipocytes in vitro. J Cell Sci 110 ( Pt 11):1279-85. Demeulemeester, D., I. Scroyen, G. Voros, J. Snoeys, B. De Geest, D. Collen, and H. R. Lijnen. 2006. Overexpression of tissue inhibitor of matrix metalloproteinases-1 (TIMP-1) in mice does not affect adipogenesis or adipose tissue development. Thromb Haemost 95:1019-24. Deryugina, E. I., and J. P. Quigley. 2006. Matrix metalloproteinases and tumor metastasis. Cancer Metastasis Rev 25:9-34. Di Simone, N., M. De Santis, E. Tamburrini, F. Di Nicuolo, M. B. Lucia, P. Riccardi, S. D'Ippolito, R. Cauda, and A. Caruso. 2007. Effects of antiretroviral therapy on tube-like network formation of human endothelial cells. Biol Pharm Bull 30:982-4. 86 62. 63. 64. 65. 66. 67. 68. 69. 70. 71. 72. 73. 74. 75. 76. Domingo, P., X. Matias-Guiu, R. M. Pujol, E. Francia, E. Lagarda, M. A. Sambeat, and G. Vazquez. 1999. Subcutaneous adipocyte apoptosis in HIV-1 protease inhibitor-associated lipodystrophy. Aids 13:2261-7. Domingo, P., F. Vidal, J. C. Domingo, S. Veloso, M. A. Sambeat, F. Torres, J. J. Sirvent, J. Vendrell, X. Matias-Guiu, and C. Richart. 2005. Tumour necrosis factor alpha in fat redistribution syndromes associated with combination antiretroviral therapy in HIV-1-infected patients: potential role in subcutaneous adipocyte apoptosis. Eur J Clin Invest 35:771-80. Dowell, P., C. Flexner, P. O. Kwiterovich, and M. D. Lane. 2000. Suppression of preadipocyte differentiation and promotion of adipocyte death by HIV protease inhibitors. J Biol Chem 275:41325-32. Eberle, D., B. Hegarty, P. Bossard, P. Ferre, and F. Foufelle. 2004. SREBP transcription factors: master regulators of lipid homeostasis. Biochimie 86:839-48. Edens, N. K., S. K. Fried, J. G. Kral, J. Hirsch, and R. L. Leibel. 1993. In vitro lipid synthesis in human adipose tissue from three abdominal sites. Am J Physiol 265:E374-9. Eeckhout, Y., and G. Vaes. 1977. Further studies on the activation of procollagenase, the latent precursor of bone collagenase. Effects of lysosomal cathepsin B, plasmin and kallikrein, and spontaneous activation. Biochem J 166:2131. El Hadri, K., M. Glorian, C. Monsempes, M. N. Dieudonne, R. Pecquery, Y. Giudicelli, M. Andreani, I. Dugail, and B. Feve. 2004. In vitro suppression of the lipogenic pathway by the nonnucleoside reverse transcriptase inhibitor efavirenz in 3T3 and human preadipocytes or adipocytes. J Biol Chem 279:15130-41. Engler, A. J., S. Sen, H. L. Sweeney, and D. E. Discher. 2006. Matrix elasticity directs stem cell lineage specification. Cell 126:677-89. Enoksson, S., M. Talbot, F. Rife, W. V. Tamborlane, R. S. Sherwin, and S. Caprio. 2000. Impaired in vivo stimulation of lipolysis in adipose tissue by selective beta2-adrenergic agonist in obese adolescent girls. Diabetes 49:2149-53. Even-Ram, S., V. Artym, and K. M. Yamada. 2006. Matrix control of stem cell fate. Cell 126:645-7. Fain, J. N., A. K. Madan, M. L. Hiler, P. Cheema, and S. W. Bahouth. 2004. Comparison of the release of adipokines by adipose tissue, adipose tissue matrix, and adipocytes from visceral and subcutaneous abdominal adipose tissues of obese humans. Endocrinology 145:2273-82. Fajas, L., K. Schoonjans, L. Gelman, J. B. Kim, J. Najib, G. Martin, J. C. Fruchart, M. Briggs, B. M. Spiegelman, and J. Auwerx. 1999. Regulation of peroxisome proliferator-activated receptor gamma expression by adipocyte differentiation and determination factor 1/sterol regulatory element binding protein 1: implications for adipocyte differentiation and metabolism. Mol Cell Biol 19:5495503. Farmer, S. R. 2006. Transcriptional control of adipocyte formation. Cell Metab 4:263-73. Farnier, C., S. Krief, M. Blache, F. Diot-Dupuy, G. Mory, P. Ferre, and R. Bazin. 2003. Adipocyte functions are modulated by cell size change: potential involvement of an integrin/ERK signalling pathway. Int J Obes Relat Metab Disord 27:1178-86. Fata, J. E., K. J. Leco, E. B. Voura, H. Y. Yu, P. Waterhouse, G. Murphy, R. A. Moorehead, and R. Khokha. 2001. Accelerated apoptosis in the Timp-3-deficient mammary gland. J Clin Invest 108:831-41. 87 77. 78. 79. 80. 81. 82. 83. 84. 85. 86. 87. 88. 89. 90. 91. 92. Ferreras, M., U. Felbor, T. Lenhard, B. R. Olsen, and J. Delaisse. 2000. Generation and degradation of human endostatin proteins by various proteinases. FEBS Lett 486:247-51. Feve, B. 2005. Adipogenesis: cellular and molecular aspects. Best Pract Res Clin Endocrinol Metab 19:483-99. Fève, B. 2003. Physiologie et différenciation du tissu adipeux. Médecine clinique endocrinologie et diabète 8:34-43. Fowlkes, J. L., K. M. Thrailkill, D. M. Serra, K. Suzuki, and H. Nagase. 1995. Matrix metalloproteinases as insulin-like growth factor binding protein-degrading proteinases. Prog Growth Factor Res 6:255-63. Frayn, K. N., F. Karpe, B. A. Fielding, I. A. Macdonald, and S. W. Coppack. 2003. Integrative physiology of human adipose tissue. Int J Obes Relat Metab Disord 27:875-88. Fukai, F., M. Ohtaki, N. Fujii, H. Yajima, T. Ishii, Y. Nishizawa, K. Miyazaki, and T. Katayama. 1995. Release of biological activities from quiescent fibronectin by a conformational change and limited proteolysis by matrix metalloproteinases. Biochemistry 34:11453-9. Fukumura, D., A. Ushiyama, D. G. Duda, L. Xu, J. Tam, V. Krishna, K. Chatterjee, I. Garkavtsev, and R. K. Jain. 2003. Paracrine regulation of angiogenesis and adipocyte differentiation during in vivo adipogenesis. Circ Res 93:e88-97. Gaedicke, S., E. Firat-Geier, O. Constantiniu, M. Lucchiari-Hartz, M. Freudenberg, C. Galanos, and G. Niedermann. 2002. Antitumor effect of the human immunodeficiency virus protease inhibitor ritonavir: induction of tumor-cell apoptosis associated with perturbation of proteasomal proteolysis. Cancer Res 62:6901-8. Galis, Z. S., and J. J. Khatri. 2002. Matrix metalloproteinases in vascular remodeling and atherogenesis: the good, the bad, and the ugly. Circ Res 90:251-62. Ghanim, H., A. Aljada, D. Hofmeyer, T. Syed, P. Mohanty, and P. Dandona. 2004. Circulating mononuclear cells in the obese are in a proinflammatory state. Circulation 110:1564-71. Goldberg, I. J. 1996. Lipoprotein lipase and lipolysis: central roles in lipoprotein metabolism and atherogenesis. J Lipid Res 37:693-707. Golubkov, V. S., S. Boyd, A. Y. Savinov, A. V. Chekanov, A. L. Osterman, A. Remacle, D. V. Rozanov, S. J. Doxsey, and A. Y. Strongin. 2005. Membrane type1 matrix metalloproteinase (MT1-MMP) exhibits an important intracellular cleavage function and causes chromosome instability. J Biol Chem 280:25079-86. Gougeon, M. L., L. Penicaud, B. Fromenty, P. Leclercq, J. P. Viard, and J. Capeau. 2004. Adipocytes targets and actors in the pathogenesis of HIV-associated lipodystrophy and metabolic alterations. Antivir Ther 9:161-77. Green, H., and O. Kehinde. 1979. Formation of normally differentiated subcutaneous fat pads by an established preadipose cell line. J Cell Physiol 101:16971. Gregoire, F. M., C. M. Smas, and H. S. Sul. 1998. Understanding adipocyte differentiation. Physiol Rev 78:783-809. Grigem, S., P. Fischer-Posovszky, K. M. Debatin, E. Loizon, H. Vidal, and M. Wabitsch. 2005. The effect of the HIV protease inhibitor ritonavir on proliferation, differentiation, lipogenesis, gene expression and apoptosis of human preadipocytes and adipocytes. Horm Metab Res 37:602-9. 88 93. 94. 95. 96. 97. 98. 99. 100. 101. 102. 103. 104. 105. 106. 107. 108. Hadigan, C., S. Borgonha, J. Rabe, V. Young, and S. Grinspoon. 2002. Increased rates of lipolysis among human immunodeficiency virus-infected men receiving highly active antiretroviral therapy. Metabolism 51:1143-7. Hausberger, F. X., and M. M. Widelitz. 1963. Distribution of labeled erythrocytes in adipose tissue and muscle in the rat. Am J Physiol 204:649-52. Hausman, G. J., J. T. Wright, and R. L. Richardson. 1996. The influence of extracellular matrix substrata on preadipocyte development in serum-free cultures of stromal-vascular cells. J Anim Sci 74:2117-28. Heissig, B., K. Hattori, S. Dias, M. Friedrich, B. Ferris, N. R. Hackett, R. G. Crystal, P. Besmer, D. Lyden, M. A. Moore, Z. Werb, and S. Rafii. 2002. Recruitment of stem and progenitor cells from the bone marrow niche requires MMP9 mediated release of kit-ligand. Cell 109:625-37. Heissig, B., S. Rafii, H. Akiyama, Y. Ohki, Y. Sato, T. Rafael, Z. Zhu, D. J. Hicklin, K. Okumura, H. Ogawa, Z. Werb, and K. Hattori. 2005. Low-dose irradiation promotes tissue revascularization through VEGF release from mast cells and MMP-9-mediated progenitor cell mobilization. J Exp Med 202:739-50. Hemmrich, K., D. von Heimburg, K. Cierpka, S. Haydarlioglu, and N. Pallua. 2005. Optimization of the differentiation of human preadipocytes in vitro. Differentiation 73:28-35. Hertel, J., H. Struthers, C. B. Horj, and P. W. Hruz. 2004. A structural basis for the acute effects of HIV protease inhibitors on GLUT4 intrinsic activity. J Biol Chem 279:55147-52. Holm, C., T. Osterlund, H. Laurell, and J. A. Contreras. 2000. Molecular mechanisms regulating hormone-sensitive lipase and lipolysis. Annu Rev Nutr 20:365-93. Hong, K. M., M. D. Burdick, R. J. Phillips, D. Heber, and R. M. Strieter. 2005. Characterization of human fibrocytes as circulating adipocyte progenitors and the formation of human adipose tissue in SCID mice. Faseb J 19:2029-31. Horowitz, J. F. 2001. Regulation of lipid mobilization and oxidation during exercise in obesity. Exerc Sport Sci Rev 29:42-6. Horton, J. D., J. L. Goldstein, and M. S. Brown. 2002. SREBPs: activators of the complete program of cholesterol and fatty acid synthesis in the liver. J Clin Invest 109:1125-31. Huber, J., M. Loffler, M. Bilban, M. Reimers, A. Kadl, J. Todoric, M. Zeyda, R. Geyeregger, M. Schreiner, T. Weichhart, N. Leitinger, W. Waldhausl, and T. M. Stulnig. 2007. Prevention of high-fat diet-induced adipose tissue remodeling in obese diabetic mice by n-3 polyunsaturated fatty acids. Int J Obes (Lond) 31:1004-13. Hudgins, L. C., A. Baday, M. K. Hellerstein, T. S. Parker, D. M. Levine, C. E. Seidman, R. A. Neese, J. D. Tremaroli, and J. Hirsch. 2007. The effect of dietary carbohydrate on genes for fatty acid synthase and inflammatory cytokines in adipose tissues from lean and obese subjects. J Nutr Biochem. Huhtala, P., M. J. Humphries, J. B. McCarthy, P. M. Tremble, Z. Werb, and C. H. Damsky. 1995. Cooperative signaling by alpha 5 beta 1 and alpha 4 beta 1 integrins regulates metalloproteinase gene expression in fibroblasts adhering to fibronectin. J Cell Biol 129:867-79. IG, G., and S. MA. 1945. Blood vessels in fat tissue: relation to problems of gas exchange. J exp Med 81:219-232. Imai, K., A. Hiramatsu, D. Fukushima, M. D. Pierschbacher, and Y. Okada. 1997. Degradation of decorin by matrix metalloproteinases: identification of the 89 109. 110. 111. 112. 113. 114. 115. 116. 117. 118. 119. 120. 121. 122. 123. cleavage sites, kinetic analyses and transforming growth factor-beta1 release. Biochem J 322 ( Pt 3):809-14. Jain, R. G., and J. M. Lenhard. 2002. Select HIV protease inhibitors alter bone and fat metabolism ex vivo. J Biol Chem 277:19247-50. Jan, V., P. Cervera, M. Maachi, M. Baudrimont, M. Kim, H. Vidal, P. M. Girard, P. Levan, W. Rozenbaum, A. Lombes, J. Capeau, and J. P. Bastard. 2004. Altered fat differentiation and adipocytokine expression are inter-related and linked to morphological changes and insulin resistance in HIV-1-infected lipodystrophic patients. Antivir Ther 9:555-64. Janneh, O., P. G. Hoggard, J. F. Tjia, S. P. Jones, S. H. Khoo, B. Maher, D. J. Back, and M. Pirmohamed. 2003. Intracellular disposition and metabolic effects of zidovudine, stavudine and four protease inhibitors in cultured adipocytes. Antivir Ther 8:417-26. Javazon, E. H., K. J. Beggs, and A. W. Flake. 2004. Mesenchymal stem cells: paradoxes of passaging. Exp Hematol 32:414-25. Jenkins, C. M., D. J. Mancuso, W. Yan, H. F. Sims, B. Gibson, and R. W. Gross. 2004. Identification, cloning, expression, and purification of three novel human calcium-independent phospholipase A2 family members possessing triacylglycerol lipase and acylglycerol transacylase activities. J Biol Chem 279:48968-75. Jiang, B., V. Y. Hebert, Y. Li, J. M. Mathis, J. S. Alexander, and T. R. Dugas. 2007. HIV antiretroviral drug combination induces endothelial mitochondrial dysfunction and reactive oxygen species production, but not apoptosis. Toxicol Appl Pharmacol. Johnson, J. A., J. B. Albu, E. S. Engelson, S. K. Fried, Y. Inada, G. Ionescu, and D. P. Kotler. 2004. Increased systemic and adipose tissue cytokines in patients with HIV-associated lipodystrophy. Am J Physiol Endocrinol Metab 286:E261-71. Johnson, M. D., H. R. Kim, L. Chesler, G. Tsao-Wu, N. Bouck, and P. J. Polverini. 1994. Inhibition of angiogenesis by tissue inhibitor of metalloproteinase. J Cell Physiol 160:194-202. Jones, K., P. G. Hoggard, S. D. Sales, S. Khoo, R. Davey, and D. J. Back. 2001. Differences in the intracellular accumulation of HIV protease inhibitors in vitro and the effect of active transport. Aids 15:675-81. Jones, S. P., O. Janneh, D. J. Back, and M. Pirmohamed. 2005. Altered adipokine response in murine 3T3-F442A adipocytes treated with protease inhibitors and nucleoside reverse transcriptase inhibitors. Antivir Ther 10:207-13. Kamiya, S., R. Kato, M. Wakabayashi, T. Tohyama, I. Enami, M. Ueki, H. Yajima, T. Ishii, H. Nakamura, T. Katayama, J. Takagi, and F. Fukai. 2002. Fibronectin peptides derived from two distinct regions stimulate adipocyte differentiation by preventing fibronectin matrix assembly. Biochemistry 41:3270-7. Kersten, S. 2001. Mechanisms of nutritional and hormonal regulation of lipogenesis. EMBO Rep 2:282-6. Kim, H. K., M. Della-Fera, J. Lin, and C. A. Baile. 2006. Docosahexaenoic acid inhibits adipocyte differentiation and induces apoptosis in 3T3-L1 preadipocytes. J Nutr 136:2965-9. Kim, J. B., P. Sarraf, M. Wright, K. M. Yao, E. Mueller, G. Solanes, B. B. Lowell, and B. M. Spiegelman. 1998. Nutritional and insulin regulation of fatty acid synthetase and leptin gene expression through ADD1/SREBP1. J Clin Invest 101:1-9. Kim, R. J., C. G. Wilson, M. Wabitsch, M. A. Lazar, and C. M. Steppan. 2006. HIV protease inhibitor-specific alterations in human adipocyte differentiation and metabolism. Obesity (Silver Spring) 14:994-1002. 90 124. 125. 126. 127. 128. 129. 130. 131. 132. 133. 134. 135. 136. 137. 138. 139. Kim, S. S., S. Rhee, K. H. Lee, J. H. Kim, H. S. Kim, M. S. Kang, and C. H. Chung. 1998. Inhibitors of the proteasome block the myogenic differentiation of rat L6 myoblasts. FEBS Lett 433:47-50. Kisselev, A. F., and A. L. Goldberg. 2001. Proteasome inhibitors: from research tools to drug candidates. Chem Biol 8:739-58. Knutson, V. P. 2000. The release of lipoprotein lipase from 3T3-L1 adipocytes is regulated by microvessel endothelial cells in an insulin-dependent manner. Endocrinology 141:693-701. Kolf, C. M., E. Cho, and R. S. Tuan. 2007. Mesenchymal stromal cells. Biology of adult mesenchymal stem cells: regulation of niche, self-renewal and differentiation. Arthritis Res Ther 9:204. Kollet, O., S. Shivtiel, Y. Q. Chen, J. Suriawinata, S. N. Thung, M. D. Dabeva, J. Kahn, A. Spiegel, A. Dar, S. Samira, P. Goichberg, A. Kalinkovich, F. ArenzanaSeisdedos, A. Nagler, I. Hardan, M. Revel, D. A. Shafritz, and T. Lapidot. 2003. HGF, SDF-1, and MMP-9 are involved in stress-induced human CD34+ stem cell recruitment to the liver. J Clin Invest 112:160-9. Kolonin, M. G., P. K. Saha, L. Chan, R. Pasqualini, and W. Arap. 2004. Reversal of obesity by targeted ablation of adipose tissue. Nat Med 10:625-32. Kovsan, J., R. Ben-Romano, S. C. Souza, A. S. Greenberg, and A. Rudich. 2007. Regulation of adipocyte lipolysis by degradation of the perilipin protein: nelfinavir enhances lysosome-mediated perilipin proteolysis. J Biol Chem 282:21704-11. Kralisch, S., M. Bluher, A. Tonjes, U. Lossner, R. Paschke, M. Stumvoll, and M. Fasshauer. 2007. Tissue inhibitor of metalloproteinase-1 predicts adiposity in humans. Eur J Endocrinol 156:257-61. Kubo, Y., S. Kaidzu, I. Nakajima, K. Takenouchi, and F. Nakamura. 2000. Organization of extracellular matrix components during differentiation of adipocytes in long-term culture. In Vitro Cell Dev Biol Anim 36:38-44. Kuri-Harcuch, W., C. Arguello, and M. Marsch-Moreno. 1984. Extracellular matrix production by mouse 3T3-F442A cells during adipose differentiation in culture. Differentiation 28:173-8. Kwan, J. A., C. J. Schulze, W. Wang, H. Leon, M. Sariahmetoglu, M. Sung, J. Sawicka, D. E. Sims, G. Sawicki, and R. Schulz. 2004. Matrix metalloproteinase-2 (MMP-2) is present in the nucleus of cardiac myocytes and is capable of cleaving poly (ADP-ribose) polymerase (PARP) in vitro. Faseb J 18:690-2. Lafontan, M. 2005. Fat cells: afferent and efferent messages define new approaches to treat obesity. Annu Rev Pharmacol Toxicol 45:119-46. Lafontan, M., and M. Berlan. 2003. Do regional differences in adipocyte biology provide new pathophysiological insights? Trends Pharmacol Sci 24:276-83. Lagathu, C., J. P. Bastard, M. Auclair, M. Maachi, M. Kornprobst, J. Capeau, and M. Caron. 2004. Antiretroviral drugs with adverse effects on adipocyte lipid metabolism and survival alter the expression and secretion of proinflammatory cytokines and adiponectin in vitro. Antivir Ther 9:911-20. Lagathu, C., B. Eustace, M. Prot, D. Frantz, Y. Gu, J. P. Bastard, M. Maachi, S. Azoulay, M. Briggs, M. Caron, and J. Capeau. 2007. Some HIV antiretrovirals increase oxidative stress and alter chemokine, cytokine or adiponectin production in human adipocytes and macrophages. Antivir Ther 12:489-500. Lagathu, C., M. Kim, M. Maachi, C. Vigouroux, P. Cervera, J. Capeau, M. Caron, and J. P. Bastard. 2005. HIV antiretroviral treatment alters adipokine expression and insulin sensitivity of adipose tissue in vitro and in vivo. Biochimie 87:65-71. 91 140. 141. 142. 143. 144. 145. 146. 147. 148. 149. 150. 151. 152. 153. 154. 155. Laimer, M., S. Kaser, M. Kranebitter, A. Sandhofer, G. Muhlmann, H. Schwelberger, H. Weiss, J. R. Patsch, and C. F. Ebenbichler. 2005. Effect of pronounced weight loss on the nontraditional cardiovascular risk marker matrix metalloproteinase-9 in middle-aged morbidly obese women. Int J Obes (Lond) 29:498-501. Lambert, E., E. Dasse, B. Haye, and E. Petitfrere. 2004. TIMPs as multifacial proteins. Crit Rev Oncol Hematol 49:187-98. Langin, D., A. Dicker, G. Tavernier, J. Hoffstedt, A. Mairal, M. Ryden, E. Arner, A. Sicard, C. M. Jenkins, N. Viguerie, V. van Harmelen, R. W. Gross, C. Holm, and P. Arner. 2005. Adipocyte lipases and defect of lipolysis in human obesity. Diabetes 54:3190-7. Large, V., S. Reynisdottir, D. Langin, K. Fredby, M. Klannemark, C. Holm, and P. Arner. 1999. Decreased expression and function of adipocyte hormone-sensitive lipase in subcutaneous fat cells of obese subjects. J Lipid Res 40:2059-66. Lenhard, J. M., E. S. Furfine, R. G. Jain, O. Ittoop, L. A. Orband-Miller, S. G. Blanchard, M. A. Paulik, and J. E. Weiel. 2000. HIV protease inhibitors block adipogenesis and increase lipolysis in vitro. Antiviral Res 47:121-9. Letexier, D., C. Pinteur, V. Large, V. Frering, and M. Beylot. 2003. Comparison of the expression and activity of the lipogenic pathway in human and rat adipose tissue. J Lipid Res 44:2127-34. Li, X., H. Y. Huang, J. G. Chen, L. Jiang, H. L. Liu, D. G. Liu, T. J. Song, Q. He, C. G. Ma, D. Ma, H. Y. Song, and Q. Q. Tang. 2006. Lactacystin inhibits 3T3-L1 adipocyte differentiation through induction of CHOP-10 expression. Biochem Biophys Res Commun 350:1-6. Lijnen, H. R., D. Demeulemeester, B. Van Hoef, D. Collen, and E. Maquoi. 2003. Deficiency of tissue inhibitor of matrix metalloproteinase-1 (TIMP-1) impairs nutritionally induced obesity in mice. Thromb Haemost 89:249-55. Lijnen, H. R., E. Maquoi, L. B. Hansen, B. Van Hoef, L. Frederix, and D. Collen. 2002. Matrix metalloproteinase inhibition impairs adipose tissue development in mice. Arterioscler Thromb Vasc Biol 22:374-9. Lijnen, H. R., E. Maquoi, P. Holvoet, A. Mertens, F. Lupu, P. Morange, M. C. Alessi, and I. Juhan-Vague. 2001. Adipose tissue expression of gelatinases in mouse models of obesity. Thromb Haemost 85:1111-6. Lijnen, H. R., H. B. Van, L. Frederix, M. C. Rio, and D. Collen. 2002. Adipocyte hypertrophy in stromelysin-3 deficient mice with nutritionally induced obesity. Thromb Haemost 87:530-5. Lilla, J., D. Stickens, and Z. Werb. 2002. Metalloproteases and adipogenesis: a weighty subject. Am J Pathol 160:1551-4. Lloreta, J., P. Domingo, R. M. Pujol, J. A. Arroyo, N. Baixeras, X. Matias-Guiu, M. Gilaberte, M. A. Sambeat, and S. Serrano. 2002. Ultrastructural features of highly active antiretroviral therapy-associated partial lipodystrophy. Virchows Arch 441:599-604. Lloyd, D. J., R. C. Trembath, and S. Shackleton. 2002. A novel interaction between lamin A and SREBP1: implications for partial lipodystrophy and other laminopathies. Hum Mol Genet 11:769-77. Lolmede, K., V. Durand de Saint Front, J. Galitzky, M. Lafontan, and A. Bouloumie. 2003. Effects of hypoxia on the expression of proangiogenic factors in differentiated 3T3-F442A adipocytes. Int J Obes Relat Metab Disord 27:1187-95. Lumeng, C. N., J. L. Bodzin, and A. R. Saltiel. 2007. Obesity induces a phenotypic switch in adipose tissue macrophage polarization. J Clin Invest 117:175-84. 92 156. 157. 158. 159. 160. 161. 162. 163. 164. 165. 166. 167. 168. 169. 170. 171. 172. Luo, D., B. Mari, I. Stoll, and P. Anglard. 2002. Alternative splicing and promoter usage generates an intracellular stromelysin 3 isoform directly translated as an active matrix metalloproteinase. J Biol Chem 277:25527-36. Madge, S., S. Kinloch-de-Loes, D. Mercey, M. A. Johnson, and I. V. Weller. 1999. Lipodystrophy in patients naive to HIV protease inhibitors. Aids 13:735-7. Mallal, S. A., M. John, C. B. Moore, I. R. James, and E. J. McKinnon. 2000. Contribution of nucleoside analogue reverse transcriptase inhibitors to subcutaneous fat wasting in patients with HIV infection. Aids 14:1309-16. Mannello, F. 2006. Multipotent mesenchymal stromal cell recruitment, migration, and differentiation: what have matrix metalloproteinases got to do with it? Stem Cells 24:1904-7. Mannello, F., F. Luchetti, E. Falcieri, and S. Papa. 2005. Multiple roles of matrix metalloproteinases during apoptosis. Apoptosis 10:19-24. Mannello, F., G. Tonti, and S. Papa. 2005. Matrix metalloproteinase inhibitors as anticancer therapeutics. Curr Cancer Drug Targets 5:285-98. Mannello, F., G. A. Tonti, G. P. Bagnara, and S. Papa. 2006. Role and function of matrix metalloproteinases in the differentiation and biological characterization of mesenchymal stem cells. Stem Cells 24:475-81. Maquoi, E., D. Demeulemeester, G. Voros, D. Collen, and H. R. Lijnen. 2003. Enhanced nutritionally induced adipose tissue development in mice with stromelysin1 gene inactivation. Thromb Haemost 89:696-704. Maquoi, E., C. Munaut, A. Colige, D. Collen, and H. R. Lijnen. 2002. Modulation of adipose tissue expression of murine matrix metalloproteinases and their tissue inhibitors with obesity. Diabetes 51:1093-101. Margeli, A., G. Kouraklis, and S. Theocharis. 2003. Peroxisome proliferator activated receptor-gamma (PPAR-gamma) ligands and angiogenesis. Angiogenesis 6:165-9. Mauriege, P., J. Galitzky, M. Berlan, and M. Lafontan. 1987. Heterogeneous distribution of beta and alpha-2 adrenoceptor binding sites in human fat cells from various fat deposits: functional consequences. Eur J Clin Invest 17:156-65. McBeath, R., D. M. Pirone, C. M. Nelson, K. Bhadriraju, and C. S. Chen. 2004. Cell shape, cytoskeletal tension, and RhoA regulate stem cell lineage commitment. Dev Cell 6:483-95. McComsey, G. A., D. M. Paulsen, J. T. Lonergan, S. M. Hessenthaler, C. L. Hoppel, V. C. Williams, R. L. Fisher, C. L. Cherry, C. White-Owen, K. A. Thompson, S. T. Ross, J. E. Hernandez, and L. L. Ross. 2005. Improvements in lipoatrophy, mitochondrial DNA levels and fat apoptosis after replacing stavudine with abacavir or zidovudine. Aids 19:15-23. McComsey, G. A., and U. A. Walker. 2004. Role of mitochondria in HIV lipoatrophy: insight into pathogenesis and potential therapies. Mitochondrion 4:111-8. McIntosh, K., S. Zvonic, S. Garrett, J. B. Mitchell, Z. E. Floyd, L. Hammill, A. Kloster, Y. Di Halvorsen, J. P. Ting, R. W. Storms, B. Goh, G. Kilroy, X. Wu, and J. M. Gimble. 2006. The immunogenicity of human adipose-derived cells: temporal changes in vitro. Stem Cells 24:1246-53. McIntyre, T. M., A. V. Pontsler, A. R. Silva, A. St Hilaire, Y. Xu, J. C. Hinshaw, G. A. Zimmerman, K. Hama, J. Aoki, H. Arai, and G. D. Prestwich. 2003. Identification of an intracellular receptor for lysophosphatidic acid (LPA): LPA is a transcellular PPARgamma agonist. Proc Natl Acad Sci U S A 100:131-6. Metallo, C. M., J. C. Mohr, C. J. Detzel, J. J. Pablo, B. J. Wie, and S. P. Palecek. 2007. Engineering the stem cell microenvironment. Biotechnol Prog 23:18-23. 93 173. 174. 175. 176. 177. 178. 179. 180. 181. 182. 183. 184. 185. 186. 187. 188. Miranville, A., C. Heeschen, C. Sengenes, C. A. Curat, R. Busse, and A. Bouloumie. 2004. Improvement of postnatal neovascularization by human adipose tissue-derived stem cells. Circulation 110:349-55. Mitchell, J. B., K. McIntosh, S. Zvonic, S. Garrett, Z. E. Floyd, A. Kloster, Y. Di Halvorsen, R. W. Storms, B. Goh, G. Kilroy, X. Wu, and J. M. Gimble. 2006. Immunophenotype of human adipose-derived cells: temporal changes in stromalassociated and stem cell-associated markers. Stem Cells 24:376-85. Miyazaki, T., Y. Kitagawa, K. Toriyama, M. Kobori, and S. Torii. 2005. Isolation of two human fibroblastic cell populations with multiple but distinct potential of mesenchymal differentiation by ceiling culture of mature fat cells from subcutaneous adipose tissue. Differentiation 73:69-78. Mondal, D., V. F. Larussa, and K. C. Agrawal. 2001. Synergistic antiadipogenic effects of HIV type 1 protease inhibitors with tumor necrosis factor alpha: suppression of extracellular insulin action mediated by extracellular matrix-degrading proteases. AIDS Res Hum Retroviruses 17:1569-84. Mori, T., H. Sakaue, H. Iguchi, H. Gomi, Y. Okada, Y. Takashima, K. Nakamura, T. Nakamura, T. Yamauchi, N. Kubota, T. Kadowaki, Y. Matsuki, W. Ogawa, R. Hiramatsu, and M. Kasuga. 2005. Role of Kruppel-like factor 15 (KLF15) in transcriptional regulation of adipogenesis. J Biol Chem 280:12867-75. Mott, J. D., and Z. Werb. 2004. Regulation of matrix biology by matrix metalloproteinases. Curr Opin Cell Biol 16:558-64. Murata, H., P. W. Hruz, and M. Mueckler. 2002. Indinavir inhibits the glucose transporter isoform Glut4 at physiologic concentrations. Aids 16:859-63. Murata, H., P. W. Hruz, and M. Mueckler. 2002. Investigating the cellular targets of HIV protease inhibitors: implications for metabolic disorders and improvements in drug therapy. Curr Drug Targets Infect Disord 2:1-8. Mynarcik, D., L. X. Wei, E. Komaroff, R. Ferris, M. McNurlan, and M. Gelato. 2005. Chronic loss of subcutaneous adipose tissue in HIV-associated lipodystrophy may not be associated with accelerated apoptosis. J Acquir Immune Defic Syndr 38:367-71. Mynarcik, D. C., T. Combs, M. A. McNurlan, P. E. Scherer, E. Komaroff, and M. C. Gelato. 2002. Adiponectin and leptin levels in HIV-infected subjects with insulin resistance and body fat redistribution. J Acquir Immune Defic Syndr 31:51420. Nagase, H., and J. F. Woessner, Jr. 1999. Matrix metalloproteinases. J Biol Chem 274:21491-4. Nakajima, I., T. Yamaguchi, K. Ozutsumi, and H. Aso. 1998. Adipose tissue extracellular matrix: newly organized by adipocytes during differentiation. Differentiation 63:193-200. Neels, J. G., T. Thinnes, and D. J. Loskutoff. 2004. Angiogenesis in an in vivo model of adipose tissue development. Faseb J 18:983-5. Negrel, R., P. Grimaldi, C. Forest, and G. Ailhaud. 1985. Establishment and characterization of fibroblast-like cell lines derived from adipocytes with the capacity to redifferentiate into adipocyte-like cells. Methods Enzymol 109:377-85. Nelson, W. J., and R. Nusse. 2004. Convergence of Wnt, beta-catenin, and cadherin pathways. Science 303:1483-7. Nelson-Dooley, C., M. A. Della-Fera, M. Hamrick, and C. A. Baile. 2005. Novel treatments for obesity and osteoporosis: targeting apoptotic pathways in adipocytes. Curr Med Chem 12:2215-25. 94 189. 190. 191. 192. 193. 194. 195. 196. 197. 198. 199. 200. 201. 202. Nishimura, S., I. Manabe, M. Nagasaki, Y. Hosoya, H. Yamashita, H. Fujita, M. Ohsugi, K. Tobe, T. Kadowaki, R. Nagai, and S. Sugiura. 2007. Adipogenesis in obesity requires close interplay between differentiating adipocytes, stromal cells, and blood vessels. Diabetes 56:1517-26. Nolan, D., E. Hammond, I. James, E. McKinnon, and S. Mallal. 2003. Contribution of nucleoside-analogue reverse transcriptase inhibitor therapy to lipoatrophy from the population to the cellular level. Antivir Ther 8:617-26. O'Connor, K. C., H. Song, N. Rosenzweig, and D. A. Jansen. 2003. Extracellular matrix substrata alter adipocyte yield and lipogenesis in primary cultures of stromalvascular cells from human adipose. Biotechnol Lett 25:1967-72. Odegaard, J. I., R. R. Ricardo-Gonzalez, M. H. Goforth, C. R. Morel, V. Subramanian, L. Mukundan, A. R. Eagle, D. Vats, F. Brombacher, A. W. Ferrante, and A. Chawla. 2007. Macrophage-specific PPARgamma controls alternative activation and improves insulin resistance. Nature 447:1116-20. Oh, J., R. Takahashi, S. Kondo, A. Mizoguchi, E. Adachi, R. M. Sasahara, S. Nishimura, Y. Imamura, H. Kitayama, D. B. Alexander, C. Ide, T. P. Horan, T. Arakawa, H. Yoshida, S. Nishikawa, Y. Itoh, M. Seiki, S. Itohara, C. Takahashi, and M. Noda. 2001. The membrane-anchored MMP inhibitor RECK is a key regulator of extracellular matrix integrity and angiogenesis. Cell 107:789-800. Oishi, Y., I. Manabe, K. Tobe, K. Tsushima, T. Shindo, K. Fujiu, G. Nishimura, K. Maemura, T. Yamauchi, N. Kubota, R. Suzuki, T. Kitamura, S. Akira, T. Kadowaki, and R. Nagai. 2005. Kruppel-like transcription factor KLF5 is a key regulator of adipocyte differentiation. Cell Metab 1:27-39. O'Reilly, M. S., L. Holmgren, Y. Shing, C. Chen, R. A. Rosenthal, M. Moses, W. S. Lane, Y. Cao, E. H. Sage, and J. Folkman. 1994. Angiostatin: a novel angiogenesis inhibitor that mediates the suppression of metastases by a Lewis lung carcinoma. Cell 79:315-28. Osuga, J., S. Ishibashi, T. Oka, H. Yagyu, R. Tozawa, A. Fujimoto, F. Shionoiri, N. Yahagi, F. B. Kraemer, O. Tsutsumi, and N. Yamada. 2000. Targeted disruption of hormone-sensitive lipase results in male sterility and adipocyte hypertrophy, but not in obesity. Proc Natl Acad Sci U S A 97:787-92. Otto, T. C., R. R. Bowers, and M. D. Lane. 2007. BMP-4 treatment of C3H10T1/2 stem cells blocks expression of MMP-3 and MMP-13. Biochem Biophys Res Commun 353:1097-104. Pacenti, M., L. Barzon, F. Favaretto, K. Fincati, S. Romano, G. Milan, R. Vettor, and G. Palu. 2006. Microarray analysis during adipogenesis identifies new genes altered by antiretroviral drugs. Aids 20:1691-705. Page-McCaw, A., A. J. Ewald, and Z. Werb. 2007. Matrix metalloproteinases and the regulation of tissue remodelling. Nat Rev Mol Cell Biol 8:221-33. Pajonk, F., J. Himmelsbach, K. Riess, A. Sommer, and W. H. McBride. 2002. The human immunodeficiency virus (HIV)-1 protease inhibitor saquinavir inhibits proteasome function and causes apoptosis and radiosensitization in non-HIVassociated human cancer cells. Cancer Res 62:5230-5. Pajvani, U. B., M. E. Trujillo, T. P. Combs, P. Iyengar, L. Jelicks, K. A. Roth, R. N. Kitsis, and P. E. Scherer. 2005. Fat apoptosis through targeted activation of caspase 8: a new mouse model of inducible and reversible lipoatrophy. Nat Med 11:797-803. Parker, R. A., O. P. Flint, R. Mulvey, C. Elosua, F. Wang, W. Fenderson, S. Wang, W. P. Yang, and M. A. Noor. 2005. Endoplasmic reticulum stress links 95 203. 204. 205. 206. 207. 208. 209. 210. 211. 212. 213. 214. 215. 216. 217. dyslipidemia to inhibition of proteasome activity and glucose transport by HIV protease inhibitors. Mol Pharmacol 67:1909-19. Parks, W. C., C. L. Wilson, and Y. S. Lopez-Boado. 2004. Matrix metalloproteinases as modulators of inflammation and innate immunity. Nat Rev Immunol 4:617-29. Pei, D., and S. J. Weiss. 1995. Furin-dependent intracellular activation of the human stromelysin-3 zymogen. Nature 375:244-7. Pendas, A. M., A. R. Folgueras, E. Llano, J. Caterina, F. Frerard, F. Rodriguez, A. Astudillo, A. Noel, H. Birkedal-Hansen, and C. Lopez-Otin. 2004. Diet-induced obesity and reduced skin cancer susceptibility in matrix metalloproteinase 19deficient mice. Mol Cell Biol 24:5304-13. Pendas, A. M., Z. Zhou, J. Cadinanos, J. M. Freije, J. Wang, K. Hultenby, A. Astudillo, A. Wernerson, F. Rodriguez, K. Tryggvason, and C. Lopez-Otin. 2002. Defective prelamin A processing and muscular and adipocyte alterations in Zmpste24 metalloproteinase-deficient mice. Nat Genet 31:94-9. Phillips, B. W., C. Vernochet, and C. Dani. 2003. Differentiation of embryonic stem cells for pharmacological studies on adipose cells. Pharmacol Res 47:263-8. Piccinini, M., M. T. Rinaudo, A. Anselmino, B. Buccinna, C. Ramondetti, A. Dematteis, E. Ricotti, L. Palmisano, M. Mostert, and P. A. Tovo. 2005. The HIV protease inhibitors nelfinavir and saquinavir, but not a variety of HIV reverse transcriptase inhibitors, adversely affect human proteasome function. Antivir Ther 10:215-23. Pistrosch, F., K. Herbrig, U. Oelschlaegel, S. Richter, J. Passauer, S. Fischer, and P. Gross. 2005. PPARgamma-agonist rosiglitazone increases number and migratory activity of cultured endothelial progenitor cells. Atherosclerosis 183:163-7. Pittenger, M. F., A. M. Mackay, S. C. Beck, R. K. Jaiswal, R. Douglas, J. D. Mosca, M. A. Moorman, D. W. Simonetti, S. Craig, and D. R. Marshak. 1999. Multilineage potential of adult human mesenchymal stem cells. Science 284:143-7. Planat-Benard, V., J. S. Silvestre, B. Cousin, M. Andre, M. Nibbelink, R. Tamarat, M. Clergue, C. Manneville, C. Saillan-Barreau, M. Duriez, A. Tedgui, B. Levy, L. Penicaud, and L. Casteilla. 2004. Plasticity of human adipose lineage cells toward endothelial cells: physiological and therapeutic perspectives. Circulation 109:656-63. Prince, A. M., J. S. May, G. R. Burton, R. E. Lyle, and R. E. McGehee, Jr. 2002. Proteasomal degradation of retinoblastoma-related p130 during adipocyte differentiation. Biochem Biophys Res Commun 290:1066-71. Prins, J. B., C. U. Niesler, C. M. Winterford, N. A. Bright, K. Siddle, S. O'Rahilly, N. I. Walker, and D. P. Cameron. 1997. Tumor necrosis factor-alpha induces apoptosis of human adipose cells. Diabetes 46:1939-44. Prins, J. B., and S. O'Rahilly. 1997. Regulation of adipose cell number in man. Clin Sci (Lond) 92:3-11. Proulx, A., P. A. Merrifield, and C. C. Naus. 1997. Blocking gap junctional intercellular communication in myoblasts inhibits myogenin and MRF4 expression. Dev Genet 20:133-44. Qi, J. H., Q. Ebrahem, N. Moore, G. Murphy, L. Claesson-Welsh, M. Bond, A. Baker, and B. Anand-Apte. 2003. A novel function for tissue inhibitor of metalloproteinases-3 (TIMP3): inhibition of angiogenesis by blockage of VEGF binding to VEGF receptor-2. Nat Med 9:407-15. Rajagopalan, S., X. P. Meng, S. Ramasamy, D. G. Harrison, and Z. S. Galis. 1996. Reactive oxygen species produced by macrophage-derived foam cells regulate 96 218. 219. 220. 221. 222. 223. 224. 225. 226. 227. 228. 229. 230. 231. 232. 233. 234. the activity of vascular matrix metalloproteinases in vitro. Implications for atherosclerotic plaque stability. J Clin Invest 98:2572-9. Ranganathan, S., and P. A. Kern. 2002. The HIV protease inhibitor saquinavir impairs lipid metabolism and glucose transport in cultured adipocytes. J Endocrinol 172:155-62. Ray, H., M. Beylot, P. Arner, D. Larrouy, D. Langin, C. Holm, and V. Large. 2003. The presence of a catalytically inactive form of hormone-sensitive lipase is associated with decreased lipolysis in abdominal subcutaneous adipose tissue of obese subjects. Diabetes 52:1417-22. Raza, S. L., L. C. Nehring, S. D. Shapiro, and L. A. Cornelius. 2000. Proteinaseactivated receptor-1 regulation of macrophage elastase (MMP-12) secretion by serine proteinases. J Biol Chem 275:41243-50. Rehman, J., D. Traktuev, J. Li, S. Merfeld-Clauss, C. J. Temm-Grove, J. E. Bovenkerk, C. L. Pell, B. H. Johnstone, R. V. Considine, and K. L. March. 2004. Secretion of angiogenic and antiapoptotic factors by human adipose stromal cells. Circulation 109:1292-8. Reitman, M. L., E. Arioglu, O. Gavrilova, and S. I. Taylor. 2000. Lipoatrophy revisited. Trends Endocrinol Metab 11:410-6. Reyes, M., A. Dudek, B. Jahagirdar, L. Koodie, P. H. Marker, and C. M. Verfaillie. 2002. Origin of endothelial progenitors in human postnatal bone marrow. J Clin Invest 109:337-46. Roche, R., I. Poizot-Martin, C. M. Yazidi, E. Compe, J. A. Gastaut, J. Torresani, and R. Planells. 2002. Effects of antiretroviral drug combinations on the differentiation of adipocytes. Aids 16:13-20. Rosell, S., and E. Belfrage. 1979. Blood circulation in adipose tissue. Physiol Rev 59:1078-1104. Rosen, E. D., and O. A. MacDougald. 2006. Adipocyte differentiation from the inside out. Nat Rev Mol Cell Biol 7:885-96. Rosen, E. D., and B. M. Spiegelman. 2000. Molecular regulation of adipogenesis. Annu Rev Cell Dev Biol 16:145-71. Rosen, E. D., C. J. Walkey, P. Puigserver, and B. M. Spiegelman. 2000. Transcriptional regulation of adipogenesis. Genes Dev 14:1293-307. Ross, J., and L. Li. 2006. Recent advances in understanding extrinsic control of hematopoietic stem cell fate. Curr Opin Hematol 13:237-42. Ross, S. E., N. Hemati, K. A. Longo, C. N. Bennett, P. C. Lucas, R. L. Erickson, and O. A. MacDougald. 2000. Inhibition of adipogenesis by Wnt signaling. Science 289:950-3. Rudich, A., S. Vanounou, K. Riesenberg, M. Porat, A. Tirosh, I. HarmanBoehm, A. S. Greenberg, F. Schlaeffer, and N. Bashan. 2001. The HIV protease inhibitor nelfinavir induces insulin resistance and increases basal lipolysis in 3T3-L1 adipocytes. Diabetes 50:1425-31. Rundhaug, J. E. 2005. Matrix metalloproteinases and angiogenesis. J Cell Mol Med 9:267-85. Rupnick, M. A., D. Panigrahy, C. Y. Zhang, S. M. Dallabrida, B. B. Lowell, R. Langer, and M. J. Folkman. 2002. Adipose tissue mass can be regulated through the vasculature. Proc Natl Acad Sci U S A 99:10730-5. Sabatakos, G., N. A. Sims, J. Chen, K. Aoki, M. B. Kelz, M. Amling, Y. Bouali, K. Mukhopadhyay, K. Ford, E. J. Nestler, and R. Baron. 2000. Overexpression of DeltaFosB transcription factor(s) increases bone formation and inhibits adipogenesis. Nat Med 6:985-90. 97 235. 236. 237. 238. 239. 240. 241. 242. 243. 244. 245. 246. 247. 248. 249. 250. Saillan-Barreau, C., B. Cousin, M. Andre, P. Villena, L. Casteilla, and L. Penicaud. 2003. Human adipose cells as candidates in defense and tissue remodeling phenomena. Biochem Biophys Res Commun 309:502-5. Sato, H., and M. Seiki. 1993. Regulatory mechanism of 92 kDa type IV collagenase gene expression which is associated with invasiveness of tumor cells. Oncogene 8:395-405. Schiller, P. C., G. D'Ippolito, W. Balkan, B. A. Roos, and G. A. Howard. 2001. Gap-junctional communication is required for the maturation process of osteoblastic cells in culture. Bone 28:362-9. Schiller, P. C., G. D'Ippolito, R. Brambilla, B. A. Roos, and G. A. Howard. 2001. Inhibition of gap-junctional communication induces the trans-differentiation of osteoblasts to an adipocytic phenotype in vitro. J Biol Chem 276:14133-8. Schmidtke, G., H. G. Holzhutter, M. Bogyo, N. Kairies, M. Groll, R. de Giuli, S. Emch, and M. Groettrup. 1999. How an inhibitor of the HIV-I protease modulates proteasome activity. J Biol Chem 274:35734-40. Sengenes, C., A. Bouloumie, H. Hauner, M. Berlan, R. Busse, M. Lafontan, and J. Galitzky. 2003. Involvement of a cGMP-dependent pathway in the natriuretic peptide-mediated hormone-sensitive lipase phosphorylation in human adipocytes. J Biol Chem 278:48617-26. Sengenes, C., K. Lolmede, A. Zakaroff-Girard, R. Busse, and A. Bouloumie. 2005. Preadipocytes in the human subcutaneous adipose tissue display distinct features from the adult mesenchymal and hematopoietic stem cells. J Cell Physiol 205:114-22. Sengenes, C., A. Miranville, M. Maumus, S. de Barros, R. Busse, and A. Bouloumie. 2007. Chemotaxis and Differentiation of Human Adipose Tissue CD34+/CD31- Progenitor Cells: Role of SDF-1 Released by Adipose Tissue Capillary Endothelial Cells. Stem Cells. Seo, D. W., H. Li, L. Guedez, P. T. Wingfield, T. Diaz, R. Salloum, B. Y. Wei, and W. G. Stetler-Stevenson. 2003. TIMP-2 mediated inhibition of angiogenesis: an MMP-independent mechanism. Cell 114:171-80. Shankar, S. S., and M. P. Dube. 2004. Clinical aspects of endothelial dysfunction associated with human immunodeficiency virus infection and antiretroviral agents. Cardiovasc Toxicol 4:261-9. Shikuma, C. M., N. Hu, C. Milne, F. Yost, C. Waslien, S. Shimizu, and B. Shiramizu. 2001. Mitochondrial DNA decrease in subcutaneous adipose tissue of HIV-infected individuals with peripheral lipoatrophy. Aids 15:1801-9. Shipley, J. M., R. L. Wesselschmidt, D. K. Kobayashi, T. J. Ley, and S. D. Shapiro. 1996. Metalloelastase is required for macrophage-mediated proteolysis and matrix invasion in mice. Proc Natl Acad Sci U S A 93:3942-6. Silha, J. V., M. Krsek, P. Sucharda, and L. J. Murphy. 2005. Angiogenic factors are elevated in overweight and obese individuals. Int J Obes (Lond) 29:1308-14. Si-Tayeb, K., A. Monvoisin, C. Mazzocco, S. Lepreux, M. Decossas, G. Cubel, D. Taras, J. F. Blanc, D. R. Robinson, and J. Rosenbaum. 2006. Matrix metalloproteinase 3 is present in the cell nucleus and is involved in apoptosis. Am J Pathol 169:1390-401. Sjostrom, L., U. Smith, M. Krotkiewski, and P. Bjorntorp. 1972. Cellularity in different regions of adipose tissue in young men and women. Metabolism 21:114353. Sorisky, A., R. Magun, and A. M. Gagnon. 2000. Adipose cell apoptosis: death in the energy depot. Int J Obes Relat Metab Disord 24 Suppl 4:S3-7. 98 251. 252. 253. 254. 255. 256. 257. 258. 259. 260. 261. 262. 263. 264. 265. 266. 267. 268. Sottrup-Jensen, L., and H. Birkedal-Hansen. 1989. Human fibroblast collagenasealpha-macroglobulin interactions. Localization of cleavage sites in the bait regions of five mammalian alpha-macroglobulins. J Biol Chem 264:393-401. Spiegelman, B. M., and S. R. Farmer. 1982. Decreases in tubulin and actin gene expression prior to morphological differentiation of 3T3 adipocytes. Cell 29:53-60. Spinale, F. G. 2002. Matrix metalloproteinases: regulation and dysregulation in the failing heart. Circ Res 90:520-30. Sternlicht, M. D., and Z. Werb. 2001. How matrix metalloproteinases regulate cell behavior. Annu Rev Cell Dev Biol 17:463-516. Stich, V., I. De Glisezinski, F. Crampes, J. Hejnova, J. M. Cottet-Emard, J. Galitzky, M. Lafontan, D. Riviere, and M. Berlan. 2000. Activation of alpha(2)adrenergic receptors impairs exercise-induced lipolysis in SCAT of obese subjects. Am J Physiol Regul Integr Comp Physiol 279:R499-504. St-Pierre, Y., J. Couillard, and C. Van Themsche. 2004. Regulation of MMP-9 gene expression for the development of novel molecular targets against cancer and inflammatory diseases. Expert Opin Ther Targets 8:473-89. Streuli, C. 1999. Extracellular matrix remodelling and cellular differentiation. Curr Opin Cell Biol 11:634-40. Strongin, A. Y., I. Collier, G. Bannikov, B. L. Marmer, G. A. Grant, and G. I. Goldberg. 1995. Mechanism of cell surface activation of 72-kDa type IV collagenase. Isolation of the activated form of the membrane metalloprotease. J Biol Chem 270:5331-8. Sutinen, J., E. Korsheninnikova, T. Funahashi, Y. Matsuzawa, T. Nyman, and H. Yki-Jarvinen. 2003. Circulating concentration of adiponectin and its expression in subcutaneous adipose tissue in patients with highly active antiretroviral therapyassociated lipodystrophy. J Clin Endocrinol Metab 88:1907-10. Taleb, S., R. Cancello, K. Clement, and D. Lacasa. 2006. Cathepsin s promotes human preadipocyte differentiation: possible involvement of fibronectin degradation. Endocrinology 147:4950-9. Tang, Q. Q., T. C. Otto, and M. D. Lane. 2004. Commitment of C3H10T1/2 pluripotent stem cells to the adipocyte lineage. Proc Natl Acad Sci U S A 101:960711. Tchoukalova, Y., C. Koutsari, and M. Jensen. 2007. Committed subcutaneous preadipocytes are reduced in human obesity. Diabetologia 50:151-7. Tedeschi. 1965. Pathological anatomy of adipose tissue.:141-68. Tran, H., S. Robinson, I. Mikhailenko, and D. K. Strickland. 2003. Modulation of the LDL receptor and LRP levels by HIV protease inhibitors. J Lipid Res 44:1859-69. Trayhurn, P., and J. H. Beattie. 2001. Physiological role of adipose tissue: white adipose tissue as an endocrine and secretory organ. Proc Nutr Soc 60:329-39. Trujillo, M. E., U. B. Pajvani, and P. E. Scherer. 2005. Apoptosis through targeted activation of caspase 8 ("ATTAC-mice"): novel mouse models of inducible and reversible tissue ablation. Cell Cycle 4:1141-5. Umezawa, A., and J. Hata. 1992. Expression of gap-junctional protein (connexin 43 or alpha 1 gap junction) is down-regulated at the transcriptional level during adipocyte differentiation of H-1/A marrow stromal cells. Cell Struct Funct 17:177-84. van der Valk, M., G. Allick, G. J. Weverling, J. A. Romijn, M. T. Ackermans, J. M. Lange, B. L. van Eck-Smit, C. van Kuijk, E. Endert, H. P. Sauerwein, and P. Reiss. 2004. Markedly diminished lipolysis and partial restoration of glucose metabolism, without changes in fat distribution after extended discontinuation of 99 269. 270. 271. 272. 273. 274. 275. 276. 277. 278. 279. 280. 281. 282. protease inhibitors in severe lipodystrophic human immunodeficient virus-1-infected patients. J Clin Endocrinol Metab 89:3554-60. van der Valk, M., E. H. Gisolf, P. Reiss, F. W. Wit, A. Japour, G. J. Weverling, and S. A. Danner. 2001. Increased risk of lipodystrophy when nucleoside analogue reverse transcriptase inhibitors are included with protease inhibitors in the treatment of HIV-1 infection. Aids 15:847-55. Van Harmelen, V., K. Rohrig, and H. Hauner. 2004. Comparison of proliferation and differentiation capacity of human adipocyte precursor cells from the omental and subcutaneous adipose tissue depot of obese subjects. Metabolism 53:632-7. van Harmelen, V., T. Skurk, K. Rohrig, Y. M. Lee, M. Halbleib, I. AprathHusmann, and H. Hauner. 2003. Effect of BMI and age on adipose tissue cellularity and differentiation capacity in women. Int J Obes Relat Metab Disord 27:889-95. Vankoningsloo, S., A. De Pauw, A. Houbion, S. Tejerina, C. Demazy, F. de Longueville, V. Bertholet, P. Renard, J. Remacle, P. Holvoet, M. Raes, and T. Arnould. 2006. CREB activation induced by mitochondrial dysfunction triggers triglyceride accumulation in 3T3-L1 preadipocytes. J Cell Sci 119:1266-82. Vernochet, C., S. Azoulay, D. Duval, R. Guedj, G. Ailhaud, and C. Dani. 2003. Differential effect of HIV protease inhibitors on adipogenesis: intracellular ritonavir is not sufficient to inhibit differentiation. Aids 17:2177-80. Vernochet, C., S. Azoulay, D. Duval, R. Guedj, F. Cottrez, H. Vidal, G. Ailhaud, and C. Dani. 2005. Human immunodeficiency virus protease inhibitors accumulate into cultured human adipocytes and alter expression of adipocytokines. J Biol Chem 280:2238-43. Vigouroux, C., M. Maachi, T. H. Nguyen, C. Coussieu, S. Gharakhanian, T. Funahashi, Y. Matsuzawa, I. Shimomura, W. Rozenbaum, J. Capeau, and J. P. Bastard. 2003. Serum adipocytokines are related to lipodystrophy and metabolic disorders in HIV-infected men under antiretroviral therapy. Aids 17:1503-11. Villarroya, F., P. Domingo, and M. Giralt. 2007. Lipodystrophy in HIV 1-infected patients: lessons for obesity research. Int J Obes (Lond). Villena, J. A., S. Roy, E. Sarkadi-Nagy, K. H. Kim, and H. S. Sul. 2004. Desnutrin, an adipocyte gene encoding a novel patatin domain-containing protein, is induced by fasting and glucocorticoids: ectopic expression of desnutrin increases triglyceride hydrolysis. J Biol Chem 279:47066-75. Vincent, S., F. Tourniaire, C. M. El Yazidi, E. Compe, O. Manches, R. Plannels, and R. Roche. 2004. Nelfinavir induces necrosis of 3T3F44-2A adipocytes by oxidative stress. J Acquir Immune Defic Syndr 37:1556-62. Voorhees, P. M., and R. Z. Orlowski. 2006. The proteasome and proteasome inhibitors in cancer therapy. Annu Rev Pharmacol Toxicol 46:189-213. Vu, T. H., and Z. Werb. 2000. Matrix metalloproteinases: effectors of development and normal physiology. Genes Dev 14:2123-33. Walker, U. A., M. Bickel, S. I. Lutke Volksbeck, U. P. Ketelsen, H. Schofer, B. Setzer, N. Venhoff, V. Rickerts, and S. Staszewski. 2002. Evidence of nucleoside analogue reverse transcriptase inhibitor--associated genetic and structural defects of mitochondria in adipose tissue of HIV-infected patients. J Acquir Immune Defic Syndr 29:117-21. Wang, C. H., N. Ciliberti, S. H. Li, P. E. Szmitko, R. D. Weisel, P. W. Fedak, M. Al-Omran, W. J. Cherng, R. K. Li, W. L. Stanford, and S. Verma. 2004. Rosiglitazone facilitates angiogenic progenitor cell differentiation toward endothelial lineage: a new paradigm in glitazone pleiotropy. Circulation 109:1392-400. 100 283. 284. 285. 286. 287. 288. 289. 290. 291. 292. 293. 294. 295. 296. 297. 298. 299. 300. Wang, E. A., D. I. Israel, S. Kelly, and D. P. Luxenberg. 1993. Bone morphogenetic protein-2 causes commitment and differentiation in C3H10T1/2 and 3T3 cells. Growth Factors 9:57-71. Wang, X., R. Sato, M. S. Brown, X. Hua, and J. L. Goldstein. 1994. SREBP-1, a membrane-bound transcription factor released by sterol-regulated proteolysis. Cell 77:53-62. Wassermann, F. 1965. The development of adipose tissue. Renold A, Cahill G (eds). Weisberg, S. P., D. McCann, M. Desai, M. Rosenbaum, R. L. Leibel, and A. W. Ferrante, Jr. 2003. Obesity is associated with macrophage accumulation in adipose tissue. J Clin Invest 112:1796-808. Weiss, S. J., G. Peppin, X. Ortiz, C. Ragsdale, and S. T. Test. 1985. Oxidative autoactivation of latent collagenase by human neutrophils. Science 227:747-9. Wentworth, J. M., T. P. Burris, and V. K. Chatterjee. 2000. HIV protease inhibitors block human preadipocyte differentiation, but not via the PPARgamma/RXR heterodimer. J Endocrinol 164:R7-R10. Westermarck, J., and V. M. Kahari. 1999. Regulation of matrix metalloproteinase expression in tumor invasion. Faseb J 13:781-92. Woessner, J. F., Jr. 1991. Matrix metalloproteinases and their inhibitors in connective tissue remodeling. Faseb J 5:2145-54. Wosnitza, M., K. Hemmrich, A. Groger, S. Graber, and N. Pallua. 2007. Plasticity of human adipose stem cells to perform adipogenic and endothelial differentiation. Differentiation 75:12-23. Wu, J., S. V. Srinivasan, J. C. Neumann, and J. B. Lingrel. 2005. The KLF2 transcription factor does not affect the formation of preadipocytes but inhibits their differentiation into adipocytes. Biochemistry 44:11098-105. Xu, H., G. T. Barnes, Q. Yang, G. Tan, D. Yang, C. J. Chou, J. Sole, A. Nichols, J. S. Ross, L. A. Tartaglia, and H. Chen. 2003. Chronic inflammation in fat plays a crucial role in the development of obesity-related insulin resistance. J Clin Invest 112:1821-30. Yamamoto, Y., and R. B. Gaynor. 2001. Therapeutic potential of inhibition of the NF-kappaB pathway in the treatment of inflammation and cancer. J Clin Invest 107:135-42. Yan, C., and D. D. Boyd. 2007. Regulation of matrix metalloproteinase gene expression. J Cell Physiol 211:19-26. Yanagiya, T., A. Tanabe, and K. Hotta. 2007. Gap-junctional communication is required for mitotic clonal expansion during adipogenesis. Obesity (Silver Spring) 15:572-82. Young, S. G., B. S. Davies, L. G. Fong, P. Gin, M. M. Weinstein, A. Bensadoun, and A. P. Beigneux. 2007. GPIHBP1: an endothelial cell molecule important for the lipolytic processing of chylomicrons. Curr Opin Lipidol 18:389-96. Yu, W. H., S. Yu, Q. Meng, K. Brew, and J. F. Woessner, Jr. 2000. TIMP-3 binds to sulfated glycosaminoglycans of the extracellular matrix. J Biol Chem 275:3122632. Zavrski, I., H. Krebbel, B. Wildemann, U. Heider, M. Kaiser, K. Possinger, and O. Sezer. 2005. Proteasome inhibitors abrogate osteoclast differentiation and osteoclast function. Biochem Biophys Res Commun 333:200-5. Zhang, B., K. MacNaul, D. Szalkowski, Z. Li, J. Berger, and D. E. Moller. 1999. Inhibition of adipocyte differentiation by HIV protease inhibitors. J Clin Endocrinol Metab 84:4274-7. 101 301. 302. 303. 304. Zhang, Q. X., C. J. Magovern, C. A. Mack, K. T. Budenbender, W. Ko, and T. K. Rosengart. 1997. Vascular endothelial growth factor is the major angiogenic factor in omentum: mechanism of the omentum-mediated angiogenesis. J Surg Res 67:147-54. Zhang, Y., R. Proenca, M. Maffei, M. Barone, L. Leopold, and J. M. Friedman. 1994. Positional cloning of the mouse obese gene and its human homologue. Nature 372:425-32. Zimmermann, R., J. G. Strauss, G. Haemmerle, G. Schoiswohl, R. BirnerGruenberger, M. Riederer, A. Lass, G. Neuberger, F. Eisenhaber, A. Hermetter, and R. Zechner. 2004. Fat mobilization in adipose tissue is promoted by adipose triglyceride lipase. Science 306:1383-6. Zuk, P. A., M. Zhu, P. Ashjian, D. A. De Ugarte, J. I. Huang, H. Mizuno, Z. C. Alfonso, J. K. Fraser, P. Benhaim, and M. H. Hedrick. 2002. Human adipose tissue is a source of multipotent stem cells. Mol Biol Cell 13:4279-95. 102 Annexes Publication 3 : Chemotaxis and Differentiation of Human Adipose Tissue CD34+/CD31- Progenitor Cells: Role of SDF-1 Released by Adipose Tissue Capillary Endothelial Cells Coralie Sengenès, Alexandra Miranville, Marie Maumus, Sandra de Barros, Rudi Busse and Anne Bouloumié. Stem Cells, 2007 103 TISSUE-SPECIFIC STEM CELLS Chemotaxis and Differentiation of Human Adipose Tissue CD34ⴙ/ CD31ⴚ Progenitor Cells: Role of Stromal Derived Factor-1 Released by Adipose Tissue Capillary Endothelial Cells CORALIE SENGENÈS,a ALEXANDRA MIRANVILLE,b MARIE MAUMUS,a SANDRA ANNE BOULOUMIÉa DE BARROS,a RUDI BUSSE,b a Institut National de la Santé et de la Recherche Médicale, U858, AVENIR Team, I2MR, Paul Sabatier University, IFR31, Toulouse, France; bInstitute of Cardiovascular Physiology, Johann Wolfgang Goethe University, Frankfurt am Main, Germany ABSTRACT The native CD34ⴙ/CD31ⴚ cell population present in the stroma-vascular fraction of human adipose tissue (hAT) displays progenitor cell properties since they exhibit adipocyte- and endothelial cell-like phenotypes under appropriate stimuli. To analyze the signals within hAT regulating their phenotypes, the influence of hAT-derived capillary endothelial cells (CECs) was studied on the chemotaxis and differentiation of the hAT-CD34ⴙ/CD31ⴚ cells. Conditioned medium from hAT-CECs led to a strong chemotaxis of the hAT-CD34ⴙ/CD31ⴚ cells that was inhibited with pretreatments with pertussis toxin, CXCR-4 antagonist, or neutralizing antibodies. Furthermore, hAT-CECs produced and secreted the CXCR-4 ligand, that is, the stromal derived factor-1 (SDF-1). Finally, hAT-CECs induced the differen- tiation of hAT-CD34ⴙ/CD31ⴚ cells toward an endothelial cell (EC) phenotype. Indeed, hAT-CECs and -CD34ⴙ/ CD31ⴚ cell coculture stimulated in a two-dimensional system the expression of the EC CD31 marker by the hATprogenitor cells and, in a three-dimensional approach, the formation of capillary-like structures via a SDF-1/CXCR-4 dependent pathway. Thus, the migration and differentiation of hAT progenitor cells are modulated by hAT-CEC-derived factors. SDF-1, which is secreted by hAT-derived CECs, and its receptor CXCR-4, expressed by hAT-derived progenitor cells, may promote chemotaxis and differentiation of hATderived progenitor cells and thus contribute to the formation of the vascular network during the development of hAT. STEM CELLS 2007;25:2269 –2276 Disclosure of potential conflicts of interest is found at the end of this article. INTRODUCTION The excessive human adipose tissue (hAT) development is associated with adipocyte hypertrophy and hyperplasia [1, 2] as well as an extension of the capillary network [3–5]. The processes involved in the increased number of mature adipocytes as well as the neovascularization within the fat mass are still to be clearly defined. We have described a cell population, present in the native stroma-vascular fraction (SVF) of hAT, characterized as positive for the hematopoietic stem cell marker CD34 and negative for the endothelial cell marker CD31. The CD34⫹/ CD31⫺ cell population was the only cell population of the SVF under adipogenic culture conditions among the capillary endothelial cells (CECs), the macrophages, and the cells negative for the CD34, CD31, and CD14 markers able to express adipocytespecific markers and metabolic lipolytic and lipogenic activities. Furthermore, under endothelial cell culture conditions, the CD34⫹/CD31⫺ cells changed their morphology and organization and expressed endothelial cell (EC)-specific markers such as CD31 and von Willebrand factor [5]. In vivo, their injection led to an increase in blood flow and capillary density within the ischemic muscle in the athymic mouse model of hindlimb ischemia, whereas injection with native hAT-derived CD34⫺ cells exerted no effects [5]. Other laboratories have reported similar proangiogenic abilities of the whole adipose tissue (AT) adherent SVF cells [6, 7]. The further characterization of the native CD34⫹/CD31⫺ cells has shown that they did not express the classic mesenchymal stem cell markers (CD105 and Stro-1) and displayed different features from the adult hematopoietic stem cells since they did not form blood colony in hematopoietic assays [8]. Thus, the native CD34⫹/CD31⫺ cell population of hAT can be considered a local pool of adipocyte as well as endothelial progenitor cells that might play a role in the formation of adipocytes but also of capillaries accompanying the development of the fat mass. Since the microenvironment, that is, soluble factors such as the stromal derived factor-1 (SDF-1) [9 –11], cellular, and extracellular matrix components have been shown to regulate the biology of hematopoietic and mesenchymal stem cells [12–14], the present study was undertaken to characterize the effects of signals arising from hAT microenvironment on the chemotaxis and differentiation of the hAT progenitor cells. Our data delineate the concept that hAT-derived CECs induce the chemotaxis and support the endothelial Correspondence: Coralie Sengenès, Ph.D., Team 1, “Vascular network, progenitor cells and immune cells from adipose tissue,” Institut National de la Santé et de la Recherche Médicale U858/I2MR, BP84225, 31432 Toulouse Cedex 4, France. Telephone: ⫹33 5 6114 5975; Fax: ⫹33 5 6125 5116; e-mail: [email protected] Received March 14, 2007; accepted for publication May 17, 2007; first published online in STEM CELLS EXPRESS May 24, 2007. ©AlphaMed Press 1066-5099/2007/$30.00/0 doi: 10.1634/ stemcells.2007-0180 STEM CELLS 2007;25:2269 –2276 www.StemCells.com Downloaded from www.StemCells.com at Inserm Disc Doc on September 7, 2007 Key Words. Human CD34⫹ cells • Stromal derived factor-1 • Endothelial differentiation • Chemotaxis • CXCR-4 • Matrigel Microvasculature • Progenitor cells Adipose Tissue Stem and Endothelial Cell Crosstalk 2270 differentiation potential of the hAT-derived progenitor cells via the SDF-1/CXCR-4 axis within hAT. human AT-derived CECs and no statistical significant differences were found (not shown). Transmigration Assay MATERIALS AND METHODS Isolation of the SVF from hAT Isolation of the CD34ⴙ/CD31ⴚ Progenitor Cells and the CD34ⴙ/CD31ⴙ CECs from the SVF of hAT CD34⫹ cells were isolated from the SVF using CD34-coupled magnetic microbeads as previously described [5]. Briefly, the SVF was incubated (room temperature, 15 minutes) with the StemCell Technologies (St. Katharinen, Germany, http://www.stemcell.com) positive selection cocktail. Following the addition of magnetic nanoparticles, cells were recovered by successive magnetic sorting steps. The CD34⫹ cells were suspended in PBS/0.1% BSA. The CD34⫹ population was depleted from the CD31⫹ cells using Dynal Biotech (Hamburg, Germany, http://www.dynalbiotech.com) CD31coupled magnetic microbeads (50 l/ml). After incubation (4°C, 20 minutes), the cell suspension containing the beads, suspended in 10 ml of PBS/0.1% BSA, was exposed to the magnet for 1 minute. The magnetic bead-free fraction, the CD34⫹/CD31⫺ cells (hAT-derived progenitor cells), was collected, centrifuged (250g, 10 minutes), and suspended in the culture medium and the CD34⫹/CD31⫹ cell fraction (hAT-derived CECs) was removed from the magnet and suspended in endothelial cell culture medium. The CD34⫹/CD31⫺ cell content of the selected fraction was 92.2% ⫾ 1.2%. Cell Culture The hAT-derived CECs were cultured in Endothelial Cell Growth Medium MV (ECGM-MV) (PromoCell, Heidelberg, Germany, http://www.promocell.com) on human fibronectin coated culture dishes. Human AT-derived CECs were used until passage 2 [5, 15]. The human AT-derived progenitor cells were cultured in Endothelial Cell Basal Medium (ECBM, which contains no growth factors) (PromoCell) supplemented with 10% FCS. Progenitor cells were used until passage 1 [5]. Human umbilical vein endothelial cells (HUVECs) were isolated [16] and cultured until passage 8. Preparation of Conditioned Media and EnzymeLinked Immunosorbent Assay Human AT-derived CECs, hAT-derived progenitor cells, hAT-resident macrophages (CD14⫹/CD31⫹) that were isolated as previously described [15], and HUVECs were incubated with an equal amount of basal ECBM supplemented with 0.1% BSA for 24 hours. Mature adipocytes (400,000 cells) were included in fibrin gels (1.5 mg fibrinogen/ml ECBM supplemented with 25 units/ml ␣-thrombin) and cultured in ECBM supplemented with 0.1% BSA for 24 hours. Control gels were prepared without adipocytes. The conditioned media were collected, centrifuged (1,000g, 10 minutes, 4°C), and stored at ⫺70°C until use. Release of SDF-1 was measured in conditioned media by enzyme-linked immunosorbent assay according to the instructions of the manufacturer (RayBiotech Inc., Norcross, GA, http://www.raybiotech.com). Note that the SDF-1 levels were measured in conditioned media from P0, P1, and P2 RNA Extraction and Real-Time Quantitative Polymerase Chain Reaction Assay Total RNAs were extracted from human mature adipocytes, hATCD34⫹/CD31⫺ cells, hAT-macrophages, and hAT-CD34⫹/CD31⫹ CECs using the RNeasy kit (Qiagen, Hilden, Germany, http:// www1.qiagen.com). RNA concentrations were determined using a fluorometric assay (RiboGreen). RNA (0.5 g) was reverse-transcribed using the SuperScript III RNase H RT system (Invitrogen, Carlsbad, CA, http://www.invitrogen.com) according to the manufacturer’s instructions (random hexamers and deoxynucleoside-5⬘triphosphates were from Life Technologies, Rockville, MD, http:// www.lifetech.com). Reverse transcription was also performed without superscript enzyme on RNA samples to ensure the absence of contaminating genomic DNA. Primers for human SDF-1 (CXCL12), hypoxia inducible factor-1␣ (HIF-1␣), and CXCR-4 were provided by Applied Biosystems (Assay-On-Demand: Hs00171022_m1, Hs00153153_m1, and Hs00607978_m1, respectively; Foster City, CA, http://www.appliedbiosystems.com). All amplification reactions were performed in duplicate from 20 ng cDNA using the Mx4000 Multiplex Quantitative PCR System (Stratagene, La Jolla, CA, http://www.stratagene.com) using the following conditions: 50°C for 2 minutes and 95°C for 10 minutes followed by 40 cycles at 95°C for 15 seconds and 60°C for 1 minute. Results were analyzed with Stratagene MX4000 software, and all values were normalized to the levels of the ribosomal RNAs. Coculture Between hAT-Derived CECs and hAT-Derived CD34ⴙ/CD31ⴚ Progenitor Cells Human AT-derived CECs plated at 60,000 cells per cm2 were cultured in ECGM-MV on human fibronectin-coated 48-well cell culture plates until confluence. Then, hAT-derived progenitor cells were labeled with PHK26 according to the instructions of the manufacturer (Sigma-Aldrich) and 2,000 –3,000 cells per well were placed in each well in ECBM/2% SVF. After 10 days of coculture, the cocultured cells were fixed and stained with the indicated antibodies. Three-Dimensional Coculture Model Human AT-derived CECs plated at 60,000 cells per cm2 were cultured in ECGM-MV on human fibronectin-coated 48-well cell culture plates. Once confluent, the hAT-CECs were covered with 200 l of unpolymerized BD Matrigel Matrix Growth Factor Reduced (BD Biosciences) and incubated at 37°C for 30 – 45 minutes. Human AT-derived progenitor cells were harvested with trypsin and labeled with PHK26 according to the instructions of the manufacturer. The progenitor cells were resuspended in ECBM/0.1% BSA and 2,000 –3,000 cells per well were loaded onto the matrigelcoated wells (200 l of cell suspension per well). After 24 hours of “coculture,” progenitor cell tube formation (red fluorescent net- Downloaded from www.StemCells.com at Inserm Disc Doc on September 7, 2007 Human AT was obtained from individuals undergoing plastic surgery by lipoaspiration. The study was approved by the ethical committees of Toulouse and Frankfurt am Main hospital universities. Subcutaneous AT was obtained from a total of 38 individuals (mean body mass index: 26.07 ⫾ 1.01 kg/m2). The AT was digested using collagenase (300 U/ml in phosphate-buffered saline [PBS], 2% bovine serum albumin [BSA], pH 7.4) for 30 minutes under constant shaking. Following removal of the floating mature adipocytes, the lower layer containing the SVF was centrifuged (300g, 10 minutes) and the pellet resuspended in erythrocyte lysis buffer (155 mmol/l NH4Cl; 5.7 mmol/l K2HPO4; 0.1 mmol/l EDTA, pH 7.3) for 10 minutes. After successive filtrations through 100-, 70-, and 40-m sieves, the cells were resuspended in PBS/2% fetal calf serum (FCS). Transmigration assays of hAT-derived progenitor cells were performed using 8-m pore HTS FluoroBlock inserts (Falcon; BD Biosciences, San Diego, http://www.bdbiosciences.com) coated with bovine gelatin (0.15 mg/cm2). The progenitor cells were loaded at 50,000 cells per insert (upper chamber) and conditioned media, SDF-1 in the presence or not of AMD3100 (Sigma-Aldrich, St. Louis, http://www.sigmaaldrich.com) or CXCR-4 neutralizing antibody (clone 12G5; R&D Systems Inc., Minneapolis, http:// www.rndsystems.com), were added to the lower chamber. The cells were allowed to migrate into the lower chamber for 20 –24 hours. After the assays, the inserts were fixed (4% paraformaldehyde) and the nuclei were stained with 4,6-diamidino-2-phenylindole. For blocking experiments, the progenitor cells were preincubated with the indicated inhibitors at 37°C for 1 hour. The cell transmigration was quantified by counting the number of nuclei using a computerassisted microscope (Nikon, Düsseldorf, Germany, http://www. nikon.com) at three distinct positions. Sengenès, Miranville, Maumus et al. 2271 RESULTS Figure 1. Human adipose tissue (AT)-derived CECs induce the chemotaxis of hAT-derived CD34⫹/CD31⫺ progenitor cells. (A): Transwell migration of human AT-derived progenitor cells in the presence of control medium (Control) or conditioned media from adipocytes (n ⫽ 14), hAT-CECs (n ⫽ 21), and HUVECs (n ⫽ 3). ⴱ p ⬍ .001 when compared with control migration. (B): Transwell migration of hATderived progenitor cells in response to hAT-CEC conditioned medium in the lower chamber (hAT-CEC conditioned medium), in the upper chamber (upper chamber hAT-CECs) (n ⫽ 3), after 1-hour preincubation with increasing concentrations of pertussis toxin (n ⫽ 4) or after protein denaturated hAT-CEC-conditioned medium (heated AT-CECs) (n ⫽ 4). ⴱ p ⬍ .01, ⴱⴱ p ⬍ .001 when compared with migration induced by hAT-CEC-conditioned medium. Abbreviations: CECs, capillary endothelial cells; hAT, human adipose tissue; HUVECS, human umbilical vein endothelial cells; PTX, pertussis toxin. work) was assessed with a computer-assisted microscope (Nikon). Microphotographs of the center of each well were taken, and tube formation was quantified by measuring the total tube length using Lucia image software (Nikon, Tokyo, http://www.nikon.com). Tube formation of progenitor cells alone was used as a control. For blocking experiments, the progenitor cells were preincubated with the indicated inhibitors at 37°C for 1 hour. Immunocytochemistry Cells were fixed with 4% paraformaldehyde and immunostained with anti-human CXCR-4 monoclonal antibody (Abcam, Cambridge, U.K., http://www.abcam.com) (1:50) or platelet endothelial cell adhesion molecule-1 (CD31) monoclonal antibody (Dako, Glostrup, Denmark, http://www.dako.com) (1:10) followed by staining with fluorescently labeled secondary antibody (1:200) (Invitrogen). AT-Derived CECs Induce the Chemotaxis of the CD34ⴙ/CD31ⴚ Cells The effect of hAT-CECs on the migration of hAT-derived CD34⫹/ CD31⫺ cells was assessed in modified Boyden chamber assays consisting of two cell chambers separated by a polycarbonate filter (8-m pores). The lower chamber was filled up with control media or 24 hour-conditioned media from confluent hAT-CECs, mature adipocytes, or confluent HUVECs, and the cell suspension of hAT-derived CD34⫹/CD31⫺ cells was placed in the upper chamber. Cells that migrated across the filter and attached to the under part of the filter after 24 hours were counted after nuclei staining. As depicted in Figure 1A, conditioned media from mature adipocytes or from HUVECs did not induce any cell migration. Conversely, conditioned media from hAT-CECs led to the robust migration of the CD34⫹/CD31⫺ cells (5.7 ⫾ 0.7-fold increase, n ⫽ 21, p ⬍ .001). Human AT-CEC conditioned media failed to induce the migration of hAT-derived CD34⫹/CD31⫺ cells after protein denaturation of the conditioned media (Fig. 1B). Moreover, the stimulatory effect of conditioned media derived from hAT-CECs was lost when the conditioned media were applied in the upper chamber together with the CD34⫹/CD31⫺ cells. Taken together, the results showed that secreted proteins from hAT-CECs stimulated the directed chemotactic migration of the hAT-derived CD34⫹/CD31⫺ (Fig. 1B). In addition, preincubation of hAT-derived progenitor cells with increasing concentrations of pertussis toxin (PTX) (200 and 400 ng/ml) led to a concentration-dependent inhibition of the hAT-CEC-mediated migration (76% ⫾ 9% of inhibition for 400 ng/ml of PTX, p ⬍ .001, n ⫽ 4) (Fig. 1B). Statistical Analysis The CXCR-4/SDF-1 Axis Is Involved in the Chemotaxis of the CD34ⴙ/CD31ⴚ Cells Mediated by AT-Derived CECs Data are expressed as mean ⫾ SEM from at least three independent experiments. Statistical analysis was performed by Student’s t test or one-way analysis of variance followed by a Bonferroni post hoc test when appropriate. Differences were considered significant when p ⬍ .05. To further identify the nature of the factor(s) involved in such an effect, the CD34⫹/CD31⫺ cells were preincubated with a CXCR-4 antagonist (AMD3100, 10 g/ml) or with neutralizing anti-CXCR-4 antibody (10 g/ml), and the effect of hAT-CEC conditioned media was then assessed. As shown in Figure 2, the www.StemCells.com Downloaded from www.StemCells.com at Inserm Disc Doc on September 7, 2007 Figure 2. The stromal derived factor-1/CXCR-4 axis is involved in the hAT-derived progenitor cell chemotaxis toward hAT-CEC conditioned media. Transwell migration of hAT-derived progenitor cells in the presence of hAT-derived CEC-conditioned media after 1 hour of preincubation with 10 g/ml of the CXCR-4 antagonist AMD3100 (⫹AMD3100) (n ⫽ 6) or with 10 g/ml of an anti-CXCR-4 neutralizing antibody (⫹Anti-CXCR-4) (n ⫽ 6). ⴱ p ⬍ .01 when compared with migration induced by hAT-CEC-conditioned media. Abbreviations: CECs, capillary endothelial cells; hAT, human adipose tissue. 2272 Adipose Tissue Stem and Endothelial Cell Crosstalk CXCR-4 neutralizing antibody (77% ⫾ 11% and 96% ⫾ 4% of inhibition, respectively, p ⬍ .01, n ⫽ 6). Moreover, as depicted in Figure 3A, increasing concentrations of recombinant SDF-1␣ or -1, ligands for the CXCR-4, induced a concentration-dependent chemotaxis of hAT-derived progenitor cells that was significantly inhibited when the progenitor cells were preincubated with AMD3100 (58% ⫾ 7% of inhibition, p ⬍ .01, n ⫽ 3) or neutralizing anti-CXCR-4 antibody (72% ⫾ 3% of inhibition, p ⬍ .01, n ⫽ 3) (Fig. 3B). Of note, the chemotaxis of the CD34⫹/CD31⫺ cells toward granulocyte monocyte colony stimulating factor (20 –100 ng/ml), stem cell factor (20 –100 ng/ml), monocyte chemoattractant protein 1 (1–20 ng/ml), and interleukin 8 (20 ng/ml) was also evaluated, and none of the chemokines induced a statistically significant migration (data not shown). Figure 3. Functionality of the CXCR-4/SDF-1 axis in human adipose tissue. (A): Human adipose tissue (AT)-derived progenitor cells were exposed to increasing concentrations of SDF-1␣ or SDF-1 (10 –100 ng/ml), and transwell migration was evaluated after 24 hours (n ⫽ 3– 8); ⴱ p ⬍ .01 and ⴱⴱ p ⬍ .001 compared with control. (B): Human AT-derived progenitor cells were preincubated (1 hour) with 10 g/ml CXCR-4 antagonist AMD3100 (n ⫽ 3) or with 10 g/ml anti-CXCR-4 neutralizing antibody (n ⫽ 3). Transwell migration toward 100 ng/ml SDF-1␣ was then evaluated after 24 hours. $ p ⬍ .001 compared with control, ⴱ p ⬍ .01 and ⴱⴱ p ⬍ .001 compared with SDF-1␣ induced migration. Abbreviation: SDF-1, stromal derived factor-1. hAT-CEC-mediated chemotaxis was suppressed when the progenitor cells were incubated with AMD3100 or with anti- The expression of CXCR-4 in hAT-derived CD34⫹/CD31⫺ cells was then investigated by real-time polymerase chain reaction (PCR) analysis. The results showed that transcripts for CXCR-4 were present in hAT-derived CD34⫹/CD31⫺ cells (Fig. 4B). Moreover, as presented in Figure 4A, the CXCR-4 protein expression was detected by immunocytochemistry on hAT-CD34⫹/CD31⫺ cells. Additionally, there was a positive correlation between the level of transcripts encoding for CXCR-4 in hAT progenitor cells and the one of HIF-1␣ in the corresponding hAT-CECs (Fig. 4B, p ⫽ .04, n ⫽ 14). In parallel, SDF-1 mRNA expression was assessed in hAT-derived CECs and compared with the one of HUVECs and other cells from the SVF such as hAT-macrophages. As depicted in Figure 4C, the SDF-1 mRNA was mainly expressed by hAT-derived CECs and was below Ct values of 40 in HUVECs. Consistent with the mRNA expression, SDF-1 release was significantly higher in hAT-derived CECs as compared with other cell fractions present in AT-derived SVF such as macrophages (412.2 ⫾ 92.9 pg/ml vs. 34.4 ⫾ 18.1 pg/ml, respectively, p ⬍ .001, n ⫽ 3–9) (Fig. 4D). The production of SDF-1 by HUVECs was 42 Figure 4. Expression of SDF-1 and CXCR-4 in hAT. (A): Upper panel: hATderived CD34⫹/CD31⫺ progenitor cells were fixed and stained with antibodies directed against CXCR-4 receptor followed by fluorescein isothiocyanate (FITC)-conjugated secondary antibodies. Lower panel: hAT-CD34⫹/CD31⫺ cells were stained with FITC-conjugated secondary antibodies. Representative fluorescence microscopy analysis is shown from n ⫽ 3. (B): Correlation between mRNA levels of CXCR-4 in hAT-progenitor cells and HIF-1 levels in hAT-CECs quantified by real-time polymerase chain reaction (PCR) experiments (p ⫽ .04, n ⫽ 14). (C): SDF-1 mRNA expression in hAT-macrophages (n ⫽ 3), HUVECs (n ⫽ 4), and hAT-CECs (n ⫽ 6) quantified by real-time PCR experiments. (D): Enzyme-linked immunosorbent assay of 24hour conditioned media from hAT-macrophages (n ⫽ 3), HUVECs (n ⫽ 4), and hAT-CECs (n ⫽ 9). ⴱ p ⬍ .05 versus macrophage SDF-1 secretion. Abbreviations: A.U., arbitrary units; CECs, capillary endothelial cells; hAT, human adipose tissue; HIF-1, hypoxia inducible factor-1; HUVECS, human umbilical vein endothelial cells; SDF-1, stromal derived factor-1. Downloaded from www.StemCells.com at Inserm Disc Doc on September 7, 2007 CXCR-4 Is Expressed on CD34ⴙ/CD31ⴚ Cells and SDF-1 Is Produced by hAT-Derived CECs Sengenès, Miranville, Maumus et al. 2273 DISCUSSION Figure 5. Human AT-derived progenitor cells incorporate into the network formed by hAT-CECs and express platelet endothelial cell adhesion molecule-1 (PECAM-1). (A): Confluent hAT-CECs were fixed and stained with antibodies directed against PECAM-1 followed by fluorescein isothiocyanate (FITC)-conjugated secondary antibodies. (B): Confluent PKH26 hAT-CD34⫹/CD31⫺ progenitor cells were fixed and stained with antibodies against PECAM-1 followed by FITCconjugated secondary antibodies. (C): Confluent hAT-CECs were cultured in the presence of PKH26-labeled hAT-derived progenitor cells for 10 days of coculture in endothelial basal medium/2% fetal calf serum. Cells were fixed and stained with antibodies directed against PECAM-1 followed by FITC-conjugated secondary antibodies. Representative fluorescence microscopy analysis is shown from n ⫽ 3 independent experiments. Abbreviations: CECs, capillary endothelial cells; DAPI, 4,6-diamidino-2-phenylindole; hAT, human adipose tissue. times lower than the one of hAT-CECs (9.84 ⫾ 3.81 pg/ml, n ⫽ 4). AT-Derived CECs Support the Differentiation of AT-Derived Progenitor Cells Toward an Endothelial Cell Phenotype Coculture experiments of hAT-derived CECs and CD34⫹/ CD31⫺ cells were performed. Human AT-derived CD34⫹/ CD31⫺ cells were labeled with PKH26 and seeded onto confluent hAT-derived CECs (Fig. 5A). After 10 days of coculture, CD31 expression in the formal CD31 negative AT-derived progenitor cells (Fig. 5B) was analyzed. hAT-derived CECs formed a dense CD31 positive network into which PKH26 positive AT-derived progenitor cells incorporated and expressed the CD31 marker (Fig. 5C). To further analyze the effect of the hAT-derived CECs on the differentiation of the CD34⫹/CD31⫺ cells, a three-dimensional coculture model was developed. PKH26 labeled CD34⫹/CD31⫺ cells were seeded on the top of www.StemCells.com Although reports show that adipogenesis and angiogenesis are tightly correlated during the growth of fat mass [3, 17–20], little is known about the mechanisms that regulate the extension of its vasculature. In the present study we report that hAT-derived CECs induce the chemotaxis of hAT-derived progenitor cells. Moreover, we demonstrate that the presence of hAT-derived CECs promotes the differentiation and organization of hATderived hAT-CD34⫹/CD31⫺ progenitor cells into capillary-like structures via a SDF-1/CXCR-4-dependent pathway. In the last years, several reports have contributed to the evidence that the SVF cells are phenotypically heterogeneous and can express under specific culture conditions adipogenic, osteogenic, chondrogenic, and myogenic lineage markers but also endothelial, epithelial, and neural markers [5, 8, 21–23]. We have previously shown that native immunoselected CD34⫹/ CD31⫺ cells present in the hAT-derived SVF display angiogenic and adipogenic potentials. Indeed, this cell population is able to differentiate into adipocyte-like cells [8] and into endothelial-like cells in vitro and in vivo to promote the neovascularization of ischemic muscle in mice [5]. Similar results were also described using adherent hAT-SVF [6, 7]. The mechanisms underlying such proangiogenic effects are still to be defined. Although the hAT-derived progenitor cells were shown to integrate into vessels in vivo [5, 6], they could also contribute to neovascularization through the production of proangiogenic factors [7, 24]. Nevertheless, such a population of progenitor cells may participate locally to the extension of the blood capillary network known to be associated with fat mass development. The present study was undertaken to analyze the potential crosstalk within the hAT between hAT-CD34⫹/CD31⫺ progenitor cells and CECs. Indeed, the EC barrier has already been shown to interact with progenitor/stem cells [25–27]. Human AT-derived CECs specifically stimulated the migration of hAT-derived CD34⫹/CD31⫺ progenitor cells through the release of soluble proteins. Human AT-derived CECs induced a chemotactic response since no random motility was observed when the cells were incubated in the same compartment with endothelial cellderived conditioned media. Moreover, since hAT-derived CD34⫹/CD31⫺ progenitor cell chemotaxis was inhibited in the presence of pertussis toxin, which specifically prevents activation of Gi proteins coupled to chemokine receptors, the involvement of a chemokine ligand/receptor interaction was strongly Downloaded from www.StemCells.com at Inserm Disc Doc on September 7, 2007 a growth factor-reduced matrigel under which confluent hATderived CECs were present or not. As shown in Figure 6A, CD34⫹/CD31⫺ cells alone did neither migrate nor form capillary-like structures. Interestingly, the presence of hAT-derived ECs under the matrigel dramatically promoted the organization of hAT-CD34⫹/CD31⫺ cells into branched structures and pseudotubes (360% ⫾ 48% of the total length obtained with hAT-CD34⫹/CD31⫺ cells alone, p ⬍ .01, n ⫽ 7) (Fig. 6B). Given the chemotactic effect mediated by the CXCR-4/SDF-1 axis, we studied the involvement of this system in the hATCEC-dependent tube formation by using a neutralizing antiCXCR-4 antibody, the CXCR-4 antagonist AMD3100, or pertussis toxin (not shown). As depicted in Figure 6C and 6D, the tube formation induced by hAT-derived CECs was significantly inhibited in a concentration-dependent manner by the inhibitors (24% ⫾ 12% and 67% ⫾ 5% of inhibition with 10 g/ml and 100 g/ml AMD3100, respectively; 41% ⫾ 15% and 93% ⫾ 2% of inhibition for 10 g/ml and 20 g/ml neutralizing antiCXCR-4 antibody, respectively; 85% ⫾ 0.5% of inhibition for 200 ng/ml pertussis toxin, n ⫽ 4 –7). 2274 Adipose Tissue Stem and Endothelial Cell Crosstalk suggested. Finally, when CXCR-4 from hAT-CD34⫹/CD31⫺ progenitor cells was neutralized by antibodies [28] or by the CXCR-4 antagonist (AMD3100) [29], hAT-derived CD34⫹/ CD31⫺ progenitor cells failed to migrate in response to hATderived CEC conditioned medium. Since real-time PCR and immunocytochemistry analyses showed the expression of CXCR-4 in native hAT-derived CD34⫹/CD31⫺ progenitor cells, the present results demonstrate that activation of CXCR-4 of the hAT-derived CD34⫹/CD31⫺ progenitor cells is involved in the hAT-derived CEC-dependent chemotaxis. In agreement, earlier work reported immunoreactivity to CXCR-4 in hAT [30], and a recent publication showed that CXCR-4 overexpression in hAT-stromal cells regulated cell motility [31]. The sole ligand of CXCR-4, described so far, is the CXCL12 chemokine also known as SDF-1 [32–34]. SDF-1, initially described as a product of bone marrow stromal cells [35], is expressed by several tissues including dendritic cells, endothelial cells and pericytes from normal skin [36], osteoblasts, and ECs from the bone marrow [37–39] and astrocytes and neurons from the brain [40]. SDF-1 exists as two isoforms, ␣ and , originating from alternative splicing of the CXCL12 gene [41– 43]. Human AT-CECs expressed and released more SDF-1 than the other cell types present in hAT. Moreover, SDF-1 was detected in very low amounts in conditioned media from HUVECs that did not stimulate the CD34⫹/CD31⫺ progenitor cell chemotaxis. Human AT-progenitor cells exhibited a concentration-dependent chemotaxis toward SDF-1␣ and SDF-1 that was inhibited in the presence of CXCR-4 antagonist or neutralizing antibodies. Taken together, the present findings suggest that SDF-1 released by hAT-CECs plays a major role in the CXCR-4-mediated chemotaxis of hAT-progenitor cells, although further experiments are needed to clearly rule out the involvement of other endothelial-derived factors. The couple SDF-1/CXCR-4 plays a pivotal role in multiple checkpoints of stem/progenitor cell biology in the bone marrow compartment including survival, proliferation, mobilization, and homing [10, 44, 45]. In a twodimensional coculture system, hAT-derived progenitor cells were shown to incorporate into the network formed by hATCECs and to express the EC marker CD31, suggesting that hAT-CECs may, in addition to their effect on the migration, regulate the differentiation of hAT-CD34⫹/CD31⫺. To better define the role of paracrine factors, three-dimensional coculture Downloaded from www.StemCells.com at Inserm Disc Doc on September 7, 2007 Figure 6. hAT-CECs induce the formation of capillary-like structures by hATderived progenitor cells via the stromal derived factor-1/CXCR-4 axis. hAT-CECs were cultured until confluence. Once confluent, hAT-CECs were covered with matrigel and PKH26 labeled hAT-derived progenitor cells were seeded onto the matrigel. After 24 hours, tube length was measured. (A): Representative pictures of hAT-derived progenitor cells alone (phase microscopy and fluorescent microscopy analyses, inset picture). (B): Representative picture of hAT-derived progenitor cells cocultured with hAT-CECs (phase microscopy and fluorescent microscopy analyses, inset picture). (C, D): Representative picture of 1-hour pretreated hATprogenitor cells with AMD3100 (100 g/ ml) (C) or neutralizing anti-CXCR-4 (20 g/ml) antibody (D) that were cocultured with hAT-CECs (phase microscopy and fluorescent microscopy analyses, inset picture). (E): Total length of the network formed by PKH26 labeled hAT-derived progenitor cells pretreated or not with increasing concentrations of AMD3100 or a neutralizing CXCR-4 antibody. ⴱ p ⬍ .05, ⴱⴱ p ⬍ .01, ⴱⴱⴱ p ⬍ .001 when compared with the network formed by adipose tissue (AT)-derived progenitor cells in the presence of AT-CECs (n ⫽ 4 –7). Abbreviations: 3D, three-dimensional; CECs, capillary endothelial cells; hAT, human adipose tissue. Sengenès, Miranville, Maumus et al. REFERENCES 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Hirsch J, Batchelor B. Adipose tissue cellularity in human obesity. Clin Endocrinol Metab 1976;5:299 –311. Bjorntorp P, Sjostrom L. Adipose tissue cellularity. Int J Obes 1979;3: 181–187. Crandall DL, Hausman GJ, Kral JG. A review of the microcirculation of adipose tissue: Anatomic, metabolic, and angiogenic perspectives. Microcirculation 1997;4:211–232. Bouloumie A, Lolmede K, Sengenes C et al. Angiogenesis in adipose tissue. Ann Endocrinol (Paris) 2002;63:91–95. Miranville A, Heeschen C, Sengenes C et al. Improvement of postnatal neovascularization by human adipose tissue-derived stem cells. Circulation 2004;110:349 –355. Planat-Benard V, Silvestre JS, Cousin B et al. Plasticity of human adipose lineage cells toward endothelial cells: Physiological and therapeutic perspectives. Circulation 2004;109:656 – 663. Rehman J, Traktuev D, Li J et al. Secretion of angiogenic and antiapoptotic factors by human adipose stromal cells. Circulation 2004;109: 1292–1298. Sengenes C, Lolmede K, Zakaroff-Girard A et al. Preadipocytes in the human subcutaneous adipose tissue display distinct features from the adult mesenchymal and hematopoietic stem cells. J Cell Physiol 2005; 205:114 –122. Aiuti A, Webb IJ, Bleul C et al. The chemokine SDF-1 is a chemoattractant for human CD34⫹ hematopoietic progenitor cells and provides a new mechanism to explain the mobilization of CD34⫹ progenitors to peripheral blood. J Exp Med 1997;185:111–120. Lapidot T, Kollet O. The essential roles of the chemokine SDF-1 and its receptor CXCR4 in human stem cell homing and repopulation of transplanted immune-deficient NOD/SCID and NOD/SCID/B2m(null) mice. Leukemia 2002;16:1992–2003. Son BR, Marquez-Curtis LA, Kucia M et al. Migration of bone marrow and cord blood mesenchymal stem cells in vitro is regulated by stromalderived factor-1-CXCR4 and hepatocyte growth factor-c-met axes and involves matrix metalloproteinases. STEM CELLS 2006;24:1254 –1264. Fuchs E, Tumbar T, Guasch G. Socializing with the neighbors: Stem cells and their niche. Cell 2004;116:769 –778. Shen Q, Goderie SK, Jin L et al. Endothelial cells stimulate self-renewal and expand neurogenesis of neural stem cells. Science 2004;304: 1338 –1340. Kaplan RN, Psaila B, Lyden D. Niche-to-niche migration of bonemarrow-derived cells. Trends Mol Med 2007;13:72– 81. Curat CA, Miranville A, Sengenes C et al. From blood monocytes to adipose tissue-resident macrophages: Induction of diapedesis by human mature adipocytes. Diabetes 2004;53:1285–1292. www.StemCells.com All together, the present results show that the migration and differentiation of hAT-derived progenitor cells are modulated by factors originating from hAT-derived CECs. The SDF-1/ CXCR-4 axis appears to play a key role. Such an effect may be involved in the recruitment of hAT-derived progenitor cells to foci where SDF-1 is highly expressed such as neovascularization sites to promote the extension of the capillary network that occurs during the growth of the fat mass. ACKNOWLEDGMENTS We are grateful to Valérie Wegner and Pauline Decaunes for their excellent technical assistance. We also thank Dr. Marie Sanson for her special help with HUVECs. This work was supported by grants from AVENIR INSERM, Alexander von Humboldt Foundation, and Sofja Kovalevskaja Price (Humboldt Foundation and the German Federal Ministry of Education and Research). DISCLOSURE OF POTENTIAL OF INTEREST CONFLICTS The authors indicate no potential conflicts of interest. 16 Busse R, Lamontagne D. Endothelium-derived bradykinin is responsible for the increase in calcium produced by angiotensin-converting enzyme inhibitors in human endothelial cells. Naunyn Schmiedebergs Arch Pharmacol 1991;344:126 –129. 17 Zhang QX, Magovern CJ, Mack CA et al. Vascular endothelial growth factor is the major angiogenic factor in omentum: Mechanism of the omentum-mediated angiogenesis. J Surg Res 1997;67:147–154. 18 Fukumura D, Ushiyama A, Duda DG et al. Paracrine regulation of angiogenesis and adipocyte differentiation during in vivo adipogenesis. Circ Res 2003;93:e88 –97. 19 Brakenhielm E, Cao R, Gao B et al. Angiogenesis inhibitor, TNP-470, prevents diet-induced and genetic obesity in mice. Circ Res 2004;94: 1579 –1588. 20 Neels JG, Thinnes T, Loskutoff DJ. Angiogenesis in an in vivo model of adipose tissue development. FASEB J 2004;18:983–985. 21 Zuk PA, Zhu M, Mizuno H et al. Multilineage cells from human adipose tissue: implications for cell-based therapies. Tissue Eng 2001;7:211–228. 22 De Ugarte DA, Alfonso Z, Zuk PA et al. Differential expression of stem cell mobilization-associated molecules on multi-lineage cells from adipose tissue and bone marrow. Immunol Lett 2003;89:267–270. 23 Rodriguez AM, Elabd C, Amri EZ et al. The human adipose tissue is a source of multipotent stem cells. Biochimie 2005;87:125–128. 24 Nakagami H, Maeda K, Morishita R et al. Novel autologous cell therapy in ischemic limb disease through growth factor secretion by cultured adipose tissue-derived stromal cells. Arterioscler Thromb Vasc Biol 2005;25:2542–2547. 25 Papayannopoulou T. Bone marrow homing: The players, the playfield, and their evolving roles. Curr Opin Hematol 2003;10:214 –219. 26 Lapidot T, Dar A, Kollet O. How do stem cells find their way home? Blood 2005;106:1901–1910. 27 Schmidt A, Ladage D, Steingen C et al. Mesenchymal stem cells transmigrate over the endothelial barrier. Eur J Cell Biol 2006;85:1179 –1188. 28 Ceradini DJ, Kulkarni AR, Callaghan MJ et al. Progenitor cell trafficking is regulated by hypoxic gradients through HIF-1 induction of SDF-1. Nat Med 2004;10:858 – 864. 29 De Clercq E. Inhibition of HIV infection by bicyclams, highly potent and specific CXCR4 antagonists. Mol Pharmacol 2000;57:833– 839. 30 Hazan U, Romero IA, Cancello R et al. Human adipose cells express CD4, CXCR4, and CCR5 [corrected] receptors: A new target cell type for the immunodeficiency virus-1? FASEB J 2002;16:1254 –1256. 31 Cho HH, Kyoung KM, Seo MJ et al. Overexpression of CXCR4 increases migration and proliferation of human adipose tissue stromal cells. Stem Cells Dev 2006;15:853– 864. 32 Kucia M, Reca R, Miekus K et al. Trafficking of normal stem cells and metastasis of cancer stem cells involve similar mechanisms: Pivotal role of the SDF-1-CXCR4 axis. STEM CELLS 2005;23:879 – 894. 33 Stellos K, Gawaz M. Platelets and stromal cell-derived factor-1 in progenitor cell recruitment. Semin Thromb Hemost 2007;33:159 –164. Downloaded from www.StemCells.com at Inserm Disc Doc on September 7, 2007 experiments were performed. The results clearly showed that hAT-derived progenitor cells migrate and assemble into capillary-like structures only in the presence of hAT-CECs. Moreover, when CXCR-4 either was antagonized or neutralized, hAT-progenitor cells failed to appropriately migrate and assemble into tubular structures on matrigel substrate. Taken together, the present results show that hAT-derived CECs, through their production of paracrine factors such as SDF-1, modulate the migration but also the differentiation and organization of the hAT-derived CD34⫹/CD31⫺ progenitor cells through the activation of CXCR-4. CXCR-4 mRNA levels are known to be upregulated by hypoxia through HIF-1 activation via the hypoxia responsive element in the 5⬘ region of the CXCR4 gene [46, 47]. In the murine AT, hypoxic areas have been shown to be associated with obesity [48]. Interestingly, the mRNA levels of CXCR-4 from the CD34⫹/CD31⫺ were found to be positively correlated to HIF-1␣ transcripts of the CECs. A recent publication has reported that the recruitment of CXCR-4 positive progenitor cells to regenerating foci or tissues was mediated by hypoxic gradients via HIF-1 induced expression of CXCR-4/SDF-1 axis [28]. Moreover, SDF-1 expression in ischemic tissue has been shown to primarily localize in ECs [36]. It is thus tempting to speculate that hypoxia within the hAT may promote the migration of resident hAT-derived CD34⫹/CD31⫺ progenitor cells at active sites of neovascularization in the fat mass. 2275 Adipose Tissue Stem and Endothelial Cell Crosstalk 2276 42 43 44 45 46 47 48 strategy for secreted proteins and type I membrane proteins. Science 1993;261:600 – 603. Shirozu M, Nakano T, Inazawa J et al. Structure and chromosomal localization of the human stromal cell-derived factor 1 (SDF1) gene. Genomics 1995;28:495–500. De La Luz Sierra M, Yang F, Narazaki M et al. Differential processing of stromal-derived factor-1alpha and stromal-derived factor-1beta explains functional diversity. Blood 2004;103:2452–2459. Lapidot T, Petit I. Current understanding of stem cell mobilization: The roles of chemokines, proteolytic enzymes, adhesion molecules, cytokines, and stromal cells. Exp Hematol 2002;30:973–981. Aicher A, Zeiher AM, Dimmeler S. Mobilizing endothelial progenitor cells. Hypertension 2005;45:321–325. Staller P, Sulitkova J, Lisztwan J et al. Chemokine receptor CXCR4 downregulated by von Hippel-Lindau tumour suppressor pVHL. Nature 2003;425:307–311. Zagzag D, Lukyanov Y, Lan L et al. Hypoxia-inducible factor 1 and VEGF upregulate CXCR4 in glioblastoma: Implications for angiogenesis and glioma cell invasion. Lab Invest 2006;86:1221–1232. Hosogai N, Fukuhara A, Oshima K et al. Adipose tissue hypoxia in obesity and its impact on adipocytokine dysregulation. Diabetes 2007; 56:901–911. Downloaded from www.StemCells.com at Inserm Disc Doc on September 7, 2007 34 Busillo JM, Benovic JL. Regulation of CXCR4 signaling. Biochim Biophys Acta 2007;1768:952–963. 35 Bleul CC, Farzan M, Choe H et al. The lymphocyte chemoattractant SDF-1 is a ligand for LESTR/fusin and blocks HIV-1 entry. Nature 1996;382:829 – 833. 36 Salvucci O, Yao L, Villalba S et al. Regulation of endothelial cell branching morphogenesis by endogenous chemokine stromal-derived factor-1. Blood 2002;99:2703–2711. 37 Imai K, Kobayashi M, Wang J et al. Selective secretion of chemoattractants for haemopoietic progenitor cells by bone marrow endothelial cells: A possible role in homing of haemopoietic progenitor cells to bone marrow. Br J Haematol 1999;106:905–911. 38 Ponomaryov T, Peled A, Petit I et al. Induction of the chemokine stromal-derived factor-1 following DNA damage improves human stem cell function. J Clin Invest 2000;106:1331–1339. 39 Yun HJ, Jo DY. Production of stromal cell-derived factor-1 (SDF-1) and expression of CXCR4 in human bone marrow endothelial cells. J Korean Med Sci 2003;18:679 – 685. 40 Tanabe S, Heesen M, Yoshizawa I et al. Functional expression of the CXC-chemokine receptor-4/fusin on mouse microglial cells and astrocytes. J Immunol 1997;159:905–911. 41 Tashiro K, Tada H, Heilker R et al. Signal sequence trap: A cloning Titre et résumé en anglais Matrix metalloproteases 2 and 9 and the differentiation of human adipose tissue progenitor cells Human adipose tissue (AT) has long attracted attention because of its capacity for excessive development and regression. Cellular and matrix remodelling can explain human AT plasticity. The matrix metalloproteinase (MMP) family is considered to play a major role in tissue remodelling. In a previous report, we demonstrated that the stroma-vascular fraction (SVF) of human AT produce and release MMP-2 and -9 during adipocyte differentiation in vitro. In this work, we evidenced that decrease of MMP-9 activity by batimastat and expression by HIV protease inhibitors decrease adipocyte differentiation of SVF cells. We showed that the way in which HIV protease inhibitor affect MMP-9 expression involve perturbations of proteasome and transcription factor NF-κB activities. Since the SVF of human AT represents a heterogeneous cell population containing capillary endothelial cells, inflammatory cells and progenitor cells that are able, under appropriate culture conditions, to express adipogenic and angiogenic abilities, we would like to determine MMP-9 involvement in the fate of progenitor cells. We defined a new culture condition in which progenitor cells express simultaneously adipogenic and angiogenic abilities. These data strongly suggests that MMP-9 modulate the differentiation of human progenitor cells and contribute to human AT remodelling and thus in this excessive development and/or regression. 104 Auteur : Sandra DE BARROS Titre : Les métalloprotéases matricielles 2 et 9 et la différenciation des cellules progénitrices du tissu adipeux humain Directeur de thèse : Dr Jean GALITZKY Lieu et date de soutenance : Toulouse, le 29 octobre 2007 Résumé : Le tissu adipeux (TA) peut se développer de manière excessive (obésité) mais aussi régresser (lipoatrophie). Cette plasticité peut s’expliquer par un remodelage cellulaire et matriciel. Les métalloprotéases matricielles (MMPs) sont des acteurs majeurs du remodelage tissulaire. Des travaux précédents menés au sein de l’équipe ont montré que les cellules de la fraction stroma vasculaire (FSV) du TA humain sécrètent les MMP-2 et -9 au cours de la différenciation adipocytaire in vitro. Durant ce travail, nous avons observé que l’inhibition de l’activité de MMP-9 par le batimastat et de son expression par les inhibiteurs de la protéase du VIH limite la différenciation adipocytaire des cellules de la FSV. L’étude des mécanismes moléculaires responsables de la diminution de l’expression de MMP-9 par les inhibiteurs de la protéase du VIH a montré que l’expression de MMP-9 est régulée par une voie impliquant l’activité du protéasome et le facteur de transcription NF-κB. Sachant que la FSV est une population cellulaire hétérogène contenant des cellules endothéliales, des cellules immunoinflammatoires et des cellules progénitrices aux capacités adipogéniques et angiogéniques, nous avons souhaité déterminer l’implication de MMP-9 dans le devenir des cellules progénitrices. Pour cela, une condition de culture permettant simultanément l’expression des capacités adipogéniques et angiogéniques des cellules progénitrices a été mise au point. L’ensemble de ce travail indique que MMP-9 influence la différenciation des cellules progénitrices du TA humain et contribuent au remodelage du TA lors de son développement et/ou de sa régression. Mots clés : tissu adipeux, MMP, adipogenèse, cellules progénitrices Discipline : Innovation pharmacologique Intitulé et adresse du laboratoire : Equipe 1/Avenir - Réseau vasculaire, cellules progénitrices et cellules immnunitaires du tissu adipeux- INSERM U858/I2MR, 37 Allées Jules Guesde, 31000 Toulouse 105