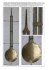Generationswechsel der Equisetopsida (Schachtelhalme)
Transcription
Generationswechsel der Equisetopsida (Schachtelhalme)
1 Generationswechsel – Equisetopsida (Schachtelhalme) © Dr. VEIT M. DÖRKEN, Universität Konstanz, FB Biologie Eine Möglichkeit, die Abhängigkeit des Befruchtungsvorgangs von freiem außeren Wasser noch stärker einzuschränken, ist eine Reduktion der Strecken, welche die Spermatozoiden zurücklegen müssen. Wie bereits erwähnt, führt Homozygotie (Selbstbefruchtung durch Gameten eines Prothalliums) nicht zur Durchmischung des Genpools. Dies kann durch die Ausbildung eingeschlechtlicher Prothallien umgangen werden. Das trifft bei Schachtelhalmen zu, was aber in dieser Gruppe nicht genetisch, sondern modifikatorisch bedingt ist. Abb. 1: Equisetum arvense, die fertilen chlorophyllfreien Sprosse werden lange vor dem Austrieb der chlorophyllhaltigen sterilen Sprosse im zeitigen Frühjahr hervorgebracht; Abb. 2: Equisetum hyemale, die Sporangiophore werden im Spätsommer/Frühherbst in zapfenartigen Ständen im terminalen Bereich chlorophyllhaltiger Sprossachsen ausgebildet; Bei Schachtelhalmen werden die sporangientragenden Blätter, die Sporophylle, terminal konzentriert am Ende der Sprossachsen (meist an den Hauptachsen) hervorgebracht. Die Sporophylle sind in Wirteln angeordnet. Die Internodien zwischen den “Stockwerken“ sind stark gestaucht, sodass eine zapfenartige Struktur entsteht. Die “Zapfen“größe variiert im interspezifischen Vergleich zwischen 0,5 und 5 cm stark. Es lassen sich zwei Typen der Sporophyll tragenden Sprossachsen unterscheiden. So kommen in der Untergattung Equisetum weitgehend chlorophyllfreie fertile Sprosse vor, die im zeitigen Frühjahr ausgebildet werden und nach Entlassung der Sporen wieder einziehen, bevor dann die chlorophyllhaltigen sterilen Sommersprosse hervorgebracht werden. Bei Arten aus der Untergattung Hippochaete werden die zapfenartigen Sporophyllstände hingegen ausschließlich am Ende chlorophyllhaltiger fertiler Sprosse gebildet. 2 Das einzelne Sporophyll besteht, wie es für ein Schildblatt typisch ist, aus einer stark abgeplatteten schildartigen Blattspreite und einem zentralen Blattstiel. Auf der Unterseite der am Rande eingekrümmten Blattspreite inserieren zahlreiche Sporangien rings um das zentrale Stielchen. Die Wand des jungen Sporangiums ist zunächst noch 3-4 Zellreihen mächtig, im reifen Stadium hingegen nur noch einschichtig. Abb. 3: Sporophyllstand mit inserierenden Sporophyllen; zahlreichen, wirtelig Abb. 4: Detail eines Sporophylls mit Schildchen und zahlreichen Sporangien; terminalen Die Sporen aller rezenten Schachtelhalme sind isospor und nicht geschlechtlich determiniert. Eine Differenzierung in weibliche Makrosporen und männliche Mikrosporen, wie sie bei einigen rezenten Bärlappgewächsen (Isoetes und Selaginella) und bei Wasserfarnen aus den Familien der Azollaceae, Salviniaceae und Marsileaceae auftritt, fehlt. Die Sporen sind reich an Chlorophyll, eine Besonderheit, die bei keiner anderen heutigen Farnverwandten zu finden ist. Unter den fossilen Schachtelhalmverwandten (z.B. bei Sphenophyllum) gab es Entwicklungslinien hin zu einer Heterosporie, die sich jedoch wahrscheinlich von noch früheren isosporen Vorläufern ableiten lässt. Die heutigen isosporen Schachtelhalme ausgestorbenen dürfen dabei heterosporen jedoch Linie nicht als verstanden Weiterentwicklung werden. Es ist dieser sehr unwahrscheinlich, dass sich aus dieser ehemaligen Heterosporie die rezente Isosporie entwickelt hat. Heterosporie ist generell als ein von einem isosporen Vorfahren abgeleitetes Merkmal zu verstehen. Wie auch die heterosporen Schachtelhalmverwandten sind die samenbildenden Formen wie z.B. Calamocarpon ebenfalls ausgestorben. 3 Die junge Meiospore hat zunächst nur eine Hüllmembran, innerhalb dieser wird dann später eine zweite ausgebildet, sodass bei reifen Sporen zwei Membranen vorhanden sind. Die äußere Membran wird als Exospor, die innere als Endospor bezeichnet. Später wird der Spore eine weitere Schicht, das sog. Perispor, aufgelagert, aus der die für diese Gruppe typischen fadenartigen Haftorgane, die Hapteren, hervorgehen. Dies sind hygroskopische Schraubenbänder, die sich bei Trockenheit entfalten und bei Feuchtigkeit wieder um die Spore einrollen. Abb. 5 & 6: Equisetum telmateia, Sporophyll (links); aufgeplatze reife Sporangien, die Sporen der Schachtelhalme sind in Form und Funktion gleichgestaltet (= isospor) und chlorophyllreich (rechts); Abb. 7 & 8: Equisetum arvense, Spore mit hygroskopischen Schraubenbändern, die sich bei Trockenheit entrollen und bei Feuchtigkeit wieder einrollen (links); Sporen werden durch die Hapteren zusammengehalten und daher als Einheit ausgebreitet (rechts); Zum Zeitpunkt der Sporenreife streckt sich die Achse des Sporophyllstands deutlich, sodass die Sporophylle nunmehr weit auseinander stehen und die Sporen optimal durch Wind ausgestreut werden können. Die Öffnung des Sporangiums erfolgt über einen durch Austrocknung entstehenden Längsriss. Die Sporenkeimung beginnt zunächst mit der Ausbildung eines Rhizoids. Aus der zweiten Zelle wird später das chlorophyllreiche, epigäische, einschichtige Prothallium (= Vorkeim) gebildet. Im 4 Unterschied zu den Prothallien der Farne i.e.S. sind die Prothallien der Schachtelhalme nicht herzförmig gestaltet, sondern recht variabel in der Form und mehrfach stark gelappt. Das weibliche Makroprothallium ist stets deutlich größer als das männliche Mikroprothallium. In das Gewebe der Mikroprothallien eingesenkt werden die Antheridien hervorgebracht, in denen zahlreiche begeißelte, polyciliate Spermatozoiden gebildet werden. Auf den weiblichen Prothallien entwickeln sich die Archegonien, die je eine große Eizelle sowie mehrere Halskanalzellen enthalten. Für eine erfolgreiche Befruchtung ist es notwendig, dass die männlichen und weiblichen Prothallien so dicht wie möglich beieinander liegen und zur Entwicklung kommen. Dies wird bei Schachtelhalmen dadurch erzielt, dass aufgrund der Ausbildung der Hapteren die Sporen nicht einzeln, sondern immer zu mehreren als verhakte Einheit Abb. 9: Equisetum arvense, junger Gametophyt; ausgebreitet werden. So entsteht nach der Keimung immer eine kleine Gruppe von Prothallien. Die zuerst keimende Spore entwickelt sich immer zu einem weiblichen Prothallium, alle übrigen zu männlichen. In Kulturversuchen lässt sich nachweisen, dass ein Prothallium grundsätzlich beide Geschlechter hervorbringen kann. Für die Geschlechtsdetermination eines Prothalliums spielt das sog. Antheridiogen-System eine entscheidende Rolle. Von weiblichen Prothallien (besser gesagt: Prothallien im weiblichen Zustand) ist bekannt, dass sie hormonartige Substanzen (Antheridiogene) produzieren, die bei benachbarten Sporen die Keimung induzieren und bewirken, dass diese Prothallien männlich werden. Dieser Vorgang der gametophytischen Geschlechtsbestimmung wird als haplomodifikatorisch bezeichnet. Dadurch umgehen Schachtelhalme die Homozygotiefalle. Allerdings tritt hier das Problem auf, dass stets mehrere Sporen bzw. Prothallien des gleichen Sporophyten nebeneinander liegen. Somit findet vielfach eine intergametophytische Selbstbefruchtung statt, also keine echte Fremdbefruchtung. 5 Nach der Verschmelzung der beiden haploiden Gameten bildet sich die diploide Zygote aus, aus der der junge Sporophyt hervorgeht. Am jungen Spross befindet sich terminal eine dreischneidige Scheitelzelle, an der der distale Zuwachs erfolgt. Im basalen Bereich wächst die Wurzel durch das Prothallium hindurch in das Substrat. Bereits in sehr frühen Entwicklungsstadien, noch vor der Wurzelbildung, werden terminal an der Sprossachse Mikrophylle hervorgebracht, sodass der empfindliche Vegetationspunkt des jungen Sporophyts bereits beim Verlassen des Archegoniums durch einen Blattquirl gut geschützt ist. Meist entwickelt sich nur ein Sporophyt je Makroprothallium. Die Sporophyten können über Jahre hinweg immer wieder sporolieren und stellen die ausdauernde Generation im Generationswechsel der Schachtelhalme dar. Sporophyll (2n) Sprossachsen (2n) mit Sporophyllstand (2n) Sporophyllstand (2n) geöffnete Sporangien Spermatozoid (n) Befruchtung Antheridium (n) Archegonium (n) ♂ adulter Sporophyt (2n) Gametophyt (n) mit 2 jungen Sporophyten (2n) ♀ Sporen (n) Prothallium (n) (Gametophyt) Abb. 10: Übersicht über den Generationswechsel der Schachtelhalme; Weiterführende Literatur AICHELE, D. & SCHWEGLER, H.-W. (1999): Unsere Moos- und Farnpflanzen. – Kosmos, Stuttgart. 6 BENNERT, H. W.; HORN, K. & BENEMANN, J. (1999): Die seltenen und gefährdeten Farnpflanzen Deutschlands. – Landwirtschaftsverlag, Münster. ENGLER, A. (2009): Syllabus of Plant Families - A. Engler's Syllabus der Pflanzenfamilien Part 3: Bryophytes and seedless Vascular Plants. ed.: FREY, W., STECH, M. & FISCHER, E. 13. ed. – Schweizerbart Science Publishers, Stuttgart. ESSER, K. (1992): Kryptogamen II, Moose, Farne. – Springer, Berlin, Heidelberg. GIFFORD, E. M. & FOSTER, A. S. (1996): Morphology and Evolution of Vascular Plants. 3rd ed. – Freeman and Company, New York. KRAMER, K. U., GREEN, P. S. & GÖTZ, E. (2010): Pteridophytes and Gymnosperms. The Families and Genera of Vascular Plants. – Springer, Berlin, Heidelberg. LUBINSKI, M. (2011): Die Schachtelhalme (Equisetaceae, Pteridophyta) der Flora Deutschlands – ein aktualisierter Bestimmungsschlüssel. – Jahrb. Boch. Bot. Ver. 2: 82-100. PROBST, W. (1986): Biologie der Moos- und Farnpflanzen. – Quelle und Meyer, Wiesbaden. TAYLOR, T. N.; TAYLOR, E. L. & KRINGS, M. (2009): Paleobotany, the biology and evolution of fossil plants. 2nd ed. – Academic Press, Burlington, London, San Diego, New York. WILSON, N. S. & ROTHWELL, G. W. (1993): Palaeobotany and the Evolution of Plants, 2nd ed. – Cambridge University Press, Cambridge.