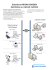Dossier « Cœur et Armées - sssm 45
Transcription
Dossier « Cœur et Armées - sssm 45
Médecine &Armées Revue du Service de santé des armées Médecine & Armées ■ TOME 34 - N°4 - Octobre 2006 ■ « Cœur et Armées » PAGES 289 à 384 Octobre 2006 N°4 TOME 34 ISSN 0300-4937 N°4 Octobre 2006 MÉDECINE ET ARMÉES Revue du Service de santé des armées SOMMAIRE Pages T. 34 - n° 4 - Octobre 2006 Direction centrale du Service de santé des armées Médecine et Armées 1, Place Alphonse Laveran, 75230 Paris Cedex 05. DIRECTEUR DE LA PUBLICATION MGI PH. LOUDES RÉDACTEUR EN CHEF MG F. FLOCARD – Tél. : 01 40 51 47 01 RÉDACTEURS EN CHEF ADJOINTS MC É. DARRÉ – MC A. SPIEGEL. SECRÉTARIAT DE RÉDACTION Mme M. SCHERZI – Melle L. CHOLLET Tél. : 01 40 51 47 44 Fax : 01 40 51 51 76 Email : [email protected] TRADUCTION MC M. AUDET-LAPOINTE COMITÉ DE RÉDACTION MC B. BARANGER – MCS B. BAUDUCEAU – MC A.-X. BIGARD – PHC P. BURNAT - MC J.D. CAVALLO – MC É. DARRÉ– MC J.-M. DEBONNE – MG R. JOSSE - CDCS PH. KAHL VBCS J.-C. KERVELLA – MC. J.-M. ROUSSEAU – MC A. SPIEGEL. COMITÉ SCIENTIFIQUE MGI G. BRIOLE – MGI P. BUFFE – MGA Y. CUDENNEC – MGI F. EULRY – MGI A. FLECHAIRE – MGI J. GUELAIN. – MG A. GALÉANO – MGI D. BÉQUET – MG G. POYOT – MGI P. QUÉGUINER – MGI B. ROUVIER – PGI C. RENAUDEAU. CONSEILLERS HONORAIRES MGI P H . ALLARD – MGI M. BAZOT – MGI B. BRISOU – MCS A. CHAGNON – MGI L. COURT – MGI J.-P. DALY – MGA J.DE SAINT JULIEN - MGI R. FORISSIER – MGI M. FROMANTIN – MGI CL. GIUDICELLI – MGI J. KERMAREC – MGI CH. LAVERDANT – MGI P. LEFEBVRE – PGI LECARPENTIER – VBGI R. LUIGI – VBGI CL. MILHAUD – MGI J. MINÉ – MCS CL. MOLINIÉ – MCS J.-L. PAILLER – MGI J.-M. VEILLARD – MGI J. VIRET – MG R. WEY. ÉDITION Délégué à l'information et à la communication de la Défense (DICoD) - BP 33, 00450 Armées. Tél. : 01 44 42 30 11 ABONNEMENT (5 NUMÉROS PAR AN) ECPAD/Service abonnements, 2 à 8 route du Fort, 94205 IVRY-SUR-SEINE Cedex. Tél. : 01 49 60 52 44 - Fax : 01 49 60 52 68. Tarif des abonnements 1 an : • Métropole et DOM-TOM : 36,5 € • Métropole et DOM-TOM militaires et - 25 ans : 25 € • Étranger : 47 € • Supplément port avion DOM-TOM et étranger : 23 € Prix du numéro : 7,5 € Les chèques sont à libeller à l’ordre de l’agent comptable de l’ ECPAD. 291 • Éditorial. R. BRION « CŒUR ET ARMÉES » : Physiologie 293 • Stress au cours du saut en parachute à très haute hauteur. Approche par l’étude de 38 holters ECG. L. AIGLE, J.-M. CHEVALIER, L. JOURNAUX, É. TREMSAL, Y. BODESCOT. 299 • Étude de la variabilité sinusale lors d’immersion totale longue durée en eau froide. G. CELLARIER, CL. ROBINET, L. MOUROT, A.-V. DESRUELLE, C. JÉGO. 305 • Influence de l’activité physique sur la distensibilité aortique. P. LAURENT, P. MARENCO, O. CASTAGNA, R. CARLIOZ, J.-P. MENU. « CŒUR ET ARMÉES » : Rythmologie 311 • Évaluation de l’influence de l’activité sportive sur l’électrocardiogramme de jeunes incorporés. Apport d’une nouvelle méthode de traitement des données. J.- R. CAIGNAULT, S. GUÉRARD, V. GRIFFET, F. BERNARD, R. BRION. 315 • Anomalies de la repolarisation ventriculaire et aptitude médico-militaire. S. K ÉRÉBEL , G. C ELLARIER ,C. J ÉGO , Y. L EDOLLEY , F. B ARBOU ,L. C ORGIE , R. P OYET , P. L AURENT , G. FOUCAULT, C. BOUCHIAT, R. CARLIOZ. 323 • Conduite à tenir devant une extrasystolie ventriculaire. G. QUINIOU, U. VINSONNEAU, A. BRONDEX, C. VANOYE, P. GODON. 329 • Indications actuelles des techniques ablatives et incidence sur l’aptitude en milieu militaire. PH. HÉNO, L. BRAEM, D. MIOULET, J.-M. PÉLONI, E. BASTARD, PH. PAULE, P. VARLET, L. FOURCADE. 335 • Dysplasie ventriculaire droite arythomgène. Étiopathogénie, diagnostic, évolution, prise en charge et retentissement sur l’aptitude au service. PH. BRANDSTÄTT, J.-M. CHEVALIER, J.-M. RIGOLLAUD, F. BIRE, P.-L. MASSOURE, R. CARLIOZ. « CŒUR ET ARMÉES » : Divers 343 • Diagnostic et pronostic de la cardiomyopathie hypertrophique en 2006. Acquis et incertitudes. P. GODON, U. VINSONNEAU, A. BRONDEX, C. VANOYE, G. QUINIOU. 349 • Myocardite à forme pseudo-infarctoïde du sujet jeune. Revue de la littérature à propos de trois observations. X. ROUX, J.-M. CHEVALIER, Y.-M. GAVEAU, P. GODON, F. BIRE, R. BRION. 355 • Intérêt du scanner dans la maladie coronaire. O. GUIRAUDET, L. BONNEVIE, P. MARION, B. BOYER, D. MARTIN, X. CHANUDET. 361 • Insuffisance cardiaque en région tropicale. Prise en charge diagnostique et thérapeutique. PH. PAULE, PH. HÉNO, D. MIOULET, J.-M. PÉLONI, L. BRAEM, B. JOP, P. VARLET, J.-É. TOUZE, L. FOURCADE. 369 • Cœur et spondylarthropaties. U. VINSONNEAU, A. BRONDEX, C. VANOYE, P. GODON, G. QUINIOU. 375 • Syndrome de Tako-tsubo. Une ballonisation apicale transitoire du ventricule gauche. F. BARBOU, S. KÉRÉBEL, Y. LEDOLEY, C. JÉGO, P. LAURENT, G. CELLARIER, G. FOUCAULT, C. BOUCHIAT, R. CARLIOZ. 379 • Syndrome du marteau hypothénar chez un jeune militaire. P.-L. M ASSOURE , M. B EUSTES -S TEFANELLI , E. D ULAURENT , F. B IRE , J.-M. R IGOLLAUD , P. S HMOOR , S. SKOPINSKI, J.-M. CHEVALIER. IMPRIMEUR ET ROUTAGE Pôle graphique de Tulle – BP 290 –19007 Tulle Cedex. Tél. : 05 55 93 61 00 Commission paritaire N° 0306 B 05721 ISSN : 0300-4937 COUVERTURE Ghislaine PLOUGASTEL www.gplougastel.com 289 CONTENTS Pages « HEART AND ARMY » : PHYSIOLOGY 293 • Stress durind hight altitude parachute jumping. Approach by holter ECG. L. AIGLE, J.-M. CHEVALIER, L. JOURNAUX, É. TREMSAL, Y. BODESCOT. 299 • Heart rate variability during long duration total body immersion in cold water. G. CELLARIER, CL. ROBINET, L. MOUROT, A.-V. DESRUELLE, C. JÉGO. 305 • Aortic distensibility and physical activity. P. LAURENT, P. MARENCO, O. CASTAGNA, R. CARLIOZ, J.-P. MENU. « HEART AND ARMY » : RYTHMOLOGY 311 • Assessment of influence of sport activity on electrocardiograms of young recruits. Utility of a data-processing new method. J.- R. CAIGNAULT, S. GUÉRARD, V. GRIFFET, F. BERNARD, R. BRION. 315 • Abnormalities of the ventricular repolarisation and military aptitude. S. K ÉRÉBEL , G. C ELLARIER ,C. J ÉGO , Y. L EDOLLEY , F. B ARBOU ,L. C ORGIE , R. P OYET , P. L AURENT , G. FOUCAULT, C. BOUCHIAT, R. CARLIOZ. 323 • Premature ventricular complex: appropriate management. G. QUINIOU, U. VINSONNEAU, A. BRONDEX, C. VANOYE, P. GODON. 329 • Radiofrequency catheter ablation of cardiac arrythima: indications and aptitude implications in military medicine. PH. HÉNO, L. BRAEM, D. MIOULET, J.-M. PÉLONI, E. BASTARD, PH. PAULE, P. VARLET, L. FOURCADE. 335 • Arrhythmogenic right ventricular cardiomypathy: etiopathogeny, diagnostis, evolution, management and aptitude to serve. PH. BRANDSTÄTT, J.-M. CHEVALIER, J.-M. RIGOLLAUD, F. BIRE, P.-L. MASSOURE, R. CARLIOZ. « HEART AND ARMY » : MISCELLANEOUS 343 • Diagnosis and prognosis of hypertrophic cardiomyopathy in 2006: knowledge and uncertainty. P. GODON, U. VINSONNEAU, A. BRONDEX, C. VANOYE, G. QUINIOU. 349 • Myocarditis mimicking myocardial infarction in the young: review of the literature about three cases reports. X. ROUX, J.-M. CHEVALIER, Y.-M. GAVEAU, P. GODON, F. BIRE, R. BRION. 355 • Interest of computed tomography in coronary artery disease. O. GUIRAUDET, L. BONNEVIE, P. MARION, B. BOYER, D. MARTIN, X. CHANUDET. 361 • Heart failure in the tropics: diagnosis and treatment. P H . P AULE , P H . H ÉNO , D. M IOULET , J.-M. P ÉLONI , L. B RAEM , B. J OP , P H . V ARLET , J.-É. T OUZE , L. FOURCADE. 369 • Cardiovascular diseases in spondylarthropathies. U. VINSONNEAU, A. BRONDEX, C. VANOYE, P. GODON, G. QUINIOU. 375 • Tako-tsubo syndrome: a left ventricular transient apical ballooning. F. BARBOU, S. KÉRÉBEL, Y. LEDOLEY, C. JÉGO, P. LAURENT, G. CELLARIER, G. FOUCAULT, C. BOUCHIAT, R. CARLIOZ. 379 • Hypothenar hammer syndrme in a young military. P.-L. M ASSOURE , M. B EUSTES -S TEFANELLI , E. D ULAURENT , F. B IRE , J.-M. R IGOLLAUD , P. S HMOOR , S. SKOPINSKI, J.-M. CHEVALIER. 290 ÉDITORIAL Il nous faut avant tout remercier la rédaction de la revue Médecine et Armées d'avoir consacré à la cardiologie militaire un numéro thématique. Ce projet a abouti grâce à la détermination de son coordonnateur, le médecin en chef J.-M. Chevalier et à la participation de presque tous les services de cardiologie des Hôpitaux d’instruction des armées qui ont produit une belle diversité de synthèses attractives et de travaux originaux dans leurs domaines d'excellence. Cette revue est également l’occasion de s’interroger sur ce que représente aujourd’hui la cardiologie militaire. Entité dynamique qui s'est très bien adaptée à l'évolution spectaculaire de la cardiologie, elle a une identité forte à laquelle ses acteurs (présents ou passés) ont un sentiment marqué d'appartenance. Depuis 1991, les cardiologues militaires se réunissent chaque année. Ces réunions initialement organisées à l’HIA du Val-de-Grâce par le médecin chef des services hors classe J.-P. Ollivier se sont dans un second temps déplacées dans d’autres HIA avec un succès constant encore renforcé par la participation plus récente des paramédicaux. Ces réunions contribuent indiscutablement à unir la spécialité. Depuis 2005, la cardiologie militaire a franchi un cap important au sein de la Société française de cardiologie (SFC) avec l’institutionnalisation d’une séance de cardiologie militaire au sein des « Journées européennes de la Société française de cardiologie ». Cette séance, sous l’égide de la Société française de médecine des armées et de la Société française de médecine aéronautique et spatiale, nous assure un espace d’expression annuel dans le congrès international phare de la SFC (8 000 cardiologues) et témoigne de la reconnaissance de notre spécificité par les instances scientifiques civiles de la cardiologie. Tout ceci est excellent mais est-ce suffisant ? Je ne le crois pas. Parmi les acteurs de la cardiologie militaire on compte une quarantaine de praticiens qualif iés, une dizaine d’internes et assistants en formation, sans oublier nos médecine et armées, 2006, 34, 4 291 indispensables ESR et vacataires. Si l’on compare le nombre des praticiens militaires certifiés au nombre de cardiologues civils en France il apparaît que nous représentons environ 0,6 % du nombre global des spécialistes en cardiologie et environ 2 % du nombre des cardiologues exerçant exclusivement en centre hospitalier public. Ces chiffres mettent en évidence le fait que si chacun des neuf services ne représente quantitativement que peu de chose, la cardiologie militaire regroupée représente un nombre de praticiens loin d’être négligeable. Or, lorsque l’on analyse le sommaire de cette revue, on s’aperçoit vite que pas une seule publication ne relate un travail multicentrique émanant de plusieurs de nos hôpitaux militaires. Force est de constater sur ce plan un éclatement en neuf entités. Si nous voulons exister à l’échelle universitaire et faire émerger une « école de la cardiologie militaire française » ce ne pourra être qu’à travers des travaux suffisamment étayés pour qu’ils s'imposent comme des références internationales et pour cela il sera indispensable d’unir nos données. Nous avons des domaines de prédilection comme les limites de la normalité, le retentissement de l’entraînement physique, l’influence des conditions extrêmes, la mise en évidence des pathologies de l’adulte jeune, le suivi régulier des populations dont nous avons la charge etc. Probablement devrons-nous également nous allier à d’autres spécialités devenues proches comme l’endocrinologie et la pathologie métabolique. Croyez bien que si nous ne saisissons pas rapidement et à l’échelle nationale les sujets qui relèvent de nos spécificités d’autres le feront à notre place. La nouvelle École du Val-de-Grâce pourrait être le support de ce type d’action commune qui devra nécessairement impliquer nos internes. Un « conseil scientifique de la spécialité » pourrait être créé, avec une représentation de chaque service et l’objectif de définir des projets communs à plus grande échelle… Ma génération de chefs de service a œuvré pour donner des moyens adaptés à chacun des services de cardiologie des HIA et à développer un véritable professionnalisme. Je crois que dans l’ensemble elle y a bien réussi. La génération suivante des chefs de services qui se met progressivement en place aura à bâtir la transversalité entre les services, condition qui sera indispensable pour que la cardiologie militaire conquière toute la place qu’elle mérite. MGI Richard Brion HIA Desgenettes, Lyon 292 médecine et armées, 2006, 34, 4 Dossier « Cœur et Armées » : Physiologie STRESS AU COURS DU SAUT EN PARACHUTE À TRÈS GRANDE HAUTEUR Approche par l’étude de 38 holters ECG L. AIGLE, J.-M. CHEVALIER, L. JOURNAUX, É. TREMSAL, Y. BODESCOT RÉSUMÉ Le saut opérationnel à très grande hauteur avec dérive sous voile est un concept aéroporté récent permettant de parcourir une grande distance sous voile, puis de se poser discrètement avant de réaliser une mission commando de jour et surtout de nuit. Pour étudier les réactions cardiovasculaires de ce type de saut extrême, nous avons posé 38 holters rythmiques ECG (13 sauts de jour, 17 sauts de nuit et 8 vols avec intention de saut) chez 18 parachutistes très expérimentés (610 sauts et 32 ans en moyenne). Comme prévu, les variations de fréquence cardiaque (Fc) scandent les différentes phases de saut : équipement, montée dans l’avion, dénitrogénation, accélération franche lors du saut, décroissance très lente lors de la dérive sous voile et rebond juste avant l’atterrissage. Aucune anomalie rythmique ou ischémique n’a été enregistrée. Mais de nuit, la Fc d’un même parachutiste est toujours significativement plus élevée que de jour, traduisant le stress psychologique engendré par les conditions environnementales extrêmes. Cette étude confirme que l’entraînement diminue les réactions de stress (et donc la Fc) au fil des sauts et que les parachutistes ont su gérer au mieux des incidents de saut, situations parfois très dangereuses se traduisant par une augmentation franche de la Fc sans trouble du rythme. Mots-clés : Holter ECG. Parachutisme à très haute altitude. Stress. I. INTRODUCTION. Le saut opérationnel à très grande hauteur (SOTGH) avec dérive sous voile est un concept récent d’opération aéroportée révélé au grand public par la très médiatisée traversée de la Manche en tandem réussie le 7 novembre 1999 par deux militaires français (largage à 8 200 mètres, 40 km parcourus en 27 minutes). Effectué à haute altitude (> 5 000 mètres) sous oxygène pur et avec ouverture immédiate du parachute après la sortie de l’avion, son but est l’infiltration discrète de personnels expérimentés en territoire hostile. L’objectif de ce travail (1) est d’approL. AIGLE, médecin principal. J.-M. CHEVALIER, médecin chef des services, praticien confirmé. L. JOURNAUX, médecin en chef. É. TREMSAL, médecin en chef. Y. BODESCOT, directeur des activités holter, Ela France. Correspondance : J.-M. CHEVALIER, Service de cardiologie, HIA Robert Picqué, BP 28, 33998 Bordeaux Armées. médecine et armées, 2006, 34, 4 ABSTRACT STRESS DURING HIGHT ALTITUDE PARACHUTE JUMPING. APPROACH BY HOLTER ECG. The high altitude parachute jumping, with drift under sail is a recent concept allowing to cover a long distance, then to land discreetly before realising his military mission daily or nightly. To study cardiovascular’s reactions of this extreme parachute jumping, we placed 38 holters ECG (13 daily jumps, 17 nightly jumps and 8 flights with jump intention) on 18 parachutists welltrained (mean 610 jumps and 32 years old). As planned, the variations of the cardiac frequency scan the different events of the jump. No rhythmical or ischemic abnormity was registered. But by night and for the same parachutist, the cardiac frequency is significantly higher than by day, translating the psychological stress consecutive to the extreme environmental conditions. This study confirms that training lowers the reactions of stress (then the cardiac frequency) jump after jump, and when incidents occur, the parachutists may be able to manage dangerous situations with an important but normal increase of the cardiac frequency. Keywords : Holter ECG. Parachuting at very high level. Stress. (Médecine et Armées, 2006, 34, 4, 293-298) cher les réactions cardio-vasculaires de stress engendrées par ce type de saut extrême en enregistrant l’activité électrocardiographique par la méthode holter ECG (étude des variations de fréquence, recherche d’une éventuelle extrasystolie aux deux étages, voire d’une ischémie) chez des parachutistes militaires très expérimentés et sans facteur de risque cardio-vasculaire. Après un rappel sur le SOTGH et ses différentes contraintes matérielles, physiologiques et psychologiques, nous décrirons les modalités de l’étude avant d’en présenter les résultats. II. CONTRAINTES DU SAUT OPÉRATIONNEL À TRÈS GRANDE HAUTEUR. Le SOTGH est une activité militaire parachutiste de haute technicité. Dans un but opérationnel (inf iltration d’agents, actions commando, mise en place d’équipes de 293 D O S S I E R recherche), des parachutistes sont largués à très haute altitude sous oxygène pur, le plus souvent de nuit (plus de 4 500 m jusqu'à 7 500 m). Ils ouvrent leur parachute dès la sortie de l’avion et effectuent ensuite une dérive sous voile (DSV) qui sera variable, en durée (10 à 30 minutes) et en distance (en moyenne une vingtaine de km, mais parfois jusqu’à 40 km) selon de nombreux paramètres (altitude de largage, direction et intensité des vents, terrain plat ou accidenté, etc.). Ce type de saut entraîne à la fois des contraintes physiologiques et des réactions de stress (2, 3), mais aussi des contraintes importantes d’ordre technique (avion particulier, qualification des personnels, matériels spécifiques). En effet, ces parachutistes emportent jusqu’à 80 kg de matériel (fig. 1) pour réaliser ce type de saut: deux parachutes, une bouteille d’oxygène pur au masque, un système de vision nocturne, des moyens sophistiqués de transmission, l’armement, le matériel de survie, etc. Figure 1. Chuteur opérationnel équipé. 294 A) CONTRAINTES PHYSIOLOGIQUES Les contraintes liées à l’altitude et à ce type de vol sont multiples (4, 5) : – baisse de la température liée à l’altitude (à 6 000 m il fait - 40 °C) ; – grande vitesse de chute initiale sous voile (10 m/s) en raison de la moindre densité de l’air dans les hautes couches de l’atmosphère ; – le vent relatif est un facteur aggravant la sensation de froid (wind chill factor) ; – la longueur des vols impose des contraintes positionnelles (ankylose des jambes par le harnais), de mobilisation des commandes de vol (difficile maintien prolongé des bras en l’air) et des difficultés de concentration nécessaire à la navigation de nuit avec jumelles de vision nocturne. L’ hypobarie d’altitude intervient sur l’organisme par trois mécanismes : – la diminution de la pression barométrique (loi de Boyle-Mariotte) responsable de barotraumatisme essentiellement lors de la chute libre initiale ; – la diminution de la pression partielle en oxygène responsable d'hypoxie aiguë qui peut avoir des conséquences dramatiques sur la vigilance (6) et qui impose la respiration d’oxygène pur pendant toute la durée du vol et de la dérive sous voile. Dès 4 500 m, les effets de l’hypoxie sont multiples, avec perturbation de la motricité, altération de la vision, atteinte psychique avec perte des capacités intellectuelles (6). Seule l’audition résiste à l’hypoxie et peut donc servir de moyen de sauvetage ultime (importance des liaisons radiophoniques) ; – la diminution de la pression partielle en azote observée lors de la montée en altitude est responsable de la pathologie de décompression (lois de dissolution des gaz de Henry) à la sortie de l’avion. En aéronautique, les formes graves sont heureusement rares. Cette décompression des gaz est prévenue par la dénitrogénation qui consiste en la respiration préalable d’oxygène pur pendant toute la durée de vol (vol stationnaire à une altitude cabine de 1 500 m environ pendant une durée variable en fonction de la hauteur de largage) afin d’éliminer la plus grande partie de l’azote résiduel. Cette oxygénation sera poursuivie durant la dérive sous voile jusqu'à l’arrivée au sol (fig. 2). Figure 2. Longue dérive sous voile. l. aigle B) CONTRAINTES DE STRESS PSYCHOLOGIQUE (3, 7-9). Le stress psychologique est un élément constant et majeur lors du saut en parachute que ce soit chez le débutant (10) ou le confirmé (4, 7) lors de sauts à ouverture automatique (4, 11) et à ouverture retardée (12) avec une gestion très individuelle du stress. Lors du SOTGH, le stress est bien sûr lié à ce type de saut que l’on peut qualifier d’extrême, mais aussi à l’anticipation de la mission à venir. Les conséquences d’une mauvaise gestion de ce stress peuvent entraîner des fautes de procédure lors des incidents de saut (retard à l’ouverture du parachute, mauvaise adhérence du masque, mauvais réglage des jumelles de vision nocturne, etc.), une dépense énergétique plus importante et surtout un épuisement psychique majeur avant même que la mission au sol ne débute. III. ÉTUDE. L’objectif a été d’approcher les réactions de stress lors du SOTGH en enregistrant de façon continue l’électrocardiogramme par la méthode holter ECG, enregistrant ainsi les variations de la fréquence cardiaque durant toutes les phases du saut, de l’équipement jusqu’à l’arrivée au sol et après si possible. Les enregistrements permettant d’étudier chez un même parachutiste la variation de Fc entre un saut de jour et un saut de nuit, entre des sauts successifs, lors des incidents de saut et lors des vols avec intention de saut (qui sont des vols avec équipement complet mais annulation du saut pour des raisons techniques, météorologiques le plus souvent). A) PERSONNELS ÉTUDIÉS. Se sont portés volontaires lors d’une campagne de SOTGH en septembre 1999 18 militaires de carrière appartenant au Commandement des opérations spéciales. Tous ces hommes étaient très expérimentés, avec une moyenne d’âge 32 ± 3,2 ans, plus élevée que celle trouvée dans les unités parachutistes conventionnelles. Ils étaient tous des sportifs de très bon niveau, sans antécédent personnel ou familial notable. Seuls deux parachutistes étaient fumeurs réguliers. Leur examen clinique était rigoureusement normal avec une fréquence cardiaque moyenne de 63,7 ± 6,5 bpm. Leur pression artérielle systolique était en moyenne de 124,5 ± 5,2 mmHg et la diastolique de 71,8 ± 9,8 mmHg. C’étaient des hommes parfaitement stables sur le plan psychologique, ayant bénéficié de nombreux tests de sélection préalable. Leur expérience parachutiste est bien sûr significative, notamment en chute libre avec un minimum de 250 sauts commandés et un maximum de 1 500, soit une moyenne de 610 ± 330 sauts. Le nombre de sauts à très grande hauteur (SOTGH) était bien sûr beaucoup plus limité (14 ± 5 sauts en moyenne, extrêmes de 5 à 25 sauts), car cette activité est d’introduction récente avec un nombre très limité (et très onéreux) de campagne de sauts. stress au cours du saut en parachute à très grande hauteur B) MATÉRIEL. N’ayant pu bénéficier d’un soutien institutionnel (projet de recherche refusé car jugé sans intérêt médico militaire !) nous avons utilisé du matériel aimablement prêté par la société ELA médical avec 5 holters rythmiques de type SYNEFLASH et 10 cartes mémoires type SYNESIS de 20 méga-octets. Le holter se compose d’un boîtier de faible encombrement (130 x 90 x 25 mm) et de faible poids (290 g) avec un écran à cristaux liquide et un raccord à cinq pistes. La séquence de mise en marche du holter est simple et rapide. L’unité centrale de la société ELA Médical nous a aussi été prêtée avec le logiciel d’interprétation SYNETEC qui a permis de sauvegarder sur place l’ensemble des holters puis une analyse secondaire. Après dégraissage de la peau, tous les holters ont été posés de la même manière juste avant que les parachutistes ne s’équipent. À l’issue du saut, les données étaient sauvegardées dans des fichiers individuels de l’unité centrale puis les cartes mémoires étaient réinitialisées pour une nouvelle utilisation. C) MÉTHODE D’ANALYSE. Avant de pouvoir analyser les variations de Fc et du segment ST, un important travail de nettoyage des tracés a été nécessaire. Il a consisté en la validation de toutes les morphologies de QRS en commençant par les véritables artefacts puis les complexes normaux et supra-ventriculaires pour finir par les vraies ESV (peu nombreuses). Ensuite, la bonne position des curseurs pour l’intervalle R-R a été vérif iée. Puis, il a fallu valider la totalité des zones artefactées (ligne de base instable, défaut de reconnaissance des complexes QRS) en revalidant si nécessaire chaque battement tant en terme de positionnement que d’identification. Le T0 (heure de largage) a ensuite été déterminé en réalisant un zoom sur le pic de Fc et en le comparant avec l’horaire connu du largage, puis validation déf initive. À l’issue de ce long travail de « nettoyage-validation » nécessaire pour obtenir des tracés fiables, les données de Fc ont été exportées dans un fichier texte par périodes de 30 secondes, puis importées dans un f ichier EXCEL et alignées sur le T0. Pour l’analyse statistique des données, une loi polynomiale d’ordre 4 a été utilisée pour le tracé de la Fc, car elle seule permettait d’obtenir des coefficients de corrélation les plus élevés possibles ainsi que la meilleure approche de la réalité des courbes. Rapidement après le début de l’analyse, de grosses variations dans les écarts-type ont contraint de modifier la méthode d’étude en moyennant les intervalles par minute puis en réalisant une moyenne glissante lissée sur quatre minutes, pour améliorer le coefficient de corrélation. Lors de l’analyse globale et statistique des holters par la société ELA Médical, deux tracés ont dû être rejetés car non exploitables. D) LIMITES DE LA MÉTHODE. Nous avons dû faire face à de nombreux problèmes. Le premier, a été la conception artisanale du protocole d’étude dans le cadre d’une thèse de doctorat en médecine, sans f inancement institutionnel et avec 295 D O S S I E R uniquement la bonne volonté des médecins parachutistes et le prêt gracieux du matériel par la Société Ela Medical. Le second problème a été l’attente d’une campagne de SOTGH. Cette campagne, plusieurs fois repoussée, dépendait de nombreux paramètres dont la disponibilité d’un avion, de différents techniciens et de la météorologie car les enchaînements de sauts sont toujours sous sa dépendance. La météo sera plutôt favorable mais de nombreux problèmes d'avionique perturberont certains sauts. En pratique, nous n’avons été prévenus que quinze jours avant le début de la campagne de SOTGH. Il a donc fallu récupérer rapidement tout le matériel d'enregistrement et d'analyse, apprendre à le manier et définir un protocole d'étude. Puis il a fallu prendre contact avec les médecins parachutistes assurant le soutien médical de la campagne afin qu’ils transmettent auprès du commandement la demande d’autorisation de réaliser cette étude. Tous ces problèmes techniques et ces contraintes expliquent surtout que nous n’ayons pas eu le temps de bien décrire aux parachutistes l’intérêt de garder les holters plus d’une heure voire 24 heures après le saut. Il n’y a pas eu de problème avec le matériel de la société ELA, simple d’emploi, fiable et très solide. Il n’y a pas eu de perte de données grâce à un délai minimum entre le recueil et la sauvegarde. Enfin, il n’y pas eu de défaut de stockage, et l’activité musculaire n’a pas perturbé le signal. Secondairement, nous avons constaté qu’il aurait fallu recueillir de façon plus précise les horaires de largage et surtout d’arrivée au sol pour affiner les résultats. Ceci aurait pu être facilement réalisable car il y avait un médecin en soute et un autre au sol susceptibles de relever ces horaires. IV. RÉSULTATS. Au cours de cette campagne de SOTGH, 39 holters ECG ont été mis en place. Un des holters n’a pas fonctionné pour une raison inconnue. Sur les 38 autres holters posés, 8 parachutistes ont été équipés correctement mais les sauts n’ont pas eu lieu (vols avec intention de saut) pour des raisons matérielles et d’avionique. Secondairement, deux tracés holter ECG ont été exclus car non exploitables. Au total, 28 holters avec dérive sous voile seront été réalisés : 12 lors d’un saut de jour (entre 5 600 et 6 300 m), 16 lors d’un saut de nuit (5 600 m), 7 personnels ayant sauté une fois de jour et une fois de nuit. L’horaire de largage a été défini comme T0. Pour l’étude, nous avons réalisé les moyennes des données en prenant comme un intervalle de temps de 120 minutes avant T0 et 60 mn après. Pour les huit vols avec intention de saut, les enregistrements s’arrêtent dans l’avion à différentes phases de la procédure de dénitrogénation. Ils sont étudiés à part. et fastidieuse (vérification du matériel). Ici les modifications de la Fc (qui varie de 95 à 105 bpm environ) sont dues principalement à un effort physique (équipement, longue station debout). En vol (2), les parachutistes sont assis au repos complet et n’ont aucune tâche à effectuer. Ils respirent de l’oxygène pur et leur fréquence cardiaque diminue très lentement mais dans des proportions moindres que l’on aurait été en droit d’attendre chez ces hommes entraînés au repos. Pendant la dénitrogénation (une heure environ), la Fc moyenne est de 85 bpm. Dans cette situation, le stress psychologique est l’élément fondamental responsable de la tachycardie relative persistante. Viennent ensuite les deux pics de Fc (3 et 4) correspondant à des efforts physiques en soute avant la sortie de l’avion. En ce qui concerne les pics de Fc à la sortie et à l'ouverture du parachute (5), ils sont quasiment simultanés car l'ouverture de la voile est très précoce (dans les cinq premières secondes). On trouve des valeurs moyennes à 132 bpm le jour et 154 bpm la nuit avec des extrêmes de 180 bpm, toujours inférieures aux Fc maximales théoriques. Juste après l'ouverture, on note un petit décroché dans la courbe (6) qui s'explique par les manœuvres à réaliser pour la navigation (tour d’horizon, vérification de l’azimut) et la sécurité de la dérive sous voile. Lors de cette dérive sous voile (7), on note une décroissance lente et régulière de la Fc, passant en moyenne à 105 bpm en dix minutes de vol. L'autre caractéristique de ces sauts est la phase d'atterrissage (8) qui entraîne un ressaut tachycardique modéré en fin de vol. Celui ci est lié à la crainte d’un obstacle imprévu, au largage près du sol de la gaine contenant le matériel emporté et à la difficulté du poser avec tout l’équipement. Lors de cette dernière phase, la Fc passe à 115 bpm en moyenne. Le dernier pic d’accélération (9) correspond au déséquipement, avec l’euphorie relative post stress (3, 8) sans différence entre un saut de jour ou de nuit. Lors des douze sauts de jour (fig. 3, tracé en bleu), on retrouve un tracé similaire à celui des 28 sauts moyennés mais décalé vers des fréquences cardiaques plus basses A) HOLTERS RYTHMIQUES DE 28 SOTGH. La figure 3 représente le diagramme des fréquences cardiaques moyennes des 28 sauts (en jaune), des 12 sauts de jour (en bleu) et des 16 sauts de nuit (en rouge). Que ce soit de jour comme de nuit, on individualise facilement huit périodes. La phase d’équipement au sol (1) est longue 296 Figure 3. Diagramme des fréquences cardiaques moyennes des 28 sauts (en jaune), des 12 sauts de jour (en bleu) et des 16 sauts de nuit (en rouge). 1 = long équipement au sol ; 2 = assis dans l’avion avec dénitrogénation en O2 pur ; 3 et 4 = lever et efforts en soute ; 5 = sortie de l’avion et ouverture immédiate ; 6 = vérification de l’azimut ; 7 = dérive sous voile ; 8 = atterrissage ; 9 = déséquipement. l. aigle (moins dix bpm) sur l’ensemble de l’enregistrement, ce qui est classique. La moyenne de Fc sous voile est de 98 bpm. C’est la seule étude dans la littérature qui rapporte les variations de Fc lors des sauts de nuit. En effet, les réactions cardiovasculaires ont été plusieurs fois étudiées par la méthode holter (8, 11, 13-15) mais toujours lors de sauts diurnes. Lors des 16 sauts de nuit enregistrés (fig. 3, ligne rouge), on retrouve les huit périodes pré décrites mais avec un Fc toujours au moins supérieure de 10 voire 15 bpm par rapport à la même période en saut de jour. Que ce soit lors de la dénitrogénation assis dans l’avion ou lors des mouvements de vérification de matériel en soute. Le pic de Fc au largage est à 154 bpm en moyenne la nuit (soit 22 bpm de Fc en plus que le jour) ce qui traduit bien le stress psychologique engendré par le saut de nuit. La différence est encore plus caricaturale lors de la dérive sous voile où la Fc est toujours supérieure à 110 bpm, soit 20 bpm de plus que le jour. Enf in, malgré un strict repérage préalable et des cartes très précises, la crainte d’un obstacle non vu à l’arrivée au sol (fossé récemment creusé, souche d’arbre non arrachée, fil de fer tendu récent) angoisse toujours ces grands professionnels (16, 17). L’étude montre que de nuit la différence est significative pour les variations de la Fc par rapport à celles de jour, et que cette variation est essentiellement due au stress psychologique car les contraintes matérielles et environnementales (froid, etc.) sont les mêmes hormis l’obscurité et le port de jumelle à vision nocturne. Lors d'études précédentes à l'ETAP (4), des vols avec intention de saut (VIS) avaient été enregistrés chez des novices lors de SOA. Il avait été noté, après une courte phase de tachycardie liée à l’agitation du personnel de soute, une bradycardie relative dès l'annonce de l'annulation du saut. B) HUIT HOLTERS LORS DE VOL AVEC INTENTION DE SAUT. Lors des huit VIS (5 de jour et 3 de nuit) les résultats sur la Fc sont différents chez ces parachutistes très expérimentés. L'annulation du saut n'a pas l'effet « libérateur de stress » comme chez de jeunes recrues (4) et la fréquence cardiaque poursuit sa rapide décroissance vers une valeur proche de la Fc de repos. C'est une nouvelle preuve de l'adaptation émotionnelle due à l’entraînement. Ceci nous permet aussi de confirmer que lors d’un vol normal, la Fc ne descend pas sous les 75 bpm traduisant bien la concentration et le stress physiologique d’avant saut. C) SEPT PERSONNELS ONT EFFECTUÉ UN SAUT DE JOUR ET UN SAUT DE NUIT. Pour chacun d’eux, la différence est significative avec une Fc de nuit toujours plus élevée que celle de jour (pour l’un des personnels, la Fc maximale de nuit est de 160 bpm, la plus basse de jour au même moment est de 80 bpm). Un parachutiste (tab. I) a effectué les 8, 10 et 11 septembre 1999 trois sauts de jour dans les mêmes conditions. Si la chute et l’ouverture du parachute entraînent une réaction catécholergique identique, on constate une nette diminution de la Fc en récupération post saut. On peut en stress au cours du saut en parachute à très grande hauteur déduire que la répétition des sauts permet une meilleure gestion du stress et donc une meilleure maîtrise de l’activité. Ce qui confirme l’importance de l’entraînement pour des activités à risque comme le SOTGH, le parachutiste devant être immédiatement apte à débuter sa mission le plus souvent en milieu hostile et inconnu. Tableau I. Évolution de la Fc après le saut d’un même parachutiste ayant réalisé trois SOTGH diurnes à trois jours d’intervalle. Temps après T0 08 /09 10/09 11/09 + 5 minutes 87 84 86 + 9 minutes 90 85 82 + 15 minutes 101 84 81 + 20 minutes 95 84 84 + 25 minutes 117 105 108 D) INCIDENTS DE SAUT. Au cours de cette étude, 4 incidents de sauts ont été enregistrés : – 2 à la sortie de l’avion (retard d’ouverture du parachute de 3 à 6 secondes) ; – 1 sous voile (inefficacité des jumelles à vision nocturne) ; – et 1 à l’atterrissage (obstacle imprévu sur l’aire de poser). Lors d’un saut de nuit, le parachutiste P. S. fait sa séquence d’ouverture mais sans succès. La voile se libère enfin après six secondes. Pour un chuteur de son expérience, cela reste une situation extrêmement anxiogène mais qui a été analysée de manière sereine (il se laissait encore trois secondes avant de tirer sur la poignée du parachute de réserve). L’ECG parle de lui même, montrant une tachycardie importante sur la durée de l’incident (165 bpm) et un lent retour à la normale. Alors que pour le même saut de jour sa Fc était à 91 sous voile. Vingt minutes après le saut, la Fc était toujours sinusale à 105 bpm après l’incident de saut, alors qu’il était préalablement à 86 bpm sans incident. Le parachutiste A. Ch. effectue un saut de nuit avec un système de vision nocturne cassé (fig. 4). Ceci se traduit par une tachycardie qui s’est prolongée tout le vol (Fc moyenne à 135 bpm sous voile) alors qu’elle était à 120 bpm lors d’un deuxième saut avec jumelles à vision nocturne. Les quatre incidents ne sont pas « critiques » si on se place dans un contexte de parachutisme de loisir. Ils prennent ici une tout autre signification : décider de libérer une voile et de repartir en chute libre avant d’ouvrir le parachute de secours de nuit, en charge sous oxygène et à 5 600 mètres n'est pas une situation que tout un chacun est à même de gérer facilement. L'expérience, la gestion du stress et des événements sont des éléments capitaux mais qui n'empêchent pas une tachycardie réactionnelle plus ou moins intense liée à la décharge physiologique d'adrénaline. Mais les fréquences maximales retrouvées (de l’ordre de 180 bpm), restent en deçà des valeurs de la FMT. Surtout, aucun trouble du rythme auriculaire ou ventriculaire significatif n’a été révélé. Dans d'autres études (10, 18) 297 D O S S I E R Figure 4. Diagramme des fréquences cardiaques moyennées toutes les 5 minutes et centrées sur T0 (sortie d’avion) chez un même parachutiste. La différence entre le saut de nuit (ligne du haut) et de jour (ligne du bas) est manifeste lors de la dérive sous voile beaucoup plus anxiogène. sans notion d'incident, des sujets plus novices passent largement au-dessus des 200 bpm. Ceci traduit bien la capacité à gérer différemment de tels événements. V. CONCLUSION. Ce travail représente la première étude des variations de fréquence cardiaque lors des sauts en parachute de nuit (jamais décrit) et de jour, qui plus est à grande hauteur (> 5 000 m) en respiration d’oxygène pur et dans des conditions d’atterrissage parfois difficiles. Cette étude a permis d’obtenir un tracé ECG continu caractéristique du SOTGH de jour et de nuit, avec ses différentes phases : équipement initial, long vol assis en cabine pressurisée avec dénitrogénation, puis saut agressif à très grande altitude (froid, hypoxie, accélération), puis assez longue dérive sous voile et atterrissage en milieu parfois hostile. Les réactions cardio-vasculaires de stress sont franches pour des personnels très entraînés sans toutefois dépasser la FMT ni révéler d’anomalie rythmique. La Fc des sauts de nuit est significativement supérieure de dix bpm au moins à celle de jour lors de toutes les phases du saut et du vol sous voile, tant individuellement que collectivement. La succession de sauts entraîne une diminution relative de la Fc moyenne et donc du stress témoignant de l’importance d’un l’entraînement régulier. Lorsque le parachutiste est équipé mais n’a pas sauté, il n’y a pas d’appréhension du saut. Par ailleurs, lors des incidents de saut, l’expérience a permis une bonne gestion des situations. Le SOTGH doit donc être considéré comme un parachutisme de l’extrême, qui nécessite une sélection médicale et technique rigoureuse des candidats. Il serait très intéressant d’envisager une préparation mentale pour ces chuteurs comme cela se pratique déjà dans de nombreux sports de haut niveau, car cette étude révèle un stress anticipatoire franc pour des chuteurs très entraînés qui, une fois au sol, auront besoin de toutes leurs capacités psychiques pour réaliser leur mission. Il serait aussi intéressant de refaire une étude en conservant les holters lors d’un enchaînement saut-exercice de combat commando afin d’étudier l’évolution de la Fc dans une situation la plus proche possible de la réalité. RÉFÉRENCES BIBLIOGRAPHIQUES 1. Aigle L. Stress au cours du saut opérationnel à très grande hauteur : apport du holter ECG. Thèse : Bordeaux II ; 2000 (52) : 89 p. 2. Herd JA. Cardiovascular response to stress. Physiological Reviews 1991 ; 71 (1) : 305-26. 3. Vanuxem P, Astolfi A, Giuriato L, Duflot JC. Le parachutisme de l’extrême. Méd Sport 1998 ; 72 : 73-7. 4. Colomb F, Chevalier JM, Beauche A. Réactions cardio-vasculaires de stress du saut en parachute. Méd Armées 1997 ; 25 (3) : 229-35. 5. Didier A, Jouffray L, Maurel C, Hiltenbrand C. Physiopathologie des sauts en haute altitude. Méd Armées 1982 ; 10 (3) : 211-2. 6. Marotte H, Bittel J. Conséquences psychomotrices de l’hypoxie aiguë d’altitude. Med Sport 1995 ; 69 (3) : 127-31. 7. Falk B, Bar-ELI M. The psycho-physiological response to parachuting among novice and experienced parachutists. Aviat Space Environ Med 1995 ; 66 : 114-7. 8. Grangier C. Stress et sport : population à risque et prévention. Enregistrement holter de la fréquence cardiaque chez 10 sujets sains libéristes montrant les effets cardiaques du stress émotionnel intense. Thèse : Grenoble ; 1985 (132) : 65 p. 9. Schedlowski M, Tewes U. Physiological arousal and perception of bodily state during parachute jumping. Psychophysiology 1992 ; 29 (1) : 95-103. 10. Galante J, Hernandez A, Colin L, Camacho B, Verdejo J, Ferez S. Continuous electrocardiographic recording during a first parachute jump. Arch Inst Cardiol Mex 1988 ; 58 (4) : 325-31. 298 11. Deroanne R, Cession-Fession A, Juchmes J, Servais JC, Petit JM. Telemetric control of heart adaptation during automatic and free-fall parachute-jumps. Aviat Space Environ Med 1975 ; 46 (2) : 128-31. 12. Léon C. Enregistrement électrocardiographique circadien chez 15 parachutistes. Med Armées 1983 ; 11 (7) : 627-9. 13. Gauthier P, Jouffray L, Rodi M, Gottesmann C. Electroencephalographic recordings during parachute jump sessions. Aviat Space Environ Med 1980 ; 51 (4) : 336-8. 14. Jung K, Schulze J. Sport-medical studies on parachute jumpers with particular reference to behaviour of heart rate. Biotelem Patient Monit 1982 ; 9 (4) : 238-50. 15. Tak T, Cats VM, Dunning AJ. Ambulatory ECG recording during competitive parachute jumping in apparently healthy young men : more evidence for intermittent vagal dominance during enhanced sympathetic activity. Eur Heart J 1986 ; 7 (2) : 110-4. 16. Green M, Turner C, Purdie DM, McClure R. Injury related risk behaviour-study of Australian. Skydivers. J Sci Med Sport 2003 ; 6 (2) : 166-75. 17. Knapik JJ, Craig SC, Hauret KG, Jones BH. Risk factors for injuries during military parachuting. Aviat Space Environ Med 2003 ; 74 (7) : 768-74. 18. Deinzer R, Kirschbaum C, Gresele C, Hellhammer DH. Adrenocortical responses to repeated parachute jumping and subsequent h-CRH challenge in inexperienced healthy subjects. Physiol Behav 1997 ; 61 (4) : 507-11. l. aigle Dossier « Cœur et Armées » : Physiologie ÉTUDE DE LA VARIABILITÉ SINUSALE LORS D’IMMERSION TOTALE DE LONGUE DURÉE EN EAU FROIDE G. CELLARIER, CL. ROBINET, L. MOUROT, A.-V. DESRUELLE, C. JÉGO, F. BARBOU RÉSUMÉ ABSTRACT La variabilité sinusale peut être utilisée comme moyen de dépistage non invasif de la fatigue physique. Nous nous sommes intéressés à ses variations lors d’immersion de longue durée en eau froide chez des nageurs de combat, afin d’apprécier le retentissement sur les capacités opérationnelles. La variabilité sinusale a été enregistrée les nuits précédant et suivant l’immersion, et durant la totalité de l’immersion, chez dix plongeurs totalement immergés pendant six heures, à 10° et à 18°. Il existe une diminution du tonus végétatif entre les nuits précédant et suivant l’immersion (SDNN : -1 % à 18°), significative à 10° (SDNN : -14,2 %, p < 0,05) et plus marquée pour le parasympathique (p < 0,05). La baisse parasympathique est plus importante à 10° qu’à 18 °C (HF : -28,4 % versus -47,6 %, p < 0,001). Durant l’immersion, il existe une majoration de la variabilité sinusale (SDNN : +16,1 % à 18° [p = 0,03], et +6,2 % à 10° [p = ns]), prépondérante au niveau du parasympathique (HF/LF : +19,9 % à 18° et +16,0 % à 10°, p = ns). Il s’agit à notre connaissance de la première expérimentation en immersion complète. La modification des paramètres de variabilité sinusale au décours d’une immersion prolongée en eau froide pourrait être en rapport avec une fatigue physique et une baisse des performances opérationnelles en fin d’immersion qui persiste jusqu’au lendemain. HEART RATE VARIABILITY DURING LONG DURATION TOTAL BODY IMMERSION IN COLD WATER. Heart rate variability can be used for non invasive detection of physical fatigue. We studied its variations during long duration immersion of combat divers in cold water, in order to evaluate the consequences on operational capacities. Heart rate variability was recorded the nights preceding and following immersion, and during the totality of immersion, on 10 divers completely immerged during 6 hours, at 10° then 18 °C. There is a decrease of vegetative tone the night following immersion comparing with the preceding one (SDNN : -1 % at 18°), significant for immersion at 10 °C (SDNN : -14.2 %, p < 0.05) and more marked for the parasympathetic tone (p < 0.05). The parasympathetic decrease is more important at 10° than at 18° (HF : - 28,4 % versus -47,6 %, p < 0,001). During immersion, we observe an increase of heart rate variability (SDNN : +16.1 % at 18° [p = 0.03], and +6.2 % at 10°, [p = ns]), more marked for the parasympathetic tone (HF/LF: + 19.9 % at 18° and + 16.0 % at 10°, p = ns). As far as we know, it is the first experimentation realized in complete immersion with such data recordings. The heart rate variability parameters modifications after a long duration immersion in cold water may suggest a fatigue and a diminution of the operational performances at the end of the diving, prolonged at least the following day. Mots-clés : Capacité opérationnelle. Fatigue physique. Immersion totale. Tonus neurovégétatif. Variabilité sinusale. Keywords : Complete immersion. Heart rate variability. Neurovegetative tone. Operational capacities. Physical fatigue. (Médecine et Armées, 2006, 34, 4, 299-303) I. INTRODUCTION. La variabilité sinusale (VS) représente les variations physiologiques des intervalles RR (entre 2 QRS), traduisant l’influence de la balance vago-sympathique sur le nœud sinusal. De nombreux auteurs ont démontré son intérêt dans l’évaluation non invasive de l’entraînement, en G. CELLARIER, médecin en chef, praticien confirmé. Cl. ROBINET, médecin en chef, spécialiste de médecine de la plongée. L. MOUROT, post-doctorant. A.-V. DESRUELLE, ingénieur d’étude et de fabrication. C. JÉGO, médecin principal, praticien confirmé. F. BARBOU, médecin principal, praticien confirmé. Correspondance : G. CELLARIER, Service de cardiologie, HIA Sainte-Anne, BP 600, 83800 Toulon Armées. médecine et armées, 2006, 34, 4 particulier pour la détection du surentraînement et de l’état de fatigue (1-9). Le but de ce travail a été d’analyser la VS chez des nageurs de combat, déterminer la faisabilité de son enregistrement chez un plongeur en immersion complète prolongée en eau froide, et étudier son application pour évaluer le retentissement sur l’aptitude opérationnelle. II. PROTOCOLE EXPÉRIMENTAL. L’expérimentation a reçu l’accord du CCPPRB de Marseille 1 (recherche biomédicale fondamentale en conditions extrêmes, sans bénéfice individuel direct). 299 D O S S I E R A) SUJETS. Nageurs de combat au nombre de dix (33 ± 3 ans, 173 ± 2 cm, 77 ± 3 kg), tous volontaires ayant signé un consentement éclairé, ont été immergés totalement pendant six heures, à deux reprises à une semaine d’intervalle, à 18 °C et à 10 °C, dans un ordre déterminé. Les plongeurs ont bénéficié d’une protection thermique identique à celle utilisée pour leurs missions opérationnelles, modifiée pour permettre le passage des différents câbles, capteurs et sondes. B) MATÉRIELS. L’immersion a été réalisée dans un bassin hors sol spécifiquement créé, avec régulation thermique de l’eau. Les sujets ont été sanglés et lestés en position demi-assise sur un siège immergé de façon à ce que la tête soit complètement sous l’eau. Un respirateur de type « Benett » a permis la ventilation des plongeurs. Un monitorage ECG et des températures cutanées et centrales complétait l’équipement qui comportait un dispositif de recueil urinaire, un enregistreur d’EMG et un cathéter sanguin permettant notamment le recueil des catécholamines plasmatiques (fig. 1, 2). C) MÉTHODES. L’enregistrement Holter a été réalisé par un appareil miniaturisé Holter Vista ® , avec un logiciel Ultima HolterSoft ® (Novacor SA), permettant 72 heures d’enregistrement continu sur deux pistes. La variabilité sinusale a été mesurée et analysée selon les recommandations ESC/NASPE (10). Les différents paramètres de VS et leur signification sont rappelés dans le tableau I. La VS a été analysée les nuits avant et après immersion et durant la totalité de l’immersion. Les résultats sont illustrés par les figures 3 à 5. Les analyses statistiques et les comparaisons de moyennes sont faites à l’aide du test t de Student et les analyses multivariées en analyse de variance (ANOVA à 1 facteur). Figure 1. Schéma du protocole expérimental. 300 Figure 2. Plongeur immergé. III. RÉSULTATS. A) ANALYSE DE LA VS AVANT ET APRÈS IMMERSION (FIG. 3). Il existe une variation des paramètres de VS témoignant d’une altération du tonus végétatif, plus marquée pour le parasympathique. 1. Immersion à 18 °C. Il existe une diminution (n’atteignant pas le seuil de signif icativité) des paramètres de VS entre la nuit précédant l’immersion et la nuit suivante. Cette Figure 3. Variations de variabilité sinusale après immersion. g. cellarier Tableau I. Paramètres de variabilité sinusale et leur signification. Analyse spectrale (reflet vago-sympathique) Analyse temporelle (équivalence spectrale) Très basses fréquences (VLF) : 0,0033 - 0,04 Hz (thermorégulation et activité vasomotrice). Basses fréquences (LF) : 0.04 - 0,15 Hz (activité sympathique). Hautes fréquences (HF) : 0.15-0,4 Hz (activité parasympathique). Rapport HF/LF : balance sympathique. SDNN, ou écart-type des RR : densité spectrale totale. SDANN 5 : écart-type sur 5 mn (LF). PNN 50 : % de triplets avec > 50 ms de différence entre 2 RR (HF). diminution concerne l’ensemble des indices de VS : globaux (SDNN = 105 ms vs 104 ms ; PNN50 = 23,8 % vs 16,8 %), activité orthosympathique (LF = 2 048 ms2 vs 1 473 ms2), activité sympathique (HF = 680 ms2 vs 487 ms 2 ), et balance sympathique témoignant d’une baisse plus marquée du tonus parasympathique (HF/LF = 0,34 vs 0,29). B) ÉVOLUTION DE LA VS AU COURS DE L’IMMERSION (FIG. 4). 2. Immersion à 10 °C. Il existe également une diminution des paramètres de VS entre la nuit précédant l’immersion et la nuit suivante, atteignant cette fois le seuil de significativité : SDNN = 120 ms vs 103 ms (p = 0,05) ; PNN50 = 27,2 % vs 16,1 % (p < 0,05) ; LF = 2 495 ms 2 vs 1 430 ms 2 (p < 0,05) ; HF = 963 ms2 vs 505 ms2 (p < 0,05) ; HF/LF = 0,37 vs 0,32 (p = ns). 1. Immersion à 18 °C. L’analyse de la VS durant l’immersion montre, entre le début et la fin de la plongée, l’existence d’une majoration des indices avec augmentation prépondérante du tonus parasympathique. SDNN = 91 ms vs 105 ms (p = 0,03) ; PNN50 = 15,4 % vs 24,3 % (p = ns) ; LF = 766 ms 2 vs 2 953 ms 2 (p = ns) ; HF = 5 335 ms2 vs 1 037 ms2 (p = ns) ; HF/LF = 0,37 vs 0,44 (p = ns), au début de l’immersion versus à la f in de l’immersion respectivement. 2. Immersion à 10 °C. SDNN = 108 ms vs 115 ms (p = ns) ; PNN50 = 25,0 % vs 33,6 % (p = 0,01) ; LF = 3 356 ms2 vs 4 257 ms2 (p = ns) ; HF = 1 472 ms2 vs 2 344 ms2 (p = ns) ; HF/LF = 0,48 vs 0,56 (p = ns), au début de l’immersion versus à la f in de l’immersion respectivement. C. INFLUENCE DE LA TEMPÉRATURE D’IMMERSION (FIG. 5). L’altération du tonus parasympathique la nuit suivant l’immersion est plus importante à 10° qu’à 18 °C : HF = 505 vs 487 ms2 (p < 0,001) ; HF/LF = 0,29 vs 0,32 (p = ns). IV. DISCUSSION. Figure 4. Évolution de la VS au cours de l’immersion. étude de la variabilité sinusale lors d’immersion totale de longue durée en eau froide Il s’agit à notre connaissance de la première expérimentation d’immersion totale, avec tête sous l’eau des sujets. Cette étude a nécessité la conception et la réalisation d’un bassin spécif ique par l’Institut de médecine navale du SSA. La tête des plongeurs était en affleurement juste sous le niveau d’eau, et la ventilation comportait une pression inspiratoire positive qui compensait la différence de pression due à l’immersion. La durée de l’immersion et les températures étudiées reflètent les conditions réelles opérationnelles des nageurs de combat. Elles ont nécessité une surveillance continue de la température centrale, qui s’abaissait à 36,24 ± 0,11 °C et 36,18 ± 0,11 °C lors des immersions à 18° et 10° respectivement (p = ns entre les deux températures d’immersion). Un monitorage cardio-respiratoire ainsi que l’enregistrement de la VS a été permis grâce 301 D O S S I E R Figure 5. Différences de variabilité sinusale après immersion selon la température. Analyse multivariée (test ANOVA 1 facteur). à l’adaptation des combinaisons permettant le passage des fils, capteurs et sondes. Concernant l’enregistrement Holter-ECG, il s’agit également de la première analyse de la variabilité sinusale en continu pendant une immersion totale. Nous retrouvons une majoration de la VS au cours de l’immersion, avec prépondérance de la majoration parasympathique. Ces données ont déjà été notées par différentes équipes lors de la soumission des sujets à un stress physique (5, 79). Il est bien sûr diff icile de faire la part du stress psychique engendrée par une immersion de cette durée à des températures particulièrement basses. Dishman et al. (11) ont rapporté l’influence inverse du stress psychique préalable sur les variations du tonus parasympathique. La connaissance de la température de plongée avant l’immersion (cinq plongeurs commençant par une immersion à 18° et cinq par une température de 10° puis inversement) a certainement joué un rôle dans la modulation de la composante HF lors de l’immersion. Ceci peut expliquer, en partie, l’incrément paradoxalement moins important des basses fréquences durant l’immersion à 10°. Les travaux précédemment conduits lors d’immersion tête hors de l’eau sont également superposables (12-17). Miwa et al. décrivent une diminution des HF au repos après trois jours d’immersion sèche (13), et retrouvent tout comme dans notre travail une majoration du parasympathique au cours d’une immersion aux épaules (14). Ces modifications au cours de l’immersion sont conf irmées par les travaux de Seps et al. qui les rapprochent de celles relevées en microgravité (15). Cette activation parasympathique en cours d’immersion peut être en partie expliquée par les altérations hémodynamiques dues à l’immersion (avec notamment élévation des pressions de perfusion thoraciques), comme l’a montré l’équipe de Schipke (16). L’influence de la température de l’eau semble néanmoins importante dans ces modif ications survenant pendant l’immersion, 302 comme l’ont montré Mourot et al. chez des plongeurs non totalement immergés à neutralité thermique puis en eau fraîche (17). Nous mesurons d’ailleurs dans notre expérimentation une sécrétion de catécholamines plus importante à 10° tout au long de l’immersion, avec un pic en milieu d’immersion plus marqué à 10° qu’à 18° (adrénaline : 80,4 vs 48,8 pg/ml, p < 0,05 ; noradrénaline : 1 752 vs 1 020 pg/ml, p < 0,05). L’activation parasympathique pendant la plongée pourrait ainsi également être la conséquence d’un à-coup vagal secondaire au stress thermique. Les travaux de l’équipe stéphanoise (4-6) ont bien montré l’influence de la fatigue physique sur la VS. Bien que réalisés dans des conditions différentes puisque étudiant les conséquences d’un entraînement intensif, ils peuvent faire émettre l’hypothèse que les modifications prédominant sur le parasympathique la nuit suivant l’immersion chez nos nageurs de combat, témoigne d’une fatigue physique qui persiste au moins jusqu’au lendemain de la plongée. D’autres travaux, incluant des mesures de paramètres de forces physiques par exemple, seront néanmoins nécessaires pour rattacher ces modifications de VS à une fatigue physique. Le rôle de la température dans ce stress physique parait en revanche évident, et est confirmé dans notre étude par une variation de la VS plus importante à 10° qu’à 18 °C (avec baisse de HF > LF). D’autres travaux issus de cette expérimentation et en cours de publication mettent en évidence une déshydratation secondaire à la plongée, persistant le lendemain, pouvant contribuer à la majoration de cette fatigue physique. A) LIMITES DE L’ÉTUDE. La taille limitée de notre effectif, conséquence de la lourdeur de l’expérimentation, explique certainement la non significativité statistique des résultats à 18°. Les conditions de stress différentes (ordre de passage et températures connus avant l’immersion) ont un rôle sur le tonus vago-sympathique. Des raisons techniques ne rendaient pas possible la modulation immédiate de la température du bassin, imposant le passage en deux groupes de températures prédéfinies des sujets. L’absence de corrélation à des tests d’exercice ne permet pas d’affirmer formellement la fatigue physique des plongeurs. V. CONCLUSIONS ET PERSPECTIVES. De cette première expérience d’analyse de la variabilité sinusale chez des sujets soumis à une immersion complète en eau froide, on retiendra, comme dans les travaux précédemment réalisés (immersion tête hors d’eau) une majoration du tonus parasympathique au cours de l’immersion, et une diminution des paramètres de variabilité sinusale au décours de l’immersion. Ces résultats pourraient être liés d’une fatigue physique corrélée à la contrainte thermique, présente lors de la récupération nocturne suivante ; des travaux g. cellarier complémentaires sont nécessaires pour étayer cette hypothèse. Ils peuvent témoigner d’une diminution des capacités opérationnelles des nageurs de combat, apparaissant dès la fin de l’immersion, et persistant au moins jusqu’au lendemain de la plongée. La confection et l’essai de tenues à réchauffage actif sont une voie de recherche af in d’optimiser ces performances opérationnelles. Dans l’attente, il faut insister sur l’importance de la réhydratation après la plongée. RÉFÉRENCES BIBLIOGRAPHIQUES 1. Coumel P, Maison Blanche P, Catuli D. Heart rate and heart variability in young adult. J Cardiovasc Electrophysiol 1994 ; 5 : 899-911. 2. Hedelin R, Kentta G, Wiklund U, Bjerle P, Henriksson-Larsen K. Short-term overtraining : effects on performance, circulatory responses, and heart rate variability. Med Sci Sports Exerc 2000 ; 32 (8) : 1 480-4. 3. Lehmann M, Foster C, Dickhuth H-H, Gastmann U. Autonomic imbalance hypothesis and overtraining syndrome. Med Science Sport Exerc 1998 ; 30 (7) : 1 140-5. 4. Pichot V, Bourin E, Roche F, Garet M, Gaspoz JM, Duverney D et al. Quantification of cumulated physical fatigue at the workplace. Pflugers Arch 2002 ; 445 (2) : 267-72. 5 Pichot V, Busso T, Roche F, Garet M, Costes F, Duverney D et al. Autonomic adaptations to intensive and overload training periods : a laboratory study. Med Sci Sports Exerc 2002 ; 34 (10) : 1 660-6. 6. Pichot V, Roche F, Gaspoz JM, Enjolras F, Antoniadis A, Minini P et al. Relation between hear rate variability and training load in middle-distance runners. Med Sci Sports Exerc 2000 ; 1 729-36. 7. Portier H, Louisy F, Laude D, Berthelot M, Guezennec CY. Intense endurance training on heart rate and blood pressure variability in runners. Med Sci Sports Exerc 2001 ; 33 (7) : 1 120-5. 8. Jouanin JC, Dussault C, Peres M, Satabin P, Pierard C, Guezennec CY. Analysis of heart rate variability after a ranger training course. Mil Med. 2004 aug ; 169 (8) : 583-7. 9. Cellarier G. Étude de la variabilité sinusale en récupération chez les nageurs de combat. Recherche de facteurs prédictifs de surentraînement. Mémoire de DEA, Université Aix-Marseille 2, 2003. étude de la variabilité sinusale lors d’immersion totale de longue durée en eau froide 10. Task Force of the European Society of Cardiology and the North American Society of Pacing and Electrophysiology. Heart rate variability. Standards of measurement, physiological interpretation, and clinical use. Circulation 1996 ; 93 : 1 043-65. 11. Dishman RK, Nakamura Y, Garcia ME, Thompson RW, Dunn AL, Blair SN. Heart rate variability, trait anxiety, and perceived stress among physically fit men and women. Int J Psychophysiology 2000 ; 37 : 121-33. 12. Perini R, Veicsteinas A. Heart rate variability and autonomic activity at rest and during exercise in various physiological conditions. Eur J Appl Physiol 2003 ; 90 (3-4) : 317-25. 13. Miwa C, Sugiyama Y, Iwase S, Mano T, Ohira Y, Grigoriev A et al. Effects of three days of dry immersion on heart rate and blood pressure variabilities during head-up tilting in humans. Environ Med 1997 ; 41 (2) : 135-7. 14. Miwa C, Sugiyama Y, Mano T, Iwase S, Matsukawa T. Spectral characteristics of heart rate and blood pressure variabilities during head-out water immersion. Environ Med 1996 ; 40 (1) : 91-4. 15. Seps B, Beckers F, Aubert AE. Head out of water immersion as simulation study : an heart rate variability study. J Gravit Physiol 2002 ; 9 (1) : 95-6. 16. Schipke JD, Pelzer M. Effect of immersion, submersion, and scuba diving on heart rate variability. Br J Sports Med 2001 ; 35 (3) : 174-80. 17. Mourot L, Gandelin E, Bouhaddi M, Cappelle S, Wolf JP, Regnard J. Réglage neurovégétatif des adaptations posturales cardiovasculaires : effets de l’immersion à neutralité thermique et en eau fraîche. Arch Mal Cœur 2004 ; 97 (4) : 413. 303 D O S S I E R VIENT DE PARAÎTRE PHYSIOLOGIE ET MÉDECINE DE LA PLONGÉE coordonnateurs B. BROUSSOLLE – J.-L. MÉLIET coordonnateur associé M. COULANGE 2e ÉDITION Par rapport à la 1re édition, les articles ont été remaniés, et pour la plupart complètement réécrits pour tenir compte de l'évolution des connaissances et des techniques de plongée, aussi bien dans le domaine sportif que professionnel, civil et militaire. L'ouvrage a été coordonné pendant quatre ans par B. BROUSSOLLE et J.-L. MÉLIET, qui se sont adjoints un comité de rédaction composé de A. BARTHÉLÉMY, E. BERGMANN, E. CANTAIS, Ph. CAVENEL, J. CORRIOL, B. GRANDJEAN, M. HUGON, J. REGNARD et J.C. ROSTAIN. M. COULANGE a été associé aux travaux pour finaliser la maquette et suivre l'édition. Qu'ils en soient tous remerciés. Ce livre tente de dresser le tableau le plus complet des connaissances dans chaque discipline, avec deux principales parties : – la physiologie et l'adaptation des principales fonctions soumises aux conditions très spécifiques du milieu aqueux hyperbare ; – la médecine, avec l'étude des accidents (barotraumatismes, accidents toxiques, accidents de décompression) et de leur traitement. Un chapitre spécial est consacré à la plongée en apnée qui connaît une vogue croissante. L'aptitude, la prévention et la réglementation concernant les différentes formes de plongées, la plongée de l'enfant et de la femme, font l'objet de chapitres particuliers. Enfin, les différentes techniques de plongée, les appareils respiratoires, les systèmes de protection, sont passés en revue. Des annexes apportent tous les renseignements utiles et un index facilite les recherches. Il s'adresse avant tout aux médecins, étudiants en médecine et personnel médical oeuvrant dans le domaine si particulier de la médecine de plongée. Mais il peut être consulté avec profit par les moniteurs, instructeurs et par les plongeurs eux-mêmes soucieux de leur sécurité. Il est complémentaire du Traité de médecine hyperbare de F. WATTEL et D. MATHIEU, paru chez le même éditeur. ISBN 978-2-7298-2983-4 – Format 17,5 x 26 cm – Pages : 880 – Prix : 75 € – ELLIPSES-Édition Marketing, 32 rue Bargue 75740 Paris cedex 15 – Tél. : 01 45 67 74 19 – www.editions-ellipses.fr 304 Dossier « Cœur et Armées » : Psysiologie INFLUENCE DE L’ACTIVITÉ PHYSIQUE SUR LA DISTENSIBILITÉ AORTIQUE P. LAURENT, P. MARENCO, O. CASTAGNA, R. CARLIOZ, J.-P. MENU RÉSUMÉ Notre étude analyse l’effet de l’activité physique sur la distensibilité aortique et la pression artérielle centrale. Trente volontaires sains (âge 34,5 +/-3 ans), 26 hommes et 4 femmes, normotendus et sans antécédent cardiovasculaire ont été inclus et répartis en deux groupes de 15 sujets selon la pratique de l’activité physique. Les paramètres physiologiques sont enregistrés au repos à distance de toute activité sportive. Les pressions centrales sont mesurées chez les sportifs, et la distensibilité aortique (évaluée par la vitesse de propagation de l’onde de pouls carotido-fémorale) est mesurée dans les deux groupes. Les deux groupes étudiés (sédentaires vs sportifs) sont appariés selon l’âge (34 +/- 3 vs 35 +/- 3 ans) et les pressions artérielles brachiales systoliques (PAS) (124 +/- 3 vs 125 +/- 3 mmHg) et diastoliques (PAD) (76 +/- 2 vs 74 +/- 3 mmHg). Il n’y a pas d’amplification de la pression pulsée aorto-brachiale chez les sportifs. La distensibilité aortique, identique statistiquement entre les deux groupes (9,1 +/- 0,3 vs 8,5 +/- 0,5 m/s, NS), est bien corrélée à l’âge (r = 0,53 ; p < 0,05) et à la PAS (r = 0,56 ; p < 0,05) chez les sujets sédentaires alors qu’elle est inversement corrélée à l’âge (r = 0,74 ; p < 0,05) et n’est pas corrélée à la PAS chez les sujets sportifs. Mots-clés : Activité physique. Amplification de la pression artérielle. Distensibilité aortique. Vitesse de propagation de l’onde de pouls. I. INTRODUCTION. Les maladies cardiovasculaires représentent un problème de santé publique en France comme dans le reste du monde. Parmi les moyens de lutte contre l’apparition de ces pathologies, figure la maîtrise des facteurs de risque cardiovasculaire ainsi que la pratique de l’activité physique (1, 2) qui permet d’atténuer l’importance de certains facteurs cardiovasculaires comme l’hypertension artérielle, la dyslipidémie, l’obésité et le diabète (3). Les recommandations du Collège américain de médecine du sport proposent de pratiquer une activité physique P. LAURENT, médecin en chef, praticien certifié. P. MARENCO, praticien hospitalier, doctorant. O. CASTAGNA, médecin des armées, adjoint IMNSSA. R. CARLIOZ, médecin chef des services, professeur agrégé du SSA. J.-P. MENU, médecin chef des services, professeur agrégé du SSA. Correspondance : P. LAURENT, Service de cardiologie, HIA Sainte Anne, BP 600, 83800 Toulon Armées. médecine et armées, 2006, 34, 4 ABSTRACT AORTIC DISTENSIBILITY ACTIVITY. AND PHYSICAL The aim of this study is to analyse the influence of physical activity on aortic compliance and central blood pressure. Thirty healthy volunteers (26 men and 4 women, age 34,5+/-3 years) without hypertension or cardiovascular diseases were included and divided in 2 groups of 15 subjects. Physiological parameters were recorded at rest 24 hours at least after a physical activity. Aortic pressure was measured in sportive patients and aortic compliance (evaluated by aortic carotido-femoral pulse wave velocity) was measured in both groups. Two groups (sedentary vs trained) were matched by age (34+/3 vs. 35+ /-3 years), systolic (124+/-3 vs. 125+/-3 mmHg), (SBP), and diastolic (76+/-2 vs. 74+/-3 mmHg), (DBP) brachial arterial pressure. No aorto-brachial pulse pressure (PP) amplification was found in the sportive subjects. There was no aortic distensibility difference (9,1+/-0,3 vs. 8,5+/-0,5 m/s: NS) between the two groups and aortic distensibility was well age (r=0,53 :p<0,05) and SBP correlated (r=0,56 :p<0,05) in the sedentary group but it was reverse age-correlated (r=0,74 :p<0,05) and not SBP correlated in the sportive group. Keywords: Aortic distensibility. Arterial pressure amplification. Physical activity. Pulse wave velocity. (Médecine et Armées, 2006, 34, 4, 305-310) quotidienne modérée d’au moins 30 minutes (4), la réduction de l’incidence des accidents coronariens étant directement proportionnelle au niveau de l’activité physique pratiquée (5). II. EFFETS DE L’EXERCICE PHYSIQUE. Il existe une relation inverse entre le niveau d’activité physique pratiquée et l’incidence des accidents cardiovasculaires, aussi bien chez les hommes que chez les femmes (6, 7). L’exercice physique fait partie des recommandations pour la prévention primaire et secondaire des pathologies cardiovasculaires (8) alors qu’aucune explication physiopathologique claire n’a été fournie concernant le rôle protecteur du sport sur le système cardiovasculaire (9, 10). L’exercice physique améliore la perfusion myocardique, mais n’a que des effets limités sur l’extension des lésions d’athérosclérose 305 D O S S I E R (11). Les effets bénéf iques de l’exercice physique régulier pourraient passer par des actions sur plusieurs facteurs dont la restauration d’une fonction endothéliale (notamment des artères coronaires) qui, lorsqu’elle est perturbée, favorise le développement de l’athérosclérose et de la thrombose (12). L’endothélium maintient un certain degré de vasodilatation (production rapide de prostacyclines et de monoxyde d’azote (NO) lors de forces de cisaillements de la paroi), et participe ainsi à la régulation de la pression artérielle. Chez l’animal (le chien), la fonction endothéliale est améliorée par l’exercice physique régulier grâce à des phénomènes d’augmentation de l’expression génique de la NO synthase (13). De nombreux travaux ont mis en évidence la pertinence de la mesure de la pression artérielle centrale comme facteur de risque cardiovasculaire (14), ceci étant très compréhensible d’un point de vue physiopathologique car la pression mesurée au niveau de l’aorte est, réellement, celle « vue par le cœur » contrairement à celle mesurée classiquement au niveau de l’artère brachiale lors d’une consultation clinique. La pression artérielle pulsée (PP) mesurée au niveau de l’artère carotide commune est quasiidentique à la PP mesurée dans la crosse aortique (15). Physiologiquement, il existe une augmentation de la pression artérielle, du cœur vers la périphérie, communément appelée « amplification ». Cette amplification est observée essentiellement pour la pression artérielle systolique (PAS) et également pour la pression artérielle pulsée (PP) qui correspond à la différence entre la PAS et la pression artérielle diastolique (PAD), cette dernière étant stable sur l’ensemble de l’arbre artériel. Or, certaines études (16-18) ont montré qu’une baisse de cette amplif ication de la PP pouvait constituer un marqueur de risque cardiovasculaire supplémentaire. La baisse d’amplification de la PP le long de l’arbre artériel peut être dû à une augmentation de la rigidité artérielle plus fréquemment observée chez les sujets âgés. Notre étude a analysé l’influence de l’activité sportive sur la pression artérielle centrale, sur l’amplification de la PP ainsi que de la distensibilité aortique. Nous avons émis l’hypothèse selon laquelle l’influence bénéfique de la pratique d’activité sportive sur les pathologies cardiovasculaires agirait par le biais d’une baisse de la pression artérielle centrale (et donc l’augmentation de l’amplification de la PP) et d’une augmentation de la distensibilité aortique. III. MÉTHODES. De manière à évaluer l’influence de l’activité sportive sur les différents paramètres hémodynamiques mesurés, nous avons comparé les résultats obtenus à partir d’un échantillon de patients sportifs à ceux issus d’une population témoin de patients sédentaires. A) POPULATION ÉTUDIÉE. Nos patients sont répartis en deux groupes : un groupe de 15 sportifs pratiquant une activité physique régulière depuis au moins une année à raison de 60 minutes par 306 séances, avec au moins 3 séances par semaine et un groupe de 15 sujets sédentaires strict. Le caractère sportif est établit sur les données aérobies de consommation maximale d’oxygène (mesure de la V02max réalisée au cours d’une épreuve d’effort) qui est supérieure à 120% de la théorique pour l’ensemble des sportifs. Aucun sujet ne présente de facteurs de risque cardiovasculaire notés lors de l’interrogatoire et de l’examen clinique. B) PARAMÈTRES HÉMODYNAMIQUES. Les paramètres hémodynamiques sont mesurés après quinze minutes de repos en décubitus dorsal, chaque volontaire étant installé dans une pièce climatisée à 21 °C. 1. Pression artérielle (PA) brachiale. Chaque PA retenue au niveau brachial est le résultat d’une moyenne de trois mesures réalisées au bras gauche avec un appareil de mesure automatique de la pression artérielle utilisant une technique de mesure par oscillométrie (Omron ® 705 CP). La fréquence cardiaque moyenne est le résultat d’une moyenne de trois mesures prises chacune sur une minute. La pression artérielle systolique (PAS), diastolique (PAD), moyenne (PAM), pulsée (PP = PAS-PAD), ainsi que la fréquence cardiaque (FC) sont monitorées toutes les cinq minutes, lors des mesures des autres paramètres hémodynamiques. 2. Pression artérielle centrale (aortique). Cette mesure est estimée lors du recueil de la pression artérielle en regard de l’artère carotide réalisée par tonométrie d’applanation (Sphygmocor®) grâce à l’aide d’une fonction de transfert mathématique validée par de nombreuses études (19, 20) permettant de calculer la pression artérielle centrale (aortique). Cette pression à été mesurée uniquement chez les sportifs car la mesure de la pression artérielle centrale a déjà été largement étudiée chez les sujets sédentaires. 3. Amplification de la pression pulsée (PP). La PP (PP =PAS-PAD) n’est pas constante, mais augmente de façon centrifuge dans les artères de gros calibre. Le calcul de l’amplification de la PP impose une mesure de celle-ci à différents niveaux de l’arbre artériel : aortique, carotidien, brachial et radial. L’amplification est définie comme la différence entre la PP distale et la PP proximale. 4. Mesure de la distensibilité aortique : calcul de la vitesse de propagation de l’onde de pouls (VOP) carotido-fémorale. La distensibilité aortique a été évaluée par la mesure de la vitesse de propagation de l’onde de pouls (VOP) carotidofémorale à l’aide du Complior®, après dix minutes de repos. Cet appareil de mesure automatisée procure une excellente reproductibilité inter et intra-observateur et a déjà été validé dans des études précédentes (21, 22). L’onde de pression générée par l’éjection ventriculaire se propage le long de l’arbre artériel en fonction des propriétés du mur p. laurent vasculaire. Deux capteurs mécanographiques cutanés sont utilisés : l’un est placé en regard de l’artère carotidienne droite, l’autre est en regard de l’artère fémorale droite. Les ondes pulsatiles enregistrées au niveau des deux sites apparaissent sur l’écran en temps réel. La tangente aux courbes de pression est automatiquement calculée, permettant de définir le pied de l’onde de pouls enregistrée. La différence de temps entre les courbes est déterminée et l’appareil fait alors le calcul de vitesse en fonction de la distance mesurée entre les deux capteurs à l’aide d’un ruban métrique appliqué sur la peau. Le résultat exprimé correspond à la moyenne d’une dizaine de mesures. Cette mesure permet d’évaluer la distensibilité aortique. 5. Étude de la fonction cardiaque. Tous les patients ont bénéficié de la réalisation d’une échocardiographie. L’évaluation des paramètres cardiaques structuraux et l’analyse de la fonction diastolique (fonction de remplissage), est toujours pratiquée par le même opérateur, sur le même appareil d’échographie doppler (General Electric Vingmed®) muni d’une sonde de 2,5 MHz et selon les recommandations de la Société française de cardiologie. Le patient est placé en décubitus latéral gauche, la main gauche derrière la tête. Les mesures doppler sont effectuées en fin d’inspiration. Les mesures sont toutes répétées trois fois à l’occasion de cycles respiratoires différents, et seule la moyenne des trois est retenue. C) ANALYSE STATISTIQUE DES DONNÉES. De manière à éviter tout biais dans l’interprétation des résultats, les deux groupes de patients (sportif et sédentaires) ont été appariés selon l’age, le poids et la pression artérielle brachiale. En raison du faible effectif de femmes (deux dans chaque groupe) aucune comparaison statistique liée au sexe n’a été réalisée. Les analyses statistiques ont été effectuées avec le logiciel Statview ® 5 (SAS intitute Inc, Cary, North Carolina, USA) utilisé avec un ordinateur PC. Les valeurs ont été exprimées en moyennes ± 1 déviation standard (DS) pour les variables quantitatives, en nombres et pourcentages pour les variables qualitatives : – les calculs de moyennes, déviation standard (DS) et erreur standard de la moyenne (ESM) sont réalisés dans les statistiques descriptives ; – les comparaisons des différentes pressions artérielles en fonction du site de mesure ont été effectuées par un test de Wilcoxon pour séries appariées ; – tests de corrélation : nous n’avons pas effectué de tests de corrélations linéaires multiples compte tenu de la taille de l’échantillon. Les volontaires des deux groupes ont été appariés sur les paramètres cliniques et hémodynamiques et comparés par un test T de Student pour séries appariées avec un seuil de significativité p < 0,05. Les corrélations recherchées entre VOP, paramètres cliniques et hémodynamiques, ont été effectuées par un test de Spearman avec également un seuil de significativité p < 0,05. influence de l’activité physique sur la distensibilité aortique IV. RÉSULTATS. A) DESCRIPTION DE LA POPULATION D’ÉTUDE. Les 30 volontaires sains normotendus ont été répartis en deux groupes appariés d’après l’âge (34 +/- 3 vs 35 +/- 3 ans : NS) et les pressions artérielles brachiales systoliques (124 +/- 3 vs 125 +/- 3 mmHg : NS) et diastoliques (76 +/2 vs 74 +/- 3 mmHg : NS). Les données sont résumées dans le tableau I. Chaque groupe est composé de 13 hommes et 2 femmes. Les sports pratiqués sont des sports d’endurance : cyclisme sur route (n = 8) et course à pieds (n = 7). Tous les volontaires de l’étude ont bénéficié d’une échocardiographie qui a confirmé la normalité de la fraction d’éjection ventriculaire gauche et l’absence de valvulopathie. B) MESURE DE LA FRÉQUENCE CARDIAQUE, DE LA PRESSION ARTÉRIELLE CENTRALE ET AMPLIFICATION DE LA PP AORTO-BRACHIALE CHEZ LE SUJET SPORTIF. La fréquence cardiaque moyenne du groupe sportif est significativement beaucoup plus basse (57 +/- 2 vs 70 +/2 batt/mn, p < 0,0001) que celle du groupe témoin. La mesure de la pression artérielle systolique aortique est de 122 +/- 4 mmHg, la PAD est mesurée à 72 +/- 2 mmHg et la pression pulsée est mesurée à 49 +/- 3 mmHg, l’amplification de la PP aorto-brachiale étant nulle. Les sportifs de notre étude, ne présentent donc aucune amplification de la PP aorto-brachiale. C) MESURE DE LA VITESSE DE PROPAGATION DE L’ONDE DE POULS. La VOP carotido-fémorale ne diffère pas entre le groupe sédentaire et le groupe sportif de l’étude (9,1 +/- 0,3 vs 8,5 +/- 0,3 m/s respectivement). La VOP est bien corrélée à l’âge (fig. 1) et à la PAS (fig. 2) chez les sujets sédentaires. Tableau I. Caractéristiques cliniques des deux groupes de volontaires. Paramètres Goupe 1 (sportifs) Groupe 2 (sédentaires) N 15 15 p Âge, années 35±3 34±3 NS Tailles, cm 173±2 173±1 NS Poids, kg 68±2 69±2 NS PAS brachiale, mmHg 125±3 124±3 NS PAD brachiale, mmHg 74±3 76±2 NS PP brachiale, mmHg 50±2 48±2 NS FC, batt/min 57±8 70±9 < 0,0001 VOP carotido-fémorale, m/s 8,5±0,5 9,1±0,3 NS Valeurs moyennes ± esm, NS (non significatif) 307 D O S S I E R Par contre, cette VOP est inversement corrélée à l’âge (fig. 1) et n’est pas du tout corrélée à la PAS (fig. 2) chez les sujets sportifs. V. DISCUSSION. Notre étude montre que la pratique de l’activité sportive n’a pas d’influence sur la mesure de la VOP moyenne carotido-fémorale au repos, notre population ayant un age moyen de 35 ans. À la différence d’autres travaux (23-25), nous n’avons pas retrouvé de différence de VOP aortique au repos entre les sportifs et les sédentaires. Cependant, les courbes de corrélation entre la VOP et l’âge ont un prof il différent entre les sédentaires et les sportifs, ces derniers semblant améliorer leur distensibilité aortique avec l’âge, allant ainsi à l’encontre du phénomène de « aging ». Il est admis que la VOP augmente avec l’âge (26), aussi bien chez l’homme que chez la femme. Les déterminants physiologiques majeurs de la VOP sont représentés par l’élasticité du vaisseau, et par la pression artérielle systolique. L’augmentation âge dépendante de la VOP est essentiellement liée à des altérations de la structure de la média des vaisseaux (augmentation du collagène, diminution de l’élastine et calcification). Elle se voit aussi en l’absence d’athérosclérose ce qui en fait un phénomène indépendant (27). L’élasticité artérielle est gouvernée par des modifications de structure de la matrice, mais aussi par la régulation endothéliale du tonus musculaire vasculaire. Étant admis que l’entraînement en endurance augmente la distensibilité artérielle et diminue la PAS, la durée et le type d’exercice ont leur importance. Au cours d’un exercice aérobie modéré, il est observé une augmentation de la distensibilité artérielle des gros vaisseaux en seulement quatre semaines chez des sujets sains normotendus (28). L’augmentation de l’élasticité artérielle associée à l’hypertension systolique isolée n’est pas réversible après huit semaines d’entraînement, alors que la pratique d’une activité physique est capable d’améliorer l’élasticité des artères de gros calibre chez les sujets jeunes normotendus en seulement quatre semaines. Figure 1. Corrélations Âge/VOP dans les groupes 1 (Sportifs) et 2 (Sédentaires), p < 0,05. 308 Figure 2. Corrélations VOP/PAS entre le groupe 1 (sportifs) et le groupe 2 (sédentaires). Lors d’un entraînement sur vélo, comme c’était le cas pour la moitié de nos volontaires, les effets sur la distensibilité artérielle sont visibles en seulement quatre semaines d’entraînement aérobie modéré (29). Les mécanismes impliqués passent par des modifications du tonus vasculaire des vasa vasorum (30). Au cours d’un exercice physique aérobie, la distensibilité artérielle augmente donc immédiatement, pour revenir à sa valeur normale dans l’heure qui suit. Ce mécanisme de vasodilatation des vasa vasorum contribue à l’augmentation de la distensibilité aortique et ainsi, à la prévention à long terme de la dégénérescence de la media et de l’épaississement intrinsèque de l’aorte. Durant et après l’exercice, il se produit une libération de métabolites vasodilatateurs au niveau du lit vasculaire. Le NO libéré par l’endothélium joue un rôle dans la réponse du flux sanguin à l’exercice (31, 32). Les effets du NO sont médiés par la relaxation isométrique des vaisseaux de telle sorte que la distensibilité puisse être modifiée indépendamment du diamètre artériel. La vasodilatation est donc un mécanisme à court terme permettant d’augmenter la distensibilité lors de l’entraînement physique. La pression artérielle varie selon le site anatomique où elle est mesurée. La PAM reste stable tout au long de l’arbre artériel car la PAS augmente progressivement mais très significativement, alors que la PAD diminue peu : La pression artérielle pulsée (PP = PAS-PAD) augmente ainsi de l’aorte vers la périphérie. Ce phénomène appelé « amplif ication de la pression pulsée » s’explique par le rôle joué par les ondes de réflexion artérielle qui viennent moduler la PP. Les ondes de réflexion qui surviennent en début de diastole permettent la bonne perfusion des artères coronaires (33). Ces ondes de réflexion sont plus tardives au niveau périphérique (car elles viennent de loin), et contribuent donc peu ou pas à l’amplification du pic de PAS et donc de la PP. Par conséquent, les pressions périphériques sousestiment l’augmentation de la PAS centrale liée à l’âge parce qu’elles ne tiennent pas compte de l’exagération du pic systolique tardif caractéristique, observée dans les artères centrales lors du vieillissement (34-36). Il est admis que le phénomène d’amplification de la PP aorto-radiale est faible chez les sujets de plus de 50 ans, en p. laurent raison d’une augmentation des ondes de réflexion précoce, alors qu’il est bien réel chez les sujets jeunes. De plus, chez les moins de 50 ans, le phénomène d’amplification diminue d’autant plus que la PAD augmente (37). Alors qu’il a été clairement mis en évidence l’existence d’une amplification centrifuge de la PP entre l’aorte et les artères des membres supérieurs et inférieurs (38, 39) dans d’autres travaux, le groupe de patients sportifs de notre étude ne présente aucune amplification de la PP aorto-brachiale. Ce résultat pourrait s’expliquer par la fréquence cardiaque basse observée dans le groupe sportif (40), l’amplification de la PP aorto-brachiale dépendant de la durée de la systole (elle augmente lorsque la durée de la systole diminue et inversement (41)). Cette augmentation de la durée de la systole est responsable d’une augmentation de la PAS centrale par addition de l’onde de pression incidente et de l’onde réfléchie au niveau de l’aorte avec pour conséquence une élévation de la PP centrale et donc une baisse du phénomène d’amplification de la PP. Bien qu’il existe des données sur le remodelage ventriculaire gauche (VG) lié au vieillissement (42, 43) ou à l’entraînement en endurance, il y a peu de données sur les interactions du sport et du vieillissement sur le ventricule gauche. Gates et collaborateurs (44) ont montré que les modifications de la structure ventriculaire gauche et de la fonction diastolique liées au vieillissement chez les sédentaires en bonne santé, s’observent également chez les sportifs malgré l’exercice physique régulier. Arbab-Zadeh et collaborateurs (45) montrent que l’entraînement prolongé en endurance préserve la compliance ventriculaire gauche du vieillissement. L’absence d’amplification de la PP (par l’augmentation de la PAS centrale dont elle résulte), risquerait donc d’augmenter la post-charge et d’aller à l’encontre des effets bénéfiques sur la distensibilité vasculaire. Le lien entre la fréquence cardiaque et l’amplification de la PP a déjà été mis en évidence lors de nos précédents travaux, à partir d’une population de patients hypertendus (46). Une PP élevée est associée à une augmentation de l’incidence des évènements cardiovasculaires (47) et une VOP élevée est un facteur prédictif indépendant d’évènements cardiovasculaires (48-50). À ces phénomènes liés au vieillissement, viennent s’ajouter des facteurs de risque cardiovasculaires additionnels comme le tabac, l’HTA, les dyslipidémies, le diabète, les facteurs génétiques. Tous ces facteurs ont une finalité commune, la genèse de l’athérosclérose. Notre étude comporte des effectifs insuffisants pour faire des corrélations multiples. Des effectifs de 30 volontaires dans chaque groupe permettraient d’avoir des données statistiquement intéressantes et d’effectuer des corrélations multiples. Les sports pratiqués sont des sports d’endurance, mais ils sont différents. Un plus grand nombre de volontaires permettra de faire des groupes homogènes et de comparer les différents sports entre eux. La moyenne de notre population est jeune et il sera intéressant de voir si ces observations persistent chez des sujets plus âgés. De plus, notre population comporte une majorité d’hommes. Étant donné que le sexe à une influence sur l’amplification de la PP (le phénomène d’amplification de la PP chez l’homme est plus important que chez la femme, surtout chez les sujets jeunes), il serait intéressant de pouvoir distinguer les hommes des femmes. Nous avons déjà montré par exemple, que la VOP est corrélée à la FC chez les hommes, mais pas chez les femmes (51). VI. CONCLUSION. La pratique d’une activité physique régulière et soutenue n’a pas d’influence sur la distensibilité aortique évaluée au repos et atténue complètement le phénomène d’amplification de la pression pulsée. Le sport en endurance rend la distensibilité aortique moins dépendante de la pression artérielle systolique et de l’âge, et pourrait donc par ce mécanisme, assurer un rôle protecteur du réseau artériel par rapport au vieillissement physiologique de la paroi artérielle aortique. L’absence d’amplif ication de la pression pulsée aorto-brachiale pose un autre problème. Elle pourrait par contre, contribuer à une augmentation de la charge myocardique et faciliter le développement d’une hypertrophie myocardique. RÉFÉRENCES BIBLIOGRAPHIQUES 1. Thompson PD, Buchner D, Pina IL et al. American Heart Association Council on Clinical Cardiology Subcommittee on Exercise, Rehabilitation, and Prevention. Circulation 2003 24 ; 107 (24) : 3 109-16. 2. Yusuf S, Hawken S, Ôunpuu S et al. Effect of potentially modifiable risk factors associated with myocardial infarction in 52 countries (the INTERHEART study) : case-control study. Lancet 2004 ; 364 : 937-52. 3. Shepard RJ, Balady GJ. Exercise as cardiovascular therapy. Circulation 1999 ; 97 : 963-72. 4. Pate RR, Pratt M, Blair SN et al. Physical activity and public health : a recommendation from the centers for Disease Control influence de l’activité physique sur la distensibilité aortique 5. 6. 7. 8. and Prevention and the American College of Sports Medicine. JAMA 1995 ; 273 : 402-7. Powell KE, Thompson PD, Caspersen CJ et al. Physical activity and the incidence of coronary heart disease. Annu Rev Public Health 1987 ; 8 : 253-87. Paffenbarger RS Jr, Hyde RT, Wing AL et al. Physical activity, all-cause mortality, and longevity of college alumni. N Engl J Med 1986 ; 314 : 605-13. Manson JE, Hu FB, Rich-Edwards JW et al. A prospective study of walking as compared with vigourous exercice in the prevention of coronary heart disease in women. N Engl J Med 1999 ; 341 : 650-8. Grundy SM, Balady GJ, Criqui MH et al. Primary prevention of 309 D O S S I E R 9. 10. 11. 12. 13. 14. 15. 16. 17. 18. 19. 20. 21. 22. 23. 24. 25. 26. 27. 28. 29. coronary heart disease : guidance from Framingham : a statement for healthcare professionals from the AHA Task Force on Risk Reduction. Circulation 1998 ; 97 : 1 876-87. Lakatta EG, Levy D. Arterial and cardiac aging : Major shareholders in cardiovascular disease enterprises. Part I : Aging arteries : A « set up » for vascular disease. Circulation 2003 ; 107 : 139-46. Vaitkevicius PV, Fleg JL, Engel JH et al. Cardiovascular risk factors, lipid and insulin : Effects of age and aerobic capacity on arterial stiffness in healthy adults. Circulation 1993; 88 (4): 1456-62. Schuler G, Hambrecht R, Schlierf G et al. Regular physical exercise and low-fat diet : effects on progression of coronary artery disease. Circulation 1992 ; 86 : 1-11. Levine GN, Keaney JF Jr, Vita JA. Cholesterol reduction in cardiovascular disease – Clinical benefits and possible mechanisms. N Engl J Med 1995 ; 332 : 512-21. Sessa WC, Pritchard K, Seyedi N et al. Chronic exercise in dogs increases coronary vascular nitric oxide production and endothelial cell nitric oxide synthase gene expression. Circ Res 1994; 74 (2): 349-53. Van Bortel LM, Balkenstein EJ, Van der Heijden-Spek J et al. Non Invasive assessment of local pulse pressure: Comparison of applanation tonometry and echo-tracking. J Hypertens 2001; 19: 1037-44. Chen CH, Ting CT, Nussbacher A et al. Validation of carotid artery tonometry as a mean of estimating augmentation index of ascending aortic pressure. Hypertension, 1996 ; 27 : 168-75. Wilkinson IB, Franklin SS, Hall IR, Tyrrell S, Cockroft JR. Pressure amplification explains why pulse pressure is unrelated to risk in young subjects. Hypertension 2001 ; 38 : 1 461-6. Mitchell GF, Moye LA, Braunwald E et al. Sphygmomanometrically determined pulse pressure is a powerful independant predictor of recurrent events after myocardial infarction in patients with impaired left ventricular function. Circulation 1997; 96: 4254-60. Franklin SS, Larson MG, Khan SA et al. Does the relation of blood pressure to coronary pressure heart disease risk change with aging ? The Framingham Heart study. Circulation 2001 ; 103 : 1 245-9. Alfredo L, Michael F, O’Rourke et al. Prospective evaluation of a method for estimating ascending aortic pressure from the radial artery pressure waveform. Hypertension 2001 ; 38 : 932-7. Chen CH, Ting CT, Nussbacher A et al. Validation of carotid artery tonometry as a means of estimating augmentation index of ascending aortic pressure. Hypertension 1996 ; 27 : 168-75. Asmar R, Benetos A, Topouchian J et al. Assessment of arterial distensibility by automatic measurement of pulse wave velocity. Validation and clinical application studies. Hypertension 1995 ; 26 : 485-90. Asmar R, Topouchian J, Pannier B et al. Pulse wave velocity as end-point in large-scale intervention trials. The Complior study. J Hypertens 2001 ; 19 : 813-8. Gauthier PJ, Chibatte F. Value of the measurement of pulse wave velocity in high level sportsmen. Practical application. Arch Mal Cœur Vaiss 1989 ; 82 : 29-33. Hayashi K, Sugawara J, Komine H et al. Effects of aerobic exercise training on the stiffness of central and peripheral arteries in middle-aged sedentary men. Jpn J Physiol, 2005 ; 55 : 235-9. Maeda S, Iemitsu M, Miyauchi T et al. Aortic stiffness and aerobic exercise : mechanistic insight from microarray analyses. Med Sci Sports Exerc 2005 ; 37 : 1 710-6. Lakatta EG, Levy D. Arterial and cardiac aging : Major shareholders in cardiovascular disease enterprises. Part I : Aging arteries : A « set up » for vascular disease. Circulation 2003 ; 107 : 139-46. Avolio A. Genetic and environnemental factors in the function and structure of the arterial wall. Hypertension 1995 ; 26 : 34-7. Ferrier KE, Waddel TK, Gatzka CD et al. Aerobic exercise training does not modify large artery compliance in isolated systolic hypertension. Hypertension 2001 ; 38 : 222-6. Kingwell BA, Berry KL, Cameron JD et al. Arterial compliance 310 30. 31. 32. 33. 34. 35. 36. 37. 38. 39. 40. 41. 42. 43. 44. 45. 46. 47. 48. 49. 50. 51. increases after moderate-intensity cycling. Am J Physiol. 1997 ; 273 : 2 186-91. Stefanidis C, Vlachopoulos C, Karayannacos H et al. Effect of vasa vasorum flow on structure and function of the aorta in experimental animals. Circulation 1995 ; 91 : 2 669-78. Endo, Imaizumi TT, Tagawa T et al. role of nitric oxide in exercise-induced vasodilatation of the forearm. Circulation 1994 ; 90 : 2 886-90. Wilson JR, Kapoor S. Contribution of endothelium-derived relaxing factor to exercise-induced vasodilatation in humans. J Appl physiol 1993 ; 75 : 2 740-4. Nichols WW, O’Rourke MF. McDonald’s blood flow in arteries ; theorical, experimental and clinical principles, 4rd edition. London : Edward Arnold : 209-22. Kelly R, Hayward C, Avolio A, O’Rourke MF. Noninvasive determination of age-related changes in the human arterial pulse. Circulation 1989 ; 80 : 1 652-9. Murgo J, Westerdorf N, Giolma J, Altobelli S. Aortic input impedance in normal man : relationship to pressure waveforms. Circulation 1980 ; 62 : 106-16. 0’Rourke MF. Arterial function in health and disease. New York : Churchill livingstone ; 1982. Wilkinson IB, Franklin SS, Hall IR et al. Pressure amplification explains why pulse pressure is unrelated to risk in young subjects. Hypertension 2001 ; 38 : 1 461-6. Karamanoglu M, O’Rourke MF, Avolio AP et al. An analysis of the relationship between central aortic and peripheral upper limb pressure waves in man. European heart Journal 1993 ; 14 : 160-7. Karamanoglu M, Gallagher DE, Avolio AP et al. Pressure wave propagation in a multy branched model of the human upper limb. Am J physiol 1995 ; 269 : H363-9. Safar ME, Laurent P. Pulse pressure and arterial stiffness in rats : comparison with humans. Am J physiol 2003 ; 285 (4) : 1 363-9. O’Rourke MF. Pressure and flow waves in systemic arteries and the anatomical design of the arterial system. J Appl physiol 1 967 ; 23 : 139-49. Jungblut PR, Osborne JA, Quigg RJ et al. Echocardiographic doppler evaluation of left ventricular diastolic filling in older, highly trained male endurance athletes. Echocardiography 2000; 17 (1): 7-16. Pelliccia A, Maron BJ, De Luca R et al. Remodeling of left ventricular hypertrophy in elite athletes after long-term deconditioning. Circulation 2002 ; 105 (8) : 944-9. Gates PE, Tanaka H, Graves J, Seals DR. Left ventricular structure and diastolic function with human ageing. Relation to habitual exercise and arterial stiffness. Eur Heart J 2003 ; 24 : 2 213-20. Arbab-Zadeh A, Dijk E, Prasad A et al. Effect of aging and physical activity on left ventricular compliance. Circulation 2004 ; 110 : 1799-805. Laurent P, Albaladejo P, Blacher J, Rudnichi A, Smulyan H, Safar ME. Heart rate and pulse pressure amplification in hypertensive subjects. Am J hypertens 2003 ; 16 : 363-70. Dart AM, Kingwell BA. Pulse pressure : a review of mechanisms and clinical relevance. J Am Coll Cardiol 2001 ; 37 : 975-84. Blacher J, Asmar R, Djane S et al. Aortic pulse wave velocity as a marker of cardiovascular risk in hypertensive patients. Hypertension 1999 ; 33 : 1111-7. Safar ME, Balcher J, Mourad JJ et al. Stiffness of carotid artery wall material and blood pressure in humans: application to antihypertensive therapy and stroke prevention. Stroke 2000; 31: 782-90. De Simone G, Roman MJ, Koren MJ et al. Stroke volume/pulse pressure ratio and cardiovascular risk in arterial hypertension. Hypertension 1999 ; 33 : 800-5. Albaladejo P, Laurent P, Pannier B et al. Influence of sex on the relation between heart rate and aortic stiffness. Journal of Hypertension 2003 ; 21 : 555-62. p. laurent Dossier « Cœur et Armées » : Rythmologie ÉVALUATION DE L’INFLUENCE DE L’ACTIVITÉ SPORTIVE SUR L’ÉLECTROCARDIOGRAMME DE JEUNES INCORPORÉS Apport d’une nouvelle méthode de traitement des données J.-R. CAIGNAULT, S. GUÉRARD, V. GRIFFET, F. BERNARD, R. BRION RÉSUMÉ La réalisation d’un électrocardiogramme est systématique lors de la visite d’aptitude dans les armées. Le diagnostic le plus fréquemment suspecté grâce aux résultats de cet examen est celui d’hypertrophie ventriculaire gauche. Ce travail rendu possible grâce à la numérisation des électrocardiogrammes enregistrés dans les centres de sélection, permet de redéfinir les normes des différents critères électriques d’hypertrophie ventriculaire gauche (indices de Sokolow, Cornell, Lewis) chez le sujet jeune. L’indice de Sokolow est significativement influencé par l’activité sportive intense (moyenne : 28 mm +/- 8 chez les sédentaires, 32 mm +/10 chez les sportifs), ce qui devrait nous conduire à tenir compte du niveau de l’entraînement sportif du sujet avant d’interpréter son électrocardiogramme. Mots-clés : Électrocardiogramme. Hypertrophie ventriculaire. Sportif. ABSTRACT ASSESSMENT OF INFLUENCE OF SPORT ACTIVITY ON ELECTROCARDIOGRAMS OF YOUNG RECRUITS. UTILITY OF A DATAPROCESSING NEW METHOD. Recording electrocardiograms of young recruits is systematic in French army. The most often suspected diagnosis is therefore left ventricular hypertrophy, in practice rarely confirmed by other means. This work, thanks to electrocardiograms numerization of young recruits, allows us to redefine normality criteria of electrical left ventricular hypertrophy of the young male (Sokolow, Cornell, Lewis index). The Sokolow criterion is significantly influenced by intense sport activity (mean 28 +/- 8 mm for the sedentaries vs 32 +/- 10 mm for the athletes). This result should bring us to evaluate electrocardiogram of a young, in the light of his sportpractice habits. Keywords : Athletes. Electrocardiogram. Myocardial hypertrophy. (Médecine et Armées, 2006, 34, 4, 311-313) I. INTRODUCTION. La réalisation systématique d’électrocardiogrammes dans les armées a pour objet d’offrir un moyen de dépistage supplémentaire des cardiopathies, en particulier de celles pouvant être à l’origine de morts subites (1). Les industriels proposent depuis plusieurs années une aide au diagnostic sous la forme d’un diagnostic automatisé. Le diagnostic le plus couramment porté chez l’adulte jeune est celui de « probable hypertrophie ventriculaire gauche », qui n’est pratiquement jamais confirmée par les méthodes d’imagerie (2). En effet, les travaux à l’origine J.-R. CAIGNAULT, médecin principal, praticien certifié. S. GUÉRARD, médecin principal, praticien certifié. V. GRIFFET, médecin principal, praticien confirmé. F. BERNARD, médecin en chef, praticien certifié. R. BRION, médecin général inspecteur, praticien certifié. Correspondance : J.-R. CAIGNAULT, Service de pathologie cardiovasculaire, HIA Desgenettes, BP 25, 69998 Lyon Armées. médecine et armées, 2006, 34, 4 de la définition des critères électriques d’hypertrophie ventriculaire gauche ont été réalisés sur des populations plus âgées, avec une sensibilité médiocre et une très bonne spécificité. En revanche, elles ne sont pas validées chez l’adulte jeune, a fortiori sain (3, 4). Le travail que nous présentons, réalisé dans le service de pathologie cardiovasculaire de l’hôpital d’instruction des armées (HIA) Desgenettes dans le cadre d’un projet de recherche du Service de santé des armées (SSA), utilise une méthode originale de numérisation des tracés, puis l’utilisation pour la détection des anomalies, non d’un algorithme prédéf ini, mais d’un tri statistique de variables (198 au total). L’anormalité se définit alors comme le tracé s’écartant le plus de la moyenne de la population étudiée (5). Cette méthode trouve tout son intérêt dans le « screening » de la population des jeunes sportifs, chez lesquels le diagnostic d’hypertrophie ventriculaire gauche (HVG) 311 D O S S I E R est le plus fréquemment porté par l’interprétation automatisée. Le diagnostic de myocardiopathie hypertrophique est alors particulièrement redouté. L’hypertrophie ventriculaire gauche retentit sur l’électrocardiogramme en augmentant les amplitudes des complexes QRS, une déviation axiale gauche, et de grandes ondes S dans les dérivations précordiales. Les anomalies de la repolarisation et d’une onde q sont importantes à prendre en considération pour le diagnostic d’hypertrophie ventriculaire gauche (1, 6). L’objectif de ce travail était plus particulièrement l’étude de la pertinence des critères classiques ECG d’hypertrophie ventriculaire gauche dans la population des jeunes sportifs, et l’établissement de nouvelles normes de positivité le cas échéant. II. CARACTÉRISTIQUES DE LA POPULATION. Notre population est constituée de 604 hommes jeunes, de sexe masculin, dont l’âge moyen est de 21,3 ans. Ils sont présumés sains grâce à l’établissement d’une fiche de recueil des données anamnéstiques, cliniques et électrocardiograhiques. On définit trois groupes selon l’activité sportive déclarée du jeune : – groupe 1 (213) : sujets sédentaires ; – groupe 2 (173) : sujets pratiquant du sport d’intensité modérée ou moyenne, de façon occasionnelle ou régulière pour des activités de loisir ; – groupe 3 (198) : sport pratiqué de façon régulière et intense voire en compétition. III. MATÉRIELS ET MÉTHODES. Au total, 710 ECG ont été enregistrés sur des jeunes incorporés du centre de sélection de Lyon, et analysés par un cardiologue ; 85 étaient inexploitables : doublons, mauvaise qualité, mauvais positionnement des électrodes ; 21 tracés pathologiques (Wolff Parkinson White, importants troubles de la repolarisation, bloc de branche) ont été écartés. La numérisation des tracés utilise un boîtier particulier (boîtier corina®, Marquette-Hellige) relié à un ordinateur utilisant le programme cardiosoft® (Marquette-Hellige). Ces outils permettent d’extraire la matrice des mesures réalisées par l’enregistreur numérique et de la traiter avec un logiciel de statistiques. Les tracés « hors normes » sont automatiquement mis en évidence ; la définition des normes devient dynamique, évoluant avec la taille de la base de données. Cette méthode permet le traitement d’une grande quantité de données et d’adapter les conclusions à la norme de la population étudiée, dans notre étude, les jeunes, sportifs ou sédentaires. Nous comparons la fréquence cardiaque, la largeur du QRS et les critères électriques d’hypertrophie ventriculaire gauche du groupe 1 et du groupe 3. Les critères ECG les plus communs, pour le diagnostic d’hypertrophie ventriculaire gauche, étudiés sont : 312 – l’indice de Sokolow : (SV1 + RV5 (ou RV6)) . Il est considéré comme positif s’il dépasse 45 mm chez l’homme avant 50 ans, 35 mm chez l’homme après 50 ans et chez la femme après 15 ans ; – l’indice de Lewis : (RD1 - RD3) + (SD3 - SD1). Il est anormal au-dessus de 17 mm, il ne peut être positif que lorsque l’axe du QRS est orienté à gauche. – l’indice de Cornell (RaVL + SV3) est considéré comme pathologique au-delà de 28 mm chez l’homme et 20 mm chez la femme. IV. RÉSULTATS. A) FRÉQUENCE CARDIAQUE. La fréquence cardiaque moyenne de repos de la population est de 71 (+/- 12)/min. Il existe une différence significative (p < 0,0001) entre la population sédentaire (75 +/- 14/min) et la population de sportifs (64 +/12/min). B) DURÉE DU QRS. La répartition des durées de QRS n’est pas gaussienne, sa valeur moyenne est de 100,8 ms. Nous n’observons pas de différence entre les sédentaires et les sportifs. C) INDICE DE SOKOLOW. La répartition des valeurs de l’indice de Sokolow répond à la loi normale. Il existe une différence significative de la valeur moyenne de l’indice de Sokolow entre les deux groupes 1 et 3 (fig. 1). Il est de 32 (+/-10) mm chez les sportifs, tandis qu’il n’est que de 28 (+/- 9) mm chez les sédentaires. Si l’on choisit comme règle pour définir la normalité la valeur en dessous de laquelle 95 % de la population étudiée se trouve, on obtient alors comme valeurs « normales » de l’indice de Sokolow : – chez le sédentaire : inférieur à 43 mm ; – chez le sujet entraîné : inférieur à 52 mm. Figure 1. Répartition des indices de Sokolow dans les populations sportives (catégorie 3, trait plein) et sédentaires (catégorie 1, pointillés). On observe une augmentation significative de l’indice de Sokolow dans la population des sportifs, par rapport à la population des sédentaires. j.-r. caignault D) INDICE DE LEWIS. La distribution de l’indice de Lewis dans nos populations répond à la loi normale. Il n’existe pas de différence significative de l’indice de Lewis entre les deux groupes de niveau d’entraînement (fig. 2). Figure 3. Répartition des indices de Cornell dans les populations de sportifs (catégorie 3, trait plein) et de sédentaires (catégories 1, pointillés). On n’observe pas d’influence de l’activité sportive sur l’indice de Cornell. Figure 2. Répartition des indices de Lewis des populations de sportifs (catégorie 3, trait plein), et de sédentaires (catégorie 1, pointillés). On n’observe aucune influence de l’activité sportive sur l’indice de Lewis. E) INDICE DE CORNELL. Il n’existe pas de différence entre les indices de Cornell des groupes 1 et 3 (fig. 3). V. CONCLUSIONS. Différents indices prédictifs d’une augmentation de la masse myocardique comme l’indice de Sokolow (SV1 + RV5 (ou RV6)), l’indice de Lewis (RD1 - RD3) + (SD3 - SD1) ou l’indice de Cornell (RaVL + SV3), fréquemment utilisés dans le dépistage d’une hypertrophie ventriculaire gauche ont été étudiés par une méthode d’électrocardiographie numérisée dans une population de 604 adultes jeunes présumés sains. En comparant les mesures réalisées sur les tracés des sédentaires par rapport à celles des sportifs, nous pouvons établir que l’indice de Sokolow moyen chez le sujet non ou peu entraîné est de 28 mm. La limite supérieure de la normale est de 43 mm. Par contre, chez le sujet entraîné, cette limite peut être portée à 52 mm. Ces données sont conformes à celles de précédents travaux (6, 7). L’indice de Lewis et l’indice de Cornell ne sont par contre pas influencés par le niveau d’entraînement sportif, ce qui les rend, à notre avis, plus intéressants pour dépister une hypertrophie ventriculaire gauche pathologique. L’association de la positivité de plusieurs critères est certainement plus pertinente Ces données sont à prendre en compte avant la réalisation d’une échocardiographie à la recherche d’une hypertrophie ventriculaire gauche. RÉFÉRENCES BIBLIOGRAPHIQUES 1. Corrado D, Culasso F, Di Paolo FM. Screening for hypertrophic cardiomyopathy in young athletes. N Engl J Med 1998 ; 339 (6) : 364-9. 2. Pelliccia A, Maron. BJ, Culasso F, Di Paolo FM, Spataro A, Biffi A et al. Clinical significance of abnormal electrocardiographic patterns in trained athletes. Circulation 2000 ; 102 (3) : 278-84. 3. Sato H, Ozaki H, Hori M. Echocardiographic examinations for mass-screening of cardiovascular abnormalities. Rinsho Byori 1995 ; 43 (11) : 1 108-12. 4. Fournier C, Pellerin D. Hypertrophies auriculaires et ventriculaires. Cardiologie. Encycl Méd Chir. Paris : Elsevier SAS, 1996 : 11-050-F-10. 5. Brion R, Gonnot G, Guérard S. Dépistage de masse des cardiomyopathies par l'électrocardiogramme de repos. Archives des maladies du cœur et des vaisseaux 2000 ; 93 (supplément au numéro 1) : 21. 6. Bjornstad H, Storstein L. Electrocardiographic findings of left, right and septal hypertrophy in athletic students and sedentary controls. Cardiology 1993 ; 82 (1) : 56-65. 7. Brion R, H F, Benjelloun A, Guige H, Warme-Janville B, Beauchene H. Étude comparative de l'électrocardiogramme numérisé chez 150 sportifs performants et 150 sédentaires de 20 ans. L'Homme à l'effort. Paris : 2e Congrès international Cœur et Sport, 1989. évaluation de l’influence de l’activité sportive sur l’électrocardiogramme de jeunes incorporés 313 D O S S I E R VIENT DE PARAÎTRE S R A S COMMENT UNE ÉPIDÉMIE GLOBALE A ÉTÉ STOPPÉE Le SRAS a causé plus de peur et de perturbations sociales que n'importe quelle autre maladie de notre époque. Bien que le nombre de personnes décédées soit peu important, il a néanmoins perturbé l'économie, paralysé le commerce et les voyages internationaux, et « dépeuplé » les rues de certaines des villes les plus prospères du monde. D'où vient cette effrayante maladie ? Comment s'est-elle propagée ? Et le monde serat-il mieux préparé si elle resurgit ? Pour la première fois, des réponses sont apportées à ces questions et d'autres dans ce remarquable ouvrage qui relate ce qui s'est réellement passé pendant ces fatidiques mois de 2003. Écrit en grande partie par les experts de la santé publique et scientifiques qui étaient au cœur de la bataille, cet ouvrage explique la manière dont le virus s'est propagé, comment il est arrivé à mettre les systèmes de santé publique à genoux et comment, à la fin, une coalition globale sans précédent l'a stoppé. Pour les spécialistes de la santé, ce livre est un guide indispensable fournissant un compte rendu détaillé des symptômes cliniques, l'éclaircissement des secrets génétiques des coronavirus du SRAS et le développement des vaccins et diagnostics. Cet ouvrage est publié par le « Regional Office for the Western Pacific » de l'OMS, regroupant plus de 95 % des 8 000 cas qui ont touché douze pays et régions, certains avec une force dévastatrice. ISBN : 92 9061 213 4 – Pages : 308 – (en langue anglaise) – WHO Press 1211 geneva 27, Switzerland – Tél. : +41 22 791 24 76 – Fax : + 41 22 791 48 57 – Email : [email protected] 314 Dossier « Cœur et Armées » : Rythmologie ANOMALIES DE LA REPOLARISATION VENTRICULAIRE ET APTITUDE MÉDICO-MILITAIRE S. KÉRÉBEL, G. CELLARIER, C. JÉGO, Y. LEDOLLEY, F. BARBOU, L. CORGIE, R. POYET, P. LAURENT, G. FOUCAULT, C. BOUCHIAT, R. CARLIOZ RÉSUMÉ La découverte d’anomalies électrocardiographiques de la repolarisation ventriculaire pose fréquemment un problème d’interprétation pour la décision d’aptitude au médecin expert. La hantise est de méconnaître l’existence d’une cardiopathie sous-jacente, potentiellement responsable d’une incapacité subite, le plus souvent du fait de la survenue d’un trouble rythmique grave. On peut schématiquement séparer les anomalies mineures, largement dominées par le syndrome de repolarisation précoce et par le « cœur du sportif », des anomalies primaires et secondaires. Ces dernières sont alors la traduction électrique d’une cardiopathie (cardiomyopathie hypertrophique, ischémique, valvulaire, dysplasie arythmogène du ventricule droit), d’une « canalopathie » (syndrome de Brugada, syndrome du QT long congénital) ou de troubles électrolytiques, métaboliques ou iatrogènes. L’anamnèse, les données de l’examen clinique et la réalisation systématique d’examens complémentaires au moindre doute doivent permettre de les différencier. Mots-clés : Anomalies de la repolarisation. Aptitude. Électrocardiogramme. I. INTRODUCTION. La découverte d’anomalies de la repolarisation ventriculaire sur un électrocardiogramme de surface est loin d’être rare et n’épargne pas la population militaire, bien que jeune le plus souvent. Dans ce contexte, il s’agit, la plupart du temps, d’anomalies mineures ou bénignes, mais le clinicien gardera à l’esprit la possibilité de cardiopathies ou d’anomalies sous-jacentes pouvant S. KÉRÉBEL, médecin principal, praticien confirmé. G. CELLARIER, médecin en chef, praticien certifié. C. JÉGO, médecin principal, praticien certifié. Y. LEDOLLEY, interne des Hôpitaux de Marseille. F. BARBOU, médecin principal, praticien confirmé. L. CORGIE, médecin lieutenant, praticien en formation. R. POYET, médecin, praticien confirmé. P. LAURENT, médecin principal, praticien certifié. G. FOUCAULT, médecin en chef, praticien certifié. C. BOUCHIAT, médecin en chef, praticien certifié. R. CARLIOZ, médecin en chef, professeur agrégé du SSA. Correspondance : S. KÉRÉBEL, Service de cardiologie, HIA Sainte-Anne, BP 600, 83800 Toulon Armées. médecine et armées, 2006, 34, 4 ABSTRACT ABNORMALITIES OF THE VENTRICULAR REPOLARISATION AND MILITARY APTITUDE. Electrocardiographic abnormalities of ventricular repolarization remain an usual problem in the decision of aptitude. The obsessive fear is to mistake the existence of an underlying cardiopathy, which can lead to sudden incapacity by severe rhythm disorders. We can schematically separate them in : minor abnormalities, largely dominated by the “early repolarization syndrome” and the "heart of the sportsman", and primary or secondary abnormalities which represent electric signs of a cardiopathy (hypertrophic cardiomyopathy, ischaemic desease, arrhythmogenic right ventricular dysplasia), a "canalopathy" (Brugada syndrome, congenital long-QT syndrome) or an electrolytic, metabolic or iatrogenic disorder. Medical history, clinical exam with the systematic realization of complementary exams in case of doubt may lead to their exact cause. Keywords : Aptitude. Electrocardiogram. Ventricular repolarization abnormalities. (Médecine et Armées, 2006, 34, 4, 315-322) mettre en jeu le pronostic vital, lié le plus souvent à l’occurrence d’un trouble rythmique grave. Nous exclurons de notre propos les troubles de repolarisation permanents ou transitoires tels que ceux rencontrés dans les syndromes coronariens aigus et les anomalies résultant d’une perturbation d’activation du ventricule comme les blocs de branche gauche (1) ou droit (bien que pouvant prêter à confusion), les préexcitations ventriculaires (2) et les syndromes post-tachycardiques (3) (effet Chatterjee). II. COURANTS IONIQUES ET REPOLARISATION. A) CONTRACTION CELLULAIRE MYOCARDIQUE. Les cellules myocardiques ont des propriétés contractiles liées à l’existence de différence de potentiels transmembranaires, en rapport avec des transferts ioniques. La sortie rapide de sodium, et plus lente de calcium, sont à 315 D O S S I E R l’origine de la dépolarisation. La repolarisation, phénomène tardif et lent, est surtout liée à une sortie de potassium (fig. 1). Toutes modifications de ces courants ioniques, d’origine primaire ou secondaire, vont être à l’origine de perturbations de la repolarisation ventriculaire (phases 1, 2 et 3 du potentiel d’action) (4). III. ANOMALIES ÉLECTROCARDIOGRAPHIQUES DE LA REPOLARISATION. A) ANOMALIES MINEURES. 1. Syndrome de repolarisation précoce. Anomalie bénigne fréquente, intéressant souvent le sujet jeune, sportif et longiligne, elle se définit comme une surélévation du point J par rapport à la ligne de base, souvent mieux vue dans les dérivations précordiales. Il existe une concavité vers le haut du segment ST (aspect en « selle de cheval »), un petit crochetage de la pente descendante de l'onde R enfin, une onde T de grande amplitude et d'aspect symétrique (fig. 2). Dans certains cas, cette élévation peut être plus marquée (pouvant atteindre 1 mm à 4 mm) et prêter à confusion avec certains aspects observés dans la péricardite aiguë ou une lésion sous-épicardique d’origine ischémique voire une forme atypique de canalopathie (cf. Syndrome de Brugada). Le contexte permet le plus souvent de redresser le diagnostic (6). Figure 1. Le potentiel d’action cellulaire : les mouvements ioniques. B) REPOLARISATION VENTRICULAIRE ET ÉLECTROCARDIOGRAMME (ECG). La repolarisation ventriculaire se déf init comme l’intervalle entre le début du point J jusqu’à la fin de l’onde T ou U. Le point J (pour « Jonction ST ») est défini comme le point où le complexe QRS rejoint le segment ST. Il correspond approximativement à la fin de la dépolarisation et au début de la repolarisation. Le segment ST est la partie du tracé comprise entre la fin du complexe QRS (point J) et le début de l'onde T. Il correspond à la phase 2, en plateau, du potentiel d'action. Le segment ST est normalement isoélectrique : son déplacement vers le haut (sus-décalage) ou vers le bas (sous-décalage) indique généralement un état pathologique. L'onde T correspond à la phase 3 terminale de la repolarisation ventriculaire. Elle a normalement un aspect asymétrique (montée plus lente que la descente) et un sommet légèrement arrondi. Son amplitude est faible (0,1 à 0,4 mvolt). Elle peut être positive, isoélectrique ou négative en V1. Elle est en règle positive de V2 à V6 chez l'adulte. Normalement, l'onde T est plus ample en V6 qu'en V1. Chez l'adulte, les dérivations périphériques montrent généralement une onde T positive, excepté en aVR où l'onde T est toujours négative. L'onde T peut être négative dans la dérivation III si la position du cœur est horizontale et dans la dérivation aVL si la position du cœur est verticale. Avec le segment ST, l'onde T est la partie du tracé qui est la plus sensible aux influences extérieures reflétant des phénomènes physiologiques ou pathologiques. Enfin, l'onde U est une déflexion positive de faible amplitude qui est parfois observée après l'onde T. Elle est presque exclusivement retrouvée dans les dérivations précordiales. Elle s’observe chez les jeunes sujets normaux, dans des cas d'hypertrophie ventriculaire, en cas de bradycardie importante ou lors de troubles ioniques (5). 316 Figure 2. Syndrome de repolarisation précoce. 2. Onde T « juvénile ». Parmi les anomalies « physiologiques », on peut retrouver chez l'enfant et l’adulte jeune (surtout chez la jeune femme) l’existence d’ondes T négatives de V1 jusqu'en V3 (fig. 3) (5). Une onde T négative en V3 chez l’homme est jusqu’à preuve du contraire pathologique et doit faire rechercher, outre une ischémie, une dysplasie arythmogène du ventricule droit (DAVD). 3. Sujet de race noire. Dans cette population, la présence d’une « pseudo » hypertrophie ventriculaire gauche et d’ondes T négatives est également possible, mais le caractère ethnique des particularités ECG reste un diagnostic d’élimination (après échocardiographie) (5). 4. « Cœur du sportif ». Avant de parler de « cœur d’athlète », il faut se rappeler que les modif ications ECG liées à un entraînement s. kérébel écarter, en particulier, une cardiomyopathie hypertrophique (CMH) (tab. I). Pellicia et al. (8) retrouvent chez 1 005 athlètes, 145 (14,4 %) ECG comportant des anomalies significatives. Ils isolent seulement 27 sujets (2,7 %) porteurs d’anomalies de la repolarisation dans les précordiales droites ou gauches, en règle associées à des cardiopathies et des « canalopathies » (cf. infra). Enfin, persiste le difficile problème du dopage chez le sportif de haut niveau qui peut être responsable de modifications structurelles myocardiques (hypertrophie et fibrose). Il faut en conclure que la présence de troubles de la repolarisation dans deux dérivations consécutives (notamment en précordiale gauche) reste exceptionnelle chez l’athlète et doit faire écarter une cardiopathie. Tableau I. Critères discriminants entre cœur de sportif et CMH. (DTDVG = diamètre télédiastolique du ventricule gauche, OG = oreillette gauche, VO2 max = consommation maximale d’oxygène) (17). Figure 3. Onde T « juvéniles » chez une femme âgée de 28 ans. (le plus souvent en endurance) ne se voient que pour des charges importantes (> 10 heures/semaine). De plus, le cœur du sportif est morphologiquement un cœur en règle normal ; l’éventuelle hypertrophie concentrique consécutive à un entraînement intensif est toujours peu importante. Il n’est cependant pas rare de retrouver sur l’ECG de ces athlètes une augmentation de l’indice de Sokolow-Lyon, parfois associé à des troubles non spécifiques de la repolarisation (ondes T négatives ou aplaties, allongement de l’intervalle QT) (fig. 4) (7). La découverte de telles anomalies doit inciter à la prudence et doit faire éliminer une cardiopathie sous-jacente. Il est indispensable de prendre un avis spécialisé, de réaliser une épreuve d’effort et une échographie cardiaque pour D O S S I E R B) ANOMALIES PRIMAIRES ET SECONDAIRES DE LA REPOLARISATION. Figure 4. Cœur de sportif « sain » (Indice de Sokolow-Lyon mesuré à 45 mm). anomalies de la repolarisation ventriculaire et aptitude médico-militaire 1. Associées à une cardiopathie. Toutes les cardiopathies peuvent être responsables de modifications de la repolarisation en rapport avec les contraintes volumiques, de surcharge et/ou les modifications structurelles. Nous détaillerons certaines d’entre elles responsables d’anomalies plus spécifiques et/ou ayant une implication particulière dans les armées. a) Cardiomyopathie hypertrophique (CMH). La cardiomyopathie hypertrophique est la maladie génétique cardiovasculaire la plus fréquente (1/500), de phénotype et pronostic variable. Ce dernier est dominé 317 par le risque de mort subite, notamment à l’effort (jusqu’à 6 % des sujets jeunes). L’électrocardiogramme peut retrouver avec une sensibilité de 60 % et une spécificité de 97 % (fig. 5, 6) : des troubles de la repolarisation (70 % des cas) aspécifiques à type de sous-décalage du segment ST, d’ondes T négatives ou plates, de territoire variable selon la localisation de l’hypertrophie ; des signes d’hypertrophie ventriculaire gauche (HVG) (tab. II) (fig. 7) dans 55 % des cas ; des ondes Q de pseudo-nécrose en territoire inférieur ou latéral dans 1/3 des cas (9, 10). Figure 7. Hypertrophie ventriculaire gauche : surcharge systolique VG. Figure 5. ECG de cardiomyopathie hypertrophique septale chez un candidat à l’engagement âgé de 18 ans. l’engagement âgé de 18 ans. Figure 6. Échocardiographie de CMH à prédominance septale chez un candidat à l’engagement âgé de 18 ans (incidence paraseptale grand axe ; VG = ventricule gauche, SIV = septum interventriculaire, OG = oreillette gauche, Ao = aorte). systématique après 40 ou 45 ans d’un ECG, d’autant plus qu’il existe des facteurs de risque cardiovasculaires et/ou des symptômes, est de pouvoir dépister une coronaropathie silencieuse ou négligée. Outre les séquelles de nécrose (ondes Q), l’ischémie chronique pourra se traduire par les troubles de repolarisation systématisés suivants : onde T négative (ischémie sous-épicardique), sous-décalage de ST (lésion sousendocardique) (fig. 8). C’est l’occasion de rappeler ici toute l’importance de posséder dans le dossier médical des ECG antérieurs de référence (10) et la nécessité de réaliser si nécessaire une épreuve d’effort (malgré sa faible sensibilité) voire une échographie de stress ou une scintigraphie cardiaque. c) Dysplasie arythmogène (DVDA). Les anomalies ECG retrouvées dans la DVDA intéressent le QRS et l'onde T (fig. 9). Il peut s'agir d'une déviation axiale, de la présence d'un bloc de branche droit complet ou incomplet, d'un élargissement localisé du QRS, d'une onde epsilon (30 %) aussi rare que spécifique, ou d'une inversion de l'onde T. Ce dernier signe est le plus classique et le plus fréquemment retrouvé (54 % des cas), bien qu’il soit considéré comme un critère mineur. Cette inversion des ondes T, b) Cardiopathies ischémiques. Théoriquement rares dans une population jeune et sélectionnée, elles peuvent néanmoins être dépistées chez les cadres plus âgés. L’intérêt de la réalisation Tableau II. Critères ECG d'hypertrophie ventriculaire gauche (HVG). Indice de Sokolow-Lyon SV1+RV5 ou RV6 > 35 mm (âge > 35ans) SV1+RV5 ou RV6 > 45 mm (âge < 35 ans) Indice de Cornell RaVL + SV5 > 28 mm (chez l'homme) RaVL + SV5 > 20 mm (chez la femme) Surcharge systolique VG Sous-décalage du point J et du segment ST convexe vers le haut, suivie d'une onde T négative ou biphasique en V5-V6, DI, aVL. Surcharge diastolique VG Aspect QS en V1, V2, jusqu'en V3 318 Figure 8. ECG de cardiopathie ischémique chronique. s. kérébel a) Syndrome de Brugada. Rare (prévalence = 5/10 000) et décrit par les frères Brugada en 1992, il s’agit d’une cardiopathie arythmogène héréditaire, à cœur échographiquement normal, dont le diagnostic repose sur l’ECG avec un aspect de surélévation du point J associé à un sus-décalage en dôme > 2 mm du segment ST sur les dérivations droites, suivi d’ondes T plates ou négatives (f ig. 11), sans cause ischémique ou métabolique, responsable de mort subite par trouble du rythme ventriculaire. L’ECG peut varier dans le temps. Il existe trois phénotypes (fig. 12) (4, 13). Figure 9. Dysplasie arythmogène du ventricule droit chez une jeune femme âgée de 22 ans (flèche : onde epsilon, aspect de « post-excitation » de faible amplitude à la partie terminale du complexe QRS traduisant le retard d’activation du ventricule droit). en l’absence de bloc de branche droit, est le plus souvent notée dans les dérivations précordiales droites, parfois en V5V6, et plus rarement en D2D3VF (11). L’authentification de cette cardiopathie dans ses formes débutantes ou focales se heurte à l’absence d’examens complémentaires fiables. d) Prolapsus valvulaire mitral. Maladie fréquente (5 % de la population), elle peut se traduire électriquement par des anomalies de la repolarisation (inversion de l’onde T dans les dérivations inférieures et latérales), ainsi que de façon inhabituelle par un allongement de l’intervalle QT (12). 2. « Canalopathies » et troubles de la repolarisation. Les canalopathies primaires se définissent comme des anomalies intrinsèques des conductances ioniques entraînant des anomalies primaires de la repolarisation ventriculaire. Elles s’opposent aux canalopathies dites secondaires, où la repolarisation est sous la dépendance de facteurs extrinsèques. Elles ont en commun l’existence de mutations génétiques et une instabilité rythmique ventriculaire, parfois létale (fig. 10) (4). Figure 10. Aspects électriques des « canalopathies » (de gauche à droite : syndrome du QT long congénital, syndrome du QT court, syndrome de Brugada). anomalies de la repolarisation ventriculaire et aptitude médico-militaire Figure 11. Syndrome de Brugada. b) Syndrome du QT long congénital (L-QT). De prévalence égale à 1/5 000, il est caractérisé par un allongement de l’intervalle QTc (normalement < 400 ms chez l'homme et 440 ms chez la femme ; un QTc > 440 ms est associé à une forte probabilité de L-QT) et l’existence de syncopes et/ou de morts subites par torsades de pointes. En France, les formes LQT1 sont les plus fréquentes (60 %), devant LQT2 (35 %), et LQT3 (5 %) (4). c) Syndrome du QT court. Récemment décrit, cette forme familiale rare de « canalopathie » se caractérise par un intervalle QT < 320 ms et des arythmies aux deux étages (14). Figure 12. Les trois types du syndrome de Brugada. 319 D O S S I E R 3. Troubles électrolytiques (5). 4. Désordres métaboliques. a) Hyperkaliémie L’augmentation d'amplitude des ondes T est la manifestation la plus précoce. Elle apparaît quand la kaliémie excède 5,5 mEq/L. Les ondes T sont amples, positives, à base étroite (aspect en « tente »), d'aspect symétriques, ou avec asymétrie inversée par rapport à celle d'une onde T normale. L'intervalle QTc reste normal ou est légèrement diminué. Le segment ST présente une image de « pseudo-lésion ». Le complexe QRS s’élargit (> 0,12 seconde) quand la kaliémie excède 6,5 mEq/L (fig. 13). a) Hypothermie profonde (< 28 °C). Elle entraîne une bradycardie sinusale et une prolongation des intervalles PR et QT. La modification la plus typique est l'onde J d’Osborn (fig. 14). Elle correspond au crochetage de la branche terminale du QRS avec sur-élévation en dôme, le point J est alors surélevé par rapport à la ligne de base (15). Figure 14. Onde J d’Osborn chez une patiente en hypothermie profonde (24 °C). Figure 13. Hyperkaliémie à 6 mmol/l. b) Hypokaliémie. L'hypokaliémie donne des troubles ECG diffus apparaissant souvent avant les signes cliniques (crampes, paresthésies…). Ces troubles s'installent dans l'ordre suivant, selon le profondeur de l'hypokaliémie : ondes T aplaties, ondes U agrandies, d'où un aspect de « pseudo» QT long (avec un espace QT normal), dépression du segment ST. Les anomalies ne sont pas aussi bien corrélées avec les taux sériques de potassium que dans l'hyperkaliémie. Les modifications caractéristiques de la repolarisation se produisent généralement lorsque le potassium sérique descend en deçà de 2,7 mEq/L. c) Hypercalcémie. L'hypercalcémie donne principalement un raccourcissement de l'intervalle QTc. Elle s’accompagne souvent d’une bradycardie sinusale. Le segment ST peut disparaître complètement, s’incorporer dans l'onde T et donner un aspect semblable à l'hyperkaliémie. L'hypocalcémie produit la manifestation ECG inverse : allongement de l'intervalle QTc aux dépens du segment ST qui devient particulièrement long tandis que la durée de l'onde T n'est pas modifiée. d) Autres électrolytes. L'hypomagnésémie et l'hypermagnésémie donnent respectivement les mêmes troubles ECG que l'hypokaliémie et l'hyperkaliémie. Enfin, notons que les anomalies de la natrémie ne provoquent pas des modifications électriques. 320 b) Hypothyroïdie. Outre la bradycardie sinusale et le micovoltage, elle peut se traduire par un discret sous-décalage du segment ST, un allongement de l’intervalle QT et par des ondes T aplaties. 5. Médicaments et repolarisation (5, 16). Nombreuses sont les spécialités pouvant modif ier la repolarisation, ce risque est majoré en cas d’association et/ou d’interactions médicamenteuses (tab. III). Le clinicien restera particulièrement vigilant aux situations « potentialisatrices » (traitement par amiodarone chez un patient sous diurétique, «canalopathie» frustre méconnue par exemple). a) Digitaliques. Ils sont responsables d’un sous-décalage du segment ST avec raccourcissement de l'intervalle QT (aspect « en cupule »), un aplatissement de l'onde T qui peut prendre un aspect biphasique ou s'inverser complètement. Tableau III. Principales causes de QT longs acquis. Médicaments Amiodarone, Bépridil, Halofantrine, Métronidazole, Pimozide, Chlorpromazine, cisapride… Troubles ioniques Hypokaliémie, hypomagnésiémie… Troubles métaboliques Hypothermie, hypothyroïdie… s. kérébel Il existe une augmentation d'amplitude de l'onde U. L'aspect le plus caractéristique de l'imprégnation digitalique est la cupule avec onde T biphasique. Cet aspect est compatible avec une concentration plasmatique correcte et indique simplement l'effet thérapeutique de la digitale. Le signe d'une possible intoxication est l'apparition d'un sous-décalage plus marqué du segment ST avec une onde T complètement négative (fig. 15). d) Amiodarone (CORDARONE®). Allonge la repolarisation (onde U fréquente). e) Autres antiarythmiques. Les médicaments de la classe IB (lidocaïne, mexilétine), de la classe IC (propafénone, flécaïnide, cibenzoline) n’ont que peu d’effets sur la repolarisation ventriculaire en l’absence d’anomalie primaire sous jacente. IV. CONSÉQUENCES SUR L’APTITUDE. Figure 15. Effets des digitaliques sur la repolarisation (A : cupule = imprégnation ; B : surdosage). b) Antipaludéens. L'halofantrine (HALFAN ® ), à un degré moindre la quinine (QUINIMAX®) provoquent un allongement de l’intervalle QT. La chloroquine (NIVAQUINE ®) a le même effet mais à doses toxiques. Un ECG est obligatoire avant le traitement pour mesurer l’intervalle QT. c) Bépridil (CORDIUM®). Il peut être responsable d’un allongement de l’intervalle QT, de torsades de pointes en cas d’hypokaliémie associée, d’aplatissement de l’onde T et d’apparition d’onde U. Concernant la décision médico-militaire, deux situations se présentent : – il s’agit à l’évidence d’anomalies mineures ou physiologiques de la repolarisation ventriculaire (syndrome de repolarisation précoce) ou « innocentes », voire attendues (cupule digitalique) : l’aptitude à l’emploi peut être maintenue, sans examen complémentaire, éventuellement sous réserve de surveillance ; – dans tous les autres cas : troubles de la repolarisation acquis (ECG modifié par rapport à la VSA précédente), anomalies inexpliquées, douteuses ou difficiles (sportif et doute sur une CMH, discret bloc de branche droite incomplet et doute sur un syndrome de Brugada…), il est indispensable d’éliminer une cardiopathie sous-jacente, potentiellement responsable de mort subite ; des examens et un avis spécialisé sont souvent nécessaires. Toutes cardiopathies et/ou « canalopathies » engendrent une inaptitude à l’engagement et des restrictions d’aptitude en visite révisionnelle voire l’inaptitude. V. CONCLUSION. L’électrocardiogramme, prolongement de l’examen clinique, peut être l’occasion de dépister des cardiopathies « silencieuses » révélées par une anomalie de la repolarisation, sous réserve d’une analyse appliquée et consciencieuse. Aucune interprétation hâtive ou facile n’est permise ; tout doute diagnostic doit être levé, et donc s’accompagner d’un avis spécialisé cardiologique. RÉFÉRENCES BIBLIOGRAPHIQUES 1. Engel T, Shah R, Depodesta L. T wave abnormalities of intermittent left bundle branch block. Ann Int Med 1978 ; 89 : 204. 2. Nicolai P, Medvedowsky JL, Delaage M. Wolf-Parkinson-White syndrome : T wave abnormalities during normal pathway conduction. J Electrocardiol 1981 ; 14 : 295. 3. Chatterjee K, Harris A, Davies G et al. Electrocardiographic changes subsequent to artificial ventricular depolarization. Brit Heart J 1969 ; 31 : 770. 4. Extramania F, Maison-Blanche P, Haggui A, Milliez P, Cauchemez B, Beaufils P et al. Anomalies primaires de la repolarisation ventriculaire. Arch Mal Cœur 2005 ; 98 (5) : 21-5. 5. Hampton JR. La pratique de l’ECG. Maloine édition ; 1993. 6. Klostsky AL, Oehm R, Cooper RA, Udaltsova N, Amstrong MH. anomalies de la repolarisation ventriculaire et aptitude médico-militaire The early repolarization normal variant electrocardiogram : correlates and consequences. Am J Med 2003 ; 115 (3) : 237-40. 7. Pellicia A, Fagard R, Bjornstad HH, Anastassakis A, Arbustini E, Assanelli D et al. Recommendations for competitive sports participation in athletes with cardiovascular disease : a consensus document from the Study Group of Sports Cardiology of the Working Group of Cardiac Rehabilitation and Exercise Physiology and the Working Group of Myocardial and Pericardial Diseases of the European Society of Cardiology. Eur Heart J 2005 ; 26 (14) : 1 422-45. 8. Pellicia A, Maron J, Culasso F, Di Paolo F, Spotro A, Biffi A et al. Clinical signifiance of abnormal electrocardiographic patterns in trained athletes. Circulation 2000 ; 102 : 278-84. 321 D O S S I E R 9. Maron BJ. Hypertrophic cardiomyopathy, a systematic review. JAMA 2002 ; 287 : 1 308-20. 10. Cellarier G, Laurent P, Bonal J, Bouchiat C, Talard P, Dussarat GV. Les ECG à risques. Médecine et Armées 1999 ; 27 (6-7) : 541-9. 11. Gemayel C, Pellicia A, Thompson PD. Arrhythmogenic right ventricular cardiomyopathy. J Am Coll Cardiol 2001 ; 38 (7) : 1 773-81. 12. Grolleau R, Leclercq FL, Carabasse D, Messner P, Fauchier JP. Les arythmies du prolapsus valvulaire mitral. Arch Mal Cœur 1994 ; 87 : 35-40. 13. Antzelevitch C, Brugada P, Borggrefe M, Brugada J, Brugada R, 14. 15. 16. 17. Corrado D et al. Brugada syndrome : report of the second consensus conference : endorsed by the Heart Rhythm Society and the European Heart Rhythm Association. Circulation 2005 ; 111 (5) : 659-70. Gaita F, Giustetto C, Bianchi F et al. Short QT Syndrome : a familial cause of sudden death. Circulation 2003 ; 108 : 965-70. Yan GX, Antzelevitch C. Cellular basis for the electrocardiographic J wave. Circulation 1996 ; 93 (2) : 372-9. www.biam2.org. Carré F, Amoretti R, Ducardonnet A, Verdier JC. Sport en competition : recommandations nord-américaines et européennes. Consensus Cardio 2006 ; 15 : 10-6. VIENT DE PARAÎTRE « MÉTÉO ET SANTÉ » Jean-CLaude COHEN, Jean-Louis SAN MARCO « Météo et santé » aborde tous les dérèglements climatiques et apporte des conseils simples de comportement face aux risques atmosphériques pour « mieux vivre » au fil des saisons en cas de canicule ou de grand froid (avec ou sans neige). On y découvre aussi un regard nouveau sur la pollution, sur les risques allergiques liés aux pollens ou sur les bienfaits et méfaits du soleil. Il est indispensable que chacun d'entre nous retrouve avec plaisir un art de vivre adapté au temps du jour (habitat, vêtements, alimentation, activités et loisirs). L'Institut national de prévention et d'éducation pour la santé (INPES), organisme créé par le ministère de la Santé, s'est associé à Météo-France pour stimuler au travers de ce guide une nouvelle culture du risque météo. Le professeur Jean-Louis SAN MARCO est à l'origine du premier système d'alerte canicule, à Marseille, suite à l'épisode caniculaire de l'été 1983. Avec cet ouvrage, la météo ouvre désormais une nouvelle voie à la médecine préventive. Les auteurs : – Jean-Claude COHEN, ingénieur à Météo-France depuis 1979, est spécialiste en biométéorologie, coordinateur « météo et santé » pour Météo France depuis 1996 et membre de la Société internationale de biométéorologie. – Jean-Louis SAN MARCO, professeur de médecine à la faculté de Marseille, a été président de l'INPS. ISBN 2-74910-408-4 – Pages 200 – Prix : 18 € – Éditions Le Cherche-Midi Collection « Santé » – Contacts presse : Météo France ; Julien GUILLAUME – Tél. : 01 45 56 71 32 – [email protected] Éditions Le Cherche-Midi ; Brigitte LIOT – Tél. : 01 6066 26 44/06 32 75 79 81 – [email protected] 322 s. kérébel Dossier « Cœur et Armées » : Rythmologie CONDUITE À TENIR DEVANT UNE EXTRASYSTOLIE VENTRICULAIRE G. QUINIOU, U. VINSONNEAU, A. BRONDEX, C. VANOYE, P. GODON RÉSUMÉ La découverte à l’électrocardiogramme d’extrasystoles ventriculaires est le plus souvent fortuite et de bon pronostic. Il s’agit d’un des motifs de consultation les plus fréquents en matière d’aptitude cardiologique. L’organicité est rare, mais potentiellement grave justifiant la réalisation d’examens complémentaires simples qui permettront dans la majorité des cas de conclure. L’apport des techniques d’imagerie récente permettra, dans les situations litigieuses, de trancher. ABSTRACT PREMATURE VENTRICULAR COMPLEX : APPROPRIATE MANAGEMENT. Premature ventricular complexes are observed commonly in clinical practice and vary from the more benign to potentially fatal. The appropriate management depends on the associated symptoms, characteristics of premature ventricular complexes and associated long term prognosis of a structural heart disease. Keyword : Premature ventricular complex. Mot-clé : Extrasystole ventriculaire. (Médecine et Armées, 2006, 34, 4, 323-327) I. INTRODUCTION. II. DÉFINITION. Circonstance très fréquente en pratique quotidienne, la découverte à l’électrocardiogramme d’extrasystoles ventriculaires (ESV) est le plus souvent fortuite. L’organicité est rare mais potentiellement grave justifiant la réalisation d’examens à la fois anatomiques et fonctionnels. Il importe alors de distinguer le bénin de ce qui ne l’est pas, la distinction à l’instant t étant parfois délicate nécessitant alors le recul du temps. L’apport des techniques d’imagerie récente permet le plus souvent sinon de trancher, du moins d’orienter. En pratique médico-militaire cardiologique, il s’agit du motif principal de demande de consultation avec l’hypertension. Depuis la fin de l’ère cosmétologique du traitement de l’extrasystolie (étude CAST en 1989 (1)), les écrits ont considérablement chuté sur le sujet. La démarche diagnostique n’en demeure pas moins une question d’actualité au sein d’une population jeune et sportive chez qui on craindra en priorité une dysplasie arythmogène du ventricule droit (DAVD) ou une myocardiopathie. Il s’agit d’une dépolarisation ventriculaire prématurée, donc élargie par rapport à un complexe de base (100 ms et le plus souvent > 120 ms), non précédée d’une activité auriculaire initiatrice, suivie d’une repolarisation de sens opposé au QRS. G. QUINIOU, médecin en chef, praticien certifié. U. VINSONNEAU, médecin principal, praticien confirmé. A. BRONDEX, médecin lieutenant, praticien en formation. C. VANOYE, médecin lieutenant, interne des hôpitaux des armées. P. GODON, médecin en chef, praticien certifié. Correspondance : G. QUINIOU, Service de cardiologie, HIA Clermont Tonnerre, BP 41, 29240 Brest Armées. médecine et armées, 2006, 34, 4 III. PRÉVALENCE. Celle-ci est particulièrement variable selon la population considérée (âge, caractère symptomatique, présence d’une cardiopathie) et surtout le mode de dépistage (clinique, ECG, holter rythmique) (2, 3). La présence d’ESV lors de l’enregistrement sur 24 heures est du domaine du physiologique (40-75 % des sujets), quelle que soit la population. Dès lors, un certain nombre de paramètres sont à prendre en considération pour séparer le banal du pathologique. IV. MÉCANISMES. A) RÉENTRÉE. Il s’agit d’un mécanisme faisant appel à une anomalie de la conduction de l’influx électrique, au sein du myocarde ventriculaire, lié à la présence d’un obstacle fonctionnel ou anatomique. 323 D O S S I E R B) FOYER AUTOMATIQUE. Lié à l’altération de l’automatisme cellulaire myocardique (spontané). C) ACTIVITÉ DÉCLENCHÉE. Elle est le résultat d’une seconde dépolarisation soit au décours, soit en fin de repolarisation et influencée par le rythme cardiaque qui la précède. V. CARACTÉRISTIQUES DE L’EXTRASYSTOLIE VENTRICULAIRE. Parfois ressentie par l’intéressé ou objectivée lors de l’examen clinique, l’extrasystolie sera le plus souvent découverte sur un électrocardiogramme systématique. A) LOCALISATION (AXE ET RETARD RENSEIGNENT SUR L’ORIGINE DU COMPLEXE PRÉMATURÉ). 1. Retard. Le retard droit (aspect de bloc de branche droit) définit une ESV naissant du ventricule gauche. Le retard gauche (aspect de bloc de branche gauche) définit le plus souvent une ESV naissant du ventricule droit (seule exception, les ESV naissant du septum ventriculaire gauche haut). 2. Axe. Il est calculé de la même manière qu’en rythme sinusal, et fait appel schématiquement à l’orientation et l’amplitude des vecteurs en D1 et aVf. Il renseigne sur le site de l’ESV. À gauche, un axe droit ou hyperdroit évoque la région apicale, un axe gauche évoquant la région septale. À droite, un axe vertical positif (au sens du cercle trigonométrique) évoque une localisation infundibulaire ou septale haute, un axe vertical négatif une localisation apexienne. B) MORPHOLOGIE. Une ESV comprise entre 100 et 120 ms est en faveur d’une origine septale haute rendant compte d’une dépolarisation peu désynchronisée des deux ventricules. Une ESV large et crochetée est par contre en faveur d’une cardiopathie. De même, la présence de plus de deux morphologies est un argument de poids en faveur d’une organicité. Mais, on prendra soin de différencier deux morphologies d’ESV, d’une fusion entre une ESV et un complexe ventriculaire normal. En effet, l’aspect de l’ESV sera alors modifié, pouvant faire croire à tort à la présence de deux morphologies distinctes. C) PRÉMATURITÉ. Elle est définie par l’intervalle de couplage reliant l’ESV au complexe précédent. Elle rend compte classiquement du potentiel de gravité de l’ESV quand elle survient dans la période réfractaire ventriculaire du complexe précédent. C’est en effet, dans cette période que le risque de déclencher un trouble du rythme soutenu (tachycardie 324 ventriculaire (TV) ou fibrillation ventriculaire (FV)) est le plus grand. On considère qu’un couplage est court quand l’index de prématurité RR/QT est < 0,85. Au-delà de 1, l’ESV est dite tardive (4). C’est ainsi que l’on explique le mécanisme du commotio cordis (traumatisme thoracique responsable de mort subite chez les joueurs de hockey sur glace, en cas d’impact à grande vitesse d’un palet sur la poitrine avant le pic de l’onde T (5)). Par analogie, le choc électrique sur l’onde T est utilisé pour déclencher une fibrillation ventriculaire lors de la mise en place d’un défibrillateur automatique implantable. D) INTERVALLE DE COUPLAGE. Le couplage de l’ESV (distance séparant l’ESV du QRS précédent) rend le plus souvent compte du mécanisme de celle-ci. Lors de la présence d’une parasystolie, on assiste fréquemment à une variation du couplage de l’ESV. En effet, il s’agit ici d’un trouble de l’automatisme d’un groupe cellulaire avec, sur l’ECG de surface, la présence d’intervalles interectopiques variables pouvant être réduite à un plus petit dénominateur commun. C’est fréquemment ici que l’on observe des phénomènes de fusion. À l’inverse, lorsqu’il existe une réentrée, le couplage est classiquement f ixe, puisque l’ESV est déclenchée par l’arrivée du rythme spontané et donc dépendante de celui-ci. Par ailleurs, le couplage de l’ESV et de l’activité auriculaire est souvent la raison de confusion. En effet, selon la séquence réalisée, on pourra suspecter une pré excitation lorsque l’espace P/ESV est court ou, à tort, prendre l’ESV pour un complexe supra ventriculaire conduit avec aberration (aspect de bloc de branche). L’étude attentive de plusieurs ESV permettra en présence de couplage variable de rectifier le diagnostic (l’espace P/ESV est alors fluctuant). Si le doute persiste, la réalisation d’un effort (dix flexions) permettra de faire varier la fréquence sinusale et les rapports à l’onde P (ici quelques millisecondes suffisent pour éliminer un diagnostic par excès de pré excitation ou d’aberration). E) NOMBRE D’ESV. La classification de Lown et Wolff (6) permet d’évaluer numériquement l’extrasystolie ventriculaire. Mais celle-ci est actuellement désuète car sans intérêt diagnostique ou pronostique, le nombre en lui-même ne représentant pas un facteur de gravité. F) CARACTÈRE RÉPÉTITIF. L’alternance régulière d’ESV et du rythme spontané, fait appel à des mécanismes électrophysiologiques sans valeur pronostique particulière. Il peut s’agir d’un bigéminisme (alternance ESV rythme sinusal) ou d’un trigéminisme (1 ESV pour 2 battements sinusaux). La présence de doublet, de triplet, voire de tachycardie ventriculaire non soutenue (plus de trois ESV de suite), est par contre plus rare dans l’extrasystolie bénigne et survient plus volontiers en présence d’anomalie organique. Mais ce caractère n’est pas univoque car il existe d’authentique tachycardie ventriculaire sur cœur sain. g. quiniou G) CONDUCTION RÉTROGRADE. Il s’agit d’une caractéristique intéressante permettant d’aff irmer l’origine ventriculaire d’un complexe (éliminant ainsi une aberration de conduction), qui signe la dépolarisation rétrograde du myocarde auriculaire via le nœud auriculo ventriculaire. Cette propriété est variable d’un individu à l’autre et fonction de la fréquence ventriculaire (phénomène de Wenckebach). Elle se caractérise par une onde P incluse dans l’onde T de l’ESV en cas de remontée complète vers l’oreillette. Cette conduction rétrograde peut aussi être responsable de phénomène de ralentissement de la conduction auriculo ventriculaire lors du battement suivant l’ESV, car le nœud auriculo ventriculaire n’a pas encore totalement récupéré. Dans ce cas, on assistera à un allongement du PR post ESV. C’est ainsi qu’on explique aussi les phénomènes de repos compensateur à l’issue d’une ESV en fonction de la dépolarisation rétrograde ou non du massif auriculaire. On assistera, soit à un repos compensateur complet (le complexe sinusal succédant à l’ESV est bloqué, il faut donc attendre l’intervalle suivant), soit à l’absence de repos compensateur (ESV interpolée), en cas de non remontée de la dépolarisation au massif auriculaire. Tous les intermédiaires sont ainsi possibles. VI. ÉTIOLOGIE. On pourra opposer les ESV sur cœur sain qui ne nécessite qu’exceptionnellement une thérapeutique (essentiellement en cas de symptomatologie) et les ESV sur cardiopathie. L’ESV sur cardiopathie ischémique est la plus fréquente, mais quelque soit la cardiopathie, il s’agit d’une manifestation satellite habituelle (myocardiopathie dilatée, myocardiopathie hypertrophique (CMH), valvulopathie, DAVD). En pratique quotidienne, une étiologie doit être recherchée. VII. RECONNAÎTRE PATHOLOGIQUE. LE BÉNIN DU A) ESV DITE BÉNIGNE DE ROSENBAUM. Observable à tout âge, et fréquemment chez l’adulte jeune (d’autant plus que l’on réalise des ECG systématiques), celle-ci présente des critères de bénignité. Elle naît de l’infundibulum pulmonaire ou du septum interventriculaire haut, de type retard gauche, axe vertical positif ne dépassant pas 120 ms à couplage variable plutôt long, le plus souvent isolée monomorphe, peu ou moyennement fréquente, non aggravée par l’effort (fig. 1). Malheureusement, d’authentiques DAVD ont cet aspect. Il est donc nécessaire de s’appuyer sur d’autres critères. B) À QUEL MOMENT UNE ESV DEVIENTELLE PRÉOCCUPANTE ? Quand elle est large et crochetée (signature d’une cardiopathie sous jacente), qu’elle est polymorphe (plus de deux morphologies traduisent l’étendue de la lésion), conduite à tenir devant une extrasystolie ventriculaire Figure 1. ESV de type retard gauche axe vertical positif. quand elle se majore à l’effort (signant sa sensibilité aux catécholamines). Le nombre à l’inverse importe peu. Quant à la répétitivité, elle est soumise à interprétation puisque les TV sur cœur sain présentent un bon pronostic (7). L’élément essentiel à prendre en considération est la présence d’une cardiopathie sous jacente, qui conditionne le pronostic. De rares publications tempèrent cette vision manichéenne. Chez seize patients présentant des FV et/ou des TV polymorphes responsables pour certains de morts subites récupérées (cinq d’entre eux), l’extrasystolie unitaire ne diffère en rien de la classique ESV de Rosenbaum (8, 9). L’équipe de Haïssaguerre a publié en f in d’année dernière une série de 36 patients présentant des FV initiées par une extrasystolie caractéristique (10). Chez huit patients étaient objectivées des ESV de type retard gauche, axe inférieur ne les différenciant en rien d’ESV bénignes. La différence clinique essentielle dans ces deux publications tient au caractère symptomatique de ces patients. Ces éléments récents doivent donc rendre prudent toute conclusion concernant une extrasystolie ventriculaire ne présentant pas tous les critères de bénignité classiques, et en particulier une histoire clinique de syncope. VIII. EN PRATIQUE. Deux cas de figures : – la cardiopathie est connue et la prise en charge est spécifique et déborde du cadre de cet article ; – l’ESV est découverte chez un sujet asymptomatique ou pauci symptomatique. L’interrogatoire doit être drastique à la recherche d’antécédents familiaux de cardiopathie ou de mort subite, d’antécédent personnel parfois oublié ou minimisé (malaise à l’effort ou lors d’un stress), et bien sur de signes cliniques tels qu’une dyspnée, des épisodes de douleur thoracique ou des sensations de tachycardie. La recherche de prise de médicaments, mais aussi de toxiques potentialisant ou révélateurs (alcool, café, cannabis, cocaïne) ou de produits dopants (surtout chez l’adulte jeune sportif), doit faire partie intégrante de l’interrogatoire. L’examen est, par contre, 325 D O S S I E R rarement contributif hormis la recherche d’un souffle organique (myocardiopathie hypertrophique, prolapsus valvulaire mitral). En fait, l’ECG sera déjà révélateur et devra être lu avec attention, à la recherche d’un QT long (QT corrigé > 440 ms, calculé par la formule de Bazett : QT corrigé = QT mesuré en milliseconde/racine carrée de l’espace RR mesuré en seconde). On sera très attentif à l’aspect du QRS en précordiale droite à la recherche d’un élargissement supérieur à 110 ms, la présence d’une onde epsilon ainsi qu’à des troubles de la repolarisation évocateurs d’une DAVD. La présence de séquelle ischémique (onde q) ou de troubles de la repolarisation évoquera une coronaropathie passée inaperçue. Une HVG électrique, un aspect pseudo infarctoïde feront rechercher une CMH. En fait, le plus souvent, celui-ci est subnormal et c’est la réalisation d’examens de première intention fonctionnels et anatomiques qui permettront de trancher. A) ÉCHOCARDIOGRAPHIE. L’échocardiographie objectivera une altération de la fonction ventriculaire gauche (FEVG) segmentaire (en cas de coronaropathie) ou globale (myocardiopathie dilatée), une valvulopathie (prolapsus valvulaire mitral). Une dilatation des cavités droites avec altération de la fonction contractile du ventricule droit, présence de trabéculations importantes, aspect d’empilement d’assiettes seront recherchés en cas de suspicion de DAVD. Une HVG avec un septum inter ventriculaire supérieur à 13 mm sera suspect de CMH (dont le diagnostic différentiel avec le cœur du sportif est parfois délicat). B) HOLTER RYTHMIQUE DES 24 HEURES. Le holter rythmique des 24 heures va permettre de caractériser, plus finement que l’ECG, cette ESV. C) RECHERCHE DE POTENTIELS TARDIFS. La recherche de potentiels tardifs (PTV) dont la valeur prédictive a surtout été objectivée dans la coronaropathie et la DAVD (positifs si trois critères positifs). D) ÉPREUVE D’EFFORT. L’épreuve d’effort qui, hormis l’aggravation possible de l’extrasystolie, s’intéressera au niveau d’effort réalisé et à l’apparition de signes d’ischémie. À l’issue de ces examens : soit l’extrasystolie est, de toute évidence, bénigne ou il existe des atypies : symptomatologie clinique, anomalies échocardiographiques, présence de phénomènes répétitifs au repos ou à l’effort, bimorphisme voire polymorphisme, PTV positifs. Dès lors, il est nécessaire de passer à des examens de seconde intention dont la plupart auront pour but d’éliminer le diagnostic de DAVD. 326 Pour certains (l’école bordelaise), le test à l’Isoprotérénol (1 ampoule dans 100 cc) représente un test d’une grande valeur dans la recherche d’une DAVD. L’IRM représente actuellement la méthode non irradiante la plus répandue. Elle peut apporter des renseignements sur la structure, l'épaisseur et la taille du VD ainsi que sa cinétique segmentaire et globale. Un hypersignal détecté dans la paroi myocardique est très spécifique de l'infiltrat adipeux. Une atteinte associée du VG peut être également recherchée. Pour Grimm (11), l’IRM présente une très bonne valeur prédictive négative permettant d’éliminer la présence d’une DAVD sur un examen normal. L'angioscintigraphie isotopique avec analyse de phase de Fourrier permet d'étudier l'hétérogénicité de la contraction ventriculaire droite et de visualiser des zones d'hypokinésie, d'akinésie ou de dyskinésie. Les fractions d'éjection droite et gauche, peuvent être évaluées d'une façon fiable. Le pronostic étant d’autant plus mauvais qu’il existe des anomalies ventriculaires gauches associées (12). L'angiographie ventriculaire droite conventionnelle est classiquement considérée comme l'examen de référence dans la DAVD. Elle doit être réalisée d'une façon sélective en deux incidences différentes. Dans les formes diffuses, les anomalies angiographiques consistent en une dilatation cavitaire droite avec dysfonction systolique et baisse de la fraction d'éjection. Ces signes ne sont malheureusement pas retrouvés dans les formes localisées et cette technique reste très opérateur dépendant. La biopsie endomyocardique a été utilisée dans certaines études pour dépister une DAVD dans les arythmies ventriculaires sur cœur apparemment sain, ou pour conf irmer le diagnostic déjà suspecté par les autres examens paracliniques. Néanmoins, cette méthode présente plusieurs limites. Les faux négatifs sont possibles dans les formes localisées de la maladie. D'autre part, un infiltrat adipeux de la paroi ventriculaire droite n'est pas toujours synonyme de DAVD (richesse particulière du VD normal en adipocytes). Enfin, la biopsie endomyocardique n'est pas sans risque dans cette pathologie où la paroi du VD est particulièrement amincie et fragilisée. Une exploration électrophysiologique sera parfois réalisée dans les formes avec ESV complexes et/ou TV, soit dans un but pré-thérapeutique d’ablation (TV soutenue), soit afin de s’assurer de l’absence de TV électro-déclenchables (en présence de TV non soutenue). À l’issue de ce panel d’examen, il est bien rare que la situation ne soit pas claire. En l’absence de certitude diagnostique le recul du temps permettra de trancher. En effet, il est de bonne pratique de réévaluer la situation à un ou deux ans du bilan initial en l’absence de stricte normalité des examens. Chez un sportif, il peut être encore plus difficile de s’assurer de la stricte bénignité des ESV, et c’est parfois l’arrêt de l’activité couplée à un bilan exhaustif qui permettront d’assurer le diagnostic de cœur de sportif (13). Dans tous les cas, il conviendra de rappeler aux patients asymptomatiques la nécessité de g. quiniou consulter en cas de signes d’appels, que sont des palpitations, un malaise ou une inadaptation à l’effort. IX. CONCLUSION. Bien qu’il s’agisse dans l’immense majorité d’une anomalie plus que d’une pathologie, la présence d’une extrasystolie ventriculaire nécessite quelques examens simples permettant d’écarter une organicité sous jacente. La présence de signes cliniques rendra prudent le clinicien, d’autant plus que depuis peu, certaines formes d’extrasystoles considérées comme bénignes ont pu être rendues responsables de mort subite. RÉFÉRENCES BIBLIOGRAPHIQUES 1. The Cardiac Arrhythmias Suppression Trial (CAST) Investigators. Preliminary report: Effect of encainide and flecainide on mortality in a randomized trial of arrhythmia suppression after myocardial infarction. The CAST Investigators. N Engl J Med 1989; 321: 406-12. 2. Cannom DS, Prystowsky EN. Management of ventricular arrhythmias. JAMA 1999 ; 281 : 172-9. 3. Kostis JB, McCrone K, Moreyra AE, Gotzoyannis S, Aglitz NM, Natarajan N et al. Premature ventricular complexes in the absence of identifiable heart disease. Circulation 1981 ; 63 : 1 351-6. 4. Leenhardt A, Extramiana F, Milliez P, Meddane M, Haggui A et Cauchemez B. Extrasystoles ventriculaires. Arch Mal Cœur 2004 ; 97 : 7-12. 5. Maron BJ, Estes NA 3rd and Link MS. Task Force 11 : commotio cordis. J Am Coll Cardiol 2005 ; 45 : 1 371-3. 6. Lown B, Wolf M. Approaches to sudden death from coronary heart disease. Circulation 1971 ; 44 : 130-42. 7. Gaita F, Giustetto C, Di Donna P, Richiardi E, Libero L, Brusin MC et al. Long-term follow-up of right ventricular monomorphic extrasystoles. J Am Coll Cardiol 2001 ; 38 : 364-70. 8. Noda T, Shimizu W, Taguchi A, Aiba T, Satomi K, Suyama K et al. Malignant entity of idiopathic ventricular tachycardia initiated conduite à tenir devant une extrasystolie ventriculaire 9. 10. 11. 12. 13. by premature extrasystoles originating from the right ventricular outflow tract. J Am Coll Cardiol 2005 ; 46 : 1 288-94. Viskin S, Antzelevitch C. The cardiologists’ worst nightmare. J Am Coll Cardiol 2005 ; 46 : 1 295-7. -Sacher F, Victor J, Hocini M, Maury P, Jais P, Boveda S et al. Caractéristiques morphologiques des extrasystoles ventriculaires initiatrices des fibrillations ventriculaires. Arch Mal Cœur 2005 ; 98 : 867-73. Grimm W, List-Hellwig E, Hoffmann J, Menz V, Hahn-Rinn R, Klose KJ et al. Magnetic resonance imaging and signal-averaged electrocardiography in patients with repetitive monomorphic ventricular tachycardia and otherwise normal electrocardiogram. Pacing Clin Electrophysiol 1997 ; 20 : 1 826-33. Le Guludec D, Gauthier H, Porcher R, Frank R, Daou D, Benelhadj S et al. Prognostic value of radionuclide angiography in patients with right ventricular arrhythmias. Circulation 2001 ; 103 : 1972-6. Biffi A, Pelliccia A, Verdile L, Fernando F, Spataro A, Caselli S et al. Long term clinical significance of frequent and complex ventricular tachyarrhythmias in trained athletes. J Am Coll Cardiol 2002 ; 40 : 446-52 327 D O S S I E R VIENT DE PARAÎTRE CODE SANITAIRE POUR LES ANIMAUX TERRESTRES L'objectif du Code sanitaire pour les animaux terrestres est d'assurer la sécurité sanitaire des échanges internationaux d'animaux terrestres et de leurs produits dérivés, grâce à la définition détaillée des mesures sanitaires que les Autorités vétérinaires des pays importateur et exportateur doivent appliquer afin d'éviter le transfert d'agents pathogènes pour l'animal ou pour l'homme, tout en prévenant la création de barrières sanitaires injustifiées. Les mesures sanitaires recommandées dans le Code terrestre (présentées sous forme de normes, lignes directrices et recommandations) sont formellement adoptées par le Comité international de l'OIE qui rassemble tous les Délégués des Pays Membres de l'OIE. La 14e édition intègre les amendements apportés au Code terrestre lors de la 73e Session générale tenue en mai 2005. Ces amendements ont été insérés dans les chapitres et annexes portant sur les sujets suivants : définitions générales, notification et informations épidémiologiques, zonage et compartimentation, critères d'inscription de maladies sur la liste de l'OIE, fièvre aphteuse, fièvre catarrhale du mouton, fièvre de la Vallée du Rift, tuberculose bovine, encéphalopathie spongiforme bovine, peste porcine classique et influenza aviaire. Y ont été également introduites de nouvelles annexes sur la semence de bovins et de petits ruminants, la surveillance générale de la santé animale et les systèmes de surveillance de l'encéphalopathie spongiforme bovine, la fièvre aphteuse, la peste porcine classique et l'influenza aviaire. La présente édition intègre quatre nouvelles lignes directrices sur le bien être animal (transport par voies maritime et terrestre, abattage à des fins prophylactiques et abattage à des fins de consommation humaine), ainsi que des annexes révisées sur l'usage des antimicrobiens. L'élaboration des normes, lignes directrices et recommandations de l'OIE est le fruit d'un travail continu entrepris par l'une des commissions spécialisées de l'OIE, la Commission des normes sanitaires pour les animaux terrestres. Cette Commission fait appel aux meilleurs spécialistes mondiaux pour préparer de nouveaux projets d'articles du Code terrestre ou bien procéder à la révision des articles déjà existants en fonction des progrès de la science vétérinaire. Le fait que les mesures figurant dans le Code terrestre résultent d'un large consensus des Autorités vétérinaires des Pays Membres de l'OIE et que cet ouvrage ait été retenu par l'Organisation mondiale du commerce dans le cadre de l'Accord sur l'application des mesures sanitaires et phytosanitaires pour être la norme internationale en matière de santé animale et de zoonoses, lui confèrent une valeur double. Dans une première partie sont présentés les définitions des termes ou expressions utilisés, la liste des maladies animales visées par l'OIE, les modalités de déclaration de ces maladies au niveau international, les règles d'éthique en matière d'échanges internationaux et de certification, les principes de l'analyse de risque à l'importation, ainsi que la façon dont doivent s'organiser les procédures d'importation et d'exportation. Une seconde partie s'attache à examiner, pour chaque maladie animale considérée par l'OIE comme importante dans les échanges internationaux, les conditions sanitaires auxquelles un pays exportateur doit répondre, en fonction des maladies sévissant sur son territoire, afin d'assurer la sécurité sanitaire des échanges internationaux d'animaux terrestres vivants, de semence, d'embryons, de produits carnés ou laitiers et d'autres produits d'origine animale. Des annexes rappellent les épreuves diagnostiques à mettre en œuvre avant l'exportation (faisant ainsi le lien avec le Manual of Diagnostic Tests and Vaccines for Terrestrial Animais de l'OIE), et décrivent les modalités du contrôle sanitaire et de l'hygiène spécialement dans le domaine de la reproduction, les procédés d'inactivation des agents pathogènes, les conditions de protection des animaux dans les transports internationaux, les principes généraux applicables aux systèmes de surveillance pour la reconnaissance du statut indemne d'une maladie ou d'une infection donnée ainsi que les lignes directrices pour le bien-être animal et pour l'antibiorésistance. En fin d'ouvrage sont présentés les modèles de certificats vétérinaires internationaux approuvés par l'OIE. Le Code terrestre est un document de référence indispensable à tous les opérateurs concernés par les échanges internationaux d'animaux terrestres et de leurs produits dérivés. Compte tenu de la nécessité d'y intégrer les dernières informations scientifiques disponibles, il fait l'objet d'éditions annuelles. ISBN 92-9044-636-6 - Pages : 682 - Format : 21 x 29,7 cm - Prix : 55 euros - OIE, 12 rue de Prony, 75017 Paris - [email protected] 328 Dossier « Cœur et Armées » : Rythmologie INDICATIONS ACTUELLES DES TECHNIQUES ABLATIVES ET INCIDENCE SUR L’APTITUDE EN MILIEU MILITAIRE PH. HÉNO, L. BRAEM, D. MIOULET, J.-M. PÉLONI, É. BASTARD, PH. PAULE, P. VARLET¸ L. FOURCADE RÉSUMÉ Les techniques ablatives sont proposées depuis un peu plus de quinze ans dans le traitement radical des arythmies. La technique la plus employée actuellement est l’ablation par radiofréquence. Cet article a pour objectif de préciser les indications, les résultats, les complications et les implications médicomilitaires des techniques ablatives en centrant notre propos sur l’ablation des arythmies rencontrées chez le sujet jeune. Les problèmes pratiques soulevés par l’aptitude en milieu militaire après ablation sont également envisagés. Mots-clés : Ablation par radiofréquence. Aptitude. Sujet jeune. ABSTRACT RADIOFREQUENCY CATHETER ABLATION OF CARDIAC ARRHYTHMIA : INDICATIONS AND APTITUDE IMPLICATIONS IN MILITARY MEDICINE. Ablation techniques are proposed since 15 years for arrhythmia treatment. The most used technique is actually radiofrequency catheter ablation. The aim of this article is to precise indications, results, and complications of this technique. We also detail medicomilitary implications of radiofrequency ablation and focus on arrhythmias of the young adult. The particular problems of military aptitude after radiofrequency catheter ablation are also discussed. Keywords : Military aptitude. Radiofrequency catheter ablation. Young adult. (Médecine et Armées, 2006, 34, 4, 329-333) I. INTRODUCTION. Les techniques ablatives sont proposées depuis un peu plus de quinze ans dans le traitement radical des arythmies. La technique la plus employée actuellement est l’ablation par radiofréquence (RF). Depuis peu, une nouvelle technique, la cryo-ablation est également disponible et est venue compléter l’arsenal thérapeutique. Ces méthodes ont récemment bénéf icié de l’essor des systèmes de cartographie cardiaque électroanatomique qui ont permis de mieux comprendre le mécanisme de certaines arythmies et de les rendre accessibles à l‘ablation. C’est le cas notamment de la fibrillation atriale (fig. 1) et des arythmies post chirurgie cardiaque, qui peuvent désormais bénéf icier d’un traitement radical par ablation. L’objectif de cet article est de préciser les indications, les résultats, les complications et Ph. HÉNO, médecin en chef, praticien certifié. L. BRAEM, médecin principal, praticien confirmé. D. MIOULET, médecin des armées, praticien confirmé. J.-M. PELONI, médecin principal, praticien confirmé. É. BASTARD, interne des hôpitaux. Ph. PAULE, médecin principal, praticien certifié. P. VARLET¸ médecin en chef, praticien certifié. L. FOURCADE médecin en chef, praticien certifié agrégé. Correspondance : P. HÉNO, Service de pathologie cardio-vasculaire, HIA Laveran, BP 50, 13998 Marseille Armées. médecine et armées, 2006, 34, 4 les implications médico-militaires des techniques ablatives, en centrant notre propos sur l’ablation des arythmies rencontrées chez le sujet jeune et les problèmes pratiques soulevés par l’aptitude en milieu militaire après ablation. Figure 1. Ablation de fibrillation atriale : isolation des veines pulmonaires avec système de cartographie électroanatomique. 329 D O S S I E R II. TECHNIQUE (1, 2). Le geste d’ablation est le plus souvent réalisé dans le même temps que l’exploration électrophysiologique (EEP). Plusieurs cathéters d’électrophysiologie diagnostique ainsi que la sonde d’ablation sont introduits sous anesthésie locale par voie veineuse fémorale, sousclavière ou dans de rares cas par voie rétrograde artérielle fémorale. Les sondes sont ensuite positionnées au niveau de l’endocarde sous contrôle radioscopique (fig. 2). L’exploration électrophysiologique permet de préciser le mécanisme de l’arythmie : existence d’un foyer, d’un circuit de réentrée, d’une dualité nodale ou d’une voie accessoire. L’utilisation de systèmes de cartographie plus sophistiqués est parfois nécessaire, en particulier pour les tachycardies atriales et la fibrillation auriculaire (FA). L’ablation endocavitaire assure le traitement radical curatif en transformant le substrat myocardique arythmogène en une cicatrice fibreuse électriquement neutre. La technique la plus utilisée est actuellement l’ablation par courant de radiofréquence, qui permet de réaliser un échauffement localisé à l’interface électrode-endocarde. Cet échauffement entraîne un effet lésionnel irréversible, lorsque la température en bout de sonde est supérieure à 50 °C. L’utilisation dans certains cas de cathéters « irrigués » permet de délivrer des puissances supérieures et de créer des lésions plus profondes. Ces cathéters limiteraient également la formation de caillots intracavitaires au contact de la sonde. Contrairement au courant de radiofréquence qui induit un échauffement tissulaire responsable de la lésion, il est possible de provoquer des lésions tissulaires par le froid, appelées cryothérapie (3). Cette technique apparue en 1991 est encore actuellement peu développée en France. Elle possède toutefois plusieurs avantages qui pourraient voir son utilisation augmenter en particulier chez le sujet jeune. Cette technique permet notamment grâce au « cryomapping » de créer des lésions tissulaires transitoires et réversibles, qui permettent de déterminer plus précisément le site proximal d’ablation, d’éviter des lésions inutiles en diminuant le nombre d’applications d’énergie et surtout de diminuer le taux de complications à type de bloc auriculoventriculaire (BAV). Cette nouvelle technique semble particulièrement intéressante dans l’ablation des tachycardies jonctionnelles par réentrée intranodale et des voies accessoires proches des voies normales de conduction (voies antéroseptales et « midseptales »), où la proximité des voies de conduction normales du cœur rend le risque de BAV iatrogène non négligeable. L’autre intérêt réside dans le fait que pendant la délivrance du froid, l’électrode se colle au tissu, la rendant parfaitement stable. III. INDICATIONS. L’ablation peut désormais être proposée dans la plupart des arythmies. Nous limiterons notre propos aux arythmies rencontrées chez le sujet jeune indemne de cardiopathie, qui correspondent aux arythmies rencontrées le plus souvent en milieu militaire. Les tachycardies jonctionnelles sont les tachycardies les plus fréquentes chez le sujet jeune. Le groupe des tachycardies jonctionnelles comprend les tachycardies par réentrée intranodale et les tachycardies utilisant une voie accessoire. A) TACHYCARDIES JONCTIONNELLES PAR RENTRÉE INTRANODALE. Les tachycardies jonctionnelles par réentrée intranodale (1, 2, 4) constituent la cause la plus fréquente de tachycardie supraventriculaire régulière (maladie de Bouveret). Ces patients présentent une dualité de la conduction nodale, et la technique consiste à aller pratiquer l’ablation de la voie lente nodale située en région postéroseptale. La complication majeure de cette procédure est représentée par le risque de survenue de BAV complet dans 1 % à 5 % des cas. Le taux de succès immédiat est de 97 %. Le taux de récidive à long terme est de 5 %. Ce type d’ablation est proposé chez les patients symptomatiques présentant des crises de tachycardie en rapport avec une réentrée intranodale, résistantes au traitement médical ou avec mauvaise tolérance du traitement. Compte tenu du risque de BAV, la radiofréquence nous semble devoir être déconseillée chez le sujet jeune, et la cryothérapie à privilégier pour l’avenir dans ce contexte (3). B) FAISCEAUX DE KENT. Figure 2. Radioscopie : incidence oblique antérieure gauche. Position des sondes endocavitaires lors de l’ablation de flutter atrial commun. 330 Les faisceaux de Kent correspondent à l’existence de connexions électriques anormales entre l’oreillette et les ventricules. L’électrocardiogramme (ECG) montre un aspect de pré-excitation ventriculaire avec PR court (inférieur à 120 ms) et empâtement du pied du QRS (onde delta). Le syndrome de Wolff-Parkinson-White est déf ini par l’association de symptômes à type de ph. heno palpitations à cet aspect électrocardiographique. Les faisceaux de Kent sont composés de fibres musculaires à conduction rapide et peuvent « court-circuiter » les voies de conductions normales. Il est possible de rencontrer différentes arythmies chez les patients porteurs d’un faisceau de Kent. Il peut s’agir de tachycardies par rythme réciproque empruntant la voie accessoire dans les sens antérograde ou rétrograde. Il peut survenir également des arythmies atriales telle que la FA avec conduction rapide aux ventricules. Il existe alors un risque de mort subite par fibrillation ventriculaire lors des passages en FA, en particulier lorsque la période réfractaire de la voie accessoire est courte (< 250 ms) et la réponse ventriculaire très rapide (> 200/mn). L’ablation des faisceaux de Kent est indiquée chez les patients porteurs d’une voie accessoire présentant une dangerosité potentielle (période réfractaire courte, profession à risque, pratique du sport en compétition), en particulier lorsque existent des antécédents d’arythmie supraventriculaire clinique ou déclenchée au cours de l’EEP (2, 4-6). C) TACHYCARDIE PERMANENTE JONCTIONNELLE RÉCIPROQUE. La tachycardie permanente jonctionnelle réciproque dite tachycardie de Coumel (7). Il s’agit d’une tachycardie empruntant une voie accessoire à conduction rétrograde lente et décrémentielle. La topographie du faisceau est généralement postéroseptale droite. L’ECG inscrit une tachycardie à QRS fins, avec onde P’ rétrograde, négative en DII, DIII, VF avec un espace RP’ supérieur à P’R. La tolérance de ces tachycardies est variable. Les formes permanentes et rapides peuvent être responsables chez l’adulte jeune de cardiomyopathies rythmiques avec altération de la fraction d’éjection ventriculaire gauche (FEVG). L’ablation par RF représente le traitement de première intention de ces tachycardies, et s’accompagne d’une amélioration de la fraction d’éjection ventriculaire gauche. D) TACHYCARDIE EMRUNTANT UNE FIBRE DE MAHAIM (7). Les fibres de Mahaim sont rares et correspondent à des voies accessoires à type de connexions fasciculo-ventriculaires, sans expression clinique, ou nodo-ventriculaires responsables de tachycardie. En tachycardie, l’ECG inscrit un QRS large à type de bloc de branche gauche avec un axe gauche. L’ablation par radiofréquence est indiquée dans les formes récidivantes et mal tolérées de tachycardie. circuit de réentrée (fig. 3). L’ablation par radiofréquence représente désormais le traitement de première intention en raison de taux de succès dépassant 96 % au terme de deux années de suivi et d’un taux de complications très faible. Le taux de récidive à long terme se situe entre 5 % et 9 % selon les séries. Dans notre expérience du flutter du sujet jeune, la procédure s’est toujours soldée par un succès. Nous ne détaillerons pas l’ablation des autres flutters (flutter atypiques, flutter cicatriciel, cardiopathies congénitales…). F) TACHYCARDIES ATRIALES. Les tachycardies atriales (1, 2), en particulier focales par automatisme anormal, peuvent survenir en l’absence de toute cardiopathie et sont rencontrées de manière sélective chez l’enfant, l’adolescent et l’adulte jeune. Elles sont très résistantes au traitement médical et l’ablation par radiofréquence est une bonne indication. Les études les plus récentes revendiquent un taux de succès de 92 % à 100 % avec un taux de récidive variant de 4 % à 10 %. G) FIBRILLATION AURICULAIRE. La fibrillation auriculaire (FA) est une arythmie qui peut être rencontrée chez le sujet jeune, en particulier dans ses formes dîtes vagales (période nocturne ou post prandiale) et cathécolergiques (lors d’un stress ou à l’effort). Cette technique d’ablation nécessite un abord de l’oreillette gauche par cathétérisme transseptal. Le risque de perforation cardiaque est très faible dans les centres entraînés (0,002 %). La technique d’ablation consiste à déconnecter les quatre veines pulmonaires où sont situées les foyers arythmogènes initiateurs de la tachycardie. Cette déconnexion est éventuellement complétée par la réalisation de lésions linéaires auriculaires gauches. Les complications sont représentées par la sténose des veines pulmonaires (1,9 %), la survenue d’accidents thromboemboliques systémiques (1,1 %) et les lésions de l’œsophage. Il existe encore un taux important de récidives (30 %) dans les premiers mois nécessitant au moins une nouvelle procédure. Malgré sa relative complexité, l’ablation de la fibrillation atriale semble E) FLUTTER ATRIAL COMMUN. Le flutter atrial commun (1, 2, 8) est une arythmie par macro réentrée atriale droite, rare chez le sujet jeune, et plus souvent rencontrée chez le patient d’âge mûr. Nous l’avons cependant rencontrée chez de jeunes militaires dans de rares cas. Le principe de l’ablation est la création d’une ligne de bloc de conduction bidirectionnelle au niveau de l’isthme cavo-tricuspide afin d’interrompre le Figure 3. Ablation de flutter atrial commun. Arrêt du flutter pendant le tir de radiofréquence. indications actuelles des techniques ablatives et incidence sur l’aptitude en milieu militaire 331 D O S S I E R pouvoir être proposée chez de jeunes patients souffrant de fibrillation atriale paroxystique invalidante, c'est-àdire demeurant symptomatiques après échec d’au moins un ou deux médicaments antiarythmiques. Une densité minimale d’arythmie est exigée avec au moins un épisode tous les quinze jours. Les indications de l’ablation de la FA ne sont toutefois pas encore complètement validées (9). H) TACHYCARDIE INTRAFASCICULAIRE SENSIBLE AU VÉRAPAMIL. La tachycardie intrafasciculaire sensible au vérapamil ou tachycardie de Belhassen, se présentent sous forme d’une tachycardie ventriculaire à QRS peu élargis (autour de 140 ms) à type de retard droit et d’axe supérieur gauche (2). Il s’agit d’une tachycardie ventriculaire sur cœur sain survenant classiquement chez l’homme entre 15 et 40 ans pouvant être responsable de cardiomyopathie rythmique avec altération de la FEVG. L’ablation est indiquée chez les patients symptomatiques présentant des lipothymies ou des syncopes, ou en cas de tachycardies récidivantes ou résistantes au traitement médical. Le taux de succès est de 80 à 90 %. Il existe d’autres tachycardies ventriculaires bénignes sur cœur sain telles que la tachycardie en salve de Gallavardin que nous n’aborderons pas. IV. COMPLICATIONS. Le taux de complications est variable selon l’arythmie traitée (10). Un travail portant sur 1 050 patients adressés pour ablation d’arythmie supraventriculaire, et comportant 1 136 gestes d’ablation a montré la survenue de complications graves chez 3 % des patients et de complications mineures chez 8,1 % des patients (11). Le taux de mortalité était de 0,2 %. Ces complications peuvent être liées à la ponction veineuse, au geste de cathétérisme, ou à l’ablation elle-même. Les complications liées à la ponction veineuse comprenaient les hématomes au point de ponction (3 %), les pseudoanévrysmes, les fistules artérioveineuses, les thromboses veineuses ou artérielles, voire une exceptionnelle infection. Il est survenu un pneumothorax en cas de ponction sous clavière chez 1 % des patients. L’ablation pouvait être compliquée d’épanchement péricardique (2 %, dont une tamponnade), de bloc auriculoventriculaire (0,8 % dont six blocs auriculoventriculaires complets) ou de troubles du rythme. Il a été également rapporté la survenue de lésions d’une artère coronaire pouvant se compliquer d’infarctus du myocarde (0,1 % dans la série de Calkins) et de lésions valvulaires responsables d’insuff isance mitrale, tricuspide ou aortique (0,1 %). Des accidents thromboemboliques peuvent survenir en particulier lors de procédures d’ablation dans les cavités gauches (1 % d’accidents vasculaires cérébraux dans le travail sus cité). Enfin, quelques patients ressentent des douleurs thoraciques transitoires pendant le tir de radiofréquence. Dans le registre européen MERFS le taux de complication était de 332 5,1 % et le risque de mortalité faible de 0,04 % (2). Le risque radique est faible (12). Il a été estimé que chaque heure de radioscopie était associée à un risque de survenue de cancer fatal de 0,1 % et d’un risque d’anomalie génétique de 20 par million de naissance. Il est à noter que la grande majorité des ablations est réalisée avec moins d’une heure de scopie. Les procédures d’ablation ne doivent bien entendu pas être réalisées en cours de grossesse, sauf cas particuliers (urgence vitale). Au regard de ce risque de complications, heureusement relativement rares mais parfois graves, on comprend que les procédures d’ablation doivent être rigoureusement justifiées, en particulier chez les sujets asymptomatiques demandeurs d’aptitude au service dans les armées. À l’opposé, plusieurs études ont montré que l’ablation des arythmies avait un impact positif sur la qualité de vie des patients traités (1, 2), aussi bien en ce qui concerne l’amélioration des symptômes que la qualité de vie générale. Plusieurs études randomisées ont également montré que l’ablation était supérieure au traitement médical en terme de qualité de vie. V. IMPLICATIONS MÉDICO-MILITAIRES. La découverte d’une arythmie à l’engagement ou en cours de carrière est souvent synonyme d’une restriction d’aptitude voire d’une inaptitude. L’ablation, technique radicale, peut permettre à ces militaires de recouvrer leur aptitude. Les modalités concernant l’aptitude après ablation ont été récemment précisées dans l’instruction de référence (13). L’aptitude doit être évaluée dans un service de cardiologie d’un hôpital d’instruction des armées (HIA). Il convient d’attendre six mois après l’ablation en raison du risque non négligeable de récidive, comme nous l’avons vu précédemment. Ce délai doit être porté à un an après ablation de FA. Le cardiologue expert doit disposer du compte rendu détaillé de l’EEP et du geste d’ablation. L’expertise doit commencer par un interrogatoire rigoureux à la recherche de la persistance des symptômes ou de l’apparition de nouveaux signes fonctionnels. L’examen clinique doit s’attacher à l’examen des points de ponction avec auscultation des axes vasculaires af in de s’assurer de l’absence de complication locale. L’examen cardiovasculaire doit être complet et rechercher en particulier l’existence d’un souffle cardiaque. Du point de vue paraclinique, un ECG 12 dérivations doit toujours être réalisé. L’échocardiographie évaluera plus précisément l’appareil valvulaire, la fonction ventriculaire gauche et le péricarde. Une épreuve d’effort et un holter ECG seront également effectués. Le holter ECG sera réalisé à la recherche de la persistance d’arythmie. L’épreuve d’effort permettra de s’assurer de l’absence de déclenchement d’arythmie en situation cathécolergique. Dans le cas d’une ablation d’une voie accessoire à conduction antérograde, un test à la Striadyne sera réalisé. L’injection rapide de 20 mg de Striadyne par voie intraveineuse permet en effet de bloquer la conduction par les voies normales et de révéler ph. heno l’existence d’une préexcitation ventriculaire résiduelle. Cet examen doit être réalisé sous monitorage continu de l’électrocardiogramme, avec de l’atropine à disposition. Ce test est contre indiqué chez les patients asthmatiques. À l’issue de cette consultation spécialisée, le patient sans cardiopathie associée ayant bénéficié avec succès de l’ablation d’une tachycardie jonctionnelle pourra être classé G = 2 ou G = 3. De même le patient sans cardiopathie associée ayant bénéficié avec succès de l’ablation d’une tachycardie atriale ou d’un flutter atrial et ne nécessitant pas de traitement médical, pourra être classé G = 2 ou G = 3. Le militaire ayant bénéficié en cours de carrière de l’ablation d’une fibrillation auriculaire pourra être classé au bout d’un an, de G = 3 à G = 5, en l’absence de récidive et de séquelle. À l’engagement, le classement sera G = 4. Les syndromes de pré-excitation ventriculaire pourront être classés après ablation de G = 2 à G = 4, en fonction de la persistance éventuelle de symptômes ou de l’existence de séquelles. En ce qui concerne les rares tachycardies ventriculaires sur cœur sain, la réglementation fixe le classement de G = 4 à G = 6, y compris après ablation. Pour tous les patients, les décisions seront prises au cas par cas. En ce qui concerne les aptitudes particulières (personnel navigant, plongée, chute opérationnelle…), la décision d’aptitude sera prononcée au cas par cas, après réalisation d’une évaluation approfondie (cf. supra) et en concertation et collaboration avec les autorités concernées (CPEMPNA, CEMPNA, CEMPP…). VI. CONCLUSION. En raison de son bon rapport eff icacité-sécurité, l’ablation par RF est devenue un traitement de choix de beaucoup d’arythmies. L’ablation par cryothérapie semble désormais une bonne alternative chez certains patients récusés pour une ablation classique à haut risque. À côté des indications indiscutables (mauvaise tolérance, altération de la FEVG, résistance aux traitements anti-arythmiques, risque de mort subite dans les cas des faisceaux de Kent « malins »), les jeunes patients sont de plus en plus demandeurs d’indications de confort (raison professionnelle, engagement, compétition sportive…). Il convient de discuter ces indications au cas par cas, en informant de manière éclairée le patient sur le rapport bénéfice/risque de la procédure. Il convient également de rappeler que même en cas d’ablation avec succès un délai de six mois à un an est nécessaire avant de pouvoir prononcer une révision d’aptitude. RÉFÉRENCES BIBLIOGRAPHIQUES 1. Morady F. Radio-frequency ablation as treatment for cardiac arrhythmias. New England Journal of Medicine 1999 ; 340 : 535-44. 2. Savouré A, Verdonck A, Ouali S, Anselme F. Méthodes ablatives. Encyc méd chir. Cardiologie. Paris : Éditions scientifiques et médicales Elsevier, 2003 : 1-036-D-10, 15 p. 3. Deprez F, Dubuc M. La cryothérapie en rythmologie. Précis de rythmologie de la Société française de Cardiologie. Montpellier : Sauramps médical éditeur, 2005 : 457-78. 4. Jaïs P, Haïssaguerre M, Gencel L, Le Métayer P, Clémenty J. L’ablation endocavitaire des tachycardies jonctionnelles. Cardiologie du sujet jeune. Paris: Arnette Blackwell SA, 1996 : 133-52. 5. Quiniou G, Chevalier JM, Polycarpe A, Bire F, Haïssaguerre M. Syndrome de Wolff-Parkinson-White et aptitude particulière. Place de l’ablation endocavitaire. Médecine et Armées 1997 ; 25 (3) : 203-7. 6. Carlioz R, Schiano P, Monteil M, Chalumeau M, Doireau P, Brandstätt P et al. Syndrome de Wolff-Parkinson-White « malin ». Médecine et Armées 1999 ; 27 (5) : 361-7. 7. Lerecouvreux M, Carlioz R, Perrier E, Plotton C, Bire F, Quiniou G et al. Aspects cliniques et électrocardiographiques des faisceaux accessoires à conduction décrémentielle. Apports de l’électrophysiologie diagnostique et interventionnelle. Médecine et Armées 2002 ; 30 (2) : 105-14. 8. Saoudi N, Yaici K, Zarkane N et al. Nouveaux concepts dans la prise en charge diagnostique et thérapeutique du flutter atrial. Archives des maladies du cœur et des vaisseaux 2004 ; 97 : 1 080-8. 9. Jaïs P, Hocini M, Sacher F et al. Place de l’ablation dans le traitement de la fibrillation auriculaire : où en sommes nous ? Où allons nous ? Archives des maladies du cœur et des vaisseaux 2004 ; 97 : 1 071-7. 10. Le Groupe de Rythmologie de la Société Française de Cardiologie. Complications de l’ablation par radiofréquence : l’expérience française. Archives des maladies du cœur et des vaisseaux 1996 ; 89 : 1 599-605. 11. Calkins H, Yong P, Miller JM et al. Catheter ablation of accessory pathways, atrioventricular nodal reentrant tachycardia, and the atrioventricular junction : final result of a prospective, multicenter clinical trial. The Atakr Multicenter Investigator Group. Circulation 1999 ; 99 : 262-70. 12. Calkins H, Niklason L, Sousa J et al. Radiation exposure during radiofrequency catheter ablation of accessory atrioventricular connections. Circulation 1991 ; 84 : 2 376-82. 13. IM N° 2100/DEF/DCSSA/AST/AME relative à la détermination de l’aptitude médicale à servir du 6 décembre 2004, livre II, titre VI, chapitre premier, article 156 (BOC, p. 6413-4. BOEM 620-4*). indications actuelles des techniques ablatives et incidence sur l’aptitude en milieu militaire 333 D O S S I E R VIENT DE PARAÎTRE L'INSTITUTION NATIONALE DES INVALIDES « HYMNE À LA VIE » François PÉDRON, Jacques BRAVO " Pour que ceux qui ont risqué leur vie ou versé leur sang pour la défense de la monarchie, finissent leurs jours dans la tranquillité " Ordonnance du roi Louis XIV, 1670. Depuis l'édification des Invalides sous le règne de Louis XIV au XVIIe siècle, l'Hôtel des Invalides abrite derrière ses hauts murs les hommes et les femmes gravement atteints en défendant la liberté ou l'indépendance de la France. Aujourd'hui, l'Institution nationale des Invalides (INI) accueille une centaine de pensionnaires. Parallèlement, c'est un établissement médical de pointe spécialisé dans le traitement du grand handicap, qui s'est ouvert depuis quelques années aux blessés civils. Avec le livre l'Institution nationale des Invalides « Hymne à la vie », édité par Corinne K REBS , le journaliste François PÉDRON et le photographe Jacques BRAVO donnent un éclairage inédit à la vie quotidienne de ce lieu, à son histoire et aux personnes qui l'animent avec passion et dévouement. En mots et en images, ils esquissent les portraits émouvants de ses pensionnaires, dernières victimes et témoins des conflits et barbaries du XXe siècle. Sommaire – Les Invalides : un morceau d'histoire de France. – Destins d'hommes et de femmes au service de la Liberté. – L'Institution Nationale des Invalides, un établissement médical de pointe dans le traitement du handicap et des traumatismes. – Le Cercle sportif de l'INI, une référence mondiale pour les sportifs handicapés de haut niveau. – La cathédrale Saint Louis des Invalides, un lieu de solennité et de recueillement bientôt tricentenaire. Les auteurs : Jacques BRAVO et François PEDRON sont allés à leur rencontre pour recueillir, souvent pour une ultime fois, leur récit, leur douleur, mais aussi leur sourire ou leur optimisme. Ils ont composé avec tendresse 10 portraits de femmes et 22 portraits d'hommes exceptionnels. Au fil des pages, nous découvrons les destins tragiques, étonnants, miraculeux et toujours dignes de ces personnes. Certaines, trop meurtries dans leur chair ou dans leur esprit, enfermées dans leur passé, communiquent avec difficulté. D'autres ont conservé une énergie, une formidable joie de vivre malgré les épreuves et ne sont pas avares d'anecdotes. L'institution Nationale des Invalides - Hymne à la vie a été dédicacé par Monsieur Jacques CHIRAC, Président de la République. Ce livre a été édité par l'association L'esprit de tous les combats, en partenariat avec le Ministère de la Défense et l'Association Les Gueules Cassées. ISBN 2 95 25428 0 5 – Pages :184 – Prix : 55 € – Contacts presse : Géraldine MUSNIER – Tél. : 06 60 94 05 49 – [email protected] – Florence Maeso 06 66 60 02 51 – [email protected] 334 Dossier « Cœur et Armées » : Rythmologie DYSPLASIE VENTRICULAIRE DROITE ARYTHMOGÈNE Étiopathogénie, diagnostic, évolution, prise en charge et retentissement sur l’aptitude au service PH. BRANDSTÄTT, J.-M. CHEVALIER, J.-M. RIGOLLAUD, F. BIRE, P.-L. MASSOURE, R. CARLIOZ RÉSUMÉ La dysplasie ventriculaire droite arythmogène est une cardiomyopathie associant des changements histologiques du myocarde ventriculaire droit et des arythmies exposant au risque de mort subite, décrite pour la première fois en 1977. Il existe une diversité de formes cliniques révélatrices, que nous avons voulu illustrer à travers trois observations qui concernent des militaires en activité. L’affirmation du diagnostic repose sur l’association d’arguments cliniques, électrocardiographiques et morphologiques que nous passons en revue avant de préciser l’évolution, le pronostic et la prise en charge thérapeutique. Les difficultés liées à la détermination d’une aptitude à servir sont illustrées à travers ces trois observations. Mots-clés : Dysplasie ventriculaire droite arythmogène. Insuffisance cardiaque. Mort subite. Troubles du rythme ventriculaire. I. INTRODUCTION. La dysplasie ventriculaire droite arythmogène (DVDA) est une cardiomyopathie associant des changements histologiques du myocarde ventriculaire droit et des arythmies. Cette entité anatomo-clinique a été décrite pour la première fois par Fontaine et al. en 1977 (1) à partir d’observations per-opératoires. Histologiquement, il s’agit d’un remplacement fibro-adipeux progressif et transmural, plus ou moins diffus, du myocarde du ventricule droit. Cette pathologie rare concerne le plus souvent des adultes jeunes avec une prédominance masculine de l’affection. PH. BRANDSTÄTT, médecin en chef, praticien certifié. J.-M. CHEVALIER, médecin en chef, praticien certifié. J.-M. RIGOLLAUD, médecin principal, praticien certifié. F. BIRE, médecin en chef, praticien certifié. P.-L. MASSOURE, médecin principal, praticien confirmé. R. CARLIOZ, médecin en chef, professeur agrégé du SSA. Correspondance : PH. BRANDSTÄTT, Service de cardiologie, HIA Robert Picqué, BP 28, 33998 Bordeaux Armées. médecine et armées, 2006, 34, 4 ABSTRACT ARRHYTHMOGENIC RIGHT VENTRICULAR CARDIOMYOPATHY: ETIOPATHOGENY, DIAGNOSIS, EVOLUTION, MANAGEMENT AND APTITUDE TO SERVE. Arrhythmogenic right ventricular cardiomyopathy is a heart muscle disease: first described in 1977, it is charaterized by histologic changes involution of the right ventricle associated with ventricular arrhythmia and sudden death. The clinical presentation is variable. The diagnosis is based on association of clinical, electrocardiographic and morphological abnormalities which are reviewed before description of natural history, prognosis and therapy. Difficulties to determine the aptitude to serve are illustrated through three observations concerning militaries. Keywords: Arrhythmogenic right ventricular dysplasia. Heart failure. Sudden death. Ventricular arrhythmia. (Médecine et armées, 2006, 34, 4, 335-342) Elle expose au risque d’arythmie ventriculaire grave à déclenchement catécholergique. À partir de trois observations concernant des militaires, colligées à l’HIA Percy et l’HIA Robert Picqué, nous rapportons les différentes formes de présentation clinique de cette affection, les moyens diagnostiques et évoquons les problèmes d’aptitude qui ne manquent pas de se poser. II. OBSERVATIONS. A) OBSERVATION 1. Une jeune femme, âgée de 26 ans, sous-officier sous contrat, présente depuis de nombreuses années des malaises sans perte de connaissance et sans relation avec l’effort, étiquetés crises de « spasmophilie ». Elle est admise aux Urgences en avril 2002 en raison d’une perte de connaissance complète précédée de manifestations 335 D O S S I E R à type de paresthésies des extrémités avec une gêne visuelle reproduisant les malaises qu’elle connaissait. Compte tenu d’anomalies de la repolarisation sur l’électrocardiogramme (ECG) avec onde T négative en D2, D3 et aVF et de V1 à V5 (fig. 1), une hospitalisation avec surveillance monitorée de l’ECG est réalisée. Celleci permet d’identifier la survenue de salves de tachycardie à complexes QRS larges à type de retard gauche-axe gauche, se prolongeant pendant plusieurs minutes (fig. 2). La présence de plusieurs complexes de fusion et de capture et l’existence d’une dissociation auriculo-ventriculaire signent l’origine ventriculaire des salves de tachycardie. Cependant, contrastant avec l’inquiétude légitime du personnel soignant alerté par les alarmes du scope, la patiente ne ressentait que les manifestations étiquetées spasmophiliques, ce qui permettait d’affirmer a posteriori le caractère ancien et répété de ces épisodes de tachycardie ventriculaire, habituellement bien tolérés avec cependant un épisode récent syncopal. Compte tenu de l’origine ventriculaire droite de cette tachycardie ventriculaire et de la négativité de l’onde T en précordiales droites, l’hypothèse d’une dysplasie ventriculaire droite est évoquée. L’échocardiographie s’avère sans particularité notamment au niveau du ventricule droit. Le Holter ECG retrouve une extrasystolie ventriculaire monomorphe non répétitive en dehors d’un quadruplet de même morphologie. Les potentiels tardifs ventriculaires (PTV) s’avèrent négatifs pour deux critères, seul le voltage RMS étant positif à 36 microvolts. Une angioscintigraphie myocardique note simplement une discrète dilatation du ventricule droit mais la cinétique pariétale et la fraction d’éjection sont normales. L’imagerie par résonance magnétique (IRM) cardiaque ne retrouve pas d’infiltration graisseuse de la paroi ventriculaire droite en spin écho mais il existe un bombement de la paroi antérieure avec une absence de contractilité compatible avec le diagnostic de DVDA. Une stimulation ventriculaire programmée réalisée sous aténolol s’avère négative mais le test à l’isoprénaline est Figure.1. ECG de la patiente 1 à l’admission. 336 Figure 2. Tachycardie ventriculaire avec complexes de fusion et complexe de capture. positif avec déclenchement de salves non soutenues de tachycardie ventriculaire. Un traitement par sotalol est proposé et progressivement augmenté à une posologie de 400 mg/j afin de contrôler l’extrasystolie ventriculaire. Un classement G = cinq est proposé et le contrat n’est pas renouvelé. La patiente interrompt son traitement par sotalol au bout d’un an ainsi que le suivi cardiologique qui avait été instauré. Deux ans après la découverte de la DVDA, il est fait mention, lors de la surveillance post-opératoire d’une appendicectomie, d’une persistance de salves de tachycardie ventriculaire non soutenues en l’absence de tout traitement. B) OBSERVATION 2. Un jeune homme, âgé de 22 ans, appelé du Service national, sans antécédent personnel ou familial, présente en 1996, lors d’un test de Cooper, un arrêt cardio-circulatoire en rapport avec une fibrillation ventriculaire qui est réduite par un choc électrique externe. Malheureusement, la récupération est incomplète avec des séquelles neurologiques importantes liées à l’anoxie cérébrale prolongée, ce qui conduit à une réforme prononcée par la Commission de réforme du Service national. Les investigations cardiologiques sont menées au cours de son séjour en rééducation. L’ECG note un élargissement anormal du ventriculogramme en précordiales droites sans trouble de la repolarisation. L’ECG à haute amplification montre une durée anormale du QRS filtré mais les deux autres critères sont négatifs. Le Holter ECG et l’épreuve d’effort n’identifient pas d’extrasystolie signif icative. L’échocardiographie suspecte des anomalies de cinétique au niveau du ventricule droit, ce que confirme l’angiographie avec une discrète dilatation du ventricule droit, une hypokinésie diffuse, des anomalies de cinétique au niveau de la portion inféro et latéro-basale avec une dilatation presque anévrysmale de la région sous-tricuspidienne, une akinésie avec image en éperon de la paroi antérolatérale de l’infundibulum pulmonaire. La stimulation ventriculaire programmée, y compris sous isoprénaline p. brandstätt Figure 3. ECG du patient 3 témoignant d’un microvoltage des complexes QRS avec onde T négative de V1 à V5. est négative. Le diagnostic de DVDA est aff irmé et compte tenu de l’arrêt cardiaque inaugural, un défibrillateur implantable est mis en place avec poursuite d’un traitement par bétaxolol 10 mg/j. Le dernier contrôle réalisé avec un recul de sept ans témoigne d’un état stable sans récidive d’un trouble du rythme. C) OBSERVATION 3. Un homme, âgé de 48 ans, sous-officier de carrière, est hospitalisé en 2001 pour prise en charge d’un tableau d’insuffisance cardiaque globale. L’interrogatoire nous apprend qu’il a déjà une longue histoire cardiologique inaugurée par une tachycardie ventriculaire en 1977, réduite par cardioversion électrique. Une évaluation deux ans plus tard fait état d’un ventricule droit un peu dilaté et le protocole de stimulation ventriculaire programmée s’avère négatif : le diagnostic retenu est celui de tachycardie ventriculaire sur cœur apparemment sain relevant d’un traitement par sotalol. Lors du suivi marqué par des épisodes de récidive du trouble du rythme, le diagnostic de DVDA est évoqué devant l’apparition d’anomalies échocardiographiques du ventricule droit qui apparaît dilaté avec des anomalies segmentaires de la contractilité. Alors que le patient n’a pas présenté de récidive de tachycardie ventriculaire depuis 1994 sous sotalol 320 mg/j, il constate une diminution progressive de ses capacités à l’effort jusqu’à l’installation du tableau d’insuffisance cardiaque globale qui conduit à son hospitalisation. L’ECG s’inscrit en rythme sinusal avec un microvoltage diffus des complexes QRS associé à une négativité de l’onde T de V1 à V5 (fig. 3) ; il n’existe cependant pas d’onde epsilon. L’échocardiographie surprend par l’aspect de dilatation bi-ventriculaire (fig. 4) avec, d’une part un ventricule droit très dilaté et hypocontractile de dysplasie ventriculaire droite arythmogène façon nette au niveau de la paroi latérale, et d’autre part un ventricule gauche globalement hypokinétique avec fraction d’éjection ventriculaire gauche estimée en Simpson monoplan à 29 %. Les potentiels tardifs ventriculaires sont positifs pour les trois critères (fig. 5). Le Holter ECG retrouve une hyperexcitabilité ventriculaire modérée mais polymorphe avec de rares doublets mais sans aucune salve. L’épreuve d’effort couplée à une étude des gaz respiratoires réalisée après stabilisation de l’état hémodynamique est limitée à 140 watts par une dyspnée importante, sans atteinte du seuil ventilatoire, le pic de VO2 s’établissant à 22 ml/kg/mn avec présence d’extrasystoles ventriculaires à type de retard gauche pendant l’effort dont un seul doublet. L’angioscintigraphie myocardique confirme l’atteinte bi-ventriculaire, la fraction d’éjection du ventricule droit étant chiffrée à 43 % avec une importante dilatation Figure 4. Dilatation bi-ventriculaire à l’échocardiographie. 337 D O S S I E R Figure 5. Potentiels tardifs ventriculaires positifs pour trois critères. cavitaire alors que le ventricule gauche non dilaté présente une cinétique altérée et une fraction d’éjection à 28 %. L’examen IRM confirme les éléments précédents avec un amincissement de la paroi ventriculaire en région antérieure mais sans infiltration pariétale par de la graisse. Le diagnostic de DVDA étant retenu sur l’ensemble de ces arguments, le patient bénéficie d’une stimulation ventriculaire programmée réalisée sous bisoprolol qui s’avère négative. Une coronarographie complète les investigations et apparaît normale, permettant d’éliminer une origine ischémique à l’atteinte du ventricule gauche. Dans un premier temps, l’intéressé est mis en congé de longue maladie pour une durée de six mois avant de faire valoir ses droits à la retraite. Avec un recul de 30 mois, le patient est stabilisé sur le plan clinique sous un traitement associant du bisoprolol 5 mg/j, un inhibiteur de l’enzyme de conversion, un diurétique et un anti-vitamine K. Il n’a présenté aucun épisode documenté de tachycardie ventriculaire. III. DISCUSSION. Depuis la première description en 1977, de nombreux progrès ont été réalisés dans le domaine de la pathogénie, de la génétique, du diagnostic de la dysplasie ventriculaire droite arythmogène, qui est intégrée depuis 1996 dans le cadre plus vaste des cardiomyopathies ventriculaires droites arythmogènes (2). La DVDA se caractérise par des anomalies structurelles et fonctionnelles du ventricule droit induites par le remplacement fibro-adipeux des cardiomyocytes. Le mécanisme de l’atrophie progressive de la paroi ventriculaire droite peut être lié à l’apoptose, qui lorsqu’elle est sévère, peut produire un certain degré de fibrose. Le mécanisme de l’adipogénèse reste cependant obscur. Avec le temps, le remplacement fibro-adipeux des cardiomyocytes du ventricule droit va s’accentuer, conduisant à une déhiscence de sa paroi qui va se dilater, manifestant par endroit des zones anévrysmales localisées, situées d’abord au niveau de la jonction trabéculo-infundibulaire de la paroi antérieure 338 du ventricule droit, l’apex puis la région sous-tricuspidienne étant atteints plus tardivement (3). Les phénomènes inflammatoires observés dans certains cas de DVDA correspondraient à des phénomènes environnementaux venant se superposer à l’anomalie génétiquement déterminée (4). La prévalence de la DVDA est d’environ 1 pour 5 000 dans la population générale (5). Les formes familiales représentent plus de 50 % des cas avec une transmission autosomique dominante sauf dans la maladie de Naxos où elle est associée à des anomalies cutanées et où la transmission est autosomique récessive. Trois gènes ont été identifiés à ce jour (6). Les premiers signes cliniques de la maladie apparaissent avant 40 ans dans plus de 80 % des cas. Une prédominance masculine est retrouvée dans toutes les séries. Les circonstances de découverte de la DVDA sont variées. À coté des formes symptomatiques de la maladie où l’arythmie ventriculaire est au premier plan, responsable de palpitations, lipothymies, syncopes ou d’une mort subite en particulier sur les terrains de sport et qui est fréquemment l’élément révélateur de la maladie (7), il existe des formes asymptomatiques ou pauci symptomatiques, découvertes devant des anomalies ECG, la présence d’extrasystoles ventriculaires (ESV) ou dans le cadre d’enquêtes familiales. La découverte d’une DVDA devant un tableau d’insuff isance cardiaque comme dans notre observation 3 reste exceptionnelle. L’ECG en rythme sinusal peut orienter le diagnostic en montrant des anomalies très évocatrices d’une DVDA : il peut s’agir d’une déviation axiale, d’un élargissement localisé du QRS supérieur à 110 ms en V1-V2 traduisant un retard de conduction pariétale dans le ventricule droit, d’une inversion de l’onde T notée le plus souvent en V1-V2-V3 mais parfois jusqu’à V5-V6 voire en D2-D3aVF. On peut observer une anomalie plus spécifique telle que l’onde « epsilon » de post-excitation ventriculaire survenant après le complexe QRS au début du segment ST. Il peut parfois exister un bas voltage des QRS comme dans les observations 1 et 3. L’arythmie ventriculaire peut se limiter à des extrasystoles ventriculaires qui typiquement ont une morphologie de retard gauche, mais des aspects de retard droit peuvent se rencontrer. Ces ESV ont tendance à se majorer à l’effort, témoignant du caractère adrénergique de l’arythmie avec survenue potentielle de salves de tachycardie ventriculaire (TV), soutenues ou non, dont l’aspect a été particulièrement étudié par Leclercq et al. à partir de 47 cas (8) : dans 96 % des cas elles ont un aspect de retard gauche, dans 91 % des cas l’axe est compris entre -80° et +110°, la largeur moyenne du QRS de la TV est de 151 +/-28 ms soit moindre que dans les cardiomyopathies congestives et le postinfarctus mais plus que dans les TV idiopathiques. L’apport de l’ECG à haute amplification est indéniable mais la recherche de potentiels tardifs ventriculaires a globalement une sensibilité de 80 % et une spécificité de 88 % pour le diagnostic de DVDA ; toutefois la valeur diagnostique des PTV est plus élevée dans les formes diffuses et en cas de présence de TV soutenue (9). p. brandstätt La normalité de l’examen ne permet cependant pas d’éliminer formellement une forme peu évoluée de DVDA comme l’illustrent nos observations 1 et 2 avec un seul critère positif. L’échocardiographie recherche une dilatation du ventricule droit, des anomalies de la cinétique pariétale et une éventuelle atteinte associée du ventricule gauche. Cependant les formes mineures restent difficiles à identifier avec cette technique. L’angioscintigraphie isotopique en contraste de phase permet d’étudier l’hétérogénéité de la contraction ventriculaire droite, d’évaluer de manière fiable les fractions d’éjection ventriculaire droite et gauche. La mise en évidence d’anomalies du ventricule droit lors d’une angioscintigraphie isotopique réalisée devant des troubles du rythme sévères provenant du ventricule droit apparaît comme hautement prédictive d’un risque de décès aussi bien que la présence d’anomalies du ventricule gauche (10). L’angiographie ventriculaire droite est encore considérée par certains experts comme la méthode de référence pour évaluer la fonction ventriculaire droite ; les critères diagnostiques actuellement retenus ont été proposés par Daubert et al. (11) : une dilatation ventriculaire droite d’importance variable mais non systématique, des anomalies de la cinétique segmentaire et des anomalies de la morphologie réalisant typiquement l’aspect de voussures arrondies, akinétiques ou dyskinétiques, ressortant nettement sur le contour télédiastolique pouvant créer de véritables images d’anévrysme. Ces anomalies sont soit isolées, soit associées chez un même patient atteignant par ordre de fréquence l’apex, la face antérieure de l’infundibulum pulmonaire et la paroi postéro-diaphragmatique du ventricule droit correspondant au triangle de la dysplasie (12). Lors d’une étude prospective portant sur 85 DVDA (13), il a été montré qu’une diminution de l’excursion de la tricuspide (TAPSE < 12 mm) permet d’identifier les patients dont la fraction d’éjection ventriculaire droite est inférieure à 35 % (sensibilité : 96 %, spécif icité : 78 %) et que la présence d’un anévrysme de l’infundibulum pulmonaire identifie ceux dont la fraction d’éjection ventriculaire gauche est inférieure à 40 % (sensibilité : 86 %, spécificité : 96 %). L’imagerie par résonance magnétique devient l’examen clé du diagnostic car elle permet d’étudier les anomalies morphologiques du ventricule droit (dilatation, amincissement pariétal, déformation des contours…) et elle met en évidence la présence de tissu adipeux se traduisant par un hypersignal en écho de spin. Enfin les techniques de ciné-IRM apportent des renseignements sur les anomalies de cinétique segmentaire du ventricule droit (akinésie ou dyskinésie) (14, 15). Le scanner multi barrettes permet également de rechercher la présence de graisse dans la paroi latérale du ventricule droit, dans le septum et la paroi latérale gauche, un aspect festonné de la paroi latérale du ventricule droit (16). La stimulation ventriculaire droite programmée recherche l’inductibilité des tachycardies ventriculaires : dans les formes diffuses, plusieurs morphologies de tachycardie ventriculaire peuvent être déclenchées. Haïssaguerre et al. ont montré que la perfusion d’isoprénaline à haute concentration permet d’induire une tachycardie ventriculaire dans 85 % des cas de DVDA (17). Tableau I. Critères diagnostiques de la DVDA d’après Mc Kenna et al. (18). Critères majeurs Critères mineurs - Dilatation importante du ventricule droit (VD) et réduction de la fraction d'éjection du VD sans (ou avec légère) altération du ventricule gauche (VG)*, - Anévrismes du VD*, - Dilatation segmentaire sévère du VD*, - Infiltration fibro-graisseuse du myocarde sur la biopsie endomyocardique, - Onde epsilon ou allongement (> 110 ms) des complexes QRS en dérivations précordiales droites (V1-V3), - Maladie familiale confirmée par nécropsie ou chirurgie. - Dilatation modérée et globale et/ou légère réduction de la fraction d'éjection du VD avec VG normal*, - Dilatation segmentaire modérée du VD*, - Hypokinésie segmentaire du VD*, - Inversion des ondes T en dérivations précordiales droites (V1-V3) (sujets de plus de 12 ans ; en l'absence de bloc de branche droit), - Présence de potentiels tardifs ventriculaires (ECG à haute amplification), - Tachycardie ventriculaire (soutenue ou non) à type de retard gauche (ECG, Holter, épreuve d'effort), - Extrasystoles ventriculaires fréquentes (> 1 000/24 heures) au Holter, - Antécédent familial de mort subite précoce (< 35 ans) due à une DVDA suspectée, - Antécédent familial (diagnostic clinique basé sur ces critères). * Détecté par échographie, angiographie, imagerie par résonance magnétique ou scintigraphie. dysplasie ventriculaire droite arythmogène 339 D O S S I E R La biopsie endomyocardique n’est que rarement réalisée compte tenu de ses limitations (des faux négatifs sont possibles dans les formes localisées) et de ses risques. Considérant les difficultés rencontrées pour établir le diagnostic de DVDA, un groupe d’experts a établi en 1994 des critères diagnostiques (18) : la présence de deux critères majeurs, ou d’un critère majeur et de deux critères mineurs, ou de quatre critères mineurs permet de retenir le diagnostic de DVDA (tab. 1). Le problème du diagnostic différentiel se pose surtout devant les manifestations rythmiques de la maladie : le diagnostic d’ESV bénignes d’origine infundibulaire ou de tachycardie ventriculaire bénigne naissant du ventricule droit nécessite la normalité des examens morphologiques et l’absence de potentiels tardifs ventriculaires mais une surveillance est indispensable afin de ne pas passer à coté d’une forme débutante et/ou focale de DVDA. Le problème du rapport entre DVDA et syndrome de Brugada reste l’objet de controverses. Certaines DVDA peuvent présenter des anomalies ECG avec un sus-décalage du segment ST comparable à ce qui est décrit dans le syndrome de Brugada. Corrado et al. (19) ont montré, lors d’une étude autopsique portant sur 273 morts subites d’origine cardiovasculaire survenues avant 35 ans, que 13 sujets présentaient à l’ECG un sus décalage du segment ST isolé (9 cas) ou associé à un bloc de branche droit (4 cas) et que tous sauf un présentaient une DVDA à l’autopsie ; mais contrairement aux DVDA sans sus décalage du segment ST de la même série, les décès étaient survenus sans relation avec l’effort chez des sujets ayant souvent présenté des changements dynamiques de l’ECG et des tachycardies ventriculaires polymorphes qui sont plutôt l’apanage des syndromes de Brugada, témoignant de formes de recouvrement entre la DVDA et le syndrome de Brugada. L’évolution et le pronostic de la DVDA sont encore mal connus. Ils restent dominés par le risque de mort subite rythmique, particulièrement au cours de l’effort sportif. Une étude histologique (20) réalisée dans la région de Venise concernant les causes de mort subite chez des jeunes gens de moins de 35 ans montre qu’un tiers des 60 décès colligés entre 1979 et 1986 sont dus à une DVDA. Furlanello et al. (21), examinant 1 642 athlètes de compétition italiens présentant des troubles du rythme, portent le diagnostic de DVDA chez 6 % d’entre eux: lors d’un suivi moyen de huit ans, 4 % présentèrent un arrêt cardiaque ou une mort subite, les sujets porteurs d’une DVDA représentant un quart du nombre total des athlètes ayant présenté l’un de ces évènements, confirmant ainsi le fait que la DVDA est la cause principale de mort subite à l’effort parmi les athlètes italiens. La relation entre la mort subite chez le sportif et la DVDA soulève plusieurs questions. D’abord, l’effort n’est-il que le facteur déclenchant du trouble du rythme fatal chez un sportif porteur d’une DVDA : à partir d’une série autopsique de 300 morts subites chez des sujets de moins de 35 ans, Corrado et al. (22) montrent que le fait de pratiquer une activité de compétition entraîne un risque significativement plus élevé de mort subite, en grande partie lié à l’existence 340 d’une pathologie cardiovasculaire sous-jacente, le sport favorisant l’émergence d’arythmies ventriculaires fatales durant l’exercice physique. Mais aussi, le sport peut-il favoriser le développement d’une DVDA: Heidbüchel (23) fait l’hypothèse que certains sports d’endurance pratiqués à un haut niveau (en particulier le cyclisme) peuvent entraîner des atteintes structurelles du ventricule droit qui ne seraient pas apparues sans cette pratique sportive, expliquant que sur une série de 46 athlètes de haut niveau (dont 80 % de cyclistes) présentant des arythmies ventriculaires complexes, 59 % étaient porteurs d’une DVDA certaine et 30 % d’une DVDA probable. Par ailleurs, avec le recul évolutif portant sur de nombreuses séries de la littérature, il est apparu que le risque d’insuffisance cardiaque s’avère être supérieur à 20 % des cas de DVDA. Fontaine et al. (4) proposent une classification des modalités évolutives de la DVDA en fonction de l’altération de la fraction d’éjection du ventricule gauche: dans le type I, la FEVG est supérieure à 50 % et le risque apparaît exclusivement rythmique ; dans le type II, la FEVG est comprise entre 30 % et 50 % : la forme est stable et peut le rester pendant de nombreuses années ; dans le type III avec une FEVG inférieure à 30 %, il existe une dégradation progressive du myocarde avec un risque d’insuffisance cardiaque progressivement irréversible. Plus récemment, une étude multicentrique à la fois clinique et histologique portant sur 42 cas de DVDA avec diagnostic histologique (autopsie ou transplantation cardiaque) démontre que l’atteinte du ventricule gauche est présente dans 76 % des cas, qu’elle apparaît dépendante de l’âge, plus fréquente en cas d’histoire clinique longue, qu’elle progresse au cours du suivi échographique et qu’elle est associée à des évènements cliniques d’ordre rythmique plus fréquents ainsi qu’à un taux d’insuffisance cardiaque plus important (24). Aussi, l’évolution semble s’établir en plusieurs phases (25) : une phase avec des changements structurels minimes du ventricule droit, sans ou avec des troubles du rythme ventriculaires peu sévères, pendant laquelle une mort subite peut être la première manifestation clinique ; une phase avec un désordre électrique manifeste responsable de troubles du rythme symptomatiques susceptibles d’être à l’origine d’un arrêt cardiaque, associé à des anomalies structurelles et fonctionnelles du ventricule droit ; une phase d’insuff isance ventriculaire droite par extension progressive de l’atteinte du ventricule droit, le ventricule gauche restant plus ou moins préservé ; enfin une dernière phase avec insuffisance cardiaque globale liée à la progression de la dysfonction ventriculaire gauche: à ce stade, la DVDA ressemble aux cardiomyopathies dilatées avec atteinte bi-ventriculaire. Les trois observations que nous rapportons illustrent parfaitement cette diversité clinique et évolutive. L’observation 2 correspond à une forme dont la première manifestation clinique est une mort subite récupérée survenue lors d’un effort sportif, l’atteinte du ventricule droit n’étant retrouvée qu’à l’angiographie ventriculaire p. brandstätt droite. L’observation 1 correspond à une atteinte ventriculaire droite pure responsable d’une tachycardie ventriculaire soutenue révélatrice de la DVDA, l’atteinte ventriculaire droite étant suspectée sur l’angioscintigraphie ventriculaire droite. Enfin la troisième observation pour laquelle existe un recul de 27 ans témoigne de l’évolutivité de l’affection avec initialement des épisodes de tachycardie ventriculaire avec atteinte isolée du ventricule droit puis apparition d’une atteinte ventriculaire gauche asymptomatique et enfin survenue d’un tableau d’insuff isance cardiaque globale sans récidive de troubles du rythme soutenus. La prise en charge thérapeutique des patients atteints de DVDA reste encore très empirique. Les patients présentant des arythmies ventriculaires bien tolérées et non menaçantes sont habituellement mis sous antiarythmiques en utilisant de préférence les bêtabloquants et en particulier le Sotalol (26), compte tenu du caractère adrénergique des troubles du rythme, en s’aidant du contrôle de l’eff icacité du traitement par la stimulation ventriculaire programmée. Les techniques ablatives constituent un complément logique du traitement antiarythmique, quand celui-ci devient inefficace pour le contrôle des récidives. Le défibrillateur automatique implantable (DAI) fait figure de protection ultime et universelle vis-à-vis de la mort subite rythmique. Cependant, les recommandations françaises et nord-américaines actuelles n’envisagent pas la DVDA comme une entité à part et la rareté de la maladie rend difficile les études randomisées. Dans ces conditions, la plupart des implantations se font à l’occasion d’un évènement clinique majeur : mort subite récupérée (comme dans l’observation 2), tachycardie ventriculaire syncopale, mal tolérée ou non contrôlée par le traitement pharmacologique ou l’ablation, les indications réellement prophylactiques (histoire familiale de mort subite liée à une DVDA, altération de la fonction ventriculaire gauche…) restant rares. La plus grande étude à ce jour a été menée chez 132 patients porteurs d’une DVDA et implantés (27) : 48 % ont eu un déclenchement approprié du DAI lors d’un suivi moyen de 39 mois dont la moitié pour un trouble du rythme potentiellement fatal. Par ailleurs, une histoire avant implantation d’arrêt cardiaque récupéré, de tachycardie ventriculaire mal tolérée hémodynamiquement, un âge jeune et une altération ventriculaire gauche étaient des facteurs prédictifs indépendants de survenue d’une fibrillation ou d’un flutter ventriculaire. Les nombreuses incertitudes concernant l’évolution spontanée et l’eff icacité des différentes thérapeutiques ont conduit à proposer en 2000 la création d’un registre international sur la DVDA (28). À l’échelon européen, il est réalisé la mise en place de banques de données cliniques, anatomo-pathologiques, génétiques ainsi qu’une évaluation des thérapeutiques avec une stratif ication du risque concernant cette pathologie, l’ensemble de ces travaux étant f inancé par la Communauté européenne (6). dysplasie ventriculaire droite arythmogène L’étendue de ces incertitudes rend bien sûr la détermination de l’aptitude médicale à servir dans les Armées très délicate : la présence ou la découverte d’une DVDA à l’engagement doit conduire à prononcer une décision d’inaptitude. L’identification formelle d’une DVDA en cours de carrière doit conduire à des restrictions importantes d’activité, imposant souvent des changements de spécialité voire une inaptitude définitive. Selon les nouvelles normes d’aptitude en cardiologie datant du 06/12/2004 (29), le classement proposé est G = quatre à six pour « autres cardiomyopathies », « tachycardies ventriculaires qu’elle qu’en soit la cause », « insuffisance cardiaque chronique » ou « insuffisance cardiaque aiguë, compliquant une affection non curable». Les éléments à prendre en compte sont représentés par la présence de troubles du rythme ventriculaire et l’efficacité de leur contrôle par les bêtabloquants en particulier, ainsi que par l’existence d’une altération de la fonction ventriculaire gauche. La survenue de complications évolutives (mort subite récupérée, insuffisance cardiaque…) ou la nécessité de certaines thérapeutiques (mise en place d’un déf ibrillateur implantable…) paraissent incompatibles avec le maintien en activité qui ne saurait s’envisager que de manière personnalisée et restrictive, par dérogation aux normes médicales et sous couvert d’un suivi cardiologique imposé. Les décisions d’inaptitude à l’emploi prononcées dans le cas de nos trois observations illustrent ces propositions : la survenue d’une mort subite récupérée avec séquelles et d’une insuffisance cardiaque étaient incompatibles avec le maintien en activité ; seule l’observation 1 aurait pu faire discuter un maintien en activité chez une secrétaire, sous réserve d’une efficacité du traitement bêtabloquant et d’un suivi périodique avec bien sûr le maintien d’une activité sédentaire stricte : cependant, le recul nous a montré l’absence de compliance et d’observance de la patiente qui valide a posteriori notre prudence initiale. IV. CONCLUSION. La DVDA est une entité anatomo-clinique rare dont la première description remonte seulement à 1977 et dont la prévalence, l’étiologie et l’évolution, malgré des progrès certains, restent encore bien mal connus. Le diagnostic, qu’il faut savoir évoquer devant des anomalies ECG en précordiales droites, des arythmies ventriculaires symptomatiques ou non, bénéficie des progrès de l’imagerie du ventricule droit et s’appuie sur des critères diagnostiques définis en 1994. En dehors du risque rythmique qui doit toujours rester à l’esprit, il existe un risque non négligeable d’insuffisance cardiaque lié à la progression de l’atteinte d’abord au niveau de l’ensemble du ventricule droit puis au niveau du ventricule gauche. L’ensemble de ces incertitudes a conduit à proposer la création d’un registre international sur la DVDA et d’un ensemble de banques de données européennes afin de progresser dans le domaine du diagnostic, de l’histoire naturelle et de la stratification du risque. 341 D O S S I E R RÉFÉRENCES BIBLIOGRAPHIQUES 1. Fontaine G, Guiraudon G, Frank R, Vedl J, Grosgogeat Y, Cabrol C et al. Stimulation studies and epicardial mapping in ventricular tachycardia: study of mechanisms and selection for surgery. In: Kulbertus HE ed. Reentrant arrhythmias. Lancaster: MTP publishing, 1977 : 334-50. 2. Richardson P, McKenna WJ, Bristow M, Maisch B, Mautner B, O’Connell J et al. Report of the1995 World Health Organization/International Society and Federation of Cardiology Task Force on the definition and classification of cardiomyopathies. Circulation 1996 ; 93 : 841-2. 3. Fontaine G. La DVDA, une maladie évolutive. Cardinale 2004 ; 16 : 26-9. 4. Fontaine G, Brestescher C, Fontaliran F, Himbert C, Tonet J, Frank R. Modalités évolutives de la dysplasie ventriculaire droite arythmogène. À propos de 4 observations. Arch Mal Cœur 1995 ; 88 : 973-9. 5. Norman NW, McKenna W. Arrhythmogenic right ventricular dysplasia/cardiomyopathy: perspectives on disease. Z Kardiol 1999 ; 88 : 550-4. 6. Basso C, Wichter T, Danieli GA, Corrado D, Czarnowska E, Fontaine G et al. Arrhythmogenic right ventricular cardiomyopathy: clinical registry and database, evaluation of therapies, pathology registry, DNA banking. Eur Heart J 2004 ; 25 : 531-4. 7. Fourcade L, Van de Walle JP, Panagides D, Mafart B, Bory M, Touze JE. Dysplasie ventriculaire droite arythmogène. Médecine et Armées 1996 ; 24 (2) : 93-7. 8. Leclercq JF, Gaita F, Cauchemez B, Maison-Blanche P, Leenhardt A, Coumel P et al. Caractéristiques et pronostic des troubles du rythme ventriculaire de la dysplasie ventriculaire droite arythmogène. Arch Mal Cœur 1988 ; 81 : 1335-41. 9. Leclercq JF, Denjoy I, Maison-Blanche P, Cauchemez B, Leenhardt A, Slama R. L’électrocardiographie à haute amplification et moyennage dans la dysplasie ventriculaire droite. Arch Mal Cœur 1990 ; 83 : 525-9. 10. Le Guludec D, Gauthier H, Porcher R, Frank R, Daou D, Benelhadj S et al. Circulation 2001 ; 103 : 1972-6. 11. Daubert C, Descaves C, Foulgoc JL, Bourdonnec C, Laurent M, Gouffault J. Critical analysis of cineangiographic criteria for diagnosis of arrhythmogenic right ventricular dysplasia. Am Heart J 1988 ; 115 : 448-59. 12. Marcus FI, Fontaine G, Guiraudon G, Frank R, Laurenceau JL, Malergue MC et al. Right ventricular dysplasia: a report of 24 cases. Circulation 1982 ; 65 : 384-99. 13. Hébert JL, Chemla D, Gérard O, Zamani K, Quillard J, Azarine A et al. Angiographic right and left ventricular function in arrhythmogenic right ventricular dysplasia. Am J Cardiol 2004 ; 93 : 728-33. 14. Roul G, Germain P, Coulbois PM, Bareiss P, Dietemann JL. Séméiologie IRM des anomalies de la contraction segmentaire dans la dysplasie arythmogène du ventricule droit. J Radiol 1998 ; 79 : 541-7. 15. Dumousset E, Alfidja A, Lamaison D, Ponsonnaille J, Ravel A, Garcier JM et al. IRM et dysplasie arythmogène du ventricule droit 342 16. 17. 18. 19. 20. 21. 22. 23. 24. 25. 26. 27. 28. 29 (DAVD). Évaluation rétrospective chez 50 patients. J Radiol 2004 ; 85 : 313-20. Deux JF. Imagerie cardiaque. J Radiol 2002 ; 83 : 927-9. Haïssaguerre M, Chavernac P, Le Metayer P, Barat JL, Montserrat P, Heraudeau A et al. Valeur complémentaire du test à l’isoprénaline et de l’ECG à haute amplification dans le diagnostic de la dysplasie arythmogène du ventricule droit. Ann Cardiol Angeiol 1992 ; 41 : 425-32. McKenna WJ, Thiene G, Nava A, Fontaliran F, BlomstromLundqvist C, Fontaine G et al. Diagnosis of arrhythmogenic right ventricular dysplasia/cardiomyopathy. Br Heart J 1994 ; 71 : 215-8. Corrado D, Basso C, Buja G, Nava A, Rossi L, Thiene G. Right bundle branch block, right precordial ST-segment elevation, and sudden death in young people. Circulation 2001 ; 103 : 710-7. Thiene G, Nava A, Corrado D, Rossi L, Pennelli N. Right ventricular cardiomyopathy and sudden death in young people. N Engl J Med 1988 ; 318 : 129-33. Furlanello F, Bertoldi A, Dallago M, Furlanello C, Fernando F, Inama G et al. Cardiac arrest and sudden death in competitive athletes with arrhythmogenic right ventricular dysplasia. Pacing Clin Electrophysiol 1998 ; 21 : 331-5. Corrado D, Basso C, Rizzoli G, Schiavon M, Thiene G. Does sports activity enhance the risk of sudden death in adolescents and young adults ? J Am Coll Cardiol 2003 ; 42 : 1959-63. Heidbüchel H, Hoogsteen J, Fagard R, Vanhees L, Ector H, Willems R et al. High prevalence of right ventricular involvement in endurance athletes with ventricular arrhythmias. Role of an electrophysiologic study in risk stratification. Eur Heart J 2003 ; 24 : 1 473-80. Corrado D, Basso C, Thiene G, McKenna WJ, Davies MJ, Fontaliran F et al. Spectrum of clinicopathologic manifestations of arrhythmogenic right ventricular cardiomyopathy/dysplasia: a multicenter study. J Am Coll Cardiol 1997 ; 30 : 1 512-20. Thiene G, Nava A, Angelini A, Daliento L, Scognamiglio R, Corrado D. Anatomoclinical aspects of arrhythmogenic right ventricular cardiomyopathy. In : Baroldi G, Camerini F, Goodwin JF eds. Advances in Cardiomyopathy. Berlin : Springer Verlag, 1990 : 397-408. Wichter T, Borggrefe M, Hoverkamp W, Chen X, Breithardt G. Efficacy of antiarrhythmic drugs in patients with arrythmogenic right ventricular disease: results in patients with inducible and noninducible ventricular tachycardia. Circulation 1992 ; 86 : 29-37. Corrado D, Leoni L, Link MS, Della Bella P, Gaita F, Curnis A et al. Implantable cardioverter-defibrillator therapy for prevention of sudden death in patients with arrythmogenic right ventricular cardiomyopathy/dysplasia. Circulation 2003 ; 108 : 3 084-91. Corrado D, Fontaine G, Marcus FI, McKenna WJ, Nava A, Thiene G et al. Arrhythmogenic right ventricular dyplasia/ cardiomyopathy: need for an international registry. Circulation 2000 ; 101 : e101-6. 1° modificatif à l’instruction n° 2100/DEF/DCSSA/AST/AME du 1er octobre 2003 (BOC, p. 7118 ; BOEM 620-4*) relative à la détermination de l’aptitude médicale à servir. BOC/PP. 6 décembre 2004. n° 50 : 6 409-35. p. brandstätt Dossier « Cœur et Armées » : Divers DIAGNOSTIC ET PRONOSTIC DE LA CARDIOMYOPATHIE HYPERTROPHIQUE EN 2006 Acquis et incertitudes P. GODON, U. VINSONNEAU, A. BRONDEX, C. VANOYE, G. QUINIOU RÉSUMÉ ABSTRACT Des progrès considérables dans la connaissance de la cardiomyopathie hypertrophique ont été accomplis au cours des dernières années. Il demeure important d’éviter les erreurs par défaut, surtout chez le sujet jeune étant donné le risque de mort subite qui s’attache à cette maladie mais, à l’inverse, les erreurs par excès entraînent un handicap psychologique et social grave. L’électrocardiogramme et l’échocardiographie sont toujours la pierre angulaire du diagnostic mais l’imagerie par résonance magnétique et l’analyse génétique peuvent contribuer aux diagnostics difficiles. La cardiomyopathie hypertrophique demeure en 2006 une maladie complexe, probablement moins grave que ce que l’on pensait initialement pour la majorité des patients mais pouvant être à l’origine d’événements cardiovasculaires majeurs et de décès prématurés encore difficilement prévisibles. Mots-clés : Cardiomyopathie Diagnostic. Mortalité. Pronostic. hypertrophique. DIAGNOSIS AND PROGNOSIS OF HYPERTROPHIC CARDIOMYOPATHY IN 2006: KNOWLEDGE AND UNCERTAINTY. Considerable progress has been accomplished in the understanding of hypertrophic cardiomyopathy (HCM) over the last years. It remains important to avoid overlooking this diagnosis especially in young subjects, because of the risk of sudden death but, conversely, false positive diagnosis can result in a serious social and psychological handicap. Electrocardiogramm and two dimensionnal echocardiography are currently the standard tests for the clinical diagnosis of HCM but magnetic resonance imaging and genetic diagnosis may be helpful for difficult diagnosis. HCM remains a complex disease, less serious than initially thought in the majority of patients, but the cause of major cardiovascular events and premature deaths wich still remain difficult to prevent. Keywords: Diagnosis. Hypertrophic cardiomyopathy. Mortality. Prognosis. (Médecine et Armées, 2006, 34, 4, 343-348) I. INTRODUCTION. La cardiomyopathie hypertrophique (CMH), bien que finalement assez peu fréquente en pratique quotidienne, continue d’occuper une place importante dans l’imaginaire médical. À l’origine de décès subits survenant chez des patients jeunes, notamment lors d’un effort sportif, elle jouit ainsi d’une mauvaise réputation et demeure, à juste titre, une préoccupation constante de nombreux médecins, qu’ils soient médecins d’unité, médecins du sport, urgentistes ou cardiologues. En sa défaveur demeure la complexité de la maladie qui, malgré un déterminisme génétique et des caractéristiques P. GODON, médecin en chef, praticien certifié. U. VINSONNEAU, médecin principal, praticien confirmé. A. BRONDEX, médecin lieutenant, praticien en formation. C. VANOYE, médecin lieutenant, praticien en formation. G. QUINIOU, médecin en chef, praticien certifié. Correspondance : P. GODON, Service de cardiologie, HIA Clermont-Tonnerre, BP 41, 29240 Brest Armées. médecine et armées, 2006, 34, 4 anatomiques univoques, s’exprime toujours avec un polymorphisme clinique et évolutif majeur et parfois déroutant. Cependant ces dernières années ont vu évoluer la maladie avec une phase diagnostique plus précise et plus rigoureuse, une stratégie de prise en charge mieux établie, un pronostic sans doute moins péjoratif que ne le laissait transparaître les premières séries, des thérapeutiques plus agressives et efficaces et, enfin, l’irruption de la génétique dans tous les aspects de la maladie. II. DÉFINITION – PHYSIOPATHOLOGIE. La CMH est une cardiomyopathie caractérisée par une hypertrophie primitive portant essentiellement sur le ventricule gauche, sans dilatation cavitaire. Cette hypertrophie est typiquement asymétrique, prédominant sur le septum interventriculaire (SIV). Toutefois le siège et le degré de l’hypertrophie peuvent être très variables. Ainsi l’hypertrophie peut siéger, outre 343 D O S S I E R le SIV, sur la paroi antérolatérale voire, plus rarement, être diffuse et symétrique (< 5 % des cas) ou purement localisée à l’apex. Quant au degré d’hypertrophie il peut être rudimentaire ou considérable, dépassant 30 mm, avec parfois une grande variabilité dans le temps chez un même individu. Microscopiquement on observe des cellules myocardiques hypertrophiées dont l’agencement est désorganisé avec une augmentation du taux de fibrose. Cette hypertrophie pathologique induit plusieurs conséquences à l’origine des manifestations cliniques de la maladie : – une altération de la fonction diastolique responsable de certains tableaux d’insuffisance cardiaque à fonction systolique conservée ; – des anomalies de la microcirculation potentiellement responsables de manifestations angineuses ; – une obstruction sous aortique dynamique, liée à l’hypertrophie septale, présente chez 30 % des patients, à l’origine du souffle caractéristique de l’affection. Cette obstruction contribue à la survenue, ou l’aggravation, de symptômes à l’effort ; – l’intrication d’une ischémie fonctionnelle, d’une inadaptation hémodynamique et d’altérations structurelles fait alors le lit des complications rythmiques qui vont influencer le pronostic vital. Longtemps suspectée sur l’existence de cas familiaux, l’origine génétique de la maladie a pu être démontée en 1989 avec l’identif ication d’un premier gène responsable. Depuis, plus de 300 mutations ont été identifiées à partir de treize gènes différents faisant de la CMH une affection particulièrement hétérogène en terme génétique. Cependant plus de 80 % des mutations retrouvées concernent deux gènes : MYBPC3 codant la protéine C qui lie la myosine et MYH 7 codant la chaîne lourde ß de la myosine. La transmission se fait sur un mode autosomique dominant à pénétrance variable, les formes familiales représentant 60 % des cas. Il faut ainsi reconnaître en 2006 notre absence totale de connaissance de la prévalence de la CMH en France ou en Europe. IV. COMMENT FAIRE LE DIAGNOSTIC ? Le diagnostic de CMH peut être évoqué dans des situations diverses : – c’est naturellement toujours la découverte d’un souffle ou d’une anomalie à l’électrocardiogramme (ECG) qui peut conduire au diagnostic ; – ce peut être aussi la survenue d’un symptôme inhabituel, malaise, syncope, dyspnée, angor, surtout lorsqu’il survient à l’effort ; – ce peut être une découverte fortuite dans le cadre d’une enquête génétique chez un patient asymptomatique mais dont l’un des apparentés est porteur de l’affection ; – enfin, malheureusement, ce peut être une découverte nécropsique, devant une mort subite inopinée, inattendue ou inexpliquée, particulièrement lors d’une séance de sport. Lorsque la possibilité d’une CMH est évoquée l’établissement d’un diagnostic formel et, si possible, rapide devient alors une nécessité absolue en raison des conséquences potentielles de cette affection et des répercussions psychologiques, sociales ou professionnelles qui peuvent en découler. A) EXAMEN CLINIQUE. L’examen clinique occupe toujours une place incontournable bien qu’il puisse être normal chez un patient asymptomatique sans gradient de pression. La principale anomalie est un souffle très particulier, présent uniquement chez les patients dont l’hypertrophie induit une obstruction ventriculaire. Le souffle est alors mésosystolique, distinct des premiers et deuxièmes bruits, accru en position debout, en expiration, par le Valsalva, diminué au contraire en position accroupie ou en inspiration. B) ECG. III. ÉPIDÉMIOLOGIE. Il faut bien reconnaître qu’elle est encore très mal connue. La plupart des publications font état d’une prévalence de 1 cas pour 500 dans la population générale mais toutes ces publications se réfèrent à l’unique étude d’envergure réalisée sur le sujet par BJ Maron en 1995 sur une population de 4 111 jeunes Américains (1). Ces conclusions suggèrent ainsi une fréquence importante de la maladie dans la population générale. Pourtant la CMH reste relativement rare en consultation cardiologique et les cohortes de suivi de patients porteurs d’une CMH sont f inalement assez peu importantes : 247 patients inclus sur une période de 28 ans par une équipe nantaise (2) ou bien encore 225 patients suivis par le Thorax Center de Rotterdam sur la période 1970-1999 (3). 344 L’ECG vient naturellement compléter l’examen clinique et se montre souvent anormal avec quatre types d’anomalies : – une HVG électrique dans 60 % à 90 % cas avec une augmentation parfois considérable de l’amplitude des ondes R en V5, V6 ; – la présence d’ondes Q anormales, supérieures à 3 mm de profondeur pour une durée supérieure à 0,04 secondes chez 30 % à 50 % des patients, siégeant particulièrement en D2, D3, VF et V4-V6 ; – des anomalies diverses de la repolarisation ; ondes T négatives amples et profondes ou au contraire géantes et pointues ; – des troubles conductifs aspécifiques. Alors que l’ECG est rarement normal, moins de 15 % des cas, ces anomalies électriques peuvent être parfois très précoces, voire survenir avant l’existence d’une réelle p. godon hypertrophie échographique du VG chez des patients porteurs d’une mutation génétique (4). C) ÉCHOCARDIOGRAPHIE. L'échocardiographie demeure la pierre angulaire du diagnostic de CMH (fig. 1). D'autres anomalies échographiques sont fréquemment retrouvées : absence de dilatation ventriculaire indispensable au diagnostic, dilatation de l'oreillette gauche, insuff isance mitrale, anomalie du doppler mitral. Plus récemment certains auteurs (6) ont rapporté des anomalies précoces du doppler tissulaire avec effondrement des vélocités myocardiques qui pourraient être contributives lors des diagnostics difficiles. D) IMAGERIE PAR RÉSONANCE MAGNÉTIQUE (IRM). Figure 1. Aspects échographiques d’une CMH à prédominance antéroseptale. Toute anomalie auscultatoire, toute constatation d’un trouble de la repolarisation ou d’une extrasystolie, a fortiori ventriculaire, sur l’ECG doit justifier la réalisation systématique d’une échocardiographie avant de délivrer un certificat d’aptitude au service et/ou au sport. L'hypertrophie ventriculaire gauche est naturellement l'anomalie dominante. Siégeant habituellement sur le septum inter ventriculaire elle peut en revanche être plus étendue, voire diffuse ou bien au contraire localisée en des topographies inhabituelles (pointe). Maron a ainsi défini quatre types de CMH en fonction du siège de l'hypertrophie, sur la partie antérieure du septum pour le type I (10 % des cas), l'ensemble du septum pour le type II (20 %), le septum et la paroi antérolatérale pour le type III (50 %) et enfin les localisations ne touchant pas le septum antérieur pour le type IV (20 % ) (5). Pour être compatible avec le diagnostic de CMH cette hypertrophie doit être significative et dépasser 15 mm (13 mm s'il existe des cas familiaux authentifiés), sans s'accompagner de dilatation cavitaire. Cette hypertrophie peut être diff icile à mettre en évidence, ou à évaluer et il est alors essentiel de savoir renouveler l'examen, si possible par un second opérateur, avant de porter un diagnostic de CMH, tant ce diagnostic peut être lourd de conséquences. La seconde anomalie essentielle à rechercher lors de l'examen échographique est l'existence d'un obstacle à l'éjection ventriculaire gauche. Celui ci s'exprime par un mouvement anormal, systolique, de la valve antérieure mitrale (SAM) et, lors de l'analyse doppler, par une accélération du flux antérograde aortique qui prend un aspect caractéristique avec pic de vélocité télésystolique (aspect en « lame de sabre »). Ces anomalies sont ainsi le reflet d'un gradient de pression à l'intérieur du VG que l'on retrouve chez environ 1/3 des patients. diagnostic et pronostic de la cardiomyophatie hypertrophique en 2006 L'IRM n'est pas systématiquement nécessaire au diagnostic de CMH. En revanche, il peut arriver que l'échocardiographie s'avère techniquement difficile, notamment chez les patients peu échogènes. L'IRM, qui fournit toujours des images de haute résolution, peut alors contribuer aux diagnostics diff iciles, surtout lorsqu'il existe une incertitude sur les mesures d'épaisseur pariétale ou lors d'une localisation inhabituelle de l'hypertrophie (apex). Certaines séquences d'acquisition IRM (tagging) permettent par ailleurs de mettre en évidence des anomalies de contractilité segmentaire pathognomoniques de la CMH. Ces séquences trouvent tout leur intérêt lors du diagnostic différentiel avec un cœur d'athlète (7). L'IRM bénéficie ainsi actuellement d'une indication de classe II dans le diagnostic de CMH (8). E) DIAGNOSTIC GÉNÉTIQUE. L'association d'un contexte clinique, d'anomalies électriques et échographiques suffit en général à porter le diagnostic de CMH (9). La découverte d'une anomalie génétique pourrait alors conforter le clinicien dans ses hypothèses diagnostiques lorsque l'on connaît le pronostic et les conséquences parfois redoutables de la CMH. Il faut alors garder à l'esprit que le diagnostic génétique représente une analyse coûteuse (6 800 € pour l'analyse de cinq gènes) et longue (1 an minimum avant le rendu définitif des résultats) et qu'elle n'identifie une mutation, dans l'état actuel des connaissances, que chez 2/3 des patients porteurs d'une authentique CMH (10). Aussi la réalisation d'un diagnostic génétique n'est-elle recommandée que dans quatre situations : – pour un diagnostic prénatal, possible dès la 10e semaine, lorsque l'un des deux parents est porteur d'une CMH avérée avec une anomalie génétique authentifiée ; – lors d'une enquête familiale chez les apparentés d'un patient porteur d'une CMH avérée, avant que ces apparentés ne développent des anomalies électriques ou échographiques ; – à titre diagnostic lorsque les anomalies électriques ou échographiques sont ambiguës, chez un sportif par exemple ; – à titre pronostic puisque certaines mutations sont considérées comme plus à risque de mort subite. Cette indication demeure toutefois controversée en raison du trop faible nombre de travaux à ce sujet. 345 D O S S I E R V. ÉCARTER CE QUI N'EST PAS UNE CMH. VI. QUELLES EXPLORATIONS COMPLÉMENTAIRES RÉALISER DEVANT UNE CMH ? Il s'agit d'un aspect essentiel puisque les conséquences et la prise en charge peuvent être radicalement différents. Outre l'ECG et l'échocardiographie qui posent le diagnostic plusieurs examens supplémentaires peuvent être envisagés. A) MALADIES PRESSION. DE SURCHARGE DE Les maladies de surcharge de pression (rétrécissement aortique, HTA) sont en règle faciles à écarter. B) PATHOLOGIES INFILTRATIVES. Les pathologies infiltratives (amylose, hémochromatose), plus rares, s'inscrivent dans un contexte souvent évocateur qui permet de redresser le diagnostic. C) AFFECTIONS TRÈS PARTICULIÈRES. Certaines affections très particulières, syndrome de Noonan, ataxie de Friedreich, myopathies mitochondriales, comportent une hypertrophie VG s'inscrivant dans un tableau clinique tel que l'ambiguïté n'est pas permise. D) MALADIE DE FABRY. La maladie de Fabry ou déficit génétique en α galactosidase A lié au chromosome X mérite d'être évoquée chez tout adulte jeune porteur d'une HVG. L'hypertrophie, souvent homogène et symétrique s'accompagne d'acroparesthésies, d'angiokératomes et d'anomalies rénales (protéinurie, insuffisance rénale). La prévalence de cette affection en présence d'une HVG n'est pas négligeable puisqu'une récente étude fait apparaître cette anomalie chez 6 patients sur 153 étiquetés CMH (11). L'intérêt d'un tel diagnostic repose sur la possibilité de mettre en oeuvre un traitement spécif ique par enzymothérapie substitutive. A) IRM CARDIAQUE ET LE GÉNOTYPAGE. L'IRM cardiaque et le génotypage de la maladie, que nous avons abordé précédemment. B) ÉPREUVE D'EFFORT. L'épreuve d'effort, plus ou moins incontournable, permet de documenter les éventuels symptômes fonctionnels des patients (dyspnée, angor, palpitations) et de les corréler à des anomalies électriques, ischémie électrique, arythmie ventriculaire ou supraventriculaire, profil tensionnel à l'effort anormal. C) ENREGISTREMENT HOLTER DE L'ECG. L'enregistrement Holter de l'ECG sur 24 h permet d'évaluer l'existence d'arythmies asymptomatiques. Si la présence d'ESV est extrêmement banale et sans signification pathologique, en revanche la découverte de tachycardies ventriculaires non soutenues (TVNS = 3 ESV ou plus) représente un marqueur de risque rythmique de signif ication péjorative. Ainsi sur un récent travail portant sur 178 patients porteurs d'une CMH et ayant bénéf icié d'un enregistrement Holter l'existence d'une ou plusieurs salves de TVNS présente une faible valeur prédictive positive (9 %) mais une bonne valeur prédictive négative (95 %) quant au risque de mort subite (13). Tableau I. Critères distinctifs usuels entre une hypertrophie d'adaptation et une CMH chez un sujet sportif. CMH Cœur d’athlète Contexte familial oui non Anomalie ECG oui non Sexe féminin oui non Regression à l'arrêt du sport non oui Hypertrophie asymétrique oui non Diamètre télédiastolique VG<45 mm oui non Dilatation OG oui non Doppler mitral anormal oui non Anomalies doppler tissulaire oui non E) « CŒUR D'ATHLÈTE ». Le « cœur d'athlète » représente le diagnostic différentiel le plus délicat à aborder pour le médecin militaire confronté à un patient jeune et sportif porteur d'une HVG. Il convient en premier lieu de s'assurer de la réalité d'un entraînement soutenu qui doit comporter au moins dix heures d'activité hebdomadaire pour engendrer un retentissement significatif sur le muscle cardiaque. Plusieurs arguments échographiques (tab. I) permettent souvent de faire le diagnostic différentiel entre une hypertrophie physiologique, « d'adaptation » ou pathologique (12). Parfois, lorsque le doute persiste, c'est l'interruption de l'entraînement sportif pendant plusieurs mois qui, en permettant d'observer la régression de l'hypertrophie fait écarter le diagnostic de CMH. 346 p. godon D) RECHERCHE DE POTENTIELS TARDIFS. La recherche de potentiels tardifs ventriculaires n'a pas démontré d'intérêt dans l'évaluation pronostique d'une CMH. E) EXPLORATION ÉLECTROPHYSIOLOGIQUE. L'exploration électrophysiologique avec stimulation ventriculaire programmée ne permet pas, sauf indication particulière, de différencier les patients à faible risque de ceux à haut risque de complications rythmiques (14). En effet, même avec des protocoles de stimulation peu agressifs, on parvient assez facilement à déclencher une arythmie ventriculaire soutenue chez ces patients sans permettre un screening satisfaisant des patients les plus à risque. Dans le cadre du suivi d'un patient porteur d'une CMH le renouvellement de ces différentes explorations, ECG, échocardiographie, épreuve d'effort, Holter ECG, s'envisage sur un rythme annuel que l'on peut éventuellement raccourcir selon les cas. VII. COMMENT ÉVALUER LE PRONOSTIC D'UNE CMH ? Une fois les diff icultés diagnostiques résolues c'est la seconde diff iculté majeure à laquelle se heurte le clinicien. En dépit de grandes incertitudes qui demeurent en 2006 sur l'évolution individuelle de la maladie il convient en effet d'essayer de répondre du mieux possible aux interrogations du patient et de son entourage, alors que la plupart des sites Internet grand public diffusent une information focalisée essentiellement sur le risque de mort subite. A) LES COMPLICATIONS DE LA CMH SONT ESSENTIELLEMENT AU NOMBRE DE QUATRE : 1. Mort subite. La plus connue en est la mort subite dont certaines observations ont parfois défrayé la chronique. En dépit de certaines avancées cette complication majeure garde son caractère peu prévisible et représente parfois la première, et seule, manifestation de la maladie. 2. Évolution progressive vers une insuff isance cardiaque. Un mode évolutif moins connu mais tout aussi fréquent est l'évolution progressive vers une insuff isance cardiaque avec amincissement progressif des parois qui contiennent de plus en plus de fibrose, dilatation cavitaire et altération progressive de la fonction systolique. 3. Accident vasculaire cérébral ischémique. L'accident vasculaire cérébral ischémique, en raison des fréquentes arythmies, et notamment de la fibrillation atriale, reste une complication classique. diagnostic et pronostic de la cardiomyophatie hypertrophique en 2006 4. Greffe endocarditique. La greffe endocarditique sur la valve mitrale ou le septum demeure rare. B) LE PRONOSTIC GLOBAL DE LA CMH DEMEURE EN 2006 MAL CONNU. Ceci est lié pour une part à la grande hétérogénéité de la maladie avec de nombreuses formes asymptomatiques qui demeureront méconnues et, à l'inverse, certaines morts subites qui restent sans étiquette en l'absence d'autopsie. Cela explique les divergences de pronostic que l'on peut observer dans la littérature selon que les données émanent de centres de référence, avec un biais de recrutement lié à des malades souvent plus « complexes », ou qu'elles proviennent de populations moins sélectionnées. Ainsi Kofflard et al. (3) ont comparé leur propre série de patients néerlandais non sélectionnés à six séries de patients provenant de centres de référence et six séries de patients « tout venant ». Lorsque les patients sont issus de séries très sélectionnées le pronostic apparaît alors sombre avec une mortalité cardiovasculaire annuelle de l’ordre de 2 % à 4 % chez les adultes et jusqu’à 6 %/an chez les enfants. En revanche lorsque l’on étudie des patients suivis dans des centres moins spécialisés la mortalité annuelle d’origine cardiovasculaire est plus faible, entre 0 % et 1,3 % et la mortalité subite annuelle est évaluée entre 0 % et 0,7 %. Le CHU de Nantes a récemment rapporté le suivi à douze ans en moyenne d’une cohorte de 243 patients porteurs d’une CMH (2). Lors du suivi, 54 patients sont décédés dont 41 d’une cause cardiovasculaire (mortalité cardiovasculaire annuelle = 1,37 %) avec 20 morts subites, 17 décès liés à une insuff isance cardiaque, 3 accidents vasculaires cérébraux et 1 complication chirurgicale. Il apparaît donc raisonnable de considérer aujourd’hui le pronostic de la CMH comme certainement moins péjoratif que ne le laissait supposer les premières données historiques dont les conclusions reposaient sur un biais de recrutement. Il n’en demeure pas moins que la CMH n’est pas une maladie bénigne et génère incontestablement une surmortalité cardiovasculaire. Celle-ci s’exprime pour moitié par des décès subits, le plus souvent chez des patients jeunes entre 10 ans et 40 ans, et pour l’autre moitié par une insuffisance cardiaque qui survient plus tardivement vers 60 ans. C) PEUT-ON PRÉDIRE LE RISQUE DE MORT SUBITE ? La CMH parait donc désormais associée à un risque de mort subite évalué entre 0 % et 1 % par an chez l’adulte, peut-être un peu plus chez l’enfant. La prédiction de ce type de risque pour un individu donné demeure l’un des problèmes les plus difficiles posés par la maladie et l’un des aspects les plus angoissants pour le patient. Un exemple récent a mis en exergue le rôle de l’activité sportive dans la survenue d’une mort subite. Cependant celle-ci survient le plus souvent dans les efforts de 347 D O S S I E R la vie quotidienne et chez des patients peu ou pas symptomatiques. Plusieurs travaux récents ont permis d’identif ier l’existence de facteurs de risque de mort subite ce qui autorise actuellement une relative stratif ication individuelle du risque de mort subite (15) : – l’existence d’antécédents personnels ou familiaux de mort subite (au moins 2 cas avant 40 ans) ; – des syncopes répétées (au moins 2 par an) ; – une faible élévation tensionnelle lors du test d’effort (moins de 25 mm) ; – une hypertrophie myocardique supérieure à 30 mm ; – l’existence de salves de tachycardie ventriculaire non soutenue sur le Holter. Ainsi l’incidence annuelle de mort subite serait inférieure à 1 % en l’absence de facteur de risque, de 1,2 % en présence d’un facteur, 3 % en présence de 2 facteurs et 11 %/an au-delà. D’autres facteurs sont également incriminés tels que l’existence d’une ischémie à l’effort ou d’un gradient intra ventriculaire gauche mais leur importance est moins démontrée. L’épaisseur myocardique tient également une certaine place puisque dans un travail portant sur 480 patients suivis 6,5 ans (15) aucune mort subite n’est survenue chez les patients dont l’épaisseur du septum inter ventriculaire n’excédait pas 15 mm (16). Enfin le type de mutation génétique en cause pourrait également influencer le pronostic et notamment le risque de mort subite. Ainsi les altérations du gène codant la chaîne lourde de la myosine (MYH 7) ou celui de la troponine T (TNNT2) comporteraient un risque plus élevé de mort subite. Cependant, bien que l’on puisse espérer à l’avenir une meilleure stratification du risque fondée sur la génétique il n’existe pas à l’heure actuelle de données suffisantes pour accorder au type de mutation une signification pronostique précise. VIII. CONCLUSION. Responsable de morts subites chez des sujets jeunes le dépistage d’une cardiomyopathie hypertrophique demeure une priorité du Service de santé des armées. Ce dépistage demeure néanmoins encore imparfait et parfois très problématique en 2006, tout particulièrement lorsque l’on se retrouve confronté à des manifestations électriques ou échocardiographiques compatibles avec un cœur d’athlète. Le diagnostic de CMH générant une inaptitude au sport et donc, de facto, à l’engagement, toute erreur de diagnostic, par excès ou par défaut, pourra inévitablement être à l’origine de contentieux. RÉFÉRENCES BIBLIOGRAPHIQUES 1. Maron BJ, Gardin JM, Flack JM et al. Prevalence of hypertrophic cardiomyopathy in a general population of young adults. Echocardiographic analysis of 4111 subjects in the CARDIA study. Circulation 1995 ; 92 : 785-9. 2. Gueffet JP, Langlard JM, Burban M et al. Cardiomyopathie hypertrophique : évolution clinique à long terme d’une cohorte régionale de 243 patients. Arch Mal Cœur 2001 ; 94 : 967-74. 3. Kofflard MJM, Ten Cate FJ, Van der Lee C et al. Hypertrophic cardiomyopathy in a large community based population: clinical outcome and identification of risk factors for sudden cardiac death and clinical deterioration. J Am Coll Cardiol 2003 ; 41 : 987-93. 4. Ryan MP, Cleland JGF, French JA et al. The standard electrocardiogramm as a screening test for hypertrophic cardiomyopathy. Am J Cardiol 1995 ; 76 : 689-94. 5. Maron BJ, Gottdiener JS, Epstein SE. Patterns and significance of distribution of left ventricular hypertrophy in hypertrophic cardiomyopathy. 6. Nagueh SF, McFalls J, Meyer D et al. Tissue doppler imaging predicts the development of hypertrophic cardiomyopathy in subjects with subclinical disease. Circulation 2003 ; 108 : 395-8. 7. Young AA, Kramer CM, Ferrari VA et al. Three dimensional left ventricular deformation in hypertrophic cardiomyopathy. Circulation 1994 ; 9 (2) : 854-67. 8. Task Force Report. The clinical role of magnetic resonance in cardiovascular disease. Eur. Heart J 1998 ; 19 : 19-39. 9. Richard P, Charron P, Komajda M, Hainque B. Cardiomyopatie 348 10. 11. 12. 13. 14. 15. 16. hypertrophique : aspects génétiques et diagnostic moléculaire. Sang Thrombose vaisseaux 2004 ; 16 (1) : 9-15. Richard P, Charron P, Carrier L et al. Hypertrophic cardiomyopathy: distribution of disease genes, spectrum of mutations and implications for a molecular diagnosis strategy. Circulation 2003 ; 107 (17) : 2227-32. Lidove O, Joly D, Barbey F et al. La maladie de Fabry chez l’adulte : aspects cliniques et progrès thérapeutiques. Rev Med Interne 2001 ; 22 (Suppl 3) : 384-92. Pellicia A, Maron BJ, Spataro A et al. The upper limit of physiologic cardiac hypertrophy in highly trained elite athletes. N Eng J Med 1991 ; 324 : 295-301. Adabag AS, Casey SA, Kuskowski MA, Zenovich AG, Maron BJ. Spectrum and prognostic significance of arrythmias on ambulatory Holter electrocardiogramm in hypertrophic cardiomyopathy. J Am Coll Cardiol 2005 ; 45 : 697-704. Kuck KH, Kunze KP, Schluter M, Nienaber CA, Costard A. Programmed electrical stimulation in hypertrophic cardiomyopathy: Results in patients with and without cardiac arrest. Eur Heart J 1989 ; 9 : 177-85. American College of Cardiology/ European Society of Cardiology clinical expert consensus document on hypertrophic cardiomyopathy. Eur Heart J 2003 ; 24 : 1965-91. Spirito P, Bellone P, Harris KM et al. Magnitude of left ventricular hypertrophy predicts the risk of sudden death in hypertrophic cardiomyopathy. N Eng J Med 2000 ; 342 : 1777-85. p. godon Dossier « Cœur et Armées » : Divers MYOCARDITE A FORME PSEUDO-INFARCTOÏDE DU SUJET JEUNE Revue de la littérature à propos de trois observations X. ROUX, J.-M. CHEVALIER, Y.-M. GAVEAU, P. GODON, F. BIRE, R. BRION RÉSUMÉ La myocardite à forme pseudo-infarctoïde est un mode de révélation fréquent des myocardites du sujet jeune désormais bien rapporté dans la littérature. Associant une douleur thoracique d’allure coronarienne, des modifications électrocardiographiques parfois systématisées évocatrices d’ischémie et une élévation plasmatique des marqueurs cardiaques, le principal problème est celui du diagnostic différentiel avec une ischémie myocardique d’origine coronarienne dont la prise en charge et le pronostic sont radicalement différents. Le développement de nouvelles techniques d’imagerie, dominées par l’IRM, permet actuellement un diagnostic plus aisé, évitant le plus souvent de recourir à la biopsie endomyocardique qui est considérée comme l’examen de référence. Nous rapportons trois observations concernant de jeunes militaires atteints de myocardite à forme pseudo-infarctoïde avant de faire une mise au point sur cette entité clinique particulière pouvant poser des problèmes médico-militaires à court ou moyen terme. Mots-clés : Douleur thoracique. Ischémie myocardique. Myocardite. Pseudo-infarctoïde. I. INTRODUCTION. La myocardite est définie par une atteinte inflammatoire du myocarde liée le plus souvent à un processus infectieux dont l’origine virale prédomine largement. Son expression clinique est variable : défaillance cardiaque aiguë fébrile, tableau de douleurs péricardiques ou parfois, mort subite dramatique chez un jeune en apparente bonne santé. La révélation d’une myocardite mimant cliniquement, électriquement et biologiquement une ischémie myocardique appelée également forme pseudoX. ROUX, lieutenant, praticien en formation. J.-M. CHEVALIER, médecin chef des services, praticien certifié. Y.-M. GAVEAU, lieutenant, praticien en formation. P. GODON, médecin en chef, praticien certifié. F. BIRE, médecin en chef, praticien certifié. R. BRION, médecin chef des services, praticien certifié. Correspondance : X. ROUX, Service de cardiologie, HIA Robert Picqué, BP 28, 33998 Bordeaux Armées. médecine et armées, 2006, 34, 4 ABSTRACT MYOCARDITIS MIMICKING MYOCARDIAL INFARCTION IN THE YOUNG : REVIEW OF THE LITERATURE ABOUT THREE CASES REPORTS. Myocarditis mimicking acute myocardial infarction is a useful clinical aspect of myocarditis of the young, well reported in the literature. This entity join a coronary-like chest pain, electrocardiographic abnormality and elevated cardiac enzyme and the main difficult is the differential diagnosis with an acute coronary syndrom because treatment is different. The developpement of new imaging technologies, particulary the Magnetic Resonance Imaging, allows an easier diagnosis and often ovoid endomyocardial biopsy, which is the gold standard. We report three cases of young military recruits with myocarditis mimicking acute myocardial infarction and a review of the literature about this clinical entity which can have a medico-military consequences in short or middle-long term. Keywords : Chest pain. Myocardial infarction. Myocarditis. (Médecine et Armées, 2006, 34, 4, 349-354) infarctoïde, est une présentation classique et désormais bien rapportée dans la littérature. Il semble également que ce mode de révélation soit plus fréquent chez les hommes jeunes, expliquant qu’un certain nombre de séries soit issues des forces armées françaises ou étrangères. Nous rapportons trois observations d’hommes jeunes ayant présenté une myocardite aiguë à forme pseudo-infarctoïde. Après analyse de leurs caractéristiques cliniques et paracliniques, nous ferons une mise au point sur cette entité clinique qui est loin d’être exceptionnelle. II. OBSERVATIONS. Voici trois observations de jeunes militaires ayant consulté dans les Hôpitaux d’instruction des armées (HIA) de Lyon ou de Bordeaux (1). 349 D O S S I E R A) OBSERVATION N° 1. Il s’agit d’un homme, âgé de 22 ans, consultant pour des douleurs thoraciques évoluant depuis 24 heures. Ces douleurs sont medio thoraciques, irradiant dans le bras droit et évoluant dans un contexte fébrile. Les facteurs de risque cardiovasculaire du patient sont un tabagisme modéré à cinq cigarettes par jour et un antécédent familial d’infarctus du myocarde à l’âge de 40 ans. L’examen physique du patient est sans particularité si ce n’est une fièvre à 38,5 °C. L’électrocardiogramme (ECG) retrouve un sus-décalage en DI, aVL et de V2 à V6. La biologie met en évidence une ascension des marqueurs cardiaques (troponine Ic à 34,4 µg/L) associée à un syndrome inflammatoire (CRP > 96 mg/L). Une échographie transthoracique (ETT) révèle une hypokinésie apicale localisée sans altération de la fonction ventriculaire gauche mais avec une petite lame d’épanchement péricardique. Une imagerie par résonance magnétique (IRM) cardiaque confirme le diagnostic de myocardite et l’épreuve d’effort à quinze jours, maximale, est négative avec une quasinormalisation de l’ECG de base. Le patient ressort de l’hôpital asymptomatique sous acide acétylsalicylique (Aspégic®) prescrit à doses anti-inflammatoires. L’étiologie virale, suspectée, n’a pu être mise en évidence. B) OBSERVATION N° 2. Il s’agit d’un homme, âgé de 21 ans, appelé du contingent, consultant pour des douleurs medio thoraciques intenses, sans irradiation, dans un contexte d’asthénie fébrile. Il rapporte quinze jours auparavant un épisode de rhino-pharyngite spontanément résolutif. L’examen physique retrouve une tachycardie à 100 battements par minute avec une tension artérielle à 120/80 sans signe de décompensation cardiaque. L’électrocardiogramme montre un sus-décalage du segment ST plutôt diffus sans image en miroir. La biologie montre une élévation des CPK et LDH avec également une CRP augmentée (55 mg/L) L’ETT réalisée est normale. Les symptômes disparaissent sous acide acétylsalicylique (Aspégic®) trois grammes par jour et le patient est asymptomatique à un mois avec épreuve d’effort négative. L’enquête étiologique est restée négative. Figure 1. Électrocardiogramme initial de l'observation N° 3 : sus-décalage du segment ST de V3 à V6 ainsi qu'en inférieur. d’anomalies sur le réseau coronaire. L’IRM est non contributive. À un mois, le patient est revu, asymptomatique, avec amélioration de l’ECG (fig. 2) et de l’ETT. Aucune étiologie n’est retrouvée. III. DISCUSSION. Ces trois observations de jeunes patients atteints de myocardite illustrent un mode de présentation classique qu’est la forme pseudo-infarctoïde. Cette entité clinique pose le difficile problème de son diagnostic différentiel que sont les syndromes coronariens aigus pour lequel tout retard diagnostic doit être évité. A) PHYSIOPATHOLOGIE. La myocardite est une atteinte inflammatoire du muscle cardiaque quelqu’en soit la cause (1, 2). Elle se caractérise histologiquement par un inf iltrat inflammatoire, de l’œdème, des foyers de nécrose et de la fibrose en proportion variable (3). Son origine est le plus souvent infectieuse et notamment virale dans la majorité des cas. La multiplicité des agents potentiellement en causes (virus, bactéries, parasites…) rend l’enquête étiologique exhaustive quasiment impossible et explique le nombre important de myocardite dite « idiopathique » pour lesquelles aucun agent infectieux précis n’a pu être identifié (4). L’atteinte myocardique est secondaire à deux mécanismes principaux : cytotoxicité directe de l’agent infectieux et réaction immunitaire à l’encontre des cellules cardiaques pouvant entraîner des phénomènes inflammatoires C) OBSERVATION N° 3. Il s’agit d’un homme, âgé de 26 ans, hospitalisé pour une douleur thoracique typiquement angineuse paroxystique alors que celui-ci est traité par macrolides depuis trois jours pour une angine. L’unique facteur de risque cardiovasculaire rapporté par le patient est un tabagisme actif évalué à cinq paquets-année. L’examen physique d’entrée est strictement normal. L’ECG initial retrouve un sus-décalage du segment ST de V3 à V6 ainsi qu’en inférieur, sans miroir (fig. 1). La biologie montre une élévation de la troponine Ic (16 µg/L) et de la myoglobine associée à une CRP à 118 mg/L. Une ETT retrouve une contraction inhomogène dans le territoire inférieur. Une coronarographie diagnostique ne retrouve pas 350 Figure 2. Électrocardiogramme à un mois : disparition du sus-décalage avec apparition secondaire d'ondes T négatives en inférieur et V5-V6. x. roux persistants responsables des complications chroniques (cardiomyopathies dilatées) (5). L’atteinte inflammatoire myocardique peut être ainsi responsable : – d’une défaillance cardiaque aiguë, allant de la simple hypotension au choc cardiogénique rapidement progressif ; – de troubles de conduction par inflammation du tissu conductif avec bloc de conduction auriculo-ventriculaire (BAV) ou intra ventriculaire ; – de troubles du rythme aux deux étages ; – d’une symptomatologie douloureuse, soit par une atteinte péricarditique fréquemment associée donnant une symptomatologie volontiers positionnelle, soit par la souffrance myocardique mimant une douleur angineuse responsable des formes pseudo-infarctoïdes ; – d’anomalies biologiques, électrocardiographiques et échographiques, variables selon les cas. B) ÉPIDÉMIOLOGIE. Bien que son incidence ne soit pas connue avec certitude en raison des diff icultés diagnostiques des formes atypiques et d’un nombre important de formes asymptomatiques, la myocardite est estimée aux alentours de 1,06 % selon une série autopsique suédoise (4). Celle-ci est bien documentée comme cause de mort subite chez le sujet jeune avec des fréquences variant de 10 % à 20 % des causes de décès d’origine cardiaque chez les jeunes recrues militaires (6-11). Cette incidence élevée chez les jeunes militaires semble liée à une plus grande promiscuité (favorisant la transmission des agents infectieux) associé à une exposition accrue aux exercices physiques intenses (facteur potentiellement aggravateur ou révélateur de myocardite) (12). La forme pseudo-infarctoïde mimant une atteinte coronarienne semble être un mode de révélation fréquent notamment chez le sujet jeune. Une série finlandaise portant sur une population de 672 672 jeunes militaires montre que la majorité des 98 myocardites se présentait avec une forme pseudo-infarctoïde (13) lorsqu’ils étaient symptomatiques. C) CLINIQUE. La myocardite, quand elle est symptomatique, peut se révéler sous différentes formes : insuffisance cardiaque aiguë fébrile, mort subite, troubles du rythme… (14). La forme pseudo-infarctoïde est définie par la triple association : – d’une douleur thoracique d’allure angineuse (rétro sternale, oppressive, parfois irradiante…) ; – de modification électrocardiographique évoquant une atteinte ischémique (cf. infra) ; – d’anomalies biologiques avec augmentation plasmatique des marqueurs cardiaques. Le terrain est souvent celui d’un sujet de sexe masculin, d’âge jeune, avec pas ou peu de facteurs de risque cardiovasculaire (15). myocardite à forme pseudo-infarctoïde du sujet jeune Sur le plan des douleurs, celles-ci sont le plus souvent rétro sternales, avec parfois des irradiations classiques d’atteinte coronarienne (bras gauche, maxillaire inférieur) comme cela est le cas chez le patient N° 1. Son caractère oppressant est régulièrement retrouvé. Des douleurs positionnelles ou majorées à l’inspiration profonde sont parfois présentes évoquant une atteinte péricarditique ou pleurale. L’examen physique est le plus souvent normal, mais peut retrouver des signes d’insuff isance cardiaque. Un frottement péricardique est parfois audible à l’auscultation (16). Les signes généraux bien que fréquents, sont inconstants avec l’existence d’une fièvre souvent modérée lorsqu’elle est présente (38-38,5°), une asthénie inconstante, rarement une franche altération de l’état général. Des signes extra cardiaques peuvent être présents, en relation avec l’agent causal : rash cutané, érythème migrant (maladie de Lyme), énanthème buccal, adénopathies cervicales… Le plus souvent, ces signes précèdent l’épisode de myocardite de quelques jours et une infection d’allure virale préalable est évocatrice du diagnostic, bien que présente moins d’une fois sur deux (17). D) PARACLINIQUE. 1. Biologie. Celle ci montre plusieurs anomalies : – anomalies non spécifiques, en rapport avec le syndrome inflammatoire lié à l’agent infectieux en cause : élévation de la CRP dans plus de la moitié des cas (17) souvent modérée, parfois plus importante, hyperleucocytose à prédominance lymphocytaire ou de polynucléaires neutrophiles selon l’étiologie (virale, bactérienne) ou quelquefois un syndrome mononucléosique franc (18) ; – anomalies spécif iques avec l’augmentation des marqueurs cardiaques. Il existe une augmentation des CPK et de la myoglobine, en règle modérée mais parfois très élevée, et de la troponine I ou T, plus spécifique d’une atteinte myocardique. La spécificité de la cinétique des marqueurs biologiques dans la myocardite reste controversée. Le « Brain natriuretic peptid » (BNP) est fréquemment augmenté dans les myocardites, témoin d’une insuffisance cardiaque associée. Bien que peu spécifique de la myocardite, il peut être intéressant pour mettre en évidence une atteinte myocardique dans un tableau typique de péricardite lorsque le dosage de troponine est normal (19). 2. Électrocardiogramme. Les anomalies électrocardiographiques observées sont, par définition, évocatrices d’une ischémie myocardique, parfois fluctuantes dans le temps. Le plus souvent, il s’agit d’une élévation du segment ST de plus d’un millimètre dans au moins deux dérivations qui se suivent avec un miroir possible, mais en règle absent. 351 D O S S I E R Il peut y avoir également un sous décalage du ST, des ondes Q pathologiques. Ces anomalies peuvent siéger en antérieur, en inférieur et des anomalies diffuses sont également possibles (13). Les formes avec ondes Q seraient de moins bon pronostic car plus fréquemment associées à une évolution fulminante (20). Des troubles du rythme sont rapportés en période aiguë avec des extrasystoles auriculaires, ventriculaires et parfois de véritables tachycardies ventriculaires engageant le pronostic vital. Des troubles de la conduction comme des blocs de branche sont décrits, plus rarement des blocs auriculo-ventriculaires parfois complets. Ces anomalies, liées à l’inflammation, tendent à disparaître en quelques jours mais peuvent persister dans le temps en cas de fibrose cicatricielle (16). 3. Échographie. L’échographie cardiaque est peu spécif ique dans la myocardite et permet surtout une évaluation rapide de la fonction ventriculaire gauche, globale et segmentaire. Des anomalies de la cinétique segmentaire sont souvent mises en évidence sans prédilection particulière pour un territoire donné. L’échographie peut également mettre en évidence une atteinte péricardique fréquemment associée, montrant un épanchement péricardique généralement modéré. 4. Autres examens d’imagerie. La scintigraphie et l’IRM myocardiques permettent d’évoquer fortement une myocardite dans le cadre d’un syndrome douloureux thoracique. La scintigraphie myocardiaque, pas toujours facile d’accès et de moins en moins pratiquée, consiste en l’injection d’anticorps anti-myosines marqués à l’indium 111 avant acquisition des images. Cet examen montre bien les zones de nécrose et, couplé à une scintigraphie traditionnelle au thallium, aurait une bonne sensibilité et spécificité dans le diagnostic de myocardite, notamment dans les formes pseudo-infarctoïdes. (21-24). L’IRM connaît un développement important dans le domaine de la cardiologie et semble présenter un intérêt dans les myocardites aiguës (25). Celle ci met en évidence de multiples foyers inflammatoires fixant le gadolinium au temps tardif de topographie le plus souvent sous épicardique. Elle permet une bonne discrimination entre inflammation myocardique et atteinte d’origine ischémique. E) DIAGNOSTIC. Le diagnostic positif de la myocardite repose sur l’étude histopathologique issue des fragments de biopsie endomyocardique. La conf irmation repose sur les critères de Dallas édité en 1987 (26). Cependant, la biopsie manque de spécificité et de sensibilité compte tenu de l’existence de zones myocardiques saines entre les foyers de nécrose responsables de faux négatifs. Son caractère invasif et les risques qui lui sont 352 associés ainsi que le peu de bénéfice attendu explique sa faible utilisation (27-30). Le diagnostic positif est donc le plus souvent porté sur un faisceau d’arguments cliniques et paracliniques où l’imagerie non invasive (IRM) prend une place croissante. Dans les formes pseudo-infarctoïdes, le principal diagnostic différentiel est celui d’un syndrome coronarien aigu et notamment d’un authentique infarctus qui nécessiterai des gestes de revascularisation en urgence. À ce titre, toute suspicion clinique d’atteinte coronarienne devant un tableau atypique (absence de fièvre, de syndrome inflammatoire) ou traînant doit faire pratiquer une coronarographie diagnostique dans les meilleurs délais. La péricardite provoque plutôt une symptomatologie positionnelle, avec des anomalies ECG diffuses parfois évocatrice (anomalies du PQ, sus-décalage concave vers le haut…) et ne s’accompagne pas d’une élévation des marqueurs cardiaques. Rappelons que les deux entités, relativement proches, peuvent être associées. Les cardiomyopathies de stress et notamment le syndrome de tako-tsubo peuvent simuler en tout point une myocardite lorsqu’elles surviennent dans un contexte infectieux (sepsis, infection sévère…). Le diagnostic est souvent porté sur l’aspect caractéristique du ventricule gauche à la ventriculographie montrant une ballonisation de tout l’apex de celui-ci avec normalité du réseau coronarien. Les autres diagnostics différentiels sont ceux de toute douleur thoracique aiguë : embolie pulmonaire, dissection aortique… à évoquer systématiquement. F) COMPLICATIONS. Les complications possibles des myocardites à forme pseudo-infarctoïde sont celles de toute myocardite. Les complications de la phase aiguë sont dominées par l’insuffisance cardiaque et les troubles du rythme et/ou conductifs. L’insuffisance cardiaque gauche ou globale peut être d’installation rapidement progressive, voir fulminante, conduisant parfois à un état de choc nécessitant un traitement rapide. Les troubles du rythme sont possibles au niveau supra ventriculaire avec extrasystoles, épisodes de f ibrillation auriculaire, tachysystolie. Les troubles du rythme ventriculaire (tachycardie ventriculaire, fibrillation ventriculaire) engagent le pronostic vital et seraient responsables d’une partie des morts subites observées chez le sujet jeune (31, 32). Les troubles de conduction sont classiques avec notamment l’apparition de bloc auriculo-ventriculaire parfois complet nécessitant une électrostimulation transitoire. Les blocs intraventriculaires (droit ou gauche) sont rarement symptomatiques. Les complications à long terme sont essentiellement représentées par la myocardiopathie dilatée. Il est maintenant clairement établi qu’un certain nombre de myocardiopathies dilatées idiopathiques sont secondaire à un épisode ancien de myocardite, symptomatique ou x. roux non (33, 34). Cette évolution reste imprévisible mais il semblerait que les formes pseudo-infarctoïdes soient un facteur protecteur (16, 18). La physiopathologie de cette évolution n’est que partiellement élucidée et ferait intervenir des mécanismes d’auto-immunité liés a la persistance d’antigènes viraux (3, 35-37). La relation entre myocardite et atteinte coronarienne est rarement observée mais pose un réel problème diagnostique dans les formes pseudo-infarctoïdes. Quelques cas de thromboses coronariennes (septale) ont été rapportés (38). Un mécanisme de vasospasme est aussi décrit (39). G) TRAITEMENT. Le traitement des myocardites à forme pseudoinfarctoïde ne présente pas de spécificité particulière si ce n’est le traitement de la douleur, souvent intense, qui ne doit pas être négligé. L’aspirine à dose anti-inflammatoire (un gramme trois fois par jour) est parfois utilisée par analogie avec la péricardite sans que son innocuité soit démontrée dans l’évolution des lésions myocardiques (40). L’utilisation de traitements immunosuppresseurs ou immunomodulateurs n’ont pas fait la preuve de leur efficacité mises à part pour quelques rares étiologies : myocardite des connectives, à cellules géantes… (41). La prise en charge de l’insuff isance cardiaque, des troubles du rythme ou de conduction ne présente pas de particularité. Le traitement de l’agent infectieux est rarement possible en dehors des causes bactériennes, fongiques ou parasitaires (42). En effet, l’agent viral en cause est rarement identifié et il n’existe bien souvent pas de traitement antiviral validé. Toute myocardite diagnostiquée doit entraîner la suspension des activités sportives pour une durée qui n’est pas codifiée mais qui devrait être de l’ordre de trois mois (9). H) ÉVOLUTION/PRONOSTIC. L’évolution classique habituelle des myocardites est la récupération ad integrum d’une fonction cardiaque normale avec disparition des symptômes, comme chez nos trois patients, une fois la phase aiguë passée. Ce bon pronostic varie en fonction de l’étiologie et un pronostic sévère et souvent défavorable s’observe dans certains types histologiques (myocardite à cellules géantes) (43). Cependant, un certain nombre de patients vont évoluer secondairement vers une cardiomyopathie dilatée d’installation progressive pouvant se révéler plusieurs années après l’épisode aigu (33-36). La nécessité d’une surveillance clinique et échocardiographique à distance de l’épisode aigu doit être expliquée au patient. IV. CONCLUSION. La myocardite aiguë à forme pseudo-infarctoïde est un mode de révélation classique des myocardites du sujet jeune. Bénéficiant des progrès récents de l’imagerie médicale, son diagnostic est devenu plus aisé mais reste parfois difficile dans les formes atypiques. La volonté de ne pas passer à côté d’une atteinte coronarienne doit être une préoccupation pour le clinicien. Le recours à des explorations complémentaires comme l’IRM, voire la coronarographie, s’impose en cas de doute diagnostique. Rarement confirmée par une biopsie, son traitement repose essentiellement sur la gestion des complications à la phase aiguë, l’exemption de toute activité physique intense pour une durée prolongée et un suivi ultérieur régulier. L’application du dogme « pas de sport en période fébrile » reste essentielle dans les unités. RÉFÉRENCES BIBLIOGRAPHIQUES 1. Gaveau YM. Myocardite aiguë du sujet jeune : à propos de six cas et revue de la littérature. Lyon : université Claude Bernard-Lyon I ; 2006 : 64 p. 2. Richardson P, McKenna WJ, Bristow M, Maisch B, Mautner B, O'Connell J et al. Report of the 1995 WHO/ISFC task force on the definition of cardiomyopathy. Circulation 1996 ; 93 : 841-2. 3. Calabrese F, Thiene G. Myocarditis and inflammatory cardiomyopathy : microbiological and molecular biological aspects. Cardiovasc Research 2003 ; 60 : 11-25. 4. Friman G, Wesslen L, Fohlman J, Karjalainen J, Rolf C. The epidemiology of infectious myocarditis, lymphocytic myocarditis and dilated cardiomyopathy. Eur Heart J 1995 ; 16 : 36-41. 5. Matsumori A, Yamada T, Suzuki H, Matoba Y, Sasayama S. Increased circulating cytokines in patients with myocarditis and cardiomyopathy. Br Heart J 1994 ; 72 : 561-6. 6. Wisten A, Forsberg H, Krantz P, Messner T. Sudden cardiac death in 15-35-year olds in Sweden during 1992-1999. J Int Medicine 2002 ; 252 : 529-36. 7. Eckart R, Scoville S, Campbell C, Shry E, Stajduhar K, Potter R myocardite à forme pseudo-infarctoïde du sujet jeune 8. 9. 10. 11. 12. 13. and al. Sudden death in young adults : a 25-year review of autopsies in military recruits. Ann Internal Med 2004 ; 141 (11) : 829-34. Phillips M, Robinowitz M, Iggins J, Boran K, Reed T, Virmani R. Sudden cardiac death in air force recruits. JAMA 1986 ; 256 (19) : 2 696-9. Wesslen L, Pahlson C, Lindquist O, Hjelm E, Gnarpes J, Larsson and al. An increase in sudden unexpected cardiac deaths among young Swedish orienteers during 1979-1992. Eur Heart J 1996 ; 17 : 902-10. Balady G. Sudden cardiac death in young military recruits : guarding the heart of a soldier. Ann Internal Med 2004 ; 141 (11) : 882-4. Basso C, Corrado D, Thiene G. Cardiovascular causes of sudden death in young individuals including athletes. Cardiology in Review 1999 ; 7 (3) : 127-34. Friman G. The incidence and epidemiology of myocarditis. Eur Heart J 1999 ; 20 : 1 063-5. Karjalainen J, Heikkila J. Incidence of three presentations of acute 353 D O S S I E R 14. 15. 16. 17. 18. 19. 20. 21. 22. 23. 24. 25. 26. 27. myocarditis in young men in military service : a 20-year experience. Eur Heart J 1999 ; 20 : 1 120-5. Carniel E, Sinagra G, Bussani R, Di Lenarda A, Pinamonti B, Lardieri G et al. Fatal myocarditis : morphologic and clinical features. Ital Heart J 2004 ; 5 (9) : 702-6. Costantini M, Tritto C, Licci E, Sticchi G, Capone S, Montinaro Aet al. Myocarditis with ST-elevation myocardial infarction presentation in young man. A case series of 11 patients. Int J Cardiol 2005 ; 101 : 157-8. Dec GW, Waldman H, Southern J, Fallon J, Hutter A, Palacios I. Viral myocarditis mimicking acute myocardial infarction. J Am Coll Cardiol 1992 ; 20 : 85-9. Sarda L, Colin P, Boccara F, Daou D, Lebtahi R, Faraggi M et al. Myocarditis in patients with clinical presentation of myocardial infarction and normal coronary angiograms. J Am Coll Cardiol 2001 ; 37 : 786-92. Talard P, Bouchiat C, Bonal J, Houplon P, Vahdat B, Dussarat GV. Les myocardites à début pseudo-infarctoïde. Ann Cardiol Angéol 1993 ; 42 (8) : 419-26. Grabowski M, Karpinski G, J Filipiak K, Rdzanek A, Pietrasik A, Wretowski D et al. Diagnostic value of BNP in suspected perimyocarditis: a preliminary report. Kardiol Pol 2004; 61 (11): 451-8. Morgera T, Di Lenarda A, Dreas L, Pinamonti B, Humar F, Bussani R et al. Electrocardiography of myocarditis revisited : clinical and prognostic signifiance of electrocardiographic changes. Am Heart J 1992 ; 124 (2) : 455-67. Narula J, Khaw BA, Dec W, Palacios IF, Southern JF, Fallon JT et al. Brief report : recognition of acute myocarditis masquerading as acute myocardial infarction. N Engl J Med 1993 ; 328 : 100-4. Dec GW, Palacios IF, Yasuda T, Fallon J, Khaw B, Strauss H et al. Antoimyosin antibody cardiac imaging : its role in the diagnosis of myocarditis. J Am Coll Cardiol 1990 ; 16 : 97-104. Narula J, Khaw BA, Dec W, Palacios I, Newell J, Southern J et al. Diagnostic accuracy of antimyosin scintigraphy in suspected myocarditis. J Nucl Cardiol 1996 ; 3 : 371-81. Lambert K, Isaac D, Hendel R. Mmasquerading as ischemic heart disease : the diagnostic utility of antimyosin imaging. Cardiology 1993 ; 82 : 415-22. Laissy JP, Hyafil F, Feldman LJ, Juliard JM, Schouman-Claeys E, Steg PG et al. Differentiating acute myocardial infarction from myocarditis : diagnostic value of early-and delayed-perfusion cardiac MR imaging. Radiology 2005 ; 237 (1) : 75-82. Aretz HT, Billingham ME, Edwards WD, Factor S, Fallon J, Fenoglio J et al. Myocarditis : a histologic definition and classification. Am J Cardiovasc Pathol 1987 ; 1 (1) : 3-14. Chow LH, Radio SJ, Sears TD, McManus BM. Insensitivity of right endomyocardial biopsy in the diagnosis of myocarditis. J Am 354 Coll Cardiol 1989 ; 14 : 915-20. 28. Davidson CJ, Fishman RF, Bonow RO. Cardiac catheterization. In : Braunwald E, editor. Heart Disease. Philadelphia : WB Saunders 1997 : 1 202-4. 29. Billingham MB. Acute myocarditis : a diagnostic dilema. Br Heart J 1997 ; 58 : 6-8. 30. Hauck AJ, Kearnez DL, Edwards WD. Evaulation of post-mortem endomyocardial biopsy specimen from 38 patients with lymphocytic myocarditis : implications for role of sampling error. Mayo Clin Proc 1989 ; 64 : 1 235-45. 31. Corrado D, Basso C, Thiene G. Sudden cardiac death in young people with apparently normal heart. Cardiovascular Research 2001 ; 50 : 399-408. 32. Theleman K, Kuiper J, Robert W. Acute myocarditis (predominately lymphocytic) causing sudden death without heart failure. Am J Cardiol ; 88 : 1 078-83. 33. Dec GW, Palacios I, Fallon J, Aretz HT, Mills J, Lee D et al. Active myocarditis in the spectrum of acute dilated cardiomyopathy : clinical features, histological correlates, and clinical outcome. N Engl J Med 1985 ; 312 (14) : 885-90. 34. Brown C, O’Connell J. Myocarditis and idiopathic dilated cardiomyopathy. Am J Med 1995 ; 99 : 309-14. 35. Kawai C. From myocarditis to cardiomyopathy : mechanisms of inflammation and cell death. Circulation 1999 ; 99 (8) : 1 091-100. 36. Takata S, Nakamura H, Umemoto S, Yamaguchil K, Sekine T, Kato T et al. Identification of autoantibodies with the corresponding antigen for repetitive coxsackie virus infectioninducted cardiomyopathy. Circ J 2004 ; 68 : 677-82. 37. Why H, Meany B, Richardson P, Olsen E, Bowles N, Cunningham L et al. Clinical and prognostic signifiance of detection of enteroviral RNA in the myocardium of patients with myocarditis or dilated cardiomyopathy. Circulation 1994 ; 89 : 2 582-9. 38. Spodick DM. Infection and infarction. Am J Med 1986 ; 81 : 661-8. 39. Diamond TM, Lotzof P, Zlady F. Acute myocardial infarction with normal coronary arteries viral myopericarditis and possible coronary vasospasm. S Afr Med J 1985 ; 67 : 892-4. 40. Constanzo-Nordin M, Reap E, O’Connell J, Robinson J, Scanlon P. A nonsteroid anti-inflammatory drug exacerbates Coxsakie B3 murine myocarditis. J Am Coll Cardiol 1985 ; 6 : 1 078-82. 41. Mason J, O’Connell J, Herskowitz A, Rose N, MacManus B Billingham M et al. A clinical trial of immunosuppressive therapy for myocarditis. N Engl J Med 1995 ; 333 : 269-75. 42. Murcia J, Reus S, Climent V, Manso M, Lopez I, Tello A. Acute myocardial failure in a young man : Q-Fever myocarditis. Rev Esp Cardiol 2002 ; 55 : 875-7. 43. Cooper L. Giant Cell Myocarditis : diagnosis and treatment. Herz 2000 ; 25 (3) : 291-7. x. roux Dossier « Cœur et Armées » : Divers INTÉRÊT DU SCANNER DANS LA MALADIE CORONAIRE O. GUIRAUDET, L. BONNEVIE, P. MARION, B. BOYER, D. MARTIN, X. CHANUDET RÉSUMÉ Le scanner prend une place croissante dans la prise en charge de la maladie coronaire. Le score calcique, largement utilisé en Amérique du Nord et dont l’utilisation se développe en Europe, permet une quantification des calcifications artérielles coronaires. Ces dernières sont un marqueur habituel de l’athérosclérose coronaire. Cette quantification présente une valeur diagnostique intéressante dans la maladie coronaire, la valeur prédictive négative d’un score nul permettant pratiquement d’éliminer la maladie. Surtout, la valeur pronostique forte, graduée, indépendante du score calcique est utilisée pour établir une stratification du risque coronaire. Le coro-scanner réalise une coronarographie non invasive. La nécessité de résolutions élevées impose l’utilisation de multi coupe (si possible au moins 64), et rend compte de la nécessité, en pré-requis, d’une fréquence cardiaque non accélérée et si possible régulière. Les calcifications coronaires sont un facteur limitant du coro-scanner, à l’origine de la grande majorité des artéfacts. La précision diagnostique progresse, expliquant son utilisation en pratique clinique par de nombreuses équipes chez les patients à niveau de risque pré test peu élevé ou intermédiaire. En analyse per-patient, la valeur diagnostique se rapproche de celle de la coronarographie conventionnelle. Mots-clés : Calcification artérielle coronaire. Coronarographie. Maladie coronaire. Scanner. Score calcique. ABSTRACT INTEREST OF COMPUTED TOMOGRAPHY IN CORONARY ARTERY DISEASE. Computed tomography takes an increasing place in coronary artery disease. Calcium scoring, widely used in North America and progressing in Europe, allows a quantification of coronary artery calcifications which are a usual marker for coronary atherosclerosis. This quantification presents an interesting diagnostic value in coronary artery disease, the negative predictive value of a null score virtually ruling out the disease. Especially, the strong, graduated, independent prognostic value of calcium scoring is used to establish a stratification of the coronary risk. The multi-slice computed tomography coronary angiography carries out a non-invasive coronarography. The need for high resolutions imposes the use of a recent multi-slice device (if possible at least 64 slices), and accounts for the need, as a prerequisite, of a non-elevated heart rate, if possible regular. Coronary calcifications are a limiting factor of multi-slice computed tomography coronary angiography, at the source of the large majority of pitfalls. The diagnostic accuracy is improving, which accounts for its use in clinical practice by many teams on patients with a relatively low or intermediate pre test risk level. In per-patient analysis, the diagnosis accuracy approaches the high standard of conventional coronarography. Keywords: Calcium scoring. Coronary artery calcification. Coronary artery disease. Multi-slice computed tomography coronary angiography. (Médecine et Armées, 2006, 34, 4, 355-359) I. INTRODUCTION. Pandémie responsable de la première cause de mortalité dans le monde, la maladie coronaire est très insidieuse, puisqu’environ la moitié des infarctus du myocarde et des morts subites sont inauguraux. Actuellement certaines O. GUIRAUDET, médecin en chef, praticien certifié. L. BONNEVIE, médecin en chef, professeur agrégé. P. MARION, médecin en chef, praticien certifié. B. BOYER, médecin chef des services, professeur agrégé. D. MARTIN, médecin chef des services, praticien certifié. X. CHANUDET, médecin chef des services, professeur agrégé. Correspondance : O. GUIRAUDET, Service de cardiologie et médecine vasculaire, HIA Bégin, 69 avenue de Paris, 00498 ARMÉES. médecine et armées, 2006, 34, 4 associations de facteurs de risque, comme le syndrome métabolique, sont en pleine expansion. Les différentes sociétés savantes (American Heart Association (AHA), European Society of Cardiology) insistent actuellement sur l’importance d’un dépistage précoce des sujets à risque intermédiaire ou à haut risque. Le calcium est un composant facultatif mais habituel de l’athérome et constitue un marqueur de l’athérosclérose coronaire, notamment infra-clinique. Le coro-scanner, en progression constante, gagne en précision diagnostique ; il est déjà utilisé par beaucoup d’équipes en routine, dans certaines indications, en remplacement de la coronarographie conventionnelle. 355 D O S S I E R II. LIMITES DES MÉTHODES ACTUELLES. Une méthode de dépistage doit être non invasive, valide, précise, facilement applicable et acceptable, non génératrice d’effets indésirables (1). Celles actuellement disponibles concernant la maladie coronaire sont limitées. Les recommandations de l’AHA de 2002 concernant la pratique de l’ECG d’effort comportent une stratif ication pré-test du niveau de risque, éventuellement facilitée grâce à l’émergence de facteurs de substitution comme l’épaisseur intima média ou l’index de pression systolique. L’indication reste de classe II b chez le sujet asymptomatique, en cas de facteurs de risque multiples ou de maladie vasculaire non coronaire connue, de classe III sinon. La sensibilité est voisine de 50 % et la spécificité de 90 % (2). Échographie de stress et scintigraphie myocardique, plus performantes, sont indiquées en cas de non faisabilité de l’ECG d’effort pour la première ; la deuxième, à l’origine d’une irradiation (10 à 15 mSv), est de plus relativement coûteuse (372 € si négative et 672 € avec la réinjection de repos en cas de positivité ; l’échographie de stress est non cotée, habituellement assimilée à une échocardiographie trans-thoracique, donc d’un montant d’environ 100 €, l’ECG d’effort coûte pour sa part environ 80 €). Compte tenu des limites des méthodes non invasives actuellement disponibles force est de souvent recourir à la coronarographie, qui reste le gold-standard La maladie coronaire est en pratique définie angiographiquement par la présence d’athérome, non sténosant pour des lésions inférieures à 50 % de perte de diamètre sur deux incidences orthogonales, sténosant au delà, réalisant alors la maladie coronaire chronique. De plus c’est la seule méthode diagnostique du spasme coronarien. Cependant, la coronarographie répond mal au pré-requis d’une méthode de dépistage : elle reste (faiblement) invasive, à l’origine d’une irradiation (2 à 4 mSv), nécessite l’injection de produit de contraste, est coûteuse (environ 300 €), de plus elle image le flux et la lumière mais méconnaît l’évaluation de la paroi, comme en témoigne l’échographie endo-coronaire. Or on connaît actuellement l’importance des lésions intermédiaires dans la genèse des accidents coronariens. III. APPORT DU SCANNER CARDIAQUE. C’est une méthode d’imagerie en coupes développée depuis 1990 pour la tomographie par faisceau d’électrons (qui n’est plus utilisée en France car trop coûteuse, trop spécifique et actuellement dépassée par son concurrent) et 1999 pour le multi-détecteur. L’apport de ce dernier est proportionnel au niveau de progression technologique et informatique le concernant, notamment pour le coro-scanner. En effet, les impératifs associés de résolution spatiale, temporelle et de contraste sont une gageure pour imager l’athérosclérose coronaire. Actuellement les 64 coupes permettent l’acquisition volumique de l’ensemble du massif cardiaque en moins de 12 secondes, avec une épaisseur de coupe infra millimétrique (0,6mm), 356 un temps de rotation du statif de 330 ms. La synchronisation ECG est indispensable à la reconstruction diastolique. La résolution temporelle est de la moitié ou du quart du temps de rotation. Le voxel est isotropique, d’environ 400 µ de coté (le double du pixel de la coronarographie). L’examen est réalisé en contraste spontané pour le calcul du score calcique coronaire (SCC) et avec injection de produit de contraste pour le coro-scanner. La quantité nécessaire de celui-ci diminue proportionnellement au nombre de détecteurs (actuellement 60 à 80 ml). L’irradiation peut nettement dépasser celle d’une coronarographie conventionnelle, atteignant jusqu’à 10 à 15 mSv (soit environ 3 à 4 fois plus). Toutefois, l’optimisation des doses en fonction de l’anatomie permet des réductions substantielles, ainsi que la modulation ECG. (« ECG pulsing »), l’association des deux permettant des réductions supérieures à 50 % et de descendre à des doses alors équivalentes à celles de la coronarographie conventionnelle. Pour le score calcique ces mesures permettent de réduire la dose délivrée au mSv. Un logiciel dédié est indispensable au calcul de ce dernier. Le post-traitement pour le coro-scanner utilise le MIP (« maximum intensity projection »), le MPR (« multi planar reconstruction »), les reconstructions curvilinéaires (curvilignes multiplanaires) et le VRT ou rendu volumique. Les limites du coro-scanner sont en partie inhérentes à ses capacités de résolutions et la coronarographie conventionnelle, dans ce domaine encore nettement plus performante, permet une meilleure luminographie. Les fréquences cardiaques élevées, régulières ou non, sont proscrites, l’optimum étant moins de 65 par minute. Le béta-blocage permet, outre la réduction des artéfacts cinétiques, de réduire l’irradiation. Certains proposent de plus, comme lors d’une coronarographie conventionnelle, l’utilisation systématique de dérivés nitrés. Une autre limite importante est représentée par les calcifications, notamment coronaires, responsables plus volontiers de faux-positif de sténose (par blooming) plutôt que de faux-négatif. Le maintien d’une apnée, dont la durée se réduit avec le nombre de détecteurs, est également à considérer. L’insuffisance rénale sévère et l’allergie sont des contre-indications relatives. Actuellement le scanner, injecté ou non, est côté Z19 soit environ 140 €. IV. SCORE CALCIQUE CORONAIRE. Les calcifications sont détectables par le scanner, ce qui permet de quantifier leur dépôt global sous forme d’un score de calcification (2). Sont considérées comme des calcifications, les images de densité supérieure ou égale à 130 UH, dont la surface est supérieure à 1 mm2. Le SCC. décrit par Agatston et al en 1990 (3) correspond à la surface totale des calcifications coronaires. Si la tomographie à faisceau d’électrons (TFE) constitue la technique de référence pour le calcul du SCC, le scanner multicoupe a été validé dans cette indication (1). De plus, il présente l’avantage d’une meilleure reproductibilité o. guiraudet Figure 1. Comparaison des images de calcifications coronaires obtenues par la tomographie par faisceau d’électrons puis avec un 4 détecteur. (fig. 1). Les études histo-pathologiques démontrent une corrélation forte avec la charge athéroscléreuse totale. Environ 2/3 des plaques sont calcifiées. Toujours pour l’AHA, le degré de calcif ication est également un marqueur de vulnérabilité au niveau de la plaque, de même que la charge calcique coronaire totale à l’étage panartériel. Au niveau systémique, la protéine C réactive (autre marqueur de vulnérabilité) est corrélée au score calcique. La calcif ication est un phénomène actif, favorisé par l’apoptose et les lipides oxydés. La vitesse de progression du score calcique a une valeur pronostique : en effet elle est corrélée au risque d’événements. A) RECOMMANDATIONS ACC/AHA 2000. Elles retiennent pour la TFE une sensibilité de 92 % et une spécificité de 55 % pour le diagnostic de sténose coronaire significative (2). La positivité du score est déterminée par une valeur seuil. Elles soulignent l’excellente valeur prédictive négative : l’absence de calcification élimine très probablement la présence de plaque d’athérosclérose. A contrario, un score élevé implique la présence de plaques et plus celui-ci est élevé plus grande est la probabilité de sténose(s) serrée(s), sans toutefois de relation absolument linéaire avec ces dernières. Il n’existe pas non plus corrélation anatomique entre la localisation des calcif ications et celle des sténoses serrées. L’intérêt diagnostique est limité par la faible spécificité. Pour le pronostic, l’insuffisance des données conduit à une proposition d’utilisation au cas par cas afin de permettre une meilleure stratif ication du risque et notamment le dépistage des patients à haut risque, dans le sous groupe des patients initialement classés comme à risque intermédiaire. B) RECOMMANDATIONS ESC 2003. Pour le diagnostic, la valeur prédictive négative de presque 100 % permet pour des douleurs atypiques avec intérêt du scanner dans la maladie coronaire un score nul « d’éviter facilement » la coronarographie, d’éliminer les faux positifs de l’ECG d’effort, très rarement pas ou peu de calcium est observé en cas d’infarctus du myocarde (1). Par contre, on tient compte des faux positifs avec coronarographie seulement en cas d’ischémie. Le score d’Agaston est devenu un facteur de risque indépendant pour l’extension de la maladie coronaire et pour le pronostic, apportant une information forte, graduée et supplémentaire à celle fournie par l’analyse des facteurs de risque conventionnels. Les valeurs seuils alors habituellement proposées se situent entre 80 et 160 ou intéressent les scores élevés (400 voire 1 000). L’utilisation des percentiles distribués en fonction de l’âge et du sexe permet une meilleure stratif ication (classes extrêmes : inférieures au 25°, supérieures au 75° ou 90° percentile). La détermination d’un niveau de risque équivalent à celui de la situation de prévention secondaire est possible ; la majorité des évènements surviennent pour des scores supérieurs au 75° percentile. Les indications restent pour l’ESC identiques à celles de l’AHA. C) ACTUELLEMENT. Principalement aux USA et en Allemagne, le score calcique est utilisé seul ou en association avec la recherche d’ischémie pour une stratification pronostique chez les sujets à risque, avec comme à l’occasion de la réalisation d’un examen diagnostique de l’ischémie, établissement d’une probabilité pré-test, puis post-test d’évènement. L’objectif étant le traitement des sujets à risque intermédiaire ou élevé (risque de morbi-mortalité cardiovasculaire à dix ans compris respectivement entre 5 % et 20 % puis dépassant 20 %). Se développe le concept d’âge coronaire, avec proposition de remplacement de l’âge de l’état civil par un équivalent dérivé du score calcique, intégré ensuite dans l’équation de Framingham, af in d’aff iner la stratification du risque. Enfin et d’importance, la valeur pronostique forte, indépendante, des calcifications coronaires est également retrouvée en prévention secondaire. V. CORO-SCANNER. Il ne fait pas encore l’objet de recommandations, actuellement en évaluation. Toutefois, les très bons résultats homogènes publiés légitiment son utilisation habituelle en pratique clinique par de nombreuses équipes. Dans certaines indications, il pourrait remplacer en effet la coronarographie conventionnelle diagnostique, et ce depuis déjà plusieurs années (fig. 2, 3). Des progrès techniques récents le conduisent vers la validation, comme en atteste l’étude de Zurich (4). Celleci est réalisée avec un 32 détecteurs effectuant 64 coupes, avec un temps de rotation de 370 ms et un tube à haute puissance (680 mA) disponible depuis 2004. Elle inclut 67 patients d’âge moyen 60 ans, de fréquence cardiaque moyenne 66 battements par minute (bpm), avec exclusion 357 D O S S I E R Figure 2. Lésion du tronc commun distal avec plaque hétérogène lipidique et calcifiée, sur une coupe native. À gauche la coronarographie, à droite l’imagerie par scanner coronaire. de la f ibrillation auriculaire, devant tous bénéf icier d’une coronarographie diagnostique. Cette dernière a montré la présence de lésions significatives chez 70 % et tritronculaires chez 50 % de l’ensemble des patients. Les coro-scanners sont réalisés sans SCC préalables (remplacés par une évaluation qualitative), ni bétablocage, ni administration de dérivés nitrés. La dosimétrie est adaptée à l’anatomie. L’ECG pulsing n’est pas utilisé car il empêche l’examen proto-diastolique supplémentaire souvent nécessaire, notamment pour la coronaire droite. La durée médiane de l’apnée est douze secondes. La reconstruction fait appel à un algorithme passant à deux secteurs en cas de fréquence cardiaque supérieure à 65 bpm. À partir de 1,5 mm de diamètre toutes les artères sont évaluées. En analyse per segment la sensibilité est de 94 %, la spécificité de 97 %, la valeur prédictive positive de 87 % et négative de 99 %, retrouvant les résultats d’une étude récente réalisée avec un 16 détecteur et un tube à haute puissance (5). Mais cette fois ci, en analyse per patient le classement est parfait, malgré un calibre seuil d’évaluation plus faible. La progression en précision prédictive est impressionnante (on rappelle les faibles valeurs prédictives négatives jusqu’alors habituelles en analyse per patient : 75 % en 2004 avec un 16 détecteurs et sur une population de caractéristiques voisines). Aucune exclusion n’a été rendue nécessaire pour des critères de qualité d’image. Toutefois la limite importante est représentée par des calcifications massives qui affectent 18 % de l’ensemble des segments. Ces calcifications importantes sont responsables de 58 % des pertes de Figure 3. Sténose serrée du genu superius de la coronaire droite. À gauche la coronarographie, à droite l’imagerie par scanner coronaire en mode M.I.P. 358 qualité d’image, de tous les faux positifs et de 72 % des faux négatifs. Les calcif ications, quand elles sont à l’origine d’erreur d’interprétation, génèrent trois fois plus de faux positifs (75 %) que de faux négatifs (25 %). Loin derrière viennent ensuite les artéfacts de mouvement, affectant 5 % des vaisseaux (et volontiers le deuxième segment de la coronaire droite). Ils sont responsables de 13 % des dégradations de qualité d’image et rendent compte des 28 % de faux négatifs restants. Ces artéfacts sont favorisés par les fréquences cardiaques élevées et peuvent être le plus souvent compensés par la sélection manuelle de la phase la moins polluée. Les problèmes d’hyposignaux deviennent également plus rares, atteignant 8 % des artères et à l’origine de 20 % des pertes de qualité d’image, la plupart survenant sur la rétro ventriculaire gauche et l’inter ventriculaire postérieure. Mais ils n’ont pas entraîné d’erreur importante d’interprétation. Enfin, les interactions avec des structures adjacentes sont peu fréquentes et à l’origine de dégradations modérées en qualité d’image. La rançon de conserver une possibilité d’analyse proto-diastolique est une dosimétrie plus élevée. La possibilité d’analyse de la paroi est une supériorité importante du scanner vis-à-vis de la coronarographie conventionnelle. De plus elle est aidée par l’acquisition volumique, qui fait également défaut à cette dernière. En effet, l’étude de la plaque d’athérome, de son volume et de sa constitution (en fonction des densités), ainsi que du remodelage sont validés par les comparaisons avec l’échographie endo-coronaire d’une part et l’anatomopathologie d’autre part. De plus, la quantification des sténoses s’enrichit alors des possibilités de planimétrie du luminogramme, technique inspirée de l’échographie endo-coronaire, mais avec une moindre précision liée à la moins bonne résolution spatiale. Nous mentionnons uniquement, car relevant de la prévention secondaire, l’intérêt du coro-scanner dans le dépistage de la maladie du greffon (précision diagnostique similaire à l’analyse du réseau natif) et l’évaluation des anastomoses (fig. 4). Le dépistage de la resténose intra-stent souffre quant à lui des artéfacts métalliques. En pratique, dans l’attente des recommandations, on peut proposer la réalisation du coro-scanner : Figure 4. Analyse en rendu volumique puis en curviligne multi planaire d’un pontage aorto-marginal. o. guiraudet – dans certaines indications de la coronarographie diagnostique, sans élargissement compte-tenu de la dosimétrie et sans logique prévisible de revascularisation dans le même temps (écartant d’emblée les patients ischémiques). Les indications pour cette dernière raison excluent la classe I et sont limitées à certaines de classe II, avec une probabilité pré-test basse à modérée. C’est le cas des coronarographies « d’élimination », comme, par exemple, celles réalisées chez des patients asymptomatiques ou présentant des douleurs thoraciques atypiques et une épreuve d’effort litigieuse ou non contributive, voire non réalisable. L’hypertrophie ventriculaire gauche connue plaide également en faveur d’une approche non invasive, comme le bilan pré chirurgie cardiaque hors cardiopathie ischémique, type remplacement valvulaire chez un patient présentant peu de facteurs de risque, ou encore le diagnostic étiologique d’une cardiomyopathie dilatée. Les rares anomalies d’origine et de trajet des coronaires constituent également une bonne indication ; – une sélection rigoureuse des patients est impérative. L’examen est différé en cas de tachycardie, régulière ou non. L’apnée, même brève, doit être réalisable. Pour beaucoup un SCC inférieur à 1000 (ou une masse calcique inférieure à 300 mg) est un pré-requis « obligatoire » pour une interprétation correcte avec un 16 détecteurs. Un SCC plus élevé, témoignant d’une athérosclérose importante, de mauvais pronostic, invite à rechercher, à l’aide d’un test sensible, une ischémie ; la présence de cette dernière est requise pour aller à la coronarographie conventionnelle en raison à la fois des limites d’interprétabilité du scanner et de la probable revascularisation associée dans le même temps ; – la préparation est également importante, avec béta-blocage (sauf contre indication) en cas de fréquence cardiaque supérieure à 65 bpm nitrés et entraînement à l’apnée (fig. 5). VI. CONCLUSION. Le scanner a déjà pris une place importante dans le dépistage de la maladie coronaire. Sur le continent nordaméricain et en Allemagne principalement, le score calcique est utilisé comme marqueur de l’athérosclérose, Indications Limitées à un sous-groupe de la coronarographie diagnostique conventionnelle : - patient non ischémique (absence d’indication prévisible de revascularisation) - prévalence pré coronarographie basse ou intermédiaire Sélection - FC < 90 bpm - bonne faisabilité de l’apnée - SCC SCC < 1 000 SCC > 1 000 Recherche d’ischémie Stop + Coronarographie conventionnelle Préparation - entraînement à l’apnée - béta-blocage en l’absence de contre-indication si FC > 65 bpm - dérivés nitrés IV Figure 5. Conditions pratiques de réalisation du coro-scanner. à valeur pronostique forte, graduée, indépendante. Le coro-scanner, en progression constante, vient d’atteindre en analyse per patient une précision diagnostique satisfaisante. Restant irradiant et requérant l’injection de produit de contraste, il remplace progressivement la coronarographie conventionnelle en cas de prévalence pré test faible ou intermédiaire. Mais tachycardie et calcifications restent des facteurs limitants. Bien qu’en termes de résolutions la coronarographie reste le goldstandard, il dépasse cette dernière dans les domaines d’acquisition volumique et d’analyse de la paroi, dont on connaît l’implication en termes de compréhension physiopathologique de la maladie coronaire. RÉFÉRENCES BIBLIOGRAPHIQUES 1. European guidelines on cardiovascular disease prevention in clinical practice. Third Joint Task Force of European and other Societies on Cardiovascular Disease Prevention in Clinical Practice. European Journal of Cardiovascular Prevention and Rehabilitation 2003 ; 10 (Suppl 1) : S1-78. 2. American College of Cardiology/American Heart Association Expert Consensus Document on Electron-Beam Computed Tomography for the Diagnosis and Prognosis of Coronary Artery Disease. A Statement for Healthcare Professionals from the American Heart Association and the American College of Cardiology. J Am Coll Cardiol 2000 ; 36 : 326-40. intérêt du scanner dans la maladie coronaire 3. Agatston AS, Janowitz WR, Hildner FJ, Zusmer NR, Viamonte M Jr, Detrano R. Quantification of coronary artery calcium using ultra fast computed tomography. J Am Coll Cardiol 1990 ; 15 : 827-32. 4. Leschka S, Alkadhi H, Plass A, Desbiolles L, Grünenfelder J, Marincek B et al. Accuracy of MSCT coronary angiography with 64slice technology: first experience. Eur Heart J 2005; 26: 1482-7. 5. Mollet N, Cademartiri F, Krestin G, McFadden E, Arampatzis C, Serryus P et al. Improved diagnostic accuracy with 16-row multislice computed tomography coronary angiography. J Am Coll Cardiol 2005 ; 45 : 128-32. 359 D O S S I E R VIENT DE PARAÎTRE LA MAÎTRISE DES MALADIES INFECTIEUSES UN DÉFI DE SANTÉ PUBLIQUE, UNE AMBITION MÉDICO-SCIENTIFIQUE Sous la direction de Gérard ORTH et Philippe SANSONETTI Le temps n'est pas éloigné où l'on pensait que les maladies infectieuses seraient maîtrisées grâce à la généralisation des mesures d'hygiène et à l'utilisation des antibiotiques et des vaccins. Cet espoir a malheureusement été déçu et l'on assiste à une résurgence des maladies infectieuses et des parasitoses et à l'émergence régulière de nouveaux agents infectieux, le plus souvent d'origine animale. Les populations les plus défavorisées de la planète payent le plus lourd tribut, mais force est de constater que le développement engendre aussi son lot de pathologies infectieuses. Ce problème de santé publique ancien se présente, depuis ces dernières décennies, avec une ampleur et des caractéristiques nouvelles. C'est pour cette raison que l'Académie des sciences a jugé indispensable de lui consacrer une réflexion approfondie. Les causes de cette situation sont multiples : elles sont analysées dans la première partie du rapport, d'où il ressort que, s'il faut admettre qu'il y aura toujours des maladies infectieuses, l'homme a sa part de responsabilité dans leur recrudescence actuelle. La deuxième partie de l'ouvrage développe les différents aspects de la réponse que nos sociétés doivent opposer à ce défi : cette réponse nécessitera un effort coordonné, sans précédent, de recherche, d'enseignement et d'actions en santé publique. Des recommandations sont adressées aux pouvoirs publics, aux différents acteurs de la santé et de la recherche, ainsi qu'à l'ensemble de nos concitoyens, car une information complète, étayée et lucide est aussi l'un des éléments de la maîtrise des maladies infectieuses. ISBN : 2-86883-888-X – 488 pages – Prix : 59 € – EDP Sciences, 17 avenue du Hoggar, Parc d'activités de Courtabœuf - BP 112, 91944 Les Ulis Cedex A – Contact Presse : Élise Chatelain – Tél. : 01 69 18 69 87 – [email protected] 360 Dossier « Cœur et Armées » : Divers INSUFFISANCE CARDIAQUE EN RÉGION TROPICALE Prise en charge diagnostique et thérapeutique PH. PAULE, PH. HÉNO, D. MIOULET, J.-M. PÉLONI, L. BRAEM, B. JOP, P. VARLET, J.-É. TOUZE, L. FOURCADE RÉSUMÉ Les maladies cardiovasculaires constituent un grave problème de santé publique à l’échelle mondiale, et les pays en développement sont de plus en plus concernés. L’évolution des facteurs de risque cardiovasculaire dans ces pays favorise notamment l’incidence des coronaropathies. L’insuffisance cardiaque est une entité fréquente, et c’est dans le cadre des missions extérieures et de l’aide médicale aux populations que le médecin militaire peut être conduit à prendre en charge ces affections. Le traitement symptomatique de l’insuffisance cardiaque ne comporte pas de particularité, mais les étiologies sont variées et les carences des systèmes de soins conduisent à une prise en charge souvent retardée. Il existe des maladies plus spécifiques du monde tropical et des causes cosmopolites qui traduisent le phénomène de transition épidémiologique dans les pays en développement. À travers des tableaux typiques, les auteurs illustrent certaines étiologies qui présentent un intérêt par leur fréquence, leur mode de survenue, leur présentation clinique ou des spécificités thérapeutiques. Ils soulignent les caractéristiques de la cardiomyopathie du péri-partum, du Béribéri cardiaque, de la fibrose endomyocardique, du rétrécissement mitral, de la péricardite chronique constrictive, de la maladie de Chagas, des cardiomyopathies associées à l’infection par le VIH, et de l’impact de l’hypertension artérielle sur l’insuffisance cardiaque. Mots-clés : Béribéri cardiaque. Cardiomyopathie du péripartum. Fibrose endomyocardique. Hypertension artérielle. Insuffisance cardiaque. Maladie de Chagas. Péricardite chronique constrictive. Rétrécissement mitral. I. INTRODUCTION. Actuellement les maladies cardiovasculaires représentent la première cause de mortalité dans le monde, et sont responsables d’environ 30 % des décès. En Afrique subsaharienne, la mortalité cardiovasculaire représente PH. PAULE, médecin principal (TA), praticien certifié. PH. HÉNO, médecin en chef, praticien certifié. D. MIOULET, médecin des armées, praticien confirmé. J.-M. PÉLONI, médecin principal, praticien confirmé. L. BRAEM, médecin principal, praticien confirmé. B. JOP, interne CHU. P. VARLET, médecin en chef, praticien certifié. J.-É. TOUZE, médecin général, praticien certifié agrégé. L. FOURCADE, médecin en chef, praticien certifié agrégé. Correspondance : PH. PAULE, Service de cardiologie, HIA Laveran, BP 50, 13998 Marseille Armées. médecine et armées, 2006, 34, 4 ABSTRACT HEART FAILURE IN THE TROPICS : DIAGNOSIS AND TREATMENT. Cardiovascular diseases constitute a serious public health issue on a worldwide scale and developing countries are more and more concerned. The emergence of cardiovascular risk factors in these countries favours the development of coronaropathy. Heart failure is a frequent entity and with the multiplication of foreign assignments and humanitarian care, the military unit’s medical officer becomes more and more involved in the management of these diseases. Symptomatic treatment does not pose a real problem but causes are very varied and the lacks in the care systems lead to a delay in the treatment. Some heart diseases are more specific to the tropical world, which together with cosmopolitan causes of heart failure conveys the epidemiological transition in developing countries. The authors illustrate some particular features of the cardiopathies observed in the tropics, which are interesting because of their frequency, their mode of occurrence, their clinical presentation or the therapeutic possibilities. They emphasize the characteristics of peri partum cardiomyopathy, cardiac beriberi, endomyocardial fibrosis, rheumatic disease, constrictive pericarditis, Chagas’ disease, cardiomyopathy associated with HIV infection and the impact of hypertension on heart failure. Keywords : Cardiac beriberi. Chagas’disease. Chronic constrictive pericarditis. Endomyocardial fibrosis. Heart failure. Hypertension. Mitral stenosis. Post-partum cardiomyopathy. (Médecine et Armées, 2006, 34, 4, 361-367) maintenant la deuxième cause de mortalité au même niveau que les infections respiratoires, alors qu’en Asie elle occupe déjà la première place (1). Expression clinique évolutive de la plupart des maladies cardiovasculaires, l’insuffisance cardiaque (IC) est très fréquemment rencontrée dans les pays en développement (PED). Dans les PED de la zone tropicale, la migration des populations vers les zones urbaines induit des modifications des habitudes alimentaires et de l’activité physique. L’augmentation de la consommation du tabac, l’élévation de l’index de masse corporelle et le développement du diabète de type 2 contribuent à la très nette augmentation de la maladie coronaire. Les facteurs 361 D O S S I E R de risque cardiovasculaire classiques des pays développés sont dorénavant transposés sous les tropiques, à l’origine du phénomène de transition épidémiologique. À côté de la pathologie ischémique en expansion, d’autres affections plus spécifiques aux PED génèrent des tableaux d’IC souvent sévères (2). Ainsi outre mer cohabitent la pathologie des pays riches et des maladies que les praticiens européens, généralistes ou spécialistes n’ont plus l’occasion de rencontrer dans leur exercice habituel. Cependant dans le cadre des OPEX, les médecins militaires sont souvent amenés à participer à l’aide médicale aux populations, et des expériences récentes ont montré l’importance de l’IC dans ce contexte. Au-delà de la prise en charge d’un épisode aigu, il importe de savoir réaliser un bilan étiologique simple afin d’orienter utilement l’attitude thérapeutique. Cet article a pour but de rappeler les éléments du diagnostic étiologique d’une poussée d’IC, avec les moyens limités disponibles dans un hôpital de campagne, afin de déterminer la prise en charge la mieux adaptée. Le diagnostic positif de l’IC congestive ainsi que le traitement purement symptomatique des épisodes aigus n’y seront pas abordés. II. DÉMARCHE DIAGNOSTIQUE. A) ÉTAPE CLINIQUE. Devant des signes d’IC, l’enquête étiologique passe avant tout par une démarche clinique minutieuse. Il s’agit dans un premier temps de rechercher des antécédents de cardiopathie ou de souffle cardiaque ancien, de rhumatisme articulaire aigu durant l’enfance, d’hypertension artérielle (HTA) négligée, de grossesse récente, la notion d’une infection à VIH ou un antécédent de tuberculose. Ces notions seront souvent difficiles à identif ier chez des patients ne bénéf iciant d’aucun suivi, opposant parfois la barrière de la langue et chez lesquels les cardiopathies sont souvent diagnostiquées tardivement. Il faut préciser les facteurs de risque cardiovasculaire identifiables, la prise de toxiques (khât à Djibouti, éthylisme…). Chez l’insuffisant cardiaque, outre l’évaluation de la dyspnée, l’interrogatoire recherche des signes fonctionnels associés tels que des précordialgies, des palpitations, des malaises. On recherche une altération de l’état général, ainsi que l’existence d’une fièvre prolongée. D’emblée, l’examen cutané et des muqueuses recherche une pâleur des conjonctives, un ictère des sclérotiques ou des signes en faveur d’un syndrome carentiel. L’examen de la peau peut être difficile chez des sujets de race noire, notamment à la recherche d’une éruption cutanée, d’un pouls capillaire, de faux panaris d’Osler (élévations rouges violacées douloureuses, situées à la pulpe du doigt, sans suppuration). L’examen des mains peut révéler un hippocratisme digital. L’attention sera retenue par la brillance du regard ou une exophtalmie. La palpation de l’aire cardiaque peut percevoir un frémissement. L’auscultation du cœur recherche des bruits surajoutés : souffles systolique ou 362 diastolique en précisant leur localisation et leur irradiation, roulement diastolique ou frottement péricardique. La recherche soigneuse des différents pouls est importante ainsi que la mesure de leur fréquence, leur régularité et le caractère bondissant ou paradoxal (diminution en inspiration) du pouls radial. L’auscultation des trajets vasculaires et la palpation de l’abdomen à la recherche d’une masse battante permettent d’évoquer l’existence d’une athérosclérose diffuse. La mesure de la pression artérielle est réalisée aux deux bras. On recherche des signes de phlébite au niveau des membres inférieurs. La palpation des aires ganglionnaires et de la rate est systématique. Cette étape clinique ne doit pas omettre le dépistage de foyers infectieux au niveau de la sphère ORL et de l’appareil dentaire. B) PARACLINIQUE. Facilement disponible, l’ECG permet d’évaluer la fréquence et le rythme du cœur, l’axe du complexe QRS, des troubles éventuels de la repolarisation. On recherche des troubles de conduction ou du rythme, des signes de surcharge ventriculaire, d’ischémie ou de nécrose. La radiographie thoracique permet la mesure de l’index cardiothoracique, la mise en évidence d’une modification de la silhouette cardiaque et de l’existence de calcifications vasculaires, annulaires ou péricardiques sur des clichés de face et de prof il. On apprécie l’état du parenchyme pulmonaire et l’existence d’un épanchement pleural. Des examens biologiques simples peuvent être réalisés, notamment la numération formule sanguine pour mettre en évidence une anémie, une polynucléose à neutrophiles ou une hyperéosinophilie. On doit rechercher une insuffisance rénale, une anomalie des tests fonctionnels hépatiques et une dysthyroïdie au moindre doute. Dans les situations aiguës, la gazométrie artérielle permet d’apprécier la sévérité de la situation clinique, et l’existence d’un effet shunt. L’élévation des enzymes cardiaques (CPK et CPK MB) et de la troponine oriente vers un syndrome coronaire aigu. La sérologie VIH doit être d’indication large. Un appareil d’échographie (non obligatoirement dédié à l’étude du cœur) peut être disponible et permettre la réalisation d’un examen de débrouillage facilitant la démarche diagnostique. On recherche une atteinte de la fonction systolique du ventricule gauche (VG), un trouble de la cinétique segmentaire, une hypertrophie ventriculaire, une dilatation des cavités cardiaques, un épanchement péricardique. La disponibilité d’un module doppler permet l’évaluation de la pression artérielle pulmonaire systolique ou d’une valvulopathie. L’étude des pressions de remplissage du VG est utile pour identifier un profil restrictif et apporter des arguments en faveur d’une péricardite chronique constrictive. Au terme de cette première évaluation, la plupart des situations paraîtront évidentes et leur diagnostic posera peu de problèmes face à des affections souvent très évoluées. Il s’agit essentiellement de causes cosmopolites. Par contre, certains tableaux plus spécifiques aux régions tropicales peuvent être individualisés et seront ph. paule détaillés dans le chapitre suivant. Enfin quelle que soit la cardiopathie en cause, on n’omettra pas de rechercher le facteur de décompensation expliquant la poussée d’insuff isance cardiaque : une surcharge en sel, un sevrage thérapeutique, une poussée hypertensive, un trouble du rythme, une ischémie, une anémie, une dysthyroidie, une pneumopathie intercurrente. III. ÉTIOLOGIES. A) QUELQUES TABLEAUX ORIGINAUX… 1. Un contexte particulier. a) Exemple 1. Une patiente, âgée de 28 ans, sans antécédent, est hospitalisée à l’Hôpital principal de Dakar pour une dyspnée au moindre effort puis au repos, survenue un mois après un accouchement non compliqué. Elle a présenté trois grossesses préalables qui se sont déroulées sans problème. Elle est admise dans un tableau clinique d’insuffisance cardiaque gauche. L’ECG enregistre une tachycardie sinusale avec une négativation de l’onde T dans les dérivations latérales. Le cliché thoracique conf irme le diagnostic d’œdème aigu du poumon et met en évidence une cardiomégalie (fig. 1). La NFS ne montre pas d’anémie. L’échocardiographie trans-thoracique (ETT) objective un VG dilaté globalement hypokinétique avec une fraction d’éjection effondrée à 25 %, sans autre anomalie par ailleurs. Il faut évoquer dans ce contexte une cardiomyopathie du péri-partum (CMPP), présente sous toutes les latitudes, mais rencontrée avec une plus grande incidence (1/100 à 1/1 000 délivrances) en Afrique sub-saharienne chez les femmes Noires de niveau social modeste et multipares. Elle survient par définition durant le dernier mois de la grossesse ou les cinq mois suivant l’accouchement chez des jeunes femmes sans antécédent cardiovasculaire (3). Elle se présente sous la forme d’une insuff isance cardiaque d’évolution aiguë, associée en échocardiographie à une dilatation cavitaire et une hypokinésie avec altération sévère de la fraction d‘éjection du VG. Le traitement symptomatique associe le repos strict et le régime hyposodé, l’utilisation de diurétique de l’anse et d’IEC puis de bêtabloquant pendant plusieurs mois, permettant la guérison ad integrum dans 30 % à 50 % des cas. Les complications rythmiques et surtout emboliques sont redoutées et imposent souvent la mise en route d’un traitement anticoagulant. La mortalité est de 10 % à 30 % à la phase aiguë et la récidive est possible lors d’une future grossesse. Cette affection d’étiopathogénie toujours mystérieuse comporte un risque d’évolution vers une cardiomyopathie dilatée et un tableau d’IC chronique (4, 5). b) Exemple 2. Un jeune réfugié, âgé de 25 ans, est recueilli à la frontière du Darfour. Très asthénique et dyspnéique au moindre effort, il est cachectique et présente des signes évidents de dénutrition. On note un tableau clinique d’insuffisance cardiaque globale à dominante droite avec de volumineux œdèmes des membres inférieurs et des organes génitaux externes. L’examen met aussi en évidence un déficit sensitivo-moteur en faveur d’une polyneuropathie des membres inférieurs. L’ECG est sans particularité. Le cliché thoracique montre une volumineuse cardiomégalie. L’ETT objective une dilatation des cavités droites avec une insuffisance tricuspidienne et une atteinte de la fonction ventriculaire droite. Les cavités gauches sont de volume normal sans altération de la fonction systolique du ventricule qui apparaît plutôt hyperkinétique. Il s’agit d’un Béribéri cardiaque associé à une atteinte neurologique signant la forme « humide » de la carence en thiamine (vitamine B1). Maladie de la misère, on la rencontre dans le contexte de populations déplacées et de camps de réfugiés (5). Elle est souvent secondaire à une alimentation à base exclusive de riz blanc, et peut être favorisée par l’éthylisme chronique. Ce déf icit vitaminique entraîne une vasodilatation systémique et l’élévation du débit cardiaque, associée à une atteinte directe du myocarde. Lorsque les mécanismes de compensation se trouvent dépassés, s’installe un tableau d’IC globale à prédominance droite. Le traitement impose l’apport de thiamine par voie parentérale (500 mg/jour) relayé par voie orale, sans lequel les mesures thérapeutiques de l’insuffisance cardiaque n’ont aucune efficacité. L’amélioration clinique rapide et spectaculaire (48 heures) confirme alors le diagnostic et l’évolution est favorable (6) sous réserve de la prise en charge de la dénutrition et d’autres éventuelles carences alimentaires. 2. Une anomalie auscultatoire. Figure 1. Cliché thoracique de face objectivant une cardiomégalie chez une patiente porteuse d’une cardiomyopathie du péri-partum. insuffisance cardiaque en région tropicale a) Exemple 1. Un adolescent ivoirien, âgé de 15 ans, consulte dans un tableau d’insuff isance cardiaque globale. Essoufflé pour des efforts minimes, il présente un retard 363 D O S S I E R staturo-pondéral, une volumineuse ascite contrastant avec des œdèmes modérés des membres inférieurs. L’auscultation perçoit un bruit de galop et un souffle holosystolique intense en jet de vapeur irradiant dans l’aisselle. L’ECG montre simplement des signes d’hypertrophie auriculaire gauche. Le cliché thoracique confirme les signes congestifs et montre l’augmentation de l’index cardiothoracique avec un double contour de l’arc inférieur droit. Il existe une hyperéosinophilie à 1 200 éléments/mm 3. L’ETT montre un comblement f ibreux de la pointe du VG, un épaississement de l’appareil sous-valvulaire mitral ainsi qu’une oreillette gauche très dilatée (fig. 2). La fonction systolique ventriculaire gauche est conservée. Il existe une insuffisance mitrale sévère sans épaississement des feuillets. On met en évidence une hypertension artérielle pulmonaire. Compte tenu du contexte épidémiologique et de la symptomatologie, il faut évoquer chez ce jeune patient une fibrose endomyocardique de Davies. Il s’agit d’une cardiomyopathie restrictive secondaire à la toxicité des protéines basiques libérées par les polynucléaires éosinophiles et dirigées contre l’endocarde. Cette affection est l’apanage presque exclusif des régions tropicales où sévissent de manière endémique les helminthiases à cycle tissulaire, contractées tôt dans l’enfance. Le comblement fibreux peut intéresser l’un ou l’autre des ventricules voire les deux, et impliquer l’appareil sous-valvulaire mitral ou tricuspidien. Il s’y associe une forte propension à la formation de thrombus intra-ventriculaire. Le phénomène de restriction au remplissage ventriculaire est presque toujours associé à des fuites valvulaires sévères (4). La symptomatologie associe de façon variable des signes d’IC gauche et/ou droite, et des fuites valvulaires mitrale et/ou tricuspidienne. Le diagnostic est affirmé par l’aspect échographique de comblement apical des ventricules et d’ectasie des oreillettes. Il existe une relation inverse entre le taux d’éosinophiles qui peut s’être normalisé et le temps écoulé depuis le début des symptômes. Le pronostic est sombre avec 50 % de décès dans les deux ans qui suivent le diagnostic (5). Seule l’endocardectomie chirurgicale peut infléchir cette évolution, associée à la réalisation d’une plastie ou d’un remplacement valvulaire (7). b) Exemple 2. Une jeune Afghane, âgée de 25 ans, enceinte de trois mois est hospitalisée dans un tableau d’œdème aigu du poumon rapidement amélioré par l’injection de furosémide IV. Son entourage rapporte de nombreuses angines inconstamment traitées durant son enfance, et des épisodes répétés de douleurs et de fluxions articulaires. Après amélioration de l’état hémodynamique, l’examen clinique retrouve un éclat du premier bruit du cœur au foyer mitral, un dédoublement du deuxième bruit et un roulement diastolique. L’ECG enregistre une fibrillation auriculaire à 120 bpm. Le cliché thoracique montre un dédoublement de l’arc inférieur droit sans augmentation de l’arc inférieur gauche. L’ETT montre un épaississement de l’extrémité des feuillets mitraux, rigides et déformés en canne de golf (fig. 3), avec un aspect de fusion des commissures valvulaires, sans calcification de l’appareil sous valvulaire. La surface mitrale est évaluée à 1 cm2 par planimétrie et le gradient de pression trans-mitral mesuré par doppler est élevé à 14 mm Hg. Il n’existe pas d’insuffisance mitrale. La fonction systolique du ventricule gauche est conservée. La pression artérielle pulmonaire systolique est évaluée à 50 mm Hg. Cette jeune patiente présente un rétrécissement mitral d’origine rhumatismale compliqué de f ibrillation auriculaire. Le traitement des angines streptococciques a permis de faire disparaître cette affection dans les pays industrialisés. Les valvulopathies rhumatismales Figure 2. Échocardiographie en incidence para-sternale grand axe : comblement fibreux du ventricule gauche et dilatation de l’oreillette gauche dans le cadre d’une fibrose endomyocardique. Figure 3. Échocardiographie en incidence para-sternale grand axe : rétrécissement mitral avec feuillets mitraux épaissis et déformés, limitation de l’ouverture mitrale en diastole. 364 ph. paule demeurent fréquentes dans les PED, représentant environ le tiers des causes d’hospitalisation en cardiologie (2). Le rétrécissement mitral se complique volontiers de troubles du rythme supra-ventriculaire et d’embolies systémiques. Outre le traitement de la poussée d’insuffisance cardiaque, ici favorisée par la grossesse, il est souhaitable de réaliser un traitement étiologique qui dépend des possibilités logistiques locales. En zone tropicale, le traitement par valvuloplastie mitrale percutanée par ballonnet continue de poser des problèmes de coût ; la commissurotomie percutanée par dispositif métallique réutilisable représente un espoir pour l’avenir (8). La commissurotomie chirurgicale à cœur fermé ne nécessite pas de circulation extra-corporelle, peut être réalisée par un chirurgien généraliste pratiquant l’abord du cœur par thoracotomie latérale, et constitue une alternative qui demeure d’actualité (9). En cas d’insuff isance mitrale associée, seul le remplacement valvulaire peut être proposé. 3. Une insuffisance cardiaque droite au premier plan. Un tchadien, âgé de 50 ans, est admis dans un tableau d’anasarque comportant des œdèmes des membres inférieurs et une ascite, une hépatomégalie et une évidente turgescence des veines jugulaires. Ses antécédents sont mal connus. L’auscultation perçoit un bruit vibrant proto-diastolique maximum à l’apex, augmenté à l’inspiration. L’ECG enregistre une tachycardie sinusale à 110 bpm, un microvoltage avec des ondes T négatives diffuses. La radiographie thoracique met en évidence un petit cœur triangulaire à bord gauche rectiligne avec des calcifications péricardiques mieux visibles sur le cliché de profil (fig. 4), un épanchement pleural bilatéral minime et une opacité parenchymateuse apicale droite. L’ETT objective des oreillettes dilatées contrastant avec des ventricules de taille normale. La fonction systolique du VG est normale, mais il existe une expansion du ventricule droit en inspiration avec inversion de la courbure septale. Au doppler, l’amplitude du flux de remplissage du cœur gauche diminue à l’inspiration. On note une dilatation de la veine cave inférieure, sans modification de son diamètre par les mouvements respiratoires. Le péricarde apparaît épaissi. Il s’agit d’un tableau de péricardite chronique constrictive. Dans ce contexte, l’origine tuberculeuse est fortement probable. L’incidence de la péricardite tuberculeuse augmente en Afrique en raison de sa fréquente association à l’infection par le VIH. L’évolution vers l’épaississement fibreux et la constriction puis la calcif ication péricardique induit un phénomène hémodynamique d’adiastolie, à l’origine des signes d’IC à prédominance droite. La prise en charge nécessite l’utilisation de diurétique afin de diminuer les signes congestifs, et un traitement antibiotique antituberculeux biphasique d’une durée de six mois. Il faut y associer une péricardectomie chirurgicale d’emblée en cas de calcification, ou après évaluation de l’efficacité d’un traitement antituberculeux de 4 à 8 semaines. En l’absence de traitement, l’affection peut évoluer vers l’IC terminale ou un tableau de pseudo-cirrhose hépatique (10). Il faut systématiquement rechercher une infection associée par le VIH. 4. Syncopes et IC en Amérique Latine. Un Garimperos d’origine brésilienne, âgé de 35 ans, consulte à l’antenne médicale du camp Régina en Guyane. Ce patient qui vit en forêt amazonienne depuis plus de vingt ans, décrit un essoufflement d’aggravation progressive survenant désormais pour des efforts modérés, et plus récemment plusieurs épisodes de syncopes au repos et à l’effort. L’examen clinique retrouve un bruit de galop à la pointe, chez un patient tachycarde. L’électrocardiogramme enregistre un rythme Figure 4. Clichés thoraciques de face et de profil : calcifications péricardiques (flèches) dans le cadre d’une péricardite chronique constrictive. insuffisance cardiaque en région tropicale 365 D O S S I E R sinusal avec un bloc de branche droit, une onde Q de V3 à V5 et de nombreuses extrasystoles ventriculaires polymorphes. Le cliché thoracique montre une cardiomégalie. L’ETT obtenue à l’hôpital de Cayenne objective une altération de la fonction systolique globale du VG qui apparaît dilaté et l’existence d’un anévrysme apical. Il s’agit d’une cardiomyopathie constituant la principale manifestation au stade chronique de la maladie de Chagas. Cette parasitose due à Trypanosoma Cruzi, protozoaire transmis par les déjections d’une punaise, constitue une cause fréquente d’insuffisance cardiaque chez les enfants et les adultes jeunes en Amérique du Sud. Seuls 15 % à 30 % des patients infectés développent une forme chronique, cardiaque ou digestive, dans un délai de 15 à 20 ans (11). L’ECG peut montrer des troubles conductifs de haut degré et des troubles du rythme ventriculaire qui se traduisent volontiers par des malaises syncopaux. L’ETT met en évidence une cardiomyopathie dilatée hypokinétique, et souvent la présence d’un anévrysme apical caractéristique pouvant se compliquer de la formation de thrombus. La mort subite secondaire à une arythmie ventriculaire émaille souvent le cours de la maladie. À ce stade, les parasites sont difficiles à mettre en évidence (xénodiagnostic de Brumpt éventuellement sensibilisé par PCR sur déjections de réduves) et les méthodes sérologiques ont une valeur d’orientation compte tenu du nombre de réactions croisées. Outre le traitement symptomatique de l’insuffisance cardiaque, la prise en charge doit prendre en compte les complications thromboemboliques par l’anti-coagulation, et les troubles du rythme peuvent nécessiter l’utilisation d’anti-arythmiques ou l’implantation d’un défibrillateur, rarement disponibles dans les PED. Tous les patients doivent bénéf icier d’un traitement anti-parasitaire (nifurtimox, benznidazole), à l’exception du stade chronique en phase terminale. B) DES CAUSES COSMOPOLITES… Il ne s’agit pas d’établir une liste fastidieuse et certainement non exhaustive des différentes cardiopathies rencontrées en zone tropicale. Celles-ci sont rappelées dans le tableau I. Cependant certaines causes cosmopolites d’IC se distinguent par leur fréquence ou par des particularités tropicales. Les facteurs de risque de la maladie coronaire sont dorénavant présents sur tous les continents et les pays tropicaux ne font plus exception. En Afrique par exemple, cinq paramètres contribuent à la survenue de 90 % des infarctus du myocarde : tabac, hypertension artérielle (HTA), diabète de type 2 et obésité, anomalies du bilan lipidique (notamment rapport apo B/apo A) (12). La consommation de tabac est en pleine expansion dans les PED où la consommation de tabac a progressé de plus de 100 % ces dernières années. Les modifications du régime alimentaire associées à l’urbanisation ont favorisé le développement de l’obésité et du diabète qui deviennent de réels problèmes de santé publique. Les projections épidémiologiques établissent ainsi une progression de la 366 mortalité cardiovasculaire en Afrique de 15 % en 1995 à 35 % en 2015 (13). Avec l’accroissement des coronaropathies, la part des cardiomyopathies ischémiques est appelée à augmenter en tant que cause d’IC, d’autant plus que les moyens thérapeutiques font cruellement défaut dans ce domaine. En l’absence de possibilité de revascularisation, l’IC constitue plus souvent un mode évolutif de la maladie coronaire. Les poussées d’IC émaillant le suivi du coronarien concernent des patients plus jeunes qu’en Europe, avec un pronostic moins bon à court et long terme. L’HTA est déjà le premier des facteurs de risque cardiovasculaire dans le monde en terme de fréquence. Dans les PED, on estime que son incidence progressera de 80 % à l’horizon de 2025, avec 1,15 milliard d’adultes hypertendus (14). Les cardiopathies hypertensives constituent un problème fréquent dans ces pays, en Afrique subsaharienne notamment. L’HTA y est fréquente et diagnostiquée avec retard, très souvent au stade des complications. L’absence de prise en charge thérapeutique adaptée favorise l’émergence des cardiopathies hypertensives (5). L’hypertrophie ventriculaire gauche concentrique est déjà présente chez 75 % des patients lorsque le diagnostic d’HTA est porté, cause possible d’IC par trouble du remplissage du VG. À plus long terme, on assiste à un remodelage du VG avec dilatation cavitaire progressive et altération de la fonction contractile. À ces stades avancés, le retentissement cardiaque de l’HTA s’associe volontiers à l’insuffisance rénale et au risque majoré d’accident vasculaire cérébral (15). En marge du phénomène mondial de transition épidémiologique qui voit globalement diminuer la morbi-mortalité de cause infectieuse, l’infection à VIH participe en Afrique de manière non négligeable à la mortalité cardiovasculaire. Si dans les pays riches nous sommes surtout confrontés actuellement au problème des effets secondaires métaboliques des trithérapies, il s’agit dans les PED de faire face aux complications cardiaques du virus et des infections Tableau I. Principales causes d’insuffisance cardiaque en zone tropicale. Atteintes cosmopolites Cardiopathie ischémique Cardiomyopathies dilatées Cardiomyopathie hypertrophique Cardiomyopathie hypertensive Cardiopathies congénitales Cardiopathies valvulaires Myocardites Endocardites Tamponnade Embolie pulmonaire Atteintes plus spécifiques aux zones tropicales Cardiopathies du VIH Cardiopathies parasitaires : maladie de Chagas, bilharziose … Cardiopathies carentielles : Béribéri, anémie, éthylisme… Cardiomyopathie du péri-partum Fibrose endomyocardique Péricardite chronique constrictive Cardiothyréose ph. paule opportunistes qui peuvent toucher les trois tuniques du cœur (5). Les séries autopsiques rapportent 30 % à 40 % de cardiomyopathie dilatées chez les sujets infectés par le VIH, surtout quand le déficit en CD4 est important au stade de SIDA. En termes de mortalité et de morbidité, même si la part rapportée aux atteintes cardiovasculaires du SIDA est difficilement chiffrable en milieu tropical, elle représente une étiologie courante de cardiopathie dilatée hypokinétique du sujet jeune (16). Il faut citer la fréquence des cardiopathies congénitales vieillies (CIV, CIA…), non dépistées durant l’enfance ou non corrigées faute de moyens. Elles constituent une cause fréquente d’IC et de complications infectieuses par endocardite à l’âge adulte. Enfin, l’anémie profonde et prolongée constitue une cause d’IC, tout particulièrement chez l’enfant où il n’est pas rare d’observer des taux d’hémoglobine inférieurs à 5 g/dl. En zone tropicale, il s’agit d’anémies souvent multifactorielles (parasitoses digestives, hémoglobinopathies, grossesses itératives, carences). L’hyperthyroïdie prise en charge tardivement est fréquemment diagnostiquée au stade de cardiothyréose associant IC et arythmie supra-ventriculaire. Dans le cas de l’anémie et de la cardiothyréose, le tableau d’IC est d’autant plus marqué qu’il existe une cardiopathie préexistante. C) À PROPOS DU PALUDISME. Si le paludisme ne se complique pas de manifestations cardiaques directement en rapport avec le rôle de l’hématozoaire, il n’en demeure pas moins qu’il existe un risque d’œdème du poumon d’origine lésionnelle au cours des accès graves. Véritable capillarite parasitaire, cet œdème lésionnel n’est pas associé à une dysfonction myocardique, mais il est favorisé par une surcharge volumique liée à une réhydratation parentérale excessive. En cas de fonction cardiaque sous jacente préalablement altérée (cardiomyopathie, valvulopathie), la situation peut alors se compliquer d’une défaillance hémodynamique avec œdème pulmonaire à la fois cardiogénique et lésionnel. Cela constitue entre autres, un argument pour souligner l’importance de la sélection des personnels militaires désignés pour servir outre mer. IV. CONCLUSION. Avec le développement inexorable des maladies cardiovasculaires dans les PED, la prise en charge de l’IC y devient un problème de santé publique. Dans le cadre de l’aide médicale aux populations locales en OPEX, le médecin militaire projeté doit pouvoir prendre en charge des patients en IC souvent jeunes et porteurs d’affections inhabituelles ou parfois oubliées des pays développés. Si la prise en charge initiale symptomatique pose peu de problèmes, il en va tout autrement du traitement étiologique. Celui-ci peut parfois s’avérer simple et peu onéreux, mais bien souvent il nécessite une prise en charge au long cours ou la mise en œuvre de moyens chirurgicaux peu accessibles à ces populations. RÉFÉRENCES BIBLIOGRAPHIQUES 1. Gaziano TA. Cardiovascular disease in the developing world and its cost-effective management. Circulation 2005 ; 112 : 3 547-53. 2. Mendez GF, Cowie MR. The epidemiological features of heart failure in developing countries : a review of the literature. Int J Cardiol 2001 ; 80 : 213-9. 3. Pearson GD, Veille JC, Rahimtoola S, Hsia J, Oakley CM, Hosenpud JD et al. Peripartum cardiomyopathy : National Heart, Lung, and Blood Institute and Office of Rare Diseases (National Institutes of Health) workshop recommendations and review. JAMA 2000 ; 283 : 1 183-8. 4. Touze JE, Peyron F, Malvy D. Médecine tropicale au quotidien, 100 cas cliniques. Format Utile 2001 : 268-73. 5. Sliwa K, Damasceno A, Mayosi BM. Epidemiology and etiology of cardiomyopathy in Africa. Circulation 2005 ; 112 : 3 577-83. 6. Blanc P, Boussuges A. Béribéri cardiaque. Arch Mal Cœur 2000 ; 93 : 371-9. 7. Fourcade L, Héno P, Cloix JJ, Touze JE. Les fibroses endomyocardiques. Réalités Cardiologiques 2000 ; 153 : 13-8. 8. Iung B, Vahanian A. Le rétrécissement mitral. Ann Cardiol Angéiol 2003 ; 52 : 117-24. 9. Fourcade L. Traitement du rétrécissement mitral en zone tropicale : insuffisance cardiaque en région tropicale le choix des armes. Med Trop 1999 ; 59 : 139-40. 10. Mayosi BM, Burgess LJ, Doubell AF. Tuberculous pericarditis. Circulation 2005 ; 112 : 3 608-16. 11. Barrrett MP, Burchmore RJS, Stich A, Lazzari JO, Fasch AC, Cazzulo JJ et al. The trypanosomiases. Lancet 2003 ; 362 : 1 469-80. 12. Steyn K, Hawken S, Commerford P, Onen C, Damasceno A, Ounpuu S et al. For the INTERHEART investigators in Africa. Risk factors associated with myocardial infarction in Africa, the INTERHEART Africa study. Circulation 2005 ; 112 : 3 554-61. 13. Zabsonré P, Sanou G, Avanzini F, Tognoni G. Connaissance et perception des facteurs de risque cardiovasculaire en Afrique subsaharienne. Arch Mal Cœur 2002 ; 95 : 23-8. 14. Kearney PM, Whelton M, Reynolds K, Muntner P, Whelton PK, He J. Global burden of hypertension : analysis of worldwide data. Lancet 2005 ; 365 : 217-23. 15. Opie LH, Seedat YK. Hypertension in sub-saharian african populations. Circulation 2005 ; 112 : 3 562-8. 16. Ntsekhe M, Hakim J. Impact of human immunodeficiency virus infection on cardiovascular disease in Africa. Circulation 2005 ; 112 : 3 602-7. 367 D O S S I E R VIENT DE PARAÎTRE RAPPORT SUR LA SANTÉ EN EUROPE 2005 L'action de santé publique : améliorer la santé des enfants et des populations Les gouvernements et les décideurs de la Région européenne de l'OMS savent que la santé est une ressource essentielle pour le développement économique et social. Ils ont tout lieu de se féliciter de l'amélioration globale de la santé dans la Région, mais il subsiste encore, entre les pays de ses parties occidentale et orientale et entre les groupes socioéconomiques dans les pays, des disparités croissantes qu'il est crucial de réduire. Le Rapport sur la santé en Europe 2005 montre que cet objectif peut être atteint. Il résume les grands problèmes de santé publique auxquels la Région doit faire face et qui touchent en particulier les enfants, et indique les moyens d'y remédier. Il contribue ainsi à diffuser les informations fiables dont il faut disposer pour prendre des décisions judicieuses dans le domaine de la santé publique. Le rapport fait la synthèse d'informations factuelles et d'analyses provenant de l'OMS et d'autres sources. Il montre que les maladies non transmissibles sont la principale cause de la charge de morbidité dans la Région et que les maladies transmissibles représentent une charge supplémentaire pour les pays de la partie orientale, en raison de la pauvreté et de l'insuffisance du financement des services de santé. Il fait valoir qu'en ayant recours à des interventions globales bien connues pour s'attaquer aux principaux facteurs de risque (tabagisme, consommation d'alcool, hypertension artérielle, hypercholestérolémie, surcharge pondérale, consommation insuffisante de fruits et de légumes, et sédentarité), il serait possible de prévenir dans une large mesure les problèmes de santé les plus préoccupants : cardiopathie ischémique, troubles dépressifs unipolaires, maladies cérébrovasculaires, troubles dus à un abus d'alcool, maladies pulmonaires chroniques, cancer du poumon et traumatismes résultant d'accidents de la circulation. Il met ainsi en évidence la nécessité d'agir. Le Rapport sur la santé en Europe 2005 porte plus particulièrement sur la santé des enfants, car celle-ci détermine la santé pendant toute l'existence et au cours de la génération suivante. Il souligne que les problèmes de santé des enfants et des adultes ne sont pas les mêmes, et qu'il existe d'importantes différences dans les causes et les taux de mortalité et de morbidité chez les enfants dans la Région. Il met ainsi en évidence la nécessité de politiques complémentaires ciblant les adultes et les enfants, et la complexité de la tâche dont les pays doivent s'acquitter pour améliorer la santé des enfants. Le rapport reconnaît que chaque pays doit suivre sa propre voie, mais montre que la pauvreté et l'inégalité socioéconomique sont les principales menaces qui pèsent sur la santé des enfants; il demande l'accomplissement d'efforts accrus en matière de protection et de promotion de la santé; et il dresse, à partir d'informations factuelles, une liste des caractéristiques des politiques et des programmes les plus efficaces. Investir dans la santé des enfants, c'est investir dans l'avenir. ISBN 92-890-2376-7 – Pages : 144 (allemand, anglais, français et russe) – WHO Press 1211 geneva 27, Switzerland – Tél. : +41 22 791 24 76 – Fax : + 41 22 791 48 57 – Email : [email protected] – http://who.int/bookorders 368 Dossier « Cœur et Armées » : Divers CŒUR ET SPONDYLARTHROPATHIES U. VINSONNEAU, A. BRONDEX, C. VANOYE, P. GODON, G. QUINIOU RÉSUMÉ Les spondylarthropathies sont caractérisées par une atteinte inflammatoire des enthèses axiales et/ou périphériques. La morbi-mortalité cardiovasculaire de ce groupement de pathologies, ne s’explique pas uniquement par les classiques complications valvulaires et les troubles conductifs rencontrés. Cette morbi-mortalité est secondaire d’une part, à une prévalence accrue de certains facteurs de risque conventionnels et au risque spécifique de cette pathologie rhumatismale et d’autre part, aux thérapeutiques utilisées et à une sous estimation des comorbidités cardiovasculaires. Ces patients nécessitent donc une prise en charge globale, dont l’estimation de leur risque cardiovasculaire absolu. Mots-clés: Mortalité cardiovasculaire. Spondylarthropathies. ABSTRACT CARDIOVASCULAR DISEASES IN SPONDYLARTHROPATHIES. Spondylarthropathies refer a group of inflammatory arthrites caracterized by an association with HLA B27 and the development of sacroiilitis and enthesitis. Spondylarthropathies appear to be associated with an increased cardiovascular mortality and morbidity. Available data indicates an increased cardiovascular risk in spondylarthropathies. This postulated could be caused by a higher prevalence of conventional cardiovascular risk factors, but also a specific risk factor for developing cardiovascular disease, and the undertreatment of cardiovascular comorbidity. Rheumatologists should be aware of the enhanced cardiovascular risk in patients with spondylarthropathies. Keywords: Cardiovascular disease. Spondylarthropathies. (Médecine et Armées, 2006, 34, 4, 369-374) I. INTRODUCTION. Les spondylarthropathies (SP) regroupent un ensemble de pathologies dont la lésion élémentaire est une atteinte inflammatoire des enthèses axiales et/ou périphériques. Les manifestations cardiovasculaires classiques sont dominées par une atteinte valvulaire aortique, des troubles conductifs, parfois des myocardites et rarement des péricardites. Celles-ci sont de sévérités variables et conditionnent le pronostic vital. Cependant, ces manifestations n’expliquent pas totalement la surmortalité d’origine cardiovasculaire (1). En effet, les SP sont associées à une augmentation de la prévalence des facteurs de risque cardiovasculaires conventionnels et sont considérées comme un facteur de risque indépendant à part entière. Paradoxalement, il existe aussi une sous estimation de la morbidité cardiovasculaire chez ces patients fréquemment algiques (2). U. VINSONNEAU, médecin principal, praticien confirmé. A. BRONDEX, médecin lieutenant, praticien en formation. C. VANOYE, médecin lieutenant, praticien en formation. P. GODON, médecin en chef, praticien certifié. G. QUINIOU, médecin en chef, praticien certifié. Correspondance : U. VINSONNEAU, Service de cardiologie, HIA Clermont Tonnerre, BP 41, 29240 Brest Armées. médecine et armées, 2006, 34, 4 II. SPONDYLARTHROPATHIES. A) DÉFINITION. Les spondylarthropathies (SP) constituent un groupe homogène de rhumatismes inflammatoires comprenant : la spondylarthrite ankylosante, les arthrites réactionnelles ou syndrome de Reiter, le rhumatisme psoriasique, les manifestations articulaires des entérocolopathies inflammatoires chroniques (maladie de Crohn et rectocolite hémorragique) ainsi que les spondylarthropathies indifférenciées. Les SP ont en commun un terrain génétique comme l’atteste l’existence de cas familiaux et la forte liaison avec l’antigène d’histocomptabilité de classe I : HLA B27. Elles sont caractérisées sur le plan clinique et radiologique par des enthésopathies axiales (pelvi-rachidienne) et des arthrites périphériques. Les atteintes extra articulaires intéressent la peau, l’appareil uro-génital, l’appareil digestif, l’œil et plus rarement le système cardiovasculaire (3). B) ÉPIDÉMIOLOGIE. Les SP se déclarent le plus souvent chez l’adulte jeune entre 16 et 30 ans, mais il existe des formes précoces avant 369 D O S S I E R l’âge de 15 ans (arthrites chroniques juvéniles) (4). En Europe 10 % à 15 % des SP débutent avant 15 ans alors que dans les pays du Maghreb ce pourcentage est de l’ordre de 30 %. On note une prépondérance masculine pour la spondylarthrite ankylosante (2 à 3 hommes pour 1 femme) ainsi que pour les formes génito-urinaires des arthrites réactionnelles (2 à 6 hommes pour 1 femme). La prévalence des SP est de l’ordre de 0,2 % à 0,5 % et donc proche de celle de la polyarthrite rhumatoïde (5, 6). Par ailleurs, il est intéressant de noter que la prévalence de la spondylarthrite ankylosante est en hausse en raison d’une meilleure connaissance des formes cliniques juvéniles, féminines et frustres et qu’il en est de même du rhumatisme psoriasique. À l’inverse, la prévalence des arthrites réactionnelles est en baisse dans les pays occidentaux du fait de la modif ication de l’écologie bactérienne et de l’utilisation plus fréquente des antibiotiques. Enfin, les sujets vivants ou originaires du Maghreb ainsi que les sujets infectés par le VIH sont plus à risque de développer une SP (7). C) CRITÈRES DIAGNOSTIQUES DES SPONDYLARTHROPATHIES. L’European Spondylarthropathy Study Group (ESSG) a établi des critères diagnostiques cliniques et radiologiques dont la sensibilité et la spécificité sont de 87 %. Il est ainsi décrit des critères mineurs et des critères majeurs. Le diagnostic est retenu si au moins un critère majeur et un critère mineur sont présents (tab. I) (8) Tableau I. Critères diagnostiques des spondylarthropathies selon l’ESSG. Critères majeurs – Douleurs rachidiennes inflammatoires – Synovites asymétriques ou prédominant aux membres inférieurs Critères mineurs – Antécédents familiaux de SP – Psoriasis – Maladie inflammatoire intestinale – Urétrite – Diarrhée aiguë – Douleurs fessières à bascule – Enthésopathie – Sacro iléite radiologique D) MORTALITÉ DES SPONDYLARTHROPATHIES. La mortalité des spondylarthropathies est accrue par rapport à une population témoin, et s’avère d’origine cardiovasculaire (9-13) (tab. II). Cette surmortalité est une notion peu connue et ne s’explique pas par les classiques complications des SP. En effet, ce groupe de pathologie rhumatismale voit son risque cardiovasculaire augmenté du fait de son mode de vie, des traitements associés et probablement des facteurs propres au rhumatisme inflammatoire (2). 370 Tableau II. Évaluation de la mortalié cardiovasculaire au cours de spondylarthrite ankylosante. Auteurs/ année Nombre de patients Décès observés Radford et al ; 1977 (10) 836 42 33 1,29 Karprove et al ; 1980 (11) 138 25 12 2,13 Smith et al ; 1982 (12) 14111 476 355 1,2 Décès Observés/ attendus attendus III. COMPLICATIONS CARDIOVASCULAIRES CLASSIQUES DES SPONDYLARTHROPATHIES. La racine aortique est la cible préférentielle de la maladie. Les lésions histologiques sont décrites au niveau des trois tuniques de la paroi artérielle. L’adventice est le siège d’un épaississement qui renferme des inf iltrats lympho-plasmocytaires non spécifiques en manchon autour des vasa-vasorum dont l’intima peut s’épaissir. La média-aortique voit son architecture élastique dissociée par des cicatrices f ibreuses mutilantes et parfois des éléments inflammatoires. L’intima est le siège d’une fibrose sous endothéliale notamment à la base d’insertion des sigmoïdes. En continuité avec cette sclérose inflammatoire aorto-sigmoidienne, des coulées d’aspect semblable viennent empâter la base des cupules sigmoidiennes et la région sous-sigmoidienne où elles forment un petit bourrelet (bombement sous-aortique ou « subaortic bump »). Une extension vers la grande valve mitrale et le septum est possible. Cette topographie lésionnelle explique les atteintes cardiaques centrées sur la valve aortique essentiellement ainsi que les troubles conductifs. A) ATTEINTE DE LA RACINE AORTIQUE ET INSUFFISANCE AORTIQUE. Les anomalies de la racine aortique (insuff isance aortique exclue) sont rapportées chez 61 % des patients porteurs d’une spondylarthrite ankylosante en échographie cardiaque (14, 15). On peut observer un épaississement pariétal de la paroi postérieure de la racine (16). Il peut exister une dilatation de la racine aortique en regard de la valve sans dilatation des sinus de Valsalva ou de la jonction sino-tubulaire (17). Malgré cette atteinte aortique, on ne rapporte pas dans la littérature de cas de dissection ou d’anévrysme de l’aorte initiale. Au niveau valvulaire, l’atteinte débute par un épaississement des sigmoïdes aortiques (épaississement de 2 mm sur au moins deux sigmoïdes). Cet épaississement peut prendre la forme d’un nodule hyper-échogène à contour régulier. L’insuffisance aortique résulte à la fois d’une distension de l’aorte initiale, d’un épaississement et de l’éversion des bords libres des sigmoïdes aortiques vers le u. vinsonneau ventricule gauche. Les prolapsus sont rares (4 % des cas) (16). L’insuffisance aortique survient habituellement vers l’âge moyen de la vie ou après 10 à 15 ans d’évolution de la maladie. Une, des premières séries, rapportée évaluait la prévalence de l’insuffisance aortique clinique au cours des spondylarthrites ankylosantes à 2% à 10 ans et à 12% après 30 ans d’évolution (18). Deux études plus récentes, sur des effectifs restreints (24 et 29 patients), ont évalué en échographie trans-thoracique (ETT) et/ou trans-œsophagienne (ETO), cette prévalence à respectivement 34 % et 30 % à 10 ans d’évolution (14, 15). Ces insuffisances aortiques sont le plus souvent modérées et nécessitent rarement un remplacement valvulaire. En échographie, le bombement sous-aortique correspond à un épaississement hyperéchogène de la jonction aorto-mitrale et est défini en ETO par une longueur supérieure à 7,7 mm et une hauteur supérieure à 3,2 mm (15, 17). B) INSUFFISANCE MITRALE. Une atteinte mitrale est rapportée en échographie trans-thoracique par Roldan et al chez 30 % de l’effectif d’une série de 44 sujets atteints d’une spondylarthrite ankylosante (16). Ils ont observé un épaississement de la base de la valve mitrale antérieure, évoquant une extension mitrale du bombement sous-aortique chez tous les patients qui avaient une insuff isance mitrale au moins modérée. Cet épaississement est à l’origine d’une restriction des mouvements de la valve mitrale antérieure avec conservation de la mobilité de ses portions moyennes et distales, responsable de l’insuffisance mitrale. D’autres mécanismes susceptibles d’entraîner une régurgitation mitrale ont aussi été décrits. Il s’agit de prolapsus valvulaires mitraux antérieurs ou postérieurs, de dilatation du ventricule gauche secondaire à une insuffisance aortique et de greffe oslérienne. L’association d’une régurgitation mitrale et aortique est parfois décrite (6). C) TROUBLES DE LA CONDUCTION AURICULO-VENTRICULAIRE. Ils sont secondaires au processus inflammatoire atteignant le septum membraneux siège des voies de conductions. Tous les degrés de bloc auriculo-ventriculaire peuvent être observés. Il s’agit en général d’un simple allongement de l’espace PR associé ou non à un trouble de la conduction intra-ventriculaire. Ils sont associés près d’une fois sur deux à une insuff isance aortique. En l’absence de celle-ci, ils sont rarement présents (19). La topographie de ces troubles appréciée par une exploration électrophysiologique objective un bloc nodal ou infra nodal (20). Les blocs auriculoventriculaires complets sont retrouvés chez 1 % à 9 % des patients atteints d’une spondylarthrite ankylosante et peuvent évoluer par poussées, régressives le plus souvent sous traitement anti-inflammatoire stéroïdien. Les blocs de haut grade permanent nécessitant la mise en place d’un stimulateur cardiaque définitif sont en fait rares et signent une cicatrice fibreuse définitive des voies de conductions cœur et spondylarthropathies (21). La prévalence d’un bloc complet au cours d’une arthrite réactionnelle est estimée à 6 % par Good et al dans une série historique de 1974 de 164 patients (22). D) AUTRES TROUBLES CONDUCTIFS. Les dysfonctions sinusales sont rares. Le mécanisme est une oblitération de l’artère du nœud sinusal secondaire à une hypertrophie de l’intima (23). E) ATTEINTES PÉRICARDIQUES. MYOCARDIQUES ET Des tableaux cliniques de myocardite et d’insuffisance cardiaque sont rapportés dans la littérature chez des patients atteints de spondylarthrite ankylosante (19). Ribeiro et al ont observé chez 28 patients atteints de spondylarthrite ankylosante une atteinte de la fonction systolique ventriculaire gauche dans 18 % des cas. Les anomalies échographiques retrouvées sont une dilatation cavitaire et une altération modérée de la fraction d’éjection (24). Brewerton et al ont biopsié le myocarde indifférencié de 30 patients atteints de spondylarthrite ankylosante et retrouvent chez 28 d’entre eux une hypertrophie du tissu de soutien sans inf iltration cellulaire inflammatoire. Ces patients étaient tous normotendus et indemnes d’ischémie myocardique ou d’atteinte valvulaire (25). La dysfonction diastolique est plus fréquente que l’atteinte systolique au cours des spondylarthrites ankylosantes (25, 26), d’autant plus que la maladie évolue depuis au moins quinze ans. Le profil de remplissage est de type trouble de la relaxation et traduit souvent une atteinte infra-clinique (27, 28). La prévalence varie de 20 % à 53 % selon les auteurs (25, 29). L’atteinte péricardique est le plus souvent asymptomatique et rare avec moins de 1 % des patients présentant un tableau clinique de péricardite (26). La présence en échographie d’un épanchement péricardique dans la spondylarthrite ankylosante est en revanche plus souvent rapportée et varie énormément selon les auteurs entre 4 % et 42 % sans explication précise (30, 31). Il est malheureusement bien diff icile de tirer des conclusions d’études non randomisées portant sur des effectifs réduits. IV. SPONDYLARTHROPATHIES ET FACTEURS DE RISQUE CARDIOVASCULAIRES CONVENTIONNELS. A) TABAGISME. Le tabagisme actif chez des patients atteints de spondylarthrites ankylosantes est un facteur de mauvais pronostic fonctionnel. En effet, les auteurs ont observé qu’un tabagisme actif est associé à une atteinte clinique et radiologique plus sévère par rapport à une population de non-fumeurs. Cette atteinte fonctionnelle est un facteur prépondérant de sédentarité, majorant ainsi (32, 33) le risque cardiovasculaire de ces patients. 371 D O S S I E R B) BILAN LIPIDIQUE. Pour certains auteurs, le prof il lipidique des SP serait caractérisé par une diminution du cholestérol total avec une baisse privilégiée du HDL cholestérol (34, 35). Mais ces résultats méritent d’être conf irmés pour Rossner et al (36). C) AUTRES FACTEURS CONVENTIONNELS. DE RISQUES La prévalence de l’hypertension artérielle au cours des SP est sensiblement identique à la population générale et est estimée entre 8 % et 18 % (2, 37). Les SP n’ont pas d’influence sur le poids des patients, en effet il n’existe pas d’augmentation significative de l’indice de masse corporelle chez les patients atteints de rhumatisme inflammatoire par rapport à la population générale (35). Enfin, il n’existe pas de données épidémiologiques sur l’association spondylarthropathies et diabète. Ainsi, pour certains auteurs, il existe une prévalence accrue des facteurs de risques cardiovasculaires conventionnels chez les patients porteurs de spondylarthropathies (2). En pratique, la modification du profil lipidique avec une diminution du HDL cholestérol ainsi que le tabagisme actif sont deux facteurs de risques cardiovasculaires majeurs à contrôler chez les patients atteints de SP. V. SPONDYLARTHROPATHIES: UN FACTEUR DE RISQUE CARDIOVASCULAIRE SPÉCIFIQUE. Une augmentation de la morbidité cardiovasculaire au cours des SP n’est pas seulement liée aux atteintes classiques des SP et à l’augmentation de la prévalence des facteurs de risques conventionnels. La diminution de l’activité physique, le terrain génétique HLA B27 et l’inflammation jouent un rôle propre (2). A) DIMINUTION DE L’ACTIVITÉ PHYSIQUE. Plusieurs critères influençant l’incapacité physique ont été mis en évidence. Il s’agit des douleurs aiguës ou chroniques, axiales et périphériques, du tabagisme actif, de la dépression, mais aussi de l’anxiété, de l’âge et du sexe féminin (38) Ces différents facteurs conduisent à terme à la sédentarité. B) TERRAIN GÉNÉTIQUE HLA B27. La physiopathologie des spondylarthropathies fait appel à un terrain immunogénétique prédisposant (HLA B27). L’enthèse est le siège électif de l’atteinte inflammatoire, mais pas seulement du fait de l’observation d’une atteinte extra articulaire notamment cardiaque au cours de ces maladies. L’Ag HLA B27 est un facteur génétique important dans la genèse de troubles conductifs de haut grade (19). En effet, Bergfeldt et al ont observé chez des patients appareillés pour troubles conductifs de haut grade et indemnes de rhumatisme inflammatoire, une prévalence augmentée de l’Ag HLA B27. Ces auteurs ont également observé sur une série de 223 patients appareillés pour bloc auriculo-ventriculaire de haut 372 grade, une prévalence supérieure à celle attendue dans une population témoin de spondylarthrites ankylosantes (13 patients soit 6 %) et d’arthrites réactionnelles (15 patients soit 9 %). L’Ag HLA B27 était présent chez 22 des 28 patients avec atteintes rhumatologiques. Les auteurs ont ainsi déf ini le concept du « HLAB27 associated cardiac disease » où l’Ag HLA B27 serait un facteur génétique prédisposant aux troubles conductifs de haut grade (19). Cependant, cette hypothèse reste à confirmer par d’autres études. C) INFLAMMATION ET ATHÉROSCLÉROSE ACCÉLÉRÉE. L’athérosclérose est responsable d’une augmentation de la mortalité cardiovasculaire au cours des maladies inflammatoires chroniques telles que la polyarthrite rhumatoïde ou le lupus érythémateux disséminé. Il est démontré que l’inflammation chronique favorise la formation des plaques d’athérome et participe à l’instabilité de celles-ci (39). Certains auteurs ont utilisé le terme d’athérosclérose accélérée secondaire aux maladies inflammatoires chroniques. L’élévation de la C réactive protéine, du fibrinogène et des plaquettes sont des marqueurs spécifiques de l’athérosclérose précoce (40-43). Cette relation n’est pas déf initivement démontrée dans les spondylarthropathies car peu de données sont disponibles. Laurent et al ont montré qu’une élévation signif icative du f ibrinogène est retrouvée chez des sujets atteints de SP et qu’elle reflète l’activité inflammatoire de la maladie (44). Les données sur la corrélation CRP et activité inflammatoire de la maladie sont contradictoires. Ruof et al ne retrouve pas d’élévation significative du taux de CRP chez des sujets atteints de spondylarthrite ankylosante en dehors des poussées inflammatoires (45), alors qu’une élévation significative et chronique de la CRP serait associée aux formes cliniques de spondylarthrite ankylosante avec arthrites périphériques ainsi qu’au rhumatisme psoriasique, pour Spoorenberg (44, 46). VI. SOUS-ESTIMATION CARDIOVASCULAIRE. DU RISQUE Les atteintes cardiaques classiques des SP sont le plus souvent bien connues par les cliniciens. En revanche, l’influence de ces pathologies sur le risque cardiovasculaire absolu l’est moins. Reldeimer et al (47) ont ainsi montré qu’il existe une sous estimation des facteurs de risque conventionnels chez les patients atteints de pathologies chroniques rhumatologiques. De plus, la prise en charge thérapeutique rhumatologique est parfois délétère d’un point de vue cardiovasculaire. En effet, le traitement des spondylarthropathies est centré sur les anti-inflammatoires non stéroïdiens (AINS) dont le rôle est reconnu dans la déstabilisation de l’équilibre tensionnel. Pope et al ont ainsi montré au cours d’une méta-analyse que les AINS interfèrent avec les traitements anti-hypertenseurs, notamment ceux dont u. vinsonneau la cible d’action est le système rénine-angiotensinealdostérone, en les inhibant (48). Whelton et al ont comparé, dans une population de patients souffrant de rhumatisme inflammatoire chronique et d’hypertension artérielle, le Celecoxib et le Rofecoxib. Les résultats ont montré que le Rofecoxib déstabilise plus l’équilibre tensionnel que le Cerecoxib lors de traitement concomitant par béta-bloquant, inhibiteur de l’enzyme de conversion ou antagoniste des récepteurs de l’angiotensine 2. En revanche, ces molécules n’ont pas d’influence sur la pression artérielle des patients traités par inhibiteurs calciques ou diurétiques (49). Depuis, le Rofecoxib a été retiré du marché devant les résultats intermédiaires de l’étude APPROVe qui montraient un risque deux fois plus important de présenter un événement cardiovasculaire de type infarctus du myocarde ou accident vasculaire cérébral chez les patients traités (50). En pratique, le clinicien doit rester vigilant devant l’association d’un traitement anti-hypertenseur et d’un AINS quant à l’équilibre tensionnel. Son choix thérapeutique doit être guidé par la connaissance des interactions des AINS et des molécules agissant sur le système rénine-angiotensine. Le traitement de fond des SP a connu une révolution avec l’avènement des anti-TNF-alpha (notamment l’Infliximab). Nous rappellerons que ce traitement présente quelques restrictions d’usage chez l’insuffisant cardiaque car contre-indiqué dans l’insuff isance cardiaque évoluée et à manier avec précautions dans les formes plus légères. Les effets secondaires rapportés sont multiples, rythmiques tensionnels et thrombotiques. Enfin, dans le cadre de la prise en charge des douleurs thoraciques aux urgences, la responsabilité du rhumatisme inflammatoire dans la genèse de ces douleurs est parfois trop rapidement évoquée, laissant dès lors peu de place au diagnostic d’insuff isance coronarienne (31). VII. RHUMATOLOGUE ET CARDIOLOGUE : UNE ALLIANCE OPPORTUNE. Ainsi, la mortalité cardiovasculaire accrue des patients atteints de spondylarthropathie nécessite une surveillance cardiologique adaptée. À côté des atteintes cardiaques classiques, la surveillance doit porter sur l’évaluation et le traitement des facteurs de risque conventionnels chez un patient susceptible de développer une athérosclérose précoce. Un bilan comprenant un examen clinique, un électrocardiogramme et une échographie transthoracique sont le plus souvent effectués à la demande des rhumatologues, en présence d’un point d’appel clinique, autour de la dixième année d’évolution, quand apparaissent les atteintes cardiaques classiques. Une évaluation plus précoce, permettant d’évaluer le risque cardiovasculaire absolu et de dépister une insuffisance coronaire, serait certainement intéressante dans la prise en charge de ces patients. Le clinicien devra alors s’adapter et proposer un examen fonctionnel interprétable (scintigraphie au dypiridamole, échographie de stress), en cas de limitations fonctionnelles. VIII. CONCLUSION. Les manifestations cardiaques au cours des spondylarthropathies ne se limitent pas aux classiques atteintes valvulaires aortiques et aux troubles conductifs. Il existe fréquemment une augmentation du risque cardiovasculaire absolu chez ces patients, nécessitant une gestion globale des spondylarthropathies, où le cardiologue a pleinement sa place. RÉFÉRENCES BIBLIOGRAPHIQUES 1. Khan MA, Khan MK, Kushner I. Survival among patients with ankylosing spondylitis : a life-table analysis. J Rheum 1981 ; 8 : 86-90. 2. Peters JM, Van der Horst-Bruinsma IE, Dijkmans BA, Nurmohamed MT. Cardiovascular risk profile of patients with spondylarthropathies, particularly ankylosing spondylitis and psoriasic arthritis. Semin Arthritis Rheum 2004 ; 34 : 585-92. 3. Sibilia J, Pham T, Sordet C, Jaulhac B, Claudepierre P. Spondylarthrite ankylosante et autres spondylarthropathies. EMCMédecine 2005 ; 2 : 488-511. 4. Guillemin F, Saraux A, Guggenbuhl P, Fardellone P, Fautrel B, Masson C et al. Prévalence de la polyarthrite rhumatoïde et des spondylarthropathies en France en 2001.Rev Rhum Mal Osteoartic 2002 ; 69 : 1 014. 5. Saraux A, Guedes C, Allain J, Devauchelle V, Valls I, Lamour A et al. Survey of rheumatoidarthritis and spondylarthropathy in brittany. J Rheumatol 1999 ; 26 : 2 622-6. 6. Abergel E, Cohen A, Gueret P, Roudaut R. Échocardiographie clinique de l’adulte. Issy-les-Moulineaux : Édition ESTEM, 2003 ; 2 : 1 173-5. cœur et spondylarthropathies 7. Zachariae H. Prevalence of joint disease in patients with psoriasis : implications for therapy. Am J Clin Dermatol 2003 ; 4 : 441-7. 8. Dougados M, Van der Linden S, Juhlin R, Huitfeldt B, Amor B, Calin A et al. The European spondylarthropathy study group preliminary criteria for the classification of spondylarthropathy. Arthritis Rheum 1991 ; 34 : 1 218-27. 9. Lehtinen K. Mortality and causes of death in 398 patients admitted to hospital with ankylosing spondylitis. Ann Rheum Dis 1993 ; 52 : 174-6. 10. Radford EP, Doll R, Smith PG. Mortality among patients with ankylosing spondylitis not given X ray therapy. N Engl J Med 1977 ; 11 : 572-6. 11. Karprove RE, Little AH, Graham DC, Rosen PS. Ankylosing spondylitis ; survival in men with and without radiotherapy. Arthritis Rheum 1980 ; 23 : 57-61. 12. Smith PG, Doll R. Mortality among patients with ankylosing spondylitis after a single treatment course with X-ray. BMJ 1982 ; 13 : 449-60. 13. Carter ET, McKenna CH, Brian DD, Curland LT. Epidemiology of ankylosing spondylitis in Rochester, Minnesota, 1935-1975. 373 D O S S I E R Arthritis Rheum 1979 ; 22 : 365-70. 14. Arnason JA, Patel AK, Rahko PS, Sundstrom WR. Transthoracic and transoesophageal echocardiographic evaluation of the aortic root and subvalvular structures in ankylosing spondylitis. J Rheumatol 1996 ; 23 : 120-3. 15. O’Neill TW, King G, Graham IM, Molony J, Bresnihan B. Echocardiographic abnormalities in ankylosing spondylitis. Ann Rheum Dis 1992 ; 51 : 652-4. 16. Roldan CA, Chavez J, Wiest PW, Qualls CR, Crawford MH. Aortic root disease and valve disease associated with ankylosing spondylitis. Am J Cardiol 1998 ; 32 : 1397-404. 17. Tucker CR, Fowles RE, Calin A, Popp RL. Aortitis in ankylosing spondylitis. Early detection of aortic root abnormalities with two dimensional echocardiography. Am J Cardiol 1982 ; 49 : 680-6. 18. Graham DC, Smythe HA. The carditis and aortitis of ankylosing spondylitis. Bull rheum Dis 1958 ; 9 : 171-4. 19. Bergfeldt L. HLAB27 associated cardiac disease. Ann Intren Med 1997 ; 127 : 621-8. 20. Hassel D, Heinsimer J, Califf RM, Benson A, Rice J, German L. Complet heart block in reiters syndrome. Am J Cardiol 1984 ; 53 : 967-8. 21. Sukenik S, Pras A, Buskila D, Katz A, Snir Y, Horowitz J. Cardiovascular manifestations of ankylosing spondylitis. Clin Rheumatol 1987 ; 6 : 588-92. 22. Good AE. Reiter’s disease a review with special attention to cardiovascular and neurologic sequelae. Semin Arthritis Rheum 1974 ; 3 : 263-86. 23. Rajs J, Karlsson T, Bergfeldt L. Cardiopathological findings in a patient suffering of HLA B27 associated heart disease. In : Somogyi E, Sotony P, eds. Proceedings of the ISNUD workshop on Sudden Cardiac death. Budapest : ISNUD Workshop, 1994 : 146-53. 24. Ribeiro P, Morley KD, Shapiro LM, Garnett RAF, Hugues GRV, Goodvin J.-F. Left ventricular function in patients with ankylosing spondylitis and reiter’s disease. Eur heart J 1984 ; 5 : 418-22. 25. Brewerton DA, Gibson DG, Goddard DH, Jones TJ, Moore RB, Pease CT et al. The myocardium in ankylosing spondylitis. A clinical, echographic, and histopathological study. Lancet 1987 ; 1 : 995-8. 26. Wilkinson M, Bywaters EGL. Clinical features and coursesof ankylosing spondylitis. As seen in follow up of 222 hospital referred cases. Ann Rheum Dis 1958 ; 17 : 208-9. 27. Sun JP, Khan MA, Farrhat AZ, Balher RC. Altérations in cardiac diastolic function in patients with ankylosing spondylitis. Int J Cardiol 1992 ; 37 : 65-72. 28. Yildirir A, Aksoyek S, Calguneri M, Oto A, Kes S. Echographic evidence of cardiac involvement in ankylosing spondylitis. Clin rheumatol 2002 ; 21 : 129-34. 29. Crowley JJ, Donnely SM, Tobin M et al. Doppler echographic evidence of the left ventricular diastolic dysfunction in ankylosing spondylitis. Am J Cardiol 1993 ; 71 : 1 337-40. 30. Shah A, Askari AD. Pericardial changes and left ventricular function in ankylosing spondylitis. Am heart J 1987 ; 113 : 1 529-31. 31. O’Neill TW, Bresninan B. The heart in ankylosing spondylitis. Ann Rheum Dis 1992 ; 51 : 705-6. 32. Averns HL, Oxtoby J, Taylor HG, Jones PW, Dziedzic K, Dawes 374 33. 34. 35. 36. 37. 38. 39. 40. 41. 42. 43. 44. 45. 46. 47. 48. 49. 50. PT. Smoking and outcome in ankylosing spondylitis. Scan J Rheumatol 1996 ; 25 : 138-42. Doran MF, Brophy S, Mackay K, Taylor G, Calin A. Predictors of long-termoutcome in ankylosing spondylitis. J Rheumatol 2003 ; 30 : 316-20. Joven J, Rubies-Prat J, Ras MR, de la Figuera M, Licence E, Masdeu S. High density lipoprotein cholesterol subfractions and apoprotein A-Iin patients with rheumatoid arthritis and ankylosing spondylitis. Arthritis Rheum 1984 ; 27 : 1 199-200. Masi AT, Aldag JC, Mohan PC. Significantly lower serum triglyceride levels in ankylosing spondylitis patients than age, gender, and medical service-matched controls : results of multivariate analysis. Arthritis rheum 2000 ; 43 (suppl) : S102. Rossner S. Further studies on serum lipoproteins in connective tissue diseases. Atherosclerosis 1978 ; 31 : 93-9. Alves MG, Espirito-Santo J, Queiroz MV, Madeira H, MaceiraCoelho E. Cardiac alterations in ankylosing spondylitis. Angiogoly 1988 ; 39 : 567-71. Ward MM. Predictors of the progression of functional disability in patients with ankylosing spondylitis. J Rheum 2002 ; 29 : 1 420-5. Van Doomun S, McColl G, Wicks IP. Accelerated astherosclerosis an extraarticular feature of rhumatoid arthritis ? Arthritis Rheum 2002 ; 46 : 862-73. Manzi S, Selzer F, Sutton-Tyrrel K, Fitzgerald SG, Rairie JE, Tracy RP. Prevalence and risk factors of carotid plaque in women in SLE. Arthritis Rheum 1999 ; 42 : 51-60. Yeh ET. CRP as a mediator of disease. Circulation 2004 ; 109 (21 suppl 1) : II 11-4. Kullo IJ, Gau GT, Jamil Tajik A. Novelrsik factors for ayherosclerosis. Mayo Clin Proc 2000 ; 75 : 369-80. Ridker PM, Hennekes CH, Buring JE, Rifai N. Creactive protein ad other markers of inflammation in the prediction of cardiovascular disease in women. N Engl J Med 2000 ; 342 : 836-43. Laurent MR, Panayi GS, Sheperd P. Circulating immune complexes, serum immunoglobins, and acute phase proteins in psoriasis and psoriasis arthritis. Ann Rheum Dis 1981 ; 40 : 66-9. Ruof J, Stucki G. Validity aspect of erythrocyte sedimentation rate and c-reactive protein in ankylosing spondylitis : a literature review. J Rheumatol 1999 ; 26 : 966-70. Spoorenberg A, Van Der Heijde D, De Klerk E, Dougados M, De Vlam K, Mielants H et al. Relative value of erythrocyte sedimentation rate and c-reactive protein in assessment of disease activity in ankylosing spondylitis. J Rheumatol 1999 ; 26 : 980-4. Reldelmeier DA, Tan SH, Booth GL. The treatment of unrelated disorders in patients with chronic medical diseases. N Engl J Med 1998 ; 338 : 1 516-20. Pope JE, Anderson JJ, Felson DT. A meta analyse of the effects of nonsteroidal anti-inflammatory drugs and blood pressure. Arch Intern Med 1993 ; 153 : 477-84. Welthon A, White WB, Bello AE, Puma AJ, Fort J, the SUCCESS-VII investigators. Effects of Celecoxib and Rofecoxib on blood pressure and edema in atients > 65 years of age with systemic Hypertension and osteoarthritis. Am J Cardiol 2002 ; 90 : 959-63. Andrejak M. Coxibs : quel risque cardio-vasculaire ? Concours Med 2004 ; 126 : 1 834-6. u. vinsonneau Dossier « Cœur et Armées » : Divers SYNDROME DE TAKO-TSUBO Une ballonisation apicale transitoire du ventricule gauche F. BARBOU, S. KÉRÉBEL, Y. LEDOLEY, C. JÉGO, P. LAURENT, G. CELLARIER, G. FOUCAULT, C. BOUCHIAT, R. CARLIOZ RÉSUMÉ ABSTRACT Le syndrome de ballonisation apicale transitoire du ventricule gauche ou syndrome de « Tako-tsubo » mime un syndrome coronarien aigu avec sus-décalage du segment ST. Il est caractérisé par une akinésie réversible des segments apicaux et moyens sans lésion coronaire associée ni élévation enzymatique concordante avec l’étendue des territoires akinétiques. Il touche principalement des femmes entre 50 ans et 60 ans et fait suite à un stress émotionnel ou physique. Le pronostic est excellent chez les survivants avec récupération rapide d’une fonction systolique normale. La physiopathologie reste discutée, excluant une myocardite au profit d’une sidération. TAKO-TSUBO SYNDROME : A LEFT VENTRICULAR TRANSIENT APICAL BALLOONING. Mots-clés : Sidération myocardique. Syndrome de ballonisation apicale transitoire du ventricule gauche. Tako-tsubo. Keywords : Left ventricular transient apical ballooning. Myocardial sideration. Tako-tsubo. The syndrome of left ventricular transient apical ballooning, or tako-tsubo syndrome, presents like acute coronary syndrome with ST segment elevation. It is characterised by reversible akinesia of the middle and apical segments with no associated coronary lesion or enzymatic elevation concordant with the extent of the akinetic areas. It mainly affects women between 50 and 60 years old and follows emotional or physical stress. The prognosis is excellent in survivors with a rapid return of normal systolic function. The pathophysiology remains debatable, excluding myocarditis in favour of sideration. (Médecine et Armées, 2006, 34, 4, 375-377) I. INTRODUCTION. II. PRÉSENTATION CLINIQUE. Le syndrome de ballonisation apicale transitoire du ventricule gauche, appelé « Tako-tsubo » par les auteurs japonais en raison de la ressemblance angiographique du ventricule gauche à un vase en terre cuite servant de piège à pieuvres, a été décrit pour la première fois par Dote (1) en 1991. Les principales séries concernent des patients japonais (2-4), plus récemment quelques cas ont été rapportés chez des sujets caucasiens (5-7). Nous nous proposons de faire le point sur cette pathologie méconnue pouvant faire évoquer à tord le diagnostic de syndrome coronarien aigu avec sus-décalage du segment ST. Le syndrome de ballonisation apicale transitoire du ventricule gauche associe un tableau clinique de syndrome coronarien aigu avec sus-décalage du segment ST à une libération limitée des enzymes de nécrose myocardique et à l’absence de sténose coronaire angiographique significative. Il touche essentiellement des femmes entre 60 ans et 70 ans (âge moyen 67 ans) (2) et débute par une douleur angineuse faisant suite à un stress émotionnel ou physique (2-7). Plus rarement, il succède à un accident vasculaire cérébral, une crise d’asthme ou une chirurgie extracardiaque (2). Un facteur déclenchant est retrouvé dans 67 % à 100 % des cas. Les patients peuvent avoir des signes d’insuffisance cardiaque gauche (6 des 13 patients de Desmet) (5), allant de la simple dyspnée d’effort jusqu’au choc cardiogénique. Plus rarement (2, 3), le motif d’hospitalisation est la survenue d’un malaise ou d’une syncope liés à des troubles de la conduction auriculo-ventriculaire (8 % à 16 % des patients). F. BARBOU, médecin principal, praticien confirmé. S. KÉRÉBEL, médecin principal, praticien confirmé. Y. LEDOLEY, praticien en formation. C. JÉGO, médecin principal, praticien certifié. P. LAURENT, médecin principal, praticien certifié. G. CELLARIER, médecin en chef, praticien certifié. G. FOUCAULT, médecin en chef, praticien certifié. C. BOUCHIAT, médecin en chef, praticien certifié. R. CARLIOZ, médecin en chef, professeur agrégé du SSA. Correspondance : F. BARBOU, Service de cardiologie, HIA Sainte-Anne, BP 600, 83800 Toulon Armées. médecine et armées, 2006, 34, 4 375 D O S S I E R Typiquement, l’électrocardiogramme (fig. 1) montre à la phase aiguë un sus-décalage du ST de V3 à V6, sans miroir, qui est suivi en quelques jours par une inversion des ondes T (3) et parfois de petites ondes q transitoires. Plus rarement, l’ECG ne montre qu’une ischémie sous-épicardique ou se révèle normal (4). L’intervalle QT est fréquemment allongé dès l’admission, avec un maximum au 2e ou 3e jour. Une équipe japonaise (8) a déterminé des critères ECG permettant de différencier le syndrome de Tako-tsubo et les patients présentant un infarctus antérieur transmural aigu. L’absence d’images en miroir assure une sensibilité de 100 %. Associée à un rapport de la somme des sus-décalages ST V4-V6/V1-V3 supérieur ou égal à un, la spécificité est de 100 %. Il s’agit néanmoins d’une étude rétrospective portant sur un collectif de seulement 26 patients. L’augmentation des biomarqueurs cardiaques est modérée et n’est jamais corrélée à l’importance des territoires akinétiques. La ballonisation apicale se caractérise à l’échocardiographie et à la ventriculographie (fig. 2) par une akinésie des segments apicaux et moyens associée à une hyperkinésie des segments de la base. La coronarographie doit toujours être réalisée en urgence de manière à éliminer une occlusion coronaire épicardique, celle-ci est le plus souvent normale et ne montre pas de lésion compatible avec l’étendue de la zone akinétique. Figure 2. Ventriculographie initiale en OAD. Akinésie des segments antérolatéral, diaphragmatique, septo-apical, inféro-postérieur, apical et hyperkinésie des segments de la base. IV. PHYSIOPATHOLOGIE. Le pronostic est bon chez les survivants avec récupération systématique d’une fonction ventriculaire gauche normale en deux semaines (fig. 3) (5). Dans la série de Tsuchihashi (2) on ne note qu’un décès pour 88 patients, survenu par défaillance poly-viscérale. La phase aiguë peut parfois être émaillée par des complications rythmiques, une insuffisance cardiaque gauche voire un choc cardiogénique nécessitant le recours aux amines vasopressives, à la mise en place d’un ballonnet de contre pulsion intra-aortique voire d’une assistance ventriculaire (2, 3). Le traitement est empirique, associant le plus souvent IEC, inhibiteurs calciques, dérivés nitrés et diurétiques. Dans quelques cas, les bêtabloquants ont été employé avec succès (5). Enfin, il semble qu’une récurrence à distance soit possible, trois cas ont été décrits avec un intervalle libre de 1 an à 6 ans (2, 5). La physiopathologie de ce syndrome reste discutée et inexpliquée. L’hypothèse d’une myocardite peut être exclue car il n’a jamais était retrouvé de syndrome inflammatoire, d’élévation des anti-corps antiviraux ni d’anomalie histologique évocatrice sur les biopsies myocardiques (3). L’altération sévère de la cinétique segmentaire associée à une libération limitée des enzymes cardiaques et à une récupération complète relativement rapide de la fonction systolique sont évocateurs d’une sidération myocardique. Cette sidération ne semble pas être liée à un spasme sur une artère épicardique car les tests de provocation sont le plus souvent négatifs (2, 4), les biopsies et les études IRM ne montrent pas de lésion de nécrose (9) et surtout les territoires akinétiques ne sont pas irrigués par une seule artère. De la même façon, on explique mal que des spasmes multiples soient responsables d’une akinésie intéressant systématiquement les mêmes territoires. Pour sa part, Mohri (10) a montré que des spasmes microvasculaires pouvaient être à l’origine d’une ischémie myocardique en l’absence d’anomalie coronaire épicardique. Cette hypothèse est peu probable dans le Tako-tsubo car l’étude doppler intracoronaire à la phase aiguë n’a pas montré d’atteinte de la microcirculation (4). Les défects scintigraphiques de perfusion myocardique, en l’absence d’anomalie du flux coronaire s’expliqueraient par une dysfonction mitochondriale (4, 11). La possibilité d’un obstacle dynamique transitoire de la chambre de chasse du ventricule gauche a été également évoquée comme pouvant être responsable de ce tableau clinique (12). En effet, il a été noté dans Figure 1. ECG initial. Sus-décalage du ST de V1 à V5 sans miroir en inférieur. Figure 3. Ventriculographie en OAD à J10, normalisation de la fonction ventriculaire gauche. III. ÉVOLUTION-PRONOSTIC. 376 f. barbou plusieurs observations l’existence d’un gradient VG/aorte à la phase aiguë (2), gradient lié à un systolic anterior motion (SAM) et régressant avec l’amélioration hémodynamique. L’exposition à une stimulation adrénergique intense serait responsable de l’apparition de cet obstacle chez des patientes présentant une chambre de chasse de petite taille associée à un volume ventriculaire réduit. Il induirait une élévation des pressions intracavitaires et pariétales, une diminution de la perfusion et l’apparition d’une ischémie des portions moyennes et apicales. Toutefois, le gradient VG-aorte n’est pas toujours mis en évidence (13 % dans la série de Bybee (13)), les biopsies endomyocardiques ne montrent pas de signe d’ischémie et Tawarahara (14) a décrit un cas d’anomalie réversible de la cinétique des segments de la base associée à une hyperkinésie apicale qui ne peut être expliquée par un obstacle à l’éjection ventriculaire. Une autre hypothèse est l’action toxique directe des catécholamines sur les myocytes comme cela a été décrit dans l’hémorragie méningée (15). Les récepteurs adrénergiques cardiaques facilitent la perméabilité de la membrane cytoplasmique au calcium qui, en excès dans le cytosol, devient cytotoxique. En outre, les récepteurs adrénergiques sont localisés de façon préférentielle à l’apex du ventricule gauche (16), permettant d’expliquer le retentissement focal du facteur autocrine. Ueyama (17) a développé un modèle animal de ballonisation transitoire du ventricule gauche en soumettant des rats à un stress émotionnel. Cette dernière hypothèse est séduisante d’autant qu’il existe des similitudes histologiques sur les biopsies endomyocardiques de ces patients et les lésions objectivées dans les cardiopathies catécholergiques (18). Le taux de catécholamines circulantes n’est toutefois pas toujours élevé (3). Enfin, Ueyama a suggéré que la baisse du taux d’œstrogènes pourrait expliquer la prédominance de ce syndrome chez la femme âgée (19). La physiopathologie de ce syndrome reste donc à explorer, l’hypothèse d’un mécanisme plurifactoriel ne pouvant être exclue. V. CONCLUSION. Le syndrome de ballonisation apicale transitoire du ventricule gauche est une cardiomyopathie transitoire induite par le stress dont le pronostic est toujours excellent en l’absence de complication initiale. La survenue d’un syndrome coronarien aigu avec sus-décalage du segment ST chez une femme âgée et dans un contexte de stress intense doit faire évoquer le diagnostic et faire préférer une coronarographie en urgence à une éventuelle fibrinolyse. RÉFÉRENCES BIBLIOGRAPHIQUES 1. Dote K, Sato H, Tateishi H et al. Myocardial stunnig due to simultaneous multivessel spasms : a review of 5 cases. J Cardiol 1991 ; 21 : 203-14. 2. Tsuchihashi K, Ueshima K, Uchida T et al. Transient left ventricular apical ballooning without coronary stenosis : a novel heart syndrome mimicking acute myocardial infarction. J Am Coll Cardiol 2001 ; 38 : 11-8. 3. Kurisu S, Sato H, Kawagoe T et al. Tako-tsubo-like left ventricular dysfunction with ST-segment elevation : a novel cardiac syndrome mimicking acute myocardial infarction. Am Heart J 2002; 143: 448-55. 4. Abe Y, Kondo M, Matsuoka R et al. Assessment of clinical features in transient left ventricular ballooning. J Am Coll Cardiol 2003 ; 41 : 737-42. 5. Desmet WJ, Adriaenssens BF, Dens JA. Apical ballooning of the left ventricule : first series in white patient. Heart 2003 ; 89 : 974-6. 6. Ibanez B, Navarro F, Farre J et al. Tako-tsubo transient left ventricular apical ballooning is associated with a left anterior descending coronary artery with a long course along the apical diaphragmatic surface of the ventricule. Rev Esp Cardiol 2004; 57: 209-16. 7. Girod J, Messerli A, Zidar F et al. Tako-tsubo-like transient left ventricular dysfunction. Circulation 2003 ; 107 : e120-1. 8. Riyo O, Yoshikazu H, Takefumi T et al. Specific findings of the standard 12-lead ECG in patients with tako-tsubo cardiomyopathy. Comparison with the findings of acute anterior myocardial infarction. Circ J 2003 ; 67 : 687-90. 9. Wittstein IS, Thieman DR, Lime JA et al. Neurohumoral features of myocardial stunning due to sudden emotional stress. N Engl J Med 2005 ; 352 : 539-48. 10. Mohri M, Koyanagi M, Egashira K et al. Angina pectoris caused by coronary microvascular spasm. Lancet 1998 ; 351 : 1 165-9. syndrome de tako-tsubo 11. Kazuki I, Hiroki S, Shuji K, Akihiro A, Masao N. Assessment of tako-tsubo cardiomyopathy using 99 m TC-tetroformin myocardial SPECT-Comparison with acute coronary syndrome. Ann Nucl Med 2003 ; 17 : 115-22. 12. Villareal RP, Achari A, Wilansky S, Wilson JM. Anteroapical stunning and left ventricular outflow tract obstruction. Mayo Clin Proc 2001 ; 76 : 79-83. 13. Bybee KA, Prasad A, Barsness GW et al. Clinical characteristics and thrombolysis in myocardial infarction frame counts in women with transient left ventricular apical ballooning syndrome. Am J Cardiol 2004 ; 94 : 343-6. 14. Tawarahara K, Matoh F, Odagiri K, Saitoh N. Nuclear cardiac imaging in “Tsubo-like (Pode-like)” transient left ventricular dysfunction. Jpn Circ J 2001 ; 65 Suppl 1A : 420. 15. Kono T, Morita H, Kuroiwa T, Onaka H, Takatsuka H, Fujiwara A. Left ventricular wall motion abnormalities in patients with subarachnoid hemorrhage : neurogenic stunned myocardium. J Am Coll Cardiol 1994 ; 24 : 636-40. 16. Mohri H, Ishikawa S, Kojima S et al. Increased responsiveness of left ventricular apical myocardium to adrenergic stimuli. Cardiovasc Res 1993 ; 27 : 192-8. 17. Ueyama T, Kasamatsu K, Hano T et al. Emotional stress induces transient left ventricular hypocontraction in the rat via activation of cardiac adrenoreceptors. Circ J 2002 ; 66 : 712-3. 18. Kawai S, Suzuki H, Yamaguchi H et al. Ampulla cardiomyopathy (“Tako tsubo” cardiomyopathy) : reversible left ventricular dysfunction with ST segment elevation. Jpn Circ J 2000 ; 64 : 156-9. 19. Ueyama T, Hano T, Kasamatsu k et al. Estrogen attenuates the emotional stress-induced cardiac responses in the animal cardiomyopathy. J Cardiovasc Phamacol 2004 ; 42 : 117-9. 377 D O S S I E R VIENT DE PARAÎTRE POUR UNE ÉTHIQUE DU MÉTIER DES ARMES Vaincre la violence Jean-René BACHELET Avec le général BACHELET – il a commandé à Sarajevo en 1995, et a été le principal artisan d'une réflexion sur l'exercice du métier des armes dans l'armée de Terre qui a abouti à un « code du soldat » –, nous découvrons une armée qui ne veut laisser dans l'ombre aucune des questions qui se posent au soldat dans ce XXIe siècle où l'affrontement armé prend des formes inédites. Mais point de bavardage chez BACHELET. Un souci de tout explorer et de tout dire. Exercer le métier des armes c'est être confronté à la violence, contraint, en dernière instance, de détruire et de tuer. On ne peut donc éluder ni les déterminants politiques, ni les implications éthiques et philosophiques. Ni celles liées directement aux modalités techniques de l'action. L'auteur nous livre ainsi une sorte d'introspection magistrale de l'armée de Terre d'une nation démocratique qui place au centre de ses principes les droits de l'homme, le respect et la dignité de l'Autre, et qui, cependant, doit aussi être capable de faire un usage « efficient » de la force. Jusqu'à tuer cet Autre dont on sait qu'il est un homme et non l'incarnation du Mal. Cela implique que l'armée soit au service de l'autorité légitime – le pouvoir national – et qu'elle ait une double obsession. Être, d'une part, une force efficiente et, d'autre part, maîtriser cette force, lui fixer des limites strictes. Pour des raisons éthiques – afin de ne pas basculer dans la barbarie –, mais aussi parce qu'une « efficience sans limites » est non seulement inutile mais de surcroît contre-productive. Max GALLO L’auteur : Jean-René BACHELET a effectué une carrière militaire complète dans l'armée de Terre jusqu'aux plus hauts niveaux de responsabilités. En tant qu'officier général, il a exercé de multiples commandements, dont celui du secteur de Sarajevo, en 1995. ISBN : 2 7117 7297 8 – Format : 16x24 cm – Pages : 192 – Prix 19 € – Éditions Vuibert 12 rue des Cordelières, 75013 Paris – Tél. : 01 44 08 49 00 – Fax : 01 44 08 49 29 – [email protected] 378 Dossier « Cœur et Armées » : Divers SYNDROME DU MARTEAU HYPOTHÉNAR CHEZ UN JEUNE MILITAIRE P.-L. MASSOURE, M. BEUSTES-STEFANELLI, E. DULAURENT, F. BIRE, J.-M. RIGOLLAUD, P. SHMOOR, S. SKOPINSKI, J.-M. CHEVALIER RÉSUMÉ Le syndrome du marteau hypothénar est une cause rare d’ischémie digitale le plus souvent secondaire à l’occlusion embolique des artères digitales résultant de traumatismes répétés de l’artère ulnaire au niveau de l’arche palmaire. Nous rapportons le cas d’un jeune militaire qui a eu une ischémie digitale secondaire à une embolie à partir d’un anévrysme d’une branche de l’artère ulnaire. Ceci était probablement en rapport avec des traumatismes répétés de la paume de la main, provoqués par son précédent emploi d’électricien. Le diagnostic topographique, difficile à préciser avec l’angiographie par résonance magnétique, a été facilité par l’artériographie préopératoire. L’intervention a consisté en une résection de l’anévrysme et suture artérielle bord à bord sans séquelle à douze mois. Mots-clés : Angiographie par résonance magnétique. Maladie professionnelle. Personnel militaire. Syndrome du marteau hypothénar. I. INTRODUCTION. Les manifestations ischémiques digitales des membres supérieurs sont rares chez l’homme jeune. L’activité professionnelle actuelle ou passée des personnels militaires ou civils est susceptible de provoquer des lésions par traumatismes répétés, en particulier des traumatismes vasculaires. L’observation que nous rapportons illustre les problèmes diagnostiques et thérapeutiques rencontrés dans le syndrome du marteau hypothénar. II. CAS CLINIQUE. Nous rapportons le cas d’un militaire, âgé de 22 ans, droitier, caucasien, engagé depuis un an dans l’armée de P.-L. MASSOURE, médecin principal, praticien confirmé. M. BEUSTESSTEFANELLI. E DULAURENT, médecin lieutenant. F. BIRE, médecin en chef, praticien certifié. J.-M. RIGOLLAUD, médecin en chef, praticien certifié. P. SCHMOOR, médecin en chef, praticien certifié. S. SKOPINSKI, médecin principal, praticien certifié. J.-M. CHEVALIER, médecin chef des services, praticien certifié. Correspondance : P.-L. MASSOURE, Service de pathologies cardio-vasculaires, HIA Robert Picqué, BP 28, 33998 Bordeaux Armées. médecine et armées, 2006, 34, 4 ABSTRACT HYPOTHENAR HAMMER SYNDROME IN A YOUNG MILITARY. Hypothenar hammer syndrome is a rare cause of finger ischemia secondary to embolic occlusion of the digital arteries as a result of repetitive trauma to the palmar ulnar artery. We report the case of a young military found to have digital embolic complications from an ulnar artery aneurysm. This is thought to have developed as a result of palmar trauma experienced during his former job as an electrician. Precise topographic diagnosis was difficult with Magnetic Resonance Angiography whereas arteriography was useful before surgery. Resection of the aneurysm and direct anastomosis was performed with favourable outcome within 12 month of follow up. Keywords : Hypothenar hammer Syndrome. Magnetic resonance angiography. Military personnel. Occupational disease. (Médecine et Armées, 2006, 34, 4, 379-382) Terre comme chauffeur de poids lourds, qui a consulté en urgence pour une sensation « de doigt mort » au niveau du majeur droit, apparue spontanément 48 heures auparavant alors qu’il marchait en montagne. Il a exercé le métier d’électricien pendant trois ans en milieu civil avant de s’engager. Son tabagisme était estimé à trois années tabac, avec consommation occasionnelle de cannabis. Il n’ a jamais pratiqué d’activité sportive particulière en dehors de son activité militaire. Il n’a pas rapporté d’antécédent médical personnel ou familial. Il a consulté en urgence pour une sensation « de doigt mort » au niveau du troisième doigt de la main droite. L’examen local a retrouvé une pâleur et une cyanose au niveau de la 2e et 3e phalange du majeur droit avec une hypoesthésie totale au niveau de ces deux phalanges sans trouble trophique. Le doigt était froid. Il n’y avait pas de lésion cutanée au niveau du doigt, de la main ou des deux membres supérieurs. La manœuvre d’Allen était positive à droite. Le diagnostic d’ischémie sub aiguë du 3e doigt de la main droite a été porté. L’examen clinique général et vasculaire était normal avec perception de tous les pouls sans souffle. La recherche d’une cardiopathie emboligène était négative (ECG, 379 D O S S I E R Holter ECG des 24 heures, échocardiographie trans thoracique et trans œsophagienne). La recherche exhaustive d’une thrombophilie congénitale et acquise était négative. L’échographie Doppler des membres supérieurs était normale au niveau brachial et antébrachial. Les manœuvres positionnelles à la recherche d’un syndrome de la traversée cervico-thoraco-brachiale étaient négatives. L’échographie Doppler artériel des artères palmaires a mis en évidence un anévrysme sur le réseau de l’artère ulnaire mesurant environ 10 mm de grand axe (f ig. 1). L’angiographie par résonance magnétique (ARM) du membre supérieur droit a mis en évidence une artère radiale et ulnaire droite de bon calibre mais il existait une malformation anévrysmale de 8 x 6 mm au dépend d’une branche artérielle siégeant au niveau du carpe médian avec défaut de la vascularisation au niveau de troisième doigt (fig. 2, relue par deux équipes différentes). L’artériographie a redressé le diagnostic topographique car l’anévrysme siégeait au niveau d’une branche de l’artère ulnaire (f ig. 3). Il n’y avait pas d’atteinte controlatérale. Figure 1. Échographie bidimensionnelle des artères palmaires révélant la présence d’un anévrysme de l’artère ulnaire droite. Figure 3. Artériographie des membres supérieurs : anévrysme de l’artère ulnaire droite. L’ensemble des signes cliniques et radiologiques était donc en faveur d’un syndrome du marteau hypothénar. L’origine professionnelle était ici probable (ancien électricien, microtraumatismes répétés au niveau du poignet droit) même si la durée d’exposition était faible. Le patient n’a pas décrit de traumatisme unique ou répété dans son activité de loisir mais il est également possible que le mécanisme causal soit ancien et soit passé inaperçu. En un mois, l’anévrysme a augmenté de volume (11 x 9 mm) et le patient a développé un trouble trophique distal (fissurations et ulcérations). Le traitement médical initial a consisté en une anticoagulation par héparine de bas poids moléculaire à dose curative et molécule vaso-active (buflomédil 400 mg/j intraveineux). Un relais per os est était ensuite proposé ; il associait aspirine (300 mg/jour) et vaso-actifs. Deux mois plus tard, l’intervention chirurgicale a consisté en une résection de l’anévrysme avec suture artérielle simple, bord à bord, sans complication secondaire. L’analyse histologique de l’anévrysme a mis en évidence une fibrodysplasie de la paroi artérielle. À six mois, les troubles trophiques étaient limités. Le patient a été maintenu apte au service (classement S 3 temporaire) à l’exclusion de tout travail de manutention potentiellement traumatique. À douze mois, il n’y avait plus de séquelle trophique. IV. DISCUSSION. Figure 2. Angiographie par résonance magnétique du membre supérieur droit mettant en évidence un anévrysme sur une branche médiane des artères du carpe. 380 Le syndrome du marteau hypothénar (SMH) se présente comme une ischémie digitale unilatérale décrite historiquement par Von Rosen en 1934 (1). Il est provoqué par l’occlusion d’une artère digitale par embolisation à partir de l’artère ulnaire palmaire et est associé à des traumatismes répétés de la paume de la main. Le substrat anatomique est déterminant. Le trajet superficiel de l’artère ulnaire rend ce vaisseau sensible aux traumatismes mécaniques répétés. Il faut noter le rôle de l’os crochu qui peut jouer le rôle « d’enclume » sur laquelle l’artère est traumatisée. De nombreuses p.-l. massoure expositions professionnelles (mécanicien, charpentier, électricien, mineur…) ou sportives (vélo tout terrain, hockey, karaté, badminton, handball, baseball, gardien de but, golf, tennis) sont rapportées (2-6). L’atteinte peut être bilatérale. Cependant, ces activités professionnelles ou sportives sont très répandues et il n’y a que très peu de cas décrits. Les occlusions de l’artère ulnaire peuvent être asymptomatiques ; Little et Ferguson ont dépisté par manœuvre d’Allen et Doppler une occlusion de cette artère chez 14 % des travailleurs manuels utilisant leur main comme un marteau (7). Le facteur traumatique n’est donc pas le seul en cause. Le plus souvent, une dysplasie f ibromusculaire des artères ulnaires est retrouvée comme pour notre patient. Sur le plan histologique, il s’agit d’une hyperplasie intimale, d’une hyperplasie de la média, parfois associée à une effraction de la limitante élastique interne. Sur le plan physiopathologique, l’ischémie peut être provoquée soit par occlusion segmentaire de l’artère ulnaire par un thrombus, soit par un spasme au niveau de l’anévrysme, soit par embolie à partir d’un thrombus intra anévrysmal. Vayssairat et al ont rapporté 17 cas de SMH avec 10 occlusions de l’artère ulnaire et 7 anévrysmes de l’artère ulnaire (6). Dans les plus larges séries, une anomalie angiographique (sténose, ectasie vasculaire, anévrysme) est toujours retrouvée chez les patients symptomatiques (2, 6). Les symptômes cliniques classiques sont l’intolérance au froid au niveau des doigts, un phénomène de Raynaud, la cyanose, une sensation de douleur ischémique comme dans notre observation. La manœuvre d’Allen est le plus souvent positive. L’examen du membre controlatéral s’impose. La palpation d’une masse pulsatile sur le trajet de l’artère ulnaire au niveau du carpe est possible. Des signes neurologiques (paresthésies distales dans le territoire ulnaire) induits par la compression au niveau de l’anévrysme ont été décrits chez 3 patients sur 5 dans la série de Duverger et al (8). Les troubles trophiques (ulcères, fissurations) ne se développent que secondairement. Dans les cas les plus graves, une gangrène digitale et des rétractions ischémiques ont été décrites. Le syndrome du canal carpien, le syndrome du canal de Guyon, et les accidents emboliques systémiques sont les principaux diagnostics différentiels. La recherche d’une thrombophilie congénitale ou acquise est en général négative (2). Les examens d’imagerie sont déterminants tant sur le plan étiologique que pré-thérapeutique. L’exploration doit être bilatérale à la recherche d’une atteinte controlatérale asymptomatique. L’échographie doppler est l’examen de première intention mais ne saurait suffire dans le cadre pré-thérapeutique. L’imagerie non invasive est performante avec en particulier l’ARM qui permet de décrire précisément les lésions, la vascularisation collatérale et permet l’exploration dans le même temps du membre controlatéral. Cependant, cet examen ne donne pas d’information dynamique sur le flux artériel. Cet examen est parfois limité par des problèmes de résolution spatiale comme dans notre observation (9). Ces problèmes sont probablement plus liés aux conditions d’acquisition, syndrome du marteau hypothénar chez un jeune militaire au choix des séquences, qu’aux limites intrinsèques de la technique. L’angioscanner spiralé multi barrettes a des performances équivalentes. Si l’angiographie sélective bilatérale reste pour beaucoup l’examen pré-opératoire de référence, elle peut être prise en défaut lorsque l’anévrysme est thrombosé, éventualité non rare. L’avantage de l’ARM et de l’angioscanner est de permettre la mise en évidence de l’anévrysme même s’il est thrombosé et d’en préciser les rapports anatomiques. Ces examens tendent à devenir les examens de référence. Chez les patients symptomatiques, le traitement chirurgical est indiqué dans les formes anévrysmales. Les interventions les plus fréquentes sont la résection de l’anévrysme et l’anastomose bord à bord comme pour notre patient, ou la résection avec interposition d’un greffon veineux saphène. L’utilisation d’un greffon artériel (épigastrique inférieur) a été récemment proposée (10). Dans les formes non anévrysmales (thrombotique isolée), le traitement est en général conservateur. Le traitement médical n’est pas clairement codif ié et repose sur les antalgiques, les traitements dermatologiques locaux, les antiagrégants et éventuellement l’ilomédine associée aux anticoagulants. La fibrinolyse in-situ (urokinase ou rt-PA) est indiquée dans les cas d’ischémie aiguë sévère avec gangrène. Des perfusions d’antagonistes calciques (diltiazem) sont parfois proposées ainsi que l’hémodilution (2, 6, 10). L’arrêt du tabac et le reclassement professionnel s’imposent (6). Une déclaration comme maladie professionnelle doit être réalisée si l’activité en cause est en lien avec une profession exercée dans la vie civile (tableau n° 69 des maladies professionnelles). Cependant, une durée d’exposition de cinq ans est requise pour pouvoir déclarer le SMH comme maladie professionnelle, ce qui n’était pas le cas de notre patient. Pour notre patient, la survenue de cette ischémie est survenue hors service et son emploi dans l’armée ne prédispose pas à cette pathologie. La poursuite des activités militaires est possible mais dans un emploi qui ne peut en aucun cas entraîner une récidive homo ou controlatérale puisqu’il existe probablement un terrain favorisant (dégénérescence fibromusculaire de la paroi artérielle). Selon l’instruction déterminant l’aptitude médicale à servir dans les forces françaises, les lésions artérielles mécaniques sont classées S, I, G 2 à 6, les anévrysmes et embolies (artères périphériques) S, I, G 4 à 6 (11). Le syndrome du marteau hypothénar, pathologie artérielle traumatique pouvant entraîner une déformation artérielle anévrysmale et des embolies digitales ne fait l’objet d’aucun classement spécifique. La détermination de l’aptitude est à moduler en fonction de la sévérité de l’atteinte, de la gène entraînée et du traitement entrepris. La correction chirurgicale et le reclassement professionnel ont été considérés comme des facteurs de bon pronostic pour notre patient, justifiant le maintien de son aptitude à servir. 381 D O S S I E R V. CONCLUSION. Ce cas typique d’ischémie digitale par syndrome du marteau hytpothénar est original par la faible durée d’exposition professionnelle, et par la difficulté du diagnostic topographique en ARM, diagnostic redressé ici par l’artériographie préopératoire. Cependant, l’ARM et l’angioscanner, examens non invasifs, tendent à devenir les examens de référence. Le traitement chirurgical est habituel devant un anévrysme ulnaire et le reclassement professionnel s’impose dans la mesure de sa compatibilité avec l’aptitude à servir lorsqu’il s’agit d’un militaire. RÉFÉRENCES BIBLIOGRAPHIQUES 1. Von Rosen S. Ein fall von thrombose in der arteria nach einwirkung von stumpfer gewalt. Acta Chir Scand 1934 ; 73 : 500-6. 2. Ferris BL, Taylor LM, Oyama K, Mc Lafferty RB, Edwards JM, Moneta GL et al. Hypothenar hammer syndrome : proposed etiology. J Vasc Surg 2000 ; 31 : 104-13. 3. Kreitner KF, Duber C, Muller LP, Degreif J. Hypothenar hammer syndrome caused by recreational sports activities and muscle anomaly in the wrist. Cardiovasc Interv Radiol 1996 ; 19 : 356-9. 4. Applegate K, Spiegel P. Ulnar artery occlusion in mountain bikers. J Sport Med Phys Fitness 1995 ; 35 : 232-4. 5. De Monaco D, Fritsche E, Rigoni G, Schlunke S, Von Wartburg U. Hypothenar hammer syndrome : retrospective study of nine cases. J Hand Surg 1999 ; 24 : 731-4. 6. Vayssairat M, Debure C, Cormier J, Bruneval P, Laurian C, Juillet Y. Hypothenar hammer syndrome : seventeen cases with longterm-follow-up. J Vasc Surg 1987 ; 5 : 838-43. 7. Little JM, Fergusson DA. The incidence of the hypothenar hammer syndrome. Arch Surg 1972 ; 105 : 684-5. 8. Duverger V, Meyrat L, Singland JD, Bonnet S, Bauer B, Vergos M. Les anévrysmes traumatiques de l’artère cubitale. À propos de cinq cas. e-mémoire de l’Académie nationale de chirurgie 2004 ; 3 (2) : 51-5. 9. Winterer JT, Ghanem N, Roth M, Schaefer O, Lehnhardt S, Thurl C et al. Diagnosis of the hypothenar hammer syndrome by highresolution contrast-enhanced MR angiography. Eur Radiol 2002 ; 12 : 2 457-62. 10. Smith HE, Dirks M, Patterson R. Hypothenar hammer syndrome : digital ulnar artery reconstruction with autologous inferior epigastric artery. J Vasc Surg 2004 ; 40 : 1 238-42. 11. Ministère de la Défense. Instruction N° 2100/DEF/DCSSA/ AST/AME du 1er octobre 2003 modifiée le 18 novembre 2004. BOC N° 50 du 6 décembre 2004 : p. 6416. VIENT DE PARAÎTRE LE COMITÉ D'EXPERTS DE L'OMS SUR LA NORMALISATION BIOLOGIQUE Ce rapport présente les recommandations d'un comité d'experts de l'OMS chargé de coordonner des activités amenant à adopter des exigences internationales pour la production et le contrôle des vaccins et d'autres produits biologiques et à établir des produits biologiques de référence sur le plan international. Le rapport commence par une discussion de sujets généraux portés à l'attention du comité et fournit des informations sur l'état et le développement de produits de référence pour différents anticorps, antigènes, produits et dérivés sanguins, cytokines, facteurs de croissance et substances endocrinologiques. La deuxième partie du rapport, relevant plus particulièrement des fabricants et des autorités législatives nationales, contient des recommandations pour la production et le contrôle de qualité des vaccins conjugués antiméningococcique du groupe C, des indications sur les exigences réglementaires en matière d'évaluation clinique des vaccins, des indications pour la production et le contrôle de la qualité du vaccin oral inactivé contre le choléra, et des indications sur les procédures d'inactivation et de suppression virales destinées à assurer la sécurité virale des produits dérivés du plasma humain. ISBN : 92 4 120924 0 – 232 pages (en langue anglaise) – WHO Press 1211 geneva 27, Switzerland – Tél. : +41 22 791 24 76 – Fax : + 41 22 791 48 57 – Email : [email protected] 382 p.-l. massoure VIENT DE PARAÎTRE SCIENCE EXPÉRIMENTALE ET CONNAISSANCE DU VIVANT La méthode et les concepts Pierre VIGNAIS, Paulette VIGNAIS Ce livre présente l'importance de l'expérimentation, à travers l'histoire jusqu'aux limites que la méthode expérimentale semble connaître aujourd'hui. L'ouvrage permet de comprendre comment les nouveaux instruments, les nouvelles techniques, les découvertes ont engendré des concepts générateurs d'idées qui, une fois testés, ont permis la mise en œuvre de la méthode expérimentale. L'analyse est prolongée jusqu'aux limites que la méthode expérimentale semble rencontrer aujourd'hui (au sens biologique, philosophique, sociologique) face à la complexité du vivant. Le lecteur se trouve ainsi placé face aux questions concernant sa propre identité biologique et l'évolution dans le futur de la science et de la société. D O S S I E R Avec précision et une grande honnêteté intellectuelle, Pierre VIGNAIS propose un travail de mémoire dont chacun peut avoir besoin, une aide à la compréhension historique, une mise au point sur la méthode expérimentale qui a amené la notion de modèles (biologiques, intellectuels). L'ouvrage concerne les biologistes, les médecins, pharmaciens, scientifiques concernés par les sciences du vivant, mais aussi les historiens et philosophes, comme tous les citoyens cultivés soucieux de comprendre les mutations de la science et de la société. Pierre VIGNAIS est professeur honoraire de Biochimie de la Faculté de médecine de Grenoble (Université Joseph F OURIER ). Ses travaux dans les domaines de la biologie cellulaire et des interactions hôtes- pathogènes (plus de 200 publications) font autorité et lui valurent la médaille d'argent du CNRS et le Grand Prix de l'Académie des Sciences. Il est l'auteur de l'ouvrage « La biologie des origines à nos jours » (Grenoble Sciences, EDP Sciences). Paulette VIGNAIS est Directeur de Recherche au CNRS, Laboratoire de Biochimie et Biophysique des Systèmes Intégrés (CEA Grenoble, Direction des Sciences du Vivant). Elle est une spécialiste reconnue des systèmes de réponse adaptative bactérienne et de l'expression des facteurs de virulence. ISBN : 2 86883 897 9 – Pages : 432 pages – Prix : 45 € – EDP Sciences, 17 avenue du Hoggar, Parc d'activités de Courtabœuf - BP 112, 91944 Les Ulis Cedex A. – Contact Presse : Élise CHATELAIN – Tél. : 01 69 18 69 87 – [email protected] 383 RECOMMANDATIONS AUX AUTEURS GÉNÉRALITÉS L'article proposé pour parution dans Médecine et Armées, relate un travail original et spécifique à la médecine dans les armées (fait médical, chirurgical, pharmaceutique, vétérinaire, historique, médico-administratif, épidémiologique…). PRÉSENTATION DU MANUSCRIT • Le manuscrit est fourni: – soit sur papier en trois exemplaires; – soit sur support numérique adressé par voie postale; – soit adressé par E. mail (Internet, Intranet, Lotus); – soit sous forme multiple. • Le manuscrit est rédigé: – en langue française (sauf exception après accord de la rédaction); – en double interlignage en Times new roman corps 12; – recto seulement marge gauche ; – paginé. • La première page comporte: – le titre précis et concis sans abréviation, en lettres capitales accentuées, – le nom du ou des auteurs en lettres capitales accentuées, précédé des initiales du prénom en lettres capitales accentuées (avec trait d'union pour les prénoms composés) séparés par un point. – le nom du ou des auteurs, précédé des initiales du prénom des auteurs suivis du grade et du titre principal; – le nom, l'adresse et les coordonnées téléphoniques, de télécopie ou E-mail de l'auteur destinataire des correspondances, des épreuves à corriger. • La deuxième page est réalisée selon les règles avec: – le titre en français en lettres capitales accentuées; – le titre en anglais ; – le résumé en français de 15 lignes maximum sans abréviation ni référence; – suivi de quatre à cinq mots-clés répertoriés, classés par ordre alphabétique et séparés par un point; – le résumé en anglais suivi des mots-clés répertoriés, classés par ordre alphabétique et séparés par un point. • Le texte: – débute à la troisième page; – est concis, précis et les évènements passés sont écrits au passé composé ; – les abréviations sont en nombre limité et exclues du titre et des résumés et sont explicites lors du premier emploi ; le terme entier est précédé de l'abréviation mise entre parenthèses lors de la première apparition dans le texte; – la terminologie est respectée (symbole, unité, nombre écrit en chiffres sauf ceux inférieurs à dix sept, lorsqu'ils commencent une phrase ou lors d'énumérations fréquentes dans le texte, médicaments). – La présentation est au carré (texte justifié) sans retrait ni interligne, ni gras dans le texte ni mot souligné et selon le plan: I. CHAPITRE. A) SECTION. 1. Article. a) Paragraphe. – alinéa; - sous alinéa, les puces • peuvent être utilisées sans renvois de bas de page. • Les figures (graphiques, illustrations et photographies): – sont en nombre limité; – sont numérotées en chiffres arabes; – sont appelées précisément dans le texte, placées entre parenthèses par ordre d'apparition ; – les photos sont fournies en trois exemplaires (idem pour les radiographies) respectent l'anonymat des patients et peuvent être remplacées par des fichiers numériques (sous format JPEG); – les diapositives sont accompagnées d'un tirage papier; – au verso des figures l'orientation est indiquée; – les légendes sont dactylographiées sur une feuille à part expliquant les unités utilisées (pour les graphiques). • Les tableaux: – sont en nombre limité; – sont numérotés en chiffres romains; – sont fournis sur une seule page avec leur titre et leur numéro; – sont précisément appelés dans le texte, placés entre parenthèses par ordre d'apparition; – doivent se suffirent à eux même sans que l'on doive se référer au texte. • Les remerciements: – sont placées en fin de texte. • Les références bibliographiques: – sont numérotées en chiffres arabes placés entre parenthèses (dans le texte, les tableaux et les figures) dans l'ordre d'apparition; – les chiffres sont séparés par des virgules, mais au-delà de deux chiffres successifs seuls les deux extrêmes sont présentés, séparés par un trait d'union; – les noms des auteurs, séparés par une virgule, sont mentionnés jusqu'à six, au-delà, le dernier des six est suivi de la mention « et al. ». – les noms des revues sont conformes aux listes officielles référencées. LES RÉFÉRENCES Les références comportent obligatoirement, dans l'ordre suivant: – noms des auteurs en minuscules accentuées (première lettre en capitale accentuée) suivis des initiales des prénoms en majuscules accentuées séparés par une virgule, le dernier étant suivi de la mention « et al. »; – titre intégral dans la langue de publication (caractères latins) et d'un point ; suivi de: À propos d'un article extrait de revue: – nom de la revue suivi de l'année de parution, puis d'un point virgule; – tome, pouvant être suivi du numéro entre parenthèses, puis deux points; – numéros de la première page et de la dernière abrégée au plus petit chiffre explicite, séparés par un trait d'union et point final. À propos d'un livre: – ville de l'éditeur puis deux points; – éditeur suivi d'un point virgule; – année d'édition et éventuellement du nombre de pages suivi d'un point final. À propos d'un chapitre extrait d'un livre: – titre du chapitre et point; – puis « in : » suivi du ou des noms et initiales des prénoms du ou des coordinnateurs suivis de « ed » ou « eds » et d'un point; – titre du livre et point; – ville de l'éditeur puis deux points; – maison d'édition et virgule; – année d'édition et deux points; – numéros de la première page et de la dernière abrégée au plus petit chiffre explicite, séparés par un trait d'union et point final. À propos d'une thèse: – ville suivie de deux points et de l'université puis d'un point virgule; – année de la thèse et nombre de pages et point final. COMITÉ DE LECTURE Les articles sont soumis anonymement pour approbation à la lecture de deux lecteurs membres du comité ou de deux lecteurs choisis pour leur compétence en la matière. Le comité de lecture se réserve le droit de demander un complément de bibliographie. Les textes, publiés ou non, ne sont pas retournés à l'auteur, à l'exception des illustrations. CORRECTION DES ÉPREUVES Les auteurs reçoivent, avant publication, les épreuves d'imprimerie sous forme papier ou fichier PDF via Internet ou Lotus qu'ils devront vérifier dans les délais indiqués dans la lettre d'accompagnement et conformément aux observations précisées. Le retour dans les huit jours est impératif. Passé ce délai, le texte sera publié tel quel sous la responsabilité de son auteur. OBLIGATIONS LÉGALES Les manuscrits originaux ne doivent avoir fait l'objet d'aucune publication antérieure, ni être en cours de publication dans une autre revue. Les opinions, exprimées dans les articles ou reproduites dans les analyses, n'engagent que leurs auteurs, notamment pour les médicaments. Les règles concernant l'exercice du droit d'expression dans les armées doivent être observées, particulièrement lorsqu'il s'agit d'informations nominatives ou protégées. En outre, le respect des dispositions de la loi du 11 mars 1957 modifiée, relative à la propriété littéraire et artistique, s'impose. Toute correspondance doit être adressée à : M. le rédacteur en chef, secrétariat « Médecine et Armées » 1, place Alphonse Laveran, 75230 Paris Cedex 05 – Tél. : 01 40 51 47 44 – Fax : 01 40 51 51 76 – Email : [email protected] 384 Revue du Service de santé des armées C htt p:/ /w ww .de PAGES 289 à 384 fen s e. g ouv .fr/ site s /sa nte /v otre _ Médecine & Armées ■ TOME 34 - N°4 - Octobre 2006 ■ esp ace / re v ues /m ed ecin e_e t_ar m ees e numéro de Médecine et Armées, entièrement consacré à la pathologie cardio-vasculaire s’adresse de façon égale aux médecins généralistes et spécialistes. Du stress lors du saut en parachute à l’insuffisance cardiaque en milieu tropical, les auteurs abordent l’ensemble des grands thèmes de la cardiologie moderne, avec chaque fois que cela a été possible l’analyse du retentissement sur l’aptitude au service. SGA/SMG Impressions N°4 TOME 34 ISSN 0300-4937 N°4 Octobre 2006