Lire l`article complet
Transcription
Lire l`article complet
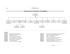
Modulation pharmacologique du stress oxydatif Pharmacological control of oxidative stress E. Descamps*, P. Gelé*, R. Bordet*, J. Vamecq* RÉSUMÉ Compte tenu de la complexité et de la variété des voies de l’oxydation, la modulation pharmacologique du stress oxydatif englobe de nombreuses stratégies. D’une manière non exhaustive, ces stratégies incluent notamment la prévention de l’émergence d’espèces oxydantes (chélateurs de métaux et inhibiteurs des activités enzymatiques génératrices d’espèces oxydantes), une meilleure efficacité de leur piégeage (composés dits antioxydants), une “métabolisation” cellulaire accrue (composés augmentant l’activité des défenses cellulaires antioxydantes) ou pharmacochimique accrue également (composés mimant une activité antioxydante enzymatique, comme l’ebselen) . En parallèle, toute une série de cibles moléculaires relatives aux voies de signalisation impliquées dans le contrôle redox cellulaire offrent une alternative ou un complément à la modulation du stress oxydatif. Un accent tout particulier est mis sur le potentiel antioxydant/antiinflammatoire du PPARα, un récepteur nucléaire activé par la famille des fibrates. L’efficacité et les limites de l’approche antioxydante dans le cadre de la thérapeutique des désordres neurodégénératifs et des maladies cardiovasculaires sont développées tout au long de cet article. Mots-clés : Antioxydants - Espèces oxydantes - Récepteurs nucléaires - Protection cardiovasculaire - PPAR Flavones - Caroténoïdes - Vitamines - Neuroprotection NADPH oxydase - Fibrates - Radicaux libres. L e French paradox fait ressortir les bienfaits du régime alimentaire de type méditerranéen chez des individus qui, malgré la présence de facteurs de risque cardiovasculaires, semblent présenter une incidence plus faible d’événements cardiovasculaires que ceux n’ayant pas ce mode de vie (1). Cet effet “protecteur” est habituellement attribué au pouvoir antioxydant, supposé ou réel, d’aliments comme l’huile d’olive, les fruits et légumes, voire le vin, caractérisés par la présence dans leur composition de substances antioxydantes, notamment les polyphénols, par ailleurs retrouvés dans différentes * Inserm UNIV 045131 (JV), EA 1046 (JV, ED, PD, RB), laboratoire de pharmacologie, faculté de médecine, université de Lille-2, 59045 Lille Cedex. SUMMARY As a consequence of the complexity and multiplicity of oxidative pathways, the pharmacological control of oxidative stress avers to cover a large number of strategies. These strategies may overlap and they may include prevention of oxidant species production (chelation of metals, inhibition of oxidant species-generating activities), improvement of free radicals scavengers (antioxidant compounds), of natural (stimulators of antioxidant enzymes) and compound-catalysed (enzyme mimics, e.g. ebselen) cell defence mechanisms. On the other hand, a large number of additional pharmacological targets may be found in cell signaling pathways physiologically involved in cell redox homeostasis. A special emphasis is here made on the antioxidant/anti-inflammatory properties of PPARα activation and agonists such as fibrates, among which fenofibrate. The benefits and limits of the antioxidant approach within the scope of the therapy of human disorders are developed throughout this article. Stratégies thérapeutiques S tratégies thérapeutiques Keywords: Antioxidants - Oxidant species - Nuclear receptors - Cardiovascular protection - PPAR - Flavones - Carotenoids - Vitamins - Neuroprotection - NADPH oxidase Fibrates - Free radicals. variétés de boissons, incluant thé et whisky. Cette association d’un apport nutritionnel riche en antioxydants et d’une protection cardiovasculaire souligne les potentialités thérapeutiques d’une approche antioxydante. D’autre part, le rôle joué par les espèces oxydantes dans l’extension des phénomènes de nécrose ou dans l’induction de l’apoptose dans des pathologies aiguës d’origine vasculaire (infarctus myocardique ou cérébral) ou dans des maladies neurodégénératives (maladie d’Alzheimer ou maladie de Parkinson) souligne le bénéfice thérapeutique que l’on pourrait tirer, dans ces cas bien précis, d’une stratégie pharmacologique dévolue à “neutraliser” l’effet délétère d’un excès de formation des espèces oxydantes. Si les bénéfices d’une approche antioxydante apparaissent en théorie largement acquis, il n’en va pas nécessairement de même en pratique. Une première raison en demeure le potentiel prooxydant des agents antioxydants, c’est-à-dire que ces molécules dotées de propriétés antioxydantes peuvent aussi, dans certaines circonstances, faire preuve d’une activité pro-oxydante. Une La Lettre du Pharmacologue - vol. 20 - n° 4 - octobre-novembre-décembre 2006 107 Stratégies thérapeutiques S tratégies thérapeutiques deuxième raison en est peut-être que les cibles pharmacologiquement visées par cette approche sont des molécules qui remplissent physiologiquement plusieurs fonctions utiles à la cellule. Comme présenté dans notre précédente mini-revue (2), une des avancées scientifiques importantes de cette dernière décennie est la démonstration que, outre leur rôle délétère établi depuis de nombreuses années, les espèces oxydantes sont aussi des messagers inter- et/ou intracellulaires impliqués dans de nombreuses voies de signalisation et de régulation, dans la modulation de l’expression de gènes et dans le contrôle cellulaire de l’homéostasie redox. Il n’est pas établi à l’heure actuelle que le fait d’interférer à l’aveugle par l’administration systématique d’antioxydants avec ces voies utiles à la vie de la cellule soit vraiment sans danger. À ce propos, l’utilisation d’agents antioxydants peut empêcher le préconditionnement cérébral (3), une observation montrant que ces agents peuvent manifester des effets non désirés. L’INHIBITION DE LA FORMATION DES ESPÈCES OXYDANTES La modulation du stress oxydatif peut viser la formation des espèces oxydantes, leur neutralisation ou leur destruction. Il est théoriquement plus judicieux de juguler d’abord la production incontrôlée des espèces oxydantes que de les laisser se former avant de les neutraliser. Assez curieusement, cette première approche, plus indiquée, est souvent mise à l’arrière-plan dans la démarche thérapeutique et, en pratique, la stratégie thérapeutique antioxydante évoque plus souvent l’utilisation d’agents neutralisateurs de radicaux libres (agents antioxydants, molécules mimant l’activité SOD en glutathion péroxydase, etc.) que celle d’agents empêchant leur formation. LES CHÉLATEURS DE MÉTAUX Les métaux de transition dans leur état réduit peuvent participer à la réaction de Fenton. Toute stratégie qui élimine ou masque le métal en question a une valeur potentiellement antioxydante. Ce rôle est naturellement rempli par des protéines telles que la transferrine (qui lie le fer) et la céruloplasmine (qui lie le cuivre). Certains métabolites comme le citrate peuvent aussi fixer les métaux. Les chélateurs de métaux emprisonnent un des acteurs indispensables à la réaction de Fenton, à savoir le métal, notamment Fe2+ ou Fe3+ (précurseur du Fe2+ par réduction). Le complexe “chélateur-métal” peut encore servir d’intervenant dans la réaction de Fenton, mais lorsque la complexation est associée à une élimination du complexe hors de l’organisme (élimination urinaire ou digestive), il en résulte une diminution ou une disparition progressive du métal pouvant être complexé. Cette mesure conduit à réduire la contribution de la réaction de Fenton à la formation d’espèces hautement toxiques telles que le radical hydroxyle ou encore les radicaux alkoxyles. 108 Divers chélateurs synthétiques de métaux ont ainsi démontré leur efficacité dans des modèles de stress oxydatif. Citons la desferrioxamine, le prototype des chélateurs du fer. D’autres molécules non toxiques peuvent chélater les métaux : l’HBED (hydroxyphényl éthylène diamine diacétate), un analogue de l’EDTA (éthylène diamine tétra-acétate), où quatre phénols remplacent les groupements carboxyliques, le PIH (pyridoxal isonicotinyl hydrazone), la disferrithiocine et les hydroxypyridones, parmi lesquelles la défériprone. La dexrazoxane est une bisdioxopiperazine qui est dotée de propriétés à la fois chélatrices du fer et antioxydantes. Cette double caractéristique en fait, depuis quelques années, un composé recommandé pour son utilisation clinique dans la cardiotoxicité induite par les agents anticancéreux de type anthracycline. Son mode d’action repose principalement sur sa capacité à mobiliser le fer du complexe “anthracycline-fer” et vraisemblablement à inhiber l’activation des anthracyclines par la NADH déshydrogénase mitochondriale (4). Ce faisant, la production de l’anion radical superoxyde induite par les anthracyclines est relativement bien contrôlée par la dexrazoxane, et cette activité antioxydante réduit, voire efface, la cardiotoxicité des anthracyclines (toxicité de l’adriamycine, par exemple). Cet effet thérapeutique bénéfique de la dexrazoxane représente son indication première en clinique humaine. L’utilisation première des chélateurs des métaux est, bien sûr, le traitement des surcharges en métaux. Néanmoins, l’impact antioxydant de cette stratégie médicamenteuse n’est pas négligeable, et en fait une option thérapeutique dans la toxicité cardiaque aux anthracyclines, mais aussi dans d’autres conditions physiopathologiques associées au stress oxydatif, telles que l’arthrite rhumatoïde, la reperfusion tissulaire, la toxicité pulmonaire au paraquat, ou encore la sclérose multiple (5). D’autre part, un certain nombre d’agents antioxydants développés plus loin dans ce numéro peuvent aussi complexer les métaux (fer ou cuivre, notamment), comme les flavonoïdes ou encore l’acide lipoïque. L’INHIBITION DES SITES PHYSIOLOGIQUES GÉNÉRATEURS D’ESPÈCES OXYDANTES Différents sites biologiques sont impliqués dans la formation d’espèces oxydantes. Ces sites ont une contribution faible à la production d’espèces oxydantes en conditions basales. Il s’agit notamment de la chaîne respiratoire, du cytochrome P450, de la xanthine déshydrogénase, des NAD(P)H oxydases phagocytaire et non phagocytaire. Dans des états physiologiques d’activation ou certaines conditions physiopathologiques, les sites précités peuvent manifester une activité quantitativement et/ou qualitativement anormale qui peut générer un stress oxydatif. Le métabolisme de l’acide arachidonique par le biais d’espèces oxydantes produites par la voie de la cyclo-oxygénase et des lipo-oxygénases peut aussi entrer dans ce cadre. Il sera abordé séparément au moment de la présentation des voies de signalisation cellulaire et de l’expression génique comme cibles de la thérapie antioxydante. La Lettre du Pharmacologue - vol. 20 - n° 4 - octobre-novembre-décembre 2006 Chaîne respiratoire L’inhibition de la chaîne respiratoire mitochondriale n’est pas une option a priori recommandée pour inhiber la formation du radical anion superoxyde formé par la mitochondrie, tout simplement parce qu’elle ajouterait un stress bioénergétique et métabolique suffisant à lui seul pour induire la mort cellulaire. En revanche, il est judicieux de ne pas surcharger la chaîne respiratoire, notamment au niveau de ses complexes I et II, et d’éviter dès lors l’apport de substrats bio-énergétiques utilisés par la mitochondrie ou la formation excessive de NADH cellulaire qui serait redirigé par les systèmes de navette redox vers la mitochondrie. Membrane cellulaire Espace Cytoplasme extracellulaire O Rac p40 gp91 p67 O2 NAD(P)H oxydase phagocytaire La NAD(P)H oxydase des phagocytes peut, elle, représenter une cible moléculaire cohérente. Physiologiquement, cette enzyme n’est pas en permanence activée. Son inhibition en dehors d’une attaque infectieuse est donc a priori tolérable sur le plan physiologique. À l’inverse, dans le cadre d’un contexte infectieux et subséquemment à la phagocytose par les cellules macrophagiques, ces dernières exposent l’élément phagocyté à une véritable explosion oxydative (6). Ce stress oxydatif est initié par la formation massive d’anion radical superoxyde catalysée par une NAD(P)H oxydase membranaire. La stratégie qui amène à délocaliser ce stress oxydatif de son site de formation à son site d’action, c’est-à-dire directement au contact de l’élément phagocyté, a été précédemment présentée (2) et implique notamment la sécrétion de myéloperoxydase dans la fente phagocytaire séparant la cellule hôte (macrophage) de l’envahisseur (par exemple, un micro-organisme). Ce stress oxydatif est physiologiquement utile, puisqu’il permet aux leucocytes et autres cellules macrophagiques d’éliminer des agents pathogènes. Néanmoins, son intervention exagérée ou inappropriée dans des conditions par exemple de recrutement des leucocytes suite à une insulte tissulaire (comme l’ischémie/reperfusion) peut aggraver l’étendue des lésions par le surajout d’un stress oxydatif. Pouvoir, dans ces conditions, bloquer le recrutement des cellules inflammatoires (par exemple, en bloquant la sécrétion ou l’expression de protéines endothéliales jouant un rôle chimiotactique ou d’ancrage), bloquer la stimulation de ces cellules inflammatoires et/ou inhiber la NAD(P)H oxydase pourrait éviter le surajout d’un stress oxydatif et l’extension subséquente de lésions cellulaires ou tissulaires. L’inhibition de la NAD(P)H oxydase macrophagique peut se concevoir de deux manières : soit par inhibition directe de l’activité enzymatique, soit par inhibition de l’activation de la NAD(P)H oxydase. L’activation de la NAD(P)H oxydase est un phénomène relativement complexe (figure 1). Elle offre plusieurs cibles moléculaires potentielles à la modulation du stress oxydatif, et plusieurs composés expérimentaux présentés peuvent déjà interférer avec l’activation de la NAD(P)H oxydase. La NAD(P)H oxydase phagocytaire est une enzyme composée de sous-unités multiples d’origine membranaire et cytosolique, dont cinq constituent le noyau dur de l’enzyme (7). Deux de ces cinq sous-unités sont représentées par les sous-unités p22 et gp91 et sont présentes dans les membranes de granules de NAD(P)H oxydase active GTP .2 p22 p47 Rap1 Membrane cellulaire Espace Cytoplasme extracellulaire P P GDP Rac P P P Les 5 sous-unités de base de la NAD(P)H oxydase active ACTIVATION Rho GDI gp91 O2 p22 Rap1 p40 p67 p47 Figure 1. Activation de la NAD(P)H oxydase phagocytaire. L’activation est nécessaire à la formation d’une NAD(P)H oxydase fonctionnelle capable de former l’anion radical superoxyde (O2λ-). L’électron nécessaire à la réduction de l’oxygène moléculaire (O2) en radical anion superoxyde est fourni par le groupement prosthétique flavinique du cytochrome b558 (hétérodimère formé de gp91 et p22) [7]. Stratégies thérapeutiques S tratégies thérapeutiques sécrétion qui fusionnent avec la membrane cellulaire lors de la phagocytose. Leur association constitue donc un hétérodimère. Cet hétérodimère correspond à une flavohémoprotéine connue aussi sous le nom de cytochrome b558. Les trois autres des cinq sous-unités sont les sous-unités p40, p47 et p67 et sont localisées dans le cytoplasme (7). L’activation de la NAD(P)H oxydase, c’est-à-dire la formation du complexe associant l’ensemble des cinq sous-unités, survient lorsque les macrophages sont stimulés. La sous-unité p47 est alors hautement phosphorylée par des protéines kinases, fusionnant avec les autres sous-unités cytoplasmiques (p40 et p67), et l’intégralité de ce complexe est alors transférée (“transloquée”) vers la membrane cellulaire, où il s’associe à l’hétérodimère flavohémoprotéique, ou cytochrome b558. Cette association des cinq sous-unités au niveau de la membrane cellulaire représente la formation d’une NAD(P)H oxydase active (7). Son activation complète requiert deux petites GTP-binding proteins apparentées au facteur Ras. Il s’agit de Rap1 et Rac1 [souris] (ou Rac2 [homme]) (7). Avant l’activation du phagocyte, le facteur Rac est localisé dans le cytoplasme, formant un complexe avec Rho GDI (Rho GDP dissociation inhibitor). Une fois lié au GTP, le facteur Rac rejoint, lors de l’activation de macrophages, la membrane, indépendamment du complexe cytosolique p40/p47/p67 mentionné plus haut. Quant au facteur Rap1, il s’associe physiquement de manière spontanée au cytochrome b558, mais perd cette faculté de liaison une fois phosphorylé (par la protéine kinase A, par exemple) [7]. Les composés expérimentaux pouvant interférer avec l’activation de la NAD(P)H oxydase incluent notamment le SB203580, un inhibiteur de la p38 MAPK (mitogen activated protein kinase) qui permet de bloquer complètement la translocation de Rac et partiellement celle de p47 ; la wortmanine et le composé LY294002, des inhibiteurs de la PI3K qui bloquent aussi l’activation de la p38 MAPK, mais également celle du facteur Rac (le composé SB203580 ne bloque pas la PI3K) ; le composé PD98059, un inhibiteur La Lettre du Pharmacologue - vol. 20 - n° 4 - octobre-novembre-décembre 2006 109 Stratégies thérapeutiques S tratégies thérapeutiques spécifique de la ERK kinase qui inhibe complètement certaines phosphorylations de p47 et partiellement d’autres, et le composé GF 109203X, un inhibiteur de la PKC (protéine kinase C) [7]. Il est à noter que l’utilisation de ces composés a pu montrer que l’axe de signalisation PI3K/p38 MAPK/Rac était impliqué dans l’activation de la NAD(P)H oxydase. Ces composés atténuent en fait la phagocytose ; à l’inverse, le GF 109203X stimule la phagocytose. Toutefois, ce dernier composé, comme mentionné plus haut, est aussi capable de diminuer la formation de l’anion radical superoxyde en inhibant l’activation de la NAD(P)H oxydase. Ces données suggèrent que p38 MAPK et PI3K modulent à la fois la phagocytose et l’activation de la NAD(P)H oxydase, alors que la PKC interviendrait seulement dans la régulation de l’activation de la NAD(P)H oxydase (7). Il est donc pharmacologiquement envisageable de disposer d’agents pouvant bloquer ou réduire la production de l’anion radical superoxyde par des cellules macrophagiques, même si celles-ci sont activées. En d’autres termes, même si, dans les suites d’une insulte tissulaire, le recrutement et l’activation de cellules inflammatoires sont déjà bien engagés, il est encore possible de contrer la formation excessive du radical anion superoxyde par ces cellules. NAD(P)H oxydase non phagocytaire La membrane plasmique, tout comme la membrane du réticulum endoplasmique de cellules non phagocytaires, peut aussi catalyser une activité NAD(P)H oxydase. Il s’agit ici de la NAD(P)H oxydase impliquée dans le sensing de l’oxygène et dans la réponse d’adaptation cellulaire subséquente (2). L’activité de cette protéine est surtout dépendante du NAD(P)H et présenterait des ressemblances structurales avec la NAD(P)H oxydase phagocytaire (8). Il est difficile à l’heure actuelle d’évaluer l’impact d’une inhibition de la NAD(P)H oxydase non phagocytaire en termes de bénéfice thérapeutique, car, si une activité antioxydante peut être apportée par une telle stratégie, celle-ci supprimerait dans le même temps la fonction physiologique remplie par cette protéine. Xanthine déshydrogénase La xanthine déshydrogénase est une enzyme qui catalyse chez l’homme les étapes terminales du catabolisme des bases puriques, à savoir la conversion de l’hypoxanthine en xanthine et celle de la xanthine en acide urique. La xanthine déshydrogénase est une oxydoréductase qui utilise normalement le NAD+ comme cofacteur et le réduit lors de l’oxydation de ses substrats. Dans certaines conditions physiopathologiques, cette oxydoréductase peut être soumise à un début de digestion protéasique ou d’altération oxydative, et peut produire le radical anion superoxyde et/ou du peroxyde d’hydrogène lors de l’oxydation de l’hypoxanthine et de la xanthine (9). La xanthine déshydrogénase est alors qualifiée de xanthine oxydase. Cette génération d’espèces oxydantes par la xanthine oxydase a été montrée dans plusieurs modèles expérimentaux comme jouant un rôle crucial dans la genèse du stress oxydatif et la sévérité des lésions observées (10). En conséquence logique, l’allopurinol, un inhibiteur de la xanthine oxydase, peut endiguer le stress oxydatif caractérisant ces modèles, réduisant ainsi la taille et la survenue des lésions. 110 Cytochrome P450 Les microsomes et leurs cytochromes, notamment le cytochrome P450, peuvent jouer un rôle important dans la genèse du stress oxydatif suite à l’administration de certains composés, mais aussi au décours de la reperfusion tissulaire. En conséquence logique, les inhibiteurs du cytochrome P450 peuvent être efficaces pour contrecarrer le stress oxydatif associé à certaines conditions physiopathologiques (11). Autres (NOS) Les NO synthases catalysent les deux étapes permettant la synthèse de NO à partir d’arginine, à savoir la conversion de l’arginine en ω-hydroxyarginine et l’oxydation de cette dernière en citrulline et NO. Dans certaines conditions, la NO synthase peut aussi produire le radical anion superoxyde, voire le peroxyde d’hydrogène (12), le premier pouvant par ailleurs se combiner au NO pour former le peroxynitrite, très réactif et hautement toxique pour la cellule. Cette activité pro-oxydante de la NO synthase peut être inhibée par des composés qui vont dès lors manifester une activité antioxydante. Cette activité antioxydante, donc protectrice, des inhibiteurs de la NO synthase (comme la N-nitro-L-arginine) a été montrée dans différents modèles (13). À remarquer que des donneurs de NO ou que des molécules pouvant augmenter le taux cellulaire de NO peuvent parfois offrir une protection dans des modèles associés à la genèse d’un stress oxydatif (14). La production de NO doit rester relativement limitée, les augmentations brusques et importantes de NO comme celles caractérisant l’activation oxydative des macrophages étant associées à l’inverse à une aggravation du stress oxydatif. Ces conditions sont aussi connues comme étant associées à l’activation de la NAD(P)H oxydase phagocytaire (voir ci-dessus). LE PIÉGEAGE DES ESPÈCES OXYDANTES Le piégeage des espèces oxydantes est un concept qui souligne que le potentiel oxydant d’un composé peut être piégé. En fait, l’agent antioxydant ne piège pas vraiment une espèce oxydante : il la réduit en un composé par définition moins oxydant et en pratique plus stable. Il existe divers composés antioxydants naturels ou synthétiques. Les antioxydants naturels incluent diverses vitamines (vitamines A, C et E), des composés pouvant être synthétisés par les cellules animales (glutathion, mélatonine, acide urique, créatine, ubiquinone, acide lipoïque) ou d’origine végétale apportés par l’alimentation (flavones, resvératrol et autres polyphénols, caroténoïdes/ lycopène). Les antioxydants synthétiques comprennent des composés antioxydants classiques (N-acétylcystéine, lazaroïdes, flavones et chalcones de synthèse, stobadine) et d’autres composés dotés d’activités catalytiques de type enzymatique (ebselen mimant l’activité glutathion peroxydase, complexes synthétiques liant le manganèse mimant l’activité superoxyde dismutase ou catalase). La Lettre du Pharmacologue - vol. 20 - n° 4 - octobre-novembre-décembre 2006 COMPOSÉS ANTIOXYDANTS NATURELS Vitamines E et C Les vitamines E et C représentent des composés antioxydants (15) étudiés depuis très longtemps. Ces vitamines sont complémentaires, occupant des sites cellulaires distincts en relation avec leur solubilité respective dans les milieux lipidiques et aqueux. De plus, elles peuvent interagir de manière synergique. ● La vitamine E, connue aussi sous le nom d’α-tocophérol, est un composé lipophile monophénolique et un antioxydant puissant, piégeant les radicaux libres. Le radical libre formé dans le milieu vient arracher un proton sur la vitamine E, générant ainsi le radical tocophéryle et le composé neutralisé correspondant. Le groupe hydroxyle de cette molécule peut donner un proton pour saturer, et donc “détoxiquer”, l’électron célibataire d’un radical libre. Quand le radical avec lequel cette vitamine réagit initialement est issu de l’attaque radicalaire des lipides, la vitamine E joue alors le rôle de “terminateur” ou “briseur” de la propagation des réactions en chaîne caractérisant la peroxydation lipidique des membranes biologiques. Ce potentiel antioxydant de la vitamine E explique son rôle protecteur vis-à-vis des membranes biologiques. La vitamine C, ou acide ascorbique, existe physiologiquement sous la forme de l’anion ascorbate. Comme dans le cas de la vitamine E, un groupe hydroxyle de cette molécule peut donner un proton pour saturer, et donc “détoxiquer”, l’électron célibataire d’un radical libre. Le radical ascorbyle est aussi stabilisé par délocalisation électronique. De plus, il peut être ultérieurement stabilisé par l’oxydation du radical ascorbyle en acide ascorbique dit oxydé ou déhydroascorbate. L’acide ascorbique a en fait un large spectre d’activité antioxydante réduisant différentes espèces oxydantes incluant notamment l’anion superoxyde ou le radical hydroxyle. L’acide ascorbique peut d’autre part régénérer la vitamine E (α-tocophérol) à partir du radical α-tocophéryle. Cette réaction participe au recyclage de la vitamine E sous sa forme réduite, c’est-à-dire sous la forme lui permettant d’exercer son activité antioxydante antiradicalaire vis-à-vis notamment de la peroxydation lipidique. Caroténoïdes et lycopènes Les caroténoïdes principalement ingérés incluent l’α- et le βcarotène, la β-cryptoxanthine, la lutéine et le lycopène (ces composés sont passés en revue dans l’ouvrage de Willis et Wians [16]). Les carotènes et la cryptoxanthine sont retrouvés dans différents fruits (abricots) et légumes (carottes). La lutéine est plutôt retrouvée dans des légumes verts (brocoli, chou de Bruxelles, haricot princesse). Les lycopènes sont abondants dans les tomates mais aussi dans le raisin ou la pastèque. La longue structure polyénique des caroténoïdes leur permet d’absorber la lumière UV. Ils peuvent réduire ou piéger les espèces réactives de l’oxygène et interférer avec des réactions radicalaires. Ils peuvent ainsi bloquer ou limiter la peroxydation lipidique. Les lycopènes exercent aussi une action antioxydante et sont dotés d’autres effets biologiques bien établis (17). Vitamine A Bien que décrite comme possédant des propriétés antioxydantes in vitro, la vitamine A, à l’inverse du β-carotène dont elle dérive, n’exercerait qu’une faible action antioxydante in vivo (16). Le rétinol et le rétinal ne “piègent” que faiblement l’oxygène singulet, et leurs propriétés antiradicalaires restent malgré tout limitées. La vitamine A peut néanmoins être active contre des cancers comme celui de la prostate, dont le développement est connu pour être retardé ou partiellement inhibé par l’administration d’agents antioxydants. Cette action de la vitamine A sur la prévention relative du cancer de la prostate est attribuée à des propriétés autres qu’antioxydantes : son potentiel inhibiteur de l’ADN polymérase en phase G1 du cycle cellulaire et son impact régulateur sur la transcription des gènes (16). Ces effets de la vitamine A peuvent expliquer une partie des propriétés manifestées par le β-carotène. Vitamine B3 (niacine) La niacine ou vitamine B3 est le nom commun pour l’acide nicotinique et la nicotinamide. Elle est aussi parfois nommée vitamine PP. Il s’agit d’une vitamine hydrosoluble pour laquelle une activité antioxydante a été documentée. Cette vitamine représente en fait un puissant agent neuroprotecteur dans des modèles animaux d’occlusion permanente de l’artère cérébrale moyenne ou encore d’ischémie/reperfusion cérébrale (18). Stratégies thérapeutiques S tratégies thérapeutiques Flavonoïdes Les flavonoïdes désignent un groupe chimiquement assez varié de composés polyphénoliques largement retrouvés dans le règne végétal, si bien qu’ils font partie de notre régime alimentaire (19). Plusieurs milliers de flavonoïdes différents ont pu être identifiés et ont été regroupés en plusieurs classes incluant les flavones, les isoflavones, les flavonols, les dihydroflavonols, les catéchines, les anthocyanidines et les chalcones. Les flavonoïdes alimentaires sont surtout apportés par le thé, les oignons, les pommes et le vin rouge, avec un apport quotidien moyen estimé entre 23 et 170 mg/kg. Les flavonoïdes alimentaires ont des propriétés antioxydantes importantes et variées. Notamment, ils peuvent neutraliser divers radicaux libres, chélater les métaux et inhiber la peroxydation lipidique. Plusieurs études épidémiologiques ont conduit à l’hypothèse que ces composés pouvaient jouer un rôle important dans la réduction et la prévention des maladies cardiovasculaires. Ce bénéfice médical est attribué notamment à la diminution de l’oxydation des lipoprotéines et à l’action antiagrégante plaquettaire des flavonoïdes. Glutathion Le glutathion est un tripeptide synthétisé par la cellule. Il correspond au γ-glutamylcystéinylglycine et présente une fonction thiol (celle de la cystéine) dotée d’un potentiel antioxydant qui s’exprime notamment vis-à-vis des hydroperoxydes (peroxyde d’hydrogène et hydroperoxydes lipidiques, notamment). Il réagit dans le cadre de réactions enzymatiques catalysées par les glutathion peroxydases (activités dites sélénodépendantes). En ce qui concerne le peroxyde d’hydrogène, le glutathion peut en La Lettre du Pharmacologue - vol. 20 - n° 4 - octobre-novembre-décembre 2006 111 Stratégies thérapeutiques S tratégies thérapeutiques plus réduire le peroxyde, assisté par les glutathion transférases (activité glutathion peroxydase dite non sélénodépendante). Au cours de la réduction des hydroperoxydes, l’oxydation du glutathion peut être conjuguée à celle d’un autre thiol conduisant à la formation de disulfures hybrides. Cette glutathionylation est réversible quand il s’agit de protéines ; elle peut transitoirement mettre à l’abri la protéine de l’oxydation de ces cystéines ou induire un changement d’activité ayant une valeur régulatrice. D’autres peptides ou protéines présentant des fonctions SH, telles que les peroxyrédoxines, glutarédoxines ou encore la thiorédoxine, sont dotés de propriétés antioxydantes (2). Bien que le glutathion soit un peptide, le lien γ-glutamyl est relativement résistant aux protéases et le glutathion peut utiliser des transporteurs pour entrer dans des cellules auxquelles il est extérieurement présenté. Le glutathion en tant qu’agent utilisé à visée pharmacologique s’est montré protecteur vis-à-vis de différents modèles animaux (20). Mélatonine La mélatonine est une neurohormone synthétisée et sécrétée par l’épiphyse, ou glande pinéale. Ce méthoxyindole est substitué par une chaîne latérale comprenant un groupement N-acétate. Les propriétés antioxydantes de la mélatonine tiennent dans le noyau méthoxyindole. Des analogues mélatoninergiques où cette structure est remplacée par un noyau napthalénique perdraient partiellement cette activité antioxydante. Il est à noter que ces analogues naphtaléniques de la mélatonine peuvent être dotés d’une affinité beaucoup plus élevée vis-à-vis des récepteurs à la mélatonine (21). La mélatonine est dotée d’un large spectre antioxydant, pouvant réduire ou neutraliser des espèces incluant l’anion superoxyde, les hydroperoxydes, le radical hydroxyle, le NO et le peroxynitrite. La mélatonine assure une protection antioxydante très puissante dans différents modèles de stress oxydatif incluant des modèles de cataracte, de maladies cardiaques et neurologiques. Son utilité pharmacologique pour réduire les dommages cellulaires et moléculaires a fait l’objet de nombreuses revues, dont celle récemment publiée par Reiter et al. (22). D’autre part, les propriétés antioxydantes de la mélatonine lui ont valu d’être considérée comme une molécule anti-vieillissement et même comme hormone de jouvence. En fait, les indications médicales potentielles de la mélatonine, seule ou comme traitement d’appoint, sont nombreuses et concernent toute condition physiopathologique associée à la génération de radicaux libres. Celles-ci incluent notamment l’exposition à divers agents toxiques (ecstasy, tétrachlorure de carbone, carcinogènes comme le safrole), aux radiations ionisantes, à l’ischémie/reperfusion (accident vasculaire cérébral, infarctus du myocarde), au choc septique, à la déplétion en glutathion ou encore à la protéine β-amyloïde (maladie d’Alzheimer) [23]. L’utilisation de la mélatonine a aussi été recommandée dans la maladie de Parkinson (23). La mélatonine possède non seulement une activité antioxydante intrinsèque, mais également la propriété d’induire les sytèmes de défenses antioxydantes cellulaires. En effet, la mélatonine a été rapportée comme pouvant 112 induire l’activité superoxyde dismutase [SOD] (stimulation de la SOD cupro/zinc-dépendante [isoenzyme cytoplasmique] et de la SOD manganèse-dépendante [isoenzyme mitochondriale]), les activités glutathion peroxydase et réductase, de même que l’activité de la glucose-6-phosphate déshydrogénase, qui est l’enzyme produisant le NAD(P)H utilisable par la glutathion réductase (23). Une propriété remarquable de la mélatonine, qui en fait un agent antioxydant pharmacologiquement exploitable, est sa bonne biodistribution et l’aisance avec laquelle cette molécule peut traverser les différentes barrières biologiques, barrière hématoencéphalique incluse. Acide urique L’acide urique est le produit terminal du catabolisme des bases puriques chez l’homme. Chez la plupart des autres mammifères, l’acide urique subit une oxydation supplémentaire catalysée par l’urate oxydase, qui permet la formation d’allantoïne, un produit relativement plus polaire. L’acide urique est doté de puissantes propriétés antioxydantes et est formé par la xanthine déshydrogénase. Il est difficilement soluble dans l’eau, limitant vraisemblablement sa concentration physiologique. Néanmoins, il faut savoir qu’il contribue à plus de 60 % au pouvoir antioxydant du plasma chez les sujets en bonne santé. Il neutralise en fait 10 à 15 % du radical hydroxyle produit quotidiennement, et peut aussi neutraliser les radicaux peroxyles, de même que l’oxygène singulet. De manière très intéressante, il peut aussi fixer le fer et stabiliser l’acide ascorbique plasmatique (20). Son potentiel antioxydant a été mis en évidence notamment dans des modèles animaux d’agression cérébrale induits par l’occlusion de l’artère cérébrale moyenne. En pratique clinique, l’acide urique reste d’une utilisation délicate, vu notamment sa faible solubilité et, dès lors, le risque de précipitation. Acide lipoïque L’acide lipoïque (acide 1,2-dithiolane-3-pentanoïque), aussi appelé acide thioctique ou acide lipodomique, possède une structure chimique comprenant deux atomes de soufre. Il a la particularité d’être hydro- et liposoluble, ce qui lui donne la capacité d’agir dans ces deux milieux et donc de neutraliser plusieurs types de radicaux libres comme le peroxynitrite, l’hypochlorite ainsi que l’oxygène singulet (24). En réalité, c’est l’acide dihydrolipoïque qui joue le rôle d’antioxydant. En neutralisant le radical libre, l’acide dihydrolipoïque est transformé en acide lipoïque, qui peut alors régénérer certains antioxydants comme la vitamine E, la vitamine C, le glutathion. L’acide lipoïque a en plus la propriété de chélater divers métaux, incluant le fer et le cuivre, une activité qui contribue à son potentiel antioxydant. L’administration expérimentale d’acide lipoïque est associée à une protection dans différents modèles animaux de stress oxydatif ou de maladies dégénératives. Son emploi chez l’homme est efficace dans la neuropathie diabétique et a été préconisé aussi dans les troubles oculaires (glaucome), ainsi que comme traitement renforçant l’état général des patients souffrant du syndrome de l’immunodéficience acquise (sida). Son extension à d’autres pathologies humaines impliquant le stress oxydatif ou la diminution des défenses antioxydantes est attendue. La Lettre du Pharmacologue - vol. 20 - n° 4 - octobre-novembre-décembre 2006 Ubiquinone ou coenzyme Q L’ubiquinone est un cofacteur naturel qui joue le rôle de transporteur d’électrons dans le cadre de la chaîne respiratoire mitochondriale. Si, d’un côté, sa structure proquinonique est impliquée dans la formation de l’anion superoxyde au décours du transport mitochondrial d’électrons, cette molécule représente, d’un autre côté, un agent antioxydant puissant. Ces aspects à la fois pro- et antioxydants de l’ubiquinone ont été considérés dans la revue d’Ernster et Dallner (25). L’ubiquinone peut interagir avec un certain nombre d’espèces oxydantes, et cette activité antioxydante lui permet d’agir comme “terminateur” de la peroxydation lipidique, comme le fait la vitamine E. Mais, à l’inverse de cette dernière, l’ubiquinone peut aussi agir comme inhibiteur de l’initiation de la peroxydation lipidique (25). De plus, l’ubiquinone assure un rôle protecteur vis-à-vis des lésions oxydatives des protéines et de l’ADN (25). Elle a été employée avec succès dans différents modèles animaux et est utilisée chez l’homme, non seulement dans le cadre de cytopathies mitochondriales (comme transporteur d’électrons), mais aussi dans le cadre de la thérapie antioxydante ou comme facteur de supplémentation antioxydant préconisé contre la fatigue et le vieillissement. Les pathologies humaines améliorées par l’ubiquinone incluent le syndrome de Prader-Willi, l’ataxie de Friedreich, la maladie de Parkinson et les affections cardiovasculaires (26). Au cours des vingt dernières années, au moins dix études portant sur 1 000 patients souffrant d’une pathologie coronarienne ont montré une influence positive de l’administration de l’ubiquinone, avec amélioration significative notamment de la fraction d’éjection et autres indices hémodynamiques (index de volume distolique). À une dose de 100 mg/j, l’ubiquinone améliore significativement les performances ventriculaires gauches dans une population de patients souffrant de défaillance cardiaque (d’origine ischémique ou fonctionnelle [i.e. cardiomyopathie dilatée]) [26]. Resvératrol Le resvératrol, ou trans-3,5,4’-trihydroxystilbène, est un composé polyphénolique naturel. Il est présent dans la peau et les pépins de raisin, ce qui explique sa forte concentration dans le vin, surtout dans le vin rouge. Cela est dû au fait que, lors du processus de fermentation du vin, les peaux et les pépins restent en contact plus longtemps avec le liquide pour le vin rouge que pour le vin blanc. Mais le resvératrol est aussi présent dans d’autres plantes, comme l’eucalyptus ou le lys, ou dans d’autres aliments, comme les mûres et les cacahouètes. Plusieurs études ont démontré que le resvératrol a un effet antioxydant. En effet, il inhibe la peroxydation lipidique des lipoprotéines de basse densité, prévient la cytotoxicité de ces lipoprotéines oxydées et protège les cellules contre la peroxydation lipidique. Le resvératrol a aussi été étudié dans le cadre de l’initiation, la promotion et la progression de cancers (27). Lors de la phase d’initiation, le resvératrol agit comme un antioxydant en inhibant la formation de radicaux libres. Lors de la phase de promotion, il inhibe la cyclo-oxygénase 1, une enzyme qui convertit l’acide arachidonique en composés pro-inflammatoires. Lors de la phase de progression tumorale, il inhibe la ribonucléotide réductase, une enzyme nécessaire à la synthèse d’ADN particulièrement active lors de la prolifération des cellules. Créatine La créatine [N-(amino-iminométhyl)-N-méthyl glycine] est un tripeptide produit de façon endogène à partir de la glycine, de la méthionine et de l’arginine dans le foie, le rein et le pancréas. Elle peut se trouver dans les muscles, mais aussi dans les tissus cérébraux. Certaines recherches expérimentales ont montré que la créatine fournit une neuroprotection contre l’ischémie et autres modèles animaux de stress oxydatif. Sullivan et al. (28) ont montré qu’une administration chronique de créatine réduit l’étendue des dommages cérébraux corticaux consécutifs à un traumatisme de jusqu’à 36 % chez la souris et 50 % chez le rat. Cette protection induite par la créatine semble être liée au maintien de la bioénergétique mitochondriale (préservation des taux d’ATP, réduction de la concentration intramitochondriale en calcium et en espèces oxydantes). La créatine semble prometteuse en vue d’études cliniques sur le traitement des dommages du système nerveux central, mais, au préalable, les doses préconisées doivent être évaluées pour déterminer la balance bénéfice thérapeutique/toxicité. Stratégies thérapeutiques S tratégies thérapeutiques Estradiol, estriol et estrone L’estradiol, l’estrone et l’estriol sont dérivés du noyau estrane et comportent un cycle aromatique. Ils représentent les trois estrogènes principalement sécrétés par les ovaires ; mais d’autres organes comme les testicules, le tissu adipeux et le cerveau peuvent les synthétiser. Les estrogènes s’opposent à l’ostéoporose ; ils réduisent la fréquence des accidents cardiovasculaires, coronaropathies et infarctus du myocarde physiologiquement chez la femme avant la ménopause et pharmacologiquement lors de leur administration médicamenteuse. Les estrogènes réduisent le taux circulant des lipoprotéines de basse densité, augmentent celui des lipoprotéines de haute densité, et induisent une vasodilatation par le biais de l’ouverture des canaux potassiques. Les estrogènes, surtout l’estradiol, sont utilisés lors du traitement des déficiences de sécrétion ovarienne à l’adolescence, l’âge adulte ou après la ménopause. Dans ce dernier cas, l’estradiol est prescrit dans le but de diminuer la progression de l’ostéoporose et des accidents cardiovasculaires. L’estriol, quant à lui, a un pouvoir estrogénique plus faible. Les estrogènes agissent principalement par le biais de récepteurs nucléaires appartenant à la superfamille des récepteurs nucléaires hormonaux. Ils exercent aussi des effets qui ne dépendent pas de l’activation de ces récepteurs aux estrogènes, notamment par le biais de propriétés antioxydantes (29). L’activité antioxydante des estrogènes est aisément compréhensible si l’on tient compte de l’analogie structurale qu’ils peuvent présenter avec la vitamine E : à savoir, une partie phénolique hydrophile riche en électrons et responsable du potentiel antioxydant de la molécule, et une partie plus lipophile, expliquant la solubilité de la molécule dans les membranes biologiques. Cette activité antioxydante est efficace contre la peroxydation lipidique associée à un stress oxydatif. Par exemple, l’estradiol est un bon piégeur du radical hydroxyle hautement toxique pour la cellule. L’efficacité de cette activité antioxydante a été démontrée dans différents modèles expérimentaux neurophysiopathologiques La Lettre du Pharmacologue - vol. 20 - n° 4 - octobre-novembre-décembre 2006 113 Stratégies thérapeutiques S tratégies thérapeutiques (30), incluant les effets positifs enregistrés dans différents modèles de la maladie d’Alzheimer et contribuant très vraisemblablement aux propriétés protectrices des estrogènes. DHEA La déhydroépiandrostérone (DHEA) est un stéroïde hormonal produit dans les glandes surrénales, les gonades et le cerveau. Les précurseurs de la DHEA sont le cholestérol, la prégnanolone et la 17-hydroxyprégnanolone. La DHEA peut aussi être métabolisée en estrogènes, estrone et estradiol. La DHEA et la DHEAS (dehydroepiandrostérone-3-sulfate, son métabolite) ont beaucoup été étudiées ces dernières années en vue d’une utilisation pharmaceutique possible. La DHEA a été développée dans le cadre de la préservation des tissus neuronaux et du myocarde face aux effets lésionnels de l’ischémie/reperfusion associée aux infarctus cardiaques ou cérébraux, ou encore à la chirurgie cardiovasculaire. Les propriétés antioxydantes de la DHEA protègent les composants subcellulaires et les lipoprotéines de basse densité contre la peroxydation lipidique ; elles réduisent les lésions oxydatives de l’ADN liées au vieillissement des cellules cérébrales et des lymphocytes circulants (31). La DHEAS, quant à elle, est utilisée dans le cadre du traitement des attaques asthmatiques aiguës. La DHEA, considérée comme une hormone de “jeunesse”, a souvent été associée à des vertus antioxydantes et à des effets anti-inflammatoires, anticancéreux, anti-obésité, antidiabétiques et anti-vieillissement. De tels effets et propriétés restent cependant à confirmer. Le sélénium Le sélénium est un oligoélément, métalloïde analogue au soufre. L’on attribue à plusieurs protéines contenant cet élément des propriétés antioxydantes, mais aussi une fonction de détoxication ou encore des effets anticancéreux. Seule notre alimentation fournit le sélénium à l’organisme. On peut le retrouver dans les produits de la mer, les légumes frais, les céréales et les abats (foie). Il intervient dans de nombreuses réactions enzymatiques comme la synthèse d’ADN, ainsi que celle des hormones thyroïdiennes ou encore des phospholipides membranaires. Le sélénium a un rôle antioxydant et détoxiquant au niveau de la cellule. Il est un constituant de la glutathion peroxydase, une enzyme qui joue un rôle intracellulaire antioxydant. Le sélénium est normalement présent en quantités importantes dans les tissus immunitaires comme le foie et la rate. Il diminue la gravité des lésions produites par les métaux toxiques (Hg, As, Cd) par formation de séléniures biologiquement inactifs ou par phénomène de compétition. De plus, on attribue au sélénium des propriétés anti-inflammatoires, et une tendance à la réduction de la fréquence des maladies cardiaques, sans réduction de la pression artérielle. Il serait aussi efficace dans le traitement de l’arthrose par le contrôle des prostaglandines et dans le traitement de l’hypothyroïdie par son effet sur la transformation de la thyroxine. Le sélénium est en fait retrouvé dans différentes protéines, qualifiées dès lors de sélénoprotéines. Outre les glutathion peroxydases, les sélénoprotéines incluent la sélénoprotéine 114 P et la thiorédoxine réductase, dont le rôle antioxydant résulte notamment de leur capacité à métaboliser le peroxynitrite (2). COMPOSÉS ANTIOXYDANTS SYNTHÉTIQUES Les antioxydants naturels représentent déjà un réservoir important de composés pouvant être utilisés de manière pharmacologique. À l’heure actuelle, l’utilisation d’un bon nombre d’entre eux reste limitée à une administration non pharmacologique, ne requérant pas de prescription médicale et restant accessible en vente libre. Ces produits naturels sont vantés notamment pour leurs propriétés cosmétiques, énergétiques et anti-vieillissement. Ces indications de “confort”, de même que leur présence parfois retrouvée dans l’alimentation, expliquent peut-être le désintérêt médical apparent dont ils ont fait jusqu’ici l’objet. Cela ne doit en rien discréditer l’intérêt thérapeutique dont ces composés naturels pourraient à l’avenir faire preuve, notamment sur la base d’études expérimentales scientifiques démontrant leur efficacité dans des conditions physiopathologiques bien précises. Il en va de même de l’intérêt préventif/thérapeutique de certaines mesures diététiques visant à enrichir l’apport nutritionnel en certains de ces agents antioxydants. Les composés antioxydants synthétiques s’inspirent néanmoins d’agents antioxydants naturels. De puissants agents pharmacologiques de synthèse représentant des analogues de ces composés naturels sont actuellement en cours d’évaluation expérimentale (par exemple : chalcone synthétique et neuroprotection [32]). Même un composé comme la Nacétylcystéine, qui est dotée d’une activité antioxydante intrinsèque, participe après hydrolyse à la synthèse d’un agent antioxydant naturel cellulaire aussi important que le glutathion. Certains agents antioxydants synthétiques, bien qu’imitant les molécules ou les défenses naturelles, sont dotés d’un potentiel antioxydant bien plus élevé que les référents naturels, comme le démontre la comparaison de l’ebselen et de la glutathion peroxydase. N-acétylcystéine La N-acétylcystéine est un composé thiolé utilisé cliniquement depuis le milieu des années 1950. La N-acétylcystéine réduit de manière efficace les espèces radicalaires et autres espèces oxydantes, en particulier le radical hydroxyle et le peroxyde d’hydrogène. La N-acétylcystéine n’est pas synthétisée de façon endogène et ne peut pas passer la barrière hématoencéphalique. Cela pourrait limiter son efficacité in vivo. Néanmoins, la Nacétylcystéine s’hydrolyse et peut générer la cystéine, qui, elle, peut théoriquement traverser la barrière hématoencéphalique. L’intérêt réside dans le fait que la cystéine participe à la synthèse du glutathion et que, dès lors, sa biodisponibilité accrue augmente les taux cellulaires de glutathion. Des études animales (principalement sur des modèles de rongeurs) montrent que la N-acétylcystéine peut être bénéfique dans le traitement des La Lettre du Pharmacologue - vol. 20 - n° 4 - octobre-novembre-décembre 2006 dommages oxydants, incluant ceux induits par ischémie-reperfusion (33). En pratique clinique humaine, la N-acétylcystéine est employée comme agent mucolytique (son potentiel antioxydant empêche l’oxydation, et par là-même l’agrégation des sécrétions pulmonaires) et comme agent de détoxication dans des syndromes aigus précipités par la genèse d’un stress oxydatif incontrôlé, notamment d’origine médicamenteuse (par exemple, nécrose tubulaire rénale induite par le paracétamol) [34]. Lazaroïdes Les lazaroïdes sont des 21-aminostéroïdes dérivés des glucocorticoïdes, mais toutefois dépourvus d’activité glucocorticoïde et minéralocorticoïde. Les propriétés antioxydantes de différents composés synthétiques tels que le tirilazad mésylate (U-74006F) ont bien été documentées, notamment l’inhibition de la peroxydation lipidique dans des modèles d’ischémie et de traumatisme cérébral (35). Ces composés peuvent ainsi réduire la taille de l’infarctus cérébral enregistré dans des modèles animaux d’ischémie-reperfusion, ou encore d’occlusion permanente de l’artère cérébrale moyenne, et protéger la barrière hématoencéphalique dans des conditions de traumatisme cérébral ou d’hémorragie subarachnoïdienne. La démonstration d’une cérébroprotection expérimentale a conduit à l’utilisation du tirilazad chez l’homme dans des indications de désordres neurologiques aigus. Les résultats peu encourageants ont été mis en rapport avec la faible absorption orale, mais surtout avec le faible passage du lazaroïde au travers de la barrière hématoencéphalique. La mise au point de lazaroïdes pouvant traverser la barrière hématoencéphalique est aujourd’hui à l’étude. Analogues synthétiques des polyphénols alimentaires Différentes générations de flavonoïdes synthétiques ont été testées pour leurs activités antioxydantes. Une chalcone synthétique, à savoir le dérivé 3,5-tert-butyl 4,2’ dihydroxychalcone, dotée d’un potentiel antioxydant lui permettant de prévenir in vitro la cytotoxicité induite par des LDL oxydées, s’est avérée protéger de manière très efficace le cerveau dans un modèle d’ischémie/reperfusion (32). Un bon parallélisme a par ailleurs été démontré entre la qualité de cette protection cérébrale et celle de l’activité des canaux potassiques Kir2.x du muscle vasculaire lisse de l’artère cérébrale moyenne sujette à l’occlusion transitoire caractérisant le modèle d’ischémie/reperfusion (32). Stobadine La stobadine est une molécule présentant des analogies structurales avec la mélatonine. Comme cette dernière, elle est dotée d’un spectre d’activité antioxydante relativement large. La stobadine (36) est en fait active vis-à-vis de diverses espèces oxydantes, incluant le radical hydroxyle, les radicaux peroxyles et alkoxyles, ou encore l’oxygène singulet. Elle diminue les lésions du myocarde relevant de mécanismes impliquant le stress oxydatif dans différents modèles animaux in vitro et in vivo (infarctus et hypoxie/réoxygénation du myocarde, surexposition aux catécholamines). La stobadine est un excellent agent neuroprotecteur expérimental dans des modèles physiopathologiques également caractérisés par un excès de radicaux libres. Elle se révèle être aussi un puissant inhibiteur de l’oxydation des lipoprotéines de basse densité, protégeant à la fois la partie protéique et la partie lipidique contre l’oxydation cuprodépendante. L’activité antioxydante de la stobadine a en outre été démontrée dans de nombreux autres modèles, incluant la mutagenèse induite par les radicaux libres. Chez l’homme, l’administration de stobadine a montré notamment une réduction significative de la fréquence des épisodes d’angine de poitrine, un effet normolipémiant et antihypertensif (36). Ebselen L’ebselen est un séléno-composé synthétique. Il a été conçu pour mimer l’activité catalytique de la glutathion peroxydase (37). L’ebselen est doté de propriétés antioxydantes puissantes qui s’expriment vis-à-vis notamment du peroxyde d’hydrogène et des peroxydes organiques (peroxydes lipidiques), mais aussi vis-à-vis du peroxynitrite, hautement toxique pour la cellule. L’activité antioxydante de l’ebselen s’est montrée bénéfique dans différents modèles animaux (réduction du volume de l’infarctus cérébral ou de l’ischémie cérébrale dans divers modèles d’occlusion – transitoire ou permanente – de l’artère cérébrale moyenne). Les études cliniques déjà réalisées chez l’homme (38) ont montré des effets encourageants en termes d’étendue des lésions cérébrales et de récupération chez des patients avec atteinte cérébrale. Des patients avec accident vasculaire cérébral ayant reçu de l’ebselen montrent une évolution plus favorable que ceux n’ayant pas reçu le composé sélénié. Ils présentent une réduction significative de leur infarctus cérébral lorsque l’ebselen est administré dans les six heures suivant l’attaque cérébrale. L’ebselen est actuellement en phase III de son expérimentation clinique. Stratégies thérapeutiques S tratégies thérapeutiques Complexes synthétiques mimant l’activité d’antioxydants catalytiques Certaines métalloprotéines, comme la superoxyde dismutase et la catalase, catalysent des réactions dont le peroxyde d’hydrogène est soit le produit soit le substrat. L’utilisation de ces protéines comme agents thérapeutiques permet de diminuer les dommages induits par les espèces activées de l’oxygène. Mais leurs limitations, notamment leur grande taille et leur courte demi-vie, ont poussé les chercheurs à développer de nouveaux antioxydants catalytiques de faible poids moléculaire. Une molécule mimétique de ces protéines doit être stable et non toxique, sa taille et sa charge pouvant aussi permettre le ciblage de sites cellulaires clés dans le stress oxydatif. Trois classes d’antioxydants catalytiques contenant un métal (manganèse) ont été développées : la classe des salens, celle des macrocycles, et enfin celle des métalloporphyrines. Dans ces groupes, on peut distinguer deux sous-divisions : les composés sélectifs et non sélectifs, fondés sur la spécificité de ces composés envers l’anion radical superoxyde lors de l’évaluation in vitro. Les antioxydants catalytiques non sélectifs comprennent les salens ainsi que La Lettre du Pharmacologue - vol. 20 - n° 4 - octobre-novembre-décembre 2006 115 Stratégies thérapeutiques S tratégies thérapeutiques les métalloporphyrines, alors que les macrocycles sont des antioxydants sélectifs (39). Ces derniers sont composés d’un atome de manganèse, au centre d’une molécule fondée sur un ligand penta-azamacrocyclique. Cet atome de manganèse catalyse des transferts à un électron. Les composés de type salens sont généralement des complexes métalliques aromatiques éthylènediamine substitués. Contrairement aux macrocycles, l’atome de manganèse piège ici d’autres espèces oxydantes que le radical anion superoxyde, à savoir le peroxyde d’hydrogène et le peroxynitrite, mais aussi les peroxydes lipidiques. Les métalloporphyrines sont structurellement différentes des protoporphyrines endogènes, et sont classées comme porphyrines méso-substituées synthétiques. Comme pour les salens, l’atome de manganèse manifeste des propriétés antioxydantes envers l’anion radical superoxyde, le peroxyde d’hydrogène, le peroxynitrite et les peroxydes lipidiques. Les antioxydants catalytiques sont actifs dans de nombreux modèles expérimentaux. Ceux-ci incluent la fibrose pulmonaire, les maladies chroniques d’obstruction des poumons, l’asthme, le syndrome de douleur respiratoire aiguë, la dysplasie bronchopulmonaire, les infarctus du myocarde, l’ischémie-reperfusion, le diabète, les transplantations, l’arthrite, la migraine, les maladies neurodégénératives, la pleurésie, la douleur, la démence, la sclérose latérale amyotrophique (39). LA “MÉTABOLISATION” DES ESPÈCES OXYDANTES La “métabolisation” des espèces oxydantes peut permettre leur dégradation et, à l’exception de quelques espèces incluant le radical hydroxyle ou les radicaux alkoxyles, tire parti du fait que la plupart d’entre elles représentent des substrats de réactions enzymatiques. Dès lors, la stimulation de ces activités enzymatiques peut avoir un potentiel anti-stress oxydatif. Néanmoins, il y a lieu d’être attentif à ne pas provoquer de déséquilibre dans la voie de métabolisation des espèces oxydantes qui peut être un facteur d’induction de stress oxydatif. Par exemple, un mode de gestion de la métabolisation des espèces oxydantes caractérisées par un déséquilibre en faveur des activités des superoxyde dismutases (dégradant le radical anion superoxyde mais génératrices d’eau oxygénée), par rapport à celles des glutathion peroxydases et de la catalase (enzymes dégradant l’eau oxygénée), induit une augmentation des concentrations cellulaires en eau oxygénée. Une telle situation existe physiologiquement dans la période néonatale suite à l’immaturité de la glutathion peroxydase. Une induction importante et sélective des superoxyde dismutases, sans induction correspondante de la glutathion peroxydase et de la catalase, aboutit théoriquement au même résultat. Par exemple, l’hyperexpression de la superoxyde dismutase par manipulation génétique dans des modèles expérimentaux aggrave la sensibilité au stress oxydatif ainsi que les lésions consécutives à une stress oxydant (40). La modulation de l’activité des enzymes oxydantes doit 116 donc être pensée non seulement en termes d’ajout de potentiel antioxydant mais aussi dans une stratégie de métabolisation de ces espèces, à adapter au type de stress oxydatif qu’il est censé contrecarrer. Dès lors, une bonne connaissance de la composante oxydative caractérisant le désordre médical auquel le pharmacologue s’adresse est nécessaire en vue d’optimiser l’approche antioxydante choisie. La métabolisation ou dégradation enzymatique/catalytique des espèces oxydantes peut être optimisée soit par la stimulation des enzymes antioxydantes physiologiques soit par l’apport de composés synthétiques mimant les activités enzymatiques antioxydantes. Notons que l’administration intraveineuse de catalase ou encore de superoxyde dismutase humaine d’origine exogène représente une option thérapeutique qui a précédemment fait ses preuves. INDUCTION DES DÉFENSES CELLULAIRES OU STIMULATION DES ENZYMES ANTIOXYDANTES PHYSIOLOGIQUES Différents éléments ou molécules peuvent induire l’activité des défenses antioxydantes cellulaires. C’est le cas notamment de la mélatonine, qui, outre ses propriétés antioxydantes intrinsèques, peut augmenter l’activité des enzymes antioxydantes cellulaires (voir ci-dessus). C’est le cas aussi de composés agissant sur des cibles moléculaires intervenant dans la régulation de la synthèse de ces protéines antioxydantes, comme les agonistes du Peroxisome Proliferator-Activated Receptor de type α (PPARα), qui peuvent induire l’activité de la glutathion peroxydase ou encore de la superoxyde dismutase cytoplasmique (voir ci-dessous). LES MIMÉTIQUES ENZYMATIQUES Les mimétiques enzymatiques incluent des composés synthétiques passés en revue plus haut dans le texte sous la rubrique consacrée aux composés antioxydants. Il s’agit de l’ebselen et de différentes classes de complexes synthétiques (salens, macrocycles et métalloporphyrines) mimant l’activité d’antioxydants catalytiques. D’autre part, il existe des mimétiques enzymatiques d’origine naturelle. Les mimétiques enzymatiques d’origine naturelle incluent les ovothiols, mercaptohistidines retrouvées dans les œufs des invertébrés marins et certains parasites tels que le trypanosome. Les ovothiols sont dotés d’une activité glutathion peroxydase et permettent de résister, notamment lors de la fécondation de l’œuf d’oursin, à l’un des stress oxydatifs physiologiques les plus intensifs existant dans la nature. La haute efficacité de cette défense antioxydante naturelle a conduit au développement d’analogues synthétiques des ovothiols. Il s’agit de composés 4-mercapto-imidazoliques synthétiques, dont le potentiel hautement neuroprotecteur a été récemment démontré de manière expérimentale (41). La Lettre du Pharmacologue - vol. 20 - n° 4 - octobre-novembre-décembre 2006 LES VOIES DE SIGNALISATION CELLULAIRE ET L’EXPRESSION GÉNIQUE : LE POTENTIEL ANTIOXYDANT DU PPARα, UN RÉCEPTEUR NUCLÉAIRE ACTIVÉ PAR LES FIBRATES Les espèces oxydantes peuvent agir comme messagers cellulaires et interagir avec diverses voies de signalisation cellulaire et de régulation de l’expression des gènes. Ces aspects fascinants ont déjà été précédemment évoqués (2) et ont fait l’objet de divers travaux (42). Un aspect retiendra l’attention en cette fin d’article : il s’agit des propriétés antioxydantes/anti-inflammatoires liées à l’activation des PPAR, et notamment du PPARα. Les propriétés antioxydantes et anti-inflammatoires des agonistes du PPARα (fénofibrate, par exemple) apparaissent aujourd’hui aussi importantes que les propriétés normolipémiantes (propriétés anti-hypertriglycéridémiantes, amélioration du rapport HDL/LDL) pour la protection cardiovasculaire offerte par ceux-ci. Même le mode d’action protecteur des statines, inhibitrices de l’HMG-CoA réductase, peut passer par l’activation du PPARα et son impact sur l’expression des gènes et voies de signalisation cellulaire [pour une vue d’ensemble du mode d’action des fibrates et des statines, le lecteur est renvoyé à la revue de Fruchart et Duriez (43)]. Parmi les processus cellulaires générateurs d’espèces oxydantes, la voie des lipo-oxygénases ou celle de la cyclo-oxygénase, par le biais de la formation des leucotriènes, des thromboxanes et des prostaglandines, sont sollicitées par la cellule pour orchestrer et développer la réponse inflammatoire. Le métabolisme de l’acide arachidonique est donc à la fois pro-oxydant et proinflammatoire. L’inhibition, par exemple, de la cyclo-oxygénase a une valeur à la fois antioxydante et anti-inflammatoire. La cyclo-oxygénase existe en fait sous deux formes, une forme constitutive ubiquitaire appelée cyclo-oxygénase 1 (COX-1), et une forme inductible appelée COX-2, observée après activation cellulaire, notamment par des cytokines. Cette COX-2 représente une cible antioxydante et anti-inflammatoire intéressante et peut être inhibée par les coxibs. D’autres agents anti-inflammatoires traditionnels inhibent à la fois COX-1 et COX-2. La COX-2, c’est-à-dire la cyclo-oxygénase inductible, peut être ciblée autrement que par inhibition directe par le composé. L’induction même de la protéine peut être bloquée par des agents pharmacologiques. Il a été démontré depuis plusieurs années déjà que l’activation du PPARα pouvait bloquer l’induction de cette COX-2 (44). Les travaux qui suivirent la mise en évidence de cet effet ont révélé que, en fait, l’activation du PPARα pouvait conduire à la dépression des voies de signalisation cellulaire construites autour des facteurs de transcription NF-κB et AP1, voies pro-inflammatoires/pro-oxydantes. Il a été documenté que ce rôle antioxydant/anti-inflammatoire de l’activation du PPARα obéissait à un mécanisme de transrépression, et que des protéines pro-inflammatoires/pro-oxydantes autres que la COX-2 pouvaient être régulées négativement au terme des effets transrépressifs du PPARα. La régulation négative de protéines (COX-2 mais aussi différentes protéines d’adhésion cellulaire comme le VCAM ou encore l’ICAM) par le PPARα joue ainsi un rôle primordial dans le contrôle anti-inflammatoire et donc protecteur exercé par les agonistes du PPARα (les fibrates, par exemple) sur le développement de l’athérosclérose et des maladies cardiovasculaires. La figure 2 résume les mécanismes impliqués dans le potentiel antioxydant/anti-inflammatoire du PPARα et des fibrates (45). De manière intéressante, le fénofibrate induit certaines activités antioxydantes et représente un composé doté Stratégies thérapeutiques S tratégies thérapeutiques Figure 2. Potentiel antioxydant/anti-inflammatoire du PPARα. Agoniste du PPARB (physiologique, le LTB4 ; L’activation du PPARα survient avec la fixation d’un ligand RXRB PPARB pharmacologique, les fibrates) agoniste (un fibrate dans le cas d’une action pharmacologique). 9-cis rétinoate PPARB Une fois activé, le PPARα peut exercer un effet régulateur sur activé l’expression génique et les voies de signalisation cellulaire NF-LB PPARB RXRB PPARB PPARB par deux mécanismes essentiellement distincts. Le premier PPARB (ou AP-1) activé activé activé activé activé mécanisme est celui qui a été le premier décrit et correspond PPRE à la fixation du PPARα activé, après hétérodimérisation avec NF-LB (ou AP-1) le RXRα, lui aussi activé par son propre ligand, sur des motifs Action retrouvés dans la région promotrice de gènes cibles, motifs Réponse normoModulation de l’ e xpression de gènes inflammatoire lipémiante impliqués dans l’oxydation et le trafic appelés PPRE (Peroxisome Proliferator [PPAR] Responsive NF-LB (ou AP-1) des acides gras et du cholestérol Elements). Ce mécanisme porte le nom de “transactivation” et conduit surtout à la stimulation de diverses protéines Bénéfice NF-LB RE Modulation de l’expression (ou AP-1 RE) (enzymes de la β-oxydation et du transport des acides gras, de gènes impliqués thérapeutique synthèse accrue de l’apo-AI), et occasionnellement à la dans le contrôle redox et les voies de l’inflammation répression d’autres (apo-CIII). Ces modifications métaboliques ont une action normolipémiante, c’est-à-dire qu’elles ont une action anti-hypertriglycéridémiante ou encore hypocholestérolémiante. Ces effets induisent en fait un profil lipidique protecteur vis-à-vis des désordres cardiovasculaires. Le rôle protecteur apporté par l’activation du PPARα dans ces désordres relève aussi du deuxième mécanisme illustré sur la figure, à savoir le mécanisme transrépressionnel. La transrépression par le PPARα s’exprime surtout vis-à-vis de facteurs de transcription impliqués dans la signalisation cellulaire relative aux voies cellulaires redox et celles de l’inflammation. Dans ce mécanisme, le PPARα activé ne se lie pas à l’ADN, mais inactive le facteur de transcription auquel il se fixe. En fait, il empêche le facteur de transcription complexé de se lier à l’ADN et, par là même, empêche celui-ci de jouer son rôle naturel de messager cellulaire, le détournant de sa fonction et suspendant ainsi ladite fonction. Les facteurs de transcription ainsi complexés par le PPARα dans le cadre de son activité transrépressionnelle incluent le NF-κB et l’AP-1, facteurs de transcription jouant un rôle clé dans les voies pro-oxydantes/pro-inflammatoires de la cellule. D’autres facteurs de transcription tels que STAT peuvent ainsi être complexés par le PPARα (45). Activation Transactivation Transrépression La Lettre du Pharmacologue - vol. 20 - n° 4 - octobre-novembre-décembre 2006 117 Stratégies thérapeutiques S tratégies thérapeutiques 118 de propriétés neuroprotectrices récemment mises en évidence dans un modèle animal de l’AVC (accident vasculaire cérébral) (ischémie/reperfusion par occlusion/désocclusion de l’artère cérébrale moyenne) [46]. ■ 23. Reiter R, Tang L, Garcia JJ, Munoz-Hoyos A. Pharmacological actions of melatonin in oxygen radical pathophysiology. Life Sci 1997;60:2255-71. RÉFÉRENCES BIBLIOGRAPHIQUES 26. Pincemail J, Defraigne JO. Le coenzyme Q10 ou ubiquinone : un antioxydant particulier. Vaisseaux, Cœur, Poumons 2003;8:55-60. 1. Richard JL, Cambien F, Ducimetière P. Epidemiologic characteristics of coronary diseases in France. Nouv Presse Med 1981;10:1111-4. 2. Vamecq J, Vallée L, Storme L, Gelé P, Bordet R. Les acteurs immédiats du stress oxydatif [Key players in oxidative stress]. La Lettre du Pharmacologue 2004;18:16-23. 3. Puisieux F, Deplanque D, Bulckaen H et al. Brain ischemic preconditioning is abolished by antioxidant drugs but does not up-regulate superoxide dismutase and glutathion peroxidase. Brain Res 2004;1027:30-7. 4. Weiss G, Loyevsky M, Gorleuk VR. Dexrazoxane (ICRF-187). Gen Pharm 1999; 32:155-8. 5. Voest EE, Vreugdenhil G, Marx JJM. Iron-chelating agents in non-iron overload conditions. Ann Intern Med 1994;120:490-9. 6. Saran M, Beck-Speier I, Fellerhoff B, Bauer G. Phagocytic killing of microorganisms by radical processes: consequences of the reaction of hydroxyl radicals with chloride yielding chlorine atoms. Free Red Biol Med 1999;26:482-90. 7. Park JB. Phagocytosis induces superoxide formation and apoptosis in macrophages. Exp Mol Med 2003;35:325-35. 8. Brandes RP, Kreuzer J. Vascular NAD(P)H oxidases: molecular mechanisms of activation. Cardiovasc Res 2005;65:16-27. 9. Nishino T. The conversion of xanthine dehydrogenase to xanthine oxidase and the role of the enzyme in reperfusion injury. J Biochem 1994;116:1-6. 10. Houston M, Estevez A, Chumley P et al. Binding of xanthine oxidase to vascular endothelium. Kinetic characterization and oxidative impairment of nitric oxide-dependent signaling. J Biol Chem 1999;274:4985-94. 11. Shiba D, Shimamoto N. Attenuation of endogenous oxidative stress-induced cell death by cytochrome P450 inhibitors in primary cultures of rat hepatocytes. Free Rad Biol Med 1999;27:1019-26. 12. Tsai P, Weaver J, Liang Cao G et al. L-arginine regulates neuronal nitric oxide synthase production of superoxide and hydrogen peroxide. Biochem Pharmacol 2005;69:971-9. 13. Hamada Y, Hayakawa T, Hattori H, Mikawa H. Inhibitor of nitric oxide synthesis reduces hypoxic-ischemic brain damage in the neonatal rat. Pediatr Res 1994;35:10-4. 14. Figueroa S, Lopez E, Arce C, Oset-Gasque MJ, Gonzalez MP. SNAP, a NO donor, induces cellular protection only when cortical neurons are submitted to some aggression process. Brain Res 2005;1034:25-33. 15. Fang YZ, Yang S, Wu G. Free radicals, antioxidants, and nutrition. Nutrition 2002;18:872-9. 16. Willis MS, Wians FH. The role of nutrition in preventing prostate cancer: a review of the proposed mechanism of action of various dietary substances. Clin Chim Acta 2003;330:57-83. 17. Rao AV, Agarwal S. Role of lycopene as antioxidant carotenoid in the prevention of chronic diseases: a review. Nutrition Res 1999;19:305-23. 18. Meyers CD, Kamanna VS, Kashyap ML. Niacin therapy in atherosclerosis. Curr Opin Lipidol 2004;15:659-65. 19. Cook NC, Samman S. Flavonoids–Chemistry, metabolism, cardioprotective effects, and dietary sources. Nutr Biochem 1996;7:66-76. 20. Gilgun-Sherki Y, Rosenbaum Z, Melamed E, Offen D. Antioxidant therapy in acute central nervous system injury: current state. Pharmacol Rev 2002;54:271-84. 21. Lesieur D, Leclerc V, Chavatte P, Marot C, Renard P, Guardiola-Lemaïtre B. La mélatonine, prototype pertinent pour l’innovation thérapeutique. Therapie 1998;53:429-37. 22. Reiter RJ, Tan DX, Gitto E et al. Pharmacological utility of melatonin in reducing oxidative cellular and molecular damage. Pol J Pharmacol 2004;56:159-70. 24. Parker L, Tritachler H, Wessel K. Neuroprotection by the metabolic antioxidant and α-lipoic acid. Free Rad Biol Med 1997;22:359-78. 25. Ernster L, Dallner G. Biochemical, physiological and medical aspects of ubiquinone function. Biochim Biophys Acta 1995;1271:195-204. 27. Latruffe N, Delmas D, Jannin B, Cherkaoui-Malki M, Passilly-Degrace P, Berlot JP. Molecular analysis on the chemopreventive properties of resveratrol, a plant polyphenol microcomponent. Int J Mol Med 2002;10:755-60. 28. Sullivan PG, Geiger JD, Mattson MP, Scheff SW. Dietary supplement creatine protects against traumatic brain injury. Ann Neurol 2000;48:723-9. 29. Behl C. Estrogen can protect neurons: mode of action. J Steroid Biochem Mol Biol 2003;83:195-7. 30. Behl C et al. Neuroprotection against oxidative stress by estrogens–Structureactivity relationship. Mol Pharmacol 1997;51:535-41. 31. Shen S, Cooley DM, Glickman LT, Glickman N, Waters DJ. Reduction in DNA damage in brain and peripheral blood lymphocytes of elderly dogs after treatment with dehydroepiandrosterone (DHEA). Mut Res 2001;480/481:153-62. 32. Pétrault O, Bastide M, Cotelle N et al. The neuroprotective effect of the antioxidant flavonoid derivate di-tert-butylhydroxyphenyl is parallel to the preventive effect on post-ischemic Kir2.x impairment but not to post-ischemic endothelial dysfunction. Arch Pharmacol 2004;370:395-403. 33. Knuckey NW, Palm D, Primiano M, Epstein MH, Johanson CE. N-acetylcysteine enhances hippocampal neuronal survival after transient forebrain ischemia in rats. Sytoke 1995;26:305-10. 34. Cotgreave IA. N-acetylcysteine: pharmacological considerations and experimental and clinical applications. Adv Pharmacol 1997;38:205-27. 35. Hall ED, McCall JM, Means ED. Therapeutic potential of the lazaroids (21aminosteroids) in acute central nervous system: trauma, ischemia and subarachnoid hemorrhage. Adv Pharmacol 1994;28:221-68. 36. Horakova L, Stolc S. Antioxidant and pharmacodynamic effects of pyroindole stobadine. Gen Pharmacol 1998;30:626-38. 37. Sies H. Ebselen, a selenoorganic compound as glutathione peroxidase mimic. Free Rad Biol Med 1993;14:313-24. 38. Ogawa A, Yoshimoto T, Kikuchi H et al. Ebselen in acute middle cerebral artery occlusion: a placebo-controlled, double-blind clinical trial. Cerebrovasc Dis 1999;9:112-8. 39. Day BJ. Catalytic antioxidants: a radical approach to new therapeutics. Drug Discovery Today (DDT) 2004;9:557-66. 40. Fullerton HJ, Ditelberg JS, Chen SF et al. Copper/zinc superoxide dismutase transgenic brain accumulates hydrogen peroxide after perinatal hypoxia ischemia. Ann Neurol 1998;44:357-64. 41. Vamecq J, Maurois P, Bac P et al. Potent mammalian cerebroprotection and neuronal cell death inhibition are afforded by a synthetic antioxidant analogue of marine invertebrate cell protectant ovothiols. Eur J Neurosci 2003;18:1110-20. 42. Haddad JJ. Oxygen sensing and oxidant/redox-related pathways. Biochem Biophys Res Commun 2004;316:969-77. 43. Fruchart JC, Duriez P. Anti-cholesterol agents, new therapeutic approaches. Ann Pharm Fr 2004;62:3-18. 44. Staels B, Koenig W, Habib A et al. Activation of human aortic smooth-muscle cells is inhibited by PPARα but not by PPARγ activators. Nature 1998;393: 790-3. 45. Ghinetti G, Fruchart JC, Staels B. Peroxisome proliferator-activated receptors and inflammation: from basic science to clinical applications. Int J Obesity 2003;27:S41-S45. 46. Deplanque D, Gelé P, Pétrault O et al. Peroxisome proliferator-activated receptor-alpha activation as a mechanism of preventive neuroprotection induced by chronic fenofibrate treatment. J Neurosci 2003;23:6264-71. La Lettre du Pharmacologue - vol. 20 - n° 4 - octobre-novembre-décembre 2006