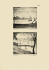Bulletin SZF 133/4 - Faculté de Biologie
Transcription
Bulletin SZF 133/4 - Faculté de Biologie
Bull. Soc. zool. Fr., 2008, 133(4) : 303-316 Histoenzymologie ÉTUDE HISTOCHIMIQUE ET HISTOENZYMOLOGIQUE DU FOIE DE PSAMMOMYS OBESUS PRIS COMME MODÈLE POUR L’ÉTUDE DU DIABÈTE ET DE SES COMPLICATIONS HÉPATIQUES par Salima EL-AOUFI 1, Boubekeur MAOUCHE 2, Souad SENNOUNE 3 et Lakhdar GRIENE 4 Une expression courante du syndrome métabolique, chez le rat des sables Psammomys obesus, étroitement relié au diabète de type 2 est un dysfonctionnement profond du système enzymatique et une sérieuse altération des hépatocytes qui induisent de graves affections hépatiques. Cette étude se propose d’évaluer les changements histopathologiques, histochimiques et histoenzymologique du tissu hépatique du Psammomys obesus soumis à un régime alimentaire hypercalorique (RHC) sans hyperphagie, pendant le développement de l’obésité et du diabète. Notre étude a duré 15 mois et a concerné 10 rats Wistar (Rattus norvegicus) et 62 rats des sables répartis en 2 lots : 24 utilisés comme témoins, soumis au régime des plantes halophiles (20-22 cal/j), et 38 (15 mâles et 23 femelles) soumis au RHC (32.5 cal/j) et de l’eau salée (0.9 %) ad libitum. Sur le plan histochimique et histoenzymologique 20 activités enzymatiques et 5 substances macromoléculaires ont été examinées. L’expérience a montré que plusieurs activités histoenzymatiques se sont profondément modifiées chez les rongeurs du désert par rapport au rat Wistar. Nous avons noté, en particulier, que les activités des estérases carboxyliques et des cholinestérases, responsables des activités lipolytiques chez le rat des sables, sont extrêmement faibles comparées à celles observées chez le rat Wistar, considéré comme un modèle animal diabétorésistant. Mais les hépatocytes du rat des sables se distinguent fondamentalement de ceux du rat Wistar, par une G6P beaucoup plus faible, qui pourrait expliquer l’adaptation métabolique de cet animal à un régime sans carbohydrates. Cette « carence » naturelle en G6P s’aggrave durant le RHC par l’accroissement de la G6Pase qui permet de mettre encore plus de glucose dans la circulation sanguine. Lorsque l’on compare les animaux atteints de diabète non insulinodépendants (DNID) aux insulinodépendants (ID), on constate que la phosphorylase et l’UDPG-synthetase, actives chez les obèses et les NID, sont absentes chez les ID pour lesquels 304 Bulletin de la Société zoologique de France 133 (4) on note une hyperactivité de certaines enzymes lysosomiales. Comme chez les humains, on note que le DNID est associé à une éosinopénie, une neutrophilie et à une croissance de la phosphatase alcaline qui indique la présence de nécroses hépatocellulaires. Durant le RHC, le foie subit des modifications pathologiques profondes induites par ce régime. Les réactions histochimiques et les modifications histoenzymologiques observées sont en parfaite corrélation avec les résultats analytiques Les perturbations des hépatocytes sont semblables à celles observées dans le diabète humain. Cette étude renforce l’idée que des désordres endocriniens, comme le DNID, peuvent être à l’origine d’affections hépatiques graves et qu’il y a un lien réciproque entre les maladies du foie et ce type de diabète. Notre animal, polygénique naturel, apparaît comme un excellent modèle bien adapté aux recherches sur les interactions environnement-régime alimentaire et leurs conséquences pathologiques au niveau endocrinien. Histochemical and histoenzymological study of the liver of Psammomys obesus as a model for the study of diabetes and its hepatic complications A current expression of the metabolic syndrome in the sand rat Psammomys obesus is a deep dysfunction of the enzymatic system and a serious alteration of the hepatocytes, which induce severe liver diseases. This study is designed to evaluate the histopathological, histochemical and histoenzymological changes of the hepatic tissue of a sand rat, fed with a high calorie diet (HCD), without hyperphagia, during the development of obesity and diabetes. Our study lasted 15 months and concerned 10 Wistar rats (Rattus norvegicus), and 62 Psammomys obesus divided into 2 groups: halophiles plant diet (20-22 cal/d), 24 animals used as the control group, and HCD (32.5 cal/d and salty water (0.9%) ad libitum), 15 males and 23 females. 20 enzymatic activities and 5 molecular substances have been investigated. The experiment showed that several histoenzymatic activities profoundly changed in the desert rodents in comparison with the Wistar rat. The healthy Psammomys group presented extremely weak activities of lipolytic enzymes, but their hepatocytes were basically distinguished from those of Wistar rat by a G6P clearly lower, which would explain the major metabolic adaptation of this animal to a diet without carbohydrates. This natural deficiency in G6P worsens during the HCD due to the increase of G6Pase which causes the release of more glucose into the blood circulation. Phosphorylase and UDPG-synthetase, which are active in obese Psammomys, were absent in diabetic individuals, for which we found, in IDDM state, a hyperactivity of lysosomal enzymes. Lastly, as in humans, diabetes is associated with an eosinopenia, a neutrophilia and growth of the alkaline phosphatase which indicates the presence of hepatocellular necrosis During the HCD the liver undergoes deep, diet-induced pathological modifications. The histochemical reactions and the histoenzymological modifications observed are in perfect correlation with the analytic results. The perturbations of the hepatocytes are similar to those observed in human diabetes. This study reinforces the idea that some endocrine disorders, like diabetes mellitus, may actually cause many liver diseases and that there is a reciprocal link between liver diseases and diabetes. The polygenic P. obesus reproduces this correlation and seems to be an excellent model, naturally adapted to research on the interactions between environment, diet, endocrine diseases and their pathological consequences. 305 Histoenzymologie du foie de Psammomys Introduction Alors que la prévalence du diabète a atteint des proportions épidémiques et touche toutes les couches de la société, cette maladie reste encore mal connue (FERY & PAQUOT, 2005). En fait le diabète n’apparaît pas comme une maladie unique mais, comme un « syndrome métabolique », qui n’a été considéré comme nouvelle entité médicale que depuis le Congrès de Mexico (MEXICO, 2000). Compte tenu du caractère chronique et débilitant de la maladie et de son coût (STRATTON et al., 2000), le diabète apparaît comme un grave et important problème de santé publique mondial, particulièrement dans les pays en développement. Selon l’OMS, ces pays, en raison des changements brutaux d’habitudes alimentaires et de style de vie, paieront le plus lourd tribut à cette épidémie dans le courant de ce siècle. On prévoit en effet que 80 % des nouveaux cas de diabète, essentiellement de type 2 (DT-2) vont apparaître dans ces pays d’ici 2025. Aujourd’hui, le diabète touche plus de 230 millions de personnes soit près de 6 % de la population mondiale adulte. De nombreuses études ont montré que l’obésité et le DT-2 sont souvent associés à un régime hypercalorique (RHC) et la relation obésité et diabète est également bien établie (KAHN & FLIER, 2000). Dans une étude précédente, nous avons montré que le Psammomys obesus sauvage peut être considéré aujourd’hui comme un animal polygénique modèle pour l’étude du DT-2 de par l’insulinorésistance rapide qu’il développe dès qu’il est soumis à un régime classique de laboratoire qui s’avère hypercalorique pour lui et nous avons montré également qu’il existe un lien direct entre ce régime, l’obésité, le diabète et les altérations athéroscléreuses observées au niveau de l’aorte de cet animal (EL-AOUFI et al., 2007). Notons que l’intérêt de cet animal va au-delà de l’étude du diabète puisqu’on le considère comme un excellent modèle pour l’étude des conséquences de l’ischémie cérébrale (LEHOTSKY et al., NAGATA et al., PHILLIS et al., 1999) ainsi que pour des études portant sur l’audition (SICHEL et al., TUCCI et al., 1999). Mais une autre manifestation courante du DT-2 est l’altération grave que subit le foie, qui peut aller, chez les humains, jusqu’à la stéatose hépatique généralisée et à la nécrose hépatocytaire (LEVINTAL & TAVILL, 1999). Les changements des activités enzymatiques induites par le DT-2 sont à l’origine de nombreuses maladies (SENNOUNE et al., 1999) qui apparaissent comme une conséquence du diabète sucré. Le dysfonctionnement enzymologique du foie a souvent pour effet, soit d’aggraver le syndrome métabolique, soit de déclencher le diabète, comme l’atteste la présence simultanée de l’hépatite C et du DT-2 chez le même patient (CHEDIN et al., 1996). En fait, l’observation courante de la prévalence de maladies chroniques du foie chez les patients diabétiques, indique qu’il existe une forte corrélation entre le métabolisme hépatique et l’homéostasie du glucose. Le rôle du foie est, en effet, central et crucial dans la régulation du métabolisme des carbohydrates et toute altération, contrôlée, de son fonctionnement peut être un indicateur précieux dans l’étude de la pathogénie de l’intolérance au glucose dans des affections hépatiques et dans le DT-2 lui-même. Dans ce travail, nous proposons une étude histologique, histochimique et histoenzymologique des altérations du tissu hépatique, induites par un régime standard de laboratoire et consécutives au développement de l’obésité et du diabète jusqu’à sa phase terminale, chez un rongeur du désert : Psammomys obesus. Cette étude vise à mieux 306 Bulletin de la Société zoologique de France 133 (4) comprendre les interactions qui relient le SM aux changements biochimiques qui se produisent en présence du diabète mais aussi à mieux cerner l’origine de l’insulinorésistance, en comparant les réponses enzymatiques induites par un RHC sur le foie de Psammomys obesus et sur celui du rat Wistar (Rattus norvegicus), modèle animal connu pour être peu sensible au diabète (CHALKLEY et al., 2002). Un même parallèle a été souligné chez les humains (KALMAN et al., 2001) où les populations habituées à une alimentation frugale développent plus rapidement une insulinorésistance, de l’obésité, de l’athérosclérose et des maladies cérébrovasculaires, que d’autres, habituées à une alimentation plus riche en calories. Matériels et méthodes Matériel Les Psammomys obesus sont capturés dans la région de Béni-Abbès (vallée de la Saoura, 30°7 Nord, 2°10 Ouest) où ils se nourrissent de plantes halophiles de la famille des Chénopodiacées et ne boivent jamais d’eau. Le tableau 1 donne la composition des régimes alimentaires hypercalorique et naturel. À leur réception au laboratoire, ils sont placés dans un vivarium à température et degré hygrométrique constants (25°C et 60 % respectivement) proches de ceux de leur biotope naturel. Cette étude a duré 15 mois et a concerné 72 animaux adultes répartis en trois lots : – 10 rats Wistar (espèce Rattus norvegicus) utilisés comme référence ; – 24 Psammomys obesus témoins nourris aux plantes halophiles à raison de 50 g/j de plantes fraîches (équivalent à 20-22 cal/j) ; – 38 animaux dont 15 mâles et 23 femelles, soumis au RHC (régime standard de laboratoire) à raison de 10 g/jour (équivalent à 32,5 cal/j) et de l’eau salée à 0.9 % ad libitum. Notons que cette prise alimentaire ne représente que la moitié de celle ingérée par un rat Wistar de poids équivalent. Au début de chaque semaine, les animaux sont pesés et du sang est extrait au niveau du sinus rétro orbital de l’œil pour le dosage du glucose, de l’insuline plasmatique, et des Tableau 1 Composition (en %) des régimes alimentaires Alimentary diet composition (in %) Éléments Régime Naturel H2O Minéraux Lipides Protéines Sucres Totaux Cellulose Lignine Hémicelluloses Indéterminées 80. 79 6. 86 0. 40 3. 53 0. 18 2. 23 1. 12 2. 62 2. 27 Remarques Hypercalorique * Taux de glucides utilisables = 100 - (taux de protéines 9 7. 1 7. 5 25.0 47.43* 4.0 / / / crues + taux de matières grasses + taux de cendres + taux de cellulose + taux d'humidité). Remarque : les hydrates de carbone (sucres totaux, lignine, cellulose, hémicelluloses et quantité indéterminée) constituent 8,42 % de la composition totale. * Rate of useful carbohydrates = 100 - (rate of crude proteins + rate of fats + rate of cinder + rate of cellulose + rate of humidity). Remark : the carbohydrates (complete sugars, lignine, cellulose, hemicelluloses and indeterminate quantity) constitute 8.42 % of the complete composition. 307 Histoenzymologie du foie de Psammomys lipides. Les échantillons d’urines sont recueillis journellement pour mesurer le taux de glucose, la cétonurie et l’albuminurie, et les tests de résistance à l’insuline sont faits régulièrement. Ce suivi permanent permet de connaître à tout moment le statut métabolique précis des animaux et, en particulier, de déterminer le moment exact du sacrifice. Techniques et méthodes utilisées 1. Dosages Nous avons utilisé les techniques classiques pour les divers tests et dosages du glucose et de l’insuline plasmatique et la technique du « clamp » euglycémique-insulinique (DEFRONZO, 1991) pour mesurer la sensibilité périphérique à l’insuline. 2. Techniques histologiques Après sacrifice de l’animal par décapitation, le foie prélevé est pesé puis plongé dans le liquide de Bouin alcoolique (Duboscq-Brasil) (GABE, 1968). Après fixation, les pièces sont recoupées, soigneusement déshydratées et éclaircies puis emparaffinées dans une étuve à 58°C. L’enrobage, réalisé grâce à des « barres de Leuckart », nous a permis de confectionner le couplage des blocs. Les coupes de 5 à 7 µm d’épaisseur ont été réalisées au moyen d’un microtome automatique « Americanoptical ». Les colorations topographiques ont été réalisées, à l’hématoxyline de Groat (préparations à froid) et au trichrome de Mallory (GANTER & JOLLES, 1970). Pour les études histochimiques nous avons utilisé la coloration classique à l’acide périodique Schiff (McMANUS, 1961, BANCROFT et al., 1996). Les coupes colorées sont montées à l’aide du baume du Canada. 3. Techniques histoenzymologiques et histochimiques Les techniques utilisées sont celles décrites dans divers ouvrages (PEARSE, 1980) et par divers auteurs (Mc MANUS, 1961 ; BANCROFT, 1996). Les fragments d’organe recueillis sur la gaze imbibée d’eau physiologique sont stockés 30 mn à 4°C puis montés sur le même bloc que ceux du Psammomys témoin correspondant. Celui-ci, après immersion (30 mn) dans de l’azote liquide, est placé dans l’enceinte du cryostat à -20°C (30 mn) puis débité en coupes de 8 mm d’épaisseur. Celles-ci sont ensuite incubées dans des milieux appropriés pour la mise en évidence de l’enzyme recherchée. Dans nos expériences, nous avons utilisé trois groupes de technique : oxydoréduction, précipitation et couplage. • La technique d’oxydoréduction nous a permis de mettre en évidence les déshydrogénases et oxydoréductases. Dans la réaction histoenzymatique on a introduit, dans un milieu accepteur final exogène, du bleu de tétranitro tétrazolium. La réduction de ce denier en Formazan donne un précipité, visible sous forme de grains bleus (NBT) ou bruns (TNBT). Le Formazan étant liposoluble, pour éviter son apposition aspécifique à la surface des lipides figurés éventuellement présents, nous avons fait subir à nos coupes une préfixation à l’acétone. Certaines des enzymes recherchées par ces techniques étant hydrosolubles (G6-PDH, LDH), nous avons ajouté une proportion de 6 % de gélose au milieu d’incubation pour réduire leur fuite éventuelle dans le milieu et voir ainsi leur activité diminuer. 308 Bulletin de la Société zoologique de France 133 (4) • La technique de précipitation met en évidence des hydrolases. Les substrats utilisés sont des esters de l’acide phosphorique, sulfurique, de naphtol mono- ou tri- esters selon l’enzyme recherchée. • Les techniques de couplage mettent en évidence certaines estérases. Le naphtol, libéré par l’hydrolase de l’ester de naphtol, ainsi que les ions de phosphate libérés au site d’activité enzymatique des différentes hydrolases, sont révélées in situ par diazocouplage pour le premier et par sulfure d’ammonium pour les seconds (MILLER & KARN, 1980). 4. Évaluation et expression des résultats Pour l’étude des macromolécules et des enzymes hépatiques les prélèvements du foie des animaux soumis au RHC et au régime des plantes halophiles ont été juxtaposés, traités et observés simultanément. Sur le plan histochimique et histoenzymologique 20 activités enzymatiques et 05 substances macromoléculaires ont été examinées. Les intensités des réactions histochimiques dans différents tissus sont comparées dans le même champ du microscope et exprimées par un indice de positivité de 0 à 4 traduisant des activités négative (0), à peine perceptible (0.5), puis de 1 à 4 pour, respectivement, « faible », « modéré », « intense » et « très intense ». Cette méthode étant « manuelle », trois observateurs indépendants ont été commis à la lecture des lames, et tous les résultats obtenus pour chaque activité enzymatique ont été validés par des tests de contrôle effectués en incubant les coupes dans un milieu sans substrat. Les activités enzymatiques mises en évidence nous ont permis de faire une étude topographique du métabolisme du tissu hépatique Résultats Polarité fonctionnelle du métabolisme glucidique et différence entre les deux espèces 1. Activités enzymatiques (tableau 2) Les foies des Psammomys soumis au régime naturel présentent une charge glycogénique normale, une absence de lipides qui explique la faible activité des enzymes lipolytiques, une basophilie et une pyroninophilie modérée qui dénote leur aptitude de synthèse. Mais ces hépatocytes révèlent des activités enzymatiques intenses pour la dégradation oxydative anaérobie (LDH) ou aérobies (G6PDH, SDH, IDH) du glucose, pour le métabolisme protéique (GLDH), le catabolisme des amines biogènes (MAO) et pour la néoglucogenèse (G6Pase). En regard des canalicules biliaires, les hépatocytes présentent une forte activité ATPasique alors qu’au même niveau, la phosphatase alcaline ALP et la 5’ nucléotidase paraissent moins positives. La phosphatase acide et l’aminopeptidase, d’activité modérée, reflètent le contenu lysosomial des hépatocytes. 2. Différences topographiques La distribution des isoenzymes et leurs paramètres cinétiques locaux varient selon les différentes zones des lobules du foie observées d’où la répartition inégale des activités 309 Histoenzymologie du foie de Psammomys Tableau 2 Activités enzymatiques du foie du Psammomys obesus, normal et diabétique Enzymatic activities of the liver of the normal and diabetic Psammomys obesus Enzymes Glucose 6PDH Lactate DH Hydroxybutyrate Isocitrate DH Succinate DH Malate DH Glutamate DH NADH2 DH NADPH2 DH MAO 5’Nucléotidase ATPase Ca++ Indoxyl Esterase Naphtyl Esterase Cholinesterase Phospatase acide Sulfatase β-Glucoronidase Glucose 6 Pase Phosphatase alcaline Aminopeptidase Glycogen synthétase Phosphorylase Leucineamino-peptidase Normal Diabétique Macromolécules Normal Diabétique 1,5 2,5 2 4 4 13+ 4 43+ 1,5 1,5 1 1 0,5 0,5 4 3 2 1,5 2 1 3 2 2,5 3 3 3 3 3 4 4 4 4 1 0,5 2,5 2,5 1,5 2 5 2 4 4 4 2 0 1 Substances PAS+ Glycogène GAG Lipides neutres ARN 2 2 0.5 0.5 1.5 4 (ou 0,5) 4- (ou 0) 4- (ou 0) 1,5 0,5 Nota : les deux colonnes de gauche correspondent aux dosages histoenzymologiques ; les deux colonnes de droite correspondent aux dosages histochimiques. Nota : both two left columns correspond to histoenzymologic dosages; the two columns on the right correspond to histochemical dosages. enzymatiques (VAN NOORDEN et al., 1995). Ainsi, le gradient d’activité de l’α-G6Pase croît nettement de la veine centrolobulaire vers la périphérie, alors que les activités de la glycogène-phosphorylase et de la glycogène synthétase sont plus intenses autour de la veine centrolobulaire (figures I-1 à 3). Il en est de même de certaines oxydoréductases qui sont mieux représentées en périphérie. Ce phénomène suggère l’existence d’une polarité fonctionnelle du métabolisme glucidique, le métabolisme du glycogène s’effectuant dans la partie périphérique du lobule hépatique alors que la néoglucogenèse se déroule autour de la veine centrale. 3. Différences entre les deux espèces de rongeurs Au niveau enzymologique la différence fondamentale entre les hépatocytes de ces deux espèces réside dans la moindre activité, chez le Psammomys, de la G6-Pase, des enzymes de la voie des pentoses (G6-PDH), de la glycolyse anaérobie (LDH), de la lipolyse, de la glycogénolyse. Les hépatocytes du Psammomys sont, par contre, mieux pourvus en enzymes lysosomiales comme la MAO et la glycuronidase (figures I-4,5). De façon générale, les activités des estérases carboxyliques, responsables de l’activité lipolytique, sont très faibles chez le Psammomys, alors que la cholinestérase bien que faible pour les deux espèces reste supérieure chez le rat Wistar. 310 Bulletin de la Société zoologique de France 133 (4) Figure I Inégale répartition de certaines activités enzymatiques au sein du lobule hépatique I.1 : Activité plus élevée autour de l’espace porte et plus faible autour de la veine centrolobulaire ; I.2 : détail du lobule hépatique (x150). I.3 : Glycogène-phosphorylase: activité très intense autour de la veine centrolobulaire. Gradient inverse de celui trouvé pour l’enzyme précédente. Unequal sharing out of certain enzymatic activities within the hepatic lobule I-1: Higher activity around portal space and weaker around the centrolobulaire vein; I-2: detail of the hepatic lobule; I-3: Glycogene-phosphorylase: very intense activity around the centrolobular vein areas. Gradient is reverses that found for the preceding enzyme. Effets du régime hypercalorique 1. Foie des animaux obèses non diabétiques ; aspects histologiques et histochimiques Dès le troisième mois, le tissu hépatique est altéré particulièrement dans la zone périlobulaire. La charge glycogénique augmente, les hépatocytes sont plus volumineux et légèrement spumeux et le système vasculaire s’efface (figures II-1,2). Après six mois (figures II-3 à 5), les cellules hépatocytaires sont hypertrophiées, le cytoplasme s’éclaircit et l’on note une importante surcharge lipidique. La dégénérescence cellulaire s’accentue progressivement, mais l’animal ne développe pas de diabète. En effet, comme cela a été montré sur des rats GK obèses, les cellules β du pancréas continuent de sécréter suffisamment d’insuline pour compenser la résistance à l’insuline induite par le RHC (WENBIN et al., 2002). 2. Psammomys obesus diabétiques : aspects histologiques Chez l’animal diabétique, le métabolisme du glucose est partiellement détérioré du fait de l’insulinopénie induite par un niveau d’AGL chroniquement élevé. Chez l’homme, l’accumulation de graisses dans le foie par suite de l’insulinorésistance, est la 311 Histoenzymologie du foie de Psammomys première étape du développement de la stéatohépatite non alcoolique (LEVINTAL et al., 1999). Si de plus on lui associe les complications habituelles du syndrome métabolique, la lésion hépatique finit par engendrer des nécroses (KAHN et al., 2000). C’est exactement ce que l’on observe au sixième mois de RHC dans ce groupe de Psammomys où apparaît une alternance de lobules normaux et de lobules atteints, de compacité accrue. Chez les Psammomys insulinodépendants, il apparaît une hyperlipémie à triglycérides et une stéatose importante avec présence de très nombreuses cellules vides ou 1. Foie « adulte sain » (x200) 1. Liver « healthy adult » 2. Foie « obèse 6 mois » (x400) 2. Liver « obese 6 months » (x400) 3. Foie « obèse 6 mois » (x1000) 3. Liver « obese 6 months » (x1000) Foie obèse : clarification cytoplasmique des hépatocytes, surcharge lipidique importante, hypertrophie et altérations cellulaires, effacement du système vasculaire. Obese liver: cytoplasm clarification of the hepatocytes, important lipid overload, hypertrophy and cellular deteriorations, obliteration of the vascular system. 4. Foie : diabète ID (x400) 4. Liver; IDDM (x400) 5. Foie : diabète ID (x1000) 5. Liver: IDDM (x1000) Nombreuses dégénérescences et hypertrophies cellulaires, apparition de nécroses périvasculaires et périlobulaires, mais le système vasculaire est mieux respecté. Many cellular degenerations and hypertrophies; appearance of perivascular and perilobular necroses but the vascular system is not obliterated. Figure II histologie du foie sain, obèse et diabétique d’un Psammomys obesus adulte II-1 : Foie-adulte sain (x200) ; II-2 : Foie-obèse 6 mois (x400) ; II-3 : Foie-obèse 6 mois (x1000). Foie obèse : clarification cytoplasmique des hépatocytes, surcharge lipidique importante, hypertrophie et altérations cellulaires, effacement du système vasculaire. II-4 : diabète ID (x400) ; II-5 : diabète ID (x1000). Nombreuses dégénérescences et hypertrophies cellulaires, apparition de nécroses périvasculaires et périlobulaires mais le système vasculaire est mieux respecté. Histology of healthy, obese and diabetic liver of adult Psammomys obesus II-1: Adult healthy (x200); II-2: Obese 6 months (x400) II-3: Obese 6 months (x1000). Obese liver: cytoplasm clarification of the hepatocytes, important lipid overload, hypertrophy and cellular deteriorations, obliteration of the vascular system. II-4: ID diabetes (x400) ; II-5: ID diabetes (x1000). Many cellular degenerations and hypertrophies; appearance of perivascular and perilobular necroses but the vascular system is not obliterated. 312 Bulletin de la Société zoologique de France 133 (4) dégénérées (figures II-4,5). L’atteinte hépatique est généralisée et l’on observe de volumineuses vacuoles intra-cytoplasmiques qui refoulent le noyau en périphérie de la cellule : c’est la stéatose macrovacuolaire. De nombreux foyers de nécroses périvasculaires et périlobulaires apparaissent même si le système vasculaire reste mieux respecté que dans le foie des animaux obèses. 1. Glycogène T: déplétion ID: surcharge T: depletion ID: overload 2. Glycogène synthétase T: disparition ID: accentuation T: disappearing ID: emphasis 3. Naphtyl-estérase T: diminution ID: augmentation T: reduction ID: increase 4. Glycogène (T): Normal (RHC) 3 mois: augmentation 6 mois: disparition (ID) (T) Healthy (RHC) 3 months: increase 6 months: disappearing (ID) 4. Ribonucléoprotéine T: augmentation ID: réduction T: increase ID: reduction 5. Phosphatase acide (D) Diabétique : augmentation du nombre de lysosomes chez le diabétique (D) Diabetics: Increase among lysosomes number at the diabetics Figure III Comparaison de certaines activités enzymatiques du Psammomys sous régime hypocalorique (T) et en état d’insulinodépendance (ID). III-1 : Glycogène - T : déplétion ; D : surcharge. III-2 : Glycogène synthétase - (T) : disparition ; D : accentuation. III-3 : Naphtyl-estérase - (T) : diminution ; D : augmentation. III-4 : Ribonucléoprotéine - (T) : augmentation ; D : réduction. III-5 : Glycogène- (T) - normal ; RHC : 3mois : augmentation; 6 mois (ID) : disparition. III-6 : Phosphatase acide- Augmentation du nombre de lysosomes chez le diabétique. Comparison of some enzymatic activities of Psammomys under hypocaloric diet (T) and in Insulin Dependant state (ID). III-1: Glycogen - T: depletion; D: overload. III-2: Glycogen synthetase - (T): disappearing; D: emphasis. III-3: Naphtyl-esterase - (T): reduction; D: increase. III-4: Ribonucleoproteins - (T): increase; D: reduction. III-5: Glycogen - (T): healthy; RHC: 3 months: increase; 6 months (ID): disappearing. III-6: Acide phosphatase - Increase among lysosomes number at the diabetics. 313 Histoenzymologie du foie de Psammomys Transformations enzymatiques chez les Psammomys obesus diabétiques Les modifications enzymatiques observées sont typiques du SM. Les plus importantes concernent les enclaves métaboliques et notamment l’ARN, le glycogène, les lipides et leurs voies métaboliques. Au troisième mois du RHC les hépatocytes deviennent moins basophiles et l’activité de la glycogène-synthétase augmente : c’est l’enzyme de la glycogénèse qui, à partir de l’UD-glucose, aboutit à la forme linéaire du glycogène. Comme chez l’homme, une décroissance de l’insuline est associée à l’activation de l’expression du gène Glu-6-Pase (MAITRA et al., 2000) qui favorise la glycogénolyse et la néoglucogenèse (NORDLE et al., 1999) et qui se traduit par une augmentation considérable du glycogène hépatique (figure III-5). Pour les Psammomys devenus ID les remaniements observés suivent les profondes modifications enzymatiques consécutives au RHC de longue durée. Les hépatocytes présentent une déplétion glycogénique totale (figures III). La pyroninophilie ainsi que le taux de ribonucléoprotéides (ARN) diminuent considérablement, de même que la capacité de synthèse des protéines des hépatocytes (figure III-4). On note également une diminution de la glycuronidase lysosomiale, une accentuation du catabolisme anaérobie du glucose reflétée par la LDH et une accentuation de la lipolyse quand les cellules contiennent des lipides. Parallèlement on observe une hyperactivité de certaines enzymes lysosomiales telles que les phosphatases-acides et les sulfatases (figure III-6), qui s’explique par la tentative d’adaptation de l’animal pour contrer cette déplétion. Enfin, la glycogénose hépatique s’accompagne d’une stéatose (figure IV) et de nombreux foyers de nécrose envahissent le tissu hépatique. (N) Normal : absence de lipoïdose. (N) Healthy: disappearing of the lipoïdose. Figure IV Lipides neutres Neutral lipids (D) Diabétique : stéatose hépatique. (D) Diabetics: hepatosteatosis. 314 Bulletin de la Société zoologique de France 133 (4) Pour établir le statut métabolique de l’animal, l’estimation de l’activité de la cholinestérase est essentielle du fait de sa relation directe avec la sévérité du diabète (KUNEC-VAJIÆ et al., 1992 ; VALLE et al., 2006). Nos résultats montrent que l’activité de cette enzyme se corrèle parfaitement aux autres variables associées au SM tels que les TAG, le cholestérol HDL et LDL, l’apolipoprotéine E et la quantité d’insuline disponible. Chez l’être humain et de façon générale, une élévation même modérée des isoenzymes du foie est toujours le signe d’une maladie active du tissu hépatique. L’une des transaminases la plus communément utilisée pour évaluer les dommages subis par ce tissu est l’ALP du fait de sa grande sensibilité (DE AMACHER et al., 2002). Il en est de même de l’alanine aminotransferase (ALT), de l’aspartate aminotransferase (AST) et surtout du glutamate dehydrogenase (GLDH) qui révèle la présence de nécroses cellulaires ; c’est ce que l’on observe chez les Psammomys soumis au RHC. Discussion Le métabolisme glucidique du Psammomys se distingue par sa glycémie très basse (la moitié de celle du rat Wistar) et un taux d’insuline naturellement élevé. Cette particularité lui permet d’activer le processus de lipogenèse de novo et de limiter l’oxydation du glucose, fourni par la synthèse endogène, aux tissus insulinoindépendants. Le changement de régime alimentaire bouleverse très rapidement l’équilibre métabolique du Psammomys. Les AG à longue chaîne, substrats énergétiques des cellules β du pancréas, sont lipotoxiques à concentration chroniquement élevée (DE FRONZO, 2004) pour ces cellules comme le sont également des concentrations élevées de glucose (DONATH et al. ; MARSHAK et al., 1999). La part relative de la glucotoxicité et de la lipotoxicité dans la destruction des cellules β n’a pas été établie, mais ces deux mécanismes sont impliqués chez les diabétiques de type 2 (POITOUT & ROBERTSON, 2002). Comme chez l’homme, le DT-2 se manifeste par une éosinopénie, une neutrophilie, une croissance, légère de l’ALP et beaucoup plus forte de la GLDH. Cette dernière est considérée aujourd’hui comme le biomarqueur préférentiel des dommages hépatiques aigus chez les rats (O’BRIEN et al., 2002) comme chez l’homme, car sa libération en grande quantité dans le sang nécessite la rupture complète des cellules mitochondriales qui la renferme. De la même façon, l’apparition de la LDH (enzyme cytosolique ubiquitaire), dans le milieu intra- et extracellulaire est marque la présence de lyses cellulaires. Grâce à l’évaluation de son activité enzymatique au niveau du tissu hépatique, nous avons pu juger de la cytotoxicité du RHC sur notre animal modèle. En conclusion, Psammomys obesus modélise convenablement les altérations hépatiques rencontrées chez le patient diabétique. Il est à l’heure actuelle un excellent modèle polygénique pour l’étude du SM. Des études récentes, menées sur des Psammomys élevés dans des fermes laboratoires, soulignent l’intérêt de ce modèle pour la recherche des gènes à l’origine de l’obésité et du diabète (COLLIER et al., 2002) et pour l’étude des interactions multiples gène-gène et gène environnement qui influencent le développement dans le DT-2 (KAISER et al., 2005). 315 Histoenzymologie du foie de Psammomys 1. Faculté des Sciences Biologiques, LBPO/Nutrition et Métabolisme, USTHB, Alger. E.mail : [email protected] 2. Laboratoire de Physicochimie Théorique et de Chimie Informatique ; Faculté de Chimie, USTHB, Alger. 3. Department of Physiology; Texas Tech University Health Sciences Center; Lubbock, Texas. 4. Laboratoire d’Hormonologie, Centre Pierre et Marie Curie, C.H.U Mustapha, Alger. RÉFÉRENCES BANCROFT, J. & STEVENS, A. (1996).- Theory and Practise of Histological Techniques. Churchill Livingstone, New York (NY). CHALKLEY, S., HETTIARACHCHI, M., CHISHOLM, D. & KRAEGEN, E. (2002).- Long-term highfat feeding leads to severe insulin resistance but not diabetes in Wistar rats. Am. J. Physiol. Endocrinol. Metab., 282 (6), 1231-1238. CHEDIN, P., CAHEN-VARSAUZ, J. & BOYER, N. (1996).- Non-insulin-dependent diabetes mellitus developing during interferon-alpha therapy for chronic hepatitis. C. Ann. Intern. Med., 125 (6), 521. COLLIER, G., WALDER, K., DE SILVA, A., TENNE-BROWN, J., SANIGORSKI, A., SEGAL, D., KANTHAM, L. & AUGERT, G. (2002).- New Approaches to Gene Discovery with Animal Models of Obesity and Diabetes. Ann. N.Y. Acad. Sci., 967 (1), 403-413. DE AMACHER (2002).- A toxicologist’s guide to biomarkers of hepatic response. Human & Exp. Toxicol., 21, 253-262. DEFRONZO, R.A. & FERRANNINI, E. (1991).- Insulin resistance: a multifaceted syndrome responsible for NIDDM, obesity, hypertension, dyslipidemia, and atherosclerotic cardiovascular disease. Diabetes Care, 14, 173-194. DEFRONZO, R.A. (2004).- Dysfunctional fat cells, lipotoxicity and type 2 diabetes. Int. J. Clin. Pract., 143, 9-21. DONATH, M.Y., GROSS, D.J., CERASI, E. & KAISER, N. (1999).- Hyperglycemia-induced beta-cell apoptosis in pancreatic islets of Psammomys obesus during development of diabetes. Diabetes, 48 (4), 738-744. EL AOUFI, S., GENDRE, P., SENNOUNE, S., RIGOARD, P., MAIXENT J.-M. & GRIENE L. (2007).A high calorie diet induces type 2 diabetes in the deserts sand rat (Psammomys obesus). Cellular and Molecular BiologyTM, 53, 942-951. FERY, F. & PAQUOT, N. (2005).- Etiopathogenesis and pathophysiology of type 2 diabetes. Revue Médicale de Liège, 60, 5-6; 361-368. GABE, M. (1968).- Techniques Histologiques. Paris, Masson et Cie. GANTER, P. & JOLLES, G. (1970).- Histochimie Normale et Pathologique, vol. 2. Paris, GauthierVillars. KAHN, B. & FLIER, J. (2000).- Obesity and insulin resistance. J. Clin. Invest., 106 (4), 473-481. KAISER, N., NESHER, R., DONATH, M.Y., FRAENKEL, M., BEHAR, V., MAGNAN, C., KTORZA, A., CERASI, E. & LEIBOWITZ, G. (2005).- Psammomys Obesus, a Model for EnvironmentGene Interactions in Type 2 Diabetes. Diabetes, 54, 137-144. KALMAN, R., ZIV, E., SHAFRIR, E., BAR-ON, H. & PEREZ, R. (2001).- Psammomys obesus and the albino rat-two different models of nutritional insulin resistance, representing two different types of human populations. Laboratory Animals, 35 (4), 346-352. KUNEC-VAJIÆ, E., BERNAT, N. & MIHOKOVIÆ, N. (1992).- Effect of hypolipidemic drugs on cholinesterase activity in the rat. General Pharmacology, 2 (23), 217-219. 316 Bulletin de la Société zoologique de France 133 (4) LEHOTSKY, J., KAPLÁN, P., RA AY, P., MÉZE OVÁ, V. & RAEYMAEKERS, L. (1999).Distribution of plasma membrane Ca2+ pump (PMCA) isoforms in the gerbil brain: effect of ischemia-reperfusion injury. Neurochem. Int., 35 (3), 221-227. LEVINTHAL, G.N. & TAVILL, A.S. (1999).- Liver Disease and Diabetes Mellitus. Clin. Diabetes, 17 (2), 73-93. MAITRA, S., WANG, S., EL-MAGHRABI, R. & HENRY, M.C. (2000).- Regulation of Liver and Kidney Glucose-6-phosphatase Gene Expression in Hemorrhage and Resuscitation. Acad. Emerg. Med., 7 (7), 731-738. MARSHAK, S., LEIBOWITZ, G., BERTUZZI, F., SOCCI, C., KAISER, N., GROSS, D.J., CERASI, E. & MELLOUL, D. (1999).- Impaired beta-cell functions induced by chronic exposure of cultured human pancreatic islets to high glucose. Diabetes, 48 (6), 1230-1236. McMANUS, J. (1961).- General Cytochemical Methods, J.F. Danielli (Ed), Academic Press (NY). MEXICO 2000: 17th International diabetes federation congress; november 6, 2000; Mexico City. MILLER R.B. & KARN R.C. (1980).- A rapid spectrophotometric method for the determination of esterase activity. J. Biochem. Biophys. Methods, 1980, 3 (6), 345-354. NAGATA, E., TANAKA, K., SUZUKI, S., DEMBO, T., FUKUUCHI, Y., FUTATSUGI, A. & MIKOSHIBA, K. (1999). Selective inhibition of inositol 1,4,5-triphosphate-induced Ca2+ release in the CA1 region of the hippocampus in the ischemic gerbil. Neuroscience, 93 (3), 995-1001. NORDLIE, R.C., FOSTER, J.D. & LANGE, A.J. (1999).- Regulation of glucose production by the liver. Annu. Rev. Nutr., 19, 79-406. O’BRIEN, P.J., SLAUGHTER, M.R., POLLEY, S.R. & KRAMER, K. (2002).- Advantages of glutamate dehydrogenase as a blood biomarker of acute hepatic injury in rats. Lab. Anim., 36 (3), 313-321. PEARSE, A.G.E. (1980).- Histochemistry, theoretical and applied. Vols 1 & 2. 4th edition (Churchill Livingstone). PHILLIS, J.W., ESTEVEZ, A.Y. GUYOT, L. & O’REGAN, H. (1999).- 5-(N-Ethyl-N-isopropyl)-amiloride, an Na+-H+ exchange inhibitor, protects gerbil hippocampal neurons from ischemic injury. Brain Res., 21, 839 (1), 199-202. POITOUT, V. & ROBERTSON, R.P. (2002).- Secondary β-cell failure in type 2 diabetes; a convergence of glucotoxicity and lipotoxicity. Endocrinology, 143, 339-342. SENNOUNE, S., GERBI, A., DURAN, M.-J., BENKOËL, L., PIERRE, S., LAMBERT, R., DODERO, F., CHAMLIAN, A., VAGUE, P. & MAIXENT, J.-M. (1999).- A Quantitative Immunocytochemical Study of Na+,K+-ATPase in Rat Hepatocytes After STZ-induced Diabetes and Dietary Fish Oil Supplementation. J. Histochem. Cytochem., 47, 809-816. SOHMER, H., PEREZ, R., SICHEL, J.-Y., PRINER, R. & FREEMAN, S. (2001).- The Pathway Enabling External Sounds to Reach and Excite the Fetal Inner Ear. Audiology & Neuro-Otology, 6, 109-116. STRATTON, I., ADLER, A., NEIL, A., MATTHEWS, D., MANLEY, S., CULL, C., HADDEN, D., TURNER, R. & HOLMAN, R. (2000).- Association of glycaemia with macro- and microvascular complications of type 2 diabetes (UKPDS 35). Br. Med. J., 321, 405-412. TUCCI, D.L., CANT, N.B. & DURHAM, D. (1999).- Conductive hearing loss results in a decrease in central auditory system activity in the young gerbil. Laryngoscope, 109 (9), 1359-1371. VALLE, A., O’CONNOR, T., TAYLOR, P., ZHU, G., MONTGOMERY, W., SLAGBOOM, E., MARTIN, G. & WHITFIELD, B. (2006).- Butyrylcholinesterase: association with the Metabolic Syndrome and Identification of 2 Gene Loci Affecting Activity. Clinical Chemistry, 52, 1014-1020. VAN NOORDEN, F. & JONGES, G. (1995).- Heterogeneity of kinetic parameters of enzymes in situ in rat liver lobules. Histochemistry and Cell Biology, 103 (2), 93-101. WENBIN, S., KOICHIRO, Y., AKIRA, T., AKIHIRO, H., MIHOKO, T., KOICHIRO, N., HEYING, Z., REI, N., HIDEYA, F., DAI, S., HIROYUKI, U., HIROKI, I., KENTARO, T., YUICHIRO, Y. & TAKESHI, K. (2002).- Effect of High Dietary Fat on Insulin Secretion in Genetically Diabetic Goto-Kakizaki Rats. Pancreas, 25 (4), 393-399. (reçu le 31/11/07 ; accepté le 13/07/08)