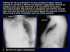
APPAREIL RESPIRATOIRE – Pneumothorax et Pleurésie 30/10/13
Transcription
APPAREIL RESPIRATOIRE – Pneumothorax et Pleurésie 30/10/13
APPAREIL RESPIRATOIRE – Pneumothorax et Pleurésie 30/10/13 BAQUE Eugénie L3 Pr Philippe Astoul Appareil respiratoire 8 pages Pneumothorax et pleurésie Plan A. Pleurésie I. Anatomie pleurale II. Fonctions de la plèvre III. Circonstances de la pleurésie B. Pneumothorax I. Physiopathologie du pneumothorax II. Circonstance de la consultation Il existe un site du collège des enseignants de pneumologie, ce site fait référence nationalement pour tout ce qui concerne la pneumo. Il est très utile pour l'ECN donc à retenir ! A. Pleurésie : La pleurésie est une accumulation de liquide dans la cavité pleurale. C'est un motif de consultation très fréquent. A l'inverse, le pneumothorax est une accumulation d'air. Objectifs pédagogiques : 1. Connaître les éléments du diagnostic positif et du diagnostic différentiel d'un épanchement pleural liquidien. 2. Savoir proposer une orientation étiologique tenant compte des données épidémiologiques essentielles, des signes cliniques associés et des résultats de l'analyse de la ponction pleurale. 3. Savoir argumenter la conduite à tenir vis-à-vis d'un exsudat qui ne fait pas la preuve de son étiologie. 4. Connaître la distinction entre épanchements parapneumoniques (compliqué ou non) I. Anatomie pleurale : La plèvre est composée de deux membranes : – plèvre viscérale : enveloppe la surface externe du poumon – plèvre pariétale : couvre la surface interne de la paroi thoracique, du médiastin, du diaphragme. 1/8 APPAREIL RESPIRATOIRE – Pneumothorax et Pleurésie L'espace pleural est VIRTUEL, et contient une faible quantité de liquide (plus ou moins 3mL/Kg). Les feuillets pleuraux sont formés par le mésothélium (monocouche de cellules mésothéliales). Ces cellules ne sont pas figées : on peut retrouver des cellules de type 1 (au repos), de type 2 (en activité, répondant à une inflammation par ex... ). Les cellules de type 3 sont en dégénérescence (apoptose). Les cellules sont accolées entre elles grâce à des desmosomes, ainsi que des zonula adherens. Ces régions ont des rôles très important dans les échanges d'eau dans la cavité pleurale. Il y a présence de graisse dans la couche sous-mésothéliale, avec dans un plan profond le fascia endothoracique. (attention à bien faire la différence entre le mésothélium et le mésothéliome qui est un cancer de la plèvre lié à l'exposition à l'amiante). II. Fonctions de la plèvre : La plèvre : – permet le glissement du poumon sur la paroi thoracique : le poumon a tendance à se rétracter (=se collaber) alors que la cage thoracique elle s'expand : création d'une pression négative dans le poumon. – filtration pleurale : assure les échanges. Il y a fabrication de liquide par la plèvre. – drainage pleural : transmésothélial et lymphatique. – est un système qui rend solidaire poumon et paroi thoracique : il y a un mouvement élastique vers l'extérieur de la paroi thoracique et un autre vers l'intérieur du poumon. Ces mouvements sont dû à une pression pleurale négative qui est proportionnelle à la pression développée dans le poumon. En fin d’expiration, les forces élastiques du thorax et du poumon s’équilibrent et la pression pleurale est de -2 à -5 cm H2O. 2/8 APPAREIL RESPIRATOIRE – Pneumothorax et Pleurésie Le liquide de la cavité pleurale est secrété de manière continue par la plèvre principalement par filtration au niveau des micro-vaisseaux de la plèvre pariétale. 3 théories du Liquide pleural : (non détaillé en cours) • Première théorie du « turnover » (1894) Cette théorie est basée sur la loi de Starling : les échanges des fluides et des soluté à travers une membrane semi-perméable dépend de l 'équilibre entre les pressions hydrostatique et oncotique de chaque côté de cette membrane. Jv = kf[(P1 – P2) – σ(π1 - π2)] Avec : Jv: Flux de liquide entre les compartiments 1 et 2 kf : coefficient de filtration P : pression hydrostatique π : pression oncotique σ : coefficient de reflection pour les protéines • Deuxième théorie du turnover : Neergard (1927) et Agostini (1957) appliquent la loi de Starling. La filtration pleurale est assurée par la plèvre pariétale, et l'absorption par la viscérale. Mais ce modèle pose deux problèmes majeurs : – l'augmentation progressive de la concentration en protéines du liquide pleural (en rapport avec la différence de perméabilité pour les liquides et les solutés) – les capacités d'absorption limitées de la plèvre viscérale (son épaisseur, sa vascularisation systémique) Ce modèle prend en considération les lymphatiques de la plèvre pariétale dans les mécanismes de filtration des liquides et des solutés. • Théorie actuelle : fin 80 – début 90 ♦ Production du liquide : filtration capillaire (loi de Starling), plèvre pariétale essentiellement ♦ Absorption : drainage lymphatique, par les lymphatiques de la plèvre pariétale qui s'ouvrent directement dans la cavité pleurale. Cette théorie montre le rôle des pores lymphatiques dans les région de la plèvre médiastinale, diaphragmatique... 3/8 APPAREIL RESPIRATOIRE – Pneumothorax et Pleurésie Il y a 2 différences entre les deux plèvres : – la plèvre viscérale est 20 à 100 fois plus épaisse que la pariétale – les lymphatiques du poumon n'ont aucune connexion avec la cavité pleurale et la plèvre viscérale, à l'inverse des lymphatique de la pariétale. La pariétale peut donc drainer du liquide pleural lorsque les capacités d'absorption des lymphatiques du poumon sont dépassées. Le liquide fuit alors dans le tissus interstitiel puis dans la cavité pleurale. L’œdème aigu du poumon entraîne donc une pleurésie, qui s'épanche généralement d'abord vers la droite, car il y a plus de place. (surface pleurale droite plus grande que la gauche à cause de la présence du cœur) En étudiant la plèvre de lapin, on a trouvé des pores au niveau pariétal, qui sont les ouvertures des lymphatiques pariétaux. Ils sont situés à des endroits spéciaux, et sont bourrés de lymphocytes, macrophages... Ils sont appelés « Pore de Wang ». La vitesse du flux lymphatique dépend de l'amplitude des mouvements du diaphragme, d'où l'importance de la kinésithérapie. III. Circonstances de la pleurésie : Une pleurésie apparaît lorsqu'il y a un problème de régulation du volume du liquide pleural. Cette régulation met en jeu la perméabilité basse de la plèvre pariétale (mésothélium), et celle encore plus basse de la plèvre viscérale (10 à 20% de l'absorption pleurale). Un épanchement pleural va apparaître avec une : – Diminution du débit, ou limitation de l'augmentation du débit lymphatique. Il y a donc un dépassement des capacités d'absorption lymphatique, dont le débit ne répond pas à la demande. La résolution de l'épanchement ne peut se faire qu'avec un retour à la normale de la perméabilité vasculaire. (Il s'agit d'un œdème aigu du poumon) – Augmentation du rapport filtration / drainage du liquide : par augmentation de la pression capillaire systémique et augmentation de la perméabilité microvasculaire (lors d'une réaction inflammatoire de la plèvre pariétale). (Il s'agit d'une inflammation) EXSUDAT : augmentation de concentration en protéines résultant d'une augmentation de la perméabilité vasculaire (inflammation). Il y a dépassement des capacités d'absorption par augmentation du liquide (rare) ou occlusion des pores lymphatiques (le + souvent). TRANSSUDAT : augmentation de la conductance à l'eau des voies paracellulaire (retenue de protéines plasmatiques reste élevée) ou augmentation des pressions veineuses pulmonaires. Ceci traduit un désordre d'ordre mécanique (œdème aigu du poumon). Rq : • • • L’œdème pulmonaire en tant que tel n’entraîne pas nécessairement un épanchement pleural parce que l'augmentation de la pression interstitielle pulmonaire génère à peine un gradient suffisamment important pour entraîner une filtration liquidienne au travers de la plèvre viscérale. Un épanchement pleural est rarement identifié dans l'insuffisance cardiaque droite. Insuffisance cardiaque gauche : l'augmentation de la pression capillaire et interstitielle, ainsi que l'augmentation de la perfusion capillaire et des perméabilités membranaire sont des facteurs multiplicatifs qui modifient l'équilibre de Starling. Les lymphatiques ne peuvent compenser. L'ICG entraîne donc fréquemment une pleurésie. 4/8 APPAREIL RESPIRATOIRE – Pneumothorax et Pleurésie a. La consultation : Généralement suite à une anomalie radiologique isolée. Ou alors suite à des Plaintes : – signes fonctionnels : toux sèche et douloureuse, apparaît aux changement de position du patient (car le liquide se répartit) , dyspnée, douleur thoracique. – signes généraux : fièvre, asthénie... a noter que le poumon, à l'inverse de la plèvre, ne contient pas de terminaison nerveuse, il n'est donc pas douloureux d'où le stade avancé des cancers lorsqu'ils sont identifiés. Dyspnée : sa rapidité d'installation et son intensité dépend du terrain sur lequel survient l'épanchement, de son abondance, de son étiologie. (la dyspnée est une sensation subjective) Douleur : latéro-thoracique, irradie l'épaule et le dos. Son intensité est variable, respiro-dépendante, exacerbée par la respiration et la toux et quelquefois augmentée par une pression pariétale. Toux : sèche, et apparaît aux changements de positions. Examen physique : Syndrome pleural : matité à la percussion abolition du murmure vésiculaire abolition de la transmission des vibrations vocales Ces signes sont évocateurs mais non spécifiques. De plus, lors d'une pleurésie, l'examen physique est le plus souvent normal si l'épanchement est de moins de 500mL. Interrogatoire : – analyse de la plainte – signes d'accompagnement : – généraux : index d'activité, amaigrissement – fonctionnels : appareil par appareil – antécédents : – personnels : mode de vie, tabac, professions (actuelle et antérieure), ATCD médicaux et chirurgicaux, co-morbidité, traitements en cours, vaccins... – familiaux : asthme, allergie, maladies infectieuses, cancers... b. Examen clinique : inspection – palpation – percutions - auscultation – physique : syndrome pleural – examen complet +++ – – Radio : physiologiquement, la poche à air gastrique (tubérosité de l'estomac) est visible. Entre son extrémité supérieure et le diaphragme il y a 1,5 cm. Si cette distance est modifiée, c'est un signe pathologique. Scanner thoracique : explore médiastin, on visualise le liquide. La courbe de Damoiseau délimite le bord supérieur de l'épanchement. Elle est concave vers le haut, ce qui signifie qu'il n'y a pas de brides : cavité pleurale libre. S'il y présence de brides : l'épanchement pleural est cloisonné (ou enkysté). Il y a un accolement de la plèvre viscérale avec la paroi, par exemple suite à une ancienne infection pulmonaire qui a entraîné une petite fibrose à l'origine de l'accolement. 5/8 APPAREIL RESPIRATOIRE – Pneumothorax et Pleurésie Le signe de la silhouette renseigne la topographie de l'anomalie : celle-ci n'efface pas le cœur, elle est donc en arrière. Une fois la pleurésie confirmée par la radio, on doit connaître le mécanisme. Il faut donc recueillir du liquide grâce à une ponction pleurale. On utilise une aiguille en 3 parties, avec un premier mandrin pointu pour perforer la peau. Il faut faire attention lors de la ponction, car la cavité pleurale descend très bas dans la cavité abdominale, et a une projection sur la rate et le foie. Il faut donc la faire dans l'espace intercostal, en s'appuyant sur la côte du dessous pour éviter le paquet nerveux. On ausculte le patient et on ponctionne là où on entend la matité. c. Distinction exsudat/transsudat : 3 types d'analyses : 1. analyse biochimique : on va doser les protides au niveau de la plèvre de façon à faire le rapport sur les protides sanguins. On dose aussi les LDH (LacticoDHase). 2. analyse cytologique : présence de cellules anormales ? Cancéreuses ? Quelle est la population de cellules (mésothéliale, PN, lymphocyte...) ? 3. Analyse microbiologique : recherche de germes. A la suite des analyses, on peut se retrouver dans deux cas : – Soit l'échantillon présente peu de protides (< 20 g/l) et LDH < 200 => il s'agit d'un transsudat. Si le rapport Protéine pleurale/Protéine sanguine <0,5, les causes sont mécaniques (insuffisance cardiaque gauche, cirrhose, anomalies rénale, atélectasie) – Soit il y a beaucoup de protéines et la LDH est élevée, avec une cellularité importante => il s'agit d'un exsudat, dans le cadre d'un processus inflammatoire. Efficacité:93%, Sensibilité 98% et spécificité 83% En présence d'un exsudat, on doit se demander s'il s'agit d'un cancer (1ere cause de pleurésie). Dans ce cas on donne priorité à l'analyse histologique. On réalise alors une biopsie pleurale, soit à l'aveugle par voie transcutanée (on fait une ponction, et en se retirant on « arrache » un petit bout de plèvre), soit lors d'une thoracoscopie. Le problème de la voie trans-cutanée est que le rendement n'est pas bon, on peut faire le prélèvement entre les nodules et rater le cancer sans oublier qu'il y a un risque de toucher un vaisceau. On préfère réaliser la biopsie lors d'une thoracoscopie. On pose ensuite un drain qui permet au poumon de se réexpandre. B. Pneumothorax : C'est un épanchement aérique dans la cavité pleurale, lié à une lésion à la surface du poumon. La plupart du temps, les pneumothorax sont spontanés et idiopathiques (= sans cause trouvée). En microscopie : – PNO sans lésion visible de la plèvre viscérale – microscopie électronique : disparition de cellules mésothéliales de la plèvre viscérale, avec anomalie d'accolement des cellules (élastofibrosis) qui crée des pores – Macroscopiquement, il y a présence de bulles et de bleps (hernie de la plèvre viscérale sans connexion avec le réseau aérien, à la différence de la bulle). La rupture des bulles ou des bleps entraîne un fuite aérienne du poumon vers la cavité pleurale. 6/8 APPAREIL RESPIRATOIRE – Pneumothorax et Pleurésie I. Physiopathologie du pneumothorax : – – – – – Plèvre viscérale poreuse +++ L'inflammation des petites voies aériennes (tabac) génère ds lésions et une physiopathologie du PNO. Nécrose du parenchyme, dût à des fistules bronchopleurales infectieuses (tuberculose...) ou non. Un mécanisme de valve, une augmentation de gradient de pression, ou une diminution de la qualité du tissus conjonctif entraîne alors une fuite au niveau de la plèvre viscérale. Rarement dût à des bulles pseudo-amphysémateuse ou à une rupture alvéolaire II. Circonstances de la consultation : C'est rarement dans le cadre d'anomalie radiologique isolée. a. Plainte : – signe fonctionnels : douleur thoracique +++ « coup de couteaux dans le thorax », dyspnée, toux rare – signes généraux : fièvre, asthénie... Plutôt rare. Douleur thoracique : latéro-thoracique, irradie l'épaule et le dos. Son intensité est variable, elle est aggravé par les mouvements respiratoire. Elle survient presque toujours au repos, et s'estompe souvent rapidement. Dyspnée : rapidité d'installation et intensité dépendent du terrain. S'atténue souvent spontanément. Examen physique : tympanisme à la percussion abolition du MV abolition de la transmission des VV Hémithorax normal ou distendu et moins mobile Ce sont des signes évocateurs mais non spécifiques. Le pneumothorax minime est de diagnostic difficile, l'imagerie est indispensable. On demande un radiographie thoracique, on recherche une ligne bordante et on voit le décollement du poumon. L'interrogatoire et l'examen clinique sont les même que ceux de la pleurésie Pneumothorax suffocant : décollement complet, avec brides pleurales. Cette bride est sous tension, il y a un risque de rupture et d'hémorragie =hémopneumothorax. Le médiastin et compressé et dévié (on parle de déplacement médiastinal), donc il y a un risque majeur de trouble cardiaque. La pression est positive dans la cavité (on a donc juste à faire un trou pour que l'air s’échappe). b. Évaluation du risque de récidive (RR) : RR après repos, oxygénothérapie ou drainage : 16-54% RR dépend du : – moment : risque maximum dans les 2 ans – patient : F<H : dût au morphotype longiligne ( grande taille ) – tabagisme (identifier clairement dans le risque de 1er épisode mais pas vraiment identifié comme facteur de récidive) – importantes variations de la pression atmosphérique RR indépendant de l'âge ou de la taille du PNO. RR indépendant du traitement en l'absence de symphyse, et de la présence de bulles. 7/8 APPAREIL RESPIRATOIRE – Pneumothorax et Pleurésie Tant qu'on n'a pas collé la plèvre, le risque de récidive est de 30% dans l'année qui suit. Faut-il administrer de l'oxygène ? – le taux de ré-expansion spontané du PNO est de 1%/j – l'administration de l'O2 peut multiplier par 4 la vitesse de résorption de l'air ds la cavité pleurale. – O2 : augmentation gradient en pression entre l'espace pleural et les capillaires sous pleuraux => accélère l'absorption d'air. – Le débit doit être élevé pour que l'O2 fonctionne (˃10L/min) (mais la mise en pratique est difficile car très désagréable) Cas clinique : • M. Pierre..., 27 ans, informaticien, sportif. Il est grand et maigre. Il consulte aux urgence pour dyspnée et douleur thoracique. Aucun ATCD. Tabagisme important. La douleur est survenue le matin même, au moment du petit déjeuner : AU REPOS => caractéristique. Douleur basi-thoracique, lui coupait le souffle, quand il inspirait à fond ou qu'il toussait. Maintenant il ne persiste qu'une gène à droite. Premier cas de figure : - auscultation : discrète diminution du MV à droite et le cliché montre un très léger décollement. - conduite moderne : on garde en observation quelques heures, et on le fait sortir si ces conditions de vie le permettent, avec de l'O2, et si le patient montre un bonne tolérance clinique. Si son PNO s'aggrave : Ce patient présente des facteurs de risque : son âge (sujet jeune : 27 ans), son morphotype longiligne, son tabagisme. On arrive dans le deuxième cas de figure : On retrouve un tympanisme et abolition du MV. Le cliché montre un décollement sur toute la hauteur de la ligne axillaire : il faut absolument évacuer l'air. On procède soit à une exsufflation (aiguille raccordée à une seringue), soit à un drainage par un petit cathéter de petit calibre lié à une valve ou à un « pleurévac ». Un pneumothorax apparaît généralement au repos, En France, on agit sur le pneumothorax si il est symptomatique. Recommandations : – sevrage tabagique – le repos ou les limitations des activités physiques ne sont plus recommandés devoir d'information : on explique au patient le risque de récidive de 30%. 3 mois plus tard, le patient revient avec un tableau identique au 2e cas de figure. On propose donc au patient une pleurodèse : il s'agit de d’accoler les deux feuillets de la plèvre. Pour cela on irrite la plèvre de façon à créer une bride inflammatoire, ou alors on fait un talcage (pulvérisation de talc). On fait cette pleurodèse car après un 2e épisode de PNO => risque de récidive de 64% 8/8