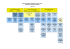
The Cardiac Conduction System
Transcription
The Cardiac Conduction System
Basic Science for Clinicians The Cardiac Conduction System David S. Park, MD, PhD; Glenn I. Fishman, MD T Downloaded from http://circ.ahajournals.org/ by guest on September 30, 2016 currents that include, but are not limited to, background sodiumsensitive current (Ib Na), L- and T-type calcium currents (ICa,L, ICa,T), sustained inward (Ist) current, and hyperpolarization-activated current (If) (Figure 2).27,31–33 The subsarcolemmal calcium clock contributes to SAN diastolic depolarization through the spontaneous, rhythmic release of Ca2⫹ from the sarcoplasmic reticulum (SR) via the ryanodine type 2 receptor (RYR2).34 The local intracellular calcium (Cai) elevations drive the sodium-calcium exchange current (INCX) to substitute 1 intracellular Ca2⫹ for 3 extracellular Na⫹. The net gain in positive charge results in membrane depolarization.35 The elevation of intracellular Ca2⫹ occurs in the latter third of diastolic depolarization and is sensitive to -adrenergic stimulation.36 Human mutations affecting the voltage clock (SCN5A and HCN4), calcium clock (RYR2 and CASQ2), or both mechanisms (ANKB) have been identified that negatively affect sinus node function.37,38 he human heart beats 2.5 billion times during a normal lifespan, a feat accomplished by cells of the cardiac conduction system (CCS). The functional components of the CCS can be broadly divided into the impulse-generating nodes and the impulse-propagating His-Purkinje system. Human diseases of the conduction system have been identified that alter impulse generation, impulse propagation, or both. CCS dysfunction is primarily due to acquired conditions such as myocardial ischemia/infarct, age-related degeneration, procedural complications, and drug toxicity. Inherited forms of CCS disease are rare, but each new mutation provides invaluable insight into the molecular mechanisms governing CCS development and function. Applying a multidisciplinary approach, which includes human genetic screening, biophysical analysis, and transgenic mouse technology, has yielded a broad array of gene families involved in maintaining normal CCS physiology (Figure 1). In this review, we discuss gene families that have been implicated in human CCS diseases of rhythm, conduction block, accessory conduction, and development (Table). We also investigate evolving therapeutic strategies that may serve as adjuvant or replacement therapy to current implantable pacemakers. SCN5A SCN5A encodes the cardiac sodium channel (Nav1.5), which generates the fast sodium current, INa. Nav1.5 dictates the amplitude and slope of phase 0 of the cardiac action potential and therefore affects conduction velocity. More than 200 mutations have now been identified in SCN5A that cause a collection of cardiac diseases that include long QT3, Brugada syndrome, progressive cardiac conduction defect, and congenital sick sinus syndrome (SSS). To date, 14 SCN5A mutations have been linked to inherited forms of SSS.27,39 Benson et al1 identified 6 SCN5A mutations in 3 kindreds with inherited SSS. The probands exhibited compound heterozygosity of the 6 SCN5A alleles (G1408R⫹P1298L, T220I⫹R1623X, delF1617⫹R1632H). Biophysical evaluation revealed that 2 of the 6 mutations resulted in nonfunctional channels while T220I, P1298L, and delF1617 demonstrated reduced INa current density and a hyperpolarizing shift in voltage-dependent inactivation. Smits et al40 identified a novel SCN5A mutation, E161K, in two kindreds with symptomatic sinus node dysfunction, generalized conduction disease, and Brugada syndrome. Whole-cell patch clamp revealed a 3-fold reduction in INa current density and a positive shift in voltage-dependent activation. Both a negative shift in voltage-dependent inactivation and a positive shift in voltagedependent activation result in narrowing of the INa current window. Diseases of Automaticity The human sinoatrial node (SAN) is a crescent-shaped, intramural structure with its head located subepicardially at the junction of the right atrium and the superior vena cava and its tail extending 10 to 20 mm along the crista terminalis.26 The SAN has complex 3-dimensional tissue architecture with central and peripheral components made up of distinct ion channel and gap junction expression profiles.27 Central and peripheral cells have different action potential characteristics and conduction properties (Figure 2).27 Experimental and computational models have demonstrated that SAN heterogeneity is necessary to maintain normal automaticity and impulse conduction.28 –30 Pacemaker automaticity is due to spontaneous diastolic depolarization of phase 4, which depolarizes the membrane to threshold potential generating rhythmic action potentials. The current paradigm of SAN automaticity has been modeled as 2 clocks that function in concert, the “membrane voltage clock” and the “calcium clock.” The membrane voltage clock is produced by the net disequilibrium between the decay of outward potassium currents (IK) and the activation of inward From the Leon H. Charney Division of Cardiology, New York University School of Medicine, New York, NY. Correspondence to Glenn I. Fishman, MD, Leon H. Charney Division of Cardiology, New York University School of Medicine, 522 First Ave, Smilow 801, New York, NY 10016. E-mail [email protected] (Circulation. 2011;123:904-915.) © 2011 American Heart Association, Inc. Circulation is available at http://circ.ahajournals.org DOI: 10.1161/CIRCULATIONAHA.110.942284 904 Park and Fishman Conduction System Disease 905 Figure 1. Cardiac conduction system cell. Genes identified in human cardiac conduction system disease are highlighted. Downloaded from http://circ.ahajournals.org/ by guest on September 30, 2016 The expression of SCN5A is restricted to the peripheral SAN and absent in the central SAN, the site of dominant pacemaking (Figure 2). A proposed mechanism of how peripherally expressed SCN5A mutations affect central SAN automaticity was computer simulated by Butters et al.41 SCN5A mutants (T220I, P1298L, delF1617, and E161K) were incorporated into single cell models and into a 2-D model of intact, rabbit SAN-atrium. Single cell simulations showed that SCN5A mutants reduced the pacemaking rate of peripheral cells with little impact on central nodal cells. In contrast, intact tissue simulations with the SCN5A mutants slowed the sinus rate within the central SAN. The atrium imposes a significant hyperpolarizing load on the SAN, which is counterbalanced by SCN5A expression in peripheral cells.41– 43 Therefore, reduced INa in the peripheral SAN exposes the central SAN to more hyperpolarized potentials, slowing pacemaking rate. In addition, impaired action potential conduction was evident across the SAN-atrium predisposing to sinus exit block, a common feature of familial SSS.41 HCN4 The pacemaker, or funny current, If, is generated by the hyperpolarization-activated cyclic nucleotide-gated (HCN) channel. The term funny current stems from the unique characteristics of HCN channels, which include permeability to K⫹ and Na⫹, activation at hyperpolarized membrane potentials, and modulation by cAMP. The biophysical properties of HCN channels make them ideally suited to function as modulators of the pacemaker potential. First, because they are activated at hyperpolarized membrane potentials (between ⫺65 and ⫺40 mV), their slow inward current contributes to diastolic depolarization; second, the main cardiac HCN channel (HCN4) is cAMP responsive, allowing If to be modulated by autonomic stimulation.44,45 Mutations in HCN4, the predominant isoform in the SAN, have been identified in patients with SSS.32,45 Using candidate gene strategies, Schulze-Bahr et al12 identified a single nucleotide deletion in HCN4 (1631delC) in a patient with sinus bradycardia and chronotropic incompetence. The 1631delC mutant lacks the cyclic-nucleotide binding domain, making it unresponsive to cAMP. Additional HCN4 mutations were identified in 2 families with asymptomatic sinus bradycardia. The 2 missense mutations, S672R and G480R, resulted in channels that activate at more hyperpolarized voltages generating smaller currents during diastolic depolarization.13,14 Investigations into animal models of HCN channel deficiency have shed light on their role in If current generation. HCN4 knockout mice were embryonic lethal at E10.5 to E11.5 and demonstrated a cardiomyocyte maturation defect. HCN4⫺/⫺ embryonic cardiomyocytes exhibited an 85% reduction in If and were chronotropically unresponsive to cAMP.46,47 To study the loss of HCN4 expression in adult mice, tamoxifen-inducible mouse models were generated.48,49 The loss of HCN4 in SAN cells resulted in a 75% reduction in If current density. Instead of manifesting sinus bradycardia, these mice developed sinus pauses up to 300 to 500 ms. Chronotropy was also preserved. HCN4⫺/⫺ SAN cells exhibited normal automaticity; however, diastolic potentials tended to drift to hyperpolarized levels at which spontaneous pacemaker activity would cease. Taken together, these results suggest that HCN4 is indispensible for SAN development and chronotropy during embryogenesis but may play only a backup role to counter membrane hyperpolarization in the adult SAN.47– 49 These results are consistent with the benign bradycardic phenotype seen in the 2 families with HCN4 mutations reported by Milanesi et al13 and Nof et al.14 The preservation of chronotropic competence in human and experimental models of HCN4 deficiency is suggestive of alternative mechanisms of SAN automaticity and sympathetic responsiveness. The first implication of Cai in diastolic depolarization was reported by Rubenstein and Lipsius50 when ryanodine treatment was found to slow automaticity in subsidiary pacemakers in cat right atria. A mechanistic link between Cai and SAN diastolic depolarization was subsequently reported by Huser et al,34 who proposed that subsarcolemmal Ca2⫹ transients released from the SR (ie, Ca2⫹ sparks) lead to activation of the Na⫹-Ca2⫹ exchanger (NCX), resulting in membrane depolarization. Bogdanov et al35 confirmed this mechanism in isolated rabbit SAN cells and directly linked Ca2⫹ sparks to late diastolic depolarization via the NCX. Vinogradova et al36,51 then showed that -adrenergic augmentation of rabbit SAN chronotropy is dependent on SR Ca2⫹ release as treatment with ryanodine blunted the pacemaker rate response to isoproterenol. Recent work by Joung et al38 examined the effect of adrenergic stimulation on intact canine SAN preparations using dual optical mapping of transmembrane potential (Vm) and Cai. Adrenergic stimulation resulted in a robust increase and superior shift in late 906 Table. Circulation March 1, 2011 Genetic Basis of Conduction System Disease Gene Name Protein Associated Condition Conduction Defect Mechanism Reduced cardiac excitability and slowed conduction; loss of depolarizing current in peripheral sinoatrial node cells References Ion channels SCN5A Nav1.5 Brugada syndrome, long QT syndrome 3 Sick sinus syndrome, progressive cardiac conduction defect, atrial standstill, atrioventricular block, bundle branch block 1–8 SCN1B Scn1b Brugada syndrome Progressive cardiac conduction defect KCNJ2 Kir2.1 Andersen-Tawil syndrome Atrioventricular block, bundle branch block Prolongation of action potential duration and reduced cardiac excitability 10, 11 HCN4 HCN4 Sinus bradycardia Reduction in pacemaker current (If) 12–14 Altered Ca2⫹ handling likely affecting the Ca2⫹ clock 15, 16 9 Ca2⫹ handling proteins Downloaded from http://circ.ahajournals.org/ by guest on September 30, 2016 RYR2 Ryr2 CPVT Sinus node dysfunction, atrioventricular block, atrial standstill CASQ2 Calsequestrin CPVT Sinus bradycardia 17 Gap junction proteins GJA5 Cx40 Atrial standstill Impaired myocyte coupling resulting in slowed conduction 3 Sinus bradycardia, atrioventricular block, bundle-branch block Specification defect of the atrioventricular node and the ventricular cardiac conduction system 18 Transcription factors TBX5 NKX2-5 Tbx5 Holt-Oram syndrome Nkx2-5 Atrioventricular block, bundle-branch block 19 Nuclear membrane proteins LMNA Lamin A/C Emery-Dreifuss muscular dystrophy Atrioventricular block Altered nuclear stress mechanics and hyperactivation of MAPK signaling 20 Sinus bradycardia and heart rate variability Altered ion channel and transporter expression and trafficking 21 WPW, atrioventricular block Altered ventricular myocyte energetics leading to glycogen-engorged vacuoles and disruption of annulus fibrosus 22, 23 WPW Maturation defects of annulus fibrosus 24 Atrioventricular block, intraventricular conduction disease Toxic mutant RNA and altered splicing factor function 25 Membrane adapter proteins ANKB Ankyrin-B Metabolic regulators PRKAG2 G subunit of AMPK Glycogen storage disease Transforming growth factor- superfamily BMP2 Bone morphogenetic protein 2 Spliceopathies DMPK 3⬘UTR Myotonic dystrophy type I (Steinert’s disease) CPVT indicates catecholaminergic polymorphic ventricular tachycardia; WPW, Wolff-Parkinson-White syndrome; MAPK, mitogen-activated protein kinase; AMPK, AMP-activated protein kinase; and UTR, untranslated region. Park and Fishman Conduction System Disease 907 Downloaded from http://circ.ahajournals.org/ by guest on September 30, 2016 Figure 2. Electrophysiological heterogeneity of the sinoatrial node (SAN). The central SAN, the site of dominant pacemaking, is electronically insulated from the hyperpolarizing atrial myocardium through the differential expression of connexins and ion channels. Peripheral SAN cells are electrophysiologically intermediate between central cells and atrial cardiomyocytes. SR indicates sarcoplasmic reticulum. diastolic Cai elevations that colocalized with the primary pacemaking site. RYR2 and CASQ2 It is therefore interesting that mutations in SR calcium handling proteins are associated with sinus node dysfunction. Sinus bradycardia is a common feature of catecholaminergic polymorphic ventricular tachycardia (CPVT), an inherited arrhythmia syndrome characterized by bidirectional or polymorphic ventricular tachycardia induced by adrenergic stress in the absence of structural heart disease. Two CPVT-linked genes have been identified in humans, the cardiac ryanodine receptor, RYR2, and cardiac calsequestrin, CASQ2. The cardiac ryanodine receptor is the main calcium release channel on the SR in cardiomyocytes. Calsequestrin is the major calcium storage protein in the SR and complexes with RYR2. Mutations in these proteins result in altered calcium release characteristics from the SR leading to catecholamine-induced spontaneous SR Ca2⫹ release, resulting in delayed afterdepolarizations and triggered activity.52,53 Postma et al16 identified 13 RYR2 missense mutations in 12 families with CPVT. A total of 54 family members were found to be carriers, and all had resting sinus bradycardia off medications. A variant of CPVT with extended features of dilated cardiomyopathy, sinus node dysfunction, progressive atrioventricular block, atrial fibrillation, and atrial standstill was reported recently. Linkage analysis and long-range polymerase chain reaction revealed an in-frame, genomic deletion involving RYR2 exon3.15 Sinus bradycardia is also a characteristic feature of CPVT due to CASQ2 mutations. Postma et al identified 3 nonsense mutations in CASQ2 (a nonsense R33X, a splicing 532⫹1 G⬎A, and a 1-bp deletion, 62delA) in 3 kindreds with CPVT; all manifested sinus bradycardia on baseline ECG.17 The association of sinus bradycardia with mutations in SR calcium handling proteins lends further support for the calcium clock hypothesis in sinoatrial pacemaking; however, the mechanism of sinus node dysfunction in CPVT will need further study. ANKB Mutations in ankyrin-B (ANKB) are associated with long QT type 454 and familial sinus node dysfunction.21 ANKB is required for the proper targeting of ion channels and transporters to specific membrane domains. Mouse models haploinsufficient for ANKB develop profound sinus bradycardia and resting heart rate variability. Biochemical analysis revealed reduced expression and improper targeting of the NCX (NCX1), Na/K-ATPase (NKA), IP3 receptor (IP3R), and Cav1.3. ICa,L and INCX were significantly reduced in AnkB⫹/⫺ SAN cells.21 Therefore, ANKB mutations likely cause sinus node dysfunction by reducing ionic currents involved in both clock mechanisms. Diseases of Conduction Block Conduction block can occur at any level of the CCS and can manifest as sinoatrial exit block, atrioventricular block, infra- 908 Circulation March 1, 2011 Downloaded from http://circ.ahajournals.org/ by guest on September 30, 2016 Hisian block, or bundle branch block. Impaired conduction can be caused by ion channel defects that alter action potential shape or by defective coupling between cardiomyocytes. Inherited defects in cardiac conduction have been linked to mutations in SCN5A and SCN1B (both affect phase 0) and KCNJ2 (affects phase 3 and 4). The cardiac sodium channel consists of the pore-forming ␣-subunit (encoded by SCN5A) and a modulatory -subunit (encoded by SCN1B). The ␣-subunit contains a voltage sensor that allows for rapid activation in response to membrane depolarization. After depolarization, the sodium channel undergoes a period of inactivation, in which it is refractory to further impulses. SCN5A requires membrane repolarization to relieve the inactivated state. The inward rectifier potassium channel, Kir2.1, encoded by KCNJ2, maintains the resting membrane potential. Therefore, proper functioning of Nav1.5 and Kir2.1 is necessary for normal cardiac excitability. SCN5A Progressive cardiac conduction defect, or Lev-Lenègre disease, is characterized by age-related, fibrosclerotic degeneration of the His-Purkinje system.6 Impulse propagation through the proximal ventricular conduction system progressively declines, resulting in bundle branch blocks and eventually complete atrioventricular block. An inherited form of Lev-Lenègre disease is associated with loss of function mutations in SCN5A and can exist alone or as overlap syndromes with Brugada or long QT syndrome 3.6 Inherited progressive cardiac conduction defect is associated with a high risk of complete atrioventricular block and Stoke-Adams syncope without ventricular dysrhythmia.7 Schott et al8 identified a mutation in SCN5A that cosegregates with Lenègre disease in a large French family. Affected individuals had variable degrees of conduction block requiring pacemaker implantation in 4 family members because of syncope or complete heart block. Linkage analysis and candidate gene sequencing identified a T⬎C substitution at position ⫹2 of the donor splice site of intron 22 (IVS22⫹2 T⬎C), which results in a mutant lacking the voltage-sensitive segment.8 Functional analysis demonstrated no transient inward sodium current in response to depolarization, consistent with a loss-of-function mutation.6 SCN1B The majority of patients with Brugada and conduction disease do not have SCN5A mutations. Therefore, modifiers of Nav1.5 expression or function have become the target of candidate gene sequencing approaches. Watanabe et al9 identified SCN1B mutations in 3 families with conduction disease with or without Brugada syndrome. Coexpression of mutant -subunits with Nav1.5 resulted in diminished sodium current. KCNJ2 Mutations in KCNJ2 have been found in a rare autosomal dominant condition called Andersen-Tawil syndrome, characterized by periodic paralysis, dysmorphic features, polymorphic ventricular tachycardia, and cardiac conduction dis- ease.10,11 ECG evaluation of 96 patients with Andersen-Tawil syndrome from 33 unrelated kindreds revealed conduction defects at multiple levels from the atrioventricular node to the distal conduction system.55 Cardiomyocytes expressing a dominant-negative subunit of Kir2.1 exhibited a 95% reduction in IK1, resulting in significant action potential prolongation. Mouse models of Andersen-Tawil syndrome exhibited a slower heart rate and significant slowing of conduction.56,57 Diseases of Accessory Conduction Wolff-Parkinson-White (WPW) syndrome is characterized by preexcitation of ventricular myocardium via an accessory pathway (bundle of Kent) that bypasses the normal slow conduction through the atrioventricular node. Ventricular preexcitation is common, with a disease prevalence of 1.5 to 3 per 1000 people.22,58 Histological evaluation of Kent bundles resected from human subjects displayed features of typical ventricular myocytes with expression of connexin 43 (Cx43).59 The expression of high-conductance gap junctions in bypass tracts enables them to preexcite ventricular myocardium, manifesting as a short PR and a slurred QRS complex, or “delta wave,” on the ECG. The vast majority of WPW cases are sporadic, and the underlying mechanism remains unknown; however, rare inherited forms have been reported. Vidaillet et al60 determined that 3.4% of probands with WPW had 1 or more first-degree relatives with accessory conduction. PRKAG2 A familial form of WPW with an autosomal dominant mode of transmission was identified in 2 families. Thirty-one affected individuals had evidence of preexcitation and cardiac hypertrophy. A missense mutation in PRKAG2 was identified that results in a constitutively active form of the ␥2 regulatory subunit of AMP-activated protein kinase.22,23 Under normal conditions, AMP-activated protein kinase responds to energydepleted states by increasing glucose uptake and promoting glycolysis. Transgenic mice expressing a heart-restricted, constitutively active mutant, PRKAG2N488I, recapitulated the human WPW phenotype of cardiac hypertrophy, preexcitation, and conduction defects. The predominant histological finding was ventricular myocyte engorgement with glycogenladen vacuoles. The disruption of the annulus fibrosus by vacuolated ventricular myocytes resulted in the preexcitation phenotype.61 Using a mouse model of reversible glycogenstorage defect, Wolf et al62 demonstrated that the cardiomyopathy and CCS degeneration seen in PRKAG2N488I mice were reversible processes. BMP2 Lalani et al24 reported a novel WPW syndrome associated with microdeletion of the bone morphogenetic protein-2 (Bmp2) region within 20p12.3 that is characterized by variable cognitive deficits and dysmorphic features. The BMPs are members of the transforming growth factor- superfamily and play a critical role in cardiac development. Mice with cardiac deletion of BMP receptor type Ia (Bmpr1a) were embryonic lethal before E18.5 because of abnormal development of trabecular and compact myocardium, interventricular Park and Fishman septum, and endocardial cushion.63 More restricted deletion of Bmpr1a in the atrioventricular canal resulted in defective atrioventricular valve formation and maturation defects in the annulus fibrosus, resulting in preexcitation.64,65 Diseases of CCS Development Downloaded from http://circ.ahajournals.org/ by guest on September 30, 2016 Congenital heart disease is the most common form of birth defect, affecting 1% to 2% of live births.66 Arrhythmias may result from defective CCS specification/patterning, malformation or displacement of the conduction system, altered hemodynamics, prolonged hypoxic states, or postoperative sequelae.67,68 Developmentally, the conduction system derives from myocardial precursor cells within the fetal heart.69 –71 The process by which conduction cells are specified or recruited into a “conduction” versus “working myocyte” lineage is determined by the regional expression of transcription factors.69 –74 The main transcription factors identified in human CCS development are the T-box and homeobox factors. TBX5 Holt-Oram syndrome is an autosomal dominant condition characterized by preaxial radial ray limb deformities (defects of the radius, carpal bones, and/or thumbs) and cardiac septation defects. The septal defects are typically ostium secundum atrial septal defects, muscular ventricular septal defects, and atrioventricular canal defects. Patients with Holt-Oram syndrome manifest variable degrees of CCS dysfunction, such as sinus bradycardia and atrioventricular block, even in the absence of overt structural heart disease. In 1997, Basson et al18 screened 2 families with Holt-Oram syndrome and identified mutations in the T-box transcription factor, TBX5. The T-box transcription factors can function as transcriptional activators or repressors and are known to be critical regulators of cardiac specification and differentiation. Seven TBX family members are expressed in the developing heart, 3 of which (TBX1, TBX5, TBX20) have been linked to human congenital heart disease.75 Mice deficient in Tbx5 were embryonic lethal at E10.5 because of arrested development of the atria and left ventricle. Tbx5⫹/⫺ mice recapitulated the upper limb and cardiac manifestations of human Holt-Oram syndrome, including the conduction abnormalities.72,76 Significant maturation defects in the atrioventricular canal and ventricular conduction system were present.76 Moskowitz et al76 demonstrated that Tbx5⫹/⫺ mice have maturation failure of the atrioventricular canal manifesting as persistent atrioventricular rings around the tricuspid and mitral valves. Patterning defects were noted in the His bundle and bundle branches, including complete absence of right bundle branch formation in some cases. Expression of CCS-enriched markers, such as atrial natriuretic factor and Cx40, were found to be significantly downregulated, implicating TBX5 as a transcriptional activator of these genes. TBX5 and the homeobox transcription factor NKX2-5 were found to act synergistically in upregulating atrial natriuretic factor and Cx40 expression.76 NKX2-5 NKX2-5, a member of the homeodomain family, plays a central role in CCS induction and maintenance. Members of Conduction System Disease 909 the homeodomain family all share a conserved 60 –amino acid DNA binding motif known as the homeobox. These transcription factors are essential in organogenesis, dictating tissue specification and differentiation. Loss of the Nkx2-5 homolog, tinman, in the fruit fly results in failure of cardiogenesis.77 The role of NKX2-5 in human CCS development was established when mutations were identified in 4 families with nonsyndromic congenital heart disease and atrioventricular conduction block.19 Pedigree analysis was consistent with an autosomal dominant mode of transmission, and the most common structural abnormality was secundum atrial septal defects. Other associated structural heart defects included ventricular septal defects, tetralogy of Fallot, pulmonary atresia, redundant mitral valve, left ventricular hypertrophy, and subvalvular aortic stenosis.19 ECG analysis revealed atrioventricular conduction defects that were not strictly dependent on underlying structural heart disease. Fourteen individuals required pacemaker implantation. Genome-wide linkage analysis and candidate gene sequencing identified 3 mutations in NKX2-5.19 Currently, ⬎60 Nkx2-5 singlenucleotide substitutions have been identified in patients with congenital heart disease, emphasizing its critical role in cardiogenesis and conduction system specification and maintenance. Mice deficient in Nkx2-5 die in utero at E9-10 because of arrested cardiac development in the linear heart tube stage. The hearts of these mice undergo partial looping morphogenesis, lack endocardial cushions and trabeculae, and have underdeveloped atrioventricular canals.78 Jay et al79 reported complete absence of atrioventricular node primordial cells in another model of Nkx2-5 deficiency (Nkx2-5neo/neo) in a background of minK-LacZ, a reporter mouse that labels the SAN, atrioventricular node, and proximal ventricular conduction system. Heterozygous Nkx2-5 mice exhibit an overall reduction in the size of the CCS from the atrioventricular node to the distal Purkinje network. Histological evaluation of the Nkx2-5⫹/neo atrioventricular node revealed that compact nodal cells (N region) that are Cx40⫺/Cx45⫹ are distinctly absent, whereas the nodo-His region that is Cx40⫹/ Cx45⫹ remains intact.79 Immunostaining for Cx40 revealed that the density of Purkinje fibers was reduced.79 Surface electrograms of Nkx2-5⫹/neo mice showed PR and QRS prolongation. Intracardiac electrograms were notable for a diminutive His depolarization amplitude, consistent with reduced size of the His bundle, and for prolonged 1:1 and 2:1 atrioventricular cycle lengths and atrioventricular node effective refractory periods suggestive of atrioventricular node dysfunction. His-ventricular intervals were unchanged likely because of sufficient expression of Cx40. Similarities in atrioventricular node dysfunction between humans and mice with Nkx2-5 haploinsufficiency point to the conserved role of NKX2-5 in the induction and maintenance of the mammalian CCS.79 – 81 NKX2-5, TBX5, and the inhibitor of differentiation 2 (Id2) are now known to function together as a conduction system transcriptome specifying the murine ventricular CCS.74 The coexpression of NKX2-5 and TBX5 in the developing ventricular conduction system results in regionally restricted expression of Id2, ANF, and Cx40. Id2 is believed to function 910 Circulation March 1, 2011 as an inhibitor of muscle differentiation allowing specification toward a conduction lineage.74 Combined haploinsufficiency of Nkx2-5 and Tbx5 (Nkx2-5⫹/⫺/Tbx5⫹/⫺) results in developmental failure of the ventricular conduction system with complete absence of the His bundle and bundle branches. Loss of CCS markers, like Cx40, in mutant hearts results in marked widening of the QRS complex on surface ECG.74 A human correlate of compound heterozygosity of Nkx2-5 and Tbx5 has not yet been identified. Conduction Disease Associated With Neuromuscular Disorders Downloaded from http://circ.ahajournals.org/ by guest on September 30, 2016 Neuromuscular disorders represent a diverse collection of diseases that commonly present with cardiac involvement. Mutations have been identified in genes involved in the cytoskeleton, nuclear envelope, and mitochondrial function. Cardiac involvement typically manifests as dilated or hypertrophic cardiomyopathy, atrioventricular conduction defects, and atrial and ventricular dysrhythmias.82 EMD and LMNA Mutations affecting the nuclear envelope have been associated with significant CCS dysfunction. The inner membrane of the nuclear envelope is a highly organized structure, composed of integral membrane proteins and nuclear cytoskeletal proteins that function together in higher-order chromatin structure and transcriptional regulation. The lamins (A, B, and C) are an integral part of an intermediate filament network that imparts structural rigidity to the inner nuclear membrane. Emerin, a member of the nuclear laminaassociated protein family, putatively mediates anchoring of chromatin to the cytoskeleton. Mutations in emerin (EMD) or lamin A/C (LMNA) result in X-linked Emery-Dreifuss muscular dystrophy and autosomal dominant Emery-Dreifuss muscular dystrophy,20 respectively. Individuals with EmeryDreifuss muscular dystrophy develop progressive skeletal muscle weakness in the first decade of life and cardiac involvement (dilated cardiomyopathy and atrioventricular block) in the second decade.82,83 Arimura et al84 engineered a mouse model of autosomal dominant Emery-Dreifuss muscular dystrophy by knocking-in an Lmna missense mutation (H222P) previously identified from a family with typical autosomal dominant Emery-Dreifuss muscular dystrophy. The mouse model faithfully recapitulated the human disease with LmnaH222P/H222P mice exhibiting locomotive defects, dilated cardiomyopathy, and CCS dysfunction. Telemetric evaluation of the mutant mice revealed PR prolongation and QRS complex widening. A similar CCS defect was seen in mice haploinsufficient in the Lmna gene. Lmna⫹/⫺ mice exhibited sinus bradycardia with variable degrees of atrioventricular block. Histological evaluation of these mice revealed nuclear deformation and apoptosis in atrioventricular node cells.85 Another engineered mouse line expressing LmnaN195K, known to cause autosomal dominant dilated cardiomyopathy with conduction disease in humans,86 exhibited high-grade atrioventricular block and complete heart block. Biochemical evaluation revealed reduced expression and mislocalization of Cx40 and Cx43 in mutant atrial tissue.87 Desmin staining also revealed structural defects of the sarcomere and intercalated discs.87 Genome-wide expression profiling of Lmna H222P mouse hearts revealed significant increases in mitogen-activated protein kinase (MAPK) signaling pathways.88 Hyperactivation of MAPK pathways is associated with cardiomyopathy and CCS dysfunction. A significant increase of the activated forms of 2 MAPKs, JNK and ERK1/2, was noted in mutant hearts that predated the onset of overt or molecularly defined cardiomyopathy.88 Treatment of Lmna H222P mice with an inhibitor of ERK phosphorylation abrogated the increase in biomarkers of cardiomyopathy and restored ejection fraction to normal levels. These findings directly link MAPK hyperactivation to the cardiomyopathic phenotype in Lmna H222P mice.89 On the basis of the phenotypes of these mouse models, lamin A/C appears to maintain the functional integrity of the CCS in 2 ways: (1) protection of the nucleus against mechanical stress and (2) maintenance of proper chromatin organization to ensure accurate gene expression, such as in connexin expression and MAPK signaling pathways.83 DMPK Myotonic dystrophy type 1 (DM1), or Steinert’s disease, is the most common muscular dystrophy in adults and is characterized by myotonia, insulin resistance, progressive skeletal muscle loss, cataracts, and cardiac conduction defects.25 CCS dysfunction is seen in 70% of patients with DM1 and can manifest as sinus bradycardia, variable degrees of atrioventricular block, and intraventricular conduction delays.90 The genetic basis of DM1 is an expanded (CTG)n repeat in the 3⬘ untranslated region (UTR) of the myotonic dystrophy protein kinase (DMPK) gene. Three molecular mechanisms linking the trinucleotide expansion with the cardiac conduction defects of DM1 have been proposed: (1) haploinsufficiency of DMPK,91 (2) underexpression of the neighboring homeodomain-encoding gene, Six5,92 and (3) toxic accumulation of mutant RNA.93 Nuclear entrapment of toxic RNA leads to sequestration and altered activity of RNA-binding proteins, including proteins involved in RNA splicing like the muscleblind-like (MBL1) family.93 To explore the pathophysiological role of the 3⬘UTR of DMPK in the DM1 phenotype, Mahadevan et al93 created a transgenic mouse that expresses an inducible transcript encoding the DMPK 3⬘UTR with green fluorescent protein. They found that overexpression of the wild-type DMPK 3⬘UTR was sufficient to induce the characteristic features of DM1, including myotonia, splicing defects, and CCS dysfunction. The authors postulated that transgenic overexpression of the wild-type DMPK 3⬘UTR with 5 (CUG)n repeats may be the pathogenetic molar equivalent of mutant 3⬘UTR with hundreds of (CUG)n repeats. Induction of the transgene first resulted in PR prolongation that progressed to complete heart block and sudden cardiac death. Interestingly, cessation of the inducing agent, doxycycline, resulted in reversion of the myotonic and some of the CCS defects. First-degree heart blocks in animals were reversible; however, atrioventricular blocks beyond second degree were not reversible. Park and Fishman Future Directions Downloaded from http://circ.ahajournals.org/ by guest on September 30, 2016 Linkage analysis with positional cloning has been a highly effective means of identifying gene mutations within kindreds of monogenic disease. More than 1000 genes have been identified with this approach, including those in this review. With the sequencing of the human genome, the promise of identifying genetic causes of complex, multifactorial diseases is becoming more of a reality. One major step in this direction was the development of genome-wide association studies.94 The genome-wide association study is a test of association between a disease and genetic markers that span the entire genome. The technique relies on the fact that variance at one locus predicts with high probability variance of an adjacent locus because of linkage disequilibrium. In other words, there is nonrandom cosegregation of a series of genetic markers that are close together in the genome. This cluster of linked markers is known as a haplotype. The first study of haplotype structure within 4 populations (Yoruban, Northern/Western Europeans, Chinese, and Japanese) was published in Nature in 2005 by the International HapMap Consortium. Their work reported that individual genetic markers (single nucleotide polymorphisms) predict adjacent markers typically with a resolution of ⬇30 000 bp. Considering that the human genome is ⬇3⫻109 bp, they projected that ⬍500 000 single nucleotide polymorphisms would be needed to survey the entire genome for all common genetic variants.94,95 Genome-wide association studies have now been used to identify genetic variants that influence ECG parameters in different populations. Intermediate parameters, such as heart rate or PR interval, were used as surrogate markers of disease for 2 reasons: (1) They have an association with cardiovascular morbidity and atrial fibrillation, and (2) they have tighter associations with gene variants than the actual disease. Holm et al96 reported several genome-wide associations using a cutoff P value ⬍1.6⫻10⫺9. One locus harboring MYH6 was associated with heart rate, 4 loci (TBX5, SCN10A, CAV1, and ARHGAP24) were associated with PR interval, and 4 loci (TBX5, SCN10A, 6p21, and 10q21) were associated with QRS duration. They went on to test these associations with individuals manifesting different arrhythmias in an Icelandic and Norwegian population. Correlations were found between atrial fibrillation and TBX5 and CAV1 (P⫽4.0⫻10⫺5 and P⫽0.00032, respectively), between advanced atrioventricular block and TBX5 (P⫽0.0067), and between pacemaker implantation and SCN10A (P⫽0.0029). Similar loci were identified by 2 additional independent genome-wide association studies in a European population and an Indian Asian population. Pfeufer et al97 reported 9 loci that were highly associated with PR interval (P⬍5⫻10⫺8) from a meta-analysis of the CHARGE Consortium with ⬎28 000 European subjects. One locus had associations with 2 sodium channels (SCN10A and SCN5A), and 6 loci were near genes involved in cardiac development (CAV1-CAV2, NKX2-5, SOX5, WNT11, MEIS1, and TBX5-TBX3). Of these, SCN10A, SCN5A, CAV1-CAV2, NKX2-5, and SOX5 were found to be associated with atrial fibrillation. Chambers et al98 also reported the association between SCN10A and PR interval in 6543 Indian Asians. Physiological testing of Scn10a-deficient mice revealed shortened PR intervals in Conduction System Disease 911 knockout mice with no significant difference in all other ECG and echocardiographic parameters. The discovery of novel gene families associated with human conduction and arrhythmic diseases with the use of genome-wide association studies is well under way. Identification of SCN10A by 3 independent groups studying different populations confirms the fidelity of this approach. Further experiments confirming the significance of these associations will need to be performed. In addition to identifying novel gene targets, this technique will also aid in the discovery of new associations with noncoding regions in which new epigenetic modifiers and transcriptional/translational regulators, such as microRNAs, will be identified. Therapeutic Strategies The current standard of care for symptomatic bradycardia due to conduction system disease is the implantation of an electronic pacemaker. Despite their success, electronic pacemakers have limitations, which include lead complications, finite battery life, potential for infection, lack of autonomic responsiveness, and size restriction in younger patients. These limitations have spurred on the development of biological pacemakers, the premise of which is to restore pacemaking activity with the use of viral-based or stem cell– based gene delivery systems.99 The identification and characterization of genes involved in generating pacemaker currents have allowed biological pacemaker technology to become a reality. The restoration of sinus pacing rates can be achieved by modulating inward and outward currents to establish or increase the slope of diastolic depolarization in cardiac tissue. Increasing inward currents and/or decreasing outward currents increase the slope of diastolic depolarization and therefore the pacing rate. Genes that have been investigated or are under current investigation include the following: (1) 2adrenergic receptor,100,101 (2) dominant-negative Kir2.1 mutants,102 (3) adenylate cyclase type VI (ACVI),103,104 and (4) HCN channels.105 The 2-adrenergic receptor and adenylate cyclase type VI both increase cAMP levels, leading to activation of endogenous HCN channels and calcium clock mechanisms. Although initial animal models using the 2adrenergic receptor showed promise with transient increases in heart rate, the potential for proarrhythmia and the inability of this approach to establish de novo pacemaker activity limited its efficacy.101 Another approach focused on modifying ionic currents that convert working myocardial cells, which have relatively stable diastolic potentials, into cells with phase 4 diastolic depolarization. It was postulated that atrial and ventricular myocytes have the potential for automaticity, but that hyperpolarizing currents, such as IK1, prevent diastolic depolarization by stabilizing the resting membrane potential. Miake et al102 confirmed this hypothesis when they demonstrated that adenoviral delivery of a dominant-negative Kir2.1 construct into the left ventricle of guinea pigs resulted in conversion of quiescent myocytes into pacemaker cells. Unfortunately, significant action potential prolongation limited the clinical utility of this treatment strategy.102 912 Circulation March 1, 2011 Downloaded from http://circ.ahajournals.org/ by guest on September 30, 2016 Rosen and colleagues105,106 demonstrated that automaticity could be induced in quiescent myocardium with the use of heterologous expression of HCN channels that produce the pacemaker current If. Qu and Plotnikov et al demonstrated that stable autonomous rhythms could be generated when adenovirus encoding HCN2 was injected into the left atrium105 or left bundle branch106 of a canine heart. To bypass the limitations of viral-based systems, such as host immune response, several groups reported the successful use of cell-based delivery systems. Plotnikov et al107 reported the successful implantation of human mesenchymal stem cells expressing HCN2 in the left ventricle of a canine model of atrioventricular block. Dogs maintained stable ectopic pacemaker activity for ⬎6 weeks without the use of immunosuppression.107 Human mesenchymal stem cells electronically couple to host myocardium through gap junctions; therefore, conditions with significant gap junction remodeling may affect the efficacy of this method. Although standalone biological pacemakers may be far into the future, adjuvant biological pacemakers may find real-world utility for current deficiencies of electronic pacemakers, such as limited battery life and device infections. For example, biological preparations used in conjunction with device therapy may be used to extend battery life, decreasing the frequency of generator changes. Transient injectable pacemakers may also function as bridge therapy after lead extraction of an infected device. The need for adjuvant biological pacemakers is clear, but continued refinement of gene- and cell-based delivery systems will be necessary to make this technology a reality.99 Conclusion Although rare, inherited arrhythmias have become an invaluable tool in identifying the genetic determinants of CCS function. Each new mutation enhances our understanding and appreciation of the biochemical and structural complexity needed for cardiac impulse generation and propagation. This methodology is hampered, however, by the relative scarcity of inherited conditions affecting the CCS. The addition of genome-wide association studies has broadened this search for novel genes beyond rare familial afflictions to include common, multifactorial conditions. It is hoped that this exciting new frontier will bring to light the complex interplay of genes and genetic/epigenetic modifiers that influence the prevalence of common diseases. These genetic screens will ultimately yield a bevy of new gene targets for pharmaceutical or gene-based therapeutics of the future. Acknowledgments We apologize to the many investigators whose work could not be cited in this review because of space constraints. Sources of Funding Studies in the Fishman laboratory are supported by National Institutes of Health grants HL64757, HL081336, and HL82727 and a New York State STEM award (to Dr Fishman) and a Heart Rhythm Foundation Fellowship (to Dr Park). Disclosures None. References 1. Benson DW, Wang DW, Dyment M, Knilans TK, Fish FA, Strieper MJ, Rhodes TH, George AL Jr. Congenital sick sinus syndrome caused by recessive mutations in the cardiac sodium channel gene (SCN5A). J Clin Invest. 2003;112:1019 –1028. 2. Makiyama T, Akao M, Tsuji K, Doi T, Ohno S, Takenaka K, Kobori A, Ninomiya T, Yoshida H, Takano M, Makita N, Yanagisawa F, Higashi Y, Takeyama Y, Kita T, Horie M. High risk for bradyarrhythmic complications in patients with Brugada syndrome caused by SCN5A gene mutations. J Am Coll Cardiol. 2005;46:2100 –2106. 3. Groenewegen WA, Firouzi M, Bezzina CR, Vliex S, van Langen IM, Sandkuijl L, Smits JP, Hulsbeek M, Rook MB, Jongsma HJ, Wilde AA. A cardiac sodium channel mutation cosegregates with a rare connexin40 genotype in familial atrial standstill. Circ Res. 2003;92:14 –22. 4. Veldkamp MW, Wilders R, Baartscheer A, Zegers JG, Bezzina CR, Wilde AA. Contribution of sodium channel mutations to bradycardia and sinus node dysfunction in LQT3 families. Circ Res. 2003;92: 976 –983. 5. Probst V, Allouis M, Sacher F, Pattier S, Babuty D, Mabo P, Mansourati J, Victor J, Nguyen JM, Schott JJ, Boisseau P, Escande D, Le Marec H. Progressive cardiac conduction defect is the prevailing phenotype in carriers of a Brugada syndrome SCN5A mutation. J Cardiovasc Electrophysiol. 2006;17:270–275. 6. Probst V, Kyndt F, Potet F, Trochu JN, Mialet G, Demolombe S, Schott JJ, Baro I, Escande D, Le Marec H. Haploinsufficiency in combination with aging causes SCN5A-linked hereditary Lenegre disease. J Am Coll Cardiol. 2003;41:643– 652. 7. Kyndt F, Probst V, Potet F, Demolombe S, Chevallier JC, Baro I, Moisan JP, Boisseau P, Schott JJ, Escande D, Le Marec H. Novel SCN5A mutation leading either to isolated cardiac conduction defect or Brugada syndrome in a large French family. Circulation. 2001;104: 3081–3086. 8. Schott JJ, Alshinawi C, Kyndt F, Probst V, Hoorntje TM, Hulsbeek M, Wilde AA, Escande D, Mannens MM, Le Marec H. Cardiac conduction defects associate with mutations in SCN5A. Nat Genet. 1999;23:20 –21. 9. Watanabe H, Koopmann TT, Le Scouarnec S, Yang T, Ingram CR, Schott JJ, Demolombe S, Probst V, Anselme F, Escande D, Wiesfeld AC, Pfeufer A, Kaab S, Wichmann HE, Hasdemir C, Aizawa Y, Wilde AA, Roden DM, Bezzina CR. Sodium channel beta1 subunit mutations associated with Brugada syndrome and cardiac conduction disease in humans. J Clin Invest. 2008;118:2260 –2268. 10. Andelfinger G, Tapper AR, Welch RC, Vanoye CG, George AL Jr, Benson DW. KCNJ2 mutation results in Andersen syndrome with sexspecific cardiac and skeletal muscle phenotypes. Am J Hum Genet. 2002;71:663– 668. 11. Plaster NM, Tawil R, Tristani-Firouzi M, Canun S, Bendahhou S, Tsunoda A, Donaldson MR, Iannaccone ST, Brunt E, Barohn R, Clark J, Deymeer F, George AL Jr, Fish FA, Hahn A, Nitu A, Ozdemir C, Serdaroglu P, Subramony SH, Wolfe G, Fu YH, Ptacek LJ. Mutations in Kir2.1 cause the developmental and episodic electrical phenotypes of Andersen’s syndrome. Cell. 2001;105:511–519. 12. Schulze-Bahr E, Neu A, Friederich P, Kaupp UB, Breithardt G, Pongs O, Isbrandt D. Pacemaker channel dysfunction in a patient with sinus node disease. J Clin Invest. 2003;111:1537–1545. 13. Milanesi R, Baruscotti M, Gnecchi-Ruscone T, DiFrancesco D. Familial sinus bradycardia associated with a mutation in the cardiac pacemaker channel. N Engl J Med. 2006;354:151–157. 14. Nof E, Luria D, Brass D, Marek D, Lahat H, Reznik-Wolf H, Pras E, Dascal N, Eldar M, Glikson M. Point mutation in the HCN4 cardiac ion channel pore affecting synthesis, trafficking, and functional expression is associated with familial asymptomatic sinus bradycardia. Circulation. 2007;116:463– 470. 15. Bhuiyan ZA, van den Berg MP, van Tintelen JP, Bink-Boelkens MT, Wiesfeld AC, Alders M, Postma AV, van Langen I, Mannens MM, Wilde AA. Expanding spectrum of human RYR2-related disease: new electrocardiographic, structural, and genetic features. Circulation. 2007; 116:1569 –1576. 16. Postma AV, Denjoy I, Kamblock J, Alders M, Lupoglazoff JM, Vaksmann G, Dubosq-Bidot L, Sebillon P, Mannens MM, Guicheney P, Wilde AA. Catecholaminergic polymorphic ventricular tachycardia: RYR2 mutations, bradycardia, and follow up of the patients. J Med Genet. 2005;42:863– 870. 17. Postma AV, Denjoy I, Hoorntje TM, Lupoglazoff JM, Da Costa A, Sebillon P, Mannens MM, Wilde AA, Guicheney P. Absence of calse- Park and Fishman 18. 19. 20. 21. 22. Downloaded from http://circ.ahajournals.org/ by guest on September 30, 2016 23. 24. 25. 26. 27. 28. 29. 30. 31. 32. 33. 34. 35. 36. questrin 2 causes severe forms of catecholaminergic polymorphic ventricular tachycardia. Circ Res. 2002;91;e21– e26. Basson CT, Bachinsky DR, Lin RC, Levi T, Elkins JA, Soults J, Grayzel D, Kroumpouzou E, Traill TA, Leblanc-Straceski J, Renault B, Kucherlapati R, Seidman JG, Seidman CE. Mutations in human TBX5 [corrected] cause limb and cardiac malformation in Holt-Oram syndrome. Nat Genet. 1997;15:30 –35. Schott JJ, Benson DW, Basson CT, Pease W, Silberbach GM, Moak JP, Maron BJ, Seidman CE, Seidman JG. Congenital heart disease caused by mutations in the transcription factor NKX2-5. Science. 1998;281: 108 –111. Bonne G, Di Barletta MR, Varnous S, Becane HM, Hammouda EH, Merlini L, Muntoni F, Greenberg CR, Gary F, Urtizberea JA, Duboc D, Fardeau M, Toniolo D, Schwartz K. Mutations in the gene encoding lamin A/C cause autosomal dominant Emery-Dreifuss muscular dystrophy. Nat Genet. 1999;21:285–288. Le Scouarnec S, Bhasin N, Vieyres C, Hund TJ, Cunha SR, Koval O, Marionneau C, Chen B, Wu Y, Demolombe S, Song LS, Le Marec H, Probst V, Schott JJ, Anderson ME, Mohler PJ. Dysfunction in ankyrinB-dependent ion channel and transporter targeting causes human sinus node disease. Proc Natl Acad Sci U S A. 2008;105:15617–15622. Gollob MH, Green MS, Tang AS, Gollob T, Karibe A, Ali Hassan AS, Ahmad F, Lozado R, Shah G, Fananapazir L, Bachinski LL, Roberts R. Identification of a gene responsible for familial Wolff-Parkinson-White syndrome. N Engl J Med. 2001;344:1823–1831. Arad M, Benson DW, Perez-Atayde AR, McKenna WJ, Sparks EA, Kanter RJ, McGarry K, Seidman JG, Seidman CE. Constitutively active AMP kinase mutations cause glycogen storage disease mimicking hypertrophic cardiomyopathy. J Clin Invest. 2002;109:357–362. Lalani SR, Thakuria JV, Cox GF, Wang X, Bi W, Bray MS, Shaw C, Cheung SW, Chinault AC, Boggs BA, Ou Z, Brundage EK, Lupski JR, Gentile J, Waisbren S, Pursley A, Ma L, Khajavi M, Zapata G, Friedman R, Kim JJ, Towbin JA, Stankiewicz P, Schnittger S, Hansmann I, Ai T, Sood S, Wehrens XH, Martin JF, Belmont JW, Potocki L. 20p12.3 Microdeletion predisposes to Wolff-Parkinson-White syndrome with variable neurocognitive deficits. J Med Genet. 2009;46:168 –175. Mahadevan M, Tsilfidis C, Sabourin L, Shutler G, Amemiya C, Jansen G, Neville C, Narang M, Barcelo J, O’Hoy K, Leblond S, EarleMacdonald J, De Jong PJ, Wieringa B, Korneluk RG. Myotonic dystrophy mutation: an unstable CTG repeat in the 3⬘ untranslated region of the gene. Science. 1992;255:1253–1255. Anderson KR, Ho SY, Anderson RH. Location and vascular supply of sinus node in human heart. Br Heart J. 1979;41:28 –32. Lei M, Zhang H, Grace AA, Huang CL. SCN5A and sinoatrial node pacemaker function. Cardiovasc Res. 2007;74:356 –365. Lei M, Jones SA, Liu J, Lancaster MK, Fung SS, Dobrzynski H, Camelliti P, Maier SK, Noble D, Boyett MR. Requirement of neuronaland cardiac-type sodium channels for murine sinoatrial node pacemaking. J Physiol. 2004;559:835– 848. Zhang H, Holden AV, Kodama I, Honjo H, Lei M, Varghese T, Boyett MR. Mathematical models of action potentials in the periphery and center of the rabbit sinoatrial node. Am J Physiol. 2000;279; H397–H421. Dobrzynski H, Li J, Tellez J, Greener ID, Nikolski VP, Wright SE, Parson SH, Jones SA, Lancaster MK, Yamamoto M, Honjo H, Takagishi Y, Kodama I, Efimov IR, Billeter R, Boyett MR. Computer threedimensional reconstruction of the sinoatrial node. Circulation. 2005; 111:846 – 854. Liu J, Noble PJ, Xiao G, Abdelrahman M, Dobrzynski H, Boyett MR, Lei M, Noble D. Role of pacemaking current in cardiac nodes: insights from a comparative study of sinoatrial node and atrioventricular node. Prog Biophys Mol Biol. 2008;96:294 –304. Liu J, Dobrzynski H, Yanni J, Boyett MR, Lei M. Organisation of the mouse sinoatrial node: structure and expression of HCN channels. Cardiovasc Res. 2007;73:729 –738. Chen PS, Joung B, Shinohara T, Das M, Chen Z, Lin SF. The initiation of the heart beat. Circ J. 2010;74:221–225. Huser J, Blatter LA, Lipsius SL. Intracellular Ca2⫹ release contributes to automaticity in cat atrial pacemaker cells. J Physiol. 2000;524(pt 2); 415– 422. Bogdanov KY, Vinogradova TM, Lakatta EG. Sinoatrial nodal cell ryanodine receptor and Na(⫹)-Ca(2⫹) exchanger: molecular partners in pacemaker regulation. Circ Res. 2001;88:1254 –1258. Vinogradova TM, Bogdanov KY, Lakatta EG. -Adrenergic stimulation modulates ryanodine receptor Ca(2⫹) release during diastolic depolar- 37. 38. 39. 40. 41. 42. 43. 44. 45. 46. 47. 48. 49. 50. 51. 52. 53. 54. 55. 56. Conduction System Disease 913 ization to accelerate pacemaker activity in rabbit sinoatrial nodal cells. Circ Res. 2002;90:73–79. Lakatta EG, Maltsev VA, Vinogradova TM. A coupled SYSTEM of intracellular Ca2⫹ clocks and surface membrane voltage clocks controls the timekeeping mechanism of the heart’s pacemaker. Circ Res. 2010; 106:659 – 673. Joung B, Ogawa M, Lin SF, Chen PS. The calcium and voltage clocks in sinoatrial node automaticity. Korean Circ J. 2009;39:217–222. Ruan Y, Liu N, Priori SG. Sodium channel mutations and arrhythmias. Nat Rev Cardiol. 2009;6:337–348. Smits JP, Koopmann TT, Wilders R, Veldkamp MW, Opthof T, Bhuiyan ZA, Mannens MM, Balser JR, Tan HL, Bezzina CR, Wilde AA. A mutation in the human cardiac sodium channel (E161K) contributes to sick sinus syndrome, conduction disease and Brugada syndrome in two families. J Mol Cell Cardiol. 2005;38:969 –981. Butters TD, Aslanidi OV, Inada S, Boyett MR, Hancox JC, Lei M, Zhang H. Mechanistic links between Na⫹ channel (SCN5A) mutations and impaired cardiac pacemaking in sick sinus syndrome. Circ Res. 2010;107:126 –137. Verheijck EE, van Kempen MJ, Veereschild M, Lurvink J, Jongsma HJ, Bouman LN. Electrophysiological features of the mouse sinoatrial node in relation to connexin distribution. Cardiovasc Res. 2001;52:40 –50. Fedorov VV, Schuessler RB, Hemphill M, Ambrosi CM, Chang R, Voloshina AS, Brown K, Hucker WJ, Efimov IR. Structural and functional evidence for discrete exit pathways that connect the canine sinoatrial node and atria. Circ Res. 2009;104:915–923. Herrmann S, Stieber J, Ludwig A. Pathophysiology of HCN channels. Pflugers Arch. 2007;454:517–522. Biel M, Wahl-Schott C, Michalakis S, Zong X. Hyperpolarization-activated cation channels: from genes to function. Physiol Rev. 2009;89: 847– 885. Stieber J, Herrmann S, Feil S, Loster J, Feil R, Biel M, Hofmann F, Ludwig A. The hyperpolarization-activated channel HCN4 is required for the generation of pacemaker action potentials in the embryonic heart. Proc Natl Acad Sci U S A. 2003;100:15235–15240. Ludwig A, Herrmann S, Hoesl E, Stieber J. Mouse models for studying pacemaker channel function and sinus node arrhythmia. Prog Biophys Mol Biol. 2008;98:179 –185. Herrmann S, Stieber J, Stockl G, Hofmann F, Ludwig A. HCN4 provides a ‘depolarization reserve’ and is not required for heart rate acceleration in mice. EMBO J. 2007;26:4423– 4432. Hoesl E, Stieber J, Herrmann S, Feil S, Tybl E, Hofmann F, Feil R, Ludwig A. Tamoxifen-inducible gene deletion in the cardiac conduction system. J Mol Cell Cardiol. 2008;45:62– 69. Rubenstein DS, Lipsius SL. Mechanisms of automaticity in subsidiary pacemakers from cat right atrium. Circ Res. 1989;64:648 – 657. Ju YK, Allen DG. How does beta-adrenergic stimulation increase the heart rate? The role of intracellular Ca2⫹ release in amphibian pacemaker cells. J Physiol. 1999;516(pt 3);793– 804. Rizzi N, Liu N, Napolitano C, Nori A, Turcato F, Colombi B, Bicciato S, Arcelli D, Spedito A, Scelsi M, Villani L, Esposito G, Boncompagni S, Protasi F, Volpe P, Priori SG. Unexpected structural and functional consequences of the R33Q homozygous mutation in cardiac calsequestrin: a complex arrhythmogenic cascade in a knock in mouse model. Circ Res. 2008;103:298 –306. Liu N, Colombi B, Memmi M, Zissimopoulos S, Rizzi N, Negri S, Imbriani M, Napolitano C, Lai FA, Priori SG. Arrhythmogenesis in catecholaminergic polymorphic ventricular tachycardia: insights from a RyR2 R4496C knock-in mouse model. Circ Res. 2006;99:292–298. Mohler PJ, Schott JJ, Gramolini AO, Dilly KW, Guatimosim S, duBell WH, Song LS, Haurogne K, Kyndt F, Ali ME, Rogers TB, Lederer WJ, Escande D, Le Marec H, Bennett V. Ankyrin-B mutation causes type 4 long-QT cardiac arrhythmia and sudden cardiac death. Nature. 2003; 421:634 – 639. Zhang L, Benson DW, Tristani-Firouzi M, Ptacek LJ, Tawil R, Schwartz PJ, George AL, Horie M, Andelfinger G, Snow GL, Fu YH, Ackerman MJ, Vincent GM. Electrocardiographic features in Andersen-Tawil syndrome patients with KCNJ2 mutations: characteristic T-U-wave patterns predict the KCNJ2 genotype. Circulation. 2005;111: 2720 –2726. Zaritsky JJ, Redell JB, Tempel BL, Schwarz TL. The consequences of disrupting cardiac inwardly rectifying K(⫹) current (I(K1)) as revealed by the targeted deletion of the murine Kir2.1 and Kir2.2 genes. J Physiol. 2001;533:697–710. 914 Circulation March 1, 2011 Downloaded from http://circ.ahajournals.org/ by guest on September 30, 2016 57. McLerie M, Lopatin AN. Dominant-negative suppression of I(K1) in the mouse heart leads to altered cardiac excitability. J Mol Cell Cardiol. 2003;35:367–378. 58. Light PE. Familial Wolff-Parkinson-White syndrome: a disease of glycogen storage or ion channel dysfunction? J Cardiovasc Electrophysiol. 2006; 17(suppl 1):S158–S161. 59. Peters NS, Rowland E, Bennett JG, Green CR, Anderson RH, Severs NJ. The Wolff-Parkinson-White syndrome: the cellular substrate for conduction in the accessory atrioventricular pathway. Eur Heart J. 1994; 15:981–987. 60. Vidaillet HJ Jr, Pressley JC, Henke E, Harrell FE Jr, German LD. Familial occurrence of accessory atrioventricular pathways (preexcitation syndrome). N Engl J Med. 1987;317:65– 69. 61. Arad M, Moskowitz IP, Patel VV, Ahmad F, Perez-Atayde AR, Sawyer DB, Walter M, Li GH, Burgon PG, Maguire CT, Stapleton D, Schmitt JP, Guo XX, Pizard A, Kupershmidt S, Roden DM, Berul CI, Seidman CE, Seidman JG. Transgenic mice overexpressing mutant PRKAG2 define the cause of Wolff-Parkinson-White syndrome in glycogen storage cardiomyopathy. Circulation. 2003;107:2850 –2856. 62. Wolf CM, Arad M, Ahmad F, Sanbe A, Bernstein SA, Toka O, Konno T, Morley G, Robbins J, Seidman JG, Seidman CE, Berul CI. Reversibility of PRKAG2 glycogen-storage cardiomyopathy and electrophysiological manifestations. Circulation. 2008;117:144 –154. 63. Gaussin V, Van de Putte T, Mishina Y, Hanks MC, Zwijsen A, Huylebroeck D, Behringer RR, Schneider MD. Endocardial cushion and myocardial defects after cardiac myocyte-specific conditional deletion of the bone morphogenetic protein receptor ALK3. Proc Natl Acad Sci U S A. 2002;99:2878 –2883. 64. Stroud DM, Gaussin V, Burch JB, Yu C, Mishina Y, Schneider MD, Fishman GI, Morley GE. Abnormal conduction and morphology in the atrioventricular node of mice with atrioventricular canal targeted deletion of Alk3/Bmpr1a receptor. Circulation. 2007;116:2535–2543. 65. Gaussin V, Morley GE, Cox L, Zwijsen A, Vance KM, Emile L, Tian Y, Liu J, Hong C, Myers D, Conway SJ, Depre C, Mishina Y, Behringer RR, Hanks MC, Schneider MD, Huylebroeck D, Fishman GI, Burch JB, Vatner SF. Alk3/Bmpr1a receptor is required for development of the atrioventricular canal into valves and annulus fibrosus. Circ Res. 2005; 97:219 –226. 66. Hoffman JI, Kaplan S. The incidence of congenital heart disease. J Am Coll Cardiol. 2002;39:1890 –1900. 67. Walsh SR, Tang T, Wijewardena C, Yarham SI, Boyle JR, Gaunt ME. Postoperative arrhythmias in general surgical patients. Ann R Coll Surg Engl. 2007;89:91–95. 68. Walsh EP, Cecchin F. Arrhythmias in adult patients with congenital heart disease. Circulation. 2007;115:534 –545. 69. Gourdie RG, Mima T, Thompson RP, Mikawa T. Terminal diversification of the myocyte lineage generates Purkinje fibers of the cardiac conduction system. Development. 1995;121:1423–1431. 70. Cheng G, Litchenberg WH, Cole GJ, Mikawa T, Thompson RP, Gourdie RG. Development of the cardiac conduction system involves recruitment within a multipotent cardiomyogenic lineage. Development. 1999;126: 5041–5049. 71. Moorman AF, Christoffels VM. Development of the cardiac conduction system: a matter of chamber development. Novartis Found Symp. 2003; 250:25–34; discussion 34 – 43, 276 –279. 72. Bruneau BG, Nemer G, Schmitt JP, Charron F, Robitaille L, Caron S, Conner DA, Gessler M, Nemer M, Seidman CE, Seidman JG. A murine model of Holt-Oram syndrome defines roles of the T-box transcription factor Tbx5 in cardiogenesis and disease. Cell. 2001;106:709 –721. 73. Christoffels VM, Smits GJ, Kispert A, Moorman AF. Development of the pacemaker tissues of the heart. Circ Res. 2010;106:240 –254. 74. Moskowitz IP, Kim JB, Moore ML, Wolf CM, Peterson MA, Shendure J, Nobrega MA, Yokota Y, Berul C, Izumo S, Seidman JG, Seidman CE. A molecular pathway including Id2, Tbx5, and Nkx2-5 required for cardiac conduction system development. Cell. 2007;129:1365–1376. 75. Stennard FA, Harvey RP. T-box transcription factors and their roles in regulatory hierarchies in the developing heart. Development. 2005;132: 4897– 4910. 76. Moskowitz IP, Pizard A, Patel VV, Bruneau BG, Kim JB, Kupershmidt S, Roden D, Berul CI, Seidman CE, Seidman JG. The T-box transcription factor Tbx5 is required for the patterning and maturation of the murine cardiac conduction system. Development. 2004;131:4107– 4116. 77. Ranganayakulu G, Elliott DA, Harvey RP, Olson EN. Divergent roles for NK-2 class homeobox genes in cardiogenesis in flies and mice. Development. 1998;125:3037–3048. 78. Tanaka M, Chen Z, Bartunkova S, Yamasaki N, Izumo S. The cardiac homeobox gene Csx/Nkx2.5 lies genetically upstream of multiple genes essential for heart development. Development. 1999;126:1269 –1280. 79. Jay PY, Harris BS, Maguire CT, Buerger A, Wakimoto H, Tanaka M, Kupershmidt S, Roden DM, Schultheiss TM, O’Brien TX, Gourdie RG, Berul CI, Izumo S. Nkx2-5 mutation causes anatomic hypoplasia of the cardiac conduction system. J Clin Invest. 2004;113:1130 –1137. 80. Wakimoto H, Kasahara H, Maguire CT, Izumo S, Berul CI. Developmentally modulated cardiac conduction failure in transgenic mice with fetal or postnatal overexpression of DNA nonbinding mutant Nkx2.5. J Cardiovasc Electrophysiol. 2002;13:682– 688. 81. Kasahara H, Wakimoto H, Liu M, Maguire CT, Converso KL, Shioi T, Huang WY, Manning WJ, Paul D, Lawitts J, Berul CI, Izumo S. Progressive atrioventricular conduction defects and heart failure in mice expressing a mutant Csx/Nkx2.5 homeoprotein. J Clin Invest. 2001;108: 189 –201. 82. Hsu DT. Cardiac manifestations of neuromuscular disorders in children. Paediatr Respir Rev. 2010;11:35–38. 83. Holaska JM. Emerin and the nuclear lamina in muscle and cardiac disease. Circ Res. 2008;103:16 –23. 84. Arimura T, Helbling-Leclerc A, Massart C, Varnous S, Niel F, Lacene E, Fromes Y, Toussaint M, Mura AM, Keller DI, Amthor H, Isnard R, Malissen M, Schwartz K, Bonne G. Mouse model carrying H222P-Lmna mutation develops muscular dystrophy and dilated cardiomyopathy similar to human striated muscle laminopathies. Hum Mol Genet. 2005;14:155–169. 85. Wolf CM, Wang L, Alcalai R, Pizard A, Burgon PG, Ahmad F, Sherwood M, Branco DM, Wakimoto H, Fishman GI, See V, Stewart CL, Conner DA, Berul CI, Seidman CE, Seidman JG. Lamin A/C haploinsufficiency causes dilated cardiomyopathy and apoptosistriggered cardiac conduction system disease. J Mol Cell Cardiol. 2008; 44:293–303. 86. Fatkin D, MacRae C, Sasaki T, Wolff MR, Porcu M, Frenneaux M, Atherton J, Vidaillet HJ Jr, Spudich S, De Girolami U, Seidman JG, Seidman C, Muntoni F, Muehle G, Johnson W, McDonough B. Missense mutations in the rod domain of the lamin A/C gene as causes of dilated cardiomyopathy and conduction-system disease. N Engl J Med. 1999;341:1715–1724. 87. Mounkes LC, Kozlov SV, Rottman JN, Stewart CL. Expression of an LMNA-N195K variant of A-type lamins results in cardiac conduction defects and death in mice. Hum Mol Genet. 2005;14:2167–2180. 88. Muchir A, Pavlidis P, Decostre V, Herron AJ, Arimura T, Bonne G, Worman HJ. Activation of MAPK pathways links LMNA mutations to cardiomyopathy in Emery-Dreifuss muscular dystrophy. J Clin Invest. 2007;117:1282–1293. 89. Muchir A, Shan J, Bonne G, Lehnart SE, Worman HJ. Inhibition of extracellular signal-regulated kinase signaling to prevent cardiomyopathy caused by mutation in the gene encoding A-type lamins. Hum Mol Genet. 2009;18:241–247. 90. Morgenlander JC, Nohria V, Saba Z. EKG abnormalities in pediatric patients with myotonic dystrophy. Pediatr Neurol. 1993;9:124 –126. 91. Berul CI, Maguire CT, Aronovitz MJ, Greenwood J, Miller C, Gehrmann J, Housman D, Mendelsohn ME, Reddy S. DMPK dosage alterations result in atrioventricular conduction abnormalities in a mouse myotonic dystrophy model. J Clin Invest. 1999;103;R1–R7. 92. Wakimoto H, Maguire CT, Sherwood MC, Vargas MM, Sarkar PS, Han J, Reddy S, Berul CI. Characterization of cardiac conduction system abnormalities in mice with targeted disruption of Six5 gene. J Interv Card Electrophysiol. 2002;7:127–135. 93. Mahadevan MS, Yadava RS, Yu Q, Balijepalli S, Frenzel-McCardell CD, Bourne TD, Phillips LH. Reversible model of RNA toxicity and cardiac conduction defects in myotonic dystrophy. Nat Genet. 2006;38: 1066 –1070. 94. Hardy J, Singleton A. Genomewide association studies and human disease. N Engl J Med. 2009;360:1759 –1768. 95. A haplotype map of the human genome. Nature. 2005;437:1299 –1320. 96. Holm H, Gudbjartsson DF, Arnar DO, Thorleifsson G, Thorgeirsson G, Stefansdottir H, Gudjonsson SA, Jonasdottir A, Mathiesen EB, Njolstad I, Nyrnes A, Wilsgaard T, Hald EM, Hveem K, Stoltenberg C, Lochen ML, Kong A, Thorsteinsdottir U, Stefansson K. Several common variants modulate heart rate, PR interval and QRS duration. Nat Genet. 2010;42:117–122. 97. Pfeufer A, van Noord C, Marciante KD, Arking DE, Larson MG, Smith AV, Tarasov KV, Muller M, Sotoodehnia N, Sinner MF, Verwoert GC, Li M, Kao WH, Kottgen A, Coresh J, Bis JC, Psaty BM, Rice K, Rotter Park and Fishman 98. 99. 100. Downloaded from http://circ.ahajournals.org/ by guest on September 30, 2016 101. JI, Rivadeneira F, Hofman A, Kors JA, Stricker BH, Uitterlinden AG, van Duijn CM, Beckmann BM, Sauter W, Gieger C, Lubitz SA, Newton-Cheh C, Wang TJ, Magnani JW, Schnabel RB, Chung MK, Barnard J, Smith JD, Van Wagoner DR, Vasan RS, Aspelund T, Eiriksdottir G, Harris TB, Launer LJ, Najjar SS, Lakatta E, Schlessinger D, Uda M, Abecasis GR, Muller-Myhsok B, Ehret GB, Boerwinkle E, Chakravarti A, Soliman EZ, Lunetta KL, Perz S, Wichmann HE, Meitinger T, Levy D, Gudnason V, Ellinor PT, Sanna S, Kaab S, Witteman JC, Alonso A, Benjamin EJ, Heckbert SR. Genome-wide association study of PR interval. Nat Genet. 2010;42:153–159. Chambers JC, Zhao J, Terracciano CM, Bezzina CR, Zhang W, Kaba R, Navaratnarajah M, Lotlikar A, Sehmi JS, Kooner MK, Deng G, Siedlecka U, Parasramka S, El-Hamamsy I, Wass MN, Dekker LR, de Jong JS, Sternberg MJ, McKenna W, Severs NJ, de Silva R, Wilde AA, Anand P, Yacoub M, Scott J, Elliott P, Wood JN, Kooner JS. Genetic variation in SCN10A influences cardiac conduction. Nat Genet. 2010; 42:149 –152. Cho HC, Marban E. Biological therapies for cardiac arrhythmias: can genes and cells replace drugs and devices? Circ Res. 2010;106: 674 – 685. Edelberg JM, Aird WC, Rosenberg RD. Enhancement of murine cardiac chronotropy by the molecular transfer of the human beta(2) adrenergic receptor cDNA. J Clin Invest. 1998;101:337–343. Edelberg JM, Huang DT, Josephson ME, Rosenberg RD. Molecular enhancement of porcine cardiac chronotropy. Heart. 2001;86:559 –562. Conduction System Disease 915 102. Miake J, Marban E, Nuss HB. Gene therapy: biological pacemaker created by gene transfer. Nature. 2002;419:132–133. 103. Ruhparwar A, Kallenbach K, Klein G, Bara C, Ghodsizad A, Sigg DC, Karck M, Haverich A, Niehaus M. Adenylate-cyclase VI transforms ventricular cardiomyocytes into biological pacemaker cells. Tissue Eng Part A. 2010;16:1867–1872. 104. Sastry A, Arnold E, Gurji H, Iwasa A, Bui H, Hassankhani A, Patel HH, Feramisco JR, Roth DM, Lai NC, Hammond HK, Narayan SM. Cardiacdirected expression of adenylyl cyclase VI facilitates atrioventricular nodal conduction. J Am Coll Cardiol. 2006;48:559 –565. 105. Qu JH, Plotnikov AN, Danilo P, Shlapakova I, Cohen IS, Robinson RB, Rosen MR. Expression and function of a biological pacemaker in canine heart. Circulation. 2003;107:1106 –1109. 106. Plotnikov AN, Sosunov EA, Qu JH, Shlapakova IN, Anyukhovsky EP, Liu LL, Janse MJ, Brink PR, Cohen IS, Robinson RB, Danilo P, Rosen MR. Biological pacemaker implanted in canine left bundle branch provides ventricular escape rhythms that have physiologically acceptable rates. Circulation. 2004;109:506 –512. 107. Plotnikov AN, Shlapakova I, Szabolcs MJ, Danilo P, Lorell BH, Potapova IA, Lu ZJ, Rosen AB, Mathias RT, Brink PR, Robinson RB, Cohen IS, Rosen MR. Xenografted adult human mesenchymal stem cells provide a platform for sustained biological pacemaker function in canine heart. Circulation. 2007;116:706 –713. KEY WORDS: action potentials 䡲 arrhythmia 䡲 conduction genome-wide association studies 䡲 ion channels 䡲 genetics 䡲 The Cardiac Conduction System David S. Park and Glenn I. Fishman Downloaded from http://circ.ahajournals.org/ by guest on September 30, 2016 Circulation. 2011;123:904-915 doi: 10.1161/CIRCULATIONAHA.110.942284 Circulation is published by the American Heart Association, 7272 Greenville Avenue, Dallas, TX 75231 Copyright © 2011 American Heart Association, Inc. All rights reserved. Print ISSN: 0009-7322. Online ISSN: 1524-4539 The online version of this article, along with updated information and services, is located on the World Wide Web at: http://circ.ahajournals.org/content/123/8/904 Data Supplement (unedited) at: http://circ.ahajournals.org/content/suppl/2013/10/17/123.8.904.DC1.html Permissions: Requests for permissions to reproduce figures, tables, or portions of articles originally published in Circulation can be obtained via RightsLink, a service of the Copyright Clearance Center, not the Editorial Office. Once the online version of the published article for which permission is being requested is located, click Request Permissions in the middle column of the Web page under Services. Further information about this process is available in the Permissions and Rights Question and Answer document. Reprints: Information about reprints can be found online at: http://www.lww.com/reprints Subscriptions: Information about subscribing to Circulation is online at: http://circ.ahajournals.org//subscriptions/ Page 396 Recherche fondamentale et applications cliniques Le système de conduction cardiaque David S. Park, MD, PhD ; Glenn I. Fishman, MD e cœur humain bat 2,5 milliards de fois au cours d’une vie normale, cet exploit étant le fait des cellules du système de conduction cardiaque (SCC). Les éléments fonctionnels qui composent ce dernier se répartissent grossièrement en un ensemble de nœuds d’où naissent les influx électriques et un système assurant leur propagation, le faisceau de HisPurkinje. Le SCC humain peut être l’objet d’atteintes ayant pour effet d’altérer la genèse des influx, leur propagation ou ces deux processus à la fois. Les troubles en question résultent le plus souvent de pathologies acquises telles qu’une ischémie ou un infarctus du myocarde, une dégénérescence liée à l’âge, des complications secondaires à une intervention chirurgicale ou une intoxication médicamenteuse. Rares sont les troubles de la conduction d’origine héréditaire, mais chaque nouvelle mutation qui est découverte présente un intérêt inestimable, car elle permet de mieux cerner les mécanismes moléculaires qui régissent le développement et le fonctionnement du SCC. Grâce à la mise en œuvre d’une approche multidisciplinaire fondée sur le dépistage génétique chez l’Homme, l’analyse biophysique et l’emploi de souris transgéniques, il a été possible d’identifier de très nombreuses familles de gènes ayant pour rôle d’assurer le fonctionnement physiologique normal du SCC (Figure 1). Dans cet article de synthèse, nous examinons les différentes familles de gènes humains qui ont été reconnues comme étant à l’origine de troubles du rythme cardiaque, de blocs de conduction, de voies de conduction accessoires et d’anomalies de développement du SCC (Tableau). Nous nous intéressons également aux stratégies thérapeutiques émergentes qui seraient susceptibles d’être utilisées en complément ou en remplacement des actuels stimulateurs cardiaques implantables. informatiques ont démontré que l’hétérogénéité structurale du NS est nécessaire au maintien aussi bien de l’automaticité physiologique que de la conduction de l’influx électrique.28–30 L’automaticité du rythme cardiaque est commandée par un processus de dépolarisation diastolique spontanée de phase 4, qui dépolarise la membrane cellulaire pour l’amener au potentiel seuil donnant naissance aux potentiels d’action rythmiques. Selon l’actuelle conception de l’automaticité du NS, celle-ci reposerait sur deux horloges fonctionnant conjointement, « l’horloge de voltage membranaire » et « l’horloge calcique ». La première est générée par le déséquilibre net entre le déclin des courants potassiques sortants (Iκ) et l’activation des courants entrants, qui comprennent, entre autres, le courant de fond sensible au sodium (Ib Na), les courants calciques de types L et T (ICa,L, ICa,T), le courant entrant prolongé (Ist) et le courant activé par l’hyperpolarisation (If) (Figure 2).27,31–33 L’horloge calcique sous-sarcolemmique induit la dépolarisation diastolique du NS en commandant la libération spontanée et rythmique d’ions Ca2+ à partir du réticulum sarcoplasmique (RS) par mise en jeu des récepteurs à la ryanodine de type 2 (RYR2).34 L’élévation locale du taux de calcium intracellulaire (Cai) conduit le courant échangeur de sodium et de calcium (INCX) à substituer 1 ion Ca2+ intracellulaire à 3 ions Na+ extracellulaires. L’augmentation nette de la charge positive qui en résulte entraîne la dépolarisation de la membrane.35 L’élévation de la concentration intracellulaire en Ca2+ se produit au cours du dernier tiers de la dépolarisation diastolique et est sensible à la stimulation bêta-adrénergique.36 Des mutations ont été identifiées chez l’Homme, qui, parce qu’elles perturbent l’horloge de voltage membranaire (SCN5A et HCN4), l’horloge calcique (RYR2 et CASQ2) ou les deux à la fois (ANKB), altèrent le fonctionnement du nœud sinusal.37,38 L Les troubles de l’automaticité Le nœud sinusal (NS) humain est une structure intramurale en forme de croissant dont la tête est située en position sous-épicardique à la jonction entre l’oreillette droite et la veine cave supérieure et dont la queue s’étend sur 10 à 20 mm le long de la crista terminalis.26 Les tissus formant le NS présentent une architecture tridimensionnelle complexe, dont les composantes cellulaires centrales et périphériques expriment des canaux ioniques et des jonctions communicantes de types distincts.27 Ces cellules diffèrent également par les potentiels d’action qu’elles génèrent et par leurs propriétés de conduction (Figure 2).27 Des modèles expérimentaux et SCN5A SCN5A code pour le canal sodique cardiaque (Nav1.5) qui donne naissance au courant sodique rapide INa. Nav1.5 régit l’amplitude et la pente de la phase 0 du potentiel d’action cardiaque et influe par là même sur la vitesse de conduction. Plus de 200 mutations de SCN5A sont d’ores et déjà répertoriées, lesquelles sont responsables de divers troubles cardiaques, comprenant le syndrome du QT long de type 3, le syndrome de Brugada, le trouble progressif de la conduction Service de Cardiologie Leon H. Charney, Faculté de Médecine de l’Université de New York, New York, New York, Etats-Unis. Correspondance : Glenn I. Fishman, MD, Leon H. Charney Division of Cardiology, New York University School of Medicine, 522 First Ave, Smilow 801, New York, NY 10016, Etats-Unis. E-mail : [email protected] (Traduit de l’anglais : The Cardiac Conduction System. Circulation. 2011;123:904–915.) © 2011 Lippincott, Williams & Wilkins Circulation est disponible sur http://circ.ahajournals.org 396 12:42:12:10:11 Page 396 Page 397 Park et Fishman Les troubles de la conduction cardiaque 397 Figure 1. Cellule du système de conduction cardiaque. Sont mentionnés les gènes identifiés comme étant responsables d’altérations de ce système chez l’Homme. Figure 2. Hétérogénéité électrophysiologique du nœud sinusal (NS). La portion centrale du NS, qui constitue le principal centre rythmogène, est électriquement isolée du myocarde auriculaire hyperpolarisant du fait de la différence d’expression des connexines et des canaux ioniques. Les cellules périphériques du NS se situent à un niveau électrophysiologique intermédiaire entre les cellules centrales et les cardiomyocytes atriaux. RS : réticulum sarcoplasmique. cardiaque et la maladie du sinus (MS) congénitale. A ce jour, 14 mutations de SCN5A ont été identifiées comme impliquées dans le développement de formes héréditaires de MS.27,39 Benson et al1 ont identifié 6 mutations de SCN5A chez 3 membres d’une même famille qui étaient atteints de MS congénitale. Ces derniers présentaient une hétérozygotie composite à l’égard des 6 allèles de SCN5A (G1408R+P1298L, T220I+R1623X, delF1617+R1632H). L’étude biophysique a montré que 2 de ces 6 mutations entraînaient une perte de fonction des canaux alors que T220I, P1298L et delF1617 avaient pour effets de diminuer la densité du courant INa et de 12:42:12:10:11 Page 397 provoquer un déplacement de la courbe d’inactivation voltage-dépendante dans le sens d’une hyperpolarisation. Smits et al40 ont, par ailleurs, découvert une nouvelle mutation de SCN5A, E161K, chez deux individus appartenant à la même famille et qui présentaient une dysfonction symptomatique du nœud sinusal, un trouble généralisé de la conduction et un syndrome de Brugada. En employant la technique de la micropipette (patch clamp) sur cellule entière, ces auteurs ont mis en évidence une diminution de la densité du courant INa à un niveau 3 fois inférieur à la normale et un déplacement positif de la courbe d’activation voltage-dépendante. Page 398 398 Circulation Tableau 12:42:12:10:11 Novembre 2011 Fondements génétiques des troubles affectant le système de conduction Page 398 Page 399 Park et Fishman Le déplacement négatif de l’inactivation voltage-dépendante et le déplacement positif de l’activation voltage-dépendante ont tous deux pour effet de réduire la fenêtre du courant INa. SCN5A est exprimé par les cellules périphériques du NS, mais ne l’est pas par les cellules centrales, qui sont les principales structures génératrices de l’influx électrique (Figure 2). En ayant recours à une simulation informatique, Butters et al41 ont proposé un mécanisme visant à expliquer comment les mutations de SCN5A exprimées par les cellules de la portion périphérique du NS perturbent l’automaticité des cellules centrales. Ces auteurs ont introduit des mutants de SCN5A (T220I, P1298L, delF1617 et E161K) dans des modèles unicellulaires et dans un modèle bidimensionnel d’oreillette de lapin comportant un NS intact. Les simulations effectuées sur les modèles unicellulaires ont montré que les mutants de SCN5A diminuent la fréquence de décharge des cellules périphériques mais n’ont quasiment aucune influence sur les cellules nodales centrales. En revanche, les simulations réalisées sur des tissus intacts ont révélé que ces mêmes mutants ralentissent le rythme des décharges au sein des cellules centrales du NS. L’oreillette impose au NS une importante charge hyperpolarisante qui est contrebalancée par l’expression de SCN5A dans les cellules périphériques.41–43 De ce fait, la diminution du courant INa dans ces dernières contraint les cellules centrales à décharger davantage de potentiels hyperpolarisés, ce qui ralentit la fréquence des impulsions. De plus, une altération de la conduction des potentiels d’action a été objectivée au sein des préparations oreillette-NS, laquelle prédispose au développement d’un bloc sinusal de sortie, couramment observé dans les MS familiales.41 HCN4 Le courant rythmogène If, auquel a été donné le nom de funny current (le « drôle de courant »), est produit par les canaux cationiques contrôlés par les nucléotides cycliques (HCN). L’appellation de funny current trouve son origine dans les caractéristiques particulières de ces canaux, qui résident dans leur perméabilité à l’égard des ions K+ et Na+, dans leur activation lors de l’hyperpolarisation du potentiel de membrane et dans leur modulation par l’AMPc. Du fait de leurs propriétés biophysiques, les canaux HCN sont idéalement conçus pour jouer le rôle de modulateurs du potentiel rythmogène. Premièrement, parce qu’ils sont activés à la phase d’hyperpolarisation du potentiel membranaire (c’est-à-dire entre –65 et –40 mV), leur lent courant entrant contribue à la dépolarisation diastolique ; deuxièmement, le principal canal HCN cardiaque (HCN4) est sensible à l’AMPc, ce qui permet au courant If d’être modulé par les stimuli neurovégétatifs.44,45 Des mutations d’HCN4, l’isoforme qui prédomine au niveau du NS, ont été identifiées chez des patients atteints de MS.32,45 En employant une stratégie fondée sur les gènes candidats, Schulze-Bahr et al12 ont mis en évidence une délétion mononucléotidique affectant HCN4 (1631delC) chez un patient présentant une bradycardie sinusale couplée à une incompétence chronotrope. Le mutant 1631delC est dépourvu du domaine de liaison des nucléotides cycliques, ce qui le rend insensible à l’AMPc. D’autres mutations d’HCN4 ont 12:42:12:10:11 Page 399 Les troubles de la conduction cardiaque 399 été identifiées dans 2 familles dont des membres étaient atteints de bradycardie sinusale asymptomatique. Les 2 mutations faux-sens, S672R et G480R, contribuaient à ce que l’activation des canaux se produise pour de plus hauts niveaux d’hyperpolarisation, de sorte que la densité des courants générés pendant la dépolarisation diastolique était diminuée.13,14 Les travaux menés sur des modèles animaux dépourvus de canaux HCN ont permis d’éclairer le rôle joué par ces derniers dans la génération du courant If. Chez la souris, la perte d’HCN4 entraîne une mort embryonnaire entre E10,5 et E11,5 ainsi qu’un trouble de la maturation des cardio–– myocytes. Chez l’embryon de souris HCN4 / , ces cellules se caractérisent à la fois par une diminution de 85 % du courant If et par une insensibilité chronotrope à l’AMPc.46,47 Pour étudier les effets de l’abolition de l’expression d’HCN4 chez la souris adulte, des investigateurs ont créé des modèles de souris inductibles par le tamoxifène.48,49 La délétion d’HCN4 dans les cellules du NS s’est traduite par une réduction de 75 % de la densité du courant If. Les souris ainsi traitées ont présenté, non pas une bradycardie sinusale, mais des pauses sinusales d’une durée ayant atteint jusqu’à 300 à 500 ms. Le chronotropisme a également été préservé. Les cellules sinusales de ces –– animaux HCN4 / conservaient leur automaticité normale ; toutefois, les potentiels diastoliques tendaient à atteindre des niveaux qui sont ceux de l’hyperpolarisation et auxquels toute activité rythmogène spontanée est abolie. Considérées dans leur globalité, ces observations conduisent à penser que le gène HCN4 est indispensable au développement et au chronotropisme du NS au cours de l’embryogenèse, mais que, à l’âge adulte, il pourrait ne jouer qu’un rôle de renfort consistant à contrecarrer l’hyperpolarisation membranaire des cellules du NS.47–49 Ces données sont en accord avec le phénotype de bradycardie bénigne mis en évidence par Milanesi et al13 et par Nof et al14 dans 2 familles porteuses de mutations d’HCN4. La conservation de la compétence chronotrope dans les modèles humains et expérimentaux de délétion d’HCN4 est en faveur de l’existence d’autres mécanismes régissant l’automaticité du NS et sa réponse aux stimuli sympathiques. La première démonstration de l’implication de Cai dans la dépolarisation diastolique a été apportée par Rubenstein et Lipsius50 lorsque ces derniers ont montré que, chez le chat, l’administration de ryanodine ralentit l’automaticité des structures rythmogènes subsidiaires situées dans l’oreillette droite. Un lien mécaniste a, par la suite, été établi par Huser et al34 entre Cai et la dépolarisation diastolique du NS, ces auteurs ayant émis l’hypothèse selon laquelle les efflux sous-sarcolemmiques transitoires de Ca2+ libérés par le RS (c’est-à-dire les « étincelles calciques ») provoqueraient l’activation de l’échangeur Na+-Ca2+ (NCX), cela entraînant la dépolarisation de la membrane. Bogdanov et al35 ont confirmé l’existence de ce mécanisme au sein de cellules nodales isolées de lapin et ont montré que les étincelles calciques contribuent directement la dépolarisation diastolique tardive par l’intermédiaire du NCX. Vinogradova et al36,51 ont ensuite montré que, chez le lapin, le renforcement bêta-adrénergique du chronotropisme est tributaire de la libération d’ions Ca2+ par le RS, car le traitement par Page 400 400 Circulation Novembre 2011 la ryanodine a pour effet d’émousser l’effet stimulant exercé par l’isoprotérénol sur la fréquence des décharges. Dans un récent travail, Joung et al38 ont étudié l’effet de la stimulation adrénergique sur des préparations de NS canin intact en ayant recours à une double cartographie optique du potentiel transmembranaire (Vm) et de Cai. Ces auteurs ont ainsi constaté que la stimulation adrénergique majore fortement l’augmentation télédiastolique de Cai ainsi que son degré de déviation, ces modifications survenant toutes deux au niveau du principal site rythmogène. RYR2 et CASQ2 Il est, dès lors, intéressant que les mutations des gènes qui codent pour les protéines régissant les mouvements du calcium au sein du RS soient responsables d’une dysfonction du nœud sinusal. La bradycardie sinusale est une manifestation courante de la tachycardie ventriculaire polymorphe catécholaminergique (TVPC), trouble du rythme héréditaire qui se caractérise par le développement d’une tachycardie ventriculaire bidirectionnelle ou polymorphe en réponse à un stress adrénergique et ce, en l’absence de toute cardiopathie structurale. Deux gènes responsables de TVPC ont été identifiés chez l’Homme ; il s’agit des gènes codant respectivement pour le récepteur cardiaque à la ryanodine (RYR2) et pour la calséquestrine cardiaque (CASQ2). Le récepteur cardiaque à la ryanodine est le principal canal par lequel est libéré le calcium issu du RS des cardiomyocytes. La calséquestrine, qui est la première protéine de stockage du calcium dans le RS, forme un complexe avec RYR2. Les mutations affectant ces protéines altèrent le processus de libération du calcium à partir du RS, ce qui entraîne un efflux spontané d’ions Ca2+ sous l’action des catécholamines, avec pour conséquences un retard à la postdépolarisation et une activité déclenchée.52,53 Postma et al16 ont décelé 13 mutations faux-sens de RYR2 dans 12 familles à TVPC. Ces familles totalisaient 54 membres porteurs d’une de ces mutations, qui présentaient tous une bradycardie sinusale de repos en l’absence de traitement médicamenteux. Il a récemment été décrit une forme de TVPC caractérisée par une amplification des manifestations de cardiomyopathie dilatée, de dysfonction du nœud sinusal, de bloc auriculo-ventriculaire progressif, de fibrillation auriculaire et de paralysie auriculaire. En procédant à une analyse de liaison génétique et à une réaction de polymérisation en chaîne « long range » (amplification de grands fragments d’ADN), il a été possible de mettre en évidence une délétion génomique encadrée intéressant l’exon 3 de RYR2.15 La bradycardie sinusale est également une manifestation caractéristique des TVPC liées à une mutation de CASQ2. Postma et al ont ainsi identifié 3 mutations non-sens de ce gène (une mutation non-sens R33X, une mutation d’épissage 532+1 G>A et une délétion d’une paire de bases, 62delA) chez 3 membres de la même famille qui étaient atteints de TVPC ; tous trois présentaient une bradycardie sinusale sur le tracé électrocardiographique initial.17 Le lien observé entre la bradycardie sinusale et les mutations affectant les gènes codant pour les protéines de transport du calcium au sein du RS conforte un peu plus l’hypothèse selon laquelle l’horloge calcique jouerait un rôle dans la conduction sino-auriculaire ; 12:42:12:10:11 Page 400 d’autres études seront toutefois nécessaires pour préciser le mécanisme de la dysfonction sinusale dans les TVPC. ANKB Les mutations du gène codant pour l’ankyrine B (ANKB) sont responsables de syndromes du QT long de type 454 et de formes familiales de maladie du sinus.21 L’ANKB est indispensable à un ancrage correct des canaux ioniques et des transporteurs aux domaines membranaires correspondants. Les souris présentant une haplo-insuffisance du gène ANKB (AnkB+/–) développent une bradycardie sinusale marquée et une variabilité de la fréquence cardiaque de repos. L’analyse biochimique a révélé que l’un des échangeurs sodium-calcium (NCX1), la Na/K-ATPase (NKA), le récepteur IP3 (IP3R) et Cav1.3 présentaient tous une expression diminuée ainsi qu’un trouble de leur ancrage. Chez ces souris AnkB+/–, il a également été mis en évidence d’importantes diminution de densité des courants ICa,L et INCX au sein des cellules sinusales.21 Il apparaît donc que la dysfonction du NS engendrée par les mutations d’ANKB résulte très vraisemblablement de la réduction des courants ioniques intervenant dans les deux types d’horloges décrits plus haut. Les blocs de conduction Un bloc de conduction peut se produire à n’importe quel niveau du SCC sous la forme d’un bloc de sortie sino-auriculaire, d’un bloc auriculo-ventriculaire, d’un bloc infra-hissien ou d’un bloc de branche. Le trouble de la conduction peut être dû à l’altération d’un canal ionique ayant pour effet de modifier le profil des potentiels d’action ou à une anomalie de couplage entre les cardiomyocytes. Les troubles de la conduction cardiaque à caractère héréditaires résultent de mutations de SCN5A et SCN1B (qui affectent toutes deux la phase 0) ou de KCNJ2 (qui altère les phases 3 et 4). Les canaux sodiques cardiaques sont constitués d’une sousunité α formant le pore de ces derniers (et qui est codée par SCN5A) et d’une sous-unité β modulatrice (codée par SCN1B). La sous-unité α renferme un détecteur de voltage qui permet l’activation rapide du canal en réponse à la dépolarisation de la membrane. Une fois celle-ci intervenue, le canal sodique connaît une période d’inactivation, pendant laquelle il est réfractaire aux autres décharges. La repolarisation de la membrane est nécessaire à SCN5A pour que celui-ci mette fin à l’état d’inactivité du canal. Le canal potassique à rectification entrante, Kir2.1, qui est codé par KCNJ2, assure le maintien du potentiel membranaire basal. L’excitabilité cardiaque normale n’est donc possible que si Nav1.5 et Kir2.1 fonctionnent de façon correcte. SCN5A Le trouble progressif de la conduction cardiaque, ou maladie de Lev-Lenègre, résulte d’une dégénérescence fibroscléreuse du faisceau de His-Purkinje liée à l’âge.6 La propagation des influx électriques au sein du système de conduction ventriculaire proximal diminue progressivement, ce qui provoque des blocs de branche puis un bloc auriculoventriculaire complet. Certaines mutations avec perte de Page 401 Park et Fishman fonction de SCN5A sont à l’origine d’une forme héréditaire de la maladie de Lev-Lenègre qui peut être isolée ou coexister avec un syndrome de Brugada ou un syndrome du QT long de type 3.6 Le trouble familial progressif de la conduction cardiaque sous-tend un risque élevé de bloc auriculoventriculaire complet et de syncope d’Adams-Stokes sans dysrythmie ventriculaire.7 Schott et al8 ont identifié une mutation de SCN5A héritée conjointement à la maladie de Lenègre dans une vaste famille française. Les individus atteints présentaient des troubles de la conduction de degré variable, ayant nécessité l’implantation d’un stimulateur cardiaque chez 4 d’entre eux en raison d’épisodes syncopaux ou d’un bloc cardiaque complet. L’analyse de liaison génétique et le séquençage du gène candidat ont permis de mettre en évidence une substitution T>C en position +2 du site d’épissage donneur de l’intron 22 (IVS22+2 T>C), laquelle aboutit à un mutant dépourvu du segment sensible au voltage.8 L’analyse fonctionnelle a montré qu’aucun courant sodique entrant transitoire n’était généré en réponse à la dépolarisation, ce qui est en faveur d’une mutation avec « perte de fonction ».6 SCN1B Les patients atteints d’un syndrome de Brugada et d’un trouble de la conduction sont pour la plupart indemnes de mutation de SCN5A. C’est pourquoi les stratégies de séquençage des gènes candidats sont aujourd’hui centrées sur les modificateurs de l’expression ou de la fonction de Nav1.5. Watanabe et al9 ont ainsi découvert des mutations de SCN1B dans 3 familles présentant des troubles de la conduction associés ou non à un syndrome de Brugada. Chez ces individus, l’expression des sous-unités β mutantes conjointement à celle de Nav1.5 avait pour effet de diminuer la densité du courant sodique. KCNJ2 Des mutations de KCNJ2 ont été mises en évidence dans une affection autosomique dominante rare appelée syndrome d’Andersen-Tawil, qui associe une paralysie périodique, des anomalies morphologiques, une tachycardie ventriculaire polymorphe et un trouble de la conduction cardiaque.10,11 Les analyses électrocardiographiques pratiquées chez 96 sujets atteints de ce syndrome et qui appartenaient à 33 groupes familiaux distincts ont objectivé des altérations de la conduction intéressant différents étages depuis le nœud auriculoventriculaire jusqu’au système de conduction distal.55 Dans les cardiomyocytes exprimant une sous-unité dominante négative de Kir2.1, la densité du courant Iκ1 était diminuée de 95 %, ce qui avait pour effet d’allonger notablement la durée des potentiels d’action. L’utilisation de modèles murins de syndrome d’Andersen-Tawil a montré que cette affection entraîne une diminution de la fréquence cardiaque et un ralentissement important de la conduction.56,57 Les anomalies des voies de conduction accessoires Le syndrome de Wolff-Parkinson-White (WPW) est dû à la pré-excitation du myocarde ventriculaire par l’intermédiaire 12:42:12:10:11 Page 401 Les troubles de la conduction cardiaque 401 d’une voie de conduction supplémentaire (le faisceau de Kent) qui court-circuite la voie de conduction lente physiologique passant par le nœud auriculo-ventriculaire. Une telle pré-excitation ventriculaire est fréquente, la prévalence du trouble variant de 1,5 à 3 cas pour 1 000.22,58 L’examen histologique de faisceaux de Kent prélevés chez des sujets humains a révélé que ces derniers étaient constitués de myocytes ventriculaires d’aspect normal exprimant la connexine 43 (Cx43).59 L’expression de jonctions communicantes à haute conductance permet à ces voies accessoires de pré-exciter le myocarde ventriculaire, cela se traduisant sur le tracé électrocardiographique par des espaces PR raccourcis et par des complexes QRS empâtés, liés à l’existence d’une « onde delta ». Le syndrome de WPW est un trouble essentiellement sporadique dont le mécanisme sous-jacent demeure inconnu ; toutefois, de rares formes héréditaires ont été décrites. Selon Vidaillet et al,60 3,4 % des propositus atteints d’un tel syndrome auraient au moins un parent au premier degré présentant une voie de conduction accessoire. PRKAG2 Une forme héréditaire de syndrome de WPW transmise sur le mode autosomique dominant a été diagnostiquée dans 2 familles. Trente et un individus atteints de l’affection présentaient des signes de pré-excitation et d’hypertrophie cardiaque. Il a été décelé une mutation faux-sens de PRKAG2 à l’origine d’une forme constitutivement active de la sousunité régulatrice γ2 de la protéine kinase activée par l’AMP.22,23 Dans les conditions normales, cette enzyme a pour fonction de corriger les états de déplétion énergétique en augmentant la captation du glucose et en stimulant la glycolyse. Les souris transgéniques qui expriment PRKAG2N488I, un mutant spécifiquement cardiaque doté d’activité constitutive, reproduisent le phénotype du syndrome de WPW humain, marqué par l’existence d’une hypertrophie cardiaque, d’une pré-excitation et de troubles de la conduction. La principale anomalie histologique consiste en une surcharge vacuolaire en glycogène des myocytes ventriculaires. Le phénotype de pré-excitation découle de la rupture de l’anneau fibreux sous l’action de ces myocytes ventriculaires vacuolisés.61 En employant un modèle murin d’anomalie réversible du stockage du glycogène, Wolf et al62 ont démontré que la cardiomyopathie et la dégénérescence du SCC observées chez la souris exprimant PRKAG2N488I sont des processus réversibles. BMP2 Lalani et al24 ont décrit une nouvelle forme de syndrome de WPW résultant de la microdélétion de la région codant pour la protéine morphogénétique osseuse (PMO) de type 2 (Bmp2) au sein de 20p12.3 et qui se caractérise par la présence de déficits cognitifs variables et de troubles morphologiques. Les PMO appartiennent à la superfamille des facteurs de croissance transformants β et jouent un rôle essentiel dans le développement cardiaque. Chez la souris, la délétion cardiaque du gène codant pour le récepteur à la PMO de type 1a (Bmpr1a) entraîne une mort embryonnaire avant E18,5 du fait du défaut de développement des tissus myocardiques trabéculaire et compact, du septum interventriculaire et des Page 402 402 Circulation Novembre 2011 bourrelets endocardiques.63 Une délétion plus restreinte de Bmpr1a au niveau du canal atrio-ventriculaire provoque une malformation de la valve auriculo-ventriculaire et un défaut de maturation de l’anneau fibreux, responsable, là encore, d’un phénomène de pré-excitation.64,65 Les troubles du développement du SCC Les cardiopathies congénitales sont les plus fréquentes des affections présentes à la naissance, touchant 1 à 2 % des nouveau-nés.66 Les troubles du rythme peuvent être la conséquence d’anomalies de la spécification et/ou de la structuration du SCC, d’une malformation ou d’un refoulement des voies de conduction, d’altérations hémodynamiques, d’une hypoxie prolongée ou de séquelles postopératoires.67,68 Sur le plan embryologique, le système de conduction est issu des précurseurs cellulaires myocardiques présents dans le cœur fœtal.69–71 C’est l’expression régionale de facteurs de transcription qui régit le processus conduisant ces cellules à se différencier en une lignée destinée à assurer la conduction cardiaque plutôt qu’en des cardiomyocytes.69–74 Les principaux facteurs de transcription identifiés à ce jour comme intervenant dans le développement du SCC humain sont les facteurs à boîte T et à boîte homéotique. TBX5 Le syndrome de Holt-Oram est une affection autosomique dominante caractérisée par des anomalies préaxiales du rayon radial (malformations du radius, des os du carpe et/ou des pouces) et par des troubles de la septation cardiaque. Les anomalies septales consistent le plus souvent en des communications inter-auriculaires de type ostium secundum, des communications inter-ventriculaires de type musculaire et des malformations du canal atrio-ventriculaire. Les patients atteints de ce syndrome présentent des troubles de la conduction cardiaque de degré variable, tels qu’une bradycardie sinusale ou un bloc auriculo-ventriculaire, cela même en l’absence de cardiopathie structurale manifeste. En 1997, Basson et al18 ont effectué un dépistage génétique au sein de 2 familles sujettes au syndrome de Holt-Oram et ont ainsi mis en évidence la présence de mutations intéressant TBX5, un facteur de transcription à boîte T. Ce type de facteur, qui peut se comporter en tant qu’activateur ou répresseur transcriptionnel, joue un rôle majeur de régulation de la spécification et de la différenciation cardiaques. Sept membres de la famille des TBX sont exprimés dans le cœur en cours de développement, dont 3 (TBX1, TBX5, TBX20) se sont révélés impliqués dans les cardiopathies congénitales humaines.75 Chez la souris, la délétion de Tbx5 se solde par une mort embryonnaire à E10,5, causée par l’arrêt du développement des oreillettes et du ventricule gauche. Les souris Tbx5+/– reproduisent les malformations des membres supérieurs et les anomalies cardiaques du syndrome de Holt-Oram décrit chez l’Homme, y compris les troubles de la conduction.72,76 Ces animaux présentent notamment d’importantes anomalies de maturation du canal atrio-ventriculaire et du système de conduction intraventriculaire.76 Moskowitz et al76 ont démontré qu’il existe, chez ces souris, un défaut de maturation du canal atrio-ventriculaire qui se manifeste par la persistance d’anneaux auriculo-ventriculaires autour des valves tricuspide 12:42:12:10:11 Page 402 et mitrale. Des anomalies de structuration ont été mises en évidence au niveau du faisceau de His et de ses branches, pouvant parfois aller jusqu’à une absence totale de formation du rameau droit. L’expression spécifique, au sein du SCC, des marqueurs tels que le facteur natriurétique auriculaire (FNA) et la Cx40, est, en outre, fortement déprimée, ce qui désigne TBX5 comme un activateur transcriptionnel de ces gènes. Il a, par ailleurs, été établi que TBX5 et le facteur de transcription à boîte homéotique NK3C2–5 agissent en synergie pour stimuler l’expression du FNA et de la Cx40.76 NKX2–5 NKX2–5, qui appartient à la famille des homéodomaines, joue un rôle clé dans l’induction et le maintien du SCC. Les membres de cette famille partagent tous la même séquence conservée de liaison à l’ADN constituée de 60 acides aminés à laquelle a été donné le nom de boîte homéotique. Ces facteurs de transcription sont indispensables à l’organogenèse, car ils contrôlent la spécification et la différenciation des tissus. Chez la drosophile, la délétion du gène tinman1, qui est l’homologue de Nkx2–5, provoque l’arrêt de la cardiogenèse.77 Le rôle de NKX2–5 dans le développement du SCC humain a été établi à la suite de la découverte de mutations du gène correspondant au sein de 4 familles dont des membres étaient atteints de cardiopathie congénitale non syndromique et de bloc de la conduction auriculoventriculaire.19 L’étude généalogique était en faveur d’un mode de transmission autosomique dominant et l’anomalie structurale la plus fréquente était une communication inter-auriculaire de type ostium secundum. Les autres malformations cardiaques étaient à type de communication interventriculaire, de tétralogies de Fallot, d’atrésie de l’artère pulmonaire, de valve mitrale surnuméraire, d’hypertrophie ventriculaire gauche et de rétrécissement aortique sous-valvulaire.19 Les enregistrements électrocardiographiques ont révélé l’existence de troubles de la conduction auriculo-ventriculaire qui n’étaient pas strictement tributaires de la cardiopathie structurale sous-jacente. L’implantation d’un stimulateur cardiaque a été nécessaire chez quatorze individus. L’analyse de liaison pan-génomique et le séquençage du gène candidat ont permis d’identifier 3 mutations de NKX2–5.19 A ce jour, plus de 60 substitutions mononucléotidiques intéressant Nkx2–5 ont été répertoriées chez des patients atteints de cardiopathies congénitales, ce qui démontre le rôle majeur que joue ce gène dans la cardiogenèse et dans la spécification et le maintien du SCC. Les souris privées de Nkx2–5 meurent in utero à E9–10, car le développement de leur cœur s’arrête au stade du tube cardiaque linéaire. Chez ces animaux, la formation de la boucle cardiaque est incomplète, les bourrelets et les trabécules endocardiques font défaut et le canal atrioventriculaire est atrophique.78 Jay et al79 ont fait état d’une absence complète de cellules primordiales du nœud auriculoventriculaire dans un autre modèle de délétion de Nkx2–5 (Nkx2–5neo/neo), faisant appel à la combinaison minK-LacZ, une lignée de souris rapporteuses qui marque le NS, le nœud auriculo-ventriculaire et la portion proximale du système de 1 « L’homme de fer blanc », du nom d’un personnage du roman Le Magicien d’Oz (N.d.T.) Page 403 Park et Fishman conduction intra-ventriculaire. Les souris hétérozygotes à l’égard de Nkx2–5 présentent une diminution globale de la taille de leur SCC depuis le nœud auriculo-ventriculaire jusqu’au réseau de Purkinje distal. L’examen histologique du nœud auriculo-ventriculaire de souris Nkx2–5+/neo a révélé que les cellules nodales compactes (région N) qui sont Cx40–/Cx45+ font clairement défaut, alors que la région nodo-hissienne, qui est Cx40+/Cx45+, demeure intacte.79 L’immunocoloration de la Cx40 a, par ailleurs, montré que la densité des fibres de Purkinje est diminuée.79 Les enregistrements électrocardiographiques de surface pratiqués sur ces souris Nkx2–5+/neo ont mis en évidence un allongement de la durée des espaces PR et des complexes QRS. Les électrogrammes cardiaques ont, en outre, montré que la dépolarisation du faisceau de His était de très faible amplitude, ce qui était en accord avec la taille réduite de cette structure, et qu’il existait un allongement aussi bien des délais auriculo-ventriculaires 1/1 et 2/1 que des périodes réfractaires efficaces au niveau du nœud auriculo-ventriculaire, ce qui était en faveur d’une dysfonction de celui-ci. Les délais de conduction hissio-ventriculaires n’étaient, en revanche, pas modifiés, sans doute parce que l’expression de Cx40 demeurait suffisante. Les similitudes entre les altérations du nœud auriculo-ventriculaire respectivement observées chez l’Homme et chez la souris dans un contexte d’haploinsuffisance de Nkx2–5 portent à considérer que le rôle joué par NKX2–5 dans l’induction et le maintien du SCC est une constante chez les mammifères.79–81 On sait aujourd’hui que, chez la souris, NKX2–5, TBX5 et l’inhibiteur de la différenciation de type 2 (Id2) agissent de conserve sous forme d’un transcriptome pour induire le développement du système de conduction intraventriculaire.74 L’expression conjointe de NKX2–5 et de TBX5 au cours de la formation de ce dernier a pour effet de limiter l’expression régionale de l’Id2, du FNA et de la Cx40. Il semblerait que l’Id2 fonctionne comme un inhibiteur de la différenciation musculaire, orientant celle-ci vers une lignée cellulaire conductive.74 L’haplo-insuffisance combinée de Nkx2–5 et de Tbx5 (Nkx2–5+/–ITbx5+/–) entraîne un défaut de développement des voies de conduction intra-ventriculaires, marqué par une absence totale du faisceau de His et de ses branches. L’abolition des marqueurs du SCC tels que la Cx40 du fait de mutations cardiaques se traduit par un important élargissement des complexes QRS sur l’ECG de surface.74 A ce jour, il n’a pas encore été découvert de correspondance humaine à l’hétérozygotie combinée de Nkx2–5 et de Tbx5. Les troubles de la conduction associés aux maladies neuromusculaires Les affections neuromusculaires forment un ensemble hétérogène de pathologies qui comportent très souvent une composante cardiaque. Il a été identifié un certain nombre de mutations intéressant les gènes qui régissent le cytosquelette, l’enveloppe nucléaire et la fonction mitochondriale. La composante cardiaque revêt généralement la forme d’une cardiomyopathie dilatée ou hypertrophique, d’anomalies de la conduction auriculo-ventriculaire et de troubles du rythme auriculaire et ventriculaire.82 12:42:12:10:11 Page 403 Les troubles de la conduction cardiaque 403 EMD et LMNA Les mutations qui affectent l’enveloppe nucléaire sont à l’origine d’importantes altérations du SCC. La membrane interne de l’enveloppe nucléaire est une structure hautement organisée, composée de protéines membranaires intrinsèques et de protéines du cytosquelette nucléaire qui participent conjointement à l’organisation supérieure de la chromatine et à la régulation de la transcription. Les lamines (A, B et C) sont des éléments essentiels du réseau de filaments intermédiaires qui confère sa rigidité structurale à la membrane nucléaire interne. L’émérine, qui appartient à la famille des protéines nucléaires associées aux lamines, est supposée avoir pour rôle de commander l’ancrage de la chromatine au cytosquelette. Les mutations affectant le gène de l’émérine (EMD) provoquent une dystrophie musculaire d’EmeryDreifuss liée à l’X, alors que celles qui influent sur les lamines A/C (LMNA) induisent une forme autosomique dominante de cette même maladie.20 Les sujets atteints d’une dystrophie musculaire d’Emery-Dreifuss présentent une atrophie progressive de leurs muscles squelettiques au cours de leurs dix premières années de vie, puis une atteinte cardiaque (cardiomyopathie dilatée et bloc auriculo-ventriculaire) au cours des années qui suivent.82,83 Arimura et al84 ont créé un modèle de dystrophie musculaire d’Emery-Dreifuss autosomique dominante en inoculant à des souris une mutation faux-sens du gène Lmna (H222P) précédemment découverte dans une famille atteinte de cette maladie dans sa forme typique. Ce modèle a fidèlement reproduit le phénotype humain, les souris LmnaH222P/H222P ayant développé les troubles moteurs, la cardiomyopathie dilatée et les anomalies du SCC caractéristiques de la maladie. L’analyse télémétrique des souris mutantes a mis en évidence un allongement des espaces PR et un élargissement des complexes QRS. Le même type d’altération du SCC a été observé chez des souris présentant une haplo-insuffisance du gène Lmna. Ces souris Lmna+/– présentaient une bradycardie sinusale et un bloc auriculoventriculaire de degré variable. L’examen histologique de ces animaux a mis en évidence une déformation nucléaire et une apoptose des cellules du nœud auriculo-ventriculaire.85 Une autre lignée murine conçue pour exprimer la mutation LmnaN195K, dont on sait que, chez l’Homme, elle provoque une cardiomyopathie dilatée autosomique dominante avec trouble de la conduction,86 a développé un bloc auriculo-ventriculaire de haut degré et un bloc cardiaque complet. L’analyse biochimique a montré que, dans les tissus auriculaires mutants, l’expression des Cx40 et Cx43 était diminuée et leur localisation incorrecte.87 La coloration par la desmine a également mis en évidence des anomalies structurales du sarcomère et des disques intercalaires.87 L’analyse de l’expression pan-génomique au sein du cœur de souris LmnaH222P a, par ailleurs, objectivé un net renforcement des voies de signalisation de la protéine-kinase activée par les mitogènes (MAPK).88 L’hyperactivation de ces voies est source de cardiomyopathie et d’altération du SCC. Dans les cœurs de ces souris mutantes, il a été décelé une forte augmentation des formes activées de 2 MAPK, JNK et ERK1/2, qui a précédé l’apparition d’une cardiomyopathie clinique ou à traduction moléculaire.88 Le traitement des Page 404 404 Circulation Novembre 2011 souris LmnaH222P par un inhibiteur de la phosphorylation d’ERK a aboli l’élévation des marqueurs biologiques de cardiomyopathie et ramené la fraction d’éjection à un niveau normal. Ces observations permettent d’établir un lien direct entre l’hyperactivation des MAPK et le phénotype cardiomyopathique chez la souris LmnaH222P.89 En se fondant sur les phénotypes de ces modèles murins, il est permis de penser que la lamine A/C assure le maintien de l’intégrité fonctionnelle du SCC de 2 façons : (1) en protégeant le noyau des contraintes mécaniques et (2) en maintenant l’organisation correcte de la chromatine pour permettre l’expression appropriée des gènes, comme cela est notamment le cas pour l’expression des connexines et la signalisation des MAPK.83 DMPK La dystrophie myotonique de type 1 (DM1), ou maladie de Steinert, est la plus fréquente des dystrophies musculaires de l’adulte et se manifeste par une myotonie, une insulinorésistance, une fonte musculaire progressive, une cataracte et des troubles de la conduction cardiaque.25 Ces derniers, qui sont présents chez 70 % des patients atteints de DM1, peuvent consister en une bradycardie sinusale, un bloc auriculoventriculaire de degré variable ou un retard à la conduction intra-ventriculaire.90 La mutation génétique à l’origine de la DM1 est une expansion en n exemplaires du triplet CTG dans la région 3’ non traduite (R3’NT) du gène DMPK (pour Dystrophy Myotonic Protein Kinase). Trois mécanismes moléculaires ont été avancés pour expliquer le rôle joué par les répétitions de ce triplet nucléotidique dans le développement des anomalies de la conduction cardiaque associées à la DM1 : (1) l’haplo-insuffisance de DMPK,91 (2) la sousexpression du gène Six5 codant pour l’homéodomaine adjacent92 et (3) l’accumulation toxique d’ARN mutant.93 Le piégeage nucléaire de cet ARN toxique provoque la séquestration et la dysfonction des protéines de liaison à l’ARN, dont celles qui, telle la famille muscleblind-like (MBL1), interviennent dans l’épissage de ce dernier.93 En vue d’établir le rôle physiopathologique joué par la R3’NT de DMPK dans le phénotype de DM1, Mahadevan et al93 ont créé une souris transgénique exprimant un transcript inductible codant pour cette région avec marquage par une protéine générant une fluorescence verte. Ces investigateurs ont ainsi constaté que la surexpression de la R3’NT du gène DMPK de type sauvage suffit à induire les manifestations caractéristiques de la DM1, dont la myotonie, les anomalies d’épissage et l’altération du SCC. Cette observation a conduit les auteurs à supposer que la surexpression transgénique d’une R3’NT de DMPK de type sauvage comportant seulement 5 répétitions du triplet CUG était peut-être l’équivalent molaire pathogénique de la R3’NT mutante dans laquelle ce triplet était répété plusieurs centaines de fois. L’induction du transgène a, dans un premier temps, entraîné un allongement des espaces PR qui a ensuite évolué vers un bloc cardiaque complet dont la sanction a été une mort subite d’origine cardiaque. Elément intéressant à noter, l’arrêt de la substance inductrice, la doxycycline, a été suivi de la disparition de la myotonie et de certaines des anomalies de la conduction. Les blocs cardiaques du premier degré engendrés 12:42:12:10:11 Page 404 chez l’animal se sont révélés réversibles ; tel n’a toutefois pas été le cas des blocs auriculo-ventriculaires qui se situaient au-delà du deuxième degré. Orientations futures L’analyse de liaison couplée à un clonage positionnel s’est révélée être un moyen extrêmement efficace de déceler les mutations génétiques au sein des familles à maladies monogéniques. Cette stratégie a déjà permis d’identifier plus d’un millier de gènes, dont ceux décrits dans le présent article. Depuis le séquençage du génome humain, l’espoir se concrétise de pouvoir un jour découvrir les fondements génétiques des affections complexes à caractère multifactoriel. Avec le développement des études d’associations pan-génomiques, un pas important a été franchi dans cette direction.94 Ce type d’étude consiste à rechercher le lien existant entre une maladie et les marqueurs génétiques présents dans la totalité du génome. La technique repose sur le fait que la variance dans un locus donné est hautement prédictive de celle prévalant dans un locus adjacent du fait du déséquilibre de liaison. En d’autres termes, il y a co-ségrégation non aléatoire d’une série de marqueurs génétiques qui sont proches les uns des autres au sein du génome. Ce groupement de marqueurs liés entre eux forme ce que l’on appelle l’haplotype. La première étude visant à établir la structure des haplotypes, menée dans 4 populations différentes (Yorubas, habitants du Nord et de l’Ouest de l’Europe, Chinois et Japonais), a été publiée dans Nature en 2005 par le consortium international HapMap. Ce travail a montré que les différents marqueurs génétiques (ou polymorphismes mononucléotidiques) sont prédictifs des marqueurs adjacents et ce, avec une résolution généralement de l’ordre de 30 000 paires de bases. Sachant que le génome humain compte environ 3x109 paires de bases, les auteurs de l’étude ont estimé que moins de 500 000 polymorphismes mononucléotidiques étaient nécessaires pour identifier l’intégralité des variants génétiques courants présents dans le génome.94,95 Les études d’associations pan-génomiques sont aujourd’hui utilisées pour identifier les mutations génétiques qui influent sur les paramètres électrocardiographiques dans différentes populations. Deux raisons ont conduit à employer les paramètres intermédiaires tels que la fréquence cardiaque ou la durée de l’espace PR comme marqueurs substitutifs de maladie : (1) ils sont corrélés avec la morbidité cardiovasculaire et la fibrillation auriculaire ; (2) ils présentent des liens plus étroits avec les variants génétiques qu’avec la maladie elle-même. Holm et al96 ont identifié plusieurs associations pan-génomiques en retenant pour seuil une valeur p inférieure à 1,6x10-9. Ces auteurs ont découvert qu’un locus hébergeant MYH6 influait sur la fréquence cardiaque, que 4 loci (TBX5, SCN10A, CAV1 et ARHGAP24) étaient associés à la durée des espaces PR et que 4 (TBX5, SCN10A, 6p21 et 10q21) étaient impliqués dans la durée des complexes QRS. Ils ont donc poursuivi ces études d’associations chez des sujets islandais et norvégiens qui présentaient différents types de troubles du rythme cardiaque. Ils ont ainsi objectivé des corrélations entre la fibrillation auriculaire et les mutations TBX5 et CAV1 (respectivement, p = 4,0x10-5 et p = 0,00032), Page 405 Park et Fishman entre le bloc auriculo-ventriculaire avancé et TBX5 (p = 0,0067) et entre la pose d’un stimulateur cardiaque et SCN10A (p = 0,0029). Des loci similaires ont été mis en évidence par 2 autres études d’associations pan-génomiques menées par des équipes distinctes dans une population européenne et parmi des habitants du sous-continent indien. Pfeufer et al97 ont fait état de 9 loci hautement associés à la durée des espaces PR (p <5x10-8) à l’issue d’une méta-analyse du consortium CHARGE ayant porté sur plus de 28 000 sujets européens. L’un de ces loci était corrélé avec 2 canaux sodiques (SCN10A et SCN5A) et 6 autres étaient situés à proximité de gènes impliqués dans le développement cardiaque (CAV1-CAV2, NKX2–5, SOX5, WNT11, ME1S1 et TBX5-TBX3). Parmi tous ces loci, SCN10A, SCN5A, CAV1-CAV2, NKX2–5 et SOX5 se sont révélés impliqués dans la fibrillation auriculaire. Chambers et al98 ont également fait état d’un lien entre SCN10A et la durée des espaces PR chez 6 543 habitants du sous-continent indien. L’examen physiologique de souris privées de Scn10a a mis en évidence, chez ces animaux, un raccourcissement des espaces PR ne s’accompagnant d’aucune autre anomalie notable des paramètres électrocardiographiques et échocardiographiques. Grâce aux études d’associations pan-génomiques, de nouvelles familles de gènes impliqués dans les troubles de la conduction et du rythme cardiaque chez l’Homme sont en passe d’être découvertes. L’identification de SCN10A effectuée par 3 équipes indépendantes dans des populations différentes confirme la fidélité de cette approche. Des études devront toutefois être menées pour valider l’impact de ces associations. Au-delà de la mise en évidence de nouvelles cibles génétiques, cette technique devrait également permettre de découvrir de nouvelles associations avec des régions non codantes et d’identifier, au sein de ces dernières, des modificateurs épigénétiques et des régulateurs transcriptionnels et translationnels, tels que des micro-ARN, encore inconnus à ce jour. Stratégies thérapeutiques Le mode actuel de prise en charge des bradycardies symptomatiques liées à un trouble du SCC réside dans l’implantation d’un stimulateur cardiaque électronique. En dépit de leur grande utilité, ces appareils présentent un certain nombre d’inconvénients, qu’il s’agisse des complications liées aux sondes, de la durée de vie limitée des batteries, du risque infectieux, de l’insensibilité aux stimuli neurovégétatifs ou des contraintes en matière de volume de l’appareil dans le cas d’un enfant. Ces inconvénients ont conduit à concevoir des stimulateurs cardiaques biologiques dont la fonction de restauration de l’activité rythmogène est assurée au moyen de systèmes de transfert génique utilisant comme vecteurs des virus ou des cellules souches.99 C’est l’identification et la caractérisation des gènes impliqués dans la production des courants de stimulation cardiaque qui ont permis à cette technologie de devenir une réalité. La restauration du rythme sinusal peut être réalisée en modulant les courants entrants et sortants de manière à rétablir ou augmenter la pente de la dépolarisation diastolique au sein des tissus cardiaques. En renforçant les courants 12:42:12:10:11 Page 405 Les troubles de la conduction cardiaque 405 entrants et/ou en diminuant les courants sortants, on augmente ladite pente et, par là même, le rythme de stimulation. Les gènes qui ont été étudiés ou qui font actuellement l’objet de recherches sont les suivants : (1) le récepteur β2-adrénergique,100,101 (2) les mutants Kir2.1 dominants négatifs,102 (3) l’adényl cyclase de type VI (ACVI)103,104 et (4) les canaux contrôlés par les nucléotides cycliques (HCN).105 Le récepteur β2-adrénergique et l’adényl cyclase de type VI augmentent tous deux les taux d’AMPc, ce qui provoque l’activation des canaux HCN endogènes ainsi que des mécanismes régissant l’horloge calcique. Bien que les études préliminaires menées avec les récepteurs β2-adrénergiques sur des modèles animaux aient fourni des résultats encourageants en termes d’augmentation transitoire de la fréquence cardiaque, cette approche n’offre qu’un intérêt limité en raison du risque de trouble du rythme qu’elle génère et de son incapacité à induire une activité rythmogène de novo.101 Une autre stratégie a consisté à modifier les courants ioniques ayant pour effet de transformer les cardiomyocytes, qui ont des potentiels diastoliques relativement stables, en cellules présentant une dépolarisation diastolique de phase 4. L’hypothèse a été émise selon laquelle les myocytes auriculaires et ventriculaires seraient potentiellement doués d’automaticité, mais que les courants hyperpolarisants tels qu’Iκ1 empêcheraient leur dépolarisation diastolique en stabilisant le potentiel membranaire de repos. Miake et al102 ont confirmé cette théorie en démontrant que l’introduction d’un construct de Kir2.1 dominant négatif au moyen d’un vecteur adénoviral dans le ventricule gauche de cobayes provoque la transformation des myocytes passifs en cellules rythmogènes. Malheureusement, l’allongement conséquent des potentiels d’action qui en résulte rend cette stratégie thérapeutique d’un intérêt clinique limité.102 Rosen et al105,106 ont montré qu’il est possible de transformer des cardiomyocytes passifs en cellules douées d’automaticité en induisant l’expression hétérologue des canaux HCN qui produisent le courant de stimulation cardiaque If. Qu et Plotnikov et al ont, par ailleurs, réussi à générer des rythmes autonomes stables en inoculant à des chiens un adénovirus codant pour HCN2, respectivement, dans l’oreillette gauche105 et dans la branche gauche du faisceau de His.106 Pour surmonter les écueils liés à l’utilisation de vecteurs viraux, dont la réaction immunitaire induite chez l’hôte, plusieurs équipes ont expérimenté avec succès des systèmes faisant appel à des vecteurs cellulaires. Plotnikov et al107 ont ainsi fait état de l’implantation fructueuse de cellules souches mésenchymateuses humaines exprimant HCN2 dans le ventricule gauche de chiens chez lesquels un bloc auriculo-ventriculaire avait été préalablement induit. Ces animaux ont présenté une activité rythmogène ectopique stable pendant plus de 6 semaines sans qu’il ait été nécessaire de les soumettre à un traitement immunosuppresseur.107 Toutefois, étant donné que les cellules souches mésenchymateuses humaines se lient électriquement au tissu myocardique hôte par l’intermédiaire des jonctions communicantes, tout processus pathologique susceptible d’engendrer un important remodelage de ces structures peut obérer l’efficacité de cette approche. Page 406 406 Circulation Novembre 2011 S’il y a vraisemblablement lieu d’attendre encore longtemps avant que les stimulateurs cardiaques biologiques deviennent auto-suffisants, utilisés sur un mode de recours, ils peuvent d’ores et déjà être d’une réelle utilité pour pallier les inconvénients des actuels stimulateurs électroniques, notamment la durée de vie limitée des batteries et l’infection du matériel. C’est ainsi que, chez les patients porteurs de stimulateurs cardiaques, il est possible d’employer des préparations biologiques destinées à prolonger la durée de vie de la batterie, de manière à réduire la fréquence de remplacement du générateur. L’injection d’une telle préparation biologique fonctionnant comme un stimulateur cardiaque peut également être pratiquée à titre de traitement temporaire après le retrait des sondes d’un appareil électronique infecté. Le besoin de stimulateurs cardiaques biologiques auxiliaires est aujourd’hui évident, mais, avant que cette technologie devienne une réalité, il faudra encore améliorer les systèmes d’inoculation par vecteurs géniques ou cellulaires.99 Conclusion En dépit de leur rareté, les troubles du rythme cardiaque à caractère héréditaire sont devenus un précieux instrument d’exploration des fondements génétiques du fonctionnement du SCC. Chaque nouvelle mutation découverte nous permet de mieux cerner la complexité des éléments biochimiques et structuraux qui président à la genèse et à la propagation des influx cardiaques. Cette approche méthodologique est toutefois entravée par le nombre relativement réduit des affections héréditaires ayant un retentissement sur le SCC. L’avènement des études d’associations pan-génomiques a permis d’étendre la recherche de nouveaux gènes des maladies familiales rares aux affections multifactorielles communes. Il est à espérer que cette nouvelle voie d’investigation passionnante permettra de percer les interactions complexes qui s’opèrent entre gènes et modificateurs génétiques et épigénétiques, lesquelles conditionnent la prévalence des maladies courantes. A terme, ces études génétiques devraient permettre d’identifier une kyrielle de gènes qui constitueront autant de nouvelles cibles des traitements pharmacologiques et des thérapies géniques de demain. Remerciements Nous présentons nos excuses aux nombreux investigateurs dont nous n’avons pu citer les travaux par manque de place. Sources de financement Les travaux menés par le laboratoire du Dr Fishman sont financés par des bourses des National Institutes of Health des Etats-Unis (HL64757, HL081336 et HL82727) ainsi que par un Prix STEM (pour Science, Technology, Engineering and Math) de l’Etat de New York (décerné au Dr Fishman) et par une bourse de la Heart Rhythm Foundation des Etats-Unis (allouée au Dr Park). Déclarations Néant. Références 1. Benson DW, Wang DW, Dyment M, Knilans TK, Fish FA, Strieper MJ, Rhodes TH, George AL Jr. Congenital sick sinus syndrome caused by recessive mutations in the cardiac sodium channel gene (SCN5A). J Clin Invest. 2003;112:1019–1028. 12:42:12:10:11 Page 406 2. Makiyama T, Akao M, Tsuji K, Doi T, Ohno S, Takenaka K, Kobori A, Ninomiya T, Yoshida H, Takano M, Makita N, Yanagisawa F, Higashi Y, Takeyama Y, Kita T, Horie M. High risk for bradyarrhythmic complications in patients with Brugada syndrome caused by SCN5A gene mutations. J Am Coll Cardiol. 2005;46:2100–2106. 3. Groenewegen WA, Firouzi M, Bezzina CR, Vliex S, van Langen IM, Sandkuijl L, Smits JP, Hulsbeek M, Rook MB, Jongsma HJ, Wilde AA. A cardiac sodium channel mutation cosegregates with a rare connexin40 genotype in familial atrial standstill. Circ Res. 2003;92:14–22. 4. Veldkamp MW, Wilders R, Baartscheer A, Zegers JG, Bezzina CR, Wilde AA. Contribution of sodium channel mutations to bradycardia and sinus node dysfunction in LQT3 families. Circ Res. 2003;92:976–983. 5. Probst V, Allouis M, Sacher F, Pattier S, Babuty D, Mabo P, Mansourati J, Victor J, Nguyen JM, Schott JJ, Boisseau P, Escande D, Le Marec H. Progressive cardiac conduction defect is the prevailing phenotype in carriers of a Brugada syndrome SCN5A mutation. J Cardiovasc Electrophysiol. 2006;17:270–275. 6. Probst V, Kyndt F, Potet F, Trochu JN, Mialet G, Demolombe S, Schott JJ, Baro I, Escande D, Le Marec H. Haploinsufficiency in combination with aging causes SCN5A-linked hereditary Lenegre disease. J Am Coll Cardiol. 2003;41:643–652. 7. Kyndt F, Probst V, Potet F, Demolombe S, Chevallier JC, Baro I, Moisan JP, Boisseau P, Schott JJ, Escande D, Le Marec H. Novel SCN5A mutation leading either to isolated cardiac conduction defect or Brugada syndrome in a large French family. Circulation. 2001;104: 3081–3086. 8. Schott JJ, Alshinawi C, Kyndt F, Probst V, Hoorntje TM, Hulsbeek M, Wilde AA, Escande D, Mannens MM, Le Marec H. Cardiac conduction defects associate with mutations in SCN5A. Nat Genet. 1999;23:20–21. 9. Watanabe H, Koopmann TT, Le Scouarnec S, Yang T, Ingram CR, Schott JJ, Demolombe S, Probst V, Anselme F, Escande D, Wiesfeld AC, Pfeufer A, Kaab S, Wichmann HE, Hasdemir C, Aizawa Y, Wilde AA, Roden DM, Bezzina CR. Sodium channel beta1 subunit mutations associated with Brugada syndrome and cardiac conduction disease in humans. J Clin Invest. 2008;118:2260–2268. 10. Andelfinger G, Tapper AR, Welch RC, Vanoye CG, George AL Jr, Benson DW. KCNJ2 mutation results in Andersen syndrome with sexspecific cardiac and skeletal muscle phenotypes. Am J Hum Genet. 2002;71:663–668. 11. Plaster NM, Tawil R, Tristani-Firouzi M, Canun S, Bendahhou S, Tsunoda A, Donaldson MR, Iannaccone ST, Brunt E, Barohn R, Clark J, Deymeer F, George AL Jr, Fish FA, Hahn A, Nitu A, Ozdemir C, Serdaroglu P, Subramony SH, Wolfe G, Fu YH, Ptacek LJ. Mutations in Kir2.1 cause the developmental and episodic electrical phenotypes of Andersen’s syndrome. Cell. 2001;105:511–519. 12. Schulze-Bahr E, Neu A, Friederich P, Kaupp UB, Breithardt G, Pongs O, Isbrandt D. Pacemaker channel dysfunction in a patient with sinus node disease. J Clin Invest. 2003;111:1537–1545. 13. Milanesi R, Baruscotti M, Gnecchi-Ruscone T, DiFrancesco D. Familial sinus bradycardia associated with a mutation in the cardiac pacemaker channel. N Engl J Med. 2006;354:151–157. 14. Nof E, Luria D, Brass D, Marek D, Lahat H, Reznik-Wolf H, Pras E, Dascal N, Eldar M, Glikson M. Point mutation in the HCN4 cardiac ion channel pore affecting synthesis, trafficking, and functional expression is associated with familial asymptomatic sinus bradycardia. Circulation. 2007;116:463–470. 15. Bhuiyan ZA, van den Berg MP, van Tintelen JP, Bink-Boelkens MT, Wiesfeld AC, Alders M, Postma AV, van Langen I, Mannens MM, Wilde AA. Expanding spectrum of human RYR2-related disease: new electrocardiographic, structural, and genetic features. Circulation. 2007;116: 1569–1576. 16. Postma AV, Denjoy I, Kamblock J, Alders M, Lupoglazoff JM, Vaksmann G, Dubosq-Bidot L, Sebillon P, Mannens MM, Guicheney P, Wilde AA. Catecholaminergic polymorphic ventricular tachycardia: RYR2 mutations, bradycardia, and follow up of the patients. J Med Genet. 2005;42:863–870. 17. Postma AV, Denjoy I, Hoorntje TM, Lupoglazoff JM, Da Costa A, Sebillon P, Mannens MM, Wilde AA, Guicheney P. Absence of calsequestrin 2 causes severe forms of catecholaminergic polymorphic ventricular tachycardia. Circ Res. 2002;91;e21–e26. 18. Basson CT, Bachinsky DR, Lin RC, Levi T, Elkins JA, Soults J, Grayzel D, Kroumpouzou E, Traill TA, Leblanc-Straceski J, Renault B, Kucherlapati R, Seidman JG, Seidman CE. Mutations in human TBX5 Page 407 Park et Fishman 19. 20. 21. 22. 23. 24. 25. 26. 27. 28. 29. 30. 31. 32. 33. 34. 35. 36. 37. 12:42:12:10:11 [corrected] cause limb and cardiac malformation in Holt-Oram syndrome. Nat Genet. 1997;15:30–35. Schott JJ, Benson DW, Basson CT, Pease W, Silberbach GM, Moak JP, Maron BJ, Seidman CE, Seidman JG. Congenital heart disease caused by mutations in the transcription factor NKX2–5. Science. 1998;281: 108–111. Bonne G, Di Barletta MR, Varnous S, Becane HM, Hammouda EH, Merlini L, Muntoni F, Greenberg CR, Gary F, Urtizberea JA, Duboc D, Fardeau M, Toniolo D, Schwartz K. Mutations in the gene encoding lamin A/C cause autosomal dominant Emery-Dreifuss muscular dystrophy. Nat Genet. 1999;21:285–288. Le Scouarnec S, Bhasin N, Vieyres C, Hund TJ, Cunha SR, Koval O, Marionneau C, Chen B, Wu Y, Demolombe S, Song LS, Le Marec H, Probst V, Schott JJ, Anderson ME, Mohler PJ. Dysfunction in ankyrinB-dependent ion channel and transporter targeting causes human sinus node disease. Proc Natl Acad Sci U S A. 2008;105:15617–15622. Gollob MH, Green MS, Tang AS, Gollob T, Karibe A, Ali Hassan AS, Ahmad F, Lozado R, Shah G, Fananapazir L, Bachinski LL, Roberts R. Identification of a gene responsible for familial Wolff-Parkinson-White syndrome. N Engl J Med. 2001;344:1823–1831. Arad M, Benson DW, Perez-Atayde AR, McKenna WJ, Sparks EA, Kanter RJ, McGarry K, Seidman JG, Seidman CE. Constitutively active AMP kinase mutations cause glycogen storage disease mimicking hypertrophic cardiomyopathy. J Clin Invest. 2002;109:357–362. Lalani SR, Thakuria JV, Cox GF, Wang X, Bi W, Bray MS, Shaw C, Cheung SW, Chinault AC, Boggs BA, Ou Z, Brundage EK, Lupski JR, Gentile J, Waisbren S, Pursley A, Ma L, Khajavi M, Zapata G, Friedman R, Kim JJ, Towbin JA, Stankiewicz P, Schnittger S, Hansmann I, Ai T, Sood S, Wehrens XH, Martin JF, Belmont JW, Potocki L. 20p12.3 Microdeletion predisposes to Wolff-Parkinson-White syndrome with variable neurocognitive deficits. J Med Genet. 2009;46:168–175. Mahadevan M, Tsilfidis C, Sabourin L, Shutler G, Amemiya C, Jansen G, Neville C, Narang M, Barcelo J, O’Hoy K, Leblond S, EarleMacdonald J, De Jong PJ, Wieringa B, Korneluk RG. Myotonic dystrophy mutation: an unstable CTG repeat in the 3′ untranslated region of the gene. Science. 1992;255:1253–1255. Anderson KR, Ho SY, Anderson RH. Location and vascular supply of sinus node in human heart. Br Heart J. 1979;41:28–32. Lei M, Zhang H, Grace AA, Huang CL. SCN5A and sinoatrial node pacemaker function. Cardiovasc Res. 2007;74:356–365. Lei M, Jones SA, Liu J, Lancaster MK, Fung SS, Dobrzynski H, Camelliti P, Maier SK, Noble D, Boyett MR. Requirement of neuronaland cardiac-type sodium channels for murine sinoatrial node pacemaking. J Physiol. 2004;559:835–848. Zhang H, Holden AV, Kodama I, Honjo H, Lei M, Varghese T, Boyett MR. Mathematical models of action potentials in the periphery and center of the rabbit sinoatrial node. Am J Physiol. 2000;279;H397–H421. Dobrzynski H, Li J, Tellez J, Greener ID, Nikolski VP, Wright SE, Parson SH, Jones SA, Lancaster MK, Yamamoto M, Honjo H, Takagishi Y, Kodama I, Efimov IR, Billeter R, Boyett MR. Computer threedimensional reconstruction of the sinoatrial node. Circulation. 2005;111:846–854. Liu J, Noble PJ, Xiao G, Abdelrahman M, Dobrzynski H, Boyett MR, Lei M, Noble D. Role of pacemaking current in cardiac nodes: insights from a comparative study of sinoatrial node and atrioventricular node. Prog Biophys Mol Biol. 2008;96:294–304. Liu J, Dobrzynski H, Yanni J, Boyett MR, Lei M. Organisation of the mouse sinoatrial node: structure and expression of HCN channels. Cardiovasc Res. 2007;73:729–738. Chen PS, Joung B, Shinohara T, Das M, Chen Z, Lin SF. The initiation of the heart beat. Circ J. 2010;74:221–225. Huser J, Blatter LA, Lipsius SL. Intracellular Ca2+ release contributes to automaticity in cat atrial pacemaker cells. J Physiol. 2000;524 (pt 2);415–422. Bogdanov KY, Vinogradova TM, Lakatta EG. Sinoatrial nodal cell ryanodine receptor and Na(+)-Ca(2+) exchanger: molecular partners in pacemaker regulation. Circ Res. 2001;88:1254–1258. Vinogradova TM, Bogdanov KY, Lakatta EG. β-Adrenergic stimulation modulates ryanodine receptor Ca(2+) release during diastolic depolarization to accelerate pacemaker activity in rabbit sinoatrial nodal cells. Circ Res. 2002;90:73–79. Lakatta EG, Maltsev VA, Vinogradova TM. A coupled SYSTEM of intracellular Ca2+ clocks and surface membrane voltage clocks controls Page 407 38. 39. 40. 41. 42. 43. 44. 45. 46. 47. 48. 49. 50. 51. 52. 53. 54. 55. 56. 57. Les troubles de la conduction cardiaque 407 the timekeeping mechanism of the heart’s pacemaker. Circ Res. 2010;106:659–673. Joung B, Ogawa M, Lin SF, Chen PS. The calcium and voltage clocks in sinoatrial node automaticity. Korean Circ J. 2009;39:217–222. Ruan Y, Liu N, Priori SG. Sodium channel mutations and arrhythmias. Nat Rev Cardiol. 2009;6:337–348. Smits JP, Koopmann TT, Wilders R, Veldkamp MW, Opthof T, Bhuiyan ZA, Mannens MM, Balser JR, Tan HL, Bezzina CR, Wilde AA. A mutation in the human cardiac sodium channel (E161K) contributes to sick sinus syndrome, conduction disease and Brugada syndrome in two families. J Mol Cell Cardiol. 2005;38:969–981. Butters TD, Aslanidi OV, Inada S, Boyett MR, Hancox JC, Lei M, Zhang H. Mechanistic links between Na+ channel (SCN5A) mutations and impaired cardiac pacemaking in sick sinus syndrome. Circ Res. 2010;107:126–137. Verheijck EE, van Kempen MJ, Veereschild M, Lurvink J, Jongsma HJ, Bouman LN. Electrophysiological features of the mouse sinoatrial node in relation to connexin distribution. Cardiovasc Res. 2001;52: 40–50. Fedorov VV, Schuessler RB, Hemphill M, Ambrosi CM, Chang R, Voloshina AS, Brown K, Hucker WJ, Efimov IR. Structural and functional evidence for discrete exit pathways that connect the canine sinoatrial node and atria. Circ Res. 2009;104:915–923. Herrmann S, Stieber J, Ludwig A. Pathophysiology of HCN channels. Pflugers Arch. 2007;454:517–522. Biel M, Wahl-Schott C, Michalakis S, Zong X. Hyperpolarizationactivated cation channels: from genes to function. Physiol Rev. 2009;89:847–885. Stieber J, Herrmann S, Feil S, Loster J, Feil R, Biel M, Hofmann F, Ludwig A. The hyperpolarization-activated channel HCN4 is required for the generation of pacemaker action potentials in the embryonic heart. Proc Natl Acad Sci U S A. 2003;100:15235–15240. Ludwig A, Herrmann S, Hoesl E, Stieber J. Mouse models for studying pacemaker channel function and sinus node arrhythmia. Prog Biophys Mol Biol. 2008;98:179–185. Herrmann S, Stieber J, Stockl G, Hofmann F, Ludwig A. HCN4 provides a ‘depolarization reserve’ and is not required for heart rate acceleration in mice. EMBO J. 2007;26:4423–4432. Hoesl E, Stieber J, Herrmann S, Feil S, Tybl E, Hofmann F, Feil R, Ludwig A. Tamoxifen-inducible gene deletion in the cardiac conduction system. J Mol Cell Cardiol. 2008;45:62–69. Rubenstein DS, Lipsius SL. Mechanisms of automaticity in subsidiary pacemakers from cat right atrium. Circ Res. 1989;64:648–657. Ju YK, Allen DG. How does beta-adrenergic stimulation increase the heart rate? The role of intracellular Ca2+ release in amphibian pacemaker cells. J Physiol. 1999;516(pt 3);793–804. Rizzi N, Liu N, Napolitano C, Nori A, Turcato F, Colombi B, Bicciato S, Arcelli D, Spedito A, Scelsi M, Villani L, Esposito G, Boncompagni S, Protasi F, Volpe P, Priori SG. Unexpected structural and functional consequences of the R33Q homozygous mutation in cardiac calsequestrin: a complex arrhythmogenic cascade in a knock in mouse model. Circ Res. 2008;103:298–306. Liu N, Colombi B, Memmi M, Zissimopoulos S, Rizzi N, Negri S, Imbriani M, Napolitano C, Lai FA, Priori SG. Arrhythmogenesis in catecholaminergic polymorphic ventricular tachycardia: insights from a RyR2 R4496C knock-in mouse model. Circ Res. 2006;99:292–298. Mohler PJ, Schott JJ, Gramolini AO, Dilly KW, Guatimosim S, duBell WH, Song LS, Haurogne K, Kyndt F, Ali ME, Rogers TB, Lederer WJ, Escande D, Le Marec H, Bennett V. Ankyrin-B mutation causes type 4 long-QT cardiac arrhythmia and sudden cardiac death. Nature. 2003;421:634–639. Zhang L, Benson DW, Tristani-Firouzi M, Ptacek LJ, Tawil R, Schwartz PJ, George AL, Horie M, Andelfinger G, Snow GL, Fu YH, Ackerman MJ, Vincent GM. Electrocardiographic features in Andersen-Tawil syndrome patients with KCNJ2 mutations: characteristic T-U-wave patterns predict the KCNJ2 genotype. Circulation. 2005;111:2720–2726. Zaritsky JJ, Redell JB, Tempel BL, Schwarz TL. The consequences of disrupting cardiac inwardly rectifying K(+) current (I(K1)) as revealed by the targeted deletion of the murine Kir2.1 and Kir2.2 genes. J Physiol. 2001;533:697–710. McLerie M, Lopatin AN. Dominant-negative suppression of I(K1) in the mouse heart leads to altered cardiac excitability. J Mol Cell Cardiol. 2003;35:367–378. Page 408 408 Circulation Novembre 2011 58. Light PE. Familial Wolff-Parkinson-White syndrome: a disease of glycogen storage or ion channel dysfunction? J Cardiovasc Electrophysiol. 2006;17(suppl 1):S158–S161. 59. Peters NS, Rowland E, Bennett JG, Green CR, Anderson RH, Severs NJ. The Wolff-Parkinson-White syndrome: the cellular substrate for conduction in the accessory atrioventricular pathway. Eur Heart J. 1994;15:981–987. 60. Vidaillet HJ Jr, Pressley JC, Henke E, Harrell FE Jr, German LD. Familial occurrence of accessory atrioventricular pathways (preexcitation syndrome). N Engl J Med. 1987;317:65–69. 61. Arad M, Moskowitz IP, Patel VV, Ahmad F, Perez-Atayde AR, Sawyer DB, Walter M, Li GH, Burgon PG, Maguire CT, Stapleton D, Schmitt JP, Guo XX, Pizard A, Kupershmidt S, Roden DM, Berul CI, Seidman CE, Seidman JG. Transgenic mice overexpressing mutant PRKAG2 define the cause of Wolff-Parkinson-White syndrome in glycogen storage cardiomyopathy. Circulation. 2003;107:2850–2856. 62. Wolf CM, Arad M, Ahmad F, Sanbe A, Bernstein SA, Toka O, Konno T, Morley G, Robbins J, Seidman JG, Seidman CE, Berul CI. Reversibility of PRKAG2 glycogen-storage cardiomyopathy and electrophysiological manifestations. Circulation. 2008;117:144–154. 63. Gaussin V, Van de Putte T, Mishina Y, Hanks MC, Zwijsen A, Huylebroeck D, Behringer RR, Schneider MD. Endocardial cushion and myocardial defects after cardiac myocyte-specific conditional deletion of the bone morphogenetic protein receptor ALK3. Proc Natl Acad Sci U S A. 2002;99:2878–2883. 64. Stroud DM, Gaussin V, Burch JB, Yu C, Mishina Y, Schneider MD, Fishman GI, Morley GE. Abnormal conduction and morphology in the atrioventricular node of mice with atrioventricular canal targeted deletion of Alk3/Bmpr1a receptor. Circulation. 2007;116:2535–2543. 65. Gaussin V, Morley GE, Cox L, Zwijsen A, Vance KM, Emile L, Tian Y, Liu J, Hong C, Myers D, Conway SJ, Depre C, Mishina Y, Behringer RR, Hanks MC, Schneider MD, Huylebroeck D, Fishman GI, Burch JB, Vatner SF. Alk3/Bmpr1a receptor is required for development of the atrioventricular canal into valves and annulus fibrosus. Circ Res. 2005;97:219–226. 66. Hoffman JI, Kaplan S. The incidence of congenital heart disease. J Am Coll Cardiol. 2002;39:1890–1900. 67. Walsh SR, Tang T, Wijewardena C, Yarham SI, Boyle JR, Gaunt ME. Postoperative arrhythmias in general surgical patients. Ann R Coll Surg Engl. 2007;89:91–95. 68. Walsh EP, Cecchin F. Arrhythmias in adult patients with congenital heart disease. Circulation. 2007;115:534–545. 69. Gourdie RG, Mima T, Thompson RP, Mikawa T. Terminal diversification of the myocyte lineage generates Purkinje fibers of the cardiac conduction system. Development. 1995;121:1423–1431. 70. Cheng G, Litchenberg WH, Cole GJ, Mikawa T, Thompson RP, Gourdie RG. Development of the cardiac conduction system involves recruitment within a multipotent cardiomyogenic lineage. Development. 1999;126:5041–5049. 71. Moorman AF, Christoffels VM. Development of the cardiac conduction system: a matter of chamber development. Novartis Found Symp. 2003;250:25–34; discussion 34–43, 276–279. 72. Bruneau BG, Nemer G, Schmitt JP, Charron F, Robitaille L, Caron S, Conner DA, Gessler M, Nemer M, Seidman CE, Seidman JG. A murine model of Holt-Oram syndrome defines roles of the T-box transcription factor Tbx5 in cardiogenesis and disease. Cell. 2001;106:709–721. 73. Christoffels VM, Smits GJ, Kispert A, Moorman AF. Development of the pacemaker tissues of the heart. Circ Res. 2010;106:240–254. 74. Moskowitz IP, Kim JB, Moore ML, Wolf CM, Peterson MA, Shendure J, Nobrega MA, Yokota Y, Berul C, Izumo S, Seidman JG, Seidman CE. A molecular pathway including Id2, Tbx5, and Nkx2–5 required for cardiac conduction system development. Cell. 2007;129:1365–1376. 75. Stennard FA, Harvey RP. T-box transcription factors and their roles in regulatory hierarchies in the developing heart. Development. 2005;132: 4897–4910. 76. Moskowitz IP, Pizard A, Patel VV, Bruneau BG, Kim JB, Kupershmidt S, Roden D, Berul CI, Seidman CE, Seidman JG. The T-box transcription factor Tbx5 is required for the patterning and maturation of the murine cardiac conduction system. Development. 2004;131: 4107–4116. 77. Ranganayakulu G, Elliott DA, Harvey RP, Olson EN. Divergent roles for NK-2 class homeobox genes in cardiogenesis in flies and mice. Development. 1998;125:3037–3048. 12:42:12:10:11 Page 408 78. Tanaka M, Chen Z, Bartunkova S, Yamasaki N, Izumo S. The cardiac homeobox gene Csx/Nkx2.5 lies genetically upstream of multiple genes essential for heart development. Development. 1999;126: 1269–1280. 79. Jay PY, Harris BS, Maguire CT, Buerger A, Wakimoto H, Tanaka M, Kupershmidt S, Roden DM, Schultheiss TM, O’Brien TX, Gourdie RG, Berul CI, Izumo S. Nkx2–5 mutation causes anatomic hypoplasia of the cardiac conduction system. J Clin Invest. 2004;113:1130–1137. 80. Wakimoto H, Kasahara H, Maguire CT, Izumo S, Berul CI. Developmentally modulated cardiac conduction failure in transgenic mice with fetal or postnatal overexpression of DNA nonbinding mutant Nkx2.5. J Cardiovasc Electrophysiol. 2002;13:682–688. 81. Kasahara H, Wakimoto H, Liu M, Maguire CT, Converso KL, Shioi T, Huang WY, Manning WJ, Paul D, Lawitts J, Berul CI, Izumo S. Progressive atrioventricular conduction defects and heart failure in mice expressing a mutant Csx/Nkx2.5 homeoprotein. J Clin Invest. 2001;108:189–201. 82. Hsu DT. Cardiac manifestations of neuromuscular disorders in children. Paediatr Respir Rev. 2010;11:35–38. 83. Holaska JM. Emerin and the nuclear lamina in muscle and cardiac disease. Circ Res. 2008;103:16–23. 84. Arimura T, Helbling-Leclerc A, Massart C, Varnous S, Niel F, Lacene E, Fromes Y, Toussaint M, Mura AM, Keller DI, Amthor H, Isnard R, Malissen M, Schwartz K, Bonne G. Mouse model carrying H222PLmna mutation develops muscular dystrophy and dilated cardiomyopathy similar to human striated muscle laminopathies. Hum Mol Genet. 2005;14:155–169. 85. Wolf CM, Wang L, Alcalai R, Pizard A, Burgon PG, Ahmad F, Sherwood M, Branco DM, Wakimoto H, Fishman GI, See V, Stewart CL, Conner DA, Berul CI, Seidman CE, Seidman JG. Lamin A/C haploinsufficiency causes dilated cardiomyopathy and apoptosistriggered cardiac conduction system disease. J Mol Cell Cardiol. 2008;44:293–303. 86. Fatkin D, MacRae C, Sasaki T, Wolff MR, Porcu M, Frenneaux M, Atherton J, Vidaillet HJ Jr, Spudich S, De Girolami U, Seidman JG, Seidman C, Muntoni F, Muehle G, Johnson W, McDonough B. Missense mutations in the rod domain of the lamin A/C gene as causes of dilated cardiomyopathy and conduction-system disease. N Engl J Med. 1999;341:1715–1724. 87. Mounkes LC, Kozlov SV, Rottman JN, Stewart CL. Expression of an LMNA-N195K variant of A-type lamins results in cardiac conduction defects and death in mice. Hum Mol Genet. 2005;14:2167–2180. 88. Muchir A, Pavlidis P, Decostre V, Herron AJ, Arimura T, Bonne G, Worman HJ. Activation of MAPK pathways links LMNA mutations to cardiomyopathy in Emery-Dreifuss muscular dystrophy. J Clin Invest. 2007;117:1282–1293. 89. Muchir A, Shan J, Bonne G, Lehnart SE, Worman HJ. Inhibition of extracellular signal-regulated kinase signaling to prevent cardiomyopathy caused by mutation in the gene encoding A-type lamins. Hum Mol Genet. 2009;18:241–247. 90. Morgenlander JC, Nohria V, Saba Z. EKG abnormalities in pediatric patients with myotonic dystrophy. Pediatr Neurol. 1993;9:124–126. 91. Berul CI, Maguire CT, Aronovitz MJ, Greenwood J, Miller C, Gehrmann J, Housman D, Mendelsohn ME, Reddy S. DMPK dosage alterations result in atrioventricular conduction abnormalities in a mouse myotonic dystrophy model. J Clin Invest. 1999;103;R1–R7. 92. Wakimoto H, Maguire CT, Sherwood MC, Vargas MM, Sarkar PS, Han J, Reddy S, Berul CI. Characterization of cardiac conduction system abnormalities in mice with targeted disruption of Six5 gene. J Interv Card Electrophysiol. 2002;7:127–135. 93. Mahadevan MS, Yadava RS, Yu Q, Balijepalli S, Frenzel-McCardell CD, Bourne TD, Phillips LH. Reversible model of RNA toxicity and cardiac conduction defects in myotonic dystrophy. Nat Genet. 2006;38:1066–1070. 94. Hardy J, Singleton A. Genomewide association studies and human disease. N Engl J Med. 2009;360:1759–1768. 95. A haplotype map of the human genome. Nature. 2005;437:1299–1320. 96. Holm H, Gudbjartsson DF, Arnar DO, Thorleifsson G, Thorgeirsson G, Stefansdottir H, Gudjonsson SA, Jonasdottir A, Mathiesen EB, Njolstad I, Nyrnes A, Wilsgaard T, Hald EM, Hveem K, Stoltenberg C, Lochen ML, Kong A, Thorsteinsdottir U, Stefansson K. Several common variants modulate heart rate, PR interval and QRS duration. Nat Genet. 2010;42:117–122. Page 409 Park et Fishman 97. Pfeufer A, van Noord C, Marciante KD, Arking DE, Larson MG, Smith AV, Tarasov KV, Muller M, Sotoodehnia N, Sinner MF, Verwoert GC, Li M, Kao WH, Kottgen A, Coresh J, Bis JC, Psaty BM, Rice K, Rotter JI, Rivadeneira F, Hofman A, Kors JA, Stricker BH, Uitterlinden AG, van Duijn CM, Beckmann BM, Sauter W, Gieger C, Lubitz SA, Newton-Cheh C, Wang TJ, Magnani JW, Schnabel RB, Chung MK, Barnard J, Smith JD, Van Wagoner DR, Vasan RS, Aspelund T, Eiriksdottir G, Harris TB, Launer LJ, Najjar SS, Lakatta E, Schlessinger D, Uda M, Abecasis GR, Muller-Myhsok B, Ehret GB, Boerwinkle E, Chakravarti A, Soliman EZ, Lunetta KL, Perz S, Wichmann HE, Meitinger T, Levy D, Gudnason V, Ellinor PT, Sanna S, Kaab S, Witteman JC, Alonso A, Benjamin EJ, Heckbert SR. Genome-wide association study of PR interval. Nat Genet. 2010;42: 153–159. 98. Chambers JC, Zhao J, Terracciano CM, Bezzina CR, Zhang W, Kaba R, Navaratnarajah M, Lotlikar A, Sehmi JS, Kooner MK, Deng G, Siedlecka U, Parasramka S, El-Hamamsy I, Wass MN, Dekker LR, de Jong JS, Sternberg MJ, McKenna W, Severs NJ, de Silva R, Wilde AA, Anand P, Yacoub M, Scott J, Elliott P, Wood JN, Kooner JS. Genetic variation in SCN10A influences cardiac conduction. Nat Genet. 2010;42:149–152. 99. Cho HC, Marban E. Biological therapies for cardiac arrhythmias: can genes and cells replace drugs and devices? Circ Res. 2010;106:674–685. 100. Edelberg JM, Aird WC, Rosenberg RD. Enhancement of murine cardiac chronotropy by the molecular transfer of the human beta(2) adrenergic receptor cDNA. J Clin Invest. 1998;101:337–343. 101. Edelberg JM, Huang DT, Josephson ME, Rosenberg RD. Molecular enhancement of porcine cardiac chronotropy. Heart. 2001;86:559–562. 12:42:12:10:11 Page 409 Les troubles de la conduction cardiaque 409 102. Miake J, Marban E, Nuss HB. Gene therapy: biological pacemaker created by gene transfer. Nature. 2002;419:132–133. 103. Ruhparwar A, Kallenbach K, Klein G, Bara C, Ghodsizad A, Sigg DC, Karck M, Haverich A, Niehaus M. Adenylate-cyclase VI transforms ventricular cardiomyocytes into biological pacemaker cells. Tissue Eng Part A. 2010;16:1867–1872. 104. Sastry A, Arnold E, Gurji H, Iwasa A, Bui H, Hassankhani A, Patel HH, Feramisco JR, Roth DM, Lai NC, Hammond HK, Narayan SM. Cardiacdirected expression of adenylyl cyclase VI facilitates atrioventricular nodal conduction. J Am Coll Cardiol. 2006;48:559–565. 105. Qu JH, Plotnikov AN, Danilo P, Shlapakova I, Cohen IS, Robinson RB, Rosen MR. Expression and function of a biological pacemaker in canine heart. Circulation. 2003;107:1106–1109. 106. Plotnikov AN, Sosunov EA, Qu JH, Shlapakova IN, Anyukhovsky EP, Liu LL, Janse MJ, Brink PR, Cohen IS, Robinson RB, Danilo P, Rosen MR. Biological pacemaker implanted in canine left bundle branch provides ventricular escape rhythms that have physiologically acceptable rates. Circulation. 2004;109:506–512. 107. Plotnikov AN, Shlapakova I, Szabolcs MJ, Danilo P, Lorell BH, Potapova IA, Lu ZJ, Rosen AB, Mathias RT, Brink PR, Robinson RB, Cohen IS, Rosen MR. Xenografted adult human mesenchymal stem cells provide a platform for sustained biological pacemaker function in canine heart. Circulation. 2007;116:706–713. M : potentiels d’action 䊏 troubles du rythme cardiaque 䊏 conduction 䊏 génétique 䊏 études d’associations pan-génomiques 䊏 canaux ioniques