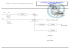
Dosage potentiométrique : Fe par MnO4
Transcription
Dosage potentiométrique : Fe par MnO4
Dosage potentiométrique : Fe2+ par MnO4(TP2 (TP2 – Série 8 Redox, et Exo 4 du TD23 TD23) Présentation du dosage : On cherche à mesurer la concentration C0 d’une solution aqueuse contenant du Fer (II) : FeSO 4 = Fe 2+ + SO 42− . Pour cela, on réalise un dosage avec du permanganate de potassium : KMnO 4 = K + + MnO 4− de concentration connue C 1 = 2.10−2 mol .L−1 . Le pH sera maintenu K + + MnO 4− constamment proche de 0, pour éviter que n’interviennent d’autres types de réactions… à C1 V Schéma du montage - électrode : Réf On a besoin de deux électrodes pour suivre le potentiel de la solution : Pt Fil de Platine (Pt) pour avoir un accès direct au potentiel de la solution Fe 2 + + SO 42 − Electrode de référence (2ème espèce) : fixe une référence… (Electrode au calomel saturé, ou au sulfate mercureux par exemple) à C0 Equation du dosage : Mn 2 + + 4 H 2O → MnO 4− + 8 H + + 5e − 2+ 3+ − Fe → Fe + e Demi-équations : − 4 + 2+ 2+ MnO + 8H + 5Fe → Mn + 4H 2O + 5Fe Equation du dosage : 2+ 5 3+ Mn Fe = 10 K = 5 8 MnO 4− Fe 2 + H + Constante de réaction : emesurée = E ⊕ − E Θ = E MnO 0 Démonstration : 4 − MnO 3+ n ∆E 0 0 ,06 E Elément titrant = 10 Ox 5× 0.74 0 ,06 = 10 Mn 2 + Fe 3 + Fe 2 + H+ H2 Fe 62 − 4 2+ Réducteur à doser Réd Fe 8 − + 3+ 0,06 MnO4 H 0 0,06 Fe + log − − log E Mn2+ Fe 3+ Fe 2+ Fe 2+ 5 1 Mn2+ Réaction TOTALE : on peut réaliser le dosage de manière satisfaisante Tableau d’avancement et évolutions : nFe 2+ Tableau d’avancement : V MnO 4− + 8 H + + 5Fe 2 + → Mn 2 + + 4 H 2O + 5Fe 3 + EI (en mol) 0 excès à t (avant EQ) 0 à l’équivalence ε solvant 0 excès C0V0-5C1V C1V solvant 5C1V excès à t (après EQ) C1V-C1VE excès Equivalence : C0V0 0 5ε C1VE solvant 5C1VE 0 C1VE solvant 5C1VE nMnO 4 − nFe 3+ nMn 2+ V V Quantité de permanganate ajouté = quantité initiale de Fer (Attention aux coefficients stoechiométriques) : n MnO − 4 _ ajout = 1 n 2+ 5 Fe _ ini ⇔ C0 = 1 ⇔ C 1V E = C 0V 0 5 5C 1V E V0 V 0 V1 2 EQ V EQ V 2EQ Calcul et Tracé des potentiels : En tout point, on a équilibre des solutions : ½ Equivalence : V 1 2 EQ = V E 2 ⇒ E solution = E Pt = E Fe 3 + On a V 2 EQ = 2V E = E M nO − 4 ⇒E1 2 EQ = E Pt = E Fe0 3+ Fe 2+ On a MnO 4− = Mn 2+ 0 ⇒ E2EQ = EMnO − Plus simple d’exprimer le potentiel du Permanganate : 4 Equivalence : M n 2+ Fe 3+ = Fe 2+ Il est plus simple d’exprimer le potentiel du Fer : Double Equivalence : Fe 2 + Mn2+ − 0,1pH Fe 3+ E 3+ 2+ = E 0 3+ 2+ + 0,06 log 2+ Fe Fe Fe Fe 1 Fe On exprime les 2 potentiels séparément 8 − + 0,06 MnO4 H 0 E E = + log MnO4− Mn2+ 2+ MnO4− Mn2+ 5 Mn M n 2+ = ξ M n O 4− = ε On a : F e 6E EQ On additionne : 6E EQ 2+ = 5 ⋅ ε et F e 3+ = 5 ⋅ ξ Fe 3+ MnO − H + 8 4 = 5E MnO − Mn2+ + E Fe 2+ Fe = 5E Fe 3+ Fe 2+ + E MnO − Mn2+ + 0,06 ⋅ log 2+ 2+ 4 4 Fe Mn 5 ⋅ξ ⋅ε 8 0 ⋅ H + = 5E Fe0 3+ Fe 2+ + E MnO − 2+ + 0,06 ⋅ log Mn 4 5 ⋅ε ⋅ξ Si pH = 0, alors 0 E EQ = Expression du potentiel avant l’équivalence : E 3+ Fe Expression du potentiel après l’équivalence : E − MnO 4 Fe 2+ Mn2+ 5 E Fe0 3 + 0 Fe 2 + 0 + E MnO 4 − M n 2+ 6 Fe 3 + C 1V 0,06 0,06 =E + log 2+ = E 20 + log Fe 1 1 C 0V 0 − 5C 1V 0 2 8 − + 0,06 MnO4 H 0,06 C1V −C1VE =E + log = E 30 + log 2 + 5 5 Mn C1VE 0 3 Remarque : Attention, la courbe n’est pas symétrique, du fait des coefficients stœchiométriques des équations. On ne peut pas appliquer la méthode des tangentes pour obtenir le point à l’équivalence.