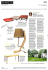experience de franck et hertz
Transcription
experience de franck et hertz
Frere Benjamin Marique Pierre-Xavier RAPPORT DE LABORATOIRE DE PHYSIQUE EXPERIENCE DE FRANCK ET HERTZ 2ème candidature sciences physiques, Université de Liège Année académique 2003-2004 1) Historique Cette expérience fut réalisée pour la première fois pas Franck et Hertz en 1914. Ils développèrent la théorie de la luminescence et cela leur a valut le prix Nobel en 1925. Einstein utilisa la même notion en 1905 pour la théorie de l’effet photoélectrique. Franck et Hertz testèrent le modèle de l’atome de Borh lors de leur expérience. 2) Objectif Le but de cette expérience est de mettre en évidence la quantification de l’énergie. Nous vérifierons ceci par le modèle des atomes développé par Bohr, dans le cas particulier des atomes de mercure (Hg). 3) Description de l'expérience et présentation du materiel Afin de mettre en évidence la quantification des niveaux d’énergie, Franck et Hertz ont pensé au choc entre des électrons et les atomes d’un gaz. Ils ont ainsi réalisé leur expérience dans le cas particulier des atomes de mercure. Voici comment nous avons reproduit cette manipulation. Nous avons utilisé un tube à vapeur de Hg contenant trois électrodes (1): - une cathode qui par effet thermoionique va émettre de électrons qui entrerons en collisions avec les atomes de Hg (2); - une grille jouant le rôle de l’anode que l’on aura portée à un potentiel V positif par rapport à la cathode (3); - une électrode d’arrêt, ou électrode de comptage, se trouvant en haut du tube. Cette électrode, qui est portée à un potentiel légèrement négatif par rapport à l’anode, sert à ‘récupérer’ les électrons possédant une énergie cinétique, c’est-à-dire une vitesse suffisante pour l’atteindre (4). La distance entre la cathode et la grille a été choisie grande par rapport au libre parcours moyen de l’électron afin que la probabilité de choc entre les électrons et les atomes soit plus importante. Par contre la distance séparant la grille de l’anode est de l’ordre du libre parcours moyen de l’électron. Le tube est placé dans un four (5) dont la température est contrôlée par un rheostat (6). La manipulation consiste à fixer une température et à augmenter progressivement la tension appliquée (7). La température du four doit se situer entre 160°C et 220°C afin d’obtenir une pression de vapeur suffisante pour qu’il y aie assez d’atomes de Hg à l’état vapeur et que nous ayons donc plus de facilité à déceler les chocs. Il suffit ensuite d’étudier l’évolution de l’intensité (8) du courant en fonction des variations que l’on impose à la tension. Donc si aucun électron, ayant percuté ou pas des atomes de Hg, n’a une vitesse suffisante pour atteindre l’électrode de comptage, le courant à la sortie sera nul. Remarque : Quelques astuces techniques nous ont aidés dans cette expérience. La première consistait à placer à la sortie du four une résistance très élevée afin d’obtenir une intensité de courant très petite. Nous avons aussi utilisé un potentiomètre à l’alimentation afin de varier plus précisément la tension appliquée. 4) Prévisions Théoriques La cathode placée sous une différence de potentiel va émettre des électrons. En appliquant une différence de potentiel entre la cathode et l’anode, les électrons vont être accélérés. Ceux-ci traversent le tube avec une énergie cinétique proportionnelle à la tension appliquée. Ils vont ensuite rentrer en contact avec les atomes de mercure. On peut prévoir ces trois cas de figure : - Les collisions entre les électrons et les atomes de mercure sont élastiques lorsque l’énergie cinétique des électrons est inférieure à la différence entre deux niveaux d’énergie consécutifs (c'est-à-dire inférieure à 4,9eV). Les atomes de mercure ne seront pas excités. La différence de potentiel entre l’anode et l’électrode de comptage va ralentir les électrons. S’ils n’ont pas une énergie cinétique suffisante, ils n’atteindront pas l’électrode de comptage et ne passeront pas dans la résistance. Cependant, le nombre d’électrons atteignant l’électrode de comptage sera le plus élevé car les chocs ne seront pas très importants. - Lorsque l’énergie cinétique des électrons est égale à 4,9eV, les atomes de mercure sont excités vers un niveau d’énergie plus important. C’est le premier niveau, celui de résonance. Après peu de temps, ils se désexcitent et ils atteignent de nouveau leur énergie initiale en émettant un rayonnement électromagnétique. Les électrons auront toujours un peu d’énergie car ils sont toujours accélérés, mais celle-ci sera trop faible pour leur permettre d’atteindre l’électrode de comptage. Il n’y aura plus de courant. C’est donc un minimum. - Lorsque l’énergie cinétique des électrons est supérieure à 4,9eV tout se passe comme dans le cas précédent sauf que les électrons gardent une énergie cinétique. Les électrons excitent les atomes de mercure de plus en plus tôt sur le trajet de l’anode, de sorte qu’ils ont été suffisamment accélérés pour atteindre l’électrode de comptage. Lorsque la tension passe par 9,8V le courant s’annule à nouveau car il y a deux collisions entre les électrons et le mercure (une à mi-chemin et l’autre juste devant la grille). L’évolution de l’intensité du courant en fonction de la tension appliquée est un phénomène périodique. La période donne la valeur de l’énergie d’excitation du mercure et la largeur du minimum dépend de la valeur de la tension appliquée à l’électrode d’arrêt, c'est-à-dire dans notre cas 1,2V. 5) Analyse des résultats Voici tout d’abord les tableaux reprenant nos valeurs expérimentales: Allure générale des courbes expérimentales Lors du premier coup d’œil sur les trois graphiques dessinés à partir de nos mesures, nous remarquons la nature grossièrement oscillante et périodique des trois courbes. Cette succession de minima et de maxima nous montre bien la quantification de l’énergie. Dans un deuxième temps, nous remarquons une augmentation successive des minima. Cela se voit surtout lorsque la température du four est basse. Cela peut s’expliquer par le fait que des électrons ayant même l’énergie suffisante pour occasionner une collision inélastique n’ont peut être pas la chance de rencontrer un atome de mercure. Et selon la loi d’ohm, plus on augmente la différence de potentiel, plus l’intensité du courant sera grande. Ce courant dépendra aussi de la résistance rencontrée durant le parcours des électrons qui ici est la présence de vapeur de mercure. Cette densité de vapeur augmentant avec la température, il est normal de surtout observer cette « montée » de la courbe lorsque que la température est plus basse. Ce qui correspond à une quantité de mercure vaporisé plus faible, et une grande probabilité que les collisions ne se produisent pas. Cette dernière remarque nous mène à la troisième observation globale des courbes. Même les électrons ne subissant qu’un choc élastique (qui entraîne une perte d’énergie cinétique relativement négligeable) peuvent perdre assez d’énergie pour ne pas atteindre l’anode à cause des innombrables collisions successives. Une quatrième particularité à noter est qu’après l’allure grosso modo périodique de la courbe, les valeurs d’intensité du courant « s’emballent » lorsqu’on augmente trop le voltage. Ce phénomène est dû à l’ionisation du mercure qui entraîne une augmentation des charges négatives dans le tube et donc du courant. On l’observe grâce à l’apparition d’un nuage bleu. Il arrive plus rapidement dans les basses températures car les ions se recombinent moins facilement avec les électrons qu’en plus haute température. Analyse plus précise des données mesurées : Lorsque l'on regarde de plus près les courbes on se rend compte qu'il y a beaucoup d'irrégularités. Mais elles s'atténuent avec la hausse de la température. Par exemple, le second minimum de la courbe à la plus basse température, est un accident flagrant et il ne faut ne peut être pas prendre en compte la valeur accidentelle de 1,14E-05 mA mesuré à 12,8 V, et plutôt prendre les 1,30E-05 mA mesuré à 12,9 V. En prenant garde à ce genre de petits accidents, voici un récapitulatifs de nos différents minimums: 155 °C +/- 5 °C Différences 7.6 12.9 Moyenne: Moyenne totale: 185 °C +/- 5 °C Différences 7.3 12.5 17.9 5.3 23 5.3 Moyenne: 5.2 5.4 5.1 5.23 205 °C +/- 5 °C Différences 6.9 12.3 5.4 17.4 5.1 22.7 5.3 27.8 5.1 33 5.2 Moyenne: 5.22 5.25 La différence, ou l’écart entre les minima, donne la valeur de l’énergie nécessaire pour exciter l’atome de Hg. La première chose à remarquer, c’est que le premier minimum se trouve aux alentours de 7,5 V au lieu des 4,9 V théorique. C’est tout simplement dû au potentiel de contact; une différence de potentiel qui apparaît lorsque deux électrodes d’un circuit sont l’une en face de l’autre même lorsque aucune tension n’est appliquée. Sinon, la moyenne de la période se trouve assez proche de la prévision théorique sans pour autant être très précise. 6) Sources d'erreur La première grosse source d’erreur est bien évidemment la température. Le thermostat contrôlant l’allumage ou l’extinction de la résistance électrique ne saurait assurer une température rigoureusement constante vu qu’à chaque allumage, elle augmente un peu et qu’à chaque extinction des résistances elle diminue. Nous avons donc une oscillation entre deux températures extrêmes. Et lorsque que l’on voit la différence entre les courbes expérimentales qu’il peut y avoir entre deux températures, nous nous rendons vraiment compte que c’est un facteur d’erreur assez important. Cependant, cet effet diminue plus la température augmente. Nous aurions pu, pour minimiser nos erreurs de mesures, les prendre en une même température, mais cela nous aurait pris énormément de temps pour le faire, et nous ne l’avions pas. Une seconde approximation liée à la première se trouve à la mesure du courant entre la cathode et la grille. Nous n'utilisions déjà pas un ampèremètre, mais un voltmètre couplé avec une très grande résistance et calculions le courant avec la loi d’ohm. Petite source d’erreur en plus. Cela étant, le voltmètre ne nous aidait pas mon non plus en oscillant tout le temps et nous devions donc en prendre une lecture moyenne. Le changement étant si rapide qu’il n’était pas simple d’avoir quelque chose d’un minimum précis. Pour ce qui est du reste, le réglage de la tension accélératrice est assez précis, surtout grâce au potentiomètre, et la mesure du voltage en était tout autant précise. Le potentiel d’arrêt qui lui étant constant pouvait aussi se régler de manière relativement précise. 7) Annexe L’atome de mercure Le modèle de Bohr révèle que chaque atome est composé d’électron(s) tournant autour du noyau. L’atome de mercure en possède quatre-vingts. Ces électrons sont répartis sur des orbites bien définies correspondant à des niveaux d’énergie. Si un électron est excité, il passe sur une « couche » supérieure. Ensuite, il retombera à son niveau d’énergie de départ en émettant un photon qui représente un quantum d’énergie. Pour passer d’un niveau à un autre, il faut que ces deux niveaux soient reliés comme dans le schéma cidessous: Remarque : il est impossible qu’un électron passe d’un niveau d’énergie à un autre s’ils ne sont pas reliés par une flèche sur le dessin sauf pour l’état d’ionisation qui est accessible de n’importe quel niveau d’énergie.