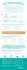La maladie de Lyme au Québec
Transcription
La maladie de Lyme au Québec
Volume 57 – n° 3 Juin 2010 À vos soins Millepertuis et contraceptifs oraux La maladie de Lyme au Québec Les Pages bleues Le syndrome des jambes sans repos Avez-vous entendu parler de... La desvenlafaxine www.professionsantequebec.ca PP 40070230 1200, avenue McGill College, bureau 800, Montréal (QC) H3B 4G7 Éditorial Gène Directrice de la rédaction Caroline Baril Rédactrice en chef Hélène-M. Blanchette, B. Pharm. Rédacteur en chef adjoint Jean-François Guévin, B. Pharm., M.B.A., Pharm. D. Adjointe à la directrice de la rédaction Mélanie Alain Direction artistique Dino Peressini Graphiste Jocelyne Demers Directeur des rédactions, Groupe Santé Rick Campbell Comité de rédaction Avez-vous entendu parler de... Isabelle Giroux, B. Pharm. M. Sc. Dominique Harvey, B. Pharm. À vos soins Sonia Lacasse, B. Pharm. Sophie Grondin, B. Pharm. M. Sc. À votre service sans ordonnance Nancy Desmarais, B. Pharm. Julie Martineau, B. Pharm. De la mère au nourrisson Caroline Morin, B. Pharm., M. Sc. D’une page à l’autre Isabelle Boisclair, B. Pharm., M. Sc. Nicolas Paquette-Lamontagne, B. Pharm., M. Sc., M.B.A. Inforoute Jean-François Bussières, B. Pharm., M. Sc., M.B.A. Les Pages bleues Chantal Duquet, B. Pharm., M. Sc. Ingrid Wagner, B. Pharm. Pharmacovigilance Marie Larouche, B. Pharm., M. Sc. Christine Hamel, B. Pharm., M. Sc. Place aux questions Élyse Desmeules, B. Pharm. Quelques conseils sur... Julie Véronneau, B. Pharm. Santé publique Suzie Lavallée, B. Pharm. Membre honoraire Georges Roy, M. Pharm. Impression Imprimeries Transcontinental Québec Pharmacie est publié 8 fois l’an par Rogers Media. Vous pouvez consulter notre politique environnementale à : www.leseditionsrogers.ca/about_rogers/ environmental.htm Nous reconnaissons l’aide financière du gouvernement du Canada par l’entremise du Fonds du Canada pour les périodiques (FCP) pour nos activités d’édition. www.professionsante.ca On a parfois de la gêne, on a assurément toujours des gènes et c’est pourquoi il faut parler de génomique. Si la génomique est une science un peu obscure pour le commun des mortels, elle a évolué quand même significativement depuis une dizaine d’années, et maintenant, tant en médecine qu’en pharmacie, on a vu des changements dans la pratique et on verra des innovations de pratique. On s’est repu des nombreuses familles de cytochromes, en y voyant l’univers ultime de métabolisation. Mais on est encore bien ignorant quant à la réelle diversité métabolique et génomique. On ne peut plus être certain de rien quand on fournit un médicament à un patient. Si la pharmacothérapie a grandement évolué dans le sens d’une multiplication des molécules actives, elle commence à peine à tenir compte des aspects génomiques propres à des patients. Comment arriver à mieux identifier les risques d’une pharmacothérapie, ou encore mieux, la nécessité d’une pharmacothérapie chez des patients dont on ne voit que la barrière externe (la peau) ? Si des tests urinaires ou sanguins existent pour mesurer certains indices biochimiques, la commercialisation de plus en plus importante de tests visant à détecter des polymorphismes modifiera assurément la pratique des médecins et des pharmaciens. La pharmacothérapie devra s’adapter au patient, et non l’inverse. Actuellement, parce que les médicaments généralement utilisés le sont en vertu de données probantes qui établissent leur efficacité, les résultats de leur utilisation sont mesurés sur de larges groupes de patients. À l’intérieur de ces groupes, on sait peu de choses sur les individus, autrement que par l’identification statistique de certains, puisqu’ils perçoivent des effets indésirables. On peut parler alors d’une pratique pharmaceutique personnalisée qui tient compte à la fois des besoins exprimés par le patient, du diagnostic et du plan de traitement faits par le médecin et d’une individualisation de la pharmacothérapie et de son suivi. Fini le suivi universalisé basé sur une ligne directrice qui n’évolue que très lentement parce que basée sur des populations très larges. C’est évident que chaque humain porte son propre génome qui l’individualise complètement. C’est tout aussi évident que la « pharmacogénothérapie » prendra de plus en plus de place. Des exemples de grande spécificité de la cible existent déjà, spécificité qui tient compte des mutations exprimées dans le génome de certains patients. Bien sûr, on ne s’attendra pas à ce que le pharmacien de pratique privée puisse identifier quel exon est défectueux chez sa patiente et, en conséquence, qu’il puisse rédiger une opinion pharmaceutique visant à modifier la dose d’un médicament. Cependant, on pourra s’attendre à ce que, à la suite de résultats obtenus dans un laboratoire ou même en autodiagnostic, la posologie d’un médicament qu’un patient doit prendre doive être ajustée. Bien sûr, même si la science avance, les coûts des nouvelles technologies peuvent être un frein à leur utilisation, mais le patient/client nous amènera à devoir les utiliser. En même temps qu’on aura l’éclairage de la génomique dans nos décisions thérapeutiques, on aura aussi des patients mieux informés. Paradoxalement, à la découverte de concepts scientifiques de plus en plus poussés, la démocratisation de l’information scientifique fournit au patient les instruments de sa propre prise en charge, et c’est lui qui sera l’entrepreneur innovateur qui cherchera à obtenir les services des fournisseurs qu’il aura choisis. C’est le patient innovateur qui s’en vient. C’est l’impulsion que le patient fournit au système de santé qui va faire que l’excellence sera atteinte. Le patient/ client ne se contentera plus de services de moindre qualité, de délais impensables ou de faux-semblants politiques. Il est probable que cela conduira à un système à deux vitesses, dans le sens où ce ne sont pas tous les patients qui voudront savoir si leur polymorphisme est important dans le traitement pharmacologique prescrit. Est-ce qu’on doit s’en surprendre ? Non. Dans tous les cas, le centre du système de soins sera encore plus véritablement le patient/client que ses professionnels de la santé. Certains patients s’exprimeront sur leurs nécessités individuelles avec moins de gêne. La pharmacogénomique n’est donc que le début d’une ère nouvelle en pharmacie. Je ne crois pas me tromper en pensant que le pharmacien de demain, comme son collègue médecin de demain, sera beaucoup plus préoccupé par ce que son patient est et peut être, au point où les conseils écrits qu’on peut remettre ne seront plus du tout pertinents ni universels. juin 2010 vol. 57 n° 3 Québec Pharmacie 3 Sommaire Volume 57 – n° 3 – juin 2010 Pour toute information 1200, avenue McGill College, bureau 800 Montréal (Québec) H3B 4G7 Téléphone : 514 845-5141 Télécopieur : 514 843-2183 [email protected] Changements d’adresses et abonnements Vous trouverez les questions de formation continue à la fin de chacun des articles. 3 Pour les pharmaciens par téléphone : 514 284-9588 par télécopie : 514 284-3420 par courriel : [email protected] Pour les non-pharmaciens Tél. : 514 843-2594 • Téléc. : 514 843-2182 7 Tarifs : Canada : 69 $ par année, 103 $ pour 2 ans, 8 $ l’exemplaire. Tarif de groupe/vrac : 55,20 $. (min. 6 exemplaires). États-Unis et international (abonnement individuel seul.) : 110 $ par année. Taxes en vigueur non comprises. 11 Éditrice Groupe Santé, Québec Directrice des ventes pour le Québec Caroline Bélisle 514 843-2569 (Montréal) Publicité/Ventes pharmaceutiques Josée Plante 514 843-2953 (Montréal) Pauline Shanks 514 843-2558 (Montréal) Norman Cook 416 764-3918 (Toronto) Stephen Kranabetter 416 764-3822 (Toronto) Sara Mills 416 764-4150 (Toronto) Teresa Tsuji 416 764-3905 (Toronto) Petites annonces Sylvle-Anne Breton 514 843-2132 Directrice de la coordination et de la production publicitaire Sylvie Graveson 514 843-2565 Coordonnatrice de la production Rosalina Lento 514 843-2557 Coordonnateur du MSG Claude Larochelle 514 843-2114 15 20 31 Éditeur exécutif et Directeur général, Opérations et développement des affaires Jean Goulet Président et chef de la direction de Rogers Media inc. Anthony P. Viner Président des Éditions Rogers Media Brian Segal Premier vice-président, Publicationsd’affaires et professionnelles John Milne Vice-président senior Michael J. Fox Vice-présidents Imme Chee Wah, Patrick Renard Vice-président – Production John Hall Directeur des opérations de publications Sean McCluskey Gêne À VOS SOINS Millepertuis et diminution de l’efficacité des contraceptifs oraux Place aux questions Antibiotiques contre la conjonctivite bactérienne en pédiatrie à votre service sans ordonnance Troubles digestifs traités par l’automédication Avez-vous entendu parler de... La desvenlafaxine (PristiqMD) Les pages bleues Syndrome des jambes sans repos 41 Santé publique Directeur de la diffusion, groupe B2B Keith Fulford 416 764-3878 [email protected] Coordonnatrice de la diffusion Francine Beauchamp 514 843-2594 [email protected] Éditorial La maladie de Lyme au Québec 44 Pharmacovigilance 51 D’une page à l’autre Mise à niveau en pharmacovigilance Impact économique des interventions cliniques du pharmacien Dans ce numéro Mise à jour diabète 2010 Dépôt légal : Bibliothèque nationale du Québec, Bibliothèque nationale du Canada ISSN 0826-9874. Toutes les annonces de produits pharmaceutiques sur ordonnance ont été approuvées par le Conseil consultatif de publicité pharmaceutique. Envoi de poste – publications, convention nº 40070230. www.professionsante.ca juin 2010 vol. 57 n° 3 Québec Pharmacie 5 À vos soins Millepertuis et diminution de l’efficacité des contraceptifs oraux S.T., 28 ans, se présente au comptoir des renseignements pharmaceutiques pour voir le pharmacien. Elle prend un contraceptif oral à faible teneur en œstrogène (AlesseMD) depuis plus d’un an, sans problème. Depuis quelques jours, elle présente des saignements entre ses règles, ce qui l’inquiète beaucoup. Après l’avoir interrogée, vous apprenez qu’elle prend du millepertuis 300 mg tid depuis quelques semaines pour remplacer son Citalopram (20 mg die), étant donné qu’elle voulait quelque chose de plus naturel pour traiter sa dépression. Discussion Le millepertuis (Hypericum perforatum ou St. John’s Wort) est une plante de la famille des hypéricacées dont on utilise surtout les parties aériennes pour leurs vertus thérapeutiques1. Ses utilisations sont variées et comprennent notamment la dépression, l’anxiété et le syndrome prémenstruel. En effet, plusieurs études ont démontré l’efficacité du millepertuis dans le traitement de la dépression légère à modérée, celui-ci étant supérieur au placebo et comparable aux antidépresseurs1,2,3. Son activité pharmacologique proviendrait en majeure partie de l’hyperforine. Ainsi, son efficacité dans le traitement de la dépression serait due à une inhibition du recaptage de la norépinéphrine, de la dopamine et de la sérotonine1,2. Ce produit de santé naturel contient aussi de l’hypéricine. On a déjà cru que celle-ci était responsable des effets thérapeutiques du millepertuis, mais c’est bel et bien l’hyperforine qui en est la source1,3. Contrairement aux croyances des patients, le millepertuis n’est pas plus sécuritaire parce qu’il est naturel ! Effectivement, le millepertuis, grâce à l’hyperforine, est un puissant inducteur de plusieurs isoenzymes du cytochrome P450, principalement le 3A4, de même que de la glycoprotéine P (Pgp)1,3-6. L’induction survient lors d’une prise chronique de suppléments, soit généralement pendant plus de 10 jours au cours desquels l’hyperforine est standardisée à plus de 1 % (l’induction causée par des suppléments qui en contiennent moins ne serait pas significative)3,7. Par conséquent, la concentration plasmatique de plusieurs médicaments peut s’en trouver diminuée. Un des exemples les mieux documentés est l’ajout de millepertuis à la prise de cyclosporine, ce qui a entraîné une diminution de la concentration de cyclosporine à des niveaux sous-thérapeutiques pouvant mener à un éventuel rejet du greffon1,3. D’un autre côté, sur le plan pharmacodynamique, le millepertuis, s’il est associé à un médicament ayant un effet sur la sérotonine (par exemple, les inhibiteurs sélectifs du recaptage de la sérotonine), peut augmenter la quantité de ce neurotransmetwww.professionsante.ca teur au niveau de la fente synaptique, ce qui pourrait causer un éventuel syndrome sérotoninergique1,3. Concernant les contraceptifs oraux, l’inter action est tout aussi présente et la documentation scientifique, bien que peu volumineuse, abonde dans ce sens. En résumé, l’ajout de millepertuis à la prise d’un contraceptif entraîne une modification de différents paramètres pharmacocinétiques, telle qu’une augmentation de la clairance du progestatif, une diminution du temps de demivie de l’éthinyl estradiol et une diminution de l’exposition totale au contraceptif (réduction de l’aire sous la courbe de l’ordre de 13 à 15 %)3-6. Le mécanisme impliqué serait une augmentation de l’expression de la Pgp et une induction du CYP3A41,3-6. Ainsi, même si ces modifications varient d’une étude à l’autre, on a constaté qu’une majorité d’entre elles entraînait une augmentation du risque de saignement pendant le cycle menstruel, ce qui peut indiquer une diminution de la concentration plasmatique du contraceptif et créer de l’inconfort chez les patientes, augmentant le risque d’arrêt du contraceptif de leur part3-6. Même si, à ce jour, aucune étude n’a été en mesure d’identifier une diminution significative de l’efficacité des contraceptifs oraux, il faut garder à l’esprit qu’il existe plusieurs données scientifiques qui abondent dans ce sens. Une étude a permis d’observer une activ i t é f o l l i c u l a i re accrue associée à une augmentation sérique de la progestérone, traduisant ainsi une potentielle ovulation, bien que cela n’ait pas été statistiquement significatif4. En plus de ces considérations théoriques, il existe quelques rapports de cas de grossesses non planifiées. Le pharmacien se doit donc de déconseiller l’usage concomitant du millepertuis et des contraceptifs oraux. Texte rédigé par Mélanie B. Gravel, étudiante en pharmacie, 2e année de Pharm. D., Université de Montréal, et Jonathan Rouisse, pharmacien, Pharmacie Claude Saucier, Nicole Héroux et Catherine Bertrand. Révision : Sonia Lacasse, B. Pharm. Texte original soumis le 12 mars 2010. Texte final remis le 23 mars 2010. juin 2010 vol. 57 n° 3 Québec Pharmacie 7 À vos soins pour un traitement d’automédication, soit le millepertuis. Cependant, après quelques semaines d’utilisation, elle a présenté des OFemme âgée de 28 ans. Elle prend un contraceptif oral (Alesse) depuis plus d’un an. Elle effets indésirables, soit des saignements irréa commencé à prendre du millepertuis (300 mg TID) il y a quelques semaines en guliers durant son cycle menstruel, malgré la remplacement de son Citalopram. prise régulière de son contraceptif oral. En effet, le millepertuis pourrait augmenACertaines données suggèrent qu’il existe une interaction potentielle entre le millepertuis ter le métabolisme de l’œstrogène et du proet les contraceptifs oraux. Puisque le millepertuis pourrait diminuer l’efficacité des gestatif, rendant leur activité contraceptive contraceptifs oraux, il est généralement recommandé d’en cesser la prise afin d’éviter potentiellement moins efficace. J’ai recoml’inefficacité de la contraception. mandé à Mme S.T. de cesser le millepertuis pour remédier à la situation et d’utiliser une P n Cesser le millepertuis autre méthode de contraception pour le n Suggérer une autre protection pour le reste du cycle reste du cycle. n Rédiger une opinion pharmaceutique Ayant cessé le Citalopram, Mme S.T. se n Recommander de consulter son médecin afin de recevoir une thérapie permettant retrouve aujourd’hui sans traitement pour de traiter sa dépression soigner sa dépression. Étant donné que ses n Faire un suivi téléphonique avec la patiente (dans 1 mois) symptômes sont toujours présents, il serait, à mon avis, approprié de recommencer le Citalopram ou de prendre un autre Présentement, l’Ordre des pharmaciens du Acte pharmaceutique facturable antidépresseur. Québec étudie la possibilité de placer le Opinion pharmaceutique; interaction : interJ’espère que ces renseignements vous millepertuis dans l’annexe 2 du Règlement rompre la prise d’un produit pharmaceuti- seront utiles et que vous pourrez les joindre sur les conditions et modalités de vente des que disponible pour autotraitement (DIN : au dossier de Mme S.T. Toutefois, si vous médicaments au Québec. Cela permettrait 00999670). aviez besoin d’informations complémentaisans doute aux pharmaciens de mieux gérer res, n’hésitez pas à communiquer avec moi et les interactions et diminuerait les risques Opinion pharmaceutique il me fera plaisir, Docteur, d’échanger à noupour les patients. En attendant, la vigilance Docteur, veau avec vous. des pharmaciens est primordiale et rensei- Je désire porter à votre attention certains rengner les patients est important afin de seignements concernant Mme S.T. Professionnellement, les sensibiliser à l’innocuité des produits Malgré la prescription de Citalopram pour Le Pharmacien traiter sa dépression, Mme S.T. a préféré opter naturels. n SS.T. présente des saignements entre ses règles et elle se sent un peu déprimée. Références 1. Jellin JM, Gregory PJ, Batz F, et coll. Pharmacist’s Letter/Prescriber’s Letter Natural Medecines Comprehensive Database. 11e éd. Stockton, CA : Therapeutic Research Faculty, 2009; 1495-505. 2. Lawvere S, Mahoney MC. St. John’s Wort. American Family Physician, 2005; 72; 2249-2254. 3. Borelli F, Izzo AA. Herb-Drug Interactions with St John’s Wort (Hypericum perforatum) : An Update on Clinical Observations. The AAPS Journal, 2009; 11; 710-27. 4. Murphy PA, Kern SE, Stanczyk F, et coll. Interaction of St. John’s Wort with Oral Contraceptives : Effects on the Pharmacokinetics of norethindrone and ethinylestradiol, ovaria activity and breakthrough bleeding. Contraception, 2005; 71; 402-8. 5. Hall SD, Wang Z, Huang S, et coll. The Interaction between St John’s Wort and an Oral Contraceptive. Clinical Pharmacology and Therapeutics, December 2003; 74: 525-35. 6. Pfrunder A, Schiesser M, Gerber S, et coll. Interaction of St John’s Wort with lowdose oral contraceptive therapy : A randomized controlled trial. Journal of Clinical Pharmacology, 2003; 56: 683-90. 7. Will-Shahab L, Bauer S, Kunter U, et coll. St John’s Wort extract does not alter the pharmacokinetics of low-dose oral contraceptive. European Journal of Clinical Pharmacology, 2009; 65: 287-94. 8. Schwarz UI, Büschel B, Kirch W. Unwanted pregnancy on self-medication with St John’s Wort despite hormonal contraception. Br J Clin Pharmacol, 2003; 55: 112-3. Question de formation continue 1) Lequel de ces énoncés est vrai ? A. L’induction enzymatique causée par le millepertuis se produit rapidement, soit en une à deux journées après la première dose. B. C’est l’hypéricine qui est responsable de l’efficacité du millepertuis dans le traitement de la dépression légère à modérée. C. Puisqu’il n’a pas été démontré que le millepertuis diminue de façon significative l’efficacité des contraceptifs oraux, une patiente sous contraceptif oral peut utiliser le millepertuis sans inquiétude. D. L’augmentation du métabolisme des médicaments est la seule interaction possible avec le millepertuis. E. L’Ordre des pharmaciens du Québec étudie actuellement la possibilité de placer le millepertuis dans l’annexe 2 du Règlement sur les conditions et modalités de vente des médicaments au Québec. Veuillez reporter votre réponse dans le formulaire de la page 78 8 Québec Pharmacie vol. 57 n° 3 juin 2010 Place aux questions Quels antibiotiques privilégier en pédiatrie dans le traitement de la conjonctivite bactérienne ? Généralement causée par Hæmophilus influenzæ, Streptococcus pneumoniæ, Moraxella catarrhalis et Staphylococcus aureus, la conjonctivite bactérienne se distingue d’une infection virale ou d’une allergie par la présence d’un écoulement purulent. Autres signes présents : hypérémie, œdème des paupières et cils collés au réveil1. Des méthodes non pharmacologiques, comme éviter l’exposition à la fumée de cigarette, au vent et aux autres irritants, et l’application de compresses humides tièdes plusieurs fois par jour contribuent à en diminuer les symptômes incommodants. Comme une résolution spontanée survient fréquemment en 10 à 14 jours et que l’utilisation des antibiotiques ophtalmiques n’a pas été entièrement documentée chez les nourrissons, on peut s’interroger sur la pertinence du traitement1. Or, le traitement a plusieurs buts : atténuer le risque de contagion, minimiser les répercussions pour l’enfant (retrait de la garderie ou de l’école, apparition d’une otite moyenne), diminuer les coûts engendrés pour les parents (gardienne, congé du travail) et permettre d’établir un nouveau diagnostic si aucune amélioration n’est notée dans un délai de 48 heures1. Les classes thérapeutiques utilisées sont nombreuses et puisqu’une analyse de culture est rarement faite, un bon traitement doit avoir un spectre d’action large, peu de résistance et une faible toxicité oculaire, et permettre un horaire d’administration simple. La pommade est une forme pharmaceutique à privilégier en pédiatrie puisqu’elle a l’avantage de ne pas être diluée par les larmes. Traitement sans ordonnance stéroïde, est déconseillé en pédiatrie, sauf dans certains cas, à la suite de l’examen par un ophtalmologiste. En effet, si l’infection est d’origine virale, il pourrait y avoir augmentation des symptômes2. Texte rédigé par Joëlle Rhéaume-Majeau, B. Pharm., Pharmacie Vandergoten et Zaccara, Saint-Eustache. Polymyxine B/triméthoprime (PolytrimMD) Texte final remis le 1er mars 2010. Une étude réalisée en 2008 comparant la rapidité d’action du PolytrimMD avec celle du VigamoxMD a démontré qu’après 48 heures de traitement, seulement 44 % des enfants traités par le Polytrim quatre fois par jour, comparativement à 81 % de ceux traités par le Vigamox trois fois par jour, présentaient une résolution complète des symptômes oculaires3. Ainsi, bien que peu coûteux, on emploie rarement le Polytrim, sauf peut-être en cas d’affection très légère. Révision : Geneviève Duperron, B. Pharm., et Élyse Desmeules, B. Pharm. Texte original soumis le 18 février 2010. Chloramphénicol (PentamycetinMD) Malgré une excellente efficacité, selon certaines études, et peu de résistance associée, il n’est pas un premier choix de traitement, surtout chez le nouveau-né, en raison de sa toxicité potentielle4,5. Entre autres, il peut provoquer une aplasie médullaire et un « gray baby syndrome », phénomène rare mais sérieux s’expliquant par le fait que les enzymes hépatiques nécessaires à son métabolisme sont immatures et qu’il y a un risque d’accumulation de l’antibiotique pouvant occasionner, entre autres, hypotension, cyanose et collapsus cardiovasculaire6. Cette section inclut la polymyxine B avec gramicidine (PolysporinMD gouttes et génériques) et la polymyxine B et bacitracine (PolysporinMD onguent et génériques). Options de traitement en vente libre peu dispendieuses, ces associations offrent l’avantage d’une protection intéressante contre les bactéries Gram-négatives grâce à la polymyxine B et contre les Gram-positives grâce à la gramicidine et à la bacitracine (plus efficace). Elles permettent dans plusieurs cas Aminoglycosides d’éviter les consultations non nécessaires en Cette classe thérapeutique inclut : GaramycinMD, TobrexMD, Optimyxin PlusMD, Neospoclinique médicale. rinMD et SoframycineMD. Sulfacétamide sodique Elle jouit d’un large spectre antimicrobien, (Bleph 10MD, DiosulfMD) mais, pourtant, sa popularité diminue au proC’est la première classe d’antibiotiques à fit d’autres agents (p. ex., fluoroquinolones), avoir été utilisée, mais compte tenu de la étant donné une augmentation de la résisrésistance marquée des bactéries Gram-posi- tance des bactéries Gram-positives. Contraitives, la sensation de brûlure à l’instillation et rement aux formulations orales qui ont un les cas d’allergie qui lui sont associés, elle potentiel toxique (neuro/oto/néphrotoxicité), n’est plus employée en première ligne1. Il les préparations ophtalmiques sont généraleexiste une formulation mixte contenant aussi ment bien tolérées1. Cependant, dans l’optide la prednisolone, le BlephamideMD, mais que d’une utilisation en néonatalité, la vigison usage, tout comme celui de toutes les lance est de mise étant donné le métabolisme formulations associant un antibiotique et un immature de l’enfant. www.professionsante.ca juin 2010 vol. 57 n° 3 Québec Pharmacie 11 Place aux questions Macrolides (érythromycine en onguent) L’érythromycine 0,5 % est une solution de traitement sécuritaire et elle est d’ailleurs utilisée dans les hôpitaux comme prophylaxie contre l’ophtalmie néonatale à Neisseria gonorrhoea1. Son spectre d’action contre les bactéries Gram-positives et certains atypiques, son faible coût et sa forme pharmaceutique en font un choix de traitement intéressant pour les cas bénins7. Acide fusidique (FucithalmicMD) Couvrant S. aureus, S. pneumoniae et H. influenzae, ce collyre visqueux est souvent prescrit en pédiatrie. Bien que des études quantitatives de bactériologie n’aient pas été menées chez des enfants de moins de deux ans, l’administration biquotidienne, son spectre d’action et sa forme pharmaceutique en font un agent intéressant5. Les effets indésirables chez les enfants de moins de deux ans seraient semblables à ceux qui se produisent chez les enfants plus vieux (sensation de brûlure passagère et irritation lors de l’administration)8. Fluoroquinolones Parmi les fluoroquinolones, on retrouve : OcufloxMD, CiloxanMD,VigamoxMD, ZymarMD et BesivanceMD. Depuis les années 1990, les fluoroquinolones de deuxième génération, l’ofloxacine et la ciprofloxacine, sont utilisées dans le traitement des infections ophtalmiques. Ces antibiotiques au large spectre (Gram-positives et négatives) sont plus dispendieux, mais ils ont l’avantage de protéger contre Pseudomonas et Hæmophilus, en plus d’être disponibles en onguents dans le cas du Ciloxan 0,3 %. Quant aux fluoroquinolones de quatrième génération, la moxifloxacine (la seule fluoroquinolone qui soit exempte de chlorure de benzalkonium comme agent de conservation, donc moins irritante) et la gatifloxacine, elles disposent du meilleur spectre antimicrobien contre S. aureus, contre les infections résistantes aux macrolides et aussi contre Chlamydia et Hæmophilus. Parmi les rares études d’innocuité menées chez les nouveau-nés, il s’en trouve une qui démontre que le Vigamox est parfaitement toléré9. Cette classe thérapeutique devrait être réservée au traitement des infections sévères, comme celles à Pseudomonas. Par ailleurs, la bésifloxacine, une autre quinolone, a été lancée sur le marché en janvier dernier et elle s’est révélée efficace et sécuritaire lors des études cliniques menées chez les enfants d’un an et plus10 . Discussion Les fluoroquinolones de quatrième génération sont recommandées par certains experts comme traitement de premier recours, surtout dans le cas des infections sévères, étant donné leur grande efficacité, mais, dans le cas d’une infection mineure prise au début des symptômes, le PolysporinMD, l’érythromycine ou le FucithalmicMD seraient des options de traitement valables. Conclusion Quel que soit l’antibiotique privilégié, puisque l’absorption systémique présente un plus grand risque chez le nourrisson en raison de l’immaturité de ses voies métaboliques, un enseignement adéquat sur son administration doit être offert aux parents. Ainsi, une seule goutte doit être instillée à la fois directement dans l’œil ou, si l’enfant est agité, il peut être couché sur le dos et l’on mettra alors une ou deux gouttes dans le coin intérieur de son œil fermé. L’occlusion du conduit naso-lacrymal durant trois à quatre minutes réduira l’absorption systémique et la toxicité jusqu’à 40 %. Quant aux doses à utiliser, il est suggéré de réduire celle pour adulte de moitié chez les enfants de 0 à 2 ans, d’un tiers chez les 2 à 3 ans, puis d’administrer la dose adulte chez les 3 ans et plus7. n Références 1. Lichtenstein S.J. The Diagnosis and Treatment of Bacterial Conjunctivitis in Pediatric Patients. [En ligne.] Medscape; juin 2008 (document consulté le 14 février 2010). cme.medscape.com/viewarticle/575864 2. Tarabishy AB, Jeng BH. Bacterial conjunctivitis : A review for internists. Cleveland Clinic Journal of Medicine 2008; 75(7): 507-12. 3. Granet DB, Dorfman M, Stroman D, Cockrum P. A multicenter comparison of polymixin B sulfate/trimethoprim opthalmic solution and moxifloxacin in the speed of clinical efficacy for the treatment of bacterial conjunctivitis. J Pediatr Ophthalmol Strabismus 2008 Nov-Dec; 45(6): 340-9. 4. Buznach N, Dagan R, Greenberg D. Clinical and Bacterial Characteristics of Acute Bacterial Conjunctivitis in Children in the Antibiotic Resistance Era. The Pediatric Infectious Disease Journal 2005; 24 (9): 823-8. 5. Normann EK, Bakken O, Peltola J, Andreàsson B, Buhl S, et coll. Treatment of acute neonatal bacterial conjunctivitis : A comparison of fucidic acid to chloramphenicol eye drops. Acta Ophthalmol Scand 2002; 80: 183-7. 6. Laferrière C, Marks M. Chloramphenicol : Properties and clinical use. The Pediatric Infectious Disease Journal 1982; 1(4): 257-64. 7. Myers T.M., Wallace D.K., Johnson S.M. Ophtalmic Medications in Pediatric Patients. [En ligne.] Medscape; juin 2005 (document consulté le 14 février 2010). www.medscape.com/viewarticle/504199. 8.Monographie du Fucithalmic dans le CPS. 9. Silver LH, Woodside AM, Montgomery DB. Clinical Safety of Moxifloxacin Ophthalmic Solution 0.5 % (VIGAMOX) in Pediatric and Nonpediatric Patients With Bacterial Conjunctivitis. Surv Ophthalmol 2005; 50:S55–S63. 10.Monographie du Besivance dans le CPS. Question de formation continue 2) Laquelle des affirmations suivantes est fausse ? A. La conjonctivite bactérienne se résout généralement en 10 à 14 jours sans traitement, mais le risque de contagion, ainsi que les conséquences pour les parents justifient souvent l’essai d’un antibiotique. B. Le chloramphénicol est utilisé fréquemment pour traiter les conjonctivites bactériennes chez les jeunes enfants étant donné le peu de résistance des bactéries à son endroit. C. L’onguent d’érythromycine apparaît comme un excellent choix de traitement de la conjonctivite bactérienne peu sévère chez le nourrisson, vu son innocuité établie chez cette clientèle. D. Pour traiter les infections plus sévères chez les jeunes enfants, le Vigamox est un choix intéressant, car il semble très bien toléré et peu de bactéries y sont résistantes. E. Puisque l’absorption systémique peut avoir des répercussions plus importantes chez l’enfant, il convient de bien expliquer aux parents comment administrer les gouttes ophtalmiques. Veuillez reporter votre réponse dans le formulaire de la page 78 12 Québec Pharmacie vol. 57 n° 3 juin 2010 À votre service sans ordonnance Les troubles digestifs traités par l’automédication Un lendemain de vins et fromages ? Une nuit difficile après un repas copieux ? Un excès de café en plus du stress occasionné par un examen ? Bien que certaines personnes soient plus à risque, tout le monde peut souffrir de troubles digestifs à un moment donné. Les symptômes sont généralement temporaires et pourront être éliminés une fois la cause trouvée. Par contre, certains sont suffisamment incommodants pour que les patients consultent un pharmacien. Les troubles digestifs peuvent inclure des brûlures d’estomac, du reflux gastro-œsophagien (RGO), le météorisme, l’éructation et les flatulences. Avec le passage de l’annexe I à l’annexe II pour la ranitidine 150 mg et la famotidine 20 mg, de nouvelles options intéressantes s’ajoutent à l’éventail de médicaments en vente libre (MVL) pour le traitement des différents troubles digestifs, plus particulièrement la dyspepsie, les brûlures d’estomac et le RGO. Nous réviserons donc la liste des MVL pour les troubles digestifs, ainsi que les principaux éléments d’une consultation sur le sujet. L’éructation, le météorisme et les flatulences ont été traités dans la rubrique « À votre service sans ordonnance » du numéro de Québec Pharmacie de juillet-août 2004 et ne feront pas l’objet de cet article. 1. Évaluer l’état du patient (qui, quoi et depuis quand ?) La dyspepsie n’est pas une pathologie en soi, mais un regroupement de symptômes non spécifiques qui peuvent survenir seuls ou en association. Les brûlures d’estomac (pyrosis), le reflux d’acide, les éructations, les ballonnements abdominaux, les nausées, la satiété précoce et la sensation de digestion anormale et/ou lente sont les symptômes qui peuvent se manifester1. Les causes possibles de la dyspepsie sont le RGO, l’ulcère gastrique et duodénal et, très rarement, le cancer de l’estomac1,2. Les brûlures d’estomac ou le pyrosis peuvent se présenter comme une douleur au quadrant supérieur de l’abdomen. C’est une sensation de brûlure au niveau du sternum pouvant irradier à la gorge et durer quelques heures. Cette douleur peut s’aggraver après avoir mangé et peut parfois irradier dans le dos et ressembler à un malaise cardiaque3. En effet, certains symptômes peuvent ressembler à de l’angine de poitrine et être de nature cardiaque. Ainsi, un patient qui n’est pas soulagé dans les 30 minutes suivant la prise d’un antiacide devrait être dirigé vers son médecin. Le pyrosis peut survenir à la suite d’une gastrite, d’un repas ou d’un stress quelconque. De plus, certains patients peuwww.professionsante.ca vent présenter un pyrosis léger, mais ce symptôme peut cacher un problème plus important, tels l’œsophagite de Barrett, l’œsophagite érosive ou, rarement, un adénocarcinome4. Le RGO, aussi nommé « reflux d’acide » ou « régurgitation acide », se décrit par de l’acidité qui remonte dans l’œsophage jusqu’à la gorge5,6,7. Il est causé par l’ouverture spontanée du sphincter œsophagien inférieur (SOI) ou par sa fermeture incomplète, permettant au contenu gastrique de refluer dans l’œsophage. Le patient peut ainsi être interrogé sur la présence d’un goût acide au fond de la bouche5. Non traité, le RGO peut causer une ulcération de l’œsophage. Il est qualifié de léger lorsque la fréquence est faible (moins de trois fois par semaine), de courte durée et de faible intensité, ou si la qualité de vie du patient n’est pas diminuée. Il devient modéré à sévère ou pathologique lorsqu’il se présente plus de trois fois par semaine, qu’il dure plus longtemps, est plus intense et que la qualité de vie est affectée5,8. Certains patients peuvent présenter un RGO léger qui cacherait en réalité un problème plus important. Les fumeurs, les patients obèses et les femmes enceintes sont plus à risque de souffrir de reflux9. Texte rédigé par Marie-Pierre Quirion, étudiante en 3e année du Pharm. D., Université de Montréal. Texte soumis le 15 octobre 2009. Texte final remis le 30 décembre 2009. Révision : Nancy Desmarais, B. Pharm. (Pharmacie Jean-François Martel) et Julie Martineau, B. Pharm. (Pharmacie J. Martineau, J. Riberdy et associés). Remerciements : Stéphanie Saint-Louis, pharmacienne, pour son aide précieuse et sa patience. 2. Vérifier les médicaments d’ordonnance et MVL (dont les PSN) déjà essayés, leur quantité et leur forme Un médecin a-t-il été consulté ? Il faut adresser à leur médecin les patients chez qui les symptômes persistent depuis plus de deux semaines malgré l’usage de MVL ou chez qui les brûlures d’estomac sont similaires à des symptômes d’angine, qui persistent 30 minutes après la prise d’antiacides. Les patients qui présentent des signes alarmants (perte de poids, anémie, anorexie, dysphagie, etc.) devraient aussi être évalués 2,10. En d’autres mots, dans un contexte d’automédication, seules les personnes ayant un reflux léger occasionnel, soit moins de trois fois par semaine, devraient être traitées10. Dans le cas du pyrosis, il faut noter que la fréquence et la gravité des brûlures ne corrèlent pas avec la juin 2010 vol. 57 n° 3 Québec Pharmacie 15 À votre service sans ordonnance présence ou l’étendue d’une atteinte de la muqueuse œsophagienne10. 3. Choisir la meilleure option en fonction du patient et de ses caractéristiques Mesures non pharmacologiques Bien qu’une réponse aux mesures non pharmacologiques ne soit pas possible chez tous les patients, elles devraient être proposées dans le cas de la dyspepsie et du RGO afin que le patient utilise celles qui fonctionnent pour lui. Parmi les modifications à proposer3,5,9,10 : si possible et si connue, éliminer la cause; n éviter les aliments et les breuvages aggravants (chocolat, menthe, agrumes, tomates, aliments gras ou épicés, alcool, café, etc.; n éviter les repas copieux, manger de plus petites portions et plus fréquemment; n éviter, si possible, les médicaments irritants, tels qu’anti-inflammatoires, acide acétylsalicylique (AAS), corticostéroïdes, fer, potassium, bisphosphonates; n cesser de fumer : le tabac inhibe la salive qui sert de tampon majeur. Le tabac pourrait aussi stimuler la production d’acide n n n n n n et favoriser la relaxation du sphincter œsophagien inférieur (SOI), permettant ainsi à l’acide gastrique de refluer; minimiser le stress; perdre du poids, si approprié; éviter de manger trois heures avant le coucher et de se pencher en avant; soulever de six à huit pouces la tête du lit à l’aide d’une planche de 4 x 4 ou en ajoutant un sous-matelas en mousse; l’ajout d’oreillers ne ferait qu’augmenter la pression intragastrique, et les symptômes n’en seraient pas améliorés; éviter de porter des vêtements serrés. Tableau I Antiacides et anti-H2 (non exhaustif) Produits Mg2+Al+CaCO3NaHCO3SubsalicyclateAlginateRanitidineFamotidineP de bismuth de sodium ANTIACIDES Gaviscon liquide 20 mg/ml 50 mg/ml Gaviscon Régulier 40 mg 200 mg Gaviscon Extra-Fort 63 ml 313 mg Pepto-Bismol comprimé 262 mg Pepto-Bismol Extra-Fort liquide 35,2 mg/ml Pepto-Bismol Original à croquer 350 mg 262 mg Maalox à croquer 600 mg Maalox à croquer, formulation nuit 500 mg 200 mg Maalox Extra-Fort à croquer 1000 mg Maalox Régulier liquide 40 mg/ml 40 mg/ml Maalox Extra-Fort liquide 80 mg/ml 80 mg/ml Maalox Multi-action liquide 35 mg/ml Phillips, Lait de magnésie usp 80 mg/ml Pepcid Complet, 165 mg 800 mg 10 mg Double action, à croquerOU Tums 750 mg 750 mg Tums 500 mg 500 mg Tums 1000 mg 1000 mg Diovol Plus (suspension) (par 5 ml) 200 mg 165 mg Diovol Plus (co croq.) 100 mg 300 mg Diovol Plus Action rapide (co croq. ) 200 mg 200 mg Rolaids Régulier 110 mg 550 mg Rolaids Bouchées tendres 1177 mg Rolaids Plus Soulagement des gaz 1177 mg Alka Seltzer AAS (effervescent) 1916 mg Eno Salt (effervescent) Gelusil (co croq.) 200 mg 153 mg ANTI-H2 Zantac 75 mg 75 mg Zantac 150 mg 150 mg Pepcid AC 10 mg Pepcid AC (concentration maximale) 20 mg Légende : Mg2+ : magnésium; Al+ : aluminium; CaCO3 : carbonate de calcium; NaHCO3 : bicarbonate de sodium; MgCO3 : carbonate de magnésium; Al(OH)3 : hydroxyde d’aluminium 16 Québec Pharmacie vol. 57 n° 3 juin 2010 Les troubles digestifs traités par l’automédication Mesures pharmacologiques prolongée des MVL pourrait ainsi retarder le pour soulager les symptômes de brûlure diagnostic et le traitement approprié de ces d’estomac5. Les antiacides regroupent les produits faits pathologies. de sels de calcium, d’aluminium, de magnéLes antiacides sium ou de sodium, ou d’une combinaison Lors de brûlures d’estomac mineures et de de ceux-ci4. Ils neutralisent l’acidité dans l’esRGO léger et occasionnel, les antiacides peu- tomac et, par le fait même, inhibent la pepvent être proposés aux patients pour soula- sine qui peut endommager l’œsophage lors ger rapidement leurs symptômes (début du reflux 12. L’activité diminuée de cette d’action < 30 minutes) pendant 20 à enzyme est par ailleurs plus marquée avec 60 minutes lorsque pris à jeun ou jusqu’à l’aluminium et le calcium puisque ces dertrois heures s’ils sont pris pendant le repas ou niers s’absorbent à elle4. Dans le cas de reflux, une heure après4,9,10. Ils représentent généra- l’effet des antiacides s’explique surtout par lement un traitement de première intention leur « adhérence » à la paroi œsophagienne pour ensuite neutraliser, pendant au moins 90 minutes après ingestion, l’acide qui se trouve dans ce tube4,9. De hautes doses sont nécessaires afin d’augmenter significativement le pH gastrique, contrairement aux PosologieRemarques inhibiteurs des pompes à protons qui, eux, diminuent le taux de sécrétion acide. Cependant, une dose excessive d’antiacide peut 10-20 ml si symptôme (max. 80 ml/jr) mener à la surproduction de bicarbonate. 2-4 cos (max. 16 co/jr) Boire beaucoup d’eau L’excès de bicarbonate sera ensuite absorbé 2-4 cos si symptôme (max. 12/jr) Boire beaucoup d’eau dans le duodénum, activant la production 2 comprimés si symptômeNoircissement possible de la langue et des selles; d’acide gastrique et occasionnant de l’acidité 30 ml si symptôme à éviter chez les enfants, car peut rebond4. 2 cos si symptôme causer le syndrome de Rye Chaque sel renferme des particularités. Le 2-3 cos si symptôme (max. 12/jr) Boire beaucoup d’eau calcium se retrouve sous forme de carbonate 2-3 cos le jour et 3-4 cos la Boire beaucoup d’eau et se dissout lentement dans l’estomac pour nuit si symptôme (max. 8/jr) former du chlorure de calcium, du dioxyde 1-2 cos si symptôme (max. 8/jr) Boire beaucoup d’eau de carbone et de l’eau. Environ 90 % du 10-20 ml si symptôme (max. 80 ml/jr) Boire beaucoup d’eau chlorure de calcium formé est converti en 10-20 ml si symptôme (max. 60 ml/jr) Boire beaucoup d’eau sel de calcium insoluble ne pouvant être 30 ml si symptôme (max. 120 ml/jr)Peut causer le noircissement de la langue et absorbé, ce qui pourrait causer de la des selles; à éviter chez les enfants constipation4. 5-15 ml si symptôme Boire beaucoup d’eau Le sodium, lui, est vendu en sels de bicar1 co si symptôme et un 2e si soulagement partielContre-indiqué pour les personnes bonate. C’est l’antiacide qui agit le plus rapiOU 1 co en prév. (max. 2/jr) avec des problèmes rénaux dement. Étant donné la rapidité d’action du 2-3 cos prn (max. 10 cos/jr) dioxyde de carbone formé, les effets indési2-4 cos prn (max. 16 cos/jr) rables du bicarbonate de sodium sont les fla1-2 co prn (max. 8 cos/jr) tulences, les éructations et la distension gas2-4 c à t prn entre les repas et hsSans sucre trique. Par ailleurs, l’excès de bicarbonate 2-4 cos prn entre les repasContient aussi MgCO3 en gel co-déshydraté peut causer une légère alcalinisation de et hs (max. 16 cos/jr) et 184 mg d’Al(OH)3 l’urine en plus, possiblement, d’une alcalose 2-4 cos prn entre les repas et hs (max. 16 cos/jr) métabolique. Le bicarbonate de sodium ne 1-2 pastilles prn (max. 14/jr) devrait pas être recommandé en raison de sa 1-2 bouchées prn (max. 6/jr) quantité élevée de sodium4. 1-2 cos prn (max. 6/jr) Le magnésium, ou plus précisément l’hy2 cos dissous q4h prn (max. 8 cos/jr)AAS 325 mg droxyde de magnésium, réagit rapidement Dissoudre un sachet dans 6 oz après un repasCitrate de sodium 2680 mg/5 g/dose; avec l’acide gastrique pour former du chloet hs (max. 5/jr) renferme 855 mg de sodium rure de magnésium qui est excrété par les 2-4 cos qid entre les repas et hs reins4. Quant à l’hydroxyde d’aluminium, il se 1 co prn, répéter après 1 heure prn (max. 2 cos/jr) dissout lentement dans l’estomac en réagis1 co 30-60 min avant le déjeuner (max. 2 cos/jr) sant avec l’acide gastrique. Quinze à 30 % du 1 co 10-15 min avant un repas, répéter chlorure d’aluminium formé lors de cette si les symptômes réapparaissent (max. 2 cos/jr) réaction est excrété par les reins. 1 co 10-15 min avant un repas, répéter Étant donné le risque d’accumulation, on si les symptômes réapparaissent (max. 2 cos/jr) évitera l’hydroxyde de magnésium et l’hydroxyde d’aluminium chez les insuffisants rénaux4. Le tableau I comprend l’arsenal thérapeutique offert en vente libre à ce jour. Voici quelques règles générales d’utilisation et approches personnalisées. Rappelons qu’il est possible de soulager ces différentes affections à l’aide de produits en vente libre pendant un maximum de deux semaines. Si ces maux sont chroniques, les patients doivent être adressés à leur médecin. En fait, il peut s’agir de troubles fonctionnels ou de symptômes d’un trouble sous-jacent, tel qu’un ulcère, la bactérie Helicobacter pylori ou même un carcinome. L’utilisation www.professionsante.ca juin 2010 vol. 57 n° 3 Québec Pharmacie 17 À votre service sans ordonnance Les anti-H2 ger les brûlures d’estomac (p. ex., Pepto-BismolMD et Maalox Multi-ActionMD). Ces formulations sont à éviter puisqu’elles irritent l’estomac. Le subsalicylate de bismuth, tout comme l’AAS, est à éviter chez les moins de 18 ans. On retrouve aussi en vente libre les antihistaminiques H2, ou anti-H2, tels que la famotidine et la ranitidine. Les récepteurs H2 retrouvés sur les cellules pariétales de l’estomac sont, eux aussi, responsables de la sécrétion d’acide9. Leur blocage permet de diminuer le taux de sécrétion d’acide dans les 1-2 heures après administration, et ce, pendant quelques heures9. Ceux-ci permettent un soulagement de plus longue durée, mais avec un début d’action plus lent. C’est pourquoi on les prendra généralement une heure avant le repas5,9. Ils sont utiles pour prévenir la dyspepsie, en particulier le pyrosis et le RGO, lorsqu’un repas riche et copieux est envisagé. La ranitidine en vente libre se trouve sous forme de comprimés de 75 ou 150 mg et, pour prévenir les symptômes, devrait normalement être administrée 30 à 60 minutes avant le repas ou la boisson pouvant occasionner un reflux ou des brûlures d’estomac6,11. Quant à la famotidine, la dose est de 10 mg 30-60 minutes avant le repas, en prévention, avec un maximum de deux comprimés par jour ou un comprimé de 20 mg. Les doses d’anti-H2 doivent être diminuées en présence d’une insuffisance rénale modérée à sévère. On peut retrouver les antiacides et les antiH2 dans une même formulation assurant un soulagement rapide (15 minutes) et de longue durée (6-8 heures)9,12. Ce type de formulation empêche mécaniquement l’acide de l’estomac de remonter dans l’œsophage et permet de neutraliser l’acide. Rappelons que ces associations ne sont avantageuses que pour un usage sporadique et non comme prophylaxie du pyrosis9. Chez les patients insuffisants rénaux, on préférera les chélateurs de phosphate en tant qu’antiacides. Le plus approprié pour cette clientèle serait le carbonate de calcium, plutôt que l’hydroxyde d’aluminium, puisque ce dernier pourrait s’accumuler. Ces deux sels sont normalement utilisés chez ces patients pour diminuer le niveau de phosphate sérique. Le sel de calcium est normalement administré en mangeant pour chélater le phosphate alimentaire4. Pour les patients souffrant d’insuffisance rénale sévère, la dose maximale de ranitidine de 150 mg per os par jour est recommandée13. Subsalicylate de bismuth Hypertension ou insuffisance cardiaque sodium), qui ont une teneur importante en sodium et sont absorbés systémiquement, devraient être évités chez les patients hypertendus ou en présence d’insuffisance cardiaque4. Insuffisance pancréatique Acide alginique L’acide alginique constitue une barrière mécanique en formant une mousse qui empêche le contenu de l’estomac de remonter vers l’œsophage, protégeant ainsi la muqueuse. L’acide alginique devient alors utile à ceux qui présentent un reflux et, lorsqu’accompagné d’un antiacide, il se prend immédiatement après le repas, si présence de pyrosis ou de reflux, et au coucher lorsque le reflux se manifeste la nuit9. Approches personnalisées sur les troubles digestifs Vous trouverez au tableau II un résumé de la médication suggérée pour chacune des situations particulières. Insuffisance rénale Chez ces patients, il faut éviter les antiacides à base de calcium ou de magnésium puisque ces sels aggravent la stéathorrée normalement présente chez ces sujets. Par contre, l’hydroxyde d’aluminium est adéquat puisqu’il diminuerait la présence de graisse dans les selles. Insuffisance hépatique Dans le cas des patients ayant une insuffisance hépatique, les doses de ranitidine pourraient être réduites puisque cette dernière est métabolisée par le foie, contrairement aux autres anti-H26. D’anciennes études suggéraient la diminution de la dose lors d’une insuffisance hépatique sévère sans toutefois apporter davantage de précisions quant à cet ajustement. La monographie du ZantacMD, elle, ne mentionne aucun ajustement pour ces sujets. Cependant, elle souligne que des troubles hépatiques majoritairement réversibles ont été rapportés par l’administration per os de la ranitidine. Dans ce cas, la ranitidine doit être arrêtée13. Pédiatrie Évitez tout produit renfermant de l’acide salicylique. En général, on référera nos jeunes patients au médecin afin de trouver la cause du problème digestif et de le traiter adéquatement. En revanche, les enfants de 12 ans et plus peuvent être traités par des MVL à moins qu’ils ne souffrent de symptômes importants14. On trouve aussi le subsalicylate de bismuth Plusieurs antiacides (p. ex., bicarbonate de Polypharmacie dans des formulations permettant de soula- sodium, citrate de sodium ou alginate de La modification du pH gastrique est à l’origine de plusieurs interactions médicamentmédicament puisque l’ionisation (p. ex., Tableau II nitrofurantoïne) et la dissolution de certains Approche personnalisée4,6,13,14 médicaments (p. ex., pénicillines) sont affectées, modifiant ainsi leur taux d’absorption. Cas À privilégier Les acides faibles sont davantage ionisables Brûlures d’estomac et reflux anticipésAnti-H2 ou acide alginique en association et ainsi moins bien absorbés, tandis que les (ex. : repas épicé) bases faibles sont moins ionisables, donc Symptômes nocturnesAnti-H2 davantage absorbées. Dans d’autres cas, l’inInsuffisance rénaleCarbonate de calcium teraction consiste en la complexation des ou hydroxyde d’aluminium (2e choix) sels, sauf le bicarbonate de sodium, avec les Hypertension ou insuffisance cardiaque Éviter les antiacides contenant du sodium médicaments4 (p. ex., phénytoïne, certains Insuffisance pancréatique Hydroxyde d’aluminium antibiotiques). Il faut ainsi espacer de Insuffisance hépatique ↓ dose de ranitidine deux heures la prise du médicament sur Pédiatrie MVL seulement chez ≥ 12 ans ordonnance avec ces médicaments. PolypharmacieEspacer de 2 h la prise des autres médicaments L’absorption de la lévodopa est augmentée avec les antiacides par les antiacides pour une autre raison que les deux premières : les antiacides modifient 18 Québec Pharmacie vol. 57 n° 3 juin 2010 Les troubles digestifs traités par l’automédication parfois la motilité gastrique en accélérant le temps de vidange gastrique. La durée de contact du médicament avec l’acidité gastrique se voit diminuée, de même que la dégradation du médicament, ce qui augmente son absorption. Les sels d’aluminium et de magnésium altèrent le pH urinaire en plus du pH gastrique : attention aux médicaments éliminés par les reins, leur taux de réabsorption pouvant être altéré4. Conclusion Les causes exactes du RGO demeurent incertaines. La relaxation du SOI lorsque l’œsophage est contracté a été observée chez ceux qui souffrent de ce problème. Sinon, des anormalités structurelles, telles qu’une hernie hiatale, peuvent être à l’origine du reflux. D’autres facteurs comme la grossesse peuvent aussi en être responsables5. Si les symptômes persistent après deux semaines de traitement par des médicaments en vente libre, le patient devrait consulter un médecin3,5,6. N’oubliez pas d’indiquer au patient d’agiter les formulations liquides avant leur utilisation et d’espacer de deux heures la prise de ces médicaments en vente libre avec tout autre médicament. Autrement, il peut également utiliser l’option des comprimés à croquer. Pour conclure, tout antiacide ou anti-H2 devrait être utilisé avec précaution pour toute population. n Références 1. Van Zanten VSJ, Flook N, Chiba N, et coll. An evidence-based approach to the management of uninvestigated dyspepsia in the era of Helicobater pylori. CMAJ 2000; 162. 2. Hunt RH. Habit, Prejudice, Powerand Politics : Issues in the conversion of H2-Receptor Antagonists to Over-TheCounter Use. Can Med Assoc J 1996; 154(1) : 49-53. 3. American College of Gastroenterology. The word on GERD. 2006 [En ligne. Page consultée le 30 août 2009.] www.acg.gi.org/patients/gerd/word.asp 4. Maton PN, Burton ME. Antacids Revisited : A review of their clinical pharmacology and recommended therapeutic use. Drugs 1999 ; 57 (6) : 857-67. 5. National Institute of Health. National Digestive Diseases Information Clearinghouse. Heartburn, Gastroesophageal Reflux (GER), and Gastroesophageal Reflux Disease (GERD). 2007. [En ligne. Page consultée le 10 septembre 2009.] http://digestive.niddk. nih.gov/ddiseases/pubs/gerd/gerd.pdf 6. AHSP Consumer Medication Information. Ranitidine. 2003 [En ligne. Page consulté le 15 septembre 2009.] www.ncbi.nlm.nih.gov/bookshelf/br.fcgi?book=meds &part=a601106 7. Jones R, Liker HR, Ducrotté P. Relationship between symptoms, subjective well-being and medication use in gastroesophageal reflux disease. Int J Clin Pract, August 2007; 61(8) : 1301-07. 8. Armstrong D, Marshall JK, Chiba N, et coll. Canadian consensus conference on the management of gastroesophageal reflux disease in adults – update 2004. Can J Gastroenterology 2005; 19 :15. énoncé 9. 9. Robinson M. What is «Appropriate» Therapy for Intermittent Heartburn ? Medscape Today 2008. [En ligne. Page consultée le 15 septembre 2009.] www.medscape.com/viewprogram/2809 10. AstraZeneca. GERD.COM – How We Are Treating GERD. 2006 [En ligne. Page consultée le 15 septembre 2009.] www.gerd.com/professional/treating-gerd.aspx 11. Jankowski J, Jones J, Delaney B, Dent J. 10 minute consultation : Gastro-oesophageal reflux disease. British Medical Journal. 2002 ; 325(7370) : 945. 12. American Academy of Family Physicians. Family Doctor. Dyspepsia : What It Is and What to Do About It. 2006. [En ligne. Page consultée le 30 août 2009.] www.familydoctor.org/online/famdocen/home/ common/digestive/disorders/474.html 13. Association des pharmaciens du Canada. e-cps : français : Monographie du médicament : Zantac. 2009 [En ligne. Page consultée le 25 avril 2010.] https://www.e-therapeutics.ca/cps.showMonograph.action?simpleMonographId=m594801 - m594 801n00017 14. Saskatoon Health Region. RxFiles – Drug Tx Info. 2008. [En ligne. Page consultée le 28 décembre 2010.] www.rxfiles.ca/rxfiles/modules/druginfoindex/druginfo.aspx Questions de formation continue 3) Parmi les patients suivants, lequel peut être traité par des MVL pour des troubles digestifs ? A.Patient âgé d’une cinquantaine d’années, ayant des brûlures d’estomac et dont la douleur irradie dans le bras gauche. B.Patiente enceinte désirant soulager ses reflux occasionnels. C. Patient pour qui les symptômes nocturnes de dyspepsie ne sont pas soulagés ni par les antiacides, ni par un anti-H2. D.Patient chez qui la prise quotidienne d’une dose adéquate d’antiacide pendant deux semaines n’a pas soulagé les symptômes diurnes. 4)Chez lequel de ces patients la prise du MVL spécifié ne devrait pas être évitée pour soulager la dyspepsie ? A.Chez un insuffisant pancréatique, les antiacides à base de calcium. B.Chez un enfant de 12 ans, une cuillère à thé de Pepto-BismolMD (subsalicylate de Bismuth). C.Chez l’insuffisant hépatique, des doses élevées de ranitidine. D.Chez tous les patients, la prise concomitante de ciprofloxacine au même moment que le carbonate de calcium avant un repas. E.Chez un hypertendu, la prise d’un anti-H2. Veuillez reporter vos réponses dans le formulaire de la page 78 www.professionsante.ca juin 2010 vol. 57 n° 3 Québec Pharmacie 19 Avez-vous entendu parler de... La desvenlafaxine (PristiqMD) La dépression majeure est une maladie fréquente qui a plusieurs conséquences néfastes dans la vie quotidienne. En effet, elle peut résulter en une diminution de la qualité de vie, des problèmes dans les relations interpersonnelles, de l’absentéisme au travail ou à l’école, des maladies chroniques et des suicides1,2. Cette maladie représente 10 à 14 % des consultations chez le médecin3. Au Canada, environ 11 % des hommes et 16 % des femmes feront une dépression majeure au cours de leur vie1. Le choix d’un antidépresseur repose principalement sur les caractéristiques des personnes affectées (symptômes observés, âge, état physique et présence de maladies concomitantes), ainsi que sur le profil d’effets indésirables et sur l’innocuité du médicament. Fait à noter, l’usage des antidépresseurs a pratiquement doublé de 1995 à 2002 au Canada. Parmi toutes les personnes traitées, environ la moitié répond à un premier antidépresseur, alors que les autres présentent des symptômes persistants3. Texte rédigé par Julie Grenier, B.Pharm., M.Sc., Pharmacie Laurier Lavoie et associés. Texte original remis le 23 juillet 2009. Texte final remis le 25 novembre 2009. Révision : Nathalie Dion, B.Pharm., M.Sc., pharmacienne, Institut universitaire en santé mentale de Québec, et professeure de clinique, Faculté de pharmacie, Université Laval, Québec. La dépression est une pathologie complexe et multifactorielle. Parmi les facteurs pouvant l’expliquer, mentionnons les facteurs neurobiologiques, génétiques et psychosociaux4. C’est dans les années 1960 que l’on a établi pour la première fois que la dépression pourrait résulter d’une déficience de certains neurotransmetteurs (entre autres, la sérotonine, la noradrénaline et la dopamine)4. Récemment, on a avancé que la réponse aux antidépresseurs pourrait être modulée par certains polymorphismes au niveau des monoamines. De plus, les systèmes neuroendocriniens et hormonaux, ainsi que les neuropeptides pourraient être impliqués dans la physiopathologie de la dépression. Les sujets soumis à un stress chronique et à des épisodes dépressifs persistants ont démontré une atrophie de l’hippocampe qui pourrait être à l’origine des déficits cognitifs présents lors de la dépression. En ce qui concerne les facteurs génétiques, le risque de présenter un épisode dépressif s’accroît de 1,5 à 3 fois lorsqu’un parent du premier degré a déjà souffert d’une dépression. De plus, les gènes pourraient également avoir un impact sur la réponse aux antidépresseurs en raison d’un polymorphisme au niveau des transporteurs de la sérotonine et de la noradrénaline. Sur le plan psychosocial, le deuil, la perte d’emploi et l’isolement sont des facteurs prédisposant à la dépression. Tableau I Principaux paramètres pharmacocinétiques de la desvenlafaxine et de la venlafaxine Biodisponibilité Cmax T½ Clairance, orale élimination Desvenlafaxine 80 % 7,5 h 11 hUrinaire (inchangée) 45 %, Glucuronidation 19 %, Oxydation 5 % Venlafaxine 45 % 6,0 h 15 hUrinaire (inchangée) 5 %, Conjuguée 26 %, Non conjuguée 29 % 20 Québec Pharmacie vol. 57 n° 3 juin 2010 Liaison aux protéines 30 % 27 % Parmi les antidépresseurs les plus récents, mentionnons la mirtazapine (RemeronMD), l’escitalopram (CipralexMD), la duloxétine (CymbaltaMD) et la desvenlafaxine (PristiqMD). La desvenlafaxine a été commercialisée au Canada le 4 février 2009 par la compagnie Wyeth. Pharmacologie Mécanisme d’action de la desvenlafaxine La desvenlafaxine, principal métabolite actif de la venlafaxine (Effexor XRMD), est un inhibiteur du recaptage de la sérotonine et de la noradrénaline (IRSN)2,4. Cette nouvelle molécule possède peu, voire aucune affinité avec les récepteurs cholinergiques, histaminergiques et alpha-adrénergiques-1. Pharmacocinétique La cinétique de la desvenlafaxine a été étudiée chez plus de 600 sujets en bonne santé, incluant ceux qui étaient atteints d’insuffisance rénale ou hépatique. À la suite de l’administration orale, la concentration maximale est atteinte après 6 à 10 heures et la biodisponibilité est de 80 %, indépendamment de la nourriture. La liaison aux protéines plasmatiques est de seulement 30 %. Le métabolisme de la desvenlafaxine se fait en grande partie par glucuronoconjugaison via les UGT, et de façon minime par oxydation, via les CYP450-3A4. La transformation de la venlafaxine en desvenlafaxine dépend des CYP450-2D6, mais cette voie ne semble pas con t r i bu er a u m é t a b o l i s m e de l a desvenlafaxine. Les études in vitro ont montré une légère inhibition possible des CYP450-2D6 pour la desvenlafaxine (peu significative cliniquement) et aucune induction enzymatique. Il n’y aurait donc pas de différence pharmacocinétique chez les métaboliseurs lents ou rapides des CYP450-2D6 avec la desvenlafaxine, contrairement à ce qui a été observé avec la venlafaxine. Ainsi, les métaboliseurs lents du CYP450-2D6 (5 à 10 % de la population caucasienne) risquent moins de présenter des effets indésirables avec la desvenlafaxine qu’avec la venlafaxine5. L’élimination La desvenlafaxine (PristiqMD) de la desvenlafaxine se fait principalement sous forme inchangée dans l’urine (45 %) et par glucuronidation (19 %). En ce qui a trait à la dialyse, aucune modification de dose n’est nécessaire. Les principales caractéristiques pharmacocinétiques de la desvenlafaxine et de la venlafaxine sont présentées au tableau I. Indications et études cliniques La desvenlafaxine est indiquée au Canada pour le soulagement des symptômes du trouble dépressif majeur3 et est approuvée aux ÉtatsUnis également pour cette indication. Au total, huit études cliniques ont été publiées sur la desvenlafaxine; une étude n’a pas été publiée6. La commercialisation du produit fait suite à la publication de quatre études positives de moins de huit semaines6,9. Deux d’entre elles seront présentées ci-dessous7,8. Actuellement, on mène des études cliniques afin d’obtenir d’autres indications, entre autres pour le soulagement des bouffées de chaleur secondaires à la ménopause10. La première étude compare la desvenlafaxine au placebo dans le traitement du trouble dépressif majeur7. Les doses fixes de 50 ou 100 mg de desvenlafaxine une fois par jour ont été comparées au placebo pendant 56 jours, suivies d’une dose de placebo ou de desvenlafaxine 50 mg par jour pour une semaine de sevrage. L’évaluation des modifications à l’échelle d’Hamilton (HAM-D17), qui permet de coter la sévérité des symptômes des patients atteints d’une dépression majeure grâce à 17 questions, était l’issue primaire. Les issues secondaires incluaient les changements sur les échelles d’impression clinique globale (CGI-I), de MADRS et de CGI-S, sur l’échelle visuelle analogue de l’intensité de la douleur (VAS-PI) et sur l’HAM-D6 (qui contient six données de la HAM-D17 : humeur dépressive, culpabilité, travail et centres d’intérêt, inhibition, anxiété psychotique et symptômes somatiques généraux). Les 447 sujets étudiés ont été recrutés dans 25 centres à travers les États-Unis. Ils avaient reçu un diagnostic de trouble dépressif majeur isolé ou récurrent selon le DSM-IV. On note, pour l’issue primaire, une amélioration significative sur l’échelle HAM-D17 pour le groupe recevant 50 mg par jour par rapport au placebo (p = 0,018). Cette différence statistiquement significative n’a pas été démontrée avec la dose de 100 mg de desvenlafaxine. Cependant, des améliorations significatives sur les échelles HAM-D6 et VAS-PI ont été démontrées avec la dose de 100 mg. La xérostomie, la constipation, l’insomnie, la diminution de l’appétit, l’hyperhidrose et les étourdissements sont les effets indésirables les plus souvent rapportés dans cette étude. Seul cet essai tient compte de l’évaluation de la douleur et il est intéressant de constater une diminution des douleurs dans les groupes traités puisque celles-ci peuvent représenter une cause du trouble dépressif majeur. La deuxième étude compare également la desvenlafaxine (50 ou 100 mg une fois par jour) avec le placebo dans le traitement du trouble dépressif majeur, pendant huit semaines8. L’objectif primaire était de mesurer les changements sur l’échelle HAM-D17 pour la dépression, et les objectifs secondaires étaient d’évaluer l’évolution des sujets selon les échelles CGI-I d’amélioration et de sévérité de la maladie. Les sujets sélectionnés venaient de 44 centres de recherche en Europe et en Afrique du Sud. Les pointages moyens avant l’étude, sur l’échelle HAM-D17 étaient de 24 pour l’ensemble des sujets et de 5 sur l’échelle CGI-S. Au terme des huit semaines de l’essai, une différence significative a été mise en évidence sur l’échelle HAM-D17 pour les groupes desvenlafaxine 50 mg (p = 0,002) et 100 mg (p < 0,001). Des différences significatives ont aussi été notées en ce qui concerne l’issue secondaire, soit une amélioration au travail et dans la vie sociale et familiale. Les effets indésirables rapportés le plus fréquemment ont été les nausées, les étourdissements, l’insomnie et la constipation. Ces deux études présentent une bonne validité en raison de la répartition aléatoire des sujets, de l’analyse en intention de traiter et du fait www.professionsante.ca qu’elles sont à double insu. Par contre, dans les deux cas, les sujets anxieux, de même que ceux avec des antécédents d’abus de substances ont été exclus. L’application de ces études en clinique est limitée en raison de l’utilisation de doses fixes et de leur courte durée (sept et huit semaines) qui ne couvrent que la phase aiguë du traitement. La dernière étude a sélectionné des sujets traités en soins ambulatoires par un placebo ou une dose de 200 à 400 mg de desvenlafaxine une fois par jour, pendant huit semaines9. L’objectif primaire était de mesurer les changements sur l’échelle HAM-D17 et les objectifs secondaires portaient sur l’évaluation de l’évolution des sujets selon l’échelle CGI-I et les échelles d’amélioration et de sévérité de la maladie. Les sujets sélectionnés venaient de 12 centres de recherche aux États-Unis. Les pointages moyens avant l’étude sur l’échelle HAM-D17 étaient de 23 pour l’ensemble des sujets et de 4,3 sur l’échelle CGI-S. Au terme des huit semaines de l’essai, aucune différence significative n’a été démontrée entre les groupes desvenlafaxine et placebo pour l’issue primaire (HAM-D17) (p = 0,78). Pour les issues secondaires, la réponse au traitement n’a pas été significative sur les échelles d’amélioration et de sévérité de la maladie. L’effet indésirable le plus souvent rapporté était les nausées. La xérostomie, l’hyperhidrose, l’insomnie et la somnolence ont été les autres effets les plus souvent signalés. Les résultats de cette étude randomisée, à double insu, contrôlée, avec groupe placebo, semblent valables, car l’analyse a inclus tous les patients enrôlés selon l’approche en intention de traiter. Par contre, la durée moyenne de l’épisode dépressif était plus longue dans le groupe placebo (27 mois, comparativement à 19 mois), ce qui porte à croire que les patients du groupe placebo étaient plus gravement malades ou plus résistants aux traitements. Aucune différence significative n’a été révélée entre les juin 2010 vol. 57 n° 3 Québec Pharmacie 21 Avez-vous entendu parler de... deux groupes, ce qui pourrait s’expliquer par le résultat sur l’échelle HAM-D17 de seulement 23, soit un résultat faible qui permet difficilement d’établir une différence avec le placebo. De plus, cette étude est difficilement applicable en clinique puisque les doses utilisées (200 ou 400 mg) sont supérieures aux doses maximales recommandées par le fabricant. Sopko et coll. ont utilisé la banque de données PubMed pour comparer la venlafaxine et la desvenlafaxine, et trouver une place à cette dernière dans l’arsenal thérapeutique11. Les auteurs concluent que les deux produits offrent une efficacité similaire pour le traitement de la dépression majeure et présentent un profil d’effets indésirables semblable. L’avantage de la desvenlafaxine se situe chez les métaboliseurs lents des CYP450-2D6 ou lors de l’utilisation d’inhibiteurs ou de substrats des CYP450-2D6. Pour le traitement de la dépression majeure, une étude de phase III, multicentrique, randomisée à double insu, comparant la desvenlafaxine (50 et 100 mg) au placebo, comportait aussi un groupe parallèle avec la duloxétine12. Cette étude a été menée auprès de 638 sujets dans 21 centres aux États-Unis. L’issue primaire était l’amélioration du pointage de l’échelle HAM-D17. Une amélioration significative par rapport au placebo a été objectivée pour la desvenlafaxine 100 mg par jour (p = 0,028) et la duloxétine (p = 0,047). Le design de l’étude ne permettait pas de comparer la desvenlafaxine à la duloxétine. Effets indésirables Le profil d’effets indésirables ressemble à celui des autres antidépresseurs ISRS et IRSN. Dans les études cliniques, la tolérance à la desvenlafaxine à des doses de 50 mg, 100 mg, 200 mg et 400 mg prises une fois par jour a été comparée à celle du placebo. Les effets indésirables rapportés avec une incidence supérieure à 5 % sont les nausées, les céphalées, la sécheresse de la bouche, l’hyper hidrose, les étourdissements, l’insomnie, la constipation, la diminution de l’appétit, la diarrhée, la fatigue, les tremblements, le dysfonctionnement érectile et l’éjaculation retardée3. Les dysfonctionnements sexuels surviennent chez près d’un tiers des personnes traitées par un ISRS4, tandis qu’environ seulement 1 à 6 % des hommes et 1 à 2 % des femmes traités par la desvenlafaxine rapportent ces effets indésirables3. À titre comparatif, ces effets sont rapportés chez 16 % des personnes qui utilisent la venlafaxine13 et chez 3 à 4 % de celles qui prennent de la duloxétine12. Comme les autres IRSN, la desvenlafaxine peut entraîner des troubles cardiovasculaires, tels que la tachycardie et les palpitations, mais elle semble avoir un effet moindre au niveau de l’élévation de la tension artérielle3,12,13. Le phénomène d’hypotension orthostatique est peu fréquent (< 1 %). Aucune différence significative sur le QTc n’a été notée malgré l’administration de doses de 200 à 600 mg. Les effets sur le poids sont variables, la perte et le gain de poids sont tous deux rapportés chez 1 à 10 % des sujets. En ce qui concerne les tests de laboratoire, de fortes doses ont entraîné des hausses du cholestérol total, du cholestérolLDL et des triglycérides dans les études qui ont suivi la commercialisation. Les principaux effets indésirables sont présentés au tableau IV. Mise en garde et contre-indications L’hypersensibilité à la desvenlafaxine ou à l’une des composantes de la formulation est une contre-indication. Ce médicament ne doit pas être utilisé chez les personnes qui prennent un inhibiteur de la monoamine oxydase (IMAO) ou qui en ont pris durant les 14 jours précédents. Après avoir cessé la desvenlafaxine, il est nécessaire d’attendre au moins sept jours avant d’entreprendre un traitement par IMAO. L’innocuité du produit reste à prouver durant la grossesse et il est important d’évaluer les risques, comparativement aux bénéfices, dans ce contexte. La monographie recommande de choisir entre la prise du médicament et l’allaitement puisque le produit est excrété dans le lait maternel et pourrait engendrer des effets indésirables sérieux chez le nourrisson. La desvenlafaxine n’est pas indiquée chez la clientèle pédiatrique, soit les enfants et les adolescents de moins de 18 ans, puisqu’aucune donnée n’est disponible en ce qui concerne son innocuité et son efficacité3. À la suite de l’analyse de nombreuses données, Santé Canada a émis, en juin 2004, une Tableau II Principales études sur la desvenlafaxine Auteurs et devis de l’étude Population à l’étude Groupes de traitementRésultats Commentaires Liebowitz MR et coll.7N : 447 Groupe placebo Différence significative Étude à répartition aléatoire, sur l’échelle HAM-D1 multicentrique, double insu, > 18 ans Groupes desvenlafaxine (p = 0,018) avec 50 mg avec placebo 50 ou 100 mg par jour par jour, mais non signi Diagnostic primaire de trouble ficative (p = 0,065) Durée : 8 semaines dépressif majeur selon le DSM-IV avec 100 mg par jour Boyer P et coll.8N : 483 Groupe placebo Différence significativeLe nombre d’abandons Étude à répartition aléatoire, sur l’échelle HAM-D17 de l’étude est multicentrique, double insu > 18 ans Groupes desvenlafaxine (p = 0,02 et p < 0,001) semblable pour les contre placebo, doses fixes 50 ou 100 mg par jour trois groupes étudiés. Diagnostic primaire de trouble Durée : 8 semaines dépressif majeur selon le DSM-IV Feiger AD et coll.9N : 235 Groupe témoin Aucune différenceLes abandons sont Étude à répartition aléatoire, placebo significative significativement plus multicentrique, double insu > 18 ans sur l’échelle élevés chez les sujets contre placebo, doses flexibles Groupes traitements HAM-D17 traités (p = 0,008). Diagnostic primaire de trouble desvenlafaxine Durée : 8 semaines dépressif majeur selon le DSM-IV 100-400 mg par jour Légende : N : nombre de sujets 22 Québec Pharmacie vol. 57 n° 3 juin 2010 La desvenlafaxine (PristiqMD) mise en garde sur l’utilisation de tous les ISRS, ainsi que sur les nouveaux antidépresseurs, selon laquelle ces médicaments peuvent augmenter les idées et gestes suicidaires chez les enfants et les adolescents15-16. L’agence gouvernementale n’émet aucune contre-indication quant à leur utilisation en pédiatrie, mais elle recommande un suivi rigoureux, notamment en ce qui a trait à l’apparition d’un syndrome d’activation. Le syndrome d’activation lié aux antidépresseurs survient au cours des premières semaines de traitement et pourrait être responsable des cas de suicide. Les symptômes à surveiller sont : anxiété importante, attaques de panique, irritabilité, impulsivité, hypomanie, agitation, insomnie, hostilité, acathisie, automutilation et virage maniaque15. En octobre 2004, la FDA américaine émet elle aussi des recommandations et oblige toutes les compagnies fabricantes à ajouter une mise en garde bien en vue sur l’emballage de tous les ISRS et nouveaux antidépresseurs13. Il est recommandé que les sujets utilisant des antidépresseurs, qu’ils soient adultes ou fassent partie de la clientèle pédiatrique, soient suivis quasi hebdomadairement afin de déceler des changements de comportement, une détérioration de l’état et le risque de suicide. Cette mise en garde se retrouve également dans la monographie canadienne de la desvenlafaxine. Enfin, d’autres précautions sont à prendre dans les cas de glaucome, d’hypertension artérielle, d’hypercholestérolémie et de problèmes cardiaques, d’antécédents de convulsions, d’hyponatrémie et de troubles rénaux. Les personnes sujettes aux ecchymoses ou aux saignements doivent aussi être vigilantes puisque la desvenlafaxine peut exercer un effet sur l’agrégation des plaquettes via la sérotonine plaquettaire. Un syndrome de retrait lié à l’arrêt brusque de la desvenlafaxine ou à une diminution de la dose est possible. La diminution graduelle doit tenir compte, si possible, des facteurs individuels, tels que la dose et la durée de traitement, ainsi que des antécédents de syndrome de retrait3. Il est à noter que la desvenlafaxine a reçu un avis de conformité de Santé Canada le 4 février 2009 et qu’elle ne figure pas sur la liste de médicaments de la Régie de l’assurance maladie du Québec de juin 2010. Interactions médicamenteuses Le syndrome sérotoninergique est possible avec l’utilisation de la desvenlafaxine. Le risque augmente lorsque la desvenlafaxine est administrée avec des produits qui influent sur la transmission sérotoninergique, tels que les triptans, les ISRS, les IRSN, le linézolide, les IMAO et les précurseurs de la sérotonine. Les antidépresseurs tricycliques, le lithium, la sibutramine, le tramadol, le millepertuis et les suppléments de tryptophane sont aussi des médicaments avec lesquels la desvenlafaxine peut interagir. L’administration de produits qui influent sur l’hémostase (AAS, AINS, warfarine) doit se faire prudemment puisque la prise d’ISRS ou d’IRSN augmente le risque de saignements gastrointestinaux3. Aucune évaluation systématique n’a été réalisée par rapport à d’autres médicaments agissant sur le système nerveux central. Il importe donc de faire preuve de vigilance si l’administration concomitante est envisagée. Posologie et coûts de traitement La dose de départ recommandée de desvenlafaxine à libération prolongée est de 50 mg une fois par jour, avec ou sans nourriture. Cette dose peut être majorée jusqu’à un maximum de 100 mg une fois par jour, bien qu’aucun bénéfice supplémentaire n’ait été démontré dans les études cliniques à des doses supérieures à 50 mg par jour. Les comprimés doivent être avalés sans être mâchés, écrasés ou coupés puisque le médicament est contenu dans une pellicule non absorbable à libération contrôlée. Chez les insuffisants rénaux sévères ayant une clairance de la créatinine inférieure à 30 ml/min, la dose de départ et thérapeutique recommandée est de 50 mg tous les deux jours3. Tableau III Conseils aux utilisateurs de desvenlafaxine3 nLa desvenlafaxine (PristiqMD) est indiquée pour le traitement de la dépression majeure. nLes comprimés à libération prolongée peuvent être pris avec ou sans nourriture, à raison d’une prise par jour, toujours au même moment de la journée. Si vous vous rendez compte que vous avez oublié de prendre une dose, prenez-la immédiatement. Mais s’il est presque l’heure de prendre la dose suivante, sautez la dose que vous avez oubliée et prenez la dose suivante à l’heure habituelle. Ne doublez jamais la dose. nLa desvenlafaxine peut causer certains effets indésirables mineurs quoiqu’ennuyeux, tels que des maux de tête, une sudation accrue, des étourdissements, de la diarrhée et de la fatigue. Consultez votre pharmacien ou votre médecin pour obtenir des conseils afin de minimiser ces effets. nL’apparition d’une anxiété importante, d’agitation, d’insomnie et de comportements inhabituels (irritabilité, hostilité, impulsivité), ainsi que des pensées ou des comportements suicidaires devraient être rapportés immédiatement à un professionnel de la santé. nL’interruption du traitement devrait être graduelle afin de minimiser le risque de symptômes de retrait, tels qu’étourdissements, nausées, maux de tête, irritabilité, diarrhée, insomnie, anxiété, rêves anormaux, fatigue ou transpiration. Ne cessez pas de prendre votre médicament sans consulter d’abord votre pharmacien ou votre médecin. www.professionsante.ca juin 2010 vol. 57 n° 3 Québec Pharmacie 23 Avez-vous entendu parler de... traitement de la dépression majeure. La prise est uniquotidienne et nécessite peu ou pas d’augmentation graduelle de la dose, son potentiel d’interaction est faible et son métabolisme est simple18. Ce nouvel agent dans la pharmacothérapie actuelle semble avoir sa place chez les sujets métaboliseurs lents des CYP450-2D6 ou lorsque la pharmacothérapie comprend d’autres inhibiteurs ou substrats de ces mêmes cytochromes. Comme le produit est indépendant des CYP450-2D6 pour son actiConclusion vité et son métabolisme, les concentrations La desvenlafaxine, métabolite actif de la venla- plasmatiques sont davantage prévisibles qu’avec faxine, est un nouvel IRSN disponible pour le la venlafaxine, quel que soit le phénotype, ce Le coût du traitement par la desvenlafaxine est de 82 $ par mois pour les posologies de 50 mg ou 100 mg par jour, selon les tarifs du fournisseur. À titre indicatif, la venlafaxine originale coûte environ 55 $ par mois si la personne utilise un seul dosage par jour, et le produit générique coûte 27 $ par mois17. Les conseils pertinents à donner aux personnes traitées par la desvenlafaxine sont présentés dans le tableau III. Tableau IV Effets indésirables liés à la desvenlafaxine lors des principales études cliniques3 Effets indésirables PlaceboDesvenlafaxineDesvenlafaxine (n = 1116) 50 mg die 100 mg die (n = 317) (n = 424) Troubles cardiaques Palpitations 2 % 1 % 3% Tachycardie 1 % 1 % <1% Augmentation de la TA 0,5 % 1,3 % 0,7 % Hypotension orthostatique < 1 % < 1 % <1% Troubles oculaires Mydriase < 1 % 2 % 2% Vision trouble 1 % 3 % 4% Troubles gastro-intestinaux Nausées 11 % 22 % 26 % Xérostomie 8 % 11 % 17 % Constipation 4 % 9 % 9% Diarrhée 9 % 11 % 9% Vomissements 2 % 3 % 4% Troubles généraux Fatigue 4 % 7 % 7% Frissons 1 % 1 % <1% Raideurs musculo-squelettiques 1 % 1 % <1% Troubles du système nerveux Étourdissements 6 % 13 % 10 % Céphalées 25 % 20 % 22 % Somnolence 4 % 4 % 9% Tremblements 2 % 2 % 3% Paresthésie 1 % 2 % 2% Dysgueusie 1 % 1 % 1% Insomnie 6 % 9 % 12 % Anxiété 3 % 3 % 5% Rêves anormaux 2 % 2 % 3% Troubles sexuels Dysfonctionnement érectile 1 % 3 % 6% Retard d’éjaculation < 1 % 1 % 5% Baisse de libido (hommes et femmes) 1 % 4 % 5% autres Élévation C-total (> 6,75 mmol/L) 2 % 3 % 4% Élévation C-LDL (> 4,91 mmol/L) < 1 % 1 % 0% Élévation triglycérides (> 3,7 mmol/L) 3 % 2 % 1% Hyperhidrose 4 % 10 % 11 % Bouffées de chaleur < 1 % 1 % 1% 24 Québec Pharmacie vol. 57 n° 3 juin 2010 qui permet de minimiser le risque d’effets indésirables chez les métaboliseurs lents ou s’il y a utilisation simultanée d’un substrat ou d’un inhibiteur des CYP450-2D6. Les effets indésirables associés à la desvenlafaxine sont semblables à ceux des autres ISRS et IRSN. Des études sont actuellement en cours sur l’utilisation de la desvenlafaxine pour d’autres indications, notamment pour le soulagement des bouffées de chaleur à la ménopause. n Références 1. Adams SM, Miller, KE, Zylstra RG, et coll. Pharmacologic Management of Adult Depression. American Family Physician, 2008; 77(6): 785-93. 2. Santé Canada. La dépression. 2009 [En ligne. Page consultée le 24 mai 2009.] www.phac-aspc.gc.ca/ mh-sm/mhp-psm/index-fra.php 3. Wyeth Canada. Monographie de PRISTIQ (desvenlafaxine). Canada, 2009. 4. Légaré N. Mise à jour sur le traitement pharmacologique de la dépression majeure. Québec Pharmacie 2008; 55(6): 21-30. 5. Wyeth Canada. Pristiq (desvenlafaxine) Pharmacokinetics, 2009 [En ligne. Page consultée le 25 juin 2009.] www.wyeth.com/hcp/pristiq/pharmacokinetics 6. Perry R. Desvenlafaxine : A new serotonin-norepinephrine reuptake inhibitor for the treatment of adults with major depressive disorder. Clinical Therapeutics 2009; (31 part 1): 1374-404. 7. Liebowitz MR, Manley AL, Padmanabhan SK, et coll. Efficacy, safety, and tolerability of desvenlafaxine 50 mg/day and 100 mg/day in outpatients with major depressive disorder. Current medical research and opinions 2008; 24(7): 1877-90. 8. Boyer P, Montgomery S, Lepola U, et coll. Efficacity, safety, and tolerability of fixed-dose desvenlafaxine 50 and 100 mg/day for major depressive disorder in a placebo-controlled trial. International Clinical Psychopharmacotherapy 2008; 23(5): 243-54. 9. Feiger AD, Tourian KA, Rosas GR, et coll. A placebo-controlled study evaluating the efficacity and safety of flexible-dose desvenlafaxine treatment in outpatients with major depressive disorder. CNS spectr 2009; 14 (1): 41-51. 10. Archer DF, Dupont CM, Constantine GD, et coll. Desvenlafaxine for the treatment of vasomotor symptoms associated with menopause : A doubleblind, randomized, placebo-controlled trial of efficacy and safety. American Journal of obstetrics & gynecology 2009; 200: 238.e1-238.e10. 11. Sopko MA, Ehret MJ et Gras M. Desvenlafaxine : Un autre médicament « Me Too » ? The Annals of pharmacotherapy 2008; 42(10): 1439-46. 12. Tourian KA, et coll. Desvenlafaxine 50 and 100 mg/d in the treatment of major depressive disorder : An 8-week, phase III, multicenter, randomised, doubleblind, placebo-controlled, parallel-group trial and post hoc pooled analysis of three studies. Clinical Therapeutics 2009; (31 part 1): 1405-23. 13.Wyeth Canada. Monographie d’Effexor XR (venlafaxine). [En ligne. Page consultée le 3 juillet 2009.] www.wyeth.ca/fr/products/effexor 14. Ely lilly. Prescribing informations Cymbalta (duloxétine hcl). [En ligne. Page consultée le 1er octobre 2009.] www.pi.lilly.com/us/cymbalta-pi.pdf 15. Wyeth. Important treatment considerations-Pristiq (desvenlafaxine). [En ligne. Page consultée le 1er juillet 2009.] www.wyeth.com/hcp/pristiq/ important-treatment-considerations 16. Santé Canada. Législation psy [En ligne. Page consultée le 1 octobre 2009.] www.legislation-psy. com/spip.php?article834 17. McKesson Canada Inc. Pharmaclick. McKesson Canada Inc 2008. [En ligne. Page consultée le 1er juillet 2009.] https://clients.mckesson.ca 18. Kamath J, Handratta V. Desvenlafaxine succinate for major depressive disorder : A critical review of the evidence. Expert Rev Neurother. 2008; 8(12): 1787-97. Avez-vous entendu parler de... Questions de formation continue 5) Parmi les énoncés suivants, lequel est faux ? A. La desvenlafaxine est un métabolite actif de la venlafaxine qui agit par l’inhibition sélective de la sérotonine et de la noradrénaline. B. La transformation et le métabolisme de la venlafaxine en desvenlafaxine dépendent des CYP450-2D6. Par contre, le métabolisme de la desvenlafaxine est indépendant des CYP450-2D6. C. La revue des études cliniques comparant la desvenlafaxine à la venlafaxine a montré une amélioration supérieure des symptômes dépressifs, selon l’HAM-D17, avec la desvenlafaxine. D. Les effets indésirables de la desvenlafaxine s’apparentent à ceux des autres IRSN. E. Il est inutile d’ajuster la dose de desvenlafaxine, comme c’est le cas pour la molécule mère, la venlafaxine. 6) Parmi les énoncés suivants, lequel est faux ? A. La desvenlafaxine peut modifier certains résultats de tests de laboratoire, par exemple le bilan lipidique. B. L’apparition de comportements étranges ou de changements de comportement à la suite de la prise de desvenlafaxine devrait être rapportée sans délai à un professionnel de la santé ou au médecin. C. L’utilisation de desvenlafaxine s’est révélée sécuritaire chez les enfants et les adolescents souffrant d’un trouble dépressif majeur. D. La desvenlafaxine interagit avec certaines classes de médicaments, dont les triptans, les ISRS, les IRSN, le linézolide, les inhibiteurs de la monoamine oxydase et les précurseurs de la sérotonine. E. L’hémostase peut être modifiée lors de la prise de desvenlafaxine. Veuillez reporter vos réponses dans le formulaire de la page 78 26 Québec Pharmacie vol. 57 n° 3 juin 2010 58 - 59 Les pharmaciens Jacques Turgeon et Hélène Blanchette L’Ordre des pharmaciens du Québec (OPQ) a souligné, récemment, l’excellence de deux pharmaciens bien connus de la profession, Jacques Turgeon et Hélène Blanchette. Ces deux pharmaciens se sont vus remettre respectivement le prix Louis-Hébert et le prix Mérite CIQ. Cette remise de prix a eu lieu lors de l’assemblée annuelle de l’OPQ, le 9 juin. Le prix Louis-Hébert à Jacques Turgeon Photos : Gracieuseté de l’OPQ L’OPQ a décerné le prix Louis-Hébert à Jacques Turgeon, pharmacien, « pour son apport remarquable à la profession en sa qualité d’enseignant, d’auteur et de chercheur. » Titulaire d’un doctorat en métabolisme des médicaments de l’Université Laval, Jacques Turgeon a complété ses études par un postdoctorat à l’Université Vanderbilt à Nashville aux États-Unis. À la tête du Centre de recherche du CHUM depuis 2007, il dirige l’un des plus importants centres de recherche francophone en santé en Amérique du Nord, comptant plus de 300 chercheurs et 1500 employés. À ce titre, il poursuit ses recherches dans le domaine de la détermination des facteurs pouvant expliquer la variabilité interindividuelle dans la réponse aux médicaments. « Rares sont les médecins ou les pharmaciens qui n’ont pas assisté à une formation de M. Turgeon sur les interactions médicamenteuses » a souligné Diane Lamarre, présidente de l’OPQ, lors de la remise de prix. « Tout en occupant des fonctions de haut niveau, M. Turgeon a toujours continué de se rendre disponible pour communiquer les dernières connaissances aux professionnels de la santé. » « La progression des connaissances dans le domaine pharmacologique a été très importante au cours des 20 dernières années », a pour sa part mentionné Jacques Turgeon, par l’entremise d’un message vidéo diffusé à l’occasion de la remise de prix. « Je me suis toujours investi pour qu’on puisse les rendre applicables. » www.professionsante.ca honorés Le prix du CIQ à Hélène Blanchette La pharmacienne Hélène Blanchette a reçu le prix Mérite CIQ des mains du président du Conseil interprofessionnel du Québec (CIQ), Richard Gagnon. Le CIQ, qui regroupe 45 ordres professionnels et plus de 326 000 membres, décerne chaque année le prix Mérite CIQ pour rendre hommage à un professionnel s’étant démarqué par son implication dans le développement de son ordre professionnel ou pour sa contribution au rayonnement de la profession. Membre de l’OPQ depuis 1990, Hélène Blanchette s’est impliquée pendant de nom breuses années dans les activités de l’Ordre à titre d’administratrice (entre 2001 et 2009) et de présidente de comités. En plus de ces activités, elle supervise, à titre de clinicienne associée à la Faculté de pharmacie de l’Université de Montréal, des étudiants en pharmacie dans le cadre de leur stage de 4e année en milieu communautaire. « Faire partie d’un ordre professionnel est un privilège », a fait observer Hélène Blanchette lors de la remise de son prix. « Le cadre législatif et réglementaire peut sembler lourd de premier abord. Mais tout comme s’adonner à certains loisirs, la voile par exemple, comporte des contraintes, il n’empêche pas moins qu’on ressent une grande liberté lorsqu’on les pratique. Comme pharmacienne, ma compétence et la confiance que m’accordent mes patients font en sorte que je me sens libre chaque jour lorsque j’exerce ma profession. Et nous sommes responsables de chérir cette liberté pour le bien de nos patients. » Communicatrice de grand talent, Hélène Blanchette est depuis 2003 la rédactrice en chef de Québec Pharmacie, une revue qui fournit à tous les pharmaciens communautaires et d’établissements francophones une formation continue exhaustive et de haut niveau. De plus, elle signe sur une base régulière un blogue très fréquenté dans ProfessionSanté.ca, un portail à l’usage exclusif des pharmaciens, des médecins, des infirmières et des gestionnaires en santé. juin 2010 vol. 57 n° 3 Québec Pharmacie 27 LES pages bleues Le syndrome des jambes sans repos Le traitement du syndrome des jambes sans repos a beaucoup évolué cette dernière décennie avec l’arrivée des agonistes dopaminergiques non dérivés de l’ergotamine. Cependant, cette pathologie demeure relativement peu connue des professionnels de la santé et de la population en général. Le présent article vise à parfaire vos connaissances sur le syndrome des jambes sans repos et sur les différents traitements offerts afin que vous soyez mieux outillés pour intervenir dans vos milieux de pratique. Introduction Le syndrome des jambes sans repos se carac térise par une sensation inconfortable dans les jambes, accompagnée d’un besoin irré sistible de les bouger quand elles sont au repos et améliorée par l’activité. Les patients parlent aussi de fourmillements, de raideurs, de picotements, d’impatience et d’une sen sation de « bougeotte ». Environ 10 % de la population canadienne souffre du syndrome des jambes sans repos et, parmi tous ceux qui en sont touchés, environ le tiers a des symptômes d’intensité modérée à élevée qui requièrent une pharmacothérapie. Le syndrome des jambes sans repos peut aussi survenir de façon secondaire à une grossesse, par exemple, ou à diverses patho logies, comme l’insuffisance rénale termi nale et l’urémie, pour ne nommer que les plus connues. On a également associé le syn drome à d’autres pathologies, entre autres l’insuffisance veineuse, les polyneuropa thies, les maladies rhumatismales, les radi culopathies, la fibromyalgie, les myélopa thies, la sclérose en plaques et la maladie de Parkinson2,3,6-9. Certains médicaments peu vent aussi exacerber les symptômes : le tableau I en dresse la liste. Épidémiologie Diagnostic Le syndrome des jambes sans repos peut se manifester à tout âge, mais, en moyenne, les premiers symptômes apparaissent avant l’âge de 18 ans (chez 33 à 45 % des patients)1,2. La prévalence du syndrome augmente avec l’âge. En général, l’état se maintient ou se dégrade jusqu’à l’âge de 70 à 80 ans et tend à s’améliorer par la suite1,2. Les femmes sont plus touchées que les hommes, pour un rap port d’environ 2:11,2,4. De plus, la prévalence dans la population asiatique est inférieure à celle dans la population caucasienne. Dans notre pays, les Canadiens français sont plus touchés que les Canadiens anglais, ce qui renforce la théorie d’une étiologie géné tique2. Quatre critères sont essentiels au diagnostic du syndrome des jambes sans repos5 : 1) un besoin irrésistible de bouger les jambes, habituellement accompagné ou causé par une sensation inconfortable dans les jam bes; 2) les symptômes surviennent ou empi rent au repos (par exemple, en position assise ou couchée); 3) les symptômes sont partiellement ou totalement soulagés par le mouvement; et 4) les symptômes empirent en soirée et durant la nuit. De plus, le dia gnostic peut être appuyé par une réponse positive à la thérapie dopaminergique, une histoire familiale positive ou la présence de mouvements périodiques des jambes durant le sommeil (contraction involontaire des jambes)5. Les symptômes sont habituellement bila téraux, mais peuvent aussi être unilatéraux. Les bras sont parfois aussi atteints, et très rarement, le tronc et le visage2,5,6. Le dia gnostic est donc basé sur l’examen clinique. Par ailleurs, le niveau de ferritine sérique devrait être mesuré chez tous les patients1-4,6,9. En effet, on sait qu’il y a une prévalence éle vée de déficit en fer chez les patients atteints (jusqu’à 25 %)2. Il y a également une relation inverse entre la gravité des symptômes et les niveaux de ferritine sérique : les patients ayant une ferritine sérique inférieure à 45-50 mcg/mL ont généralement des symp tômes plus importants1-3,9. Il est également possible d’évaluer la gravité des symptômes à l’aide d’un questionnaire (10 questions) Pathophysiologie Dans la plupart des cas, le syndrome des jambes sans repos est idiopathique. La cause précise du syndrome des jambes sans repos primaire n’est pas encore connue et de nom breuses recherches ont été effectuées. On estime que des facteurs génétiques ont un rôle à jouer, ce qui s’appuie notamment sur le fait que, selon les études, 40 à 90 % des patients souffrant du syndrome des jambes sans repos idiopathique ont une histoire familiale positive1-3,5-7. De plus, les travaux de recherche pointent vers l’implication d’une anomalie du système dopaminergi que dans le système nerveux central et d’un déficit en fer dans la pathogenèse du syndrome1,2,6,8. www.professionsante.ca Texte rédigé par Marie-Ève Legris, B. Pharm., étudiante à la maîtrise en pratique pharmaceutique, option établissement de santé, Université de Montréal, et Marie-Ève Morin, B. Pharm., Pharmacie André Lajeunesse et associée. Révision : Dre Amélie Fradet, omnipraticienne au CHUQ (Hôpital Saint-François-d’Assise), et Chantal Duquet, B. Pharm., M Sc. Texte original soumis le 22 janvier 2010. Texte final remis le 26 avril 2010. Tableau I Médicaments exacerbant le syndrome des jambes sans repos1-3,7,8 Antagonistes des récepteurs dopaminergiques centraux (ex. : neuroleptiques, métoclopramide) Antihistaminiques Lithium Antidépresseurs n surtout les tricycliques, la mirtazapine et les inhibiteurs sélectifs du recaptage de la sérotonine n sauf le bupropion Caféine juin 2010 vol. 57 n° 3 Québec Pharmacie 31 LES pages bleues mis au point et validé par l’International Restless Legs Syndrome Study Group10. Un examen neurologique complet, des tests de laboratoire (formule sanguine, fonction rénale) et une électromyographie peuvent permettre d’éliminer d’autres causes des symptômes rapportés par le patient (surtout s’il y a une présentation atypique) et d’iden tifier les syndromes des jambes sans repos secondaires2. Impacts sur la qualité de vie Évidemment, puisque les symptômes sont à leur paroxysme au coucher, le syndrome des jambes sans repos entraîne des troubles du sommeil. En conséquence, les patients peu vent souffrir d’épuisement et de somnolence diurne excessive, ainsi que de dépression et d’anxiété associée1,2,6,9. Ils ont également de la difficulté à supporter les positions assises prolongées, par exemple lors d’une réunion, d’une séance de cinéma ou d’un voyage en avion. Un traitement devrait être instauré lors que les symptômes sont importants ou dérangeants pour le patient et que les mesu res non pharmacologiques sont ineffica ces 2,8 . Les symptômes sont considérés comme modérés à intenses lorsqu’ils sur viennent au moins 15 jours par mois ou que le patient obtient un score de plus de 15 au questionnaire de gravité mentionné plus haut1. réfractaire correspond à un syndrome quoti dien traité par un agoniste dopaminergique, mais avec une réponse inadéquate : une réponse initiale sous-optimale malgré une dose adéquate de médication, une réponse inadéquate avec le temps malgré une aug mentation des doses, des effets secondaires intolérables liés au traitement ou à une inten sification des symptômes qui ne peuvent être maîtrisés à l’aide d’une dose additionnelle de médication plus tôt dans la journée3. Puisque le traitement du syndrome des jambes sans repos est possiblement à vie, il importe de donner la plus petite dose efficace possible4,6. Le tableau II montre les doses et les princi paux effets indésirables des différents médica ments utilisés dans le syndrome des jambes sans repos. Cas clinique 1 Madame LP, une femme de 34 ans, souffre du syndrome des jambes sans repos depuis quelques années. Sa maladie est présentement bien maîtrisée grâce à du pramipexole (MirapexMD) 0,25 mg die. La semaine dernière, elle a consulté son médecin qui lui a prescrit de la mirtazapine (RemeronMD) à raison de 15 mg die pour une dépression. Deux à trois jours après l’instauration de cette thérapie, les symptômes du syndrome des jambes sans repos de madame LP se sont aggravés. Quelles sont vos interventions ? Principes de traitement Objectifs thérapeutiques Traitement non pharmacologique Dans la prise en charge du syndrome des jambes sans repos, on vise à améliorer la qualité de vie des patients en éliminant les symptômes à la fois la nuit et lors des activi tés sédentaires, ce qui permet au patient d’améliorer la qualité de son sommeil, de minimiser sa somnolence diurne et de par ticiper sans souci à des activités demandant une position assise prolongée2. Le traitement du syndrome des jambes sans repos commence souvent par l’identification de différents éléments modifiables pouvant aggraver les symptômes chez un patient. Par exemple, plusieurs médicaments sont associés à une aggravation du syndrome des jambes sans repos (tableau I). La première étape est donc, si possible, de modifier ou d’éviter la prise des médicaments concernés1-3,7,8. Certai nes références mentionnent aussi qu’une bonne hygiène de sommeil pourrait être béné fique. Par exemple, il est recommandé de se coucher et de se lever à des heures régulières, de restreindre au minimum les activités dans la chambre à coucher et d’éviter les activités perturbantes avant le coucher8. Des mesures physiques peuvent aussi être tentées lors d’un syndrome des jambes sans repos d’intensité légère. Par exemple, les patients peuvent essayer de bouger les jambes, de prendre des bains chauds, de se faire des massages, d’étirer les membres inférieurs ou d’utiliser des dispo sitifs à compression pneumatique pour dimi nuer leurs symptômes2,6,8,11. Des exercices phy siques modérés peuvent aussi faire partie du traitement de base. L’inactivité ou les activités Approche thérapeutique Le choix d’un traitement pour un patient donné doit tenir compte de la fréquence et de la gravité de ses symptômes. La figure 1 pré sente un algorithme de traitement selon les trois types de syndrome des jambes sans repos : intermittent, quotidien et réfractaire. Le syndrome des jambes sans repos intermit tent se définit par des symptômes qui sont assez dérangeants pour nécessiter une théra pie, mais qui ne sont pas assez fréquents pour être traités par une médication régulière. Le syndrome des jambes sans repos quotidien présente des symptômes fréquents et assez dérangeants pour nécessiter une médication régulière. Le syndrome des jambes sans repos 32 Québec Pharmacie vol. 57 n° 3 juin 2010 physiques trop intenses peuvent, au contraire, précipiter les symptômes. On mentionne éga lement que des activités procurant une stimu lation mentale (p. ex., jeux vidéo, mots croi sés) pourraient diminuer les symptômes1. Le maintien d’un poids santé et une bonne ali mentation sont aussi à privilégier8. De plus, certaines données suggèrent qu’un apport limité en alcool, en tabac et en caféine pourrait également être bénéfique chez ces patients1,3,8. Bref, plusieurs approches non pharmacolo giques peuvent être tentées pour améliorer la qualité de vie des patients atteints du syn drome des jambes sans repos, mais il existe très peu de données confirmant le réel impact bénéfique de ces mesures1,3,4. Traitement pharmacologique Cas clinique 2 Monsieur RM, un homme de 42 ans, est traité pour le syndrome des jambes sans repos avec deux comprimés de lévodopa/carbidopa (SinemetMD) 100/25 mg, une heure avant le coucher. Depuis deux semaines, ses symptômes apparaissent plus tôt dans l’après-midi, et même quelques fois le matin. Quelles sont vos interventions ? 1. Agents dopaminergiques Plusieurs classes de médicaments peuvent être utiles pour soulager et/ou atténuer les symp tômes associés au syndrome des jambes sans repos. Parmi ceux-ci, les agents dopaminergi ques sont considérés comme une première ligne de traitement lors d’un syndrome d’in tensité modérée à importante9. Cette classe de médicaments est aussi utile pour traiter un syndrome des jambes sans repos d’intensité faible ou de type intermittent qui ne répond pas adéquatement aux mesures non pharmacologiques2. Ces dernières années, le traitement du syn drome des jambes sans repos a beaucoup évo lué. Jusqu’en 2004, les deux médicaments les plus recommandés étaient la lévodopa (conte nue dans le SinemetMD et le ProlopaMD ) et le pergolide (PermaxMD)8. Depuis ce temps, deux agonistes dopaminergiques, le ropinirole (RequipMD) et le pramipexole (MirapexMD), ont été respectivement les premier et deuxième agents à obtenir l’indication officielle aux États-Unis et au Canada pour le traitement du syndrome des jambes sans repos. Ce sont aujourd’hui les agents ayant été les plus étu diés pour cette indication1. a) Lévodopa Le premier agent dopaminergique utilisé dans le syndrome des jambes sans repos a été la lévodopa. Ce précurseur de la dopamine, Le syndrome des jambes sans repos principalement utilisé dans la maladie de Par kinson, provoque une augmentation des niveaux de dopamine dans le cerveau2. La lévodopa doit être associée à un inhibiteur de la décarboxylase ne traversant pas la barrière hémato-encéphalique (tel que la carbidopa ou le bensérazide) afin de minimiser la dégrada tion de la lévodopa en dopamine dans les tis sus périphériques2. Plusieurs études ont démontré que la combi naison de ces deux médicaments est efficace dans le traitement du syndrome des jambes sans repos12-14. La lévodopa peut être adminis trée seulement au besoin (chez les patients ayant des symptômes intermittents) ou selon un horaire régulier. La lévodopa est l’agent dopaminergique qui agit le plus rapidement2. Par contre, à cause de sa faible demi-vie, la pré paration à libération immédiate ne supprime pas toujours les symptômes durant toute la nuit. Il est alors nécessaire d’utiliser les prépa rations à libération prolongée ou de fraction ner les doses au cours de la journée pour obte nir une efficacité de plus longue durée15. Chez certains patients (principalement ceux ayant besoin de plus faibles doses ou ceux souf frant de symptômes intermittents), cette théra pie peut demeurer efficace et avec un profil d’effets indésirables tolérable pendant plu sieurs années2. Ces effets indésirables pour raient même être moins fréquents avec la lévo dopa qu’avec d’autres agents dopaminergiques8. Par contre, l’inconvénient principal associé à la lévodopa est une aggravation des symptômes à la suite d’une prise régulière, communément appelée « intensification »1-3,5-7,16. Ce phéno mène est principalement lié aux agents dopa minergiques : en effet, aucun cas d’aggrava tion des symptômes n’a été rapporté avec des thérapies non dopaminergiques, sauf de façon anecdotique chez un petit nombre de patients sous tramadol2,4,16,17. Lorsque ce phénomène se produit, les symptômes de la maladie peu vent apparaître plus tôt qu’à l’habitude, par exemple l’après-midi et même le matin. L’in tensité des symptômes peut aussi augmenter. De plus, des parties du corps qui n’étaient pas touchées auparavant, principalement les bras, peuvent l’être dorénavant2,9. Même si des étu des ont montré que l’intensification pouvait aussi survenir avec les agonistes des récepteurs dopaminergiques18, ce phénomène se mani feste surtout avec la lévodopa. L’apparition de cet effet indésirable, qui a une prévalence pou vant aller jusqu’à 73 %16, est aussi plus élevée lors de l’utilisation de doses plus importantes de lévodopa (≥ 200 mg/jour), ainsi que lors que la première prise de la journée a lieu avant 18 h. Pour minimiser l’aggravation des symp tômes, il peut être nécessaire de diminuer les doses, de modifier le moment de la prise et même de sevrer l’agent2,16. On note également comme effet secondaire particulier l’effet rebond qui représente une récurrence des symptômes au petit matin survenant chez 20 à 35 % des patients3. Bref, la lévodopa n’est plus une première ligne de traitement lors d’un syndrome des jambes sans repos d’intensité modérée à éle vée, mais elle demeure une excellente option de traitement lors d’une utilisation occasion nelle (lors de symptômes intermittents) ou en présence de symptômes légers nécessitant de faibles doses (maximum 200 mg/jour)8. Cette médication est aussi utile quand le syndrome est associé à certaines activités spécifiques, tel les qu’un voyage en avion, un long trajet en voiture ou une soirée au théâtre3. b) Agonistes des récepteurs dopaminergiques dérivés de l’ergotamine Les agonistes dopaminergiques ont la capacité de lier les récepteurs à la dopamine et de pro duire des effets similaires à ce neurotransmet teur. Les agonistes dopaminergiques peuvent être séparés en deux grandes classes : les déri vés de l’ergotamine et les non-dérivés de l’ergotamine. Les agents dérivés de l’ergotamine, tels que la cabergoline (DostinexMD), le pergolide (Per maxMD) et la bromocriptine (ParlodelMD), ont montré une efficacité dans le traitement du syndrome des jambes sans repos. Par contre, ces agents ne font pas partie de l’arsenal théra peutique de base pour ce syndrome. En effet, en raison de sa courte demi-vie (deux à huit heures), l’utilisation de la bromocriptine est limitée lors des symptômes courants2. De plus, la Federal Drug Administration (FDA) américaine n’a pas approuvé ces médicaments pour cette indication à cause des effets secon daires potentiellement graves qui leur sont reliés. En effet, la cabergoline et le pergolide sont associés à un risque de complications cardiaques (valvulopathie cardiaque) et de fibrose pulmonaire, ce qui a même entraîné le retrait du marché du pergolide en 20071. Bref, les agonistes dopaminergiques dérivés de l’er gotamine ne sont pas recommandés comme première ligne de traitement dans le syn drome des jambes sans repos. S’ils sont utili sés, un monitorage cardiopulmonaire étroit doit être effectué pour détecter la présence de fibrose pulmonaire et de problème valvulaire16. c) Agonistes des récepteurs dopaminergiques non dérivés de l’ergotamine En raison des effets indésirables cardiaques liés aux agonistes dopaminergiques dérivés de l’er gotamine, ceux-ci ont cédé leur place aux agents non dérivés de l’ergotamine : le ropini role et le pramipexole. Ces derniers sont pré sentement les deux seuls agents ayant l’indica tion officielle au Canada et aux États-Unis pour le traitement du syndrome des jambes sans repos1,2,8,16. La rotigotine, un autre agent de cette classe présenté sous forme de timbre cutané, est en vente aux États-Unis pour le traitement de la maladie de Parkinson et est présentement en instance d’approbation par la FDA pour le traitement du syndrome des jam bes sans repos. Contrairement aux dérivés de l’ergotamine, aucun monitorage pour évaluer Figure 1 Algorithme de traitement du syndrome des jambes sans repos3,8,31 Syndrome des jambes Syndrome des jambesSyndrome des jambes sans repos intermittent sans repos quotidien sans repos réfractaire nLévodopa nAgoniste dopaminergique nChanger pour : nAgoniste dopaminergique n Gabapentine n autre agoniste dopaminergique nOpiacé de faible puissance nOpiacé de faible puissance n gabapentine n Benzodiazépine ou tramadol n opiacé de forte puissance ou tramadol nAjouter : n benzodiazépine n opiacé de faible puissance n gabapentine Mesures non pharmacologiques www.professionsante.ca juin 2010 vol. 57 n° 3 Québec Pharmacie 33 LES pages bleues la fibrose valvulaire n’est recommandé avec les agonistes non dérivés de l’ergotamine. Plusieurs études ont démontré l’efficacité du ropinirole19-22 et du pramipexole23-26 dans le traitement du syndrome des jambes sans repos. Contrairement aux autres classes de médicaments étudiées, le ropinirole et le pra mipexole ont fait l’objet d’études de plus grande envergure (avec un nombre plus consi dérable de patients et pendant une plus longue période). Par exemple, une étude multicentri que de 200721 effectuée sur plus de 300 patients a démontré l’efficacité du ropinirole dans le syndrome des jambes sans repos, et cette effi cacité s’est même maintenue après 52 semai nes de traitement. Cette étude rapporte aussi que le phénomène d’aggravation des symptô mes (tel qu’observé avec la lévodopa) peut sur venir avec le ropinirole, mais avec une inci dence beaucoup plus faible (environ 2,3 % après un an de traitement). Parmi les études les plus récentes sur le pramipexole, l’équipe de Winkelman26 a publié en 2006 une étude ran domisée à double insu d’une durée de 12 semaines évaluant l’efficacité et l’innocuité de ce traitement chez 344 patients. Le prami pexole a été démontré statistiquement supé rieur au placebo pour amoindrir les symptô mes et améliorer le sommeil chez les patients atteints d’un syndrome des jambes sans repos d’intensité modérée à importante. En somme, il y a suffisamment de preuves pour conclure que le ropinirole et le pramipexole sont clini quement efficaces pour soulager les symptô mes et améliorer le sommeil des patients atteints du syndrome des jambes sans repos16. Au total, les études sur le ropinirole ont porté sur plus de 1000 patients et celles sur le prami pexole en ont regroupé autant. Toutes les étu des comparant le ropinirole ou le pramipexole au placebo ont été favorables à l’agoniste dopa minergique non dérivé de l’ergotamine. La prévalence des effets indésirables les plus fré quemment rapportés (tels que les nausées, la somnolence et les étourdissements) n’était pas constante dans toutes les études et il paraît dif ficile de déterminer si l’un ou l’autre des deux traitements est mieux toléré. Pour le moment, aucune donnée ne permet de préférer un agent dopaminergique non dérivé de l’ergotamine par rapport à un autre7. L’équipe de Quilici27 a publié en 2008 une méta-analyse comparant l’efficacité et l’innocuité du ropinirole et du pramipexole pour soulager le syndrome des jambes sans repos. Les auteurs concluent que le pramipexole serait le plus efficace et le mieux toléré. Par contre, il est important de noter qu’aucune étude comparant directement les deux traitements n’a été effectuée jusqu’à pré sent. De plus, la méta-analyse a été financée et menée par la compagnie qui commercialise le pramipexole. 34 Québec Pharmacie vol. 57 n° 3 juin 2010 Par ailleurs, les patients atteints du syn drome des jambes sans repos nécessitent des doses plus faibles d’agonistes dopaminergi ques que les personnes atteintes de Parkinson. Cela pourrait expliquer pourquoi les effets secondaires plus importants se manifestant chez les patients atteints de Parkinson (comme les dyskinésies, les hallucinations, les attaques de sommeil et les psychoses) sont beaucoup plus rarement rapportés chez les patients atteints du syndrome des jambes sans repos7,8,28. L’impulsivité (pouvant se manifes ter par le jeu compulsif, une augmentation importante de la libido ou des achats compul sifs) apparaît aussi principalement chez les parkinsoniens prenant des agonistes dopami nergiques, mais quelques cas ont été rapportés chez des patients atteints du syndrome des jambes sans repos2,28. 2. Les anticonvulsivants Les anticonvulsivants sont une solution de rechange thérapeutique aux agents dopami nergiques pour le traitement du syndrome des jambes sans repos. Cependant, ils ont généra lement une meilleure efficacité chez les patients présentant des douleurs ou des neu ropathies périphériques16. a) Gabapentine (NeurontinMD) Les raisons expliquant l’efficacité de la gaba pentine dans le syndrome des jambes sans repos ne sont pas encore claires, mais il est probable qu’une combinaison de l’effet sédatif et de l’effet modulateur au niveau sensoriel soit une partie de la réponse16. Un nombre limité d’études démontrent que la gabapentine est efficace pour soulager les symptômes présents lors d’un syndrome des jambes sans repos29,30. L’équipe de Gar cia-Borreguero29 a effectué une étude croisée (24 patients ont reçu un placebo pendant six semaines et la gabapentine pour six autres semaines) qui a démontré une amélioration des symptômes chez les patients prenant de la gabapentine. Pour sa part, l’équipe de Happe30 a effectué une étude randomisée ouverte de quatre semaines avec 16 patients comparant la gabapentine et le ropinirole, et les deux agents ont démontré une efficacité comparable. La gabapentine est souvent considérée comme une bonne solution de rechange aux agonistes dopaminergiques lorsque les patients y sont intolérants ou que le phéno mène d’aggravation des symptômes survient. Ce médicament est aussi considéré comme un traitement de choix chez les patients ayant un syndrome des jambes sans repos douloureux ou associé à des neuropathies périphériques ou à un syndrome de douleurs chroniques indépendant 3,31. b) Carbamazépine (TegretolMD) La carbamazépine a été le premier anticon vulsivant à être étudié pour le syndrome des jambes sans repos dans les années 198032,33. L’étude de Lundvall32, une étude croisée ran domisée à double insu, a évalué l’efficacité de la carbamazépine par rapport au placebo chez six patients atteints d’un syndrome des jambes sans repos (deux périodes de quatre semaines). Les auteurs concluent que la car bamazépine est supérieure au placebo pour le soulagement des symptômes bien que leur analyse ne repose que sur des paramètres subjectifs et aucune statistique. Telstad et coll.33 ont aussi mené une étude randomisée à double insu comparant la carbamazépine au placebo chez 174 patients pendant cinq semaines. Les auteurs ont démontré que les patients ayant reçu la carbamazépine ont eu un nombre inférieur d’épisodes par semaine. Par contre, puisque ces deux études ont été effectuées il y a plusieurs années, avant la mise en place de critères objectifs pour poser le diagnostic et faire le suivi du syndrome des jambes sans repos, il est préférable de conser ver la carbamazépine comme solution de rechange aux traitements dont l’efficacité est mieux prouvée16. De plus, son profil d’effets secondaires potentiellement graves nécessite un monitorage étroit, ce qui limite l’utilisa tion de la carbamazépine dans la pratique actuelle. c) Acide valproïque (DepakeneMD) Une étude randomisée a évalué l’efficacité de l’acide valproïque dans le syndrome des jam bes sans repos : l’équipe de Eisensehr34 a comparé l’acide valproïque à libération pro longée au lévodopa/bensérazide chez 20 patients inclus dans une étude randomi sée, croisée et à double insu (période de trois semaines pour chacun des traitements). Les auteurs concluent qu’il n’y a pas de différence significative entre les deux traitements pour le soulagement des paresthésies et des pro blèmes de sommeil. Par contre, considérant le profil d’effets indésirables potentiellement graves, le monitorage étroit requis et les don nées limitées, l’utilisation de l’acide val proïque ne devrait être considérée qu’en tant que solution de rechange. D’autres études seraient nécessaires pour établir avec certi tude l’efficacité de ce médicament dans le syndrome des jambes sans repos, quoique leur utilité soit discutable étant donné l’ac cessibilité à des options qui causent moins d’effets indésirables16. d) Topiramate (TopamaxMD) Très peu d’études ont évalué spécifiquement l’efficacité du topiramate pour soulager le syndrome des jambes sans repos. Une étude Le syndrome des jambes sans repos prospective espagnole de 90 jours pendant laquelle 19 patients ont pris le topiramate démontre une certaine efficacité de cet agent à réduire les symptômes. La qualité du sommeil s’est aussi améliorée mais de façon non statis tiquement significative. Cependant, les patients recrutés présentaient des symptômes atypiques, ce qui rend une extrapolation diffi cile. Bref, il est évident que d’autres études de plus grande envergure sont nécessaires pour confirmer l’efficacité du topiramate dans le syndrome des jambes sans repos16. Par ailleurs, le topiramate présente aussi, comme la carbamazépine et l’acide val proïque, plusieurs effets indésirables typi ques des anticonvulsivants. Il présente égale ment un potentiel à induire un état d’acidose, dû à son effet inhibiteur sur l’anhydrase Tableau II Traitements pharmacologiques du syndrome des jambes sans repos 3,9,16,31 Médicaments Posologie quotidienneEffets indésirables Commentaires Carbidopa/ Dose initiale de 25/100 mg (½ à 1 co) Nausée, diarrhée, dyspepsie, hypotensionAdministrer de 1 à 2 heures avant le début lévodopa et augmenter ad 50/200 mg orthostatique, étourdissements, faiblesse des symptômes. Début d’action rapide, musculaire, somnolence, maux de tête, souvent dès la première dose effet rebond, intensification Agonistes dopaminergiques dérivés de l’ergotamine Cabergoline 0,5 à 3 mg/jrNausée, vomissements, constipation, maux Longue demi-vie (> 24 h) de tête, étourdissements, somnolence. Fibrose pulmonaire et valvulopathie cardiaque avec la cabergoline Bromocriptine 5 à 15 mg/jrFaible demi-vie Agonistes dopaminergiques non dérivés de l’ergotamine Pramipexole Dose initiale : 0,125 mg/jr Nausée, vomissements, sédation, Ajustement : augmenter de 0,125 mg confusion, étourdissements tous les 2 à 3 jours. Dose efficace : 0,5 à 2 mg Moment optimal de prise : 2 h avant le coucher. Peut être divisé en 2 ou 3 doses si besoin Ropinirole Dose initiale : 0,25 mg Nausée, étourdissements, fatigue, Ajustement : augmenter de 0,25 mg somnolence tous les 2 à 3 jours Dose efficace : 1 et 4 mg Anticonvulsivants Gabapentine 300 à 3600 mg/jr en 2 ou 3 prises Sédation, étourdissements, ataxie, si besoin fatigue, gain de poids, tremblements, œdème périphérique Carbamazépine 200 à 600 mg/jrSomnolence, ataxie, anémie aplasique, Inducteur enzymatique agranulocytose, thrombocytopénie Acide valproïque Pas de dose officielle : Sédation, étourdissements, tremblements, étudiée à 600 mg/jr nausée, diarrhée, gain de poids, thrombocytopénie Topiramate 25 à 100 mg/jr Étourdissements, somnolence, ataxie, ralentissement psychomoteur, risque de néphrolithiase Opiacés Oxycodone 5-30 mg/jr en 1 à 3 prisesSédation, constipation, nausée, rétention urinaire, dépression respiratoireAussi : codéine 30-180 mg/jr ou propoxyphène 100-600 mg/jr, en 2 à 3 prises Méthadone 2,5-20 mg/jr en 2 prises Tramadol 50-100 mg/jr en 1 à 3 prises Benzodiazépines Clonazépam 0,25 à 2 mg au coucherSédation, étourdissement, tolérance, risque de chutes www.professionsante.ca juin 2010 vol. 57 n° 3 Québec Pharmacie 35 LES pages bleues carbonique, ce qui nécessite un monitorage taire aux thérapies de première ligne plus courte demi-vie, telle que le lorazépam prophylactique16. puisqu’elle n’a été étudiée que dans cette (AtivanMD), l’oxazépam (SeraxMD) ou le téma zépam (RestorilMD)31. population spécifique3,16. 3. Les opiacés Bref, cette classe de médicaments ne fait pas Bien que les opiacés n’aient pas d’indication c) Tramadol (TramacetMD/ZytramMD) partie de la première ligne de traitement pour officielle dans le traitement du syndrome des Le tramadol a été étudié dans un essai clini le syndrome des jambes sans repos et elle est jambes sans repos, ils sont souvent utilisés en que ouvert37 chez 12 patients. L’efficacité était plutôt utilisée chez des patients avec des symp monothérapie ou en association avec un évaluée par une échelle de gravité des symp tômes légers ou intermittents, particulière agent dopaminergique. Cependant, aucune tômes qui n’a pas été validée. Dix patients ment les jeunes patients, ou chez les patients étude n’a évalué l’efficacité et l’innocuité ont trouvé le tramadol plus efficace que les présentant des difficultés à trouver le som d’une telle association16. L’effet des opiacés autres traitements qu’ils avaient essayés par meil6,7,31. Une benzodiazépine peut aussi être dans le syndrome des jambes sans repos n’est le passé, un patient n’y a vu qu’un effet combinée aux agonistes dopaminergiques pas connu, mais il ne dépend possiblement modeste, alors que le dernier patient n’a res dans les cas réfractaires1. que de leurs propriétés sédatives et analgési senti aucun soulagement. À cause de la faible ques31. Il est recommandé de les réserver en qualité de cette étude, le tramadol doit être 5. Autres traitements deuxième ligne, chez les patients qui ne peu considéré en dernière ligne dans le traite Les suppléments de fer par voie orale pour vent tolérer les agents dopaminergiques ou ment du syndrome des jambes sans repos2,16. raient être bénéfiques chez les patients qui ne sont pas soulagés par ces derniers4,7. Il De plus, des cas rapportés d’aggravation des sont déficients en fer, tandis que les supplé s’agit aussi d’un choix raisonnable chez les symptômes chez un petit nombre de patients, ments par voie intraveineuse pourraient être patients avec un syndrome des jambes sans comme celle observée avec les agents dopa bénéfiques chez les patients dont le syn repos douloureux1. minergiques, suggère une utilité limitée du drome des jambes sans repos est lié à une Le potentiel d’abus des opiacés ne devrait tramadol 16 . D’autres études seraient insuffisance rénale terminale4,6,16. Cependant, d’autres études sont nécessaires pour clari pas limiter leur utilisation dans le traitement nécessaires. fier le rôle du fer dans le traitement du syn du syndrome des jambes sans repos. En effet, drome des jambes sans repos. Une revue la dépendance aux opiacés dans ce contexte 4. Les benzodiazépines est rare, sauf chez les patients ayant une his Théoriquement, les bénéfices des benzodia Cochrane est par ailleurs en cours sur le toire antérieure d’abus3. Par ailleurs, il est zépines dans le syndrome des jambes sans sujet41. On recommande pour l’instant de recommandé de surveiller l’apparition de repos consisteraient en une réduction de traiter par du fer jusqu’à ce que la ferritine problèmes respiratoires, tels que l’apnée du l’insomnie, du temps d’endormissement et soit supérieure à 50 mcg/L et le pourcentage sommeil2,16. Les trois opiacés présentés ci- des éveils causés par les mouvements invo de saturation de la transferrine, supérieur à dessous sont ceux qui ont fait l’objet d’études lontaires des jambes durant la nuit. La ben 20 %1,3. D’autres médicaments ont été étudiés pertinentes. Les autres opiacés, comme la zodiazépine la plus utilisée dans cette indica codéine ou le propoxyphène, pourraient tion est le clonazépam (RivotrilMD). Par dans le cas du syndrome des jambes sans aussi être considérés dans le choix de contre, il existe un nombre restreint d’études repos, mais ils ne sont cités qu’à titre inforévaluant son efficacité dans le traitement du matif à cause de leur plus faible efficacité, de traitement3,31. syndrome des jambes sans repos38-40. Ces étu leur profil d’effets indésirables moins favoMD a) Oxycodone (Supeudol ) des, qui ont été effectuées pendant de courtes rable et/ou des données limitées. Ces traiteL’oxycodone a été évaluée dans une étude périodes (quelques jours à huit semaines) et ments comprennent la clonidine (Catacroisée35 dans laquelle chacun des 11 patients avec un nombre limité de patients (6 à 26), presMD), l’amantadine (SymmetrelMD), le recevait un traitement pendant deux semai ne démontrent pas avec certitude l’efficacité baclofen (LioresalMD), l’acide folique et le nes et un placebo pendant deux semaines du clonazépam dans l’amélioration de l’état magnésium2-4,16. également. L’oxycodone s’est montrée supé global des patients atteints du syndrome des rieure au placebo dans l’amélioration de l’in jambes sans repos. L’équipe de Saletu40 a Populations spéciales confort dans les jambes, du sommeil et de la montré que le clonazépam entraînait une Grossesse vigilance diurne. Ce médicament est donc amélioration de la qualité du sommeil chez La grossesse peut précipiter un syndrome des considéré comme une solution de rechange les patients traités. Par contre, il n’y a eu jambes sans repos, principalement au troi efficace dans le traitement du syndrome des aucune différence entre le groupe clonazé sième trimestre. Toutefois, les symptômes se pam et le groupe placebo en ce qui a trait au résorbent généralement après l’accouche jambes sans repos1-3,16. nombre de mouvements périodiques des ment1,2,6,8. L’utilisation de médicaments pour MD b) Méthadone (Metadol ) soulager les symptômes doit être prise en jambes durant la nuit. La méthadone a, quant à elle, fait l’objet De plus, la somnolence diurne, les étourdis considération puisque les troubles du som d’une étude de cas36. Durant cette étude, sements ainsi que le risque de chutes associé meil liés au syndrome des jambes sans repos 27 patients, qui avaient connu un échec avec limitent quelque peu l’utilisation des benzo peuvent contribuer à un accouchement diffi au moins deux agonistes dopaminergiques, diazépines, surtout chez les personnes âgées. cile ou à la prématurité2,8. Néanmoins, le trai ont essayé la méthadone pendant une durée Le développement possible d’une dépendance tement est habituellement réservé aux cas gra moyenne de 23 mois. Parmi les 27 patients, à cette classe de médicaments est aussi une ves. Les opiacés (particulièrement la codéine huit ont quitté l’étude à cause d’effets indési autre préoccupation quant à l’utilisation à et la morphine43) sont l’option la plus sécuri rables ou d’un manque d’efficacité. Ceux qui long terme des benzodiazépines. Ces effets taire durant la grossesse2,8. Cependant, un sont restés ont vu une amélioration de leurs indésirables sont d’autant plus importants suivi étroit est nécessaire, car ils peuvent symptômes d’environ 75 %. Cette thérapie avec le clonazépam, compte tenu de sa longue potentiellement exposer le bébé à un sevrage devrait ainsi être réservée aux patients avec demi-vie. Il pourrait être préférable de le ou à une dépression respiratoire à la nais un syndrome des jambes sans repos réfrac modifier pour une benzodiazépine ayant une sance43. 36 Québec Pharmacie vol. 57 n° 3 juin 2010 Le syndrome des jambes sans repos Pédiatrie Le syndrome des jambes sans repos est rare chez les enfants et est plus difficile à diagnos tiquer. Il est souvent associé à un trouble déficitaire de l’attention avec hyperactivité (TDAH)2,7,8. Puisque les études sont limitées dans la population pédiatrique, il est préféra ble de commencer par les mesures non phar macologiques (hygiène de sommeil, restric tion de stimulants et caféine, etc.). Les agonistes dopaminergiques se sont montrés efficaces dans le soulagement du syndrome des jambes sans repos et, si nécessaire, pour raient bénéficier aux symptômes du TDAH2,7,8. Insuffisance rénale et urémie Dans le cas du syndrome des jambes sans repos associé à l’insuffisance rénale et à l’uré mie, le meilleur traitement est d’en éliminer la cause. En effet, ces patients ne sont pas soulagés par la dialyse, mais par une greffe rénale1,2,6-8. L’administration de fer par voie intraveineuse peut aussi être efficace, mais son effet tend à s’atténuer avec le temps. Il pourrait être nécessaire de répéter le traitement16. Effet placebo Puisque le syndrome des jambes sans repos répond à la fois à des agents dopaminergi ques et à des opiacés, deux systèmes forte ment impliqués dans l’effet placebo, une méta-analyse44 a été effectuée en 2008 pour quantifier l’ampleur de l’effet placebo dans cette pathologie. Les auteurs ont constaté qu’en moyenne le tiers des patients ont eu une amélioration substantielle de leurs symptômes, alors qu’ils recevaient un pla cebo. L’effet placebo était important en ce qui concerne la gravité des symptômes (mesurée à l’aide du questionnaire de l’Inter national Restless Legs Syndrome Study Group), modéré pour la qualité de vie et fai ble pour la somnolence diurne, la qualité et la durée du sommeil44. Cet effet placebo est comparable à celui lié à l’insomnie ou à la dépression44. Prise de position À la suite de l’analyse des différentes référen ces consultées, il appert que la pierre angulaire du traitement pharmacologique du syndrome des jambes sans repos demeure le ropinirole et le pramipexole. Cependant, tel que mentionné précédemment, il n’y a pas encore de données probantes prouvant la supériorité d’un de ces deux agents. Puisque l’étiologie de la patholo gie n’est pas entièrement connue, des essais portant sur d’autres molécules de différentes classes ont été réalisés avec un succès mitigé. Il reste à démontrer si la sédation induite par les anticonvulsivants, les opiacés et les benzodia zépines est un avantage ou non de ces classes, comparativement aux agonistes dopaminer giques. D’une part, cet effet pourrait favoriser un meilleur sommeil, mais cela pourrait aussi occasionner de la somnolence diurne non souhaitée16. Ces agents sont donc conservés comme solution de rechange. En ce qui concerne les associations, les experts les sug gèrent dans les cas de symptômes réfractaires, bien que ni leur efficacité ni leur innocuité n’aient été établies9. En outre, plusieurs questions demeurent sans réponse. Tout d’abord, une meilleure compréhension du mécanisme de la patho logie nous permettrait de mettre au point des médicaments plus spécifiques, et donc plus efficaces. Pour l’instant, il serait perti nent de comparer les traitements disponi bles entre eux. En effet, la majorité des étu des publiées évalue l’efficacité des traitements par rapport au placebo. De plus, les études cliniques devraient inclure un nombre plus important de patients pour avoir un plus grand impact statistique. Enfin, une durée de suivi d’un minimum de deux à trois ans serait plus adéquate pour évaluer l’incidence du phénomène d’aggra vation des symptômes. En attendant des études plus approfondies, les meilleures options de traitement demeurent le ropini role et le pramipexole. Conclusion : le rôle du pharmacien À notre avis, le rôle du pharmacien dans la prise en charge des patients souffrant du syn drome des jambes sans repos est tout d’abord d’en connaître les symptômes pour pouvoir adresser à un médecin ceux qui les présentent. Ensuite, comme pour tous les patients, le pharmacien devrait assurer le suivi de l’effica cité et de l’innocuité de la médication en étant particulièrement à l’affût de l’apparition de l’effet rebond ou de l’intensification des symp tômes. Enfin, puisque le syndrome des jambes sans repos est relativement peu connu des professionnels de la santé, le pharmacien devrait être prêt à répondre à des questions éventuelles sur le sujet. n Références 1. Bayard M, Avonda T, Wadzinski J. Restless legs syndrome. Am Fam Physician 2008; 78: 235-40. 2. Satija P, Ondo WG. Restless legs syndrome : pathophysiology, diagnosis and treatment. CNS Drugs 2008; 22: 497-518. 3. Silber MH, Ehrenberg BL, Allen RP, et coll. An algorithm for the management of restless legs syndrome. Mayo Clin Proc 2004; 79: 916-22. 4. Trenkwalder C, Hogl B, Winkelmann J. Recent advances in the diagnosis, genetics and treatment of restless legs syndrome. J Neurol 2009; 256: 539-53. 5. Allen RP, Picchietti D, Hening WA, et coll. Restless legs syndrome: diagnostic criteria, special considerations, and epidemiology. A report from the restless legs syndrome diagnosis and epidemiology workshop at the National Institutes of Health. Sleep Med 2003; 4: 101-19. 6. Ekbom K, Ulfberg J. Restless legs syndrome. J Intern Med 2009; 266: 419-31. 7. Ondo WG. Restless legs syndrome. Neurol Clin 2009; 27: 779-99, vii. 8. Hening WA. Current guidelines and standards of practice for restless legs syndrome. Am J Med 2007; 120: S22-7. 9. Earley CJ. Clinical practice. Restless legs syndrome. N Engl J Med 2003; 348: 2103-9. 10. Walters AS, LeBrocq C, Dhar A, et coll. Validation of the International Restless Legs Syndrome Study Group rating scale for restless legs syndrome. Sleep Med 2003; 4: 121-32. 11.Lettieri CJ, Eliasson AH. Pneumatic compression devices are an effective therapy for restless legs syndrome : a prospective, randomized, double-blinded, www.professionsante.ca sham-controlled trial. Chest 2009; 135: 74-80. 12. Benes H, Kurella B, Kummer J, et coll. Rapid onset of action of levodopa in restless legs syndrome : a double-blind, randomized, multicenter, crossover trial. Sleep 1999; 22: 1073-81. 13. Collado-Seidel V, Kazenwadel J, Wetter TC, et coll. A controlled study of additional sr-L-dopa in L-doparesponsive restless legs syndrome with late-night symptoms. Neurology 1999; 52: 285-90. 14. Saletu M, Anderer P, Hogl B, et coll. Acute doubleblind, placebo-controlled sleep laboratory and clinical follow-up studies with a combination treatment of rr-L-dopa and sr-L-dopa in restless legs syndrome. J Neural Transm 2003; 110: 611-26. 15.Calado PS. Le syndrome des jambes sans repos. Pharmactuel 2001; 34: 65-9. 16.Trenkwalder C, Hening WA, Montagna P, et coll. Treatment of restless legs syndrome : an evidencebased review and implications for clinical practice. Mov Disord 2008; 23: 2267-302. 17. Garcia-Borreguero D, Allen RP, Kohnen R, et coll. Diagnostic standards for dopaminergic augmentation of restless legs syndrome : report from a World Association of Sleep Medicine-International Restless Legs Syndrome Study Group consensus conference at the Max Planck Institute. Sleep Med 2007; 8: 520-30. 18. Winkelman JW, Johnston L. Augmentation and tolerance with long-term pramipexole treatment of restless legs syndrome (RLS). Sleep Med 2004; 5: 9-14. 19. Allen R, Becker PM, Bogan R, et coll. Ropinirole decreases periodic leg movements and improves sleep parameters in patients with restless legs syndrome. Sleep 2004; 27: 907-14. 20. Bliwise DL, Freeman A, Ingram CD, et coll. Randomized, double-blind, placebo-controlled, short-term trial of ropinirole in restless legs syndrome. Sleep Med 2005; 6: 141-7. 21. Garcia-Borreguero D, Grunstein R, Sridhar G, et coll. A 52-week open-label study of the long-term safety of ropinirole in patients with restless legs syndrome. Sleep Med 2007; 8: 742-52. 22. Trenkwalder C, Garcia-Borreguero D, Montagna P, et coll. Ropinirole in the treatment of restless legs syndrome : results from the TREAT RLS 1 study, a 12 week, randomized, placebo controlled study in 10 European countries. J Neurol Neurosurg Psychiatry 2004; 75: 92-7. 23. Miranda M, Kagi M, Fabres L, et coll. Pramipexole for the treatment of uremic restless legs in patients undergoing hemodialysis. Neurology 2004; 62: 831-2. 24. Montplaisir J, Nicolas A, Denesle R, et coll. Restless legs syndrome improved by pramipexole : a double-blind randomized trial. Neurology 1999; 52: 938-43. 25. Saletu M, Anderer P, Saletu-Zyhlarz G, et coll. Acute placebo-controlled sleep laboratory studies and clinical follow-up with pramipexole in restless legs syndrome. Eur Arch Psychiatry Clin Neurosci 2002; 252: 185-94. 26. Winkelman JW, Sethi KD, Kushida CA, et coll. Efficacy and safety of pramipexole in restless legs syndrome. Neurology 2006; 67: 1034-9. juin 2010 vol. 57 n° 3 Québec Pharmacie 37 LES pages bleues 27. Quilici S, Abrams KR, Nicolas A, et coll. Meta-analysis of the efficacy and tolerability of pramipexole versus ropinirole in the treatment of restless legs syndrome. Sleep Med 2008; 9: 715-26. 28.Stoner SC, Dahmen MM, Makos M, et coll. An exploratory retrospective evaluation of ropinirole-associated psychotic symptoms in an outpatient population treated for restless legs syndrome or Parkinson’s disease. Ann Pharmacother 2009; 43: 1426-32. 29. Garcia-Borreguero D, Larrosa O, de la Llave Y, et coll. Treatment of restless legs syndrome with gabapentin : a double-blind, cross-over study. Neurology 2002; 59: 1573-9. 30. Happe S, Sauter C, Klosch G, et coll. Gabapentin versus ropinirole in the treatment of idiopathic restless legs syndrome. Neuropsychobiology 2003; 48: 82-6. 31. Lafontaine AL. Restless legs syndrome. Dans : Gray J, ed. Therapeutic Choices. 5th éd. Ottawa : Association des pharmaciens du Canada; 2007: 239-46. 32. Lundvall O, Abom PE, Holm R. Carbamazepine in restless legs. A controlled pilot study. Eur J Clin Pharmacol 1983; 25: 323-4. 33. Telstad W, Sorensen O, Larsen S, et coll. Treatment of the restless legs syndrome with carbamazepine : a double blind study. Br Med J (Clin Res Ed) 1984; 288: 444-6. 34. Eisensehr I, Ehrenberg BL, Rogge Solti S, et coll. Treatment of idiopathic restless legs syndrome (RLS) with slow-release valproic acid compared with slowrelease levodopa/benserazid. J Neurol 2004; 251: 579-83. 35. Walters AS, Wagner ML, Hening WA, et coll. Successful treatment of the idiopathic restless legs syndrome in a randomized double-blind trial of oxycodone versus placebo. Sleep 1993; 16: 327-32. 36. Ondo WG. Methadone for refractory restless legs syndrome. Mov Disord 2005; 20:345-8. 37. Lauerma H, Markkula J. Treatment of restless legs syndrome with tramadol : an open study. J Clin Psychiatry 1999; 60: 241-4. 38. Boghen D, Lamothe L, Elie R, et coll. The treatment of the restless legs syndrome with clonazepam : a prospective controlled study. Can J Neurol Sci 1986; 13: 245-7. 39. Montagna P, Sassoli de Bianchi L, Zucconi M, et coll. Clonazepam and vibration in restless legs syndrome. Acta Neurol Scand 1984; 69: 428-30. 40. Saletu M, Anderer P, Saletu-Zyhlarz G, et coll. Restless legs syndrome (RLS) and periodic limb movement disorder (PLMD) : acute placebo-controlled sleep laboratory studies with clonazepam. Eur Neuropsychopharmacol 2001; 11: 153-61. 41.Trotti LM, Bhadriraju S, Becker LA. Iron for restless legs syndrome. Cochrane Database of Systematic Reviews 2009, Issue 2. Art. No.: CD007834. DOI: 10.1002/14651858.CD007834. 42.Rottach KG, Schaner BM, Kirch MH. Restless legs syndrome as a side effect of second generation antidepressants. Journal of Psychiatric Research 2009; 43: 70-5. 43. Morin C, Prot-Labarte S, Ferreira E, et coll. Migraines et douleurs. Dans : Ferreira E, ed. Grossesse et allaitement : Guide thérapeutique. Montréal : Éditions du CHU Sainte-Justine; 2007: 599-637. 44. Fulda S, Wetter TC. Where dopamine meets opioids : a meta-analysis of the placebo effect in restless legs syndrome treatment studies. Brain 2008; 131: 902-17. Questions de formation continue 7) Parmi les énoncés suivants, lequel n’est pas un critère essentiel au diagnostic du syndrome des jambes sans repos ? A. Un inconfort dans les jambes causant une envie irrésistible de les bouger B. Un soulagement apporté par le mouvement des jambes C. Des troubles du sommeil D. Une augmentation des symptômes au repos E. Une augmentation des symptômes le soir et la nuit 8) Parmi les énoncés suivants concernant la pathophysiologie du syndrome des jambes sans repos, lequel est vrai ? A. Le syndrome des jambes sans repos est une forme précoce de maladie de Parkinson. B. Les patients ayant un niveau de ferritine sérique élevé ont généralement des symptômes plus importants. C. La dompéridone exacerbe les symptômes du syndrome des jambes sans repos. D. Le bupropion n’exacerbe pas les symptômes du syndrome des jambes sans repos. E. La grossesse n’a aucune influence sur le syndrome des jambes sans repos. 9) Parmi les approches thérapeutiques énoncées ci-dessous, laquelle est la meilleure pour un patient atteint du syndrome des jambes sans repos qui présente également des neuropathies périphériques ? A. Lévodopa/carbidopa B. Gabapentine C. Clonazépam D. Oxycodone E. Sulfate ferreux 10) Parmi les énoncés suivants concernant le traitement du syndrome des jambes sans repos, lequel est faux ? A. Les mesures non pharmacologiques sont très efficaces dans le traitement du syndrome des jambes sans repos. B. La méthadone devrait être réservée aux patients ayant des symptômes réfractaires. C. La lévodopa n’est pas considérée comme une première ligne de traitement lors des symptômes quotidiens d’intensité modérée à élevée. D. Le clonazépam peut être utile chez les patients dont le sommeil est très dérangé par le syndrome des jambes sans repos. E. L’effet placebo est relativement important dans le syndrome des jambes sans repos : environ un patient sur trois voit ses symptômes s’améliorer sous placebo. 11) Parmi les énoncés suivants concernant les agents dopaminergiques, lequel est faux ? A. L’effet rebond est plus important avec la lévodopa qu’avec les autres agents dopaminergiques. B. Le pramipexole et le ropinirole sont les deux seuls agents à avoir une indication officielle au Canada pour le traitement du syndrome des jambes sans repos. C. La cabergoline n’est plus une première ligne de traitement compte tenu des risques de fibrose pulmonaire et de valvulopathie cardiaque associés. D. Les études ont montré avec certitude que le pramipexole est mieux toléré et plus efficace que le ropinirole pour soulager le syndrome des jambes sans repos. E. Les effets secondaires plus sérieux rapportés avec le pramipexole et le ropinirole dans la maladie de Parkinson (dyskinésies, hallucinations, attaques de sommeil, psychoses, impulsivité) sont beaucoup moins fréquents chez les patients atteints d’un syndrome des jambes sans repos. Veuillez reporter vos réponses dans le formulaire de la page 78 38 Québec Pharmacie vol. 57 n° 3 juin 2010 Mise à jour diabète 2010 Le diabète en pédiatrie AUSSI... Quoi de neuf dans le traitement du diabète ? Un supplément de Quoi de neuf en matière de diabète ? Aperçu des nouvelles tendances en matière de prévention, des nouveaux outils d’évaluation pour la pratique, des risques de cancer et des nouveaux traitements Par Maryann Hopkins, BSP, éducatrice certifiée en diabète Réviseur scientifique de la version française : Frédéric Poitras, B. Pharm., pharmacien de pratique communautaire, chargé de cours et responsable des soins pharmaceutiques I et II, Faculté de pharmacie, Université Laval. Mise à jour diabète 2010 En 2009, le Modèle canadien des coûts du diabète, un nouvel outil économique mis au point pour l’Association canadienne du diabète, a permis de prédire que 9,9 % de la population canadienne sera atteinte de diabète en 2020, en hausse par rapport à 4,2 % en 20001. Ce qu’indique cette statistique, en définitive, c’est qu’actuellement, au Canada, 20 personnes en moyenne reçoivent un diagnostic de diabète toutes les heures, jour après jour. Ce même rapport estime que le fardeau économique du diabète au Canada s’élèvera à 16,9 milliards $ en 2020, contre 12,2 milliards, actuellement en 2010. Les pharmaciens seront particulièrement intéressés de savoir que l’on s’attend à ce que les médicaments représentent 4 % de cette estimation de dépense. Maryann Hopkins ([email protected]) est une pharmacienne clinicienne spécialisée dans les soins aux diabétiques à l’Hôpital d’Ottawa, en Ontario. Elle fait également partie du comité des experts qui ont participé à l’élaboration des Lignes directrices de pratique clinique 2008 de l’Association canadienne du diabète pour la prévention et le traitement du diabète au Canada. www.professionsante.ca juin 2010 vol. 57 n° 3 Québec Pharmacie S3 Prévention du diabète Modifications du mode de vie ou metformine : efficacité pendant au moins une dizaine d’années Bien que des études d’intervention aient démontré que les modifications du mode de vie ou la prise de metformine peuvent prévenir ou retarder l’apparition du diabète, on ne sait pas encore très bien pendant combien de temps ces interventions peuvent être efficaces2,3. L’étude DPPOS (Diabetes Prevention Program Outcomes Study), une extension de l’étude Diabetes Prevention Program Study originale, a été publiée en novembre 20094. Celle-ci a déterminé qu’une intervention intensive sur le mode de vie appliquée sur 10 ans permet de réduire de 34 % l’incidence du diabète, comparativement au placebo. Ces interventions sur le mode de vie consistaient en des stratégies visant à aider les patients à perdre 7 % de leur poids corporel et à les inciter à faire un minimum de 150 minutes d’activité physique d’intensité modérée par semaine. Par ailleurs, chez les autres sujets pour qui l’intervention consistait à prendre de la metformine au cours de la période de suivi de 10 ans, une réduction de 18 % de la progression vers le diabète fut observée, comparativement au placebo. Par conséquent, l’utilisation d’interventions sur le mode de vie ou la prise de la metformine peut prévenir ou retarder le développement du diabète de type 2 pendant au moins 10 ans. Les chercheurs du groupe Diabetes Prevention Program (DPP) prévoient maintenant une troisième phase de suivi de cette étude afin de chercher à évaluer les résultats et les bénéfices de ces interventions mises en application à long terme et, donc, de bien définir les avantages de la prévention du diabète. S4 Québec Pharmacie vol. 57 n° 3 juin 2010 Mise en application de lignes directrices de pratique clinique pour le traitement du diabète Les Lignes directrices de pratique clinique 2008 de l’Association canadienne du diabète pour la prévention et le traitement du diabète au Canada sont des lignes directrices fondées sur des données probantes reconnues internationalement. Elles ont été élaborées afin de guider les praticiens dans le traitement et la prévention du diabète au Canada5. De nombreux guides cliniques ont été établis pour le traitement de différentes maladies ou problèmes de santé; toutefois, le groupe qui s’est Vous pouvez télécharger le document sur www.diabetes.ca intéressé au diabète est allé un peu plus loin en créant des outils pour aider les professionnels de la santé à incorporer les recommandations relatives au diabète à leur pratique quotidienne. Quoi de neuf dans le traitement du diabète ? www.professionsante.ca une exposition prolongée aux toxines exogènes, à une production accrue d’acides biliaires qui peuvent devenir cancérigènes et à l’hyperinsulinémie11. L’association entre le cancer et le diabète de type 1 est toutefois moins claire. Il semble cependant que le diabète de type 1 accroît d’environ 20 % le risque global de cancer – les cancers de l’estomac, de l’endomètre et du col de l’utérus étant ceux qui y sont le plus étroitement associés16. Les traitements du cancer et le diabète Tel que mentionné au préalable, des publications récentes se sont concentrées sur l’association entre l’insuline glargine et le cancer7-10. Les données de ces publications ont cependant donné lieu à beaucoup de débats17,18. Les spécialistes du diabète ont des avis partagés, les patients sont souvent inquiets, les professionnels de la santé sont parfois dans la confusion, et les comités et les commissions ont fait des commentaires peu utiles dans la pratique quotidienne, car ils laissent le choix de maintenir ou de retirer le traitement insulinique aux professionnels de la santé. Les associations américaines et canadiennes du diabète ont fait des déclarations laissant penser que les données observées sont contradictoires et discutables, et qu’on ne sait pas très bien si une sorte d’insuline accroît plus le risque de cancer qu’une autre19,20. Ces associations juin 2010 vol. 57 n° 3 Québec Pharmacie Mise à jour diabète 2010 Cancer et diabète Des publications récentes suggérant une association potentielle entre l’insuline glargine et le cancer7-10 ont incité de nombreux diabétiques à poser des questions à leur pharmacien au sujet de leurs risques d’avoir un cancer. Il faut d’abord faire ressortir que des données épidémiologiques récentes permettent de penser que le fait d’être diabétique peut être un facteur de risque indépendant de développement de divers types de cancer11. Les résultats d’une vaste étude de mortalité menée par Coughlin et coll. permettent de penser que le diabète peut être lié aux décès par cancers du côlon, du foie, du pancréas et de la vessie chez les hommes, et du côlon, du pancréas et du sein chez les femmes11. En 2005, une méta-analyse (portant sur plus de 9000 sujets) a fait une revue systématique de 36 études qui avaient étudié l’association entre le cancer du pancréas et le diabète12. L’étude a elle aussi conclu que le diabète de type 2 est un facteur de risque indépendant de cancer du pancréas, avec une augmentation du risque de 1,7 fois. Larson et coll. ont eux aussi réalisé plusieurs méta-analyses pour déterminer la relation entre divers cancers et le diabète. Leur méta-analyse de 2007 a montré une multiplication potentielle par 1,2 du risque de cancer du sein chez les femmes diabétiques13, tandis que leur méta-analyse de 2006 avait montré une multiplication par 1,2 du risque de cancer de la vessie chez les sujets diabétiques14. Selon leur méta-analyse de 2005, les sujets diabétiques avaient un risque de cancer colorectal multiplié par 1,315. On pense actuellement que l’association entre le diabète de type 2 et le cancer serait médiée par l’hyperinsulinémie, l’hyperglycémie, le syndrome métabolique et la résistance à l’insuline11. Le lien se ferait par l’intermédiaire de modifications dans la croissance des cellules, via les récepteurs de l’insuline et les récepteurs des facteurs de croissance insulinomimétiques 1 (IGF-1R). On pense que l’association avec le cancer du côlon serait liée à un temps de transit ralenti de la nourriture et, de ce fait, à ments e g n a se Les ch vie et la pri nt e de d o m peuve e au n i er tform de me ir ou retard e t n diabè préve u d n ritio l’appa e 2. de typ S5 Quoi de neuf dans le traitement du diabète ? Nouveaux agents antidiabétiques Deux nouveaux agents pour le traitement du diabète de type 2 ont été mis sur le marché en 2009. Une association sitagliptine/ 1. metformine Le médicament Janumetmd, une association de metformine et de sitagliptine, a été le premier traitement associant la metformine et un inhibiteur de la dipeptidyl peptidase-4 (DPP-4) à être mis en vente au Canada. Cet agent est indiqué dans les cas où la metformine et les modifications du mode de vie ne permettent pas une maîtrise optimale du diabète ou chez les sujets qui prennent déjà de la metformine et de la sitagliptine séparément. Janumet doit être pris deux fois par jour à raison de 50 mg de sitagliptine par comprimé, associé à un choix de trois doses de metformine (500 mg, 750 mg ou 1 000 mg par comprimé). En plus d’être une nouvelle option de traitement, cette association permet de réduire le grand nombre de comprimés que doivent prendre les sujets diabétiques. Il faut également noter que, le 15 décembre 2009, la sitagliptine a été approuvée au Canada en monothérapie pour traiter les patients qui ne peuvent pas prendre de metformine ou qui ne la tolèrent pas. 2. Un nouvel inhibiteur de la DPP-4 Un deuxième inhibiteur de la DDP-4 a fait son entrée sur le marché canadien en 2009. La saxagliptine (Onglyzamd) a été approuvée pour le www.professionsante.ca traitement du diabète de type 2 en tant que thérapie d’association à la metformine ou à une sulfonylurée. La dose recommandée est de 5 mg une fois par jour à prendre toujours à la même heure avec ou sans nourriture. Dans une étude clinique à répartition aléatoire à double insu contrôlée avec placebo, De Fronzo et coll. ont montré que la saxagliptine 5 mg par jour associée à la metformine fait baisser le taux d’hémoglobine glyquée (HbA1c) de moins de 1 % (c.-à-d. 0,69 % avec la saxagliptine, contre une augmentation de 0,13 % avec le placebo)22. Avec la dose quotidienne de 5 mg, 44 % des sujets ont atteint un taux d’HbA1C inférieur à 7 %, comparativement à 17 % des sujets recevant le placebo. Dans un essai multicentrique randomisé à double insu, une association de 5 mg par jour de saxagliptine et de 7,5 mg par jour de glyburide a été comparée à un placebo associé à une dose de 10 mg de glyburide (augmentée progressivement à un maximum de 15 mg). Le taux d’HbA1c a été réduit de 0,64 % dans le groupe saxagliptine, comparativement à une augmentation de 0,08 % dans le groupe placebo23. Bien que les inhibiteurs de la juin 2010 vol. 57 n° 3 Québec Pharmacie Mise à jour diabète 2010 conseillent aussi aux patients de ne pas cesser de s’administrer de l’insuline, mais de parler avec leur médecin de la façon de traiter leur diabète. D’autres études seront nécessaires pour examiner la relation entre l’utilisation de l’insuline et le cancer. Il est à noter que la metformine semble réduire le risque de cancer du pancréas21. moins t n e i o s u’ils s q n ’autre r e i d B e u ces q baisse a r effica u o p iments c, les inhib e t i a r t ’HbA1 4 pris en d x u a le t DPPs a l e d rent le o i l é teurs m tion a émie c a i y c l o g s as e la ons d i t a i r diale. va n a r p post S7 Quoi de neuf dans le traitement du diabète ? Mise à jour diabète 2010 DPP-4 existants soient moins efficaces pour abaisser le taux d’HbA1c que d’autres traitements dont nous disposons pour traiter le diabète de type 2, ils améliorent les variations de la glycémie postprandiale quand ils sont associés à la metformine ou, dans le cas de la saxagliptine, à une sulfonylurée22,23. Il s’agit là d’un effet clinique très significatif dans la mesure où le taux d’HbA1c se rapproche de 7 %, car l’abaissement de la glycémie postprandiale s’associe de façon plus importante à l’HbA1c que l’abaissement la glycémie plasmatique à jeun24. Les effets secondaires les plus fréquemment signalés avec la saxagliptine dans les évaluations S8 préalables à la mise en marché ont été les infections des voies respiratoires, les infections urinaires et les maux de tête. Quand cet agent est ajouté à une sulfonylurée, les patients peuvent être plus à risque de faire de l’hypoglycémie25. L’efficacité de cet agent, ainsi que ses effets indésirables semblent être actuellement similaires à ceux de la sitagliptine. Cependant, comme on ne dispose pas encore de résultats d’études comparatives, il est difficile de déterminer si un agent est supérieur à l’autre. On peut maintenant utiliser ces deux nouveaux médicaments pour traiter les diabétiques. Des observations consécutives à la mise en marché aideront à définir leur place dans le traitement. | Références 1. Canadian Diabetes Association. An economic tsunami : the cost of diabetes in Canada, décembre 2009. www.diabetes.ca/documents/get-involved/FINAL_Economic_Report.pdf (consulté le 7 janvier 2010). 2. Knowler WC, Barrett-Connor E, Fowler SE et coll. Reduction in the incidence of type 2 diabetes with lifestyle intervention or metformin. N Engl J Med, 2002;346:393-403. 3. Pan XR, Li GW, Hu YH et coll. Effects of diet and exercise in preventing NIDDM in people with impaired glucose tolerance. The Da Qing IGT and Diabetes study. Diabetes Care, 1997;20:537-44. 4. Diabetes Prevention Program Research Group. 10-year follow-up of diabetes incidence and weight loss in the Diabetes Prevention Program Outcomes Study. Lancet, 2009;374:1677-86. 5. Canadian Diabetes Association. Canadian Diabetes Association 2008 clinical practice guidelines for the prevention and management of diabetes in Canada. Can J Diabetes, 2008;32(Suppl 1). www.diabetes.ca/files/cpg2008/cpg-2008.pdf (consulté le 7 janvier 2010). 6. Canadian Diabetes Association. Introducing the 2008 clinical practice guidelines tool kit. Theme #1: cardiovascular risk assessment and reduction. www.diabetes.ca/for-professionals/resources/cpg-toolkit/ (consulté le 7 janvier 2010). 7. Colhoun HM, SDRN Epidemiology Group. Use of insulin glargine and cancer incidence in Scotland: a study from the Scotish Diabetes Research Network Epidemiology Group. Diabetologia, 2009;52:1755-65. 8. Hemkens LG, Grouven U, Bender R et coll. Risk of malignancies in patients with diabetes treated with human insulin or insulin analogues: a cohort study. Diabetologia, 2009;52:1732-44. 9. Jonasson JM, Ljunj R, Talback M et coll. Insulin glargine use and short-term incidence of malignancies–a population-based follow-up study in Sweden. Diabetologia, 2009; 52:1745-54. 10. Currie CJ, Poole CD, Gale EAM. The influence of glucose-lowering therapies on cancer risk in type 2 diabetes. Diabetologia, publié en ligne le 2 juillet 2009. http://webcast.easd.org/press/glargine/d ownload/090740Curriecorrectedproofs.pdf (consulté le 7 janvier 2010). 11. Coughlin SS, Calle EE, Teras LR et coll. Diabetes mellitus a predictor of cancer mortality in a large cohort of US adults. Am J Epidemiol, 2004;159;1160-7. 12. Huxley R, Ansary-Moghaddam A, Berrington de Gonzalez A et coll. Type II diabetes and pancreatic cancer: a meta-analysis of 36 studies. Br J Cancer, 2005;92:2076-83. 13. Larson SC, Mantzoros CS, Wolk A. Diabetes mellitus and risk of breast cancer: a meta-analysis. Int J Can, 2007;121:856-62. 14. Larson SC, Orsinii N, Bismark K et coll. Diabetes mellitus and risk of bladder cancer; a meta-analysis. Diabetologia, 2006;49:2819-23. 15. Larson SC, Orsinii N, Wolk A. Diabetes mellitus and risk of colorectal cancer: a metaanalysis. J Natl Cancer Inst, 2005;97:1679-87. 16. Smith U, Gale EAM. Does diabetes therapy influence the risk of cancer? Diabetologia, 2009;52:1699-708. 17. Stumvoll M, Nawroth PP. The insulin glargine dilemma: an opportunity for the diabetes community? Diabetologia, 2009;52:1987-9. 18. Simon D. Diabetes treatment with insulin glargine and risk of malignancy: methodological pitfalls and ethical issues. Diabetologia, libre accès, 27octobre 2009. www.springerlink.com/content/hv0184142k832k37/?p=aac67d27c2ba4b13af8477bd248dc941&pi=1 (consulté le 7 janvier 2010). 19. Canadian Diabetes Association statement on insulin glargine and the possible link to cancer; 3 juillet 2009. www.diabetes.ca/get-involved/news/canadian-diabetes-association-statement-on-insulin-glargine-and-the-possibl/ (consulté le 7 janvier 2010). 20. American Diabetes Association. Statement from the American Diabetes Association related to studies published in Diabetologia; 26 juin 2009. www.diabetes.org/for-media/2009/statement-from-theamerican-2009-1.html (consulté le 7 janvier 2010). 21. Donghui LI, Yeung SJ, Hassan MM et coll. Antidiabetic therapies affect risk of pancreatic cancer. Gastroenterology, 2009;137;482-8. 22. DeFronzo RA, Hissa MN, Garber JL et coll. The efficacy and safety of saxagliptin when added to metformin therapy in patients with inadequately controlled type 2 diabetes with metformin alone. Diabetes Care, 2009;32:1649-55. 23. Chacra AR, Tn GH, Apanovitch A et coll. Saxagliptin added to a submaximal dose of sulfonylurea improves glycemic control compared with uptitration with sulfonylurea in patients with type 2 diabetes: a randomized controlled trial. Int J Clin Pract, 2009;63:1395-406. 24. Monnier L, Lapinski H, Colette C. Contributions of fasting and postprandial plasma glucose increments to the overall diurnal hyperglycemia of type 2 diabetic patients. Diabetes Care, 2003;26:881-5. 25. Bristol-Myers Squibb Canada. Onglyza (saxagliptin), monographie de produit. Montréal (QC); 14 septembre 2009. www.bmscanada.ca/upload/ File/pdf/products/ONGLYZA%20PM%20English%20Approved%202009-09-14.pdf (consulté le 15 janvier 2010). Québec Pharmacie vol. 57 n° 3 juin 2010 Le diabète en pédiatrie Prise en charge, surveillance et précautions particulières chez les enfants et les adolescents Par Peggy Apostolides, B. Sc. Pharm., éducatrice agréée en diabète* Révision scientifique de la version française : Jean-François Bussières, B. Pharm. M. Sc., M.B.A., F.C.S.H.P., chef du département de pharmacie et de l’unité de recherche en pratique pharmaceutique, CHU Sainte-Justine. Mise à jour diabète 2010 Le diabète sucré est la maladie endocrinienne la plus courante et c’est l’une des maladies chroniques auto-immunes les plus fréquentes chez les enfants1. Le diabète de type 1 est le type de diabète le plus souvent diagnostiqué chez les enfants, représentant plus de 90 % des cas chez les enfants et les adolescents2. Au Canada, l’incidence moyenne du diabète de type 1 est d’environ 25 cas pour 100 000 chez les enfants de la naissance à l’âge de 14 ans2. Un très grand nombre de données permettent désormais de penser que l’incidence du diabète de type 1 est en augmentation chez les enfants. Plusieurs théories ont été mises de l’avant pour expliquer cette augmentation, dont le nombre accru de naissances par césarienne, des facteurs alimentaires (p. ex., carence en vitamine D ou exposition aux protéines du lait de vache ou aux céréales), exposition réduite aux infections infantiles et hausse de l’obésité chez les enfants)3. Peggy Apostolides ([email protected]) est pharmacienne clinicienne et éducatrice agréée en diabète à l’unité pédiatrique médicale de l’IWK Health Centre d’Halifax, en Nouvelle-Écosse. Ses domaines de pratique clinique actuels sont les soins aux patients pédiatriques hospitalisés en médecine générale, ainsi que les services de distribution et de préparations stériles à la pharmacie centrale. L’auteure remercie Sheilagh Crowley, RN, BN, CDE, infirmière enseignante en diabète à la clinique de diabète pédiatrique de l’IWK, et Robin Shaw, B. Sc. Pharm., de l’IWK Health Centre, pour l’aide qu’elles lui ont apportée dans la rédaction de cet article. www.professionsante.ca juin 2010 vol. 57 n° 3 Québec Pharmacie S11 Le diabète de type 2 est également en hausse chez les enfants. Aux États-Unis, on estime que l’incidence du diabète de type 2 chez les enfants a été multipliée par 10 à 30 dans les 10 à 15 dernières années1. Le diabète de type 2 est souvent associé à certaines populations à haut risque (ex. : Autochtones, Afro-Américains, Hispaniques, Asiatiques)4 et il est plus souvent diagnostiqué dans la deuxième décennie de la vie chez les enfants et les adolescents obèses2. D’autres facteurs de risque sont les antécédents familiaux, l’obésité, l’exposition au diabète in utero, l’acanthosis nigricans, le syndrome des ovaires polykystiques, l’hypertension, la dyslipidémie et la stéatose hépatique non alcoolique2. Étiologie/physiopathologie Comme le diabète de type 1 se caractérise par une carence absolue de la sécrétion d’insuline, les personnes atteintes sont prédisposées à l’acidocétose. La pathogenèse est complexe, la plupart des cas étant causés par la destruction médiée par les lymphocytes T des cellules bêta des îlots du pancréas, entraînant des symptômes qui se développent de façon insidieuse avec le temps, après que plus de 90 % des cellules bêta ont été détruites2. Le processus peut commencer des mois ou des années avant l’apparition des symptômes cliniques2,5 et on pense qu’il implique des déclencheurs environnementaux (chimiques ou viraux) qui provoquent la destruction des cellules bêta du pancréas. Bien que ces déclencheurs restent largement inconnus, on associe l’infection à entérovirus au développement d’anticorps associés au diabète dans certaines populations. La rubéole congénitale est un déclencheur connu2. En dehors de l’agrégation familiale, qui compte pour environ 10 % des cas de diabète de type 1, il n’y a pas de modèle d’acquisition reconnaissable2. On distingue souvent les sujets à risque accru de développer le diabète de type 1 par la mesure des anticorps, par les marqueurs génétiques et par des tests intraveineux de tolérance au glucose3. À l’heure actuelle, on ne connaît aucun moyen de prévenir ou de retarder l’apparition du diabète de type 1, bien que plusieurs études en cours tentent d’examiner le rôle de divers traitements (ex. : S12 Québec Pharmacie vol. 57 n° 3 juin 2010 vaccination par l’acide glutamique décarboxylase6 en vue de prévenir la maladie ou d’induire une rémission1,2). Le diabète de type 2 survient quand la sécrétion d’insuline est insuffisante pour faire face à la demande accrue associée à la résistance à l’insuline. Cela peut aller d’une prédominance de la résistance à l’insuline avec une carence relative en insuline à un défaut prédominant de la sécrétion associé à une résistance à l’insuline. Le diabète est souvent associé à d’autres caractéristiques de la résistance à l’insuline (ex. : hyperlipidémie, hypertension, obésité). L’âge moyen au moment du diagnostic chez les jeunes est de 13,5 ans, ce qui coïncide avec les changements associés à la puberté et au développement d’une résistance à l’insuline chez certains sujets qui pouvaient n’avoir eu aucun symptôme jusque-là2. Diagnostic Chez l’enfant, le diagnostic de diabète, quel qu’en soit le type, est généralement établi sur la base de l’absence ou de la présence de symptômes cliniques (ex. : polyurie, polydipsie, fatigue, vision brouillée, perte de poids et hyperglycémie manifeste (qui doit être mesurée en laboratoire et non pas à l’aide d’un glucomètre personnel). Le tableau 1 propose une liste des symptômes de diabète qui peuvent se manifester chez les enfants et les adolescents. Trois méthodes peuvent être utilisées pour diagnostiquer le diabète (tableau 2). En l’absence d’une hyperglycémie manifeste accompagnée d’une décompensation métabolique aiguë1, chaque méthode doit être confirmée dans les jours suivants par l’une des trois méthodes indiquées au tableau 2. Au moment de la manifestation de la maladie, une bandelette réactive trempée dans l’urine confirmera généralement la présence de glycosurie. Environ 21 % des sujets nouvellement diagnostiqués présentent de l’acidocétose diabétique7. En biochimie, l’acidocétose diabétique se définit par une glycémie > 11 mmol/L (200 mg/dL), par un pH veineux de 7,3 ou par un taux de bicarbonate < 15 mmol/L, ainsi que par une cétonémie et une cétonurie2. L’acidocétose diabétique se produit quand il y a un manque relatif ou absolu d’insuline circulante, ce qui entraîne une augmentation des taux Le diabète en pédiatrie Tableau 1 Symptômes possibles de diabète chez les enfants et les adolescents2 Symptômes non émergentsaSymptômes émergentsb Énurésie (peut être confondue avec Hyperventilation (peut être confondue avec une infection urinaire ou attribuée à une la pneumonie ou l’asthme) consommation de liquide plus importante) Mauvais développement/perte de poids Déshydratation grave/ vomissements fréquents chez un enfant jusque-là en bonne santé Candidose vaginale (en particulier Polyurie constante malgré la présence chez les filles prépubères) de déshydratation Vomissements (peuvent être confondus Joues rouges/haleine fruitée due à l’acidocétose avec une gastroentérite) Infection cutanée récurrente Conscience défaillante Irritabilité et baisse des résultats scolaires Choc/hypotension d’hormones contre-régulatoires (c.-à-d. glucagon, cortisone, hormone de croissance) qui accélère le catabolisme des réserves de glucose (glycogénolyse) et accroît la production de glucose par le foie et par les reins (gluconéogenèse). Cela mène à l’hyperglycémie, à l’hyperosmolalité et à une augmentation de la lipolyse et de la cétogenèse. La formation de cétones est pour l’organisme la façon de produire une « source de carburant de rechange » puisque, sans insuline, le glucose ne parvient pas à pénétrer dans les cellules; cependant, l’acétose crée, à son tour, un état d’acidose métabolique qui se traduit parfois par une haleine « fruitée ». Les symptômes de l’acidocétose diabétique sont la déshydratation, une respiration rapide et profonde (aussi appelée respiration de Kussmaul), la nausée, les vomissements, les douleurs abdominales, la perte progressive des capacités mentales et la perte de connaissance2. Si l’acidocétose diabétique n’est pas traitée rapidement, elle mène au coma et finalement à la mort. Ses complications sont l’œdème cérébral, l’hypoglycémie, l’hypokaliémie et l’acidose hyperchlorémique2. Chez l’enfant, les facteurs de risque sont un mauvais contrôle métabolique ou des épisodes antérieurs d’acidocétose diabétique, l’oubli d’administrer de l’insuline, une défaillance de la pompe à insuline, le fait d’être une fille prépubère ou adolescente, ou un enfant ayant des troubles psychiatriques (dont des troubles de l’alimentation)2. On observe un taux plus élevé d’acidocétose diabétique lors du diagnostic initial chez les enfants de moins de cinq ans, chez qui certains des symptômes sont difficiles à discerner. Il faut mentionner que www.professionsante.ca les enfants atteints de diabète de type 2 peuvent également présenter une acidocétose diabétique2. Les autres facteurs à prendre en considération quand on pose un diagnostic de diabète chez les enfants sont l’utilisation de médicaments susceptibles d’accroître la glycémie de façon transitoire ou de provoquer une résistance à l’insuline. Il s’agit des corticostéroïdes (ex. : prednisone, dexaméthasone), de certains médicaments d’oncologie (ex. : L-asparaginase), des immunosuppresseurs (ex. : tacrolimus, cyclosporine) et des antipsychotiques atypiques (ex. : rispéridone, olanzapine)2. Traitement Quel que soit le type de diabète, le traitement doit porter à la fois sur la médication, sur le régime alimentaire et sur l’exercice physique. Il faut également proposer un soutien psychologique puisque le patient va devoir traverser une phase d’adaptation à son diagnostic de diabète et qu’une assistance permanente sera nécessaire pour aider l’enfant ou l’adolescent à s’adapter à son nouveau mode de vie. Diabète de type 1 L’insulinothérapie reste la pierre angulaire du traitement des enfants et adolescents atteints de diabète de type 1, même si des recherches se penchent sur la possibilité d’utiliser des traitements d’appoint (ex. : des analogues synthétiques de l’amyline, comme le pramlintide, et des peptides ayant des effets semblables à ceux de l’hormone incrétine humaine GLP-1 [glucagon-like peptide-1], comme l’exénatide)8. juin 2010 vol. 57 n° 3 Québec Pharmacie Mise à jour diabète 2010 A) Les symptômes non émergents sont ceux qui ne sont généralement pas considérés comme urgents par les parents. B) Les symptômes émergents sont ceux qui sont normalement constatés dans les services d’urgence. S13 Le diabète en pédiatrie Tableau 2 Critères du diagnostic de diabète sucré1,2 Le pancréas fabrique naturellement l’insuline de deux façons : par une lente sécrétion continue dans le sang (l’insuline basale) et par des sécrétions plus importantes qui se produisent par à-coups quand la glycémie s’élève, habituellement après les repas (l’insuline à bolus). Le traitement consiste à imiter ce processus physiologique à l’aide d’injections quotidiennes multiples (IQM) sous-cutanées d’insuline ou d’une perfusion continue d’insuline en administration sous-cutanée à l’aide d’une pompe à insuline. Le régime choisi dépend de plusieurs facteurs, dont l’âge de l’enfant, le coût du traitement et la personne qui administrera l’insuline. Par exemple, la plupart des écoles n’autorisent pas les enseignants ou leur personnel à administrer l’insuline (ni le glucagon). Ainsi, un enfant d’âge scolaire qui est incapable de s’injecter son insuline aura besoin d’un protocole excluant l’insuline lors du repas du midi. Pour traiter les enfants, on préfère généralement les insulines à action rapide (ex. : insuline lispro, insuline aspart ou insuline glulisine), car il est souvent difficile de prédire quand un bébé ou un petit enfant mangera et quelle quantité de nourriture il absorbera. Du fait de leur délai d’action rapide (10 à 15 minutes), ces insulines permettent une souplesse d’administration après que l’enfant a mangé9. Il sera nécessaire d’associer à l’insuline à action rapide une insuline à action intermédiaire (ex. : NPH) ou une insuline basale (ex. : insulines glargine ou détémir). Les protocoles couramment appliqués aux enfants sont : n un régime « deux fois par jour (bid) » dans lequel une insuline NPH et une insuline à action rapide sont www.professionsante.ca administrées avant le petit-déjeuner et avant le souper. n un régime « trois fois par jour (tid) » dans lequel une insuline à action rapide est administrée au petit-déjeuner et au souper, et une insuline à action intermédiaire au petit-déjeuner et au coucher. n un régime par injections quotidiennes multiples dans lequel on administre une insuline à action rapide avant l’heure des repas (en fonction du rapport insuline/ glucides) et une insuline intermédiaire ou à longue durée d’action à l’heure du coucher. Le régime par injections quotidiennes multiples (IQM) permet plus de souplesse et assure la meilleure maîtrise de la glycémie2, mais il exige de compter les glucides que l’on va absorber, ce qui peut s’avérer compliqué. Ce type de régime exige également de contrôler plus fréquemment la glycémie et les enfants doivent être capables de s’administrer eux-mêmes leur dose d’insuline au moment du repas de midi, ce qui n’est pas toujours possible. Le tableau 3 donne des conseils sur l’utilisation de l’insuline avec les enfants. On utilise désormais de plus en plus souvent des pompes à insuline (qui injectent continuellement de l’insuline en sous-cutané) chez les bébés et les enfants. Beaucoup de patients les préfèrent, car elles constituent la méthode la plus physiologique d’administration de l’insuline que nous ayons à notre disposition10. Des études ont montré que la maîtrise du diabète à l’aide des pompes à insuline est similaire à celle obtenue avec les IQM, avec des taux d’hypoglycémie qui juin 2010 vol. 57 n° 3 Québec Pharmacie Mise à jour diabète 2010 1. Symptômes du diabète plus concentration de glucose plasmatique aléatoire ≥ 11,1 mmol/L (200 mg/dL). (aléatoire = à n’importe quel moment de la journée sans tenir compte de l’heure du dernier repas) ou 2. Concentration de glucose plasmatique à jeun ≥ 7,0 mmol/L (≥ 126 mg/dL) (à jeun = aucun apport calorique depuis au moins huit heures) ou 3. Glycémie ≥ 11,1 mmol/L (≥ 200 mg/dL) deux heures après une surcharge de glucose dans le cadre d’un test oral de tolérance au glucose (un test oral de tolérance au glucose doit être effectué en suivant les indications de l’OMS, à l’aide d’une surcharge de glucose contenant l’équivalent de 75 g de glucose anhydre dissous dans de l’eau [ou 1,75 g par kg de poids corporel jusqu’à un maximum de 75 g])16 S15 ce Astu vertir on Pour c e glycémie d tures /L, c e l s mmol de n e L /d de mg z la valeur divise ar 18. p L d / en mg semblent comparables, sinon inférieurs10,11. Les pompes fonctionnent en programmant un taux basal d’insuline à perfuser en continu dans la circulation sanguine, ainsi que S16 Québec Pharmacie vol. 57 n° 3 juin 2010 des ajouts de bolus pour contrebalancer les apports de glucides. Les pompes les plus récentes comportent des caractéristiques « intelligentes » permettant à l’utilisateur de programmer le nombre de glucides qu’il doit absorber et la pompe calcule ensuite la dose du bolus nécessaire pour tel ou tel repas. On peut également, si on le désire, programmer plus d’un taux basal pour différents moments de la journée en fonction des fluctuations individuelles de la glycémie. Normalement, on utilise des insulines à action rapide avec les pompes à insuline 9,10. Il est très important que l’utilisateur connaisse bien les signes et les symptômes de l’hyperglycémie, car l’acidocétose peut se développer très rapidement en cas de mauvais fonctionnement de la pompe ou de problème d’absorption de l’insuline au point d’injection. II est recommandé à tous les utilisateurs d’une Le diabète en pédiatrie pompe à insuline de se servir d’un appareil de contrôle du taux de cétone sanguin, qui mesure l’hydroxybutyrate-bêta, la cétone qui est la plus rapidement produite par l’organisme. On doit conseiller aux utilisateurs de pompe à insuline de vérifier la présence de cétones dans leur sang quand leur glycémie est supérieure à 14,0 mmol/L2. Ils doivent aussi apprendre à utiliser des stylos injecteurs ou des seringues d’insuline en cas de doute quant au bon fonctionnement de la pompe. Dans ce cas, plus tôt on s’injecte de l’insuline, moins le risque d’acidocétose diabétique est élevé. Diabète de type 2 Mise à jour diabète 2010 Le traitement du diabète de type 2 doit s’attaquer au mode de vie et aux habitudes de santé de l’ensemble de la famille en mettant l’accent sur une alimentation saine et sur l’activité physique. Il faut éventuellement parler aussi d’abandon du tabac, de perte de poids et de traitement des problèmes psychologiques. Les médicaments utilisés pour abaisser la glycémie chez les enfants sont la metformine orale et l’insuline, ainsi que, parfois, les sulfonylurées2. On doit toujours commencer par essayer la metformine, car elle permet de perdre du poids sans risque d’hypoglycémie. On ne dispose actuellement que de peu d’information sur l’utilisation d’autres classes de médicaments chez les enfants et les adolescents. De nouvelles études seront nécessaires pour évaluer l’utilité des nouveaux traitements4. Il est possible que la protéinurie, l’hypertension, l’obésité et la dyslipidémie soient présentes au moment du diagnostic de diabète de type 2. Le médecin doit réévaluer ces aspects au minimum une fois par an et www.professionsante.ca juin 2010 vol. 57 n° 3 Québec Pharmacie S17 Tableau 3 Conseils pour l’utilisation de l’insuline chez les enfants2 Conserver les fioles d’insuline non ouvertes au réfrigérateur. Une fois ouverts, les fioles/stylos injecteurs sont utilisables pendant quatre semaines à température ambiante. Utiliser un stylo injecteur pour chaque type d’insuline. Mélanger l’insuline à action intermédiaire en faisant rouler lentement 10 à 20 fois les fioles/stylos d’insuline entre les mains avant de les utiliser. Quand on aspire plus d’un type d’insuline dans une seringue, il faut toujours commencer par l’insuline claire, puis aspirer l’insuline trouble pour éviter l’inactivation de l’insuline à courte durée d’action ou à action rapide. Pour éviter le gaspillage, on peut se procurer des cartouches de 3 ml au lieu de 10 ml pour les enfants qui sont traités à l’aide de petites doses d’insuline. Les très jeunes enfants ont parfois besoin d’insuline diluée (avec un diluant provenant de chez le fabricant), mais il faut prendre des précautions particulières pour diluer le produit et l’aspirer dans la seringue. L’insuline à action rapide peut être diluée à 10 unités/ml ou à 50 unités/ml avec un diluant NPH stérile et conservée pendant un mois pour être utilisée dans des pompes pour bébés ou pour très jeunes enfants. Injecter l’insuline selon un angle de 90° par rapport à la peau. Les zones d’injection acceptables sont l’abdomen, les fesses, le devant de la cuisse ou la face latérale du bras; s’assurer d’utiliser une zone où il y a suffisamment de tissu adipeux sous-cutané (l’abdomen et les fesses de préférence). Faire une rotation des points d’injection dans une même zone anatomique pour éviter l’apparition de lipohypertrophie. Des seringues de plus petit format (30, 50 ou 100 unités) peuvent être nécessaires pour les enfants, de même que des aiguilles plus courtes pour les seringues et les stylos injecteurs. Ne jamais réutiliser les aiguilles ou les lancettes, car cela peut causer plus de douleur, ainsi qu’un risque d’infection. Il faut toujours évaluer les causes des injections douloureuses pour vérifier si l’angle et la profondeur de l’injection sont corrects (et si on ne pénètre pas dans le muscle). mesurer la tension artérielle à chaque visite. Un inhibiteur de l’enzyme de conversion de l’angiotensine (IECA) ou, en cas de contre-indication, un antagoniste des récepteurs de l’angiotensine (ARA) peuvent être utilisés pour traiter l’hypertension. Les patients doivent être suivis pour surveiller les effets secondaires potentiels des IECA : hyperkaliémie, toux sèche, maux de tête et impuissance2. On utilise parfois des statines et des chélateurs des acides biliaires pour traiter la dyslipidémie chez les enfants en cas d’échec des mesures portant sur l’alimentation, mais tout le monde n’est pas d’accord pour traiter ce problème de santé chez les enfants du fait du manque de données d’innocuité à long terme sur l’utilisation des statines chez les enfants12. Si on utilise une statine, il est prudent de surveiller les symptômes au niveau des muscles et des tissus conjonctifs (du fait du risque potentiel accru de rhabdomyolyse) ainsi que les enzymes hépatiques (du fait d’un risque accru d’hépatotoxicité). De même, tous les adolescents sexuellement actifs devraient être conseillés en matière de contra- S18 Québec Pharmacie vol. 57 n° 3 juin 2010 ception du fait du risque tératogénique potentiel des statines et des IECA12. Surveillance du diabète L’autosurveillance glycémique (ASG) est un aspect bien établi du plan de traitement du diabète. Le tableau 4 passe en revue les valeurs cibles de la glycémie et de l’hémoglobine glyquée (HbA1c) chez les enfants et les adolescents. La fréquence de l’ASG varie selon les individus, mais, habituellement, quatre à six contrôles journaliers sont associés à une meilleure maîtrise de la glycémie chez les patients qui reçoivent de l’insuline. L’ASG doit être effectuée avant les repas afin de déterminer les doses d’insuline. Il faut aussi l’effectuer chaque fois que l’on soupçonne une situation d’hypoglycémie, avant, pendant et après un exercice et plus souvent quand l’enfant est malade. Il peut aussi être utile, aussi bien pour les diabétiques de type 2 que de type 1 qui utilisent la méthode des IQM dosées en fonction du rapport insuline/glucides, de connaître leur glycémie postprandiale. De plus, il faudrait Le diabète en pédiatrie Tableau 4 Cibles de glycémie et d’HbA1c recommandées pour les enfants et les adolescents atteints de diabète de type 1 1,2 Âge HbA1c (%)aTaux de glucose Taux de glucoseCommentaires (an) plasmatique à plasmatique 2 h jeun/préprandial après un repasb (mmol/L) (mmol/L) < 6 < 8,5 6,0-12,0 – Prendre des précautions particuliè res pour minimiser les risques d’hypoglycémie du fait de la possi ble association entre l’hypoglycé mie grave et une déficience cognitive par la suite Les valeurs cibles doivent être gra6-12 < 8,0 4,0-10,0 – duées en fonction de l’âge de l’enfant 13-18 ≤ 7,0 4,0-7,0 5,0-10,0 Appropriées pour la plupart des adolescentsC HbA1c = hémoglobine glyquée A) L’ISPAD (International Society for Pediatric and Adolescent Diabetes) recommande une valeur cible d’HbA1c < 7,5 % pour toutes les tranches d’âge. B) On effectue rarement un contrôle postprandial chez les jeunes enfants, sauf chez ceux qui utilisent une pompe à insuline pour qui on ne dispose pas de valeurs cibles. C) Pour les adolescents chez qui cela peut être fait en toute sécurité, on peut envisager de viser une plage de glycémie normale (c.-à-d., pour un taux d’HbA1c ≤ 6,0 %, une glycémie à jeun/préprandiale de 4,0 à 6,0 mmol/L et un taux de glucose plasmatique deux heures après un repas de 5,0 à 8,0 mmol/L). mesurer la glycémie à 3 h du matin si on soupçonne une hypoglycémie nocturne ou en cas d’hyperglycémie se produisant systématiquement le matin. Il est utile de tenir un journal des valeurs de glycémie pour déceler des tendances ou des présentations qui reviennent régulièrement, ce qui peut servir à adapter le traitement. Au moins une fois par an, les valeurs glycémiques obtenues à l’aide du glucomètre de l’enfant doivent être comparées à des valeurs obtenues en laboratoire afin de s’assurer de la précision des lectures réalisées à l’aide du glucomètre. Les lectures ne doivent pas varier de plus de 20 % pour les glycémies supérieures à 4,2 mmol/L et une variation moindre doit être acceptée en cas de glycémie inférieure ou égale à 4,2 mmol/L1. Les systèmes de surveillance continue de la glycémie mesurent les concentrations de glucose dans le liquide interstitiel. Il existe deux types d’appareils : les systèmes « en temps réel », qui affichent les résultats de la glycémie directement sur le système de surveillance, et d’autres qui n’ont pas cette capacité. Il a été démontré que les appareils à affichage en temps réel permettent de réduire la durée de l’hypoglycémie nocturne, de l’hyperglycémie et de l’hypoglycémie chez les patients traités par l’insuline1, et qu’ils ont un effet positif sur l’HbA1c2,13. On a toutefois constaté des discordances entre les données de ce type d’appareil et les www.professionsante.ca véritables glycémies à des périodes où la glycémie fluctuait rapidement1,2. De ce fait, il reste nécessaire d’effectuer des tests de glycémie capillaire afin de calibrer l’appareil et de prendre des décisions thérapeutiques. Les appareils qui ne donnent pas un affichage en temps réel sont utilisés de façon rétrospective, en général sur une période de 72 heures. Les résultats peuvent être téléchargés sur un ordinateur pour être analysés et ils peuvent aider à détecter des épisodes d’hypoglycémie ou d’hyperglycémie passés inaperçus. On constate aussi des écarts avec les appareils qui ne donnent pas un affichage en temps réel. Comme il y a de plus en plus de patients qui utilisent ces nouvelles technologies, il est important que les professionnels de la santé connaissent bien ces nouveaux systèmes13. Complications Hypoglycémie L’hypoglycémie est la complication aiguë la plus fréquente dans le traitement du diabète de type 1. Elle se définit par une glycémie inférieure à 4,0 mmol/L, bien que des symptômes puissent être ressentis au-dessus de cette limite s’il y a eu une importante variation du taux de glucose sanguin habituel d’un individu1. Les symptômes de l’hypoglycémie sont résumés au tableau 5. juin 2010 vol. 57 n° 3 Québec Pharmacie S19 Le diabète en pédiatrie Tableau 5 Symptômes de l’hypoglycémie2 SignesSymptômesSymptômes autonomes neuroglycopéniques non spécifiques Tremblements Difficulté à se concentrer Mal de tête Palpitations cardiaques Vision brouillée Fatigue Sudation Trouble de l’élocution Symptômes comportementaux Pâleur Perte de connaissance Faim Convulsions Irritabilité Nausée Confusion Cauchemars Fourmillement Faiblesse/somnolence Pleurs inconsolables Non traitée, l’hypoglycémie peut entraîner la mort. Il s’agit d’une complication particulièrement effrayante à laquelle les familles doivent faire face, car les enfants d’âge préscolaire et les bébés sont incapables de détecter ou de traiter par eux-mêmes ne serait-ce que des hypoglycémies mineures. Il est donc important que les pharmaciens connaissent bien le traitement et qu’ils participent à l’information des membres de la famille pour leur apprendre à réagir promptement. On traite les hypoglycémies de légères à modérées (le patient ressent des symptômes, mais il est capable de s’autotraiter) avec 15 g de glucose. Soit avec : n 15 g de glucose sous forme de tablettes n ¾ de tasse de jus ou 175 mL d’une boisson non alcoolisée standard (c.-à-d., non diète) n 6 bonbons Life Savers n 15 mL (1 cuillère à soupe) de miel n 15 mL (3 cuillères à café) ou 3 sachets de sucre dissous dans un verre d’eau toujours inférieure à 4,0 mmol/L, ils doivent prendre 15 g de glucose de plus. Une fois que la crise d’hypoglycémie a été traitée avec succès, il faut prendre le repas ou la collation habituelle selon le moment de la journée. Mais s’il leur faut attendre plus d’une heure pour le repas prévu, ils doivent prendre une collation (comportant 15 g de glucides et une source de protéines) afin d’éviter le retour de l’hypoglycémie1. Dans le cas d’un enfant inconscient de cinq ans et moins, l’hypoglycémie devrait être traitée à l’aide de glucagon 0,5 mg administré en injection sous-cutanée (SC) ou intramusculaire (IM). Les sujets de plus de cinq ans doivent recevoir 1 mg de glucagon SC ou IM. Les membres de la famille qui s’occupent d’un enfant diabétique doivent être formés à l’utilisation du glucagon le plus rapidement possible après le diagnostic afin de savoir comment réagir en cas d’urgence1. Une hypoglycémie grave chez une personne consciente (qui a besoin de l’aide d’une autre personne et dont la glycémie est de façon caractéristique inférieure à 2,8 mmol/L) devrait être traitée au moyen de 20 g de glucides, de préférence sous forme de tablettes de glucose1. Quel que soit le degré de l’hypoglycémie, tous les patients doivent savoir qu’il faut attendre 15 minutes après avoir traité une crise avant de revérifier la glycémie. Si celle-ci est Hyperglycémie, plan d’action pour les jours de maladie www.professionsante.ca Les signes et les symptômes de l’hyperglycémie sont semblables à ceux qui ont été constatés au moment du diagnostic (p. ex., polyurie, polydipsie, nausée et vomissements, perte de poids). Quand la glycémie s’élève au-dessus de 14,0 mmol/L, des tests pour vérifier la présence de cétones dans le sang ou dans les urines juin 2010 vol. 57 n° 3 Québec Pharmacie S21 Tableau 6 Voyager quand on est diabétique – Conseils pratiques pour les patients17,18 À faireÀ Emportez en double tout ce dont vous avez besoin (piles supplémentaires, glucomètre et pompe à insuline, contenant pour objets pointus et tranchants, insulines à courte et à longue durée d’action et seringues, glucagon [même pour les utilisateurs de pompes en cas de panne de la pompe]). Gardez vos médicaments dans vos bagages à main; si possible, demandez à un compagnon de voyage de prendre N des fournitures supplémentaires dans ses bagages à main au cas où les vôtres seraient perdus ou volés; utilisez des sacs isothermes pour conserver l’insuline; tenez votre sac bien organisé (avec les médicaments secs séparés des fournitures pour le diabète). Faites une liste de tout ce dont vous avez besoin (ordonnances, médicaments, fournitures) – donnez une copie de vos ordonnances à quelqu’un qui reste chez vous au cas où vous les perdriez. Notez les réglages de votre pompe et gardez-les avec vous. Notez le numéro de votre médecin pour les cas d’urgence et cherchez où se trouve l’hôpital local et comment vous y rendre si vous voyagez à l’étranger. Renseignez-vous sur votre destination : y a-t-il un réfrigérateur ? Où se trouve l’épicerie la plus proche ? Y a-t-il un médecin à proximité? Votre assurance vous couvre-t-elle au cas où vous devriez être hospitalisé(e) d’urgence ? Communiquez avec la compagnie aérienne avant de partir pour savoir si elle a des exigences de sécurité particulières et s’il est possible de choisir ses repas à bord des avions. Pour plus de renseignements, consultez le site www.tsa.gov doivent être effectués2. Le test des cétones dans le sang est plus précis et il devrait être recommandé à toutes les personnes qui utilisent une pompe à insuline, car elles sont à risque plus élevé d’évoluer plus rapidement vers l’acidocétose diabétique puisqu’elles n’ont pas de dépôts sous-cutanés d’insuline2. Un plan d’action devrait être établi pour la famille au cas où des cétones seraient détectées dans le sang ou dans les urines. Un plan d’action devrait également être établi pour les jours de maladie, où il est conseillé de surveiller plus fréquemment la glycémie. On ne devrait jamais interrompre les injections d’insuline en période de maladie, car cela accroîtrait le risque d’acidocétose diabétique. En cas de vomissements violents, une évaluation par du personnel médical peut être nécessaire pour éviter la déshydratation et la progression vers l’acidocétose diabétique2. Précautions particulières Adolescents Le soin des adolescents peut représenter un défi particulier dans la mesure où ils ont tendance à vouloir faire des S22 Québec Pharmacie vol. 57 n° 3 juin 2010 expériences et à ne pas respecter le traitement. Par conséquent, le soutien ou la supervision des parents sont extrêmement importants. Par ailleurs, les taux d’hormones fluctuants sont souvent associés à un besoin d’insuline accru, ce qui complique le maintien d’une bonne maîtrise de la glycémie durant cette période2. Il est important de parler de la consommation de tabac et d’alcool, de la contraception et de la grossesse aux adolescents, car tout cela peut avoir un impact important sur le traitement du diabète et sur l’incidence de complications futures. Les questions relatives à l’image de soi peuvent aussi poser un problème chez les adolescents et même chez les filles prépubères, et il n’est pas rare que des enfants de cet âge omettent de s’injecter leur insuline afin de perdre du poids. On doit réagir aussitôt devant un tel comportement, car il peut se traduire par le développement de l’acidocétose diabétique, une mauvaise maîtrise de la glycémie, la dépression et des troubles de l’alimentation. L’acquisition du permis de conduire peut aussi poser un problème à cette période, mais elle est possible à condition qu’il n’y ait pas d’antécédents d’inconscience de l’hypoglycémie. Le diabète en pédiatrie À ne pas faire Faire ses bagages à la dernière minute : vérifiez au moins huit semaines avant le départ auprès de votre équipe de soins diabétiques afin de vous assurer d’avoir vos lettres attestant la nécessité médicale (qui devraient préciser le type de maladie et les médicaments et fournitures nécessaires pour la traiter, vos ordonnances, les vaccins dont vous pourriez avoir besoin et les conseils pour ajuster les doses d’insuline en fonction du décalage horaire). Ne mettez pas vos médicaments ou vos fournitures dans vos bagages à enregistrer à cause des risques de retard ou de perte des bagages. Commander vos médicaments à la pharmacie à la dernière minute : il faut s’y prendre tôt pour être certain que les fournitures supplémentaires arriveront à temps. Le diabète à l’école Les parents d’enfants d’âge scolaire nouvellement diagnostiqués s’inquiètent souvent de la façon dont leurs enfants vont pouvoir gérer leur diabète dans le contexte de l’école. L’Association canadienne du diabète a publié des normes de soins à l’intention des enfants atteints du diabète de type 1 qui vont à l’école14. Bien que les règlements et les lois varient d’une province à l’autre, certains grands thèmes communs peuvent être abordés. Les parents sont incités à aller rencontrer les enseignants et la direction de l’école afin de s’assurer qu’un système d’éducation adéquat a été mis en place pour satisfaire aux besoins de leur enfant. S’ils ont besoin d’aide dans ce domaine, un éducateur en diabète peut être appelé pour assurer la liaison en présence de représentants de l’école et des parents. Les enseignants sont parfois en mesure d’apporter leur aide pour l’autosurveillance glycémique si une formation leur a été donnée et ils devraient pouvoir mettre www.professionsante.ca un endroit tranquille à la disposition de l’enfant pour qu’il fasse ses tests de glycémie. Il peut être bon de faire une présentation dans la classe de l’enfant afin que ses camarades aussi bien que ses professeurs soient au courant des signes et des symptômes de l’hypoglycémie et de l’hyperglycémie, et qu’ils soient en mesure de les reconnaître. L’enfant devrait porter un bracelet d’alerte médicale et disposer impérativement en tout temps d’une provision de tablettes de glucose et de collations en cas d’hypoglycémie14. Des études laissent penser qu’il y a place pour des améliorations en matière de soins du diabète dans le contexte scolaire; elles suggèrent aussi qu’il serait nécessaire qu’une infirmière scolaire supervise le soin des élèves diabétiques et que l’on mette l’accent sur la formation du personnel scolaire15. Mise à jour diabète 2010 Sortir les médicaments de leur emballage d’origine : laissez vos médicaments dans l’emballage portant l’étiquette de la pharmacie pour éviter tout problème avec la sécurité dans les aéroports. Supposer que vous trouverez facilement les aliments/collations que vous consommez habituellement : mieux vaut emporter/préparer votre propre nourriture pour de courts voyages; pour les voyages aériens, assurez-vous que les collations/les repas sont bien emballés au cas où il y aurait des retards; parlez de la planification détaillée de vos repas avec une diététicienne. Partir du principe que la maîtrise de la glycémie se passera comme chez vous : des activités différentes (p. ex., natation, randonnées), des repas différents, des changements d’horaires peuvent influer sur la glycémie. Il est essentiel de bien planifier ces aspects pour conserver une bonne maîtrise. Suite à la page S30 juin 2010 vol. 57 n° 3 Québec Pharmacie S23 Le diabète en pédiatrie Le diabète en camp de vacances et lors des voyages Il existe partout au Canada des camps de vacances pour enfants diabétiques qui constituent un excellent moyen pour les enfants de côtoyer d’autres jeunes qui ont les mêmes problèmes d’adaptation du mode de vie qu’eux. Il y a des camps de vacances pour différents âges (depuis les plus jeunes écoliers aux adolescents) avec des activités adaptées en fonction de l’âge. Les parents qui envoient leurs enfants dans des camps « approuvés par l’Association canadienne du diabète » peuvent être certains que des professionnels de la santé formés à l’administration de l’insuline, à l’autosurveillance glycémique et au traitement des complications figurent parmi le personnel, et que les enfants qui ne peuvent pas fournir leur propre insuline ou assurer leur autosurveillance glycémique recevront toute l’aide nécessaire. Il peut être problématique de voyager avec des enfants diabétiques, mais cela est possible avec une bonne planification. Il est recommandé de prendre contact avec l’équipe des soins diabétiques plusieurs semaines avant le départ, surtout quand on doit partir à l’étranger, afin de s’assurer de passer des vacances en toute sécurité et en étant bien préparé. Le tableau 6 donne quelques conseils pratiques et une liste de sites Internet. | Références 1. Canadian Diabetes Association/Association canadienne du diabète. Canadian Diabetes Association 2008 clinical practice guidelines for the prevention and management of diabetes in Canada. Can J Diabetes, 2008;32(Suppl 1):S1-S201. (En français : www.diabetes.ca/documents/ about-diabetes/CPG_FR.pdf) 2. International Society for Pediatric and Adolescent Diabetes (ISPAD) clinical practice consensus guidelines 2009 compendium. Pediatr Diabetes, 2009:10(Suppl 12):3– 32;71-99;134-45;185-94. 3. Ma RCW, Chan JCN. Incidence of childhood type 1 diabetes: a worrying trend. www.medscape.com/viewarticle/709733 (consulté le 6 octobre 2009). 4. Weigensberg MJ, Goran MI. Type 2 diabetes in children and adolescents. Lancet, 2009;373:1743-4. 5. Taplin CE, Barker JM. Natural evolution, prediction, and prevention of type 1 diabetes in youth. Endocr Res, 2008;33(12):17-33. 6. Ludvigsson J. Therapy with GAD in diabetes. Diabetes Metab Res Rev, 2009;25:307-15. 7. Neu A. Ketoacidosis at diabetes onset is still frequent in children and adolescents. A multicenter analysis of 14,664 patients from 106 institutions. Diabetes Care, 2009;32:1647-8. 8. Raman VS, Heptulla RA. New potential adjuncts to treatment of children with type 1 diabetes mellitus. Pediatr Res, 2009;65:370-4. 9. Miles HL, Acerini CL. Insulin analog preparations and their use in children and adolescents with type 1 diabetes mellitus. Paediatr Drugs, 2008;10(3):163-76. 10. Shalitin S, Phillip M. The use of insulin pump therapy in the pediatric age group. Horm Res, 2008;70(1):14-21. 11. Churchill JN, Ruppe RL, Smaldone A. Use of continuous insulin infusion pumps in young children with type 1 diabetes: a systematic review. J Pediatr Health Care, 2009;23:173-9. 12. Maahs DM, Wadwa RP, Bishop F et coll. Dyslipidemia in youth with diabetes: to treat or not to treat? J Pediatr, 2008;153:458-65. 13. Danne T, Lange K, Kordonouri O. Real-time glucose sensors in children and adolescents with type-1 diabetes. Horm Res, 2008;70:193-202. 14. Association canadienne du diabète. Normes de soins à l’intention des élèves atteints de diabète de type 1 à l’école; 2008;1-7. http://www.diabetes.ca/documents/get-involved/FINAL_Standards_of_Care_French_D2.pdf (consulté le 18 janvier 2010). 15. Tolbert R. Managing type 1 diabetes at school: an integrative review. J Sch Nurs, 2009;25(1):55-61. 16. World Health Organization. Definition, diagnosis and classification of diabetes mellitus and its complications. Part 1: Diagnosis and classification of diabetes mellitus. WHO/NCD/NCS/99.2. Geneva. Ref Type: Report. 1999. 17. Boerner H. Tips to trip by. Diabetes Forecast, 2008;61(5):42-5. 18. Lumber T, Strainic PA. Have insulin, will travel. Diabetes Forecast, 2005;58(8):50-4. S30 Québec Pharmacie vol. 57 n° 3 juin 2010 SantéPUBLIQUE La maladie de Lyme au Québec Encore peu connue au Québec, la maladie de Lyme est un problème de santé publique dans plusieurs régions des États-Unis. Les États les plus touchés sont nos voisins directs, soit ceux du nord-est du pays. Selon le CDC (Center for Disease Control and Prevention), plus de 35 000 cas auraient été rapportés aux États-Unis en 2008, soit deux fois plus qu’en 19981. Un phénomène d’autant plus inquiétant que cette maladie est largement sous-diagnostiquée : seulement 25 à 30 % des cas seraient rapportés aux autorités de la Santé publique2. Dans cet article, nous analyserons les facteurs expliquant la progression de cette maladie, puis nous verrons pourquoi elle est si difficile à diagnostiquer. Nous ferons le point sur sa présence au Québec et préciserons le rôle du pharmacien dans la lutte contre cette maladie. L’agent et le vecteur Mais saurons-nous les reconnaître ? En effet, la maladie de Lyme est également appelée « la grande imitatrice ». L’éventail de symptômes possibles est large et peu spécifique (fatigue, éruptions cutanées, douleurs articulaires, méningite et troubles cognitifs). De fait, elle est souvent confondue avec d’autres maladies, comme la sclérose en plaques, la fatigue chronique et l’arthrose4. Le symptôme le plus important à reconnaître par le pharmacien est la première étape de la maladie, appelée « stade précoce localisé »; ainsi il pourra orienter son patient vers le médecin. À cette étape, le patient présente un érythème migrant (EM) : plaque rouge de plus de 5 cm de diamètre (en moyenne 16 cm), évolutive, généralement en forme de cible, qui apparaît à l’endroit de la morsure 3 à 30 jours après la fin du Texte rédigé par Christophe Augé, Pharm. D., M.Sc., Ph.D. chimie thérapeutique (France), étudiant en actualisation, Université de Montréal. Texte original soumis le 22 février 2010. Texte final remis le 20 mars 2010. L’agent causal est une bactérie spirochète du Révision : Marie-France Beauchesne, Pharm. D., professeure agrégée de clinique, Faculté de genre Borrelia (Borrelia burgdoferi) transmise pharmacie, Université de Montréal. par la morsure des tiques du genre Ixodes. Dans l’est de l’Amérique du Nord, il s’agit de la tique Ixodes scapularis, communément appelée « tique du chevreuil » ou « tique à pattes noires », caractéristique qui la différencie d’autres espèces aux pattes plus claires. La tique n’est pas un insecte, mais un acarien, elle n’a donc pas trois paires de pattes mais quatre, ce qui la distingue des puces, des poux et des punaises. La présence de ce parasite hématophage, seul vecteur de cette maladie, est une condi- Figure 1 tion sine qua non pour déclarer une zone Cycle de vie des tiques de l’espèce Ixodes scapularis « endémique ». La progression de la maladie Printemps Été est donc directement liée à la dissémination de ce parasite. Œufs Comme toutes les tiques, Ixodes scapularis a un cycle de vie de deux ans et trois repas Larve (figure 1). Comme les deux premiers repas sanguins peuvent avoir lieu aussi bien sur des mammifères que sur des oiseaux, tout particulièrement les oiseaux migrateurs, la tique peut parcourir plusieurs centaines de kilomèNymphe tres au cours de ses repas, qui dureront trois à cinq jours. Lorsqu’elle se détache, si elle se trouve dans un milieu propice à la suite de son cycle, elle pourra se développer, se reproduire et, à terme, créer une nouvelle zone endémique. Toutefois, les grands froids ne sont pas les Hiver Automne conditions idéales de leur développement. C’est pour cette raison que, jusqu’à récemment, les autorités sanitaires pensaient le Québec indemne de tout risque. Une étude effectuée à l’Université de MonAdulte tréal, basée sur les changements climatiques, prévoit, d’ici 10 à 30 ans, une dissémination d’Ixodes scapularis, avec un risque dit « modéré » sur l’ensemble du territoire (excepté le Grand Nord du Québec) et un risque élevé dans les Nymphe régions du sud, notamment la Montérégie3. Œufs La maladie Les cas de maladie de Lyme pourraient donc devenir plus fréquents d’ici quelques années. www.professionsante.ca juin 2010 vol. 57 n° 3 Québec Pharmacie 41 SantéPUBLIQUE repas et peut durer de quelques jours à huit semaines. Cet érythème est présent dans 68 à 80 % des cas. Il est à noter que seul 20 % des patients se souviennent d’avoir été mordus4. En effet, la tique mesure 0,3 à 5 mm et la morsure est indolore. Si la maladie n’est pas traitée à cette étape, elle va poursuivre son évolution vers les stades précoce disséminé (rashs multiples, atteintes articulaires, méningite, paralysie faciale, troubles cardiaques…) et tardif disséminé (troubles cognitifs, arthrite récidivante…). Diagnostic Le diagnostic est principalement clinique : la présence de symptômes associés à une exposition potentielle à des tiques en région endémique peut justifier une sérologie4. Le sérodiagnostic de la maladie de Lyme se fait par la combinaison de deux tests : un test immunologique ELISA effectué au Laboratoire de santé publique du Québec (LSPQ) et, en cas de positivité, un test Western Blot au Laboratoire national de microbiologie de Winnipeg. La sérologie est utile pour confirmer le diagnostic, mais le nombre élevé de faux positifs (dus à d’autres infections à spirochètes ou virales, ou encore à des maladies auto-immunes) et de faux négatifs (faibles concentrations d’anticorps : seuls 20 % des patients présentant un érythème migrant auront une sérologie positive) limite son utilisation diagnostique. Cela implique qu’en région non endémique, la majorité des résultats positifs sont réputés faussement positifs, à moins que le tableau clinique ne soit très évocateur de la maladie de Lyme. D’où l’importance d’un suivi étroit de la carte d’endémicité. Traitement L’algorithme de traitement est résumé dans le tableau I. Le choix du traitement est fonction du stade de la maladie. Le stade 1 ainsi que les stades 2 dits « légers » seront traités par des agents oraux. Les stades 2 compliqués (avec atteinte neurologique) et les stades 3 nécessitent des agents parentéraux. On peut trouver plus de détails sur les choix de traitements dans les travaux de Wormser5. L’efficacité du traitement serait de l’ordre de 95 à 100 % au stade précoce localisé, mais elle diminuerait avec l’évolution Tableau I Traitements recommandés pour la maladie de Lyme à ses différents stades4,5. Stade 1Érythème migransAdultes : Doxycycline 100 mg per os b.i.d. 14-21 jours Stade 2Érythème migransAmoxicilline 500 mg per os t.i.d. 14-21 jours multipleCéfuroxime axetil 500 mg per os b.i.d 14-21 jours Paralysie faciale Enfants > 8 ans : Arthrite sans atteinte Doxycycline 2 mg/kg b.i.d 14-21 j (max 100 mg b.i.d) neurologique Bloc cardiaqueEnfants < 8 ans : de premier degréAmoxicilline 40 à 50 mg/kg/jour en 3 doses 14-21 j (max 500 mg t.i.d.) Céfuroxime axetil 15 mg/kg b.i.d. 14-21 j (max 500 mg b.i.d.) Neuro-borréliose Adultes : Ceftriaxone 2 g IV q24 h 10-28 jours Arthrite avec atteinteCéfotaxime 2 g IV q8 h 10-28 jours neurologiquePénicilline G 3 à 4 millions UI q4 h 10-28 jours Doxycycline 100 à 200 mg per os b.i.d Bloc cardiaque (si allergie aux ß-lactames) 10-28 jours de deuxième et troisième degrés Enfants : Stade 3Arthrite récurrenteCeftriaxone 50 à 75 mg/kg IV q24 h (max 2 g) 10-28 jours Céfotaxime 50 à 66 mg/kg IV q8 h 10-28 jours Atteinte neurologiquePénicilline G 33 000 to 66 000 UI/kg q4 h 10-28 jours tardive Doxycycline 2 à 4 mg/kg b.i.d. (si allergie aux ß-lactames) 10-28 jours (uniquement chez les enfants > 8 ans) 42 Québec Pharmacie vol. 57 n° 3 juin 2010 vers le stade tardif 4. Il est à noter que, lors du traitement, 15 % à 30 % des patients présenteront une réaction de Jarisch-Herxheimer. Cette réaction se traduit par une aggravation des symptômes (fièvre, céphalées et exacerbation de l’atteinte cutanée) durant les 24 premières heures du traitement, due à la libération des antigènes lors de l’élimination des bactéries. Le vecteur est-il présent au Québec ? Au Canada, le nombre de sites où la tique I. scapularis est réputée établie est passé de 1 en 1993 à 13 en 20086. Ces sites se trouvent en Ontario, en Nouvelle-Écosse et au Manitoba. Il est à noter que la confirmation de l’établissement d’une population de tiques exige l’identification des trois stades de la tique (larve, nymphe et adulte) sur deux années consécutives, dans un lieu donné. De plus, pour qu’un site soit considéré comme endémique, on doit retrouver la bactérie à la fois chez le vecteur et le réservoir. En ce qui concerne le Québec, la polémique sur la présence ou non du vecteur et de la maladie fait rage depuis plusieurs années. Une surveillance passive basée sur l’envoi de tiques au LSPQ, principalement par les vétérinaires, a permis de constater une augmentation constante du nombre de tiques de l’espèce en question. De 1990 à 2006, environ 11 % des tiques recueillies de cette espèce étaient positives pour B. burgorferi. Pour faire le point, l’Institut national de santé publique du Québec (INSPQ) a lancé en 2007 une étude épidémiologique sur les zoonoses transmises par les tiques dans le sud-ouest du Québec6. Lors de cette étude, les tiques ont été récoltées et analysées de juin à octobre sur 46 sites différents, surtout en Montérégie et en Estrie. Des prélèvements sérologiques ont également été faits sur les hôtes potentiels (principalement des souris et des cerfs de Virginie) pour vérifier leur exposition à la bactérie. Parmi les 717 tiques récoltées, 353 appartenaient à l’espèce I. scapularis (99 larves, 49 nymphes, 78 femelles et 127 mâles adultes). Par ailleurs, 3 nymphes, 11 adultes et 3 souris étaient positives à B. bugdorferi. La deuxième partie de l’étude (2008) n’a pas été publiée à ce jour, toutefois, dans son feuillet d’information sur la maladie de Lyme paru en janvier 20107, l’INSPQ nous informe que celle-ci a confirmé que la tique survit et se reproduit dans quelques sites situés en Montérégie, à proximité des rivières Richelieu et Yamaska et le long du fleuve Saint-Laurent. Peut-on être infecté au Québec ? La maladie de Lyme est à déclaration obligatoire (MADO) au Québec depuis novembre 2003. Mais malgré la polémique, jusqu’à récemment, aucun cas n’était reconnu acquis au Québec. Les quelques cas avérés chaque année étaient tous réputés avoir été acquis à l’étranger. De fait, La maladie de Lyme au Québec notre province était déclarée indemne de cette maladie et l’absence de voyage en zone endémique était un critère d’exclusion du diagnostic. Cela n’est plus le cas. Dans le bulletin du réseau d’alerte et d’information zoosanitaire du ministère de l’Agriculture, des Pêcheries et de l’Alimentation du Québec (MAPAQ) de décembre 2009, on apprend que le premier cas reconnu acquis au Québec a été diagnostiqué en septembre 2008, chez un résidant du Centre-du-Québec. On nous y informe également que, depuis 2008, quelques cas ont été diagnostiqués chez des personnes n’ayant pas voyagé à l’extérieur de la province8. Si le risque de contracter la maladie de Lyme demeure très faible, il pourrait augmenter dans les prochaines années. C’est dès maintenant qu’il importe d’informer la population et de promouvoir les mesures préventives pour éviter les morsures de tiques. En tant que professionnel de la santé de première ligne, le pharmacien se doit de jouer un rôle dans cette lutte. Rôle du pharmacien : informations et mesures de prévention Les tiques vivent généralement dans les régions boisées ou les hautes herbes. Afin de prendre chacun de ses repas, la tique monte en haut d’une tige ou d’un brin d’herbe et tente d’accrocher les hôtes potentiels qui passent à sa portée. Le premier conseil est donc de porter des vête- ments longs et clairs, ainsi que des souliers fermés lors des promenades en forêt et de rester sur les sentiers en évitant les hautes herbes. L’utilisation d’un insectifuge contenant du DEET (N,N-diéthyl-3-méthylbenzamide) a démontré son efficacité9. Il est assez délicat de convertir les μmoles/cm2 utilisées dans les études cliniques en pourcentage de concentration et en nombre d’applications journalières nécessaires à une protection optimale. Toutefois, il semble qu’il n’y ait pas avantage à utiliser des produits ayant une concentration supérieure à 30 %4. Après les promenades, il faut examiner minutieusement son corps, ainsi que celui des enfants et des animaux de compagnie afin de déceler la présence de tiques. Le repérage précoce est très important puisque la transmission de la maladie du vecteur vers l’hôte ne se fait qu’après 24 à 36 heures. En effet, la bactérie vit à l’intérieur des intestins du vecteur, soit la tique, et pour être transmise, elle doit remonter vers l’appareil buccal. Un retrait précoce de la tique diminue donc grandement le risque d’infection. Toute manipulation nécessite le lavage des mains. Pour prélever une tique, on doit utiliser une pince à cils placée contre la peau, sur les parties dures de la tique. La pince doit être serrée sur la tête de la tique, puis délicatement mais fermement tirée afin d’extraire les pièces buccales de la peau. Il est important de ne pas laisser une partie de la tique dans la plaie, qui pourrait alors s’infecter. Il faut également veiller à ne pas presser les parties molles de la tique, car cela provoquerait une régurgitation qui augmenterait les risques de transmission. La désinfection du site de la morsure complète l’extraction. Pour l’identification, il est conseillé de placer la tique, si possible intacte, dans un contenant hermétique et de l’emmener chez un médecin ou un vétérinaire. Pour plus d’informations et pour imprimer le formulaire devant accompagner le spécimen, consultez la référence 4. Étant donné la faible incidence de la maladie au Québec, toutes les morsures de tiques ne nécessitent pas une prophylaxie. Toutefois, si des symptômes de la maladie se manifestent ou si une rougeur apparaît à l’endroit de la morsure, le patient devra être dirigé rapidement vers un médecin. Il faut préciser que la maladie de Lyme n’est pas la seule maladie transmise par la morsure de tiques. D’autres pathologies, comme les rickettsioses (Rickettsia rickettsii responsable de la fièvre pourprée des montagnes rocheuses, ou Rocky Mountain spotted fever), les ehrlichioses (Anaplasma phagocytophilum), la tularémie (Francisella tularensis) et bien d’autres infections notamment virales (Arbovirus, Coltivirus), peuvent être véhiculées par des tiques de toutes espèces. Il revient donc au pharmacien d’ouvrir l’œil au retour du beau temps. n gie, manifestations cliniques, diagnostic, traitement et prévention à l’intention des professionnels de la santé. Agence de la santé et des services sociaux de l’Estrie. Septembre 2009. [En ligne. Page consultée le 11 mars 2010.] www.santeestrie.qc.ca/sante_publi que/protection_maladies_infectieuses/documents/ MaladiedeLyme_sept09.pdf 5. Wormser GP, et coll. The Clinical Assessment, Treatment, and Prevention of Lyme Disease, Human Granulocytic Anaplasmosis, and Babesiosis : Clinical Practice Guidelines by the Infectious Diseases Society of America. Clin Infect Dis 2006 : 43(9); 1089-134. 6. Nguon S, Milord F, Ogden N, Trudel L, Lindsay R, Bouchard C. Étude épidémiologique sur les zoonoses transmises par les tiques dans le sud-ouest du Québec – Premier volet : année 2007. [En ligne. Page consultée le 11 mars 2010.] www.inspq.qc.ca/pdf/ publications/865_ EtudeEpiZoonoses.pdf 7. Trudel L, Serhir B. La maladie de Lyme. [En ligne. Page consultée le 11 mars 2010.] www.inspq.qc.ca/ pdf/publications/ 1042_Lyme2009.pdf 8. Vincent C, Pépin M. La maladie de Lyme. Raizo, bulletin zoosanitaire 2009 : 67; 1-7. [En ligne. Page consultée le 11 mars 2010.] www.mapaq.gouv.qc.ca/NR/ rdonlyres/138B8C0A- 073D -409E -ADE0 7D60BEA54F89/0/Bulletinlymedecembre09.pdf 9. Carroll JF, Klun JA, Debboun M. Repellency of deet and SS220 applied to skin involves olfactory sensing by two species of ticks. Med Vet Entomol 2005 : 19; 101–6. Références 1. Centers for Disease Control and Prevention. Division of Vector Borne Infectious Diseases, Lyme Disease Statistics. [En ligne. Page consultée le 11 mars 2010.] www.cdc.gov/ncidod/dvbid/lyme/ld_statistics.htm 2. Naleway AL, Belongia EA, Kazmierczak JJ, Greenlee RT, Davis JP. Lyme Disease Incidence in Wisconsin : A Comparison of State-reported Rates and Rates from a Population-based Cohort. Am J Epidemiol 2002 : 155; 1120-7. 3. Ogden, NH. et coll. Risk maps for range expansion of the Lyme disease vector, Ixodes scapularis, in Canada now and with climate change. International Journal of Health Geographics, 2008 : 7; 24-39. 4. Drapeau M. Agence de la santé et des services sociaux de l’Estrie. La maladie de Lyme. Épidémiolo- Questions de formation continue 12) Lequel de ces énoncés est faux ? A. Ixodes scapularis prend trois repas sanguins au cours de son cycle. B. Ixodes scapularis est présente dans certaines régions du Québec. C. Dans la majorité des cas, un diagnostic d’érythème migrant est signe d’une sérologie positive. D. Le DEET 30 % est un moyen de protection efficace. E. Au moins un cas de maladie de Lyme a été acquis au Québec. 13) Lequel de ces énoncés est vrai ? A. La prophylaxie consécutive à une morsure de tique doit être administrée automatiquement. B. La sérologie est une méthode diagnostique fiable. C. L’efficacité du traitement varie en fonction du stade de la maladie. D. L’érythème migrans apparaît toujours 3 à 30 jours après la morsure. E. La doxycycline est toujours le premier choix de traitement. Veuillez reporter vos réponses dans le formulaire de la page 78 www.professionsante.ca juin 2010 vol. 57 n° 3 Québec Pharmacie 43 Pharmacovigilance Mise à niveau en pharmacovigilance L’Organisation mondiale de la santé (OMS) a adopté, à sa vingtième assemblée, il y a environ 40 ans, une résolution sur la création d’un système international de surveillance des effets indésirables (EI) des médicaments. Le Canada s’est joint à cette initiative en 1968. Depuis, plus de 90 pays participent à ce réseau international de surveillance1. Texte rédigé par Jean-François Bussières, B. Pharm., M.Sc., M.B.A., F.C.S.H.P., chef du département de pharmacie et de l’unité de recherche en pratique pharmaceutique, CHU Sainte-Justine, et professeur titulaire de clinique, Faculté de pharmacie, Université de Montréal, Denis Lebel, B. Pharm., M.Sc., F.C.S.H.P., et Aurélie Closon, assistante de recherche, unité de recherche en pratique pharmaceutique, CHU Sainte-Justine. Texte original soumis le 15 décembre 2009. Texte final remis le 17 janvier 2010. Révision : Christine Hamel, B. Pharm., M.Sc. L’OMS définit la pharmacovigilance comme la « science qui s’intéresse à la détection, à l’évaluation et à la prévention des EI des médicaments. La pharmacovigilance a pour objectifs la détection précoce des interactions et des EI nouveaux, la détection des augmentations de la fréquence des effets indésirables connus, l’identification des facteurs de risque et des mécanismes pouvant expliquer les EI, l’évaluation du rapport bénéfice/risque et la diffusion de l’information nécessaire à l’amélioration de la prescription et de la réglementation du médicament »2. L’OMS propose quatre catégories pour décrire la fréquence d’un EI, soit très commun (> 10 %), commun (> 1 % et < 10 %), peu commun (> 0,1 % et < 1 %), rare (> 0,01 % et < 0,1 %) et très rare (< 0,01 %)3. L’objectif de cet article est de présenter une mise à jour de certains éléments relatifs à la pharmacovigilance pour le pharmacien en pratique communautaire et hospitalière. Cette mise à jour présente le programme Canada Vigilance et les nouveautés en matière de déclaration et de consultation des données, l’évolution de la pratique pharmaceutique en ce qui concerne la pharmacovigilance, l’émergence de la pharmacogénomique et la mise à jour de nos livres et signets utiles. Canada Vigilance Figure 1 Profil de la base de données de Canada Vigilance4 Accueil › Médicaments et produits de santé › MedEffet Canada › Base de données des effets indésirables Médicaments et produits de santé Recherche dans la base de données en ligne des effets indésirables de Canada Vigilance 1. Critères de recherche de déclaration Canada Vigilance 44 Québec Pharmacie vol. 57 n° 3 juin 2010 Santé Canada définit le Programme Canada Vigilance comme un « programme de surveillance après la mise en marché de Santé Canada qui recueille et évalue les déclarations d’effets indésirables présumés associés aux produits commercialisés au Canada ». Les données sont principalement recueillies à l’aide d’un système de surveillance spontané. Santé Canada précise qu’on ne devrait pas dresser de comparaisons numériques entre les effets indésirables associés à différents produits de santé à partir des données des listes sommaires. Les produits de santé commercialisés visés par ce programme incluent les médicaments sur ordonnance ou en vente libre, les produits biologiques, y compris les produits de fractionnement du sang, ainsi que les vaccins thérapeutiques et diagnostiques, les produits de santé naturels et les produits radiopharmaceutiques. Ce programme recueille des déclarations d’effets indésirables présumés depuis 1965. Les déclarations d’effets indésirables sont transmises à Santé Canada par les professionnels de la santé et les patients sur une base volontaire ou par l’inter- médiaire des fabricants (détenteurs d’une autorisation de mise en marché) à partir du formulaire papier (SC/HC 4016) ou en ligne21. Le programme Canada Vigilance est alimenté par sept bureaux régionaux, dont le bureau de Canada Vigilance, qui offrent un point de service aux professionnels et aux consommateurs. Les bureaux régionaux recueillent les déclarations et les transmettent ensuite au bureau national de Canada Vigilance pour une analyse plus approfondie. La production d’une déclaration peut maintenant se faire en ligne, par téléphone ou en soumettant le formulaire de déclaration de Canada Vigilance par télécopieur ou par la poste4. Santé Canada définit un effet indésirable (EI) comme « une réaction nocive et non intentionnelle à un produit de santé commercialisé ». Un EI est réputé grave « s’il nécessite ou prolonge l’hospitalisation, entraîne une malformation congénitale ou une invalidité ou incapacité persistante ou importante, met la vie en danger ou entraîne la mort ». Santé Canada précise qu’un EI, comparativement à un événement indésirable, se caractérise par le soupçon d’un lien causal entre le médicament et la manifestation. Ainsi « un événement indésirable, tel que le définit la ligne directrice E2D de l’International Conference on Harmonization, signifie toute manifestation médicale importune se manifestant chez un patient qui a reçu un produit médicinal et ne devant pas nécessairement présenter une relation de cause à effet avec le traitement en cours. Un événement indésirable peut donc correspondre à tout signe défavorable et non intentionnel (par exemple, un résultat de laboratoire anormal), symptôme ou maladie temporellement associés à l’usage d’un produit médicinal, qu’il soit ou non considéré comme relié à ce produit ». En 2008, Santé Canada a reçu 20 360 déclarations d’EI provenant du Canada, dont 69 % ont été considérées comme graves5. En comparaison, les détenteurs d’autorisation de mise en marché ont reçu de l’étranger, pour la même période, 241 417 déclarations. Ces déclarations de l’étranger ne font pas partie de la banque de données canadienne. Les produits pharmaceutiques représentent plus de 71 % des cas d’EI déclarés, suivis des produits de biotechnologies (20 %), des produits biologiques (5 %), des radio-pharmaceutiques (moins de 2 %) et Mise à niveau en pharmacovigilance des produits de santé naturels (moins de 2 %). Les déclarations viennent des détenteurs de l’autorisation de mise en marché (72 %), des patients et des professionnels de la santé hors hôpital (23 %), des hôpitaux (5 %) et autres (moins de 1 %). Les déclarants sont patients ou consommateurs (30 %), médecins (25 %), pharmaciens (18 %), professionnels de la santé (15 %), infirmières (9 %) ou autres (3 %). Santé Canada rapporte une augmentation de 16 % des déclarations de 2007 à 2008. Bien que le système de pharmacovigilance canadien soit volontaire, les détenteurs d’une autorisation de mise en marché (DAMM) sont tenus de soumettre les déclarations d’EI reçues conformément aux exigences de la Loi sur les aliments et drogues et son règlement d’application. Les DAMM sont tenus de faire parvenir au Programme Canada Vigilance, dans un délai de 15 jours, toutes les déclarations d’EI graves survenus au Canada et toutes les déclarations d’EI graves et imprévus survenus à l’étranger. Santé Canada a publié à l’été 2009 un nouveau document d’orientation à l’intention de l’industrie concernant la déclaration des effets indésirables des produits de santé commercialisés6. Chaque détenteur doit soumettre tous les 12 mois un rapport synthèse de pharmacovigilance pour ses produits. Ce rapport peut être utilisé pour soutenir les demandes de modifications apportées à la monographie d’un produit de santé. Le tableau I présente un profil comparé des données à recueillir selon Santé Canada, dans le cadre des lignes directrices émises à l’inten- tion de l’industrie et selon Kelly et coll7. L’article de Kelly et coll. hiérarchise l’importance des données à recueillir (p. ex., essentiel, nécessaire, souhaitable) dans la perspective de publier un cas de pharmacovigilance. Ce tableau met en évidence les points communs et les différences, et peut guider la collecte de données du pharmacien avant de procéder à la revue documentaire et à la déclaration ou à la publication d’un cas. Pour les produits de santé naturels, il est suggéré d’inscrire le binôme latin, la référence de l’auteur, la famille, le type d’extrait (p. ex., aqueux ou alcoolique, incluant le pourcentage de solvant), les parties de la plante utilisées (pour les produits à base d’herbes médicinales), les ingrédients et la quantité utilisée de chacun d’eux (pour les produits mixtes – l’ingrédient suspect) ainsi que le taux de dilution homéopathique (pour les produits homéopathiques). Enfin, en vertu des lignes directrices émises à l’intention de l’industrie, Santé Canada requiert des données sur le déclarant, notamment la source de la déclaration (p. ex., essai clinique, ouvrage littéraire, déclaration spontanée, autorité de réglementation), la date à laquelle la déclaration d’événements a été reçue pour la première fois par le détenteur d’une autorisation de mise en marché, le pays dans lequel l’effet s’est produit, le type (initial ou subséquent) et l’ordre (premier, deuxième, etc.) des renseignements relatifs aux cas signalés à Santé Canada, le nom et l’adresse du détenteur d’une autorisation de mise en marché, les noms et adresses postale et électronique, les numéros de téléphone et de télécopieur d’une personne-ressource chez le détenteur d’une autorisation de mise en marché et, enfin, le numéro d’identification du détenteur d’une autorisation de mise en marché pour le cas en cause (le numéro doit être le même pour la déclaration initiale et pour toute déclaration subséquente pour un même cas). Santé Canada a mis en ligne le 13 novembre 2009 une version améliorée de sa base de données des effets indésirables (figure 1 - disponible en ligne). Cette nouvelle version a permis de simplifier la mise en pages des critères de recherche, d’ajouter une fonction de recherche par nom de commerce ou par ingrédient actif d’un produit de santé ainsi que par terme(s) ou groupe(s) de termes décrivant un effet indésirable signalé, de présenter des renseignements supplémentaires permettant d’obtenir de l’aide et un contexte, et d’intégrer une fonction d’impression/ d’enregistrement/ d’exportation des résultats de recherche en format de fichier Adobe PDF ou Microsoft Excel. Santé Canada indique que la banque de données sera mise à jour sur une base trimestrielle. Cet organisme rappelle également aux usagers que « bien que la base de données permette effectivement aux consommateurs de voir le genre d’effets indésirables qui ont été signalés par des individus utilisant un produit en particulier, l’information présentée est le reflet de l’opinion des personnes qui produisent les rapports. La base de données ne fournit pas de renseignements Figure 2 Déterminants de la déclaration d’effets indésirables aux médicaments Système expert Paradoxe des idéaux Paradoxe de l’éloignement Méfiance envers Santé Canada Défiance envers l’industrie La pharmacovigilance Importance du principeComparaison avec mais non application d’autres systèmes experts dans la pratique Rétroactions inadéquates Déclaration Gravité principe commun mais application différente Pharmacovigilance en second plan Cercle vicieux de l’incertitude du lien EI et M Interdépendance des rôles de chacun Le risque qui désensibilise Paradoxe de la perception Paradoxe de l’implication L’individu www.professionsante.ca juin 2010 vol. 57 n° 3 Québec Pharmacie 45 Pharmacovigilance concluants sur l’innocuité des produits de santé et ne peut remplacer les consultations médicales ». De plus, il précise « qu’on ne peut que soupçonner la plupart des effets indésirables (EI) des produits de santé à l’égard desquels on ne peut établir de lien prouvé de cause à effet. Les notifications spontanées d’EI ne peuvent servir pour déterminer l’incidence des EI, étant donné que les EI ne sont pas suffisamment signalés et que l’étendue d’exposition des patients est inconnue ». Enfin, Santé Canada précise que « la base de données est régulièrement vérifiée pour des déclarations en double ». Bien que la base de données soit davantage utile aux fins de recherche et de surveillance pour l’identification de signaux, elle peut être utile dans le domaine clinique, notamment pour vérifier si un médicament donné comporte des déclarations quant à un effet indésirable particulier. Il est à noter que la recherche par ingrédient actif (dénomination commune ou nom générique) doit se faire en utilisant l’épellation anglaise. Par exemple, la recherche de toutes les déclarations pour la phénytoïne depuis 1965 jusqu’à ce jour donne plus de 1170 déclarations de différents EI. Rappelons ici que Santé Canada étudie depuis quelques années le modèle d’homologation progressive qui repose sur une meilleure gestion des risques et une surveillance continue de l’innocuité, de la qualité et de l’efficacité. 46 Québec Pharmacie vol. 57 n° 3 juin 2010 Bibliothèque idéale Avec la refonte du doctorat professionnel en pharmacie et l’évolution des différents programmes de formation, la pharmacovigilance est enseignée à la faculté de pharmacie de l’Université de Montréal au premier cycle (par exemple dans plusieurs cours systèmes intégrant la pharmacothérapie et la surveillance de la thérapie médicamenteuse, PHA-3210 – Le pharmacien et la communauté) et au deuxième cycle, dans le cadre du D.E.S.S. en développement du médicament (p. ex., PHL-6092 – Pharmacovigilance). Le tableau II (page 48) présente une sélection d’ouvrages et de liens utiles à la pharmaco vigilance. Pratique pharmaceutique Dans le cadre de l’Enquête canadienne sur la pharmacie hospitalière 2007-2008, les répondants ont rapporté un score moyen de 2,3 pour le monitorage d’effets indésirables au dixième rang sur 22 activités pharmaceutiques cliniques pouvant être cotées. Une note de 1 est attribuée pour un service systématique à tous les patients qui en ont besoin, une note de 2 est attribuée à un service ciblant ceux qui en ont le plus besoin, une note de 3 est attribuée à un service limité dans le temps et pour la disponibilité des ressources, tandis qu’une note de 4 est attribuée à un service qui n’est pas assuré/offert8. Bien que la pré- vention et la détection des effets indésirables fassent partie intégrante des soins pharmaceutiques, la déclaration à une autorité réglementaire ou à un fabricant, ou la publication d’un cas rapporté est beaucoup plus limitée. À titre d’exemple, les pharmaciens du CHU Sainte-Justine ont effectué un total de 36 449 interventions cliniques dont 5,5 % ont porté sur la pharmacovigilance (prévention, prise en charge), soit 60 % en oncologie, 27 % aux soins intensifs pédiatriques, 7 % en pédiatrie, 2 % en obstétrique-gynécologie, et 4 % détectés dans le cadre de l’administration des médicaments au cours de l’exercice financier 2008-2009. Le département est doté d’un service de pharmacovigilance soutenu par la présence d’un assistant de recherche en soutien aux cliniciens pour la documentation et la déclaration. Le service comprend la tournée quasi quotidienne des unités de soins afin d’encourager la déclaration spontanée d’effets indésirables survenus au cours des dernières 24 heures, la recherche documentaire en soutien aux cliniciens, la déclaration en ligne à Santé Canada, la rédaction de cas aux fins de publication et la participation à des activités de recherche. Parmi les 1996 interventions pharmaceutiques liées à la pharmacovigilance et documentées dans le journal de bord des pharmaciens, seuls 20 effets indésirables ont fait l’objet d’une déclaration à Santé Canada par l’assistant de recherche et seuls quelques- Mise à niveau en pharmacovigilance uns ont fait l’objet d’une soumission9 ou d’une publication 10-14 au cours des deux dernières années. Dans le cadre d’un projet de recherche sur la pharmacovigilance de notre équipe, nous avons étudié les déterminants de la nondéclaration d’un effet indésirable par les cliniciens15. La figure 2 présente un diagramme d’Ishikawa modélisant les quatre principaux obstacles à la déclaration d’un effet indésirable et les éléments explicatifs. Nul doute que le pharmacien est le spécialiste du médicament et qu’il doit participer plus activement à la documentation des effets indésirables des médicaments, compte tenu de leur impact sur la morbidité et la mortalité16. Par exemple, Ackroyd-Stolarz et coll. ont publié récemment une revue documentaire des coûts associés aux effets indésirables des médicaments chez les patients âgés de plus de 65 ans, au Canada17. Les auteurs concluent que la survenue d’un effet indésirable fait passer en moyenne la durée d’hospitalisation en Nouvelle-Écosse de 9,8 à 20,2 jours, pour un coût moyen additionnel de 7500 $ par patient. Les scores obtenus par l’utilisation d’algorithmes comme ceux de Naranjo et coll. ne devraient jamais être utilisés pour prendre une décision clinique en ce qui concerne un patient ou pour orienter la décision de rapporter un cas ou non. Toutefois, ils peuvent www.professionsante.ca être des outils utiles en recherche. Il existe d’autres algorithmes, notamment celui de l’OMS, le Karch & Lasagna Scale, le Kramer’s Scale et le European ABO System18. Pharmacogénomique La pharmacogénomique est l’identification et l’étude des gènes et des produits correspondants qui influent sur les variations individuelles de l’efficacité et/ou de la toxicité des produits thérapeutiques et de l’application des données de génomique visant à donner une assise informationnelle en vue de la mise au point et/ou de l’application clinique des produits thérapeutiques. Le génome humain comporte plus de 3 milliards de bases dont 99,9 % sont identiques d’un individu à l’autre. Toutefois, il existe des polymorphismes (plus de 3 millions de nucléotides) qui expliquent les différences entre les individus. Certains polymorphismes peuvent expliquer la variabilité de la réponse à une dose de médicament. Le département de pharmacie du CHU Sainte-Justine participe depuis 2006 à un réseau canadien de pharmacovigilance pédiatrique. Financé par Génome Canada et Génome-UBC, le projet Genotypic Approaches to Therapy in Childhood (GATC) a mené à la création d’un réseau (CPNDS – Canadian Pharmacogenomics Network for Drug Safety)19. Ce réseau propose un projet de recherche soumis localement aux comités d’éthique de chaque établissement participant. Dans le cadre du service de pharmacovigilance du CHU Sainte-Justine, l’équipe de cliniciens (pharmaciens, médecins, infirmières) identifie des patients consommateurs de médicaments cibles présentant ou non un effet indésirable. En collaboration avec le pharmacien de l’équipe clinique, l’assistant de recherche recrute les patients (généralement par l’entremise des parents), et l’infirmière prélève un échantillon de salive permettant le séquençage de l’ADN. À partir des données recueillies et des effets indésirables identifiés, l’équipe de recherche cherche à établir des liens d’association entre la présence de polymorphismes et certains effets indésirables20. À titre d’exemple, l’équipe de UBC a établi un lien d’association entre des polymorphismes (TMPT-rs12201199 et COMT-rs9332377) et la survenue d’ototoxicité avec la cisplatine. Conclusion Cet article présente une mise à jour des éléments clés relatifs à la pharmacovigilance à l’intention du pharmacien en pratique communautaire et hospitalière. n Références et questions de formation continue aux pages 48 et 49 juin 2010 vol. 57 n° 3 Québec Pharmacie 47 Pharmacovigilance Références 1. Upsala Monitoring Centre (2009, octobre). « WHO Programme for International Drug Monitoring ». Organisation mondiale de la santé. [En ligne, site consulté le 27 novembre 2009.] Adresse URL : www.who-umc. org/DynPage.aspx?id=13140&mn=1514#4 2. Upsala Monitoring Centre (2000, décembre). « Surveillance de la sécurité d’emploi des médicaments guide pour la création et le fonctionnement d’un centre de pharmacovigilance ». [En ligne, site visité le 26 novembre 2009.] Adresse URL : www.who-umc.org/ graphics/7125.pdf 3. Upsala Monitoring Centre (1995, décembre). « Frequency of adverse drug reactions ». Organisation mondiale de la santé. [En ligne, site visité le 27 novembre 2009.] Adresse URL : www.who-umc.org/Dynpage. aspx?id=22684 4. MedEffet Canada (2009, novembre). « Programme Canada Vigilance ». Santé Canada. [En ligne, site visité le 24 novembre 2009.] Adresse URL : www.hc-sc.gc. ca/dhp-mps/medeff/vigilance-fra.php 5. MedEffet Canada (2008, décembre). « Déclaration d’effets indésirables et d’incidents 2008 ». Santé Canada. [En ligne, site visité 10 décembre 2009.] Adresse URL : www.hc-sc.gc.ca/dhp-mps/medeff/ bulletin/carn-bcei_v19n2-fra.php#tab2 6. Santé Canada (2009, août). « Document d’orientation à l’intention de l’industrie - Déclaration des effets indésirables des produits de santé commercialisés ». [En ligne, site visité le 23 novembre 2009.] Adresse URL : www.hc-sc.gc.ca/ahc-asc/branch-dirgen/hpfbdgpsa/mhpd-dpsc/guidance-directrice_reportingnotification-fra.php 7. Kelly WN, Arellano FM, Barnes J et coll. Guidelines for submitting adverse event reports for publication. Drug Saf 2007; 30(5):367-73. 8. Hall K, Bussières JF, Harding J, et coll (2009, janvier). « Rapport canadien sur la pharmacie hospitalière 2007-2008 ». [En ligne, site visité le 27 novembre 2009.] Adresse URL : www.lillyhospitalsurvey.ca 9. Skalli S, Barret P, Villier C, et coll. CarbamazepineInduced Acute Generalized Exanthematic Pustulosis (soumis pour publication). 10. Vandelecaere M, Barret P, Bussières JF. Thrombocytopénie avec pipéracilline. Québec Pharmacie 2009; 56(4):22-6. 11. Winterfeld U, Barret P, Bussières JF. Néphropathie interstitielle aiguë médicamenteuse. Québec Pharmacie 2009; 56(2):31-4. 12. Coureau B, Bussières JF, Tremblay S. Cushing syndrome induced by misuse of moderate to high-potency topical corticosteroids. Annals of Pharmacother 2008; 42(12):1903-7. 13. Bussières JF, Barret P, Ferreira E. Réaction cutanée d’hypersensibilité retardée des héparines et héparinoïdes durant la grossesse. Québec Pharmacie 2008; 55(6):45-7. 14. Daudé MS, Barret P, Lebel D, et coll. Syndrome de Stevens-Johnson induit par la phénytoïne et recommandations de génotypage. Québec Pharmacie 2010 (sous presse). 15. Nichols V, Thériault-Dubé I, Touzin J, et coll. Risk perception and reasons for noncompliance in pharmacovigilance : A qualitative study conducted in Canada. Drug Saf 2009; 32(7):579-90. Tableau II Sélection d’ouvrages et de liens utiles à la pharmacovigilance Organismes réglementaires Canada – Canada Vigilance nInformation sur les effets indésirables www.hc-sc.gc.ca/dhp-mps/medeff/advers-react-neg/index-fra.php nBulletin canadien sur les effets indésirables www.hc-sc.gc.ca/dhp-mps/medeff/bulletin/index-fra.php nAvis, mises en garde et retraits www.hc-sc.gc.ca/dhp-mps/medeff/advisories-avis/index-fra.php nRapports et publications www.hc-sc.gc.ca/dhp-mps/pubs/medeff/index-fra.php nAbonnement à l’avis électronique Medeffet www.hc-sc.gc.ca/dhp-mps/medeff/subscribe-abonnement/index-fra.php nOutils de déclaration d’effets indésirables www.hc-sc.gc.ca/dhp-mps/medeff/report-declaration/index-fra.php nInterprétation des renseignements sur les effets indésirables www.hc-sc.gc.ca/dhp-mps/medeff/databasdon/interpretation-fra.php nCentre d’apprentissage sur les effets indésirables www.hc-sc.gc.ca/dhp-mps/medeff/centre-learn-appren/index-fra.php Europe – Eudravigilance neudravigilance.emea.europa.eu/human/index.asp nec.europa.eu/enterprise/pharmaceuticals/eudralex/vol-9/pdf/ vol9a_09-2008.pdf Ce site permet la déclaration en ligne et le suivi des effets indésirables pour tous les produits pharmaceutiques commercialisés au sein de la Communauté européenne. Il ne comporte aucune base de données accessible au grand public. De plus, la documentation Eudralex présente les bonnes pratiques de déclaration en matière de pharmacovigilance. États-Unis - Food and Drug Administration – Medwatch nwww.fda.gov/Safety/MedWatch/default.htm Cette section du site permet de faire des recherches en texte libre sur un problème de santé lié à l’utilisation d’un médicament chez l’humain. Le site ne comporte aucune base de données accessible au grand public. On peut aussi rechercher par nom générique de médicament. nwww.fda.gov/Drugs/DrugSafety/PostmarketDrugSafetyInformationfor PatientsandProviders/ucm111085.htm Organisation mondiale de la santé - Uppsala Monitoring Center nwww.who-umc.org/ Cet organisme a le mandat d’organiser la pharmacovigilance pour l’OMS. 48 Québec Pharmacie vol. 57 n° 3 juin 2010 Ouvrages nMann RD, Andrews EB. Pharmacovigilance. Wiley. 2nd ed. 2007. 702 pages. Un excellent ouvrage à caractère général sur la pharmacovigilance qui comporte cinq grands thèmes (notions de base, genèse d’un signal, effets indésirables par systèmes, thèmes d’actualité et perspectives futures) et 52 chapitres. nCobert B. Manual of Drug Safety and pharmacovigilance. Jones & Bartlett Publishing Co. 2nd ed. 2006. 292 pages. Un excellent ouvrage synthétique, à caractère général, sur la pharmacovigilance qui comporte 50 chapitres du général au spécifique et précisant le cadre réglementaire américain et celui de plusieurs pays, les populations cibles, etc. Chaque chapitre comporte une foire aux questions pratiques. nRick NG. Drugs : from discovery to approval. Wiley-Blackwell. 2nd ed. 2008. 466 pages. Un bon ouvrage à caractère général sur la mise au point des médicaments. Un pharmacien ne peut faire de pharmacovigilance sans bien comprendre toutes les étapes de la mise au point du médicament. nMhra B. Good Pharmacovigilance Practice Guide. Pharmaceutical Press. 1st ed. 2008. 211 pages. Un bon ouvrage britannique à caractère général sur la pharmacovigilance. nBiron P. La pharmacovigilance de A à Z. 1997. Traité de pharmacovigilance présenté par ordre alphabétique et destiné aux professionnels de la santé. Il ne semble plus y avoir de version électronique disponible sans frais. nFood and Drug Administration - Good Pharmacovigilance Practices and Pharmacoepidemiologic Assessment nwww.fda.gov/downloads/RegulatoryInformation/Guidances/ UCM126834.pdf Ce document établit les bonnes pratiques en pharmacovigilance américaine. Mise à niveau en pharmacovigilance 16. Van Grootheest AC, de Jong-van den Berg LT. The role of hospital and community pharmacists in pharmacovigilance. Res Social Adm Pharm 2005; 1(1):126-33. 17. Ackroyd-Stolarz S, Guernsey JR, MacKinnon NJ, et coll. Adverse events in older patients admitted to acute care : A preliminary cost description. Healthcare Manage Forum 2009. 22(3): 32-6. 18. Organisation mondiale de la santé (2009, décembre). « Pharmacovigilance – Creating pharmacovigilance awareness. Causality Assessment » [En ligne, site visité le 11 décembre 2009.] Adresse URL : www.pharmacovigilance.co.in/casualityassesment.html 19. Genome British Columbia (2009, décembre). « Canadian pharmacogenomics network for drug safety » [En ligne, site visité le 8 décembre 2009.] Adresse URL : www.genomebc.ca/genomics_programs/research_projects/applied_health/gatc.htm 20. Ross CJ, Katzov-Eckert H, Dubé MP, et coll. CPNDS Consortium. Genetic variants in TPMT and COMT are associated with hearing loss in children receiving cisplatin chemotherapy. Nat Genet 2009; 41(12):1345-9. 21. Santé Canada. «Déclaration des effets indésirables». [En ligne.] Adresse URL : https://www6.hc-sc.gc.ca/ medeffect/intro.do?method=intro ASSOCIATIONS et autres nInternational - International Society of Pharmacovigilance www.isoponline.org/ Cette association publie notamment la revue Drug Safety. nPharma Co – Pharmacovigilance www.pharmacovigilance.co.in/home.html Ce site indien du ministère de la Santé offre un portail d’autant plus intéressant sur les outils disponibles que de plus en plus de médicaments sont fabriqués en Inde. nPharmaceutical Information and Pharmacovigilance Association (PIPA) www.pipaonline.org.uk/ Il s’agit de l’organisme britannique de pharmacovigilance. nEuropean network of centres for pharmacoepidemiology and pharmacovigilance www.encepp.eu/ Cet organisme regroupe les centres de pharmacovigilance en Europe. nPharmacoepidemiology and Drug Safety www3.interscience.wiley.com/journal/5669/ home?CRETRY=1&SRETRY=0 Périodique ayant un intérêt en pharmacovigilance. nÉUA - Adverse drug events spontaneous triggered event reporting (ASTER) www.asterstudy.com/ Cette étude a été menée afin d’évaluer la mise au point d’un nouvel outil de déclaration des effets indésirables. www.professionsante.ca Questions de formation continue 14) Parmi les énoncés suivants sur la pharmacovigilance au Canada, indiquez celui qui est vrai. A. En 2008, Santé Canada a reçu 10 360 déclarations d’effets indésirables provenant du Canada, dont 69 % ont été considérées comme graves. B. Les produits pharmaceutiques représentent plus de 91 % des effets indésirables rapportés à Santé Canada. C. Les déclarations d’effets indésirables proviennent de détenteurs de l’autorisation de mise en marché dans 72 % des cas. D. Les déclarants sont patients ou consommateurs dans 50 % des cas. 15) Parmi les énoncés suivants sur la mise à jour qui a été publiée sur la pharmacovigilance, lequel est vrai ? A. Il est recommandé d’indiquer le binôme latin dans la déclaration d’effets indésirables aux produits de santé naturels. B. Il n’est pas nécessaire d’indiquer la date de survenue de l’événement indésirable déclaré. C. Santé Canada a publié de nouvelles lignes directrices sur la déclaration des effets indésirables en 2010. D. Une version améliorée de la base de données des effets indésirables au Canada a été mise en ligne en novembre 2007. Veuillez reporter vos réponses dans le formulaire de la page 78 juin 2010 vol. 57 n° 3 Québec Pharmacie 49 D’une page à l’autre Impact économique des interventions cliniques du pharmacien Objectif Présenter les évaluations économiques des études portant sur les interventions cliniques de pharmaciens en milieu hospitalier. Plan de l’étude Revue documentaire; il ne s’agit pas d’une revue systématique ni d’une méta-analyse. Lieu Les études incluses ont été recueillies et analysées de façon indépendante par un pharmacien hospitalier et un pharmacoéconomiste de l’Université de Louvain, en Belgique. En cas de désaccord lors de l’analyse, un autre pharmacien hospitalier était amené à participer afin que l’on arrive à un consensus. Toujours en cas de désaccord, l’étude était revue par un comité composé de sept pharmaciens hospitaliers et d’un pharmacoéconomiste. Participants La revue documentaire porte sur les études sélectionnées de 1996 à 2007, à partir des bases de données suivantes : PubMed, National Health Service Economic Evaluation Database, Cochrane Library, EconLit et Social Sciences Citation Index. Parmi les 21 études sélectionnées, 18 ont été menées en Amérique du Nord, une en Australie, une autre aux PaysBas et une dernière en Malaisie. Ont été incluses dans la revue les études comportant minimalement un comparateur et des données de coûts et de résultats en lien avec l’intervention clinique. Ont été exclues les études portant sur les activités ambulatoires. Interventions L’équipe de recherche a regroupé les interventions cliniques du pharmacien en cinq grandes catégories, soit : a) les interventions ciblant une réduction des coûts; b) les interventions en équipe interdisciplinaire, incluant les tournées; c) les interventions ciblant la prévention des événements indésirables et des erreurs de prescription; d) les interventions portant sur la gestion optimale de l’antibiothérapie; et e) les autres interventions. Paramètres évalués Pour chaque étude incluse dans l’analyse ont été répertoriés le pays, l’année, le type d’évaluation économique, la taille de l’échantillon, le contexte de pratique, l’intervention clinique pharmaceutique, la durée de l’étude, les coûts www.professionsante.ca et les résultats. De plus, une évaluation qualitative de la méthodologie utilisée dans chacune des études incluses a été réalisée à partir d’une liste de critères pré-établis. Cette liste a permis d’évaluer le devis ou le type d’étude utilisé, les paramètres étudiés pour évaluer l’impact des interventions sur les plans économique et clinique, ainsi que la méthode employée dans l’estimation ou l’évaluation des coûts qui y sont associés, et la mise en pratique d’une analyse différentielle des coûts et des résultats obtenus. Texte rédigé par Grégory Perrier, 5e année hospitalo-universitaire, Université Claude-Bernard (Lyon 1), France, et Jean-François Bussières, B.Pharm, M.Sc., MBA, FCSHP, chef du département de pharmacie et de l’unité de recherche en pratique pharmaceutique, CHU Sainte-Justine. Résultats Texte final remis le 6 octobre 2009. Révision : Nicolas Paquette-Lamontagne, B.Pharm, M.Sc., MBA, PMP. Texte original soumis le 24 septembre 2009. La recherche documentaire faite à partir de mots-clés a permis d’identifier initialement 314 articles. Vingt et un d’entre eux ont été retenus selon les critères d’inclusion représentant un total de 33 376 interventions pharmaceutiques pour 210 664 patients, dans des études variant entre 30 jours et 4 ans. Dix-sept types d’interventions cliniques ont été identifiés, notamment le bilan comparatif des médicaments à l’arrivée et au départ, incluant les conseils, le monitorage thérapeutique, l’ajustement des doses en insuffisance rénale ou hépatique, la détection et la prévention des interactions et événements indésirables, le maintien d’une liste locale de médicaments, la participation active à la tournée médicale, la revue d’utilisation et les programmes de formation et de substitution. Sur le plan économique, on recense des études de coûts-minimisation, de coûts-efficacité et de coûts-avantages. Les économies calculées et annualisées varient entre 5800 $ et 4 254 345 $. La majorité des interventions pharmaceutiques décrites ne sont pas liées à des activités de prestations. La plupart des études se déroulent dans des milieux de soins universitaires (p. ex., le plus souvent rédigées par des résidents en formation) et décrivent une grande variété d’interventions et différentes clientèles (p. ex., médecine, chirurgie et soins intensifs). Les coûts retenus incluent généralement les médicaments, les tests de laboratoire et, plus rarement, les salaires des pharmaciens. Dans certaines études, les coûts évités (p. ex., les économies liées à la prévention d’un effet indésirable) sont inclus. Parmi les issues retenues, on retrouve principalement la durée de séjour, la probabilité ou le taux de réadmission et le taux de mortalité. Les auteurs soulignent les lacunes importantes en ce qui concerne l’évaluation économique des études évaluées. Ces études ne tiennent compte que de la perspective hospitalière (et pas de la perspective du système de santé ou de juin 2010 vol. 57 n° 3 Québec Pharmacie 51 Impact économique des interventions cliniques du pharmacien la société). Dans plusieurs cas, elles ont comparé les coûts à des sources et à des barèmes externes qui ne sont pas forcément comparables ou applicables. La plupart des études reposent sur des issues intermédiaires plutôt que finales (p. ex., on évalue la nécessité de recourir à un médicament pour contrer un effet indésirable plutôt que l’impact sur la durée d’hospitalisation ou la mortalité), souvent sans groupe témoin. De façon générale, les études ne précisent pas les méthodes utilisées pour évaluer les interventions pharmaceutiques. Plusieurs d’entre elles ont omis de tenir compte des coûts liés à la prestation des soins pharmaceutiques. Conclusion La plupart des évaluations pharmacoéconomiques des interventions cliniques des pharmaciens comportent des limites qualitatives et quantitatives. Les auteurs recommandent que les prochaines études soient comparatives avec un groupe témoin et qu’elles incluent une approche de coût-efficacité. Discussion est toujours concurrente de celle d’autres professionnels et de leur apprentissage au fil du temps. Est-il nécessaire que le pharmacien soit toujours présent ou l’effet de sa présence ne transforme-t-il pas la pratique des médecins et des infirmières qui le côtoient ? Quelle est l’utilité de cette étude dans le contexte québécois ? Le ministère de la Santé et des Services sociaux, en collaboration avec l’Ordre des pharmaciens du Québec, a mené en 2009 une revue documentaire sur la hiérarchisation des soins en établissements de santé afin de proposer un modèle de pratique dans le contexte de la reconnaissance éventuelle des pharmaciens spécialistes, de la pénurie de ressources, de l’évolution du circuit du médicament, de la nouvelle norme sur la gestion du médicament proposée par Agrément Canada et de l’évolution des pratiques professionnelles. Cette revue documentaire, comme plusieurs autres, doit être connue des pharmaciens québécois, pas seulement en milieu hospitalier, mais aussi en milieu communautaire, parce que ceux-ci sont appelés de plus en plus à travailler en continuité, avec des outils papier et électroniques communs et, surtout, avec les mêmes patients. Si, une fois de plus, ces études décrivent des pratiques hospitalières spécialisées et un impact économique favorable, le rôle du pharmacien devrait être reconnu : il détient une formation universitaire de deuxième cycle depuis bientôt cinq décennies, il est formé pour réaliser les interventions spécialisées décrites dans plusieurs de ces études, dans un contexte de soins spécialisés, et il pourrait être encore mieux utilisé et avoir plus d’impact s’il était davantage reconnu. n Les auteurs proposent une discussion éclairée de leur analyse. Il faut retenir que les économies semblent plus importantes dans les milieux universitaires et les secteurs de soins spécialisés où l’on a recours à une pharmacothérapie plus complexe et coûteuse. Compte tenu du nombre d’interventions pharmaceutiques et d’issues mesurées, il est impossible de comparer ces études et de présenter des résultats agrégés de l’impact économique. Force est de constater que presque toutes les études montrent que des économies ont été réalisées, mais toutes ne prennent pas en compte adéquatement tous les coûts pertinents. On peut raisonnablement Référence affirmer que le biais de publication qui limite De Rijdt T, Willems L, Simoens S. Economic effects of généralement la diffusion de résultats négatifs clinical pharmacy interventions : A literature review. Am J Health-Syst Pharm 2008; 65: 1161-72. affecte aussi les études portant sur l’impact du pharmacien. S’il est vrai que les études devraient Lecture suggérée présenter de façon plus détaillée la nature de Kaboli P. Realizing the pharmacoeconomic benefit of clinl’intervention pharmaceutique, cette dernière ical pharmacy. Am J Health-Syst Pharm 2008; 65: 1123. Question de formation continue 16)Parmi les énoncés suivants inspirés de la revue documentaire sur l’impact économique des interventions cliniques du pharmacien, lequel est vrai ? A.Les évaluations économiques ne sont que des études coûts-avantages. B.Les évaluations économiques indiquent des économies annuelles d’au plus 144 500 $. C.La plupart des évaluations économiques comportent des limites qualitatives et quantitatives. D.La plupart des études se déroulent dans des milieux de soins non universitaires et décrivent une variété limitée d’interventions. E. La plupart des interventions des pharmaciens sont réalisées lors d’activités de prestations. Veuillez reporter votre réponse dans le formulaire de la page 78 www.professionsante.ca juin 2010 vol. 57 n° 3 Québec Pharmacie 53 En exclusivité sur votre portail ProfessionSanté.ca Blogues Lisez les blogues de vos collègues pharmaciens qui n’hésitent pas à prendre position sur des sujets qui vous tiennent à cœur. Hélène Blanchette Marc Parent Lisez aussi le blogue du jounaliste Christian Leduc. Georges-Étienne Gagnon Consultez également le blogue de Nicolas Dugré afin de suivre les péripéties de cet étudiant en pharmacie en mission humanitaire au Pérou. Moteur de recherche Un puissant moteur de recherche vous permet, grâce à un ou des mots-clés, de trouver les articles qui vous intéressent dans la version papier de Québec Pharmacie ou encore des articles exclusifs au portail ProfessionSanté.ca. Archives Les numéros de Québec Pharmacie sont accessibles sous l’onglet Archives, à droite de votre écran. www.professionsante.ca juin 2010 vol. 57 n° 3 Québec Pharmacie 55 DANS LE PROCHAIN NUMÉRO DE LA MÈRE AU NOURRISSON Le traitement de l’insomnie chez la femme enceinte Des troubles du sommeil sont fréquemment observés chez la femme enceinte, bien que leur incidence exacte demeure inconnue. Les modifications hormonales, physiologiques, physiques et comportementales peuvent affecter à la fois la qualité et la durée du sommeil durant la grossesse. Outre les impacts de la grossesse sur le sommeil seront explorées les données d’efficacité de différentes options pharmacologiques dans le traitement de l’insomnie de la population générale, puis les données d’innocuité reliées à l’utilisation de ces mêmes agents pharmacologiques durant la grossesse. LES PAGES BLEUES Physiopathologie de la maladie de Crohn et thérapies biologiques La maladie de Crohn est une maladie inflammatoire intestinale chronique et progressive qui peut affecter tout le tube gastro-intestinal, mais qui touche davantage l’iléon terminal, le côlon ascendant et la région ano-rectale. Les causes exactes des maladies inflammatoires intestinales ne sont pas connues. Les rémissions sont généralement difficiles à obtenir. Ainsi, la majorité des patients devront prendre à vie leur médication, d’où l’importance de l’arsenal thérapeutique. INFOROUTE Impact des sites de réseaux sociaux en pratique pharmaceutique Le développement du Web depuis les années 1990 a bouleversé la gestion de l’information, les échanges entre les personnes et les entreprises. Si le courriel demeure un véhicule privilégié de communication, les internautes recourent de plus en plus aux réseaux sociaux, aux blogues, aux wikis et autres outils Web facilitant le travail en équipe. Mais quel est l’impact des outils de réseaux sociaux en pratique pharmaceutique ? www.professionsante.ca juin 2010 vol. 57 n° 3 Québec Pharmacie 57 Répondez en ligne sur Programme de formation continue 1200, avenue McGill College, bureau 800, Montréal (QC) H3B 4G7 Télécopieur : 514 843-2940 Questions de Formation continue Noircir les cases. 9.A B C D E Formulaire de réponses 1.A B C D E 10.A B C D E 2.A B C D E 11.A B C D E 3.A B C D E 12.A B C D E 4.A B C D E 13.A B C D E 5.A B C D E 14.A B C D E 6.A B C D E 15.A B C D E 7.A B C D E 16.A B C D E 8.A B C D E 2,8 UFC de l’OPQ Juin 2010 Répondre à 10 des 16 questions proposées Réponses au questionnaire de novembre 2009 1. D 2.A 3. B 4. B 5. D 6. D Date limite : le 24 septembre 2010 7.C 8. B 9. D 10.C 11.C Veuillez écrire lisiblement. Les réponses illisibles, ambiguës ou multiples seront rejetées. N° de permis :Année d’obtention du diplôme : Nom :Prénom : Nom de la pharmacie : Téléphone (bureau) :Télécopieur (bureau) : Adresse : Ville :Province :Code postal : Hôpital Industrie Université/enseignement Propriétaire de pharmacie Indépendant Chaîne/franchise Bannière Gouvernement Autre – spécifiez : Salarié en pharmacie communautaire Indépendant Temps complet Chaîne/franchise Temps partiel Bannière Remplaçant Pharmacien membre de l’Ordre des pharmaciens du Nouveau-Brunswick N° de permis : Veuillez nous confirmer que ce contenu vous a été utile en répondant aux questions suivantes : 1)Après avoir lu ce contenu, pensez-vous être plus en mesure d’offrir des soins pharmaceutiques à vos patients ? Oui Non 78 2)Ce contenu vous est-il utile dans l’exercice de votre profession ? Oui Non Québec Pharmacie vol. 57 n° 3 juin 2010 3)Pourrez-vous mettre en pratique cette information ? Oui Non N.A. 4) Dans l’ensemble, êtes-vous satisfait(e) de ce contenu ? Très Assez Pas du tout www.professionsante.ca Courriel : Pour répondre en ligne à cette leçon de formation continue Si vous avez déjà ouvert une session dans notre programme de FC en ligne, veuillez revenir à la page « Leçons disponibles en ligne » et cliquez sur « Lien vers les questions » correspondant à cette leçon de FC. Si vous n’avez pas encore ouvert une session, mais que vous êtes inscrit à notre programme de FC en ligne, veuillez cliquer ici : ce.pharmacygateway.com/Pharmacie/login/index.asp Si vous ne vous êtes pas encore inscrit à notre programme de FC en ligne et si vous désirez répondre aux questions en ligne, veuillez cliquer ici : ce.pharmacygateway.com/Pharmacie/login/adduser.asp Pour toute question, veuillez communiquer avec : Francine Beauchamp Formation continue pour Québec Pharmacie et L’actualité pharmaceutique Fax : (514) 843-2182 Courriel : [email protected] Mayra Ramos Formation continue de Pharmacy Practice, de Pharmacy Post, des FC de Novopharm, d’autres FC approuvées par le CCEPP, de Tech Talk (anglais) ou Coin Technipharm (français). Fax : (416) 764-3937 Courriel : [email protected]