Télécharger la présentation (J. Kirilovsky)
Transcription
Télécharger la présentation (J. Kirilovsky)
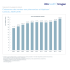
L'innovation dans les industries de la santé: les nouveaux enjeux Jorge KIRILOVSKY Centre de Recherches François Hyafil Laboratoires GlaxoSmithKline 31 mai 2012 L’industrie du médicament doit faire face à un nouvel environnement La croissance vient de nouvelles aires géographiques Le marché se polarise entre génériques et produits de spécialité • Les USA et les pays matures d’Europe ne sont plus générateurs de croissance. Les marchés “Pharmergents” tirent la croissance • Les génériques occupent le plus souvent la première ligne des grandes aires thérapeutiques • L’innovation se positionne en seconde ligne • Les agences réglementaires et les payeurs diminuent le pouvoir du prescripteur • Les barrières à l’entrée se multiplient • J. Kirilovsky – 31 mai 2012 Un marché pharmaceutique mondial dominé (en CA) par des produits généricables à faible échéance Classement mondial 2010 LIPITOR PLAVIX • Les premiers produits mondiaux sont génériqués à court terme SERETIDE NEXIUM SEROQUEL CRESTOR • Aucun produit de spécialité ne dépasse aujourd’hui la moitié du CA du Tahor/Lipitor® ENBREL HUMIRA ZYPREXA REMICADE 0 2 4 6 8 10 12 milliards $ Source: IMS Health MIDAS CMA Décembre 2010 J. Kirilovsky – 31 mai 2012 14 Les produits généricables en France en 2012 : 1,2 milliards d’euros (9% du marché hors répertoire) 450, 417,3 400, % du CA 350, 300, 250, 200, 150, 130,7 110,1 109,7 100, 86,8 67,8 62,7 50, , Source Gers Ville Performance Commerciale & Etudes de Marché J. Kirilovsky – 31 mai 2012 58,4 41,8 41,7 39, 34,6 26,9 14,1 PFIZER MERCK SANOFI NOVARTIS AZ TAKEDA JANSSEN IPSEN EISAI GSK 32,5 % 11,8 % 9,8 % 9,0 % 8,2 % 22,6 % 7,7 % 10,7 % 84,5 % 1,7 % 160B$ de pertes de brevets sur 2010 – 2015 Les nouveaux produits seront-ils capables de remplacer ces pertes de revenus? 50 $46.7Bn 45 40 $32.4Bn 35 . $31.2Bn $27.8Bn 30 Ventes ($B) Zyprexa 25 Seroquel 20 Plavix 15 Oxycontin $20.5Bn $16.7Bn Actos 10 5 0 Seretide Nexium Lipitor Aricept Alna Lipitor Exp 2010 Exp 2011 Singulair Lexapro Exp 2012 Exp 2013 Cymbalta Celebrex Abilify Exp 2014 Exp 2015 Source: IMS Health MIDAS Market Segmentation December 2009. Products shown have >$2Bn sales in 2009 Date d’expiration : CMA Dec *Assumptions based on no price erosion following generic entry to the market. J. Kirilovsky – 31 mai 2012 Le coût de l’innovation en croissance exponentielle depuis 20 ans Évolution du coût du développement d'une molécule innovante de 1976 à 2003 900 800 800 En millions de dollars 700 750 600 500 500 400 300 300 200 200 100 0 50 1976 100 1986 1987 1990 1996 2000 Sources : 1976-1996 : Pharma et Scrip, 2000 : Pharma ethical, 2003 : Tuft center J. Kirilovsky – 31 mai 2012 2003 La découverte de nouveaux médicaments est longue et coûteuse : >10 ans, > 1 milliard € Preclinical 3 – 6 Years 250 Scale-Up to Manufacture PostMarketing Surveillance Phase III 5 1 Approved New Medicine IND Submitted Pre-Discovery Phase Phas I e II ~ 5000 – 10000 Compounds Regulatory Review Clinical Trials Number of Patients / Subjects 20 – 100 100 – 500 1,000 – 30.000 6 – 7 Years NDA Submitted Drug Discovery 0.5 – 2 Years Indefinite Sources : Drug Discovery and Development: Understanding the R&D Process, www.innovation.org; CBO, Research and Development in the Pharmaceutical Industry, 2006 J. Kirilovsky – 31 mai 2012 Les connaissances scientifiques et la technologie évoluent très rapidement • Les médicaments actuellement sur le marché ne touchent que 120 cibles différentes Source : Nature Drug Discovery J. Kirilovsky – 31 mai 2012 La productivité de la R&D pharma en baisse !!! J. Kirilovsky – 31 mai 2012 La découverte des médicaments ne suit pas l’évolution rapide des sciences Les années ‘90 J. Kirilovsky – 31 mai 2012 Connaissances scientifiques Nouveaux médicaments Les Biotech ont pris une part prépondérante dans la R&D pharmaceutique Part dominante de biotechs en R&D (nombre de molécules en Phase III) 165 169 220 374 239 149 2000 2005 Biotech / Petites pharma J. Kirilovsky – 31 mai 2012 2007 Big Pharma Le marché global des produits biopharmaceutiques a presque doublé en plus de dix ans Valeurs et % des Produits Biologiques Les biologiques représentent un tiers des produits en fin de développement* (Déc. 2009) 16.9% 10.2% 17% Biotech 16% Autres Biologiques 67% Autres produits Biologiques *488 produits recensés en décembre 2009 en phase III et en phase d’autorisation auprès d’une autorité de régulation Sources: IMS Health MIDAS MAT Décembre 2009; IMS Life Cycle R&D Focus, Juin 2010 J. Kirilovsky – 31 mai 2012 Autres La réalité de la R&D et du marché pharmaceutique Perte des brevets sur principaux produits (30-40 % du CA d’ici 2013) Compétion de génériques Pas de renouvellement suffisant du portefeuille Cycles très longs (12 ans au minimum) Taille critique atteinte (4-5 milliards d’€) ↑ Niveau d’exigence des autorités de santé ( ↑ bénéfice / ↓ risque ; ↓ dépenses) Des besoins thérapeutiques non satisfaits J. Kirilovsky – 31 mai 2012 Les besoins médicaux non satisfaits Cancer(s) Maladies neurodégénératives Maladies auto-immunes / inflammatoires Obésité Diabète Les pandémies Maladies des pays émergeants (tuberculose, malaria,…) Maladies rares J. Kirilovsky – 31 mai 2012 Quelle est la solution ? Développer des médicaments qui correspondent à des besoins thérapeutiques Diminuer le risque en développement Prendre des bonnes décisions en amont Diminuer le temps des cycles de la R&D S’ouvrir vers l’extérieur Augmenter les partenariats public / privé Sélectionner les domaines thérapeutiques où les avancées scientifiques permettent d’envisager l’innovation J. Kirilovsky – 31 mai 2012 La R&D pharmaceutique doit changer son modèle – Hier : blockbusters –Populations larges –Coûts de traitement faibles – Aujourd’hui : molécules à forte valeur ajoutée et très innovants – Médecine personnalisée (produits biopharmaceutiques) – Populations étroites – Coûts de traitement élevés – Ouverture vers des partenaires extérieurs J. Kirilovsky – 31 mai 2012 Le modèle entrepreneurial de la Drug Discovery chez GSK Centres d’excellence par domaine thérapeutique ou technologique: Neurosciences, Métabolisme/CV, Maladies Infectieuses, Respiratoire, Oncologie, Biopharmacéutiques Chaque Centre d’Excellence est constitué par 3-5 Discovery Performance Units (DPUs) Les DPUs sont : – Autonomes – Co-localisés – Ouverts vers l’extérieur – Responsables (‘accountable’) – Focalisés sur un domaine scientifique précis – Petite taille (5-60 scientifiques) – Chimistes, biologistes, DMPK, cliniciens – Responsables de tout le processus de découverte d’un médicament (identification de la cible → preuve du concept chez l’homme phase IIa) Les DPUs doivent soumettre un Business Plan à un comité d’investissement. Les plans (et les budgets) sont approuvés pour une durée déterminée. J. Kirilovsky – 31 mai 2012 La philosophie : laisser les experts prendre les décisions Cardiovascular / Metabolic Oncology Academic Incubator Maladies négligées Biopharm ImmunoInflammation Neurosciences Respiratory Partenariats Ceedd académiques DPU J. Kirilovsky – 27 janvier 2012 Virtual PoC Stem cells Infectious Diseases Sirtris Ophtalmo Maladies rares Partenariats flexibles /acquisitions Rapprocher académiques et industriels Un modèle différent Open Innovation Patent pooling Publications Echange de personnel Partage de risque J. Kirilovsky – 31 mai 2012 Ouverture vers l’extérieur et partage de la science J. Kirilovsky – 31 mai 2012 En partant du monolithe… Externe Drug Discovery virtuelle DPUs Interne Pharma Centralisé J. Kirilovsky – 31 mai 2012 Décentralisé La transformation de la Drug Discovery commence à porter ses fruits ? J. Kirilovsky – 31 mai 2012 L’avenir de la R&D pharmaceutique Focalisation sur le patient Pressions réglementaires et sur la propriété intellectuelle Innovation appliquée Forte surveillance des consommateurs Ouverture et partenariats J. Kirilovsky – 31 mai 2012 Focalisation sur la création de valeur par l’innovation